Алюминий — свойства, харакретистики, обзорная статья
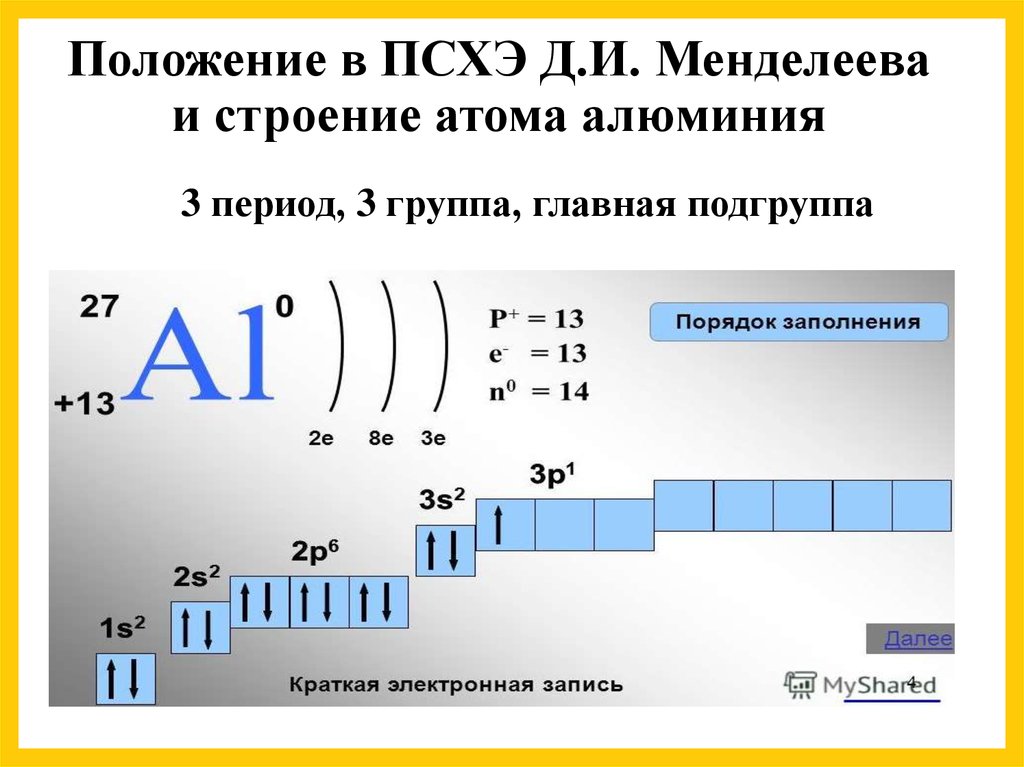
Алюминий – это пластичный и лёгкий металл белого цвета, покрытый серебристой матовой оксидной плёнкой. В периодической системе Д. И. Менделеева этот химический элемент обозначается, как Al (Aluminium) и находится в главной подгруппе III группы, третьего периода, под атомным номером 13. Купить алюминий вы можете на нашем сайте.
История открытия
В 16 веке знаменитый Парацельс сделал первый шаг к добыче алюминия. Из квасцов он выделил «квасцовую землю», которая содержала оксид неизвестного тогда металла. В 18 веке к этому эксперименту вернулся немецкий химик Андреас Маргграф. Оксид алюминия он назвал «alumina», что на латинском языке означает «вяжущий». На тот момент металл не пользовался популярностью, так как не был найден в чистом виде.
Долгие годы выделить чистый алюминий пытались английские, датские и немецкие учёные. В 1855 году в Париже на Всемирной выставке металл алюминий произвёл фурор. Из него делали только предметы роскоши и ювелирные украшения, так как металл был достаточно дорогим. В конце 19 века появился более современный и дешёвый метод получения алюминия. В 1911 году в Дюрене выпустили первую партию дюралюминия, названного в честь города. В 1919 из этого материала был создан первый самолёт.
В конце 19 века появился более современный и дешёвый метод получения алюминия. В 1911 году в Дюрене выпустили первую партию дюралюминия, названного в честь города. В 1919 из этого материала был создан первый самолёт.
Физические свойства
Металл алюминий характеризуется высокой электропроводностью, теплопроводностью, стойкостью к коррозии и морозу, пластичностью. Он хорошо поддаётся штамповке, ковке, волочению, прокатке. Алюминий хорошо сваривается различными видами сварки. Важным свойством является малая плотность около 2,7 г/см³. Температура плавления составляет около 660°С.
Механические, физико-химические и технологические свойства алюминия зависят от наличия и количества примесей, которые ухудшают свойства чистого металла. Основные естественные примеси – это кремний, железо, цинк, титан и медь.
По степени очистки различают алюминий высокой и технической чистоты. Практическое различие заключается в отличии коррозионной устойчивости к некоторым средам. Чем чище металл, тем он дороже. Технический алюминий используется для изготовления сплавов, проката и кабельно-проводниковой продукции. Металл высокой чистоты применяют в специальных целях.
Технический алюминий используется для изготовления сплавов, проката и кабельно-проводниковой продукции. Металл высокой чистоты применяют в специальных целях.
По показателю электропроводности алюминий уступает только золоту, серебру и меди. А сочетание малой плотности и высокой электропроводности позволяет конкурировать в сфере кабельно-проводниковой продукции с медью. Длительный отжиг улучшает электропроводность, а нагартовка ухудшает.
Теплопроводность алюминия повышается с увеличением чистоты металла. Примеси марганца, магния и меди снижают это свойство. По показателю теплопроводности алюминий проигрывает только меди и серебру. Благодаря этому свойству металл применяется в теплообменниках и радиаторах охлаждения.
Алюминий обладает высокой удельной теплоёмкостью и теплотой плавления. Эти показатели значительно больше, чем у большинства металлов. Чем выше степень чистоты алюминия, тем больше он способен отражать свет от поверхности. Металл хорошо полируется и анодируется.
Алюминий имеет большое сродство к кислороду и покрывается на воздухе тонкой прочной плёнкой оксида алюминия. Эта плёнка защищает металл от последующего окисления и обеспечивает его хорошие антикоррозионные свойства. Алюминий обладает стойкостью к атмосферной коррозии, морской и пресной воде, практически не вступает во взаимодействия с органическими кислотами, концентрированной или разбавленной азотной кислотой.
Химические свойства
Алюминий — это достаточно активный амфотерный металл. При обычных условиях прочная оксидная плёнка определяет его стойкость. Если разрушить оксидную плёнку, алюминий выступает как активный металл-восстановитель. В мелкораздробленном состоянии и при высокой температуре металл взаимодействует с кислородом. При нагревании происходят реакции с серой, фосфором, азотом, углеродом, йодом. При обычных условиях металл взаимодействует с хлором и бромом. С водородом реакции не происходит. С металлами алюминий образует сплавы, содержащие интерметаллические соединения – алюминиды.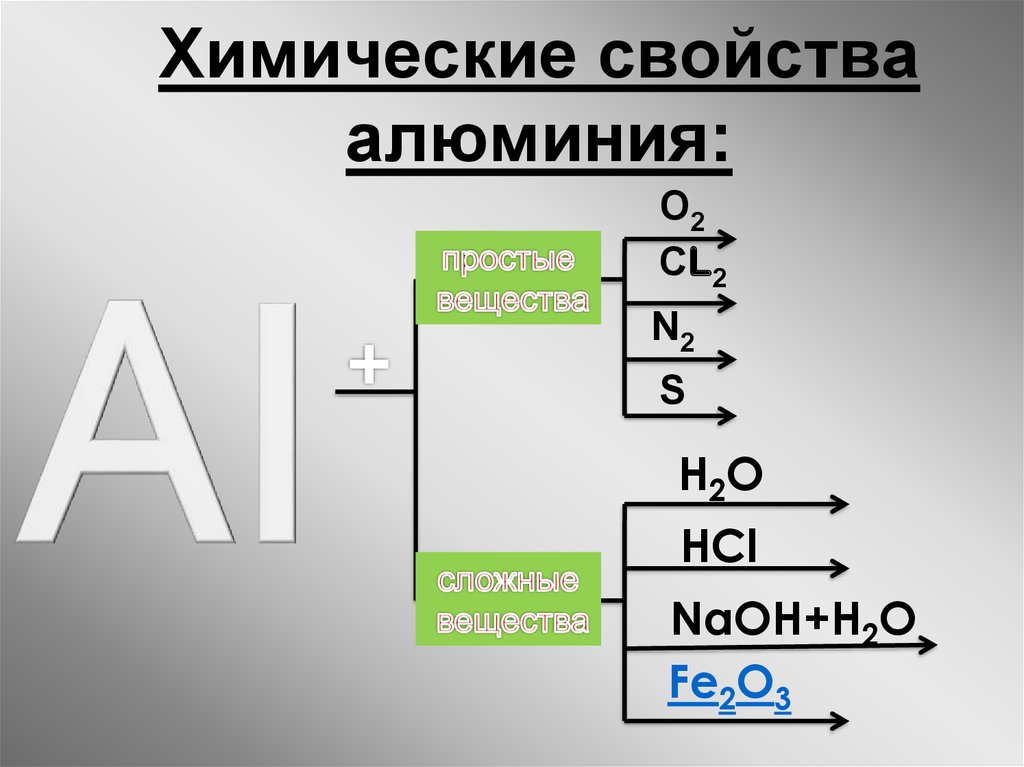
При условии очищения от оксидной пленки, происходит энергичное взаимодействие с водой. Легко протекают реакции с разбавленными кислотами. Реакции с концентрированной азотной и серной кислотой происходят при нагревании. Алюминий легко реагирует со щелочами. Практическое применение в металлургии нашло свойство восстанавливать металлы из оксидов и солей – реакции алюминотермии.
Получение
Алюминий находится на первом месте среди металлов и на третьем среди всех элементов по распространённости в земной коре. Приблизительно 8% массы земной коры составляет именно этот металл. Алюминий содержится в тканях животных и растений в качестве микроэлемента. В природе он встречается в связанном виде в форме горных пород, минералов. Каменная оболочка земли, находящаяся в основе континентов, формируется именно алюмосиликатами и силикатами.
Алюмосиликаты – это минералы, образовавшиеся в результате вулканических процессов в соответствующих условиях высоких температур. При разрушении алюмосиликатов первичного происхождения (полевые шпаты) сформировались разнообразные вторичные породы с более высоким содержанием алюминия (алуниты, каолины, бокситы, нефелины). В состав вторичных пород алюминий входит в виде гидроокисей или гидросиликатов. Однако не каждая алюминийсодержащая порода может быть сырьём для глинозёма – продукта, из которого при помощи метода электролиза получают алюминий.
В состав вторичных пород алюминий входит в виде гидроокисей или гидросиликатов. Однако не каждая алюминийсодержащая порода может быть сырьём для глинозёма – продукта, из которого при помощи метода электролиза получают алюминий.
Наиболее часто алюминий получают из бокситов. Залежи этого минерала распространены в странах тропического и субтропического пояса. В России также применяются нефелиновые руды, месторождения которых располагаются в Кемеровской области и на Кольском полуострове. При добыче алюминия из нефелинов попутно также получают поташ, кальцинированную соду, цемент и удобрения.
В бокситах содержится 40-60% глинозёма. Также в составе имеются оксид железа, диоксид титана, кремнезём. Для выделения чистого глинозёма используют процесс Байера. В автоклаве руду нагревают с едким натром, охлаждают, отделяют от жидкости «красный шлам» (твёрдый осадок). После осаждают гидроокись алюминия из полученного раствора и прокаливают её для получения чистого глинозёма. Глинозём должен соответствовать высоким стандартам по чистоте и размеру частиц.
Из добытой и обогащённой руды извлекают глинозём (оксид алюминия). Затем методом электролиза глинозём превращают в алюминий. Заключительным этапом является восстановление процессом Холла-Эру. Процесс заключается в следующем: при электролизе раствора глинозёма в расплавленном криолите происходит выделение алюминия. Катодом служит дно электролизной ванны, а анодом – угольные бруски, находящиеся в криолите. Расплавленный алюминий осаждается под раствором криолита с 3-5% глинозёма. Температура процесса поднимается до 950°С, что намного превышает температуру плавления самого алюминия (660°С). Глубокую очистку алюминия проводят зонной плавкой или дистилляцией его через субфторид.
Применение
Алюминий применяется в металлургии в качестве основы для сплавов (дуралюмин, силумин) и легирующего элемента (сплавы на основе меди, железа, магния, никеля). Сплавы алюминия используются в быту, в архитектуре и строительстве, в судостроении и автомобилестроении, а также в космической и авиационной технике. Алюминий применяется при производстве взрывчатых веществ. Анодированный алюминий (покрытый окрашенными плёнками из оксида алюминия) применяют для изготовления бижутерии. Также металл используется в электротехнике.
Алюминий применяется при производстве взрывчатых веществ. Анодированный алюминий (покрытый окрашенными плёнками из оксида алюминия) применяют для изготовления бижутерии. Также металл используется в электротехнике.
Рассмотрим, как используют различные изделия из алюминия.
Алюминиевая лента представляет собой тонкую алюминиевую полосу толщиной 0,3-2 мм, шириной 50-1250 мм, которая поставляется в рулонах. Используется лента в пищевой, лёгкой, холодильной промышленности для изготовления охлаждающих элементов и радиаторов.
Круглая алюминиевая проволока применяется для изготовления кабелей и проводов для электротехнических целей, а прямоугольная для обмоточных проводов.
Алюминиевые трубы отличаются долговечностью и стойкостью в условиях сельских и городских промышленных районов. Применяются они в отделочных работах, дорожном строительстве, конструкции автомобилей, самолётов и судов, производстве радиаторов, трубопроводов и бензобаков, монтаже систем отопления, магистральных трубопроводов, газопроводов, водопроводов.
Алюминиевые втулки характеризуются простотой в обработке, монтаже и эксплуатации. Используются они для концевого соединения металлических тросов.
Алюминиевый круг — это сплошной профиль круглого сечения. Используется это изделие для изготовления различных конструкций.
Алюминиевый пруток применяется для изготовления гаек, болтов, валов, крепежных элементов и шпинделей.
Около 3 мг алюминия каждый день поступает в организм человека с продуктами питания. Больше всего металла в овсянке, горохе, пшенице, рисе. Учёными установлено, что он способствует процессам регенерации, стимулирует развитие и рост тканей, оказывает влияние на активность пищеварительных желёз и ферментов.
Алюминиевый лист
Алюминиевая плита
Алюминиевые чушки
Алюминиевые уголки
Алюминиевая проволока
При использовании алюминиевой посуды в быту необходимо помнить, что хранить и нагревать в ней можно исключительно нейтральные жидкости. Если же в такой посуде готовить, к примеру, кислые щи, то алюминий поступит в еду, и она будет иметь неприятный «металлический» привкус.
Если же в такой посуде готовить, к примеру, кислые щи, то алюминий поступит в еду, и она будет иметь неприятный «металлический» привкус.
Алюминий входит в состав лекарственных препаратов, используемых при заболеваниях почек и желудочно-кишечного тракта.
Алюминий: химические свойства и способность вступать в реакции с другими веществами
[Deposit Photos]Металлы относятся к удобным для обработки материалам, и лидером среди них является алюминий, химические свойства которого давно известны людям. Этот металл, благодаря своим характеристикам, широко применяется в быту, и отыскать у себя дома изделие из алюминия сможет почти каждый человек. Следует детально рассмотреть свойства этого металла как элемента и как простого вещества.
[Deposit Photos]Как был открыт алюминий
С давних времен люди использовали алюмокалиевые квасцы — соединение алюминия, способное придавать прочность и устойчивость тканям и коже. Такое свойство металла нашло свое применение в кожевничестве: с помощью алюмокалиевых квасцов скорняки выделывали кожу, придавая ей прочность и устойчивость. О том, что оксид алюминия присутствует в природе в чистом виде, люди узнали только во второй половине XVIII столетия, но получать чистое вещество в те времена еще не научились.
Такое свойство металла нашло свое применение в кожевничестве: с помощью алюмокалиевых квасцов скорняки выделывали кожу, придавая ей прочность и устойчивость. О том, что оксид алюминия присутствует в природе в чистом виде, люди узнали только во второй половине XVIII столетия, но получать чистое вещество в те времена еще не научились.
Впервые это удалось сделать Хансу Кристиану Эрстеду, который обработал соль амальгамой калия, выделив затем из полученной смеси порошок серого цвета. Таким образом, данная химическая реакция помогла добыть чистый алюминий. В то же время были установлены такие характеристики металла, как высокая восстановительная способность и сильная активность.
После открытия металла работу Эрстеда по получению алюминия продолжал Фридрих Вёлер: в 1827 году он получил алюминиевый порошок, а в 1845-м — шарики металла. А первый промышленно значимый эксперимент был поставлен французским ученым Девилем в 1854 году. Именно этот выдающийся химик предложил электрохимический способ получения алюминия и сумел изготовить первые слитки металла (данный способ сохранил свою актуальность и в наши дни).
В XX столетии началось промышленное производство алюминия, который сразу же стал высоко цениться за свои уникальные свойства. Этот металл в настоящее время активно применяется в быту и промышленности: машиностроении, авиации, приборостроении, электротехнической промышленности и многих других сферах жизнедеятельности человека. Здесь вы найдете увлекательные эксперименты с алюминием.
Атом алюминия и его общая характеристика
Чтобы понять, что из себя представляет атом алюминия, необходимо выделить из периодической системы Менделеева несколько его основных характеристик:
- порядковым номером металла является цифра 13;
- элемент расположен в третьем малом периоде, главной подгруппе, третьей группе;
- атомная масса элемента – 26,98;
- у элемента сильно выражены металлические свойства;
- алюминий имеет всего 27 изотопов с разными массовыми числами;
- элемент встречается в двух степенях окисления: 0 и +3.
Алюминий и его химические свойства
[Deposit Photos]Если рассматривать химические реакции, чистый алюминий — это сильный восстановитель, проявляющий высокую химическую активность в свободном виде. Чтобы многократно усилить его активность, необходимо убрать оксидную пленку. Алюминий способен вступать в реакции с серой, галогенами, кислотами и щелочами. В обычных условиях данный металл не способен взаимодействовать с водой, без нагревания может вступать в реакцию только с тремя галогенами: хлором, бромом и йодом. Важной химической характеристикой алюминия является способность металла восстанавливать некоторые другие элементы, а также их соединения.
Чтобы многократно усилить его активность, необходимо убрать оксидную пленку. Алюминий способен вступать в реакции с серой, галогенами, кислотами и щелочами. В обычных условиях данный металл не способен взаимодействовать с водой, без нагревания может вступать в реакцию только с тремя галогенами: хлором, бромом и йодом. Важной химической характеристикой алюминия является способность металла восстанавливать некоторые другие элементы, а также их соединения.
В какие реакции вступает алюминий
Взаимодействие с неметаллами: алюминий реагирует с углеродом, серой, азотом и остальными неметаллами (со многими – только после нагревания, без которого реакция не произойдет). В результате реакции происходит выделение большого количества тепла.
Взаимодействие с кислотами (например, с соляной): в результате выделяется водород.
via GIPHY
Взаимодействие с оксидами реакция замещения атомов металла в оксиде на алюминий позволяет получить большое количество теплоты и новый металл в свободном виде.
Взаимодействие с солями, а именно с растворами некоторых менее активных солей.
Взаимодействие со щелочами: по причине сильного взаимодействия с растворами щелочей, их растворы нельзя хранить в посуде из алюминия.
Алюминотермия — процесс восстановления металлов, сплавов и неметаллов посредством воздействия на их оксиды металлическим алюминием. Благодаря данной особенности алюминия, металлурги могут добывать такие тугоплавкие металлы, как молибден, вольфрам, цирконий, ванадий.
Физические свойства алюминия как простого вещества
В качестве простого вещества алюминий представляет собой металл серебристого цвета. Он способен окисляться на воздухе, покрываясь плотной оксидной пленкой.
Данная особенность металла обеспечивает его высокую стойкость к коррозии. Это свойство алюминия, наравне с другими характеристиками, делает его чрезвычайно популярным металлом, широко применяемым в быту. Кроме того, алюминий имеет легкий вес, сохраняя при этом высокую прочность и пластичность.
via GIPHY
Далеко не каждое известное людям вещество имеет совокупность подобных характеристик.
Физические свойства алюминия
Алюминий — пластичный и ковкий металл, применяется для изготовления тончайшей фольги, из алюминия прокатывают проволоку.
Температура кипения металла составляет 2518 °С.
Температура плавления алюминия составляет 660 °С.
Плотность алюминия составляет 2,7 г/см³.
Широкое применение алюминия в сферах жизнедеятельности обусловлено его химическими и физическими свойствами.
Характеристики, области применения и свойства алюминия
Алюминий
Искать Другие материалы
< Назад
Вы находитесь здесь:
Дата создания
Последнее обновление
Производство диэлектриков
Характеристики алюминия
Этот металл широко используется для компонентов в аэрокосмической, транспортной и строительной отраслях.
- Некоррозионный
- Легко обрабатывается и отливается
- Легкий, но прочный
- Немагнитный и искробезопасный
- Хороший проводник тепла и электричества
Применения для алюминия
- Корпуса электронных устройств
- Линии электропередач
- Радиаторы для транзисторов и процессоров
Свяжитесь со специалистом по производству диэлектриков, чтобы обсудить использование алюминия для ваших компонентов. 93 Dielectric Manufacturing, Ричфилд, Висконсин, США dielectricmfg. Свойства алюминиевого материала, предоставленные компанией Dielectric Manufacturing, Richfield, Wisconsin Алюминий — самый распространенный металл в мире и третий по распространенности элемент, составляющий 8% земной коры. Универсальность алюминия делает его наиболее широко используемым металлом после стали. Алюминий чаще всего сплавляют с медью, цинком, магнием, кремнием, марганцем и литием. Существует более 300 деформируемых сплавов, 50 из которых широко используются. Обычно они идентифицируются по четырехзначной системе, которая возникла в США и в настоящее время общепринята. Таблица 1 описывает систему для деформируемых сплавов. Литые сплавы имеют аналогичные обозначения и используют пятизначную систему. Таблица 1. Обозначения деформируемых алюминиевых сплавов. Легирующий элемент Нет (99%+ алюминий) — 1XXX Сплановый элемент Медь — 2xxx Спланный элемент Манганец — 3xxx Спланный элемент кремния — 4xxx Malloy -Element Magnesium — 5xxx Malloying Element Magnember + Silicon — 6xx Alloying Element ZINC -700077 -lementhing Alloying ZICL -70007 70007 7 -lementhing Zinc -70007 70007 70007 700067 7 7 7 7 7 7 7 7 7 7 7 7 7 7 7 7 7 7 7 Механический Предел текучести 3e7 — 5e8 Па 4,35 — 72,5 тыс.фунтов/кв.дюйм Прочность на растяжение 5,8e7 — 5e8 Па 8,41 — 79,8 тыс.  фунтов/кв.дюйм
фунтов/кв.дюйм Удлинение 0,01 — 0,44 % деформации % деформации 96 фунтов на кв. дюйм Термический Максимальная рабочая температура 120–210 °C 248–410 °F Температура плавления 475 — 677 °C 887 — 1,25e3 °F Изолятор или проводник Хороший Проводник Хороший дирижер Удельная теплоемкость 857 — 990 Дж/кг °C 0,205 — 0,236 БТЕ/фунт. °F Коэффициент теплового расширения 2.1e-5 — 2.4e-5 деформация/°C 11,7 — 13,3 мкстр/°F Электрика Изолятор или проводник Хороший проводник °C Хороший проводник °F Удельное электрическое сопротивление 2,5e-8 — 6,5e-8 °C 2,5 — 6,5 °F Эко След CO2 1,85–2,04 кг/кг 11,2–13,1 фунт/фунт Перерабатываемый Да Да  com
com – общая информация
Технические характеристики
Алюминий получают из минерального боксита. Бокситы превращаются в оксид алюминия (глинозем) с помощью процесса Байера. Затем глинозем преобразуется в металлический алюминий с использованием электролизеров и процесса Холла-Эру.
Мировой спрос на алюминий составляет около 29миллионов тонн в год. Около 22 миллионов тонн – это новый алюминий и 7 миллионов тонн – переработанный алюминиевый лом. Использование переработанного алюминия экономически и экологически выгодно. Для производства 1 тонны нового алюминия требуется 14 000 кВтч. И наоборот, для переплавки и переработки одной тонны алюминия требуется всего 5%. Нет никакой разницы в качестве между первичным и переработанным алюминиевыми сплавами.
И наоборот, для переплавки и переработки одной тонны алюминия требуется всего 5%. Нет никакой разницы в качестве между первичным и переработанным алюминиевыми сплавами.
Чистый алюминий мягок, пластичен, устойчив к коррозии и обладает высокой электропроводностью. Он широко используется для фольги и проводящих кабелей, но для обеспечения более высокой прочности, необходимой для других применений, необходимо легирование другими элементами. Алюминий — один из самых легких инженерных металлов, по соотношению прочности к весу превосходящий сталь.
Благодаря использованию различных комбинаций своих преимущественных свойств, таких как прочность, легкость, коррозионная стойкость, возможность вторичной переработки и формуемость, алюминий используется во все большем числе областей применения. Ассортимент продукции варьируется от конструкционных материалов до тонкой упаковочной пленки. Обозначения сплавов
 Также производятся небольшие добавки хрома, титана, циркония, свинца, висмута и никеля, и железо всегда присутствует в небольших количествах.
Также производятся небольшие добавки хрома, титана, циркония, свинца, висмута и никеля, и железо всегда присутствует в небольших количествах. Обозначения сплавов Продолжение…