Хром и его соединения
Хром
Открытие хрома относится к периоду бурного развития химико-аналитических исследований солей и минералов. В России химики проявляли особый интерес к анализу минералов, найденных в Сибири и почти неизвестных в Западной Европе. Одним из таких минералов была сибирская красная свинцовая руда (крокоит), описанная еще Ломоносовым. Минерал исследовался, но ничего, кроме окислов свинца, железа и алюминия в нем не было найдено. Однако в 1797 году Вокелен, прокипятив тонко измельченный образец минерала с поташом и осадив карбонат свинца, получил раствор, окрашенный в оранжево – красный цвет. Из этого раствора он выкристаллизовал рубиново-красную соль, из которой выделили окисел и свободный металл, отличный от всех известных металлов. Вокелен назвал его Хром (Chrome) от греческого слова — окраска, цвет; правда здесь имелось в виду свойство не металла, а его ярко окрашенных солей.
Нахождение в природе.
Важнейшей рудой хрома, имеющей практическое значение, является хромит, приблизительный состав которого отвечает формуле FeCrO4.

Он встречается в Малой Азии, на Урале, в Северной Америке, на юге Африки. Техническое значение имеет также вышеназванный минерал крокоит – PbCrO4. В природе встречаются также оксид хрома (3) и некоторые другие его соединения. В земной коре содержание хрома в пересчете на металл составляет 0,03%. Хром обнаружен на Солнце, звездах, метеоритах.
Физические свойства.
Хром – белый, твердый и хрупкий металл, исключительно химически стойкий к воздействию кислот и щелочей. На воздухе он окисляется, имеет на поверхности тонкую прозрачную пленку оксида. Хром имеет плотность 7,1 г/см3 , его температура плавления составляет +18750С.
Получение.
При сильном нагреве хромистого железняка с углем происходит восстановление хрома и железа:
FeO * Cr2O3 + 4C = 2Cr + Fe + 4CO
В результате этой реакции образуется сплав хрома с железом, отличающийся высокой прочностью. Для получения чистого хрома, его восстанавливают из оксида хрома(3) алюминием:
Cr2O3 + 2Al = Al2O3 + 2Cr
В данном процессе обычно используют два оксида – Cr2O3 и CrO3
Химические свойства.
Благодаря тонкой защитной пленке оксида, покрывающей поверхность хрома, он весьма устойчив к воздействию агрессивных кислот и щелочей. Хром не реагирует с концентрированными азотной и серной кислотами, а также с фосфорной кислотой. Со щелочами хром вступает во взаимодействие при t = 600-700оC. Однако хром взаимодействует с разбавленными серной и соляной кислотами, вытесняя водород:
2Cr + 3H2SO4 = Cr2(SO
2Cr + 6HCl = 2CrCl3 + 3H2
При высокой температуре хром горит в кислороде, образуя оксид(III).
Раскаленный хром реагирует с парами воды:
2Cr + 3H2O = Cr2O3 + 3H2
Хром при высокой температуре реагирует также с галогенами, галоген — водородами, серой, азотом, фосфором, углем, кремнием, бором, например:
Cr + 2HF = CrF2 + H2
2Cr + N2 = 2CrN
2Cr + 3S = Cr2S3
Cr + Si = CrSi
Вышеуказанные физические и химические свойства хрома нашли свое применение в различных областях науки и техники. Так, например, хром и его сплавы используются для получения высокопрочных, коррозионно-стойких покрытий в машиностроении. Сплавы в виде феррохрома используются в качестве металлорежущих инструментов. Хромированные сплавы нашли применение в медицинской технике, при изготовлении химического технологического оборудования.

Положение хрома в периодической системе химических элементов:
Хром возглавляет побочную подгруппу VI группы периодической системы элементов. Его электронная формула следующая:
+24Cr IS22S22P63S23P63d54S1
В заполнении орбиталей электронами у атома хрома нарушается закономерность, согласно которой сначала должна была бы заполнятся 4S – орбиталь до состояния 4S2. Однако, вследствие того, что 3d – орбиталь занимает в атоме хрома более выгодное энергетическое положение, происходит ее заполнение до значения 4d5. Такое явление наблюдается у атомов некоторых других элементов побочных подгрупп. Хром может проявлять степени окисления от +1 до +6. Наиболее устойчивыми являются cоединения хрома со степенями окисления +2, +3, +6.
Соединения двухвалентного хрома.
Оксид хрома (II) CrO – пирофорный черный порошок (пирофорность – способность в тонкораздробленном состоянии воспламенятся на воздухе). CrO растворяется в разбавленной соляной кислоте:
CrO + 2HCl = CrCl2 + H2O
На воздухе при нагревании свыше 1000С CrO превращается в Cr2O3.
Соли двухвалентного хрома образуются при растворении металлического хрома в кислотах. Эти реакции проходят в атмосфере малоактивного газа (например H2), т.к. в присутствии воздуха легко происходит окисление Cr(II) до Cr(III).
Гидроксид хрома получают в виде желтого осадка при действии раствора щелочи на хлорид хрома (II):
CrCl2 + 2NaOH = Cr(OH)2 + 2NaCl
Cr(OH)2 обладает основными свойствами, является восстановителем. Гидратированный ион Cr2+ окрашен в бледно – голубой цвет. Водный раствор CrCl 2 имеет синюю окраску. На воздухе в водных растворах соединения Cr(II) переходят в соединения Cr(III). Особенно это ярко выражается у гидроксида Cr(II):
4Cr(OH)2 + 2H2O + O2 = 4Cr(OH)3
Соединения трехвалентного хрома.
Оксид хрома (III) Cr2O3 – тугоплавкий порошок зеленого цвета. По твердости близок к корунду. В лаборатории его можно получить нагреванием дихромата аммония:
(NH4)2Cr2O7 = Cr2O3 + N2 + 4H2
Cr2O3 – амфотерный оксид, при сплавлении со щелочами образует хромиты: Cr2O3 + 2NaOH = 2NaCrO2 + H2O
Гидроксид хрома также является амфотерным соединением:
Cr(OH)3 + HCl = CrCl3 + 3H2O
Cr(OH)3 + NaOH = NaCrO
Безводный CrCl3 имеет вид листочков темно-фиолетового цвета, совершенно нерастворим в холодной воде, при кипячении он растворяется очень медленно. Безводный сульфат хрома (III) Cr2(SO4)3 розового цвета, также плохо растворим в воде. В присутствии восстановителей образует фиолетовый сульфат хрома Cr2(SO4)3*18H2O. Известны также зеленые гидраты сульфата хрома, содержащие меньшее количество воды. Хромовые квасцы KCr(SO4)2*12H2O выкристаллизовываются из растворов, содержащих фиолетовый сульфат хрома и сульфат калия. Раствор хромовых квасцов при нагревании становится зеленым благодаря образованию сульфатов.
Реакции с хромом и его соединениями
Почти все соединения хрома и их растворы интенсивно окрашены. Имея бесцветный раствор или белый осадок, мы можем с большой долей вероятности сделать вывод об отсутствии хрома.
- Сильно нагреем в пламени горелки на фарфоровой чашке такое количество бихромата калия, которое поместится на кончике ножа. Соль не выделит кристаллизационной воды, а расплавится при температуре около 400 0С с образование темной жидкости. Погреем ее еще несколько минут на сильном пламени. После охлаждения на черепке образуется зеленый осадок. Часть его растворим в воде ( она приобретает желтый цвет), а другую часть оставим на черепке. Соль при нагревании разложилась, в результате образовался растворимый желтый хромат калия K2CrO4 и зеленый Cr2O3.
- Растворим 3г порошкообразного бихромата калия в 50мл воды. К одной части добавим немного карбоната калия. Он растворится с выделением CO2, а окраска раствора станет светло – желтой. Из бихромата калия образуется хромат. Если теперь по порциям добавить 50% раствор серной кислоты, то снова появится красно – желтая окраска бихромата.
- Нальем в пробирку 5мл. раствора бихромата калия, прокипятим с 3мл концентрированной соляной кислоты под тягой. Из раствора выделяется желто-зеленый ядовитый газообразный хлор, потому, что хромат окислит HCl до Cl
- При добавлении раствора нитрата свинца выпадает желтый хромат свинца; при взаимодействии с раствором нитрата серебра образуется красно – коричневый осадок хромата серебра.
- Добавим пероксид водорода к раствору бихромата калия и подкислим раствор серной кислотой. Раствор приобретает глубокий синий цвет благодаря образованию пероксида хрома. Пероксид при взбалтывании с некоторым количеством эфира перейдет в органический растворитель и окрасит его в голубой цвет. Данная реакция специфична для хрома и очень чувствительна. С ее помощью можно обнаружить хром в металлах и сплавах. Прежде всего необходимо растворить металл. При длительном кипячении с 30% — ной серной кислотой (можно добавить и соляную кислоту) хром и многие стали частично растворяются. Полученный раствор содержит сульфат хрома (III). Чтобы можно было провести реакцию обнаружения, сначала нейтрализуем его едким натром. В осадок выпадает серо-зеленый гидроксид хрома (III), который растворится в избытке NaOH и образует зеленый хромит натрия. Профильтруем раствор и добавим 30% -ый пероксид водорода. При нагревании раствор окрасится в желтый цвет, так как хромит окислится до хромата. Подкисление приведет к появлению голубой окраски раствора. Окрашенное соединение можно экстрагировать, встряхивая с эфиром.
Аналитические реакции на ионы хрома.
- К 3-4 каплям раствора хлорида хрома CrCl3 прибавьте 2М раствор NaOH до растворения первоначально выпавшего осадка. Обратите внимание на цвет образовавшегося хромита натрия. Нагрейте полученный раствор на водяно бане. Что при этом происходит?
- К 2-3 каплям р-ра CrCl3 прибавьте равный объем 8М раствора NaOH и 3-4 капли 3% р-ра H2O2. Нагрейте реакционную смесь на водяной бане. Что при этом происходит? Какой осадок образуется, если полученный окрашеный раствор нейтрализовать, добавить к нему CH3COOH, а затем Pb(NO3)2?
- Налейте в пробирку по 4-5 капель растворов сульфата хрома Cr2(SO4)3, IMH2SO4 и KMnO4. Нагрейте реакционную смест в течение нескольких минут на водяной бане. Обратите внимание на изменение окраски раствора. Чем оно вызвано?
- К 3-4 каплям подкисленного азотной кислотой раствора K2Cr2O7 прибавьте 2-3 капли раствора H2O2 и перемешайте. Появляющиеся синее окрашивание раствора обусловлено возникновением надхромовой кислоты H2CrO6:
Cr2O72- + 4H2O2 + 2H+ = 2H2CrO6 + 3H2O
Обратите внимание на на быстрое разложение H2CrO6:
2H2CrO6 + 8H+ = 2Cr3+ + 3O2 + 6H2O
синий цвет зеленый цвет
Надхромовая кислота значительно более устойчива в органических растворителях.
- К 3-4 каплям подкисленного азотной кислотой раствора K2Cr2O7 прибавьте 5 капель изоамилового спирта, 2-3 капли раствора H2O2 и взболтайте реакционную смесь. Всплывающий на верх слой органического растворителя окрашен в ярко-синий цвет. Окраска исчезает очень медленно. Сравните устойчивость H2CrO6 в органической и водных фазах.
- При взаимодействии CrO42- и ионами Ba2+ выпадает желтый осадок хромата бария BaCrO4.
- Нитрат серебра образует с ионами CrO42- осадок хромата серебра кирпично-красного цвета.
- Возьмите три пробирки. В одну из них поместите 5- 6 капель раствора K2Cr2O7, во вторую – такой же объем раствора K2CrO4, а в третью – по три капли обоих растворов. Затем добавте в каждую пробирку по три капли раствора иодида калия. Объясните полученный результат. Подкислите раствор во второй пробирке. Что при этом происходит? Почему?
Занимательные опыты с соединениями хрома
- Смесь CuSO4 и K2Cr2O7 при добавлении щелочи становится зеленой, а в присутствии кислоты становится желтой. Нагревая 2мг глицерина с небольшим количеством (NH4)2Cr2O7 с последующим добавлением спирта, после фильтрования получается ярко-зеленый раствор, который при добавлении кислоты становится желтым, а в нейтральной или щелочной среде становится зеленым.
- Поместить в центр консервной банки с термитом «рубиновую смесь» — тщательно растертый и помещенный в алюминиевую фольгу Al2O3 (4,75г) с добавкой Cr2O3(0,25г). Чтобы банка подольше не остывала, необходимо закопать под верхний обрез в песок, а после поджигания термита и начала реакции, накрыть ее железным листом и засыпать песком. Банку выкопать через сутки. В итоге образуется красно – рубиновый порошок.
- 10г бихромата калия растирают с 5г нитрата натрия или калия и 10г сахара. Смесь увлажняют и смешивают с коллодием. Если порошок спрессовать в стеклянной трубке, а затем вытолкнуть палочку и поджечь ее с торца, то начнет выползать «змея», сначала черная, а после охлаждения — зеленая. Палочка диаметром 4 мм горит со скоростью около 2мм в секунду и удлиняется в 10 раз.
- Если смешать растворы сульфата меди и дихромата калия и добавить немного раствора аммиака, то выпадет аморфный коричневый осадок состава 4СuCrO4 * 3NH3 * 5H2O, который растворяется в соляной кислоте с образованием желтого раствора, а в избытке аммиака получается зеленый раствор. Если далее к этому раствору добавить спирт, то выпадет зеленый осадок, который после фильтрации становится синим, а после высушивания – сине-фиолетовым с красными блестками, хорошо видимыми при сильном освещении.
- Оставшийся после опытов «вулкан» или «фараоновы змеи» оксид хрома можно регенерировать. Для этого надо сплавить 8г Cr2O3 и 2г Na2CO3 и 2,5г KNO3 и обработать остывший сплав кипятком. Получается растворимый хромат, который можно превратить и в другие соединения Cr(II) и Cr(VI), в том числе и исходный дихромат аммония.
Примеры окислительно – восстановительных переходов с участием хрома и его соединений
1. Cr2O72- — Cr2O3 — CrO2— — CrO42- — Cr2O72-
a) (NH4)2Cr2O7 = Cr2O3 + N2 + 4H2O б) Cr2O3 + 2NaOH = 2NaCrO2 + H2O
б) Cr2O3 + 2NaOH = 2NaCrO2 + H2O
в) 2NaCrO2 + 3Br2 + 8NaOH = 6NaBr +2Na2CrO4 + 4H2O
г) 2Na2CrO4 + 2HCl = Na2Cr2O7 + 2NaCl + H2O
2. Cr(OH)2 — Cr(OH)3 — CrCl3 — Cr2O72- — CrO42-
а) 2Cr(OH)2 + 1/2O2 + H2O = 2Cr(OH)3
б) Cr(OH)3 + 3HCl = CrCl3 + 3H2O
в) 2CrCl3 + 2KMnO4 + 3H2O = K2Cr2O7 + 2Mn(OH)2 + 6HCl
г) K2Cr2O7 + 2KOH = 2K2CrO4 + H2O
3. CrO — Cr(OH)2 — Cr(OH)3 — Cr(NO3)3 — Cr2O3 — CrO—2
Cr2+
а) CrO + 2HCl = CrCl2 + H2O
б) CrO + H2O = Cr(OH)2
в) Cr(OH)2 + 1/2O2 + H2O = 2Cr(OH)3
г) Cr(OH)3 + 3HNO3 = Cr(NO3)3 + 3H2O
д) 4Сr(NO3)3 = 2Cr2O3 + 12NO2 + O2
е) Cr2O3 + 2 NaOH = 2NaCrO2 + H2O
Элемент хром в роли художника
Химики довольно часто обращались к проблеме создания искусственных пигментов для живописи. В XVIII-XIXвв была разработана технология получения многих живописных материалов. Луи Никола Воклен в 1797г., обнаруживший в сибирской красной руде ранее неизвестный элемент хром, приготовил новую, замечательно устойчивую краску – хромовую зелень. Хромофором ее является водный оксид хрома (III). Под названием « изумрудная зеленая» ее начали выпускать в 1837 году. Позже Л.Вокелен предложил несколько новых красок: баритовую, цинковую и хромовые желтые. Со временем они были вытеснены более стойкими желтыми, оранжевыми пигментами на основе кадмия.
Зеленая хромовая – самая прочная и светостойкая краска, не поддающаяся воздействию атмосферных газов. Растертая на масле хромовая зелень обладает большой кроющей силой и способна к быстрому высыханию, поэтому с XIX в. ее широко применяют в живописи. Огромное значение она имеет в росписи фарфора. Дело в том, что фарфоровые изделия могут декорироваться как подглазурной, так и надглазурной росписью. В первом случае краски наносят на поверхность лишь слегка обожженного изделия, которое затем покрывают слоем глазури. Далее следует основной, высокотемпературный обжиг: для спекания фарфоровой массы и оплавления глазури изделия нагревают до 1350 – 14500С. Столь высокую температуру без химических изменений выдерживают очень немногие краски, а в старину таких вообще было только две – кобальтовая и хромовая. Черный оксид кобальта, нанесенный на поверхность фарфорового изделия, при обжиге сплавляется с глазурью, химически взаимодействуя с ней. В результате образуются ярко-синие силикаты кобальта. Такую декарированную кобальтом синюю фарфоровую посуду все хорошо знают. Оксид хрома (III) не взаимодействует химически с компонентами глазури и просто залегает между фарфоровыми черепками и прозрачной глазурью «глухим» слоем.
Помимо хромовой зелени художники применяют краски, полученные из волконскоита. Этот минерал из группы монтмориллонитов (глинистый минерал подкласса сложных силикатов Na(Mo,Al), Si4O10(OH)2 был обнаружен в 1830г. русским минералогом Кеммерером и назван в честь М.Н Волконской – дочери героя битвы при Бородино генерала Н.Н. Раевского, жены декабриста С.Г.Волконского. Волконскоит представляет собой глину, содержащую до 24% оксида хрома, а так же оксиды аллюминея и железа (III). Непостоянство состава минерала, встечающегося на Урале, в Пермской и Кировской областях, обусловливает его разнообразную окраску – от цвета зимней потемневшей пихты до ярко-зеленого цвета болотной лягушки.
Пабло Пикассо обращался к геологам нашей страны с просьбой изучить запасы волконскоита, дающего краску неповторимо свежего тона. В настоящее время разработан способ получения искусственного волконскоита. Интересно отметить, что по данным современных исследований, русские иконописцы использовали краски из этого материала еще в средние века, задолго до его «официального» открытия. Известной популярностью пользовалась у художников и зелень Гинье (создана в 1837г.), хромоформ которой является гидрат окиси хрома Cr2O3 * (2-3) H2O, где часть воды химически связана, а часть адсорбирована. Этот пигмент придает краске изумрудный оттенок.
© blog.tutoronline.ru, при полном или частичном копировании материала ссылка на первоисточник обязательна.
blog.tutoronline.ru
формула, характеристика и химические свойства :: SYL.ru
Среди многообразия химических элементов и их соединений сложно выделить наиболее полезное для человечества вещество. Каждое уникально по своим свойствам и возможностям применения. Технический прогресс значительно облегчает исследовательский процесс, но и ставит перед ним новые задачи. Химические элементы, открытые несколько сотен лет назад и изученные во всех проявлениях, получают в современном мире более технологичные направления использования. Данная тенденция распространяется на соединения, существующие в природе и созданные людьми.
Оксид
В земной коре и на просторах Вселенной существует множество химических соединений, которые отличаются по классам, типам, характеристикам. Одним из самых распространенных видов соединений является оксид (окись, окисел). К нему относят песок, воду, углекислый газ, т. е. основополагающие вещества для существования человечества и всей биосферы Земли. Оксидами называют вещества, которые имеют в составе атомы кислорода со степенью окисления -2, при этом связь между элементами является бинарной. Их образование происходит в результате химической реакции, условия которой разнятся в зависимости от состава оксида.
Характерными признаками данного вещества являются три позиции: вещество сложное, состоит из двух атомов, один из них – кислород. Большое количество существующих оксидов объясняется тем, что многие химические элементы образуют несколько веществ. Они идентичны по составу, но атом, вступающий в реакцию с кислородом, проявляет несколько степеней валентности. Например, оксид хрома (2, 3, 4, 6), азота (1, 2, 3, 4 ,5) и т. д. При этом их свойства зависят от степени валентности элемента, вступающего в окислительную реакцию.
По принятой классификации оксиды бывают основными и кислотными. Также выделяется амфотерный вид, который проявляет свойства основного окисла. Кислотные оксиды – это соединения неметаллов или элементов с высокой валентностью, их гидратами являются кислоты. К основным окислам относят все вещества, имеющие связь кислород + металл, их гидратами являются основания.

Хром
В 18 веке химик И. Г. Леман обнаружил неизвестный минерал, который был назван красным сибирским свинцом. Профессор Парижской минералогической школы Вокелен провел ряд химических реакций с полученным образцом, в результате которых был выделен неизвестный металл. Основными свойствами, обозначенными ученым, стали его устойчивость к кислотным средам и тугоплавкость (жаропрочность). Название «хром» (Chromium) возникло из-за широкой цветовой гаммы, которая характеризуется соединениям элемента. Металл достаточно инертен, в чистом виде не встречается в природных условиях.
Основными минералами, содержащими хром, являются: хромит (FeCr2O4), меланохроит, вокеленит, дитцеит, тарапакаит. Химический элемент Cr располагается в 6 группе периодической системы Д. И. Менделеева, имеет атомный номер 24. Электронная конфигурация атома хрома позволяет элементу иметь валентность +2, +3, +6, при этом наиболее устойчивыми являются соединения трехвалентного металла. Возможны реакции, при которых степень окисления равна +1, +5, +4. Хром химически не активен, поверхность металла покрывается пленкой (эффект пассивирования), предотвращающей реакции с кислородом и водой при нормальных условиях. Оксид хрома, образующийся на поверхности, предохраняет металл от взаимодействия с кислотами и галогенами при отсутствии катализаторов. Соединения с простыми веществами (не металлами) возможны при температуре от 300 оС (хлор, бром, сера).
При взаимодействии со сложными веществами требуются дополнительные условия, например, с раствором щелочи реакция не происходит, с ее расплавами процесс происходит очень медленно. С кислотами хром вступает в реакцию при наличии в качестве катализатора высокой температуры. Оксид хрома можно получить из различных минералов путем воздействия температуры. В зависимости от будущей степени окисления элемента применяются концентрированные кислоты. При этом валентность хрома в соединении варьируется от +2 до +6 (высший оксид хрома).

Применение
За счет уникальных антикоррозийных свойств и жаропрочности большое практическое значение имеют сплавы на основе хрома. При этом в процентном соотношении его доля не должна превышать половины общего объема. Большим недостатком хрома является его хрупкость, что уменьшает возможности обработки сплавов. Наиболее распространенным способом применения металла является изготовление покрытий (хромирование). Защитная пленка может составлять слой в 0,005 мм, но она будет надежно предохранять металлическое изделие от коррозии и внешних воздействий. Соединения хрома используются для изготовления жаропрочных конструкций в металлургической промышленности (плавильные печи). Антикоррозийные покрытия декоративного направления (металлокерамика), специальная легированная сталь, электроды для сварочных аппаратов, сплавы на основе кремния, алюминия являются востребованными на мировых рынках. Оксид хрома за счет низкой возможности окисления и высокой жаропрочности служит катализатором многих химических реакций, протекающих при высоких температурах (1000 оС).

Двухвалентные соединения
Оксид хрома (2) CrO (закись) является порошком ярко-красного или черного цвета. В воде нерастворим, при нормальных условиях не окисляется, проявляет ярко выраженные основные свойства. Вещество твердое, тугоплавкое (1550 оС), не является токсичным. В процессе нагревания до 100 оС окисляется до Cr2O3. В слабых растворах азотной и серной кислот не растворяется, реакция происходит с хлороводородной кислотой.

Получение, применение
Данное вещество считается низшим оксидом. Имеет достаточно узкую сферу применения. В химической промышленности оксид хрома 2 используется для очистки углеводородов от кислорода, который он притягивает в процессе окисления при температуре свыше 100 оС. Получить закись двухвалентного хрома можно тремя способами:
- Разложением карбонила Cr(CO)6 при наличии в качестве катализатора высокой температуры.
- Восстанавливая при помощи фосфорной кислоты оксид хрома 3.
- Амальгама хрома окисляется кислородом или азотной кислотой.
Трехвалентные соединения

Для оксидов хрома степень окисления +3 является самой устойчивой формой вещества. Cr2O3 (хромовая зелень, сесквиоксид, эсколаид) в химическом отношении инертен, нерастворим в воде, имеет высокую температуру плавления (более 2000 оС). Оксид хрома 3 – зеленый тугоплавкий порошок, очень твердый, имеет амфотерные свойства. Вещество растворимо в концентрированных кислотах, реакция со щелочами происходит в результате сплавления. Может восстанавливаться до чистого металла при взаимодействии с сильным восстановителем.
Получение и применение
За счет высокой твердости (сопоставимой с корундом) наиболее распространено использование вещества в абразивных и полирующих материалах. Оксид хрома (формула Cr2O3) имеет зеленый цвет, поэтому его применяют в качестве пигмента при изготовлении стекол, красок, керамики. Для химической промышленности данное вещество используется как катализатор для протекания реакций с органическими соединениями (синтез аммиака). Трехвалентный оксид хрома применяется для создания искусственных драгоценных камней и шпинелей. Для получения используется несколько видов химических реакций:
- Окисление закиси хрома.
- Нагревание (прокаливанием) бихромата или хромата аммония.
- Разложение гидроксида трехвалентного хрома или шестивалентного оксида.
- Прокаливание хромата или бихромата ртути.
Шестивалентные соединения
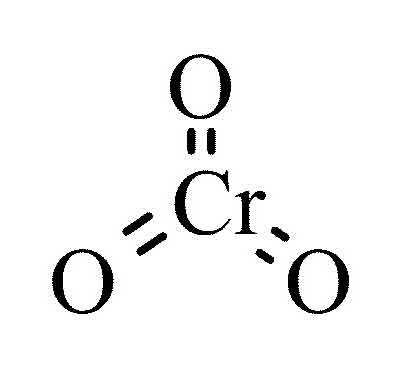
Формула высшего оксида хрома – CrO3. Вещество фиолетового или темно-красного цвета, может существовать в виде кристаллов, игл, пластин. Химически активен, токсичен, при взаимодействии с органическими соединениями существует опасность самовозгорания и взрыва. Оксид хрома 6 — хромовый ангидрид, трёхокись хрома — хорошо растворим в воде, при нормальных условиях взаимодействует с воздухом (расплывается), температура плавления – 196 оС. Вещество имеет ярко выраженные кислотные характеристики. При химической реакции с водой образуется дихромовая или хромовая кислота, без дополнительных катализаторов взаимодействует со щелочами (хроматы желтого цвета). Для галогенов (йод, сера, фосфор) является сильным окислителем. В результате нагревания свыше 250 оС образуется свободный кислород и трехвалентный оксид хрома.

Как получают и где применяют
Оксид хрома 6 получают обработкой хроматов (бихроматов) натрия или калия концентрированной серной кислотой либо при реакции хромата серебра с хлороводородной кислотой. Высокая химическая активность вещества обуславливает основные направления его применения:
- Получение чистого металла — хрома.
- В процессе хромирования поверхностей, в том числе электролитическим способом.
- Окисление спиртов (органических соединений) в химической промышленности.
- В ракетной технике используется в качестве воспламенителя топлива.
- В химических лабораториях очищает посуду от органических соединений.
- Используется в пиротехнической отрасли.
www.syl.ru
Оксид хрома
Несколько химических соединений, состоящих из двух простых элементов — Cr и O, — относятся к классу неорганических соединений — оксидов. Их общее название — оксид хрома, далее в скобках принято римскими цифрами указывать валентность металла. Другие их названия и химические формулы:
- хром (II) оксид — закись хрома, CrO;
- хром (III) оксид — хромовая зелень, сесквиоксид хрома, Cr2O3;
- хром (IV) оксид — окись хрома, CrO2;
- хром (VI) оксид — хромовый ангидрид, трехокись хрома, CrO3.
Соединение, в котором металл шестивалентен, и есть высший оксид хрома. Это твердое вещество без запаха, по внешнему виду представляющее собой темно-красные кристаллы (на воздухе они расплываются из-за сильной гигроскопичности). Молярная масса — 99,99 г/моль. Плотность при 20 °С равняется 2,70 г/см³. Температура плавления — 197 °С, кипения — 251 °С. При 0 °С в воде растворяется 61,7 г/100, при 25 °С — 63 г/100 мл, при 100 °С — 67,45 г/100 мл. Окисел также растворяется в серной кислоте (это хромовая смесь, которую используют в лабораторной практике для мытья химической посуды) и азотной кислоте, этиловом спирте, этиловом эфире, уксусной кислоте, ацетоне. При 450 °С разлагается до Cr2O3.
Хром (VI) оксид применяется в процессе электролиза (для получения чистого хрома), для хроматирования оцинкованных изделий, в электролитическом хромировании, как сильный окислитель (для производства индиго и изатина). Высший оксид хрома используется для обнаружения алкоголя в выдыхаемом воздухе. Взаимодействие протекает по схеме: 4CrO3 + 6h3SO4 + 3C2H5OH → 2Cr2(SO4)3 + 3Ch4COOH +9h3O. На наличие алкоголя указывает изменение окраски раствора (приобретает зеленый цвет).
Хром (VI) оксид, как и все соединения шестивалентного Cr, является сильным ядом (летальная доза — 0,1 г). Из-за своей высокой активности CrO3 вызывает возгорание (со взрывами) органических веществ при соприкосновении с ними. Несмотря на малую летучесть, высший оксид хрома опасен при вдыхании, так как вызывает рак легких. При контакте с кожей (даже при скором его удалении) вызывает раздражения, дерматиты, экземы, провоцирует развитие рака.
Окисел с четырехвалентным хромом CrO2 по внешнему виду представляет собой твердое вещество в виде черных тетраэдрических ферромагнитных кристаллов. Оксид хрома 4 имеет молярную массу 83,9949 г/моль, плотность 4,89 г/см³. Вещество плавится, одновременно разлагаясь, при температуре 375 °С. В воде не растворяется. Используется в носителях магнитной записи в качестве рабочего вещества. С ростом популярности компакт-дисков и DVD-дисков использование хрома (IV) оксида снизилось. Был впервые синтезирован в 1956 году химиком из компании EI DuPont Норман Л. Коксом путем разложения триоксида хрома в присутствии воды при температуре 640 °С и давлении 200 МПа. По лицензии DuPont выпускается компаниями Sony в Японии и BASF в Германии.
Оксид хрома 3 Cr2O3 представляет собой твердое мелкокристаллическое вещество от светло- до темно-зеленого цвета. Молярная масса равняется 151,99 г/моль. Плотность — 5,22 г/см³. Температура плавления — 2435 °С, кипения — 4000 °С. Показатель преломления чистого вещества — 2,551. Этот окисел не растворяется в воде, в спирте, ацетоне, кислоте. Поскольку его плотность приближается к плотности корунда, его вводят в составы полирующих средств (например, пасты ГОИ). Это один из основных оксидов хрома, который используется в качестве пигмента. Впервые по секретной технологии он был получен в 1838 году в виде прозрачной гидратированной формы. В природе встречается в виде хромистого железняка FeO•Cr2O3.
Окисел двухвалентного хрома — твердое вещество черного или красного цвета с температурой плавления 1550 °С. Плавится с разложением. Молярная масса — 67,996 г/моль. Оксид хрома (II) красного цвета не пирофорен, а это же вещество черного цвета является пирофорным. Порошок самовоспламеняется на воздухе, поэтому его можно хранить только под слоем в воды, так как с ней он не взаимодействует. Черную закись хрома получить в чистом виде очень сложно.
Для оксидов хрома с низшей валентностью характерны основные свойства, а для окисла с высшей валентностью — кислотные.
fb.ru
Хром — общая характеристика элемента, химические свойства хрома и его соединений
Хром — элемент побочной подгруппы 6-ой группы 4-го периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 24. Обозначается символом Cr (лат. Chromium). Простое вещество хром— твёрдый металл голубовато-белого цвета.
Химические свойства хрома
При обычных условиях хром реагирует только со фтором. При высоких температурах (выше 600°C) взаимодействует с кислородом, галогенами, азотом, кремнием, бором, серой, фосфором.
4Cr + 3O2 –t° →2Cr2O3
2Cr + 3Cl2 –t°→ 2CrCl3
2Cr + N2 –t°→ 2CrN
2Cr + 3S –t°→ Cr2S3
В раскалённом состоянии реагирует с парами воды:
2Cr + 3H2O → Cr2O3 + 3H2
Хром растворяется в разбавленных сильных кислотах (HCl, H2SO4)
В отсутствии воздуха образуются соли Cr2+, а на воздухе – соли Cr3+.
Cr + 2HCl → CrCl2 + H2
2Cr + 6HCl + O2 → 2CrCl3 + 2H2O + H2
Наличие защитной окисной плёнки на поверхности металла объясняет его пассив-ность по отношению к концентрированным растворам кислот – окислителей.
Соединения хрома
Оксид хрома (II) и гидроксид хрома (II) имеют основной характер.
Cr(OH)2 + 2HCl → CrCl2 + 2H2O
Соединения хрома (II) — сильные восстановители; переходят в соединения хрома (III) под действием кислорода воздуха.
2CrCl2 + 2HCl → 2CrCl3 + H2
4Cr(OH)2 + O2 + 2H2O → 4Cr(OH)3
Оксид хрома (III) Cr2O3 – зелёный, нерастворимый в воде порошок. Может быть получен при прокаливании гидроксида хрома (III) или дихроматов калия и аммония:
2Cr(OH)3 –t°→ Cr2O3 + 3H2O
4K2Cr2O7 –t°→ 2Cr2O3 + 4K2CrO4 + 3O2
(NH4)2Cr2O7 –t°→ Cr2O3 + N2+ 4H2O (реакция «вулканчик»)
Амфотерный оксид. При сплавлении Cr2O3 со щелочами, содой и кислыми солями получаются соединения хрома со степенью окисления (+3):
Cr2O3 + 2NaOH → 2NaCrO2 + H2O
Cr2O3 + Na2CO3 → 2NaCrO2 + CO2
При сплавлении со смесью щёлочи и окислителя получают соединения хрома в степени окисления (+6):
Cr2O3 + 4KOH + KClO3 → 2K2CrO4+ KCl + 2H2O
Гидроксид хрома (III) Сr(ОН)3 . Амфотерный гидроксид. Серо-зеленый, разлагается при нагревании, теряя воду и образуя зеленый метагидроксид СrО(ОН). Не растворяется в воде. Из раствора осаждается в виде серо-голубого и голубовато-зеленого гидрата. Реагирует с кислотами и щелочами, не взаимодействует с гидратом аммиака.
Обладает амфотерными свойствами — растворяется как в кислотах, так и в щелочах:
2Cr(OH)3 + 3H2SO4 → Cr2(SO4)3 + 6H2O Сr(ОН)3 + ЗН+ = Сr3+ + 3H2O
Cr(OH)3 + KOH → K[Cr(OH)4] , Сr(ОН)3 + ЗОН— (конц.) = [Сr(ОН)6]3-
Cr(OH)3 + KOH → KCrO2+2H2O Сr(ОН)3 + МОН = МСrO2(зел.) + 2Н2O (300—400 °С, М = Li, Na)
Сr(ОН)3→(120oC –H2O) СrO(ОН) →(430-10000С –H2O) Cr2O3
2Сr(ОН)3 + 4NаОН(конц.) + ЗН2O2(конц.) =2Na2СrO4 + 8Н20
Получение: осаждение гидратом аммиака из раствора солей хрома(Ш):
Сr3+ + 3(NH3 Н2O) = Сr(ОН)3↓ + ЗNН4+
Cr2(SO4)3 + 6NaOH → 2Cr(OH)3 ↓+ 3Na2SO4 (в избытке щелочи — осадок растворяется)
Соли хрома (III) имеют фиолетовую или тёмно-зелёную окраску. По химическим свойствам напоминают бесцветные соли алюминия.
Соединения Cr (III) могут проявлять и окислительные, и восстановительные свойства:
Zn + 2Cr+3Cl3 → 2Cr+2Cl2 + ZnCl2
2Cr+3Cl3 + 16NaOH + 3Br2 → 6NaBr + 6NaCl + 8H2O + 2Na2Cr+6O4
Соединения шестивалентного хрома
Оксид хрома (VI) CrO3 — ярко-красные кристаллы, растворимые в воде.
Получают из хромата (или дихромата) калия и H2SO4(конц.).
K2CrO4 + H2SO4 → CrO3 + K2SO4 + H2O
K2Cr2O7 + H2SO4 → 2CrO3 + K2SO4 + H2O
CrO3 — кислотный оксид, со щелочами образует жёлтые хроматы CrO42-:
CrO3 + 2KOH → K2CrO4 + H2O
В кислой среде хроматы превращаются в оранжевые дихроматы Cr2O72-:
2K2CrO4 + H2SO4 → K2Cr2O7 + K2SO4 + H2O
В щелочной среде эта реакция протекает в обратном направлении:
K2Cr2O7 + 2KOH → 2K2CrO4 + H2O
Дихромат калия – окислитель в кислой среде:
К2Сr2O7 + 4H2SO4 + 3Na2SO3 = Cr2(SO4)3 + 3Na2SO4 + K2SO4 + 4H2O
K2Cr2O7 + 4H2SO4 + 3NaNO2 = Cr2(SO4)3 + 3NaNO3 + K2SO4 + 4H2O
K2Cr2O7 + 7H2SO4 + 6KI = Cr2(SO4)3 + 3I2 + 4K2SO4 + 7H2O
K2Cr2O7 + 7H2SO4 + 6FeSO4 = Cr2(SO4)3 + 3Fe2(SO4)3 + K2SO4 + 7H2O
Хромат калия К2 CrО4. Оксосоль. Желтый, негигроскопичный. Плавится без разложения, термически устойчивый. Хорошо растворим в воде (желтая окраска раствора отвечает иону СrO42-), незначительно гидролизуется по аниону. В кислотной среде переходит в К2Cr2O7. Окислитель (более слабый, чем К2Cr2O7). Вступает в реакции ионного обмена.
Качественная реакция на ион CrO42- — выпадение желтого осадка хромата бария, разлагающегося в сильнокислотной среде. Применяется как протрава при крашении тканей, дубитель кож, селективный окислитель, реактив в аналитической химии.
Уравнения важнейших реакций:
2K2CrO4+H2 SO4(30%)=K2Cr2O7 +K2SO4 +H2O
2K2CrO4(т)+16HCl(конц.,гор.) =2CrCl3+3Cl2↑+8H2O+4KCl
2K2CrO4+2H2O+3H2S=2Cr(OH)3↓+3S↓+4KOH
2K2CrO4+8H2O+3K2S=2K[Сr(ОН)6]+3S↓+4KOH
2K2CrO4+2AgNO3=KNO3+Ag2CrO4(красн.)↓
Качественная реакция:
К2СгO4 + ВаСl2 = 2КСl + ВаCrO4↓
2ВаСrO4(т)+ 2НСl (разб.) = ВаСr2O7(p)+ ВаС12 + Н2O
Получение: спекание хромита с поташом на воздухе:
4(Сr2Fe‖‖)O4 + 8К2CO3 + 7O2 = 8К2СrO4 + 2Fе2O3 + 8СO2 (1000 °С)
Дихромат калия K2Cr2O7 . Оксосоль. Техническое название хромпик. Оранжево-красный, негигроскопичный. Плавится без разложения, при дальнейшем нагревании разлагается. Хорошо растворим в воде (оранжевая окраска раствора отвечает иону Сr2O72- ). В щелочной среде образует К2CrO4 . Типичный окислитель в растворе и при сплавлении. Вступает в реакции ионного обмена.
Качественные реакции — синее окрашивание эфирного раствора в присутствии Н2O2 , синее окрашивание водного раствора при действии атомарного водорода.
Применяется как дубитель кож, протрава при крашении тканей, компонент пиротехнических составов, реагент в аналитической химии, ингибитор коррозии металлов, в смеси с Н2SO4 (конц.) — для мытья химической посуды.
Уравнения важнейших реакций:
4К2Cr2O7=4K2CrO4+2Cr2O3+3O2 (500-600o C)
K2Cr2O7(т)+14HCl (конц) =2CrCl3+3Cl2↑+7H2O+2KCl (кипячение)
K2Cr2O7(т)+2H2SO4(96%) ⇌2KHSO4+2CrO3+H2O (“хромовая смесь”)
K2Cr2O7+KOH (конц ) =H2O+2K2CrO4
Cr2O72- +14H+ +6I— =2Cr3+ +3I2↓+7H2O
Cr2O72- +2H+ +3SO2(г)=2Cr3+ +3SO42- +H2O
Cr2O72- +H2O +3H2S(г)=3S↓+2OH— +2Cr2(OH)3↓
Cr2O72- (конц )+2Ag+(разб.) =Ag2Cr2O7 (т. красный)↓
Cr2O72-(разб.) +H2O +Pb2+=2H+ + 2PbCrO4 (красный)↓
K2Cr2O7(т) +6HCl+8H0(Zn)=2CrCl2(син)+7H2O+2KCl
Получение: обработка К2СrO4 серной кислотой:
2К2СrO4 + Н2SO4(30%) = К2Cr2O7 + К2SO4 + Н2O
himege.ru
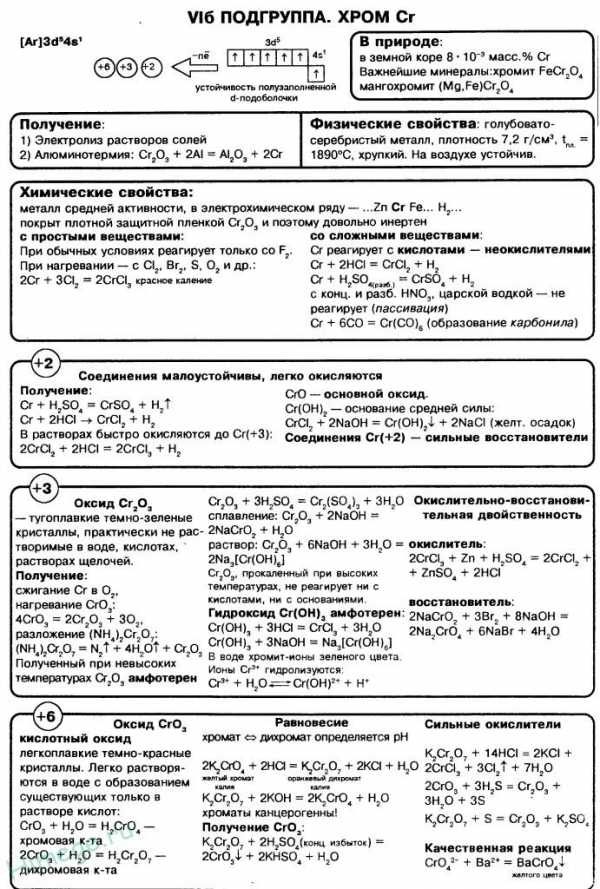
64. Оксиды и гидроксиды хрома
Хром образует три оксида: CrО, Cr2О3 и CrО3. Оксид хрома II (CrО) – основный оксид – черный порошок. Сильный восстановитель. CrО растворяется в разбавленной соляной кислоте: CrО + 2НСl = CrСl2 + Н2О.
При нагревании на воздухе выше 100 °C CrО превращается в Cr2О3: 4CrО + О2 = 2Cr2О3.
Оксид хрома III (Cr2О3) – тугоплавкий порошок зеленого цвета (температура плавления – 2265 °C). Твердость кристаллов близка к корунду, поэтому его вводят в состав полирующих средств. Получают из хромистого железняка (FeCr2O4). При окислительно-щелочном сплавлении последнего с содой образуются хромат натрия NaCrO4: 2Fe(CrO2)2 + 4Na2CO3 + 1/2O2 = 4Na2CrO4 + Fe2O3 + 4CO2.
Затем Na2CrO4 переводят в Na2Cr2O7 – дихромат: Na2CrO4 + Н2SO4 = Na2Cr2O7 + Н2О + Na2SO4.
Далее дихромат восстанавливают углем и получают Cr2О3: Na2Cr2O7 + 2С = Na2CO3 + Cr2О3 + СО?.
В лаборатории Cr2О3 получают термическим разложением дихромата аммония: (Nh5)2Cr2O7?Cr2О3 + N2 + 4Н2О.
Cr2О3 – амфотерный оксид: реагирует с основаниями и кислотами при сплавлении его со щелочами образует хромиты: Cr2О3 + NaОН = 2NaCrO2 + Н2О.
Оксид хрома VI (CrО3) – темно-красные кристаллы, хорошо растворимые в воде. CrО3 – кислотный оксид, с избытком воды образует хромовую кислоту: CrO3 + h3O?h3CrO4.
CrO3 – ангидрид хромовой кислоты. При большой концентрации CrO3 образуются дихромовая кислота: 2CrO3 + h3O?h3CrO7.
CrO3 при нагревании до 250 °C разлагается: 4CrO3?2Cr2О3 + 3О2?.
Получение: взаимодействием дихромата калия с концентрированной h3S04 : К2CrO7 + Н2SO4 = CrO3? + К2SO4 + h3O. CrO3 – сильный окислитель – окисляет йод, серу, уголь, фосфор, превращаясь при этом в Cr2 О3.
Гидроксид хрома II Сг(ОН)2 желтого цвета, в воде не растворим, обладает основными свойствами, является восстановителем, получается действием щелочи на хлорид хрома CrСl2, получаемого при взаимодействии Cr c НСl:
Соединения Cr II неустойчивы и легко окисляются кислородом воздуха:
Гидроксид хрома III (Cr(OH)3)n – это сложный полимер зеленого цвета, не растворимый в воде, обладает амфотерными свойствами – растворяется в кислотах и в щелочах; реагирует с кислотами с образованием солей хрома (III):
со щелочами – с образованием сине-фиолетовых растворов – гидроксохромитов:
При сплавлении Cr(ОН)3 со щелочами получают хромиты, а с избытком – метахромиты:
65. Хроматы и дихроматы
Хроматы – соли хромовой кислоты Н2Сг04, существующей лишь водных растворах с концентрацией не выше 75 %. Валентность хрома в хроматах – 6. Хроматы щелочных металлов и магния имеют хорошую растворимость в воде, а растворимость щелочноземельных металлов очень резко снижается в ряду CaCrO4 – SrCrO4 – BaCrO4 – RaCrO4. Хроматы – желтые кристаллические вещества – желтую окраску обеспечивает хромат-ион Сг042- . Дихроматы – соли дихромовой кислоты Н2Сг07 . В отличие от хроматов, почти все соли-дихроматы хорошо растворимы в воде. Дихроматы имеют ярко-оранжевую окраску, обеспеченную дихромат-ионом: Сг072-. Хромат и дихромат-ионы способны к взаимопревращению в зависимости от кислотности среды: если раствор подкислить, то хромат-ионы будут переходить в дихромат-ионы по схеме:
Если добавить щелочи, то пойдет обратная реакция:
Хроматы получают взаимодействием оксида хрома (VI) или раствора хромовой кислоты h3CrO4 с оксидами, гидроксидами, карбонатами металлов или при обменной реакции с участием растворимых солей-хроматов, или путем окисления комплексных солей – гидроксохроматов в избыточном растворе щелочи:
Хромат калия K2CrO 4 – кристаллы желтого цвета, при нагревании краснеют. Кристаллогидратов не образует. Дихроматы – сильные окислители:
Получают дихроматы из соединений Cr (III) в кислой среде:
Дихромат аммония (Nh5)2Cr2O7 – оранжевые кристаллы, не образует кристаллогидратов. При слабом нагревании он самовоспламеняется с выбросом искр – раскаленных частиц Cr2O3 , N2 и паров воды – «химический вулкан».
Дихромат калия K2Cr2O7?2h3O и Na2Cr2O7 – хромпики, оранжево-красные кристаллы, кристаллогидратов не образует. Используется в пиротехнике, в хроматометрии, в производстве спичек. Смесь равных объемов раствора K2Cr2O7 и концентрированной серной кислоты – хромовая смесь – является очень сильным окислителем, в лабораториях применяется для мытья стеклянной посуды. Хроматы применяются для протравы семян, при крашении, в лакокрасочной, кожевенной (в качестве дубящих реагентов кожи), текстильной промышленности; используются в лабораторном способе разделения хрома-тов кальция, стронция и бария.
Наиболее распространенным в природе, минералом является минерал PbCrO 4 – крокоит . Хромат – тарапакаит и дихромат калия – лопецит – также являются природными минералами.
studfiles.net
описание, свойства, формула и характеристика
Хром – химический элемент с атомным номером 24. Это твердый, блестящий, серо-стального цвета металл, который хорошо полируется и не тускнеет. Используется в сплавах, таких как нержавеющая сталь, и в качестве покрытия. Организму человека требуются небольшие количества трехвалентного хрома для метаболизма сахара, но Cr (VI) очень токсичен.
Различные соединения хрома, такие как окись хрома (III) и хромат свинца, ярко окрашены и используются в красках и пигментах. Красный цвет рубина обусловлен наличием этого химического элемента. Некоторые вещества, особенно бихромат калия и натрия, являются окислителями, используемыми для окисления органических соединений и (вместе с серной кислотой) для очистки лабораторной посуды. Кроме того, окись хрома (VI) применяется в производстве магнитной ленты.

Открытие и этимология
История открытия химического элемента хром такова. В 1761 году Иоганн Готлоб Леман нашел в Уральских горах оранжево-красный минерал и назвал его «сибирским красным свинцом». Хотя он ошибочно был идентифицирован как соединение свинца с селеном и железом, материал на самом деле являлся хроматом свинца с химической формулой PbCrO4. Сегодня он известен как минерал кроконт.
В 1770 году Петр Симон Паллас посетил то место, где Леман нашел красный свинцовый минерал, который имел очень полезные свойства пигмента в красках. Использование сибирского красного свинца в качестве краски получило быстрое развитие. Кроме того, ярко-желтый цвет из кроконта стал модным.
В 1797 году Николя-Луи Воклен получил образцы красной свинцовой руды. Путем смешивания кроконта с соляной кислотой он получил оксид CrO3. Хром как химический элемент был выделен в 1798 году. Воклен получил его при нагревании окисла с древесным углем. Он также смог обнаружить следы хрома в драгоценных камнях, таких как рубин и изумруд.
В 1800-х годах Cr в основном применялся в составе красок и кожевенных солей. Сегодня 85% металла используется в сплавах. Остальная часть применяется в химической промышленности, производстве огнеупорных материалов и литейной промышленности.
Произношение химического элемента хром соответствует греческому χρῶμα, что означает «цвет», из-за множества цветных соединений, которые из него можно получить.

Добыча и производство
Элемент производят из хромита (FeCr2O4). Примерно половина этой руды в мире добывается в Южной Африке. Кроме того, Казахстан, Индия и Турция являются его крупными производителями. Разведанных месторождений хромита достаточно, но географически они сконцентрированы в Казахстане и на юге Африки.
Залежи самородного металлического хрома встречаются редко, но они есть. Например, его добывают на шахте «Удачная» в России. Она является кимберлитовой трубкой, богатой алмазами, и восстановительная среда помогла образоваться чистому хрому и алмазам.
Для промышленного производства металла хромитовые руды обрабатывают расплавленной щелочью (едким натром, NaOH). При этом образуется хромат натрия (Na2CrO4), который восстанавливается углеродом до оксида Сг2O3. Металл получают при нагревании окисла в присутствии алюминия или кремния.
В 2000 году было добыто около 15 млн т хромитовой руды, которая была переработана в 4 млн т феррохрома, на 70% состоящего из сплава хрома с железом, приблизительная рыночная стоимость которых составила 2,5 млрд долларов США.

Основные характеристики
Характеристика химического элемента хрома обусловлена тем, что он является переходным металлом четвертого периода таблицы Менделеева и расположен между ванадием и марганцем. Входит в VI группу. Плавится при температуре 1907 °С. В присутствии кислорода хром быстро образует тонкий слой оксида, который защищает металл от дальнейшего взаимодействия с кислородом.
Как переходный элемент, он реагирует с веществами в различных соотношениях. Таким образом он образует соединения, в которых имеет различные степени окисления. Хром – химический элемент с основными состояниями +2, +3 и +6, из которых +3 является наиболее устойчивым. Кроме того, в редких случаях наблюдаются состояния +1, +4 и +5. Соединения хрома в степени окисления +6 представляют собой сильные окислители.
Какого цвета хром? Химический элемент придает анодированному алюминию рубиновый оттенок. Сг2O3, используемый для полировки металла, также применяется в качестве пигмента под названием «хромовая зелень». Его соли окрашивают стекло в изумрудно-зеленый цвет. Хром – химический элемент, присутствие которого делает рубин красным. Поэтому он используется в производстве синтетических рубинов.

Изотопы
Изотопы хрома обладают атомным весом от 43 до 67. Обычно данный химический элемент состоит из трех стабильных форм: 52Cr, 53Cr и 54Cr. Из них наиболее распространен 52Cr (83,8% всего природного хрома). Кроме того, описаны 19 радиоизотопов, из которых наиболее стабильным является 50Cr с периодом полураспада, превышающим 1,8×1017 лет. У 51Cr период полураспада – 27,7 дней, а у всех остальных радиоактивных изотопов он не превышает 24 ч, причем у большинства из них он длится менее одной минуты. Элемент также имеет два метасостояния.
Изотопы хрома в земной коре, как правило, сопутствуют изотопам марганца, что находит применение в геологии. 53Cr образуется при радиоактивном распаде 53Mn. Соотношение изотопов Mn/Cr подкрепляет другие сведения о ранней истории Солнечной системы. Изменения в соотношениях 53Cr/52Cr и Mn/Cr из разных метеоритов доказывает то, что новых атомные ядра были созданы непосредственно перед формированием Солнечной системы.

Химический элемент хром: свойства, формула соединений
Оксид хрома (III) Сг2O3, также известный как полуторная окись, является одним из четырех окислов этого химического элемента. Его получают из хромита. Соединение зеленого цвета обычно называют «хромовой зеленью», когда используют в качестве пигмента для живописи по эмали и стеклу. Оксид может растворяться в кислотах, образуя соли, а в расплавленной щелочи – хромиты.
Бихромат калия
K2Cr2O7 является мощным окислителем и ему отдается предпочтение в качестве средства для очистки лабораторной посуды от органики. Для этого используется его насыщенный раствор в концентрированной серной кислоте. Иногда, однако, его заменяют бихроматом натрия, исходя из более высокой растворимости последнего. Кроме того, он может регулировать процесс окисления органических соединений, преобразуя первичный спирт в альдегид, а затем в углекислоту.
Бихромат калия способен вызвать хромовый дерматит. Хром, вероятно, является причиной сенсибилизации, ведущей к развитию дерматита, особенно рук и предплечий, который носит хронический характер и трудно излечим. Как и другие соединения Cr (VI), бихромат калия канцерогенен. С ним нужно обращаться в перчатках и соответствующими средствами защиты.

Хромовая кислота
Соединение обладает гипотетической структурой H2CrO4. Ни хромовая, ни дихромовая кислоты не встречаются в природе, но их анионы находят в различных веществах. «Хромовая кислота», которую можно встретить в продаже, на самом деле является ее кислотным ангидридом – триоксидом CrO3.
Хромат свинца (II)
PbCrO4 обладает ярко-желтой окраской и практически не растворим в воде. По этой причине он нашел применение в качестве красящего пигмента под названием «желтый крон».
Cr и пятивалентная связь
Хром отличается своей способностью образовывать пятивалентные связи. Соединение создается Cr (I) и углеводородным радикалом. Пятивалентная связь формируется между двумя атомами хрома. Его формула может быть записана как Ar–Cr–Cr–Ar, где Ar представляет собой специфическую ароматическую группу.

Применение
Хром – химический элемент, свойства которого обеспечили ему множество различных вариантов применения, некоторые из которых приведены ниже.
Металлам он придает устойчивость к коррозии и глянцевую поверхность. Поэтому хром входит в состав таких сплавов, как нержавеющая сталь, используемых, например, в столовых приборах. Он также применяется для нанесения хромированного покрытия.
Хром является катализатором различных реакций. Из него делают формы для обжига кирпича. Его солями дубят кожу. Бихромат калия применяют для окисления органических соединений, таких как спирты и альдегиды, а также для очистки лабораторной посуды. Он служит фиксирующим агентом для окрашивания ткани, а также используется в фотографии и фотопечати.
CrO3 применяется для изготовления магнитных лент (например, для аудиозаписи), которые обладают лучшими характеристиками, чем пленки с оксидом железа.
Роль в биологии
Трехвалентный хром – химический элемент, необходимый для метаболизма сахара в организме человека. Напротив, шестивалентный Cr очень токсичен.
Меры предосторожности
Металлический хром и соединения Cr (III), как правило, не считаются опасными для здоровья, но вещества, содержащие Cr (VI), могут быть токсичными, если их принимать внутрь или вдыхать. Большинство таких веществ оказывают раздражающее действие на глаза, кожу и слизистые оболочки. При постоянном воздействии соединения хрома (VI) могут вызвать повреждение глаз, если их не лечить должным образом. Кроме того, это признанный канцероген. Смертельная доза данного химического элемента – около половины чайной ложки. Согласно рекомендациям Всемирной организации здравоохранения, предельно допустимая концентрация Cr (VI) в питьевой воде составляет 0,05 мг на литр.
Так как соединения хрома используются в красителях и для дубления кожи, они часто встречаются в почве и грунтовых водах заброшенных промышленных объектов, требующих экологической очистки и восстановления. Грунтовка, содержащая Cr (VI), до сих пор широко применяется в аэрокосмической промышленности и автомобилестроении.
Свойства элемента
Основные физические свойства хрома следующие:
- Атомное число: 24.
- Атомный вес: 51,996.
- Температура плавления: 1890 °C.
- Температура кипения: 2482 °C.
- Степень окисления: +2, +3, +6.
- Конфигурация электронов: [Ar]3d54s1.
fb.ru
Соединения хрома
Оксид хрома(II) и гидроксид хрома(II) имеют основной характер
Cr(OH)+2HCl→CrCl+2HO
Соединение хрома(II)-сильные восстановители; переходят в соединение хрома(III) под действием кислорода воздуха.
2CrCl+ 2HCl → 2CrCl+ H
4Cr(OH)+O+ 2HO→4Cr(OH)
Оксид хрома(III) CrO- зеленый, нерастворимый в воде порошок. Может быть получен при прокаливании гидроксида хрома(III) или дихроматов калия и аммония:
2Cr(OH)-→CrO+ 3HO
4KCrO-→ 2CrO + 4KCrO + 3O
(NH)CrO-→ CrO+ N+ HO
С концентрированными растворами кислот и щелочей взаимодействует с трудом:
Сr2О3 + 6 КОН + 3Н2О = 2К3[Сr(ОН)6]
Сr2О3 + 6НСl = 2СrСl3 + 3Н2О
Гидроксид хрома (III) Сr(ОН)3 получают при действии щелочей на на растворы солей хрома (III):
СrСl3 +3КОН = Сr(ОН)3↓ + 3КСl
Гидроксид хрома (III) представляет собой осадок серо – зеленого цвета, при получении которого, щелочь надо брать в недостатке. Полученный таким образом гидроксид хрома (III), в отличие от соответствующего оксида легко взаимодействует с кислотами и щелочами, т.е. проявляет амфотерные свойства:
Сr(ОН)3 + 3НNО3 = Сr(NО3)3 + 3Н2О
Сr(ОН)3 + 3КОН = К3[Сr(ОН)6](гексагидроксохромит К)
При сплавлении Сr(ОН)3 со щелочами получаются метахромиты и ортохромиты:
Cr(OH)3 + KOH = KCrO2(метахромит К) + 2H2O
Cr(OH)3 + KOH = K3CrO3(ортохромит К)+ 3H2O
Соединения хрома(VI).
Оксид хрома (VI) — СrО3 – темно – красное кристаллическое вещество, хорошо растворимо в воде – типичный кислотный оксид. Этому оксиду соответствует две кислоты:
СrО3 + Н2О = Н2СrО4 (хромовая кислота – образуется при избытке воды)
СrО3 + Н2О =Н2Сr2О7 (дихромовая кислота – образуется при большой концентрации оксида хрома (3)).
Оксид хрома (6) – очень сильный окислитель, поэтому энергично взаимодействует с органическими веществами:
Окисляет также иод, серу, фосфор, уголь:
При нагревании до 2500С оксид хрома (6) разлагается:
Оксид хрома (6) можно получить при действии концентрированной серной кислоты на твердые хроматы и дихроматы:
Хромовая и дихромовая кислоты.
Хромовая и дихромовая кислоты существуют только в водных растворах, образуют устойчивые соли, соответственно хроматы и дихроматы. Хроматы и их растворы имеют желтую окраску, дихроматы – оранжевую.
Хромат — ионы СrО42- и дихромат – ионы Сr2О72- легко переходят друг в друга при изменении среды растворов
В кислой среде раствора хроматы переходят в дихроматы:
В щелочной среде дихроматы переходят в хроматы:
При разбавлении дихромовая кислота переходит в хромовую кислоту:
Зависимость свойств соединений хрома от степени окисления.
Степень окисления | +2 | +3 | +6 |
Оксид | СrО | Сr2О3 | СrО3 |
Характер оксида | основной | амфотерный | кислотный |
Гидроксид | Сr(ОН)2 | Сr(ОН)3 – Н3СrО3 | Н2СrО4 Н2Сr2О7 |
Характер гидроксида | основной | амфотерный | кислотный |
→ ослабление основных свойств и усиление кислотных→ | |||
Окислительно – восстановительные свойства соединений хрома.
Реакции в кислотной среде.
В кислотной среде соединения Сr+6 переходят в соединения Сr+3 под действием восстановителей: H2S, SO2, FeSO4
Реакции в щелочной среде.
В щелочной среде соединения хрома Сr+3 переходят в соединения Сr+6 под действием окислителей: J2, Br2, Cl2, Ag2O, KClO3, h3O2, KMnO4:
studfiles.net

