Оксид бария
Наиболее распространенное применение вещества «оксид бария» основано на его свойстве гигроскопичности — умении вбирать в себя воду. Именно поэтому непосредственно в химическом производстве оно используется как компонент для получения пероксида бария. В промышленности оксид незаменим при производстве керамических магнитов. Кроме того, в современных условиях оксид бария, формула которого BaO, нашел огромное применение в микроэлектронике и электротехнике. Для производства магнитокерамики используют феррат бария, который получают путем соединения в мощном магнитном поле под прессом смеси порошков оксидов бария и железа.
Однако главным направлением применения является производство термоэмиссионных катодов. Еще в начале прошлого века ученый из Германии Венельт занимался изучением закона испускания электронов, который был совсем недавно открыт английским исследователем Ричардсоном. Для опытов Венельт использовал куски проволоки из платины. Первые опытные результаты полностью подтверждали выводы, сделанные впоследствии английским физиком. Но потом опыт не удался, и Венельт предположил, что поток электронов намного превышает норму потому, что на поверхности рабочего вещества – платины – могли появиться какие-либо примеси. Проверив свое предположение, Венельт установил, что источником отклонения величины потока электронов является оксид бария, попавший на поверхность платины в составе смазки технических устройств, используемых в эксперименте. Выводы Венельта долгое время оставались непризнанными, потому что ученое сообщество не могло экспериментально воспроизвести его опыт. Понадобилось почти сто лет для того, чтобы английский физик Колер доказал правоту Венельта. Колер на основании многократных опытов доказал, что если оксид бария подвергнуть постепенному подогреву при низком давлении, то интенсивность термоэлектронной эмиссии стремительно возрастает.
Только в тридцатые годы прошлого века немецкий ученый-химик Поль высказал предположение, состоящее в том, что электроны активизируются именно из-за наличия примеси бария в оксиде. В ходе реакции, которая проводится при низком давлении, часть кислорода улетучивается из оксида. Остающийся при этом барий ионизируется и тем самым способствует появлению свободных электронов. Эти электроны и были теми, которые покидали кристаллическую структуру при нагревании и которые когда-то наблюдал Венельт.
И лишь в начале второй половины прошлого века была окончательно доказана справедливость данной гипотезы. Химики А. Бундель и П. Ковтун (СССР) смогли не только численно установить величину концентрации примесей бария в оксиде, но и экспериментальным путем сопоставить ее значение с величиной потока термоэмиссии. Именно поэтому оксид бария используется в качестве активного вещества при изготовлении термоэмиссионных катодов. В качестве примера можно привести пучок электронов, с помощью которого создается изображение на экране простого телевизора или монитора компьютера. В качества источника потока здесь выступает оксид бария.
Если это вещество попытаться растворить в воде, то обнаруживается, что оксид бария реагирует с водой при нагревании раствора. При этом получается вещество гидроксид бария — белый порошок с температурой плавления всего 78°C. Это соединение отлично взаимодействует с углекислым газом, а потому водный раствор, часто называемый «баритовой водой», широко применяется в качестве реактива для углекислого газа.
В качестве исходного и необходимого компонента соединение входит в состав различных красящих материалов, смазок и масел. Такое использование оксида бария предсказывал еще Д.И. Менделеев.
fb.ru
Оксид бария — это… Что такое Оксид бария?
Оксид бария — одно из бинарных неорганических веществ, имеющее химическую формулу BaO. Является основным оксидом.
Описание
Оксид бария при стандартных условиях представляет собой бесцветные кристаллы с кубической решёткой [2]. Из-за высокой химической активности рекомендуется применять меры предосторожности.
Получение
1. Взаимодействие металлического бария с кислородом:
В этом случае наряду с оксидом бария образуется пероксид бария:
2. Разложение карбоната бария при нагревании:
Химические свойства
1. Энергичное взаимодействие с водой с образованием щёлочи и выделением тепла:
2. Взаимодействие с кислотными оксидами с образованием соли:
3. Взаимодействие с кислотами с образованием соли и воды:
4. Взаимодействие с кислородом при температуре около 600 °C с образованием пероксида:
5. Восстановление до металла при нагревании с магнием, цинком, алюминием и кремнием
Применение
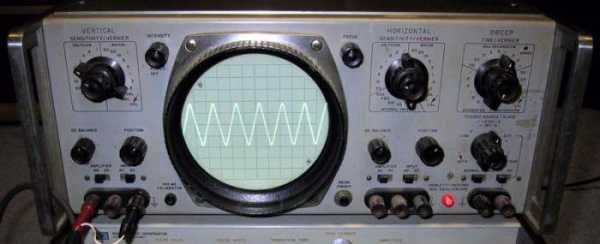
Оксид бария применяется для покрытия катодов, в экранно-лучевых трубках, для производства некоторых видов стекла, например , оптического. В некоторых реакциях используется как катализатор.
Примечания
dic.academic.ru
получение и применение :: ashanet.ru
Многообразие окружающего мира не перестает удивлять человечество. Исследователи открывают перед нами новые горизонты, основываясь на полученных результатах предыдущего поколения. В этом смысле химия – наука, которая не может быть полностью изученной, современные технологические решения находят наиболее оптимальные и необходимые области применения для уже познанных человечеством элементов. XIX век стал временем открытий, XXI – периодом более эффективного их использования. Например, оксид бария, — вещество, изученное многосторонне, но кто знает, какие новые технологии будут связаны с ним в будущем.
Барий
Щелочноземельный металл, который входит в состав земной коры привлек внимание химиков в XVIII веке. Первое упоминание об этом элементе связано с его кислородным соединением – оксидом бария. Он имеет очень высокую для своего вида плотность, поэтому получил название «тяжелый», которое в дальнейшем стало названием самого элемента. Металл химически активен, поэтому для его получения в чистом виде необходимо провести ряд реакций в присутствии катализатора. Наиболее распространенным в природе минералом, содержащим барий, является его сульфат BaSO4 (тяжелый шпат барит) и BaCO3 (витерит). Именно с данными соединениями связан процесс получения такого вещества, как оксид бария. В дальнейшем оно используется для выделения металла в чистом виде и имеет собственные направления применения.

Важнейшие соединения
Как и все типичные металлы, барий вступает в химическую реакцию с кислородом, при этом полученное вещество зависит от условий процесса и катализатора. Например, простая реакция окиси с водой дает возможность образовывать Ba(OH)2 — гидроксид бария. Оксид бария получают из нитрата. Типичны соединения со всеми галогенами: BaF2, BaCI2, BaI2, BaS, BaBr2. Образование нитратов, сульфидов, сульфатов, происходит за счет взаимодействия минералов с соответствующими кислотными растворами. На сегодняшний день все важнейшие соединения бария находят свое применение. Но исключить новые открытия в сферы использования данного вещества нельзя, с ростом технологичности приборов его значение будет только возрастать как на промышленном, так и на бытовом уровне.

Оксиды
Бинарная связь химического элемента с кислородом наиболее распространенная форма вещества в природе. При этом оксиды образуют металлы и неметаллы. Именно характеристика элемента при взаимодействии с кислородом стала основой формирования периодической системы Менделеева Д. И. Для металлургической отрасли наиболее приемлемым способом выделения вещества является процесс его получения из оксида. Предварительно металлическая природная руда (соли металлов) подвергается различным химическим воздействиям, направленным на получение окиси. Как правило, данный процесс сопровождается нагреванием до необходимой температуры. Исключением не является и оксид бария. Формула полученного вещества имеет вид: BaO. Оксиды можно получить и другими способами. Например, из гидроксидов, солей и самих оксидов более высокой степени окисления.
Оксид бария
Прежде всего необходимо отметить, что все соединения данного металла токсичны (исключение составляет сульфат), поэтому требуется соблюдать элементарные правила безопасности при работе. Это касается многих химических элементов. Другое название – барит безводный — не следует путать с сульфатом, который является природным минералом. В нормальных (стандартных) условиях белые кристаллы или порошок, иногда бесцветные с типичной решеткой кубического вида, являются соединением металла с кислородом и называются оксид бария. Формула вещества — BaO. Техническая модификация оксида может иметь серый цвет, который ему придает уголь, не полностью выведенный из состава.

Физические свойства
Типичное агрегатное состояние оксида твердое, плотность 5,72 (200С), молярная масса – 153,34 г/моль. Соединение имеет достаточно высокую теплопроводность 4,8-7,8 Вт/(мК)(80-1100К), и тугоплавкость температура кипения – 20000С, плавления – 19200С. Оксид бария был открыт в 1774 году Шееле Карлом Вильгельмом.
Получение
Существует несколько способов выделения такого вещества, как оксид бария. Применяются они в соответствии с поставленной целью и количеством получаемого вещества. Для лабораторных и промышленных условий подходят все способы, поэтому как получить оксид бария выбирает производитель. Применяемые методы:
- Кальцинированием предварительно осажденного нитрата бария, которое происходи с выделением чистого кислорода. 2Ba(NO3)2 = 2BaO + 4NO2 + O2.
- Реакция взаимодействия с кислородом металлического бария. 2Ba + O2 = 2BaO. Катализатором служит температура 500-6000С, в этом случае не исключено получение пероксида. 2Ba + O2 = 2BaO2. При дальнейшем нагревании до 7000С вещество распадается на свободный кислород и оксид бария.
- Для процесса разложения карбоната бария на оксид и углекислый газ необходимо воздействие высокой температуры. BaCO3 = BaO + CO2. Для получения более чистого конечного вещества необходимо удалить излишки углекислорода.
Химические свойства
Большинство бинарных соединений металла с кислородом проявляют основные свойства. Уравнение оксида бария (формула ВаО) показывает, что данное вещество относится именно к таким окислам. При этом данное соединение является солеобразующим. Типичные химические взаимодействия происходят со следующими классами веществ:
- Взаимодействие с водой происходит достаточно бурно, с выделением тепла и образование щелочного раствора. BaO + H2O = Ba(OH)2.
- С кислородом оксид взаимодействует при наличии катализатора (высокая температура 600-5000С), результатом является пероксид, разлагаемый в дальнейшем на составные части для выделения чистого металла или оксида. При этом необходимо увеличить нагрев до 7000С. 2Ba + O2 = 2BaO2.
- Как типичный основной оксид бария взаимодействует с кислотами, в результате химической реакции получается вода и соответствующая соль. BaO + H2SO4 = H2O + BaSO4 или BaO + 2HCI = H2O + BaCI2.
- Кислотные оксиды вступают в реакцию с BaO, результатом взаимодействия являются соли. BaO + CO2 = BaCO3 или BaO + SO3 = BaSO4.
- Для высвобождения чистого бария оксид прокаливают с металлами, которые забирают выделяемый кислород. В качестве таковых выступают кремний, алюминий, цинк или магний.
Применение
Барий и его соединения дают очень мощную яркость цвета при покрытии поверхности других веществ. Поэтому оксиды марганца и бария служат единицами измерения коэффициента яркости. Используется для получения зеленого цвета в пиротехнике, при декоративной отделке в составе глазурей и эмалей. Достаточно низкая стоимость обработки и получения, высокий уровень выделения тепла дает возможность использования окисла в качестве катализатора при проведении химических реакций. В частности, данное вещество применяется для выделения чистого металла (Ва), получения гидроксида и пероксида. Производство керамики, используемой при наиболее низких температурах (жидкий азот), происходит с участием оксида бария. В процесс синтеза включаются редкоземельные металлы и окись меди. Достаточно широк спектр применения вещества в приборостроении. Оксид бария используется для покрытия осциллографических и телевизионных трубок, различных видов катодов, электронновакуумных изделий. Служит в качестве активной массы для мощных аккумуляторов медноокисного вида. Оксид бария является одним из основных элементов в составе стекла, которое имеет достаточно специфичное направление применения, используется для покрытия поверхности стержней из урана. Для создания оптических стекол данное вещество так же незаменимо.
ashanet.ru
Оксид бария — Википедия (с комментариями)
Материал из Википедии — свободной энциклопедии
Оксид бария — соединение бария с кислородом, имеющее химическую формулу BaO. Является основным оксидом. При стандартных условиях представляет собой бесцветные кристаллы с кубической решёткой [1].
Получение
1. Взаимодействие металлического бария с кислородом:
<math>\mathsf{2Ba + \ O_2 \longrightarrow 2 \ BaO}</math>
В этом случае наряду с оксидом бария образуется пероксид бария:
<math>\mathsf{Ba + \ O_2 \longrightarrow \ BaO_2}</math>
2. Разложение карбоната бария при нагревании:
<math>\mathsf{BaCO_3 \longrightarrow \ BaO + \ CO_2 \uparrow}</math>
3. Разложение нитрата бария при нагревании. 2Ba(NO3)2 = 2BaO + 4NO2 + O2
Химические свойства
1. Энергичное взаимодействие с водой с образованием щёлочи и выделением тепла:
<math>\mathsf{BaO + \ H_2O \longrightarrow \ Ba(OH)_2}</math>
2. Взаимодействие с кислотными оксидами с образованием соли:
<math>\mathsf{BaO + \ CO_2 \longrightarrow \ BaCO_3}</math>
<math>\mathsf{BaO + \ SO_3 \longrightarrow \ BaSO_4 \downarrow}</math>
3. Взаимодействие с кислотами с образованием соли и воды:
<math>\mathsf{BaO + 2\ HCl \longrightarrow \ BaCl_2 + \ H_2O}</math>
<math>\mathsf{BaO + \ H_2SO_4 \longrightarrow \ BaSO_4 \downarrow + \ H_2O}</math>
4. Взаимодействие с кислородом при температуре около 600 °C с образованием пероксида:
<math>\mathsf{2BaO + O_2 \longrightarrow \ 2BaO_2}</math>
5. Восстановление до металла при нагревании с магнием, цинком, алюминием и кремнием [3].
Применение
Поскольку работа выхода оксида бария низка, то при невысокой стоимости и технологичности он давно и широко применяется для покрытия катодов различных электронно-вакуумных приборов, телевизионных, осциллографических трубках и др.
Также используется для производства некоторых видов стекла, например, оптического.
В некоторых реакциях используется как катализатор.
Яркость поверхности, покрытой оксидом бария или оксидом магния, принимается за единицу при измерениях коэффициента яркости других поверхностей.
Напишите отзыв о статье «Оксид бария»
Примечания
- ↑ [www.xumuk.ru/encyklopedia/471.html Описание оксида бария на XuMuK.Ru]
- ↑ [www.xumuk.ru/spravochnik/378.html Оксид бария на XuMuK.Ru]
- ↑ Фрумина Н. С., Горюнова Н. Н., Еременко С. Н. Аналитическая химия бария — Москва: Наука, 1977. — 200 с
Отрывок, характеризующий Оксид бария
– Михаил Феоклитыч, – обратился он к эсаулу, – ведь это опять от немца. Он пг’и нем состоит. – И Денисов рассказал эсаулу, что содержание бумаги, привезенной сейчас, состояло в повторенном требовании от генерала немца присоединиться для нападения на транспорт. – Ежели мы его завтг’а не возьмем, они у нас из под носа выг’вут, – заключил он.В то время как Денисов говорил с эсаулом, Петя, сконфуженный холодным тоном Денисова и предполагая, что причиной этого тона было положение его панталон, так, чтобы никто этого не заметил, под шинелью поправлял взбившиеся панталоны, стараясь иметь вид как можно воинственнее.
– Будет какое нибудь приказание от вашего высокоблагородия? – сказал он Денисову, приставляя руку к козырьку и опять возвращаясь к игре в адъютанта и генерала, к которой он приготовился, – или должен я оставаться при вашем высокоблагородии?
– Приказания?.. – задумчиво сказал Денисов. – Да ты можешь ли остаться до завтрашнего дня?
– Да как тебе именно велено от генег’ала – сейчас вег’нуться? – спросил Денисов. Петя покраснел.
– Да он ничего не велел. Я думаю, можно? – сказал он вопросительно.
– Ну, ладно, – сказал Денисов. И, обратившись к своим подчиненным, он сделал распоряжения о том, чтоб партия шла к назначенному у караулки в лесу месту отдыха и чтобы офицер на киргизской лошади (офицер этот исполнял должность адъютанта) ехал отыскивать Долохова, узнать, где он и придет ли он вечером. Сам же Денисов с эсаулом и Петей намеревался подъехать к опушке леса, выходившей к Шамшеву, с тем, чтобы взглянуть на то место расположения французов, на которое должно было быть направлено завтрашнее нападение.
– Ну, бог’ода, – обратился он к мужику проводнику, – веди к Шамшеву.
Денисов, Петя и эсаул, сопутствуемые несколькими казаками и гусаром, который вез пленного, поехали влево через овраг, к опушке леса.
Дождик прошел, только падал туман и капли воды с веток деревьев. Денисов, эсаул и Петя молча ехали за мужиком в колпаке, который, легко и беззвучно ступая своими вывернутыми в лаптях ногами по кореньям и мокрым листьям, вел их к опушке леса.
Денисов и Петя подъехали к нему. С того места, на котором остановился мужик, были видны французы. Сейчас за лесом шло вниз полубугром яровое поле. Вправо, через крутой овраг, виднелась небольшая деревушка и барский домик с разваленными крышами. В этой деревушке и в барском доме, и по всему бугру, в саду, у колодцев и пруда, и по всей дороге в гору от моста к деревне, не более как в двухстах саженях расстояния, виднелись в колеблющемся тумане толпы народа. Слышны были явственно их нерусские крики на выдиравшихся в гору лошадей в повозках и призывы друг другу.
– Пленного дайте сюда, – негромко сказал Денисоп, не спуская глаз с французов.
wiki-org.ru