Плавка черного металла. Особенности, последовательность и технологии плавки в мартеновской печи.
Главная » Обработка металла » Плавка
Плавка
Автор perminoviv На чтение 4 мин Просмотров 435 Опубликовано
Во всем мире дорожают добыча руд и получение из них цветных металлов. Правильная последовательность плавки черного металла обеспечивает надежность работы оборудования, машин и механизмов всех отраслей промышленного производства.
Содержание
- Подготовка сырья к плавке
- Выплавка черного металла в мартеновских печах
- Мартеновская плавка черного металла: последовательность, технология
Подготовка сырья к плавке
Производство черного металла требует определенной подготовки исходных материалов как по качеству, так и по размеру кусков. Самой простой является подготовка кокса, от которого отделяют мелочь. Флюсы дробят в специальных дробилках и сортируют по размеру кусков на специальных грохотах. Специальная подготовка руды дает возможность повысить производительность доменной печи и снизить расходы топлива. Основными операциями подготовки руд является измельчение, сортировка, обогащение, обжиг и спекание.
Специальная подготовка руды дает возможность повысить производительность доменной печи и снизить расходы топлива. Основными операциями подготовки руд является измельчение, сортировка, обогащение, обжиг и спекание.
Промывание водой позволяет отделить от железной руды часть песчано-глинистой пустой породы. Магнитная сепарация заключается в том, что измельченную руду помещают в магнитное поле. Магнит притягивает частицы руды, содержащие оксиды железа и имеют магнитные свойства, отделяя их от пустой породы.
В результате обогащения получают концентраты — продукты с повышенным содержанием железа.
Процесс спекания руд мелких фракций, концентрата, колошникового пыли, оборота агломерата (отходов) называется агломерация. Эти материалы смешивают с измельченным твердым топливом (кокситом), увлажняют и подают в агломерационная машина, в которой температура в слое шихты достигает 1300-1600°С.
Выплавка черного металла в мартеновских печах
Производство черного металла в мартеновских печах на отечественных металлургических заводах составляет около 60% (мировое производство — < 20%).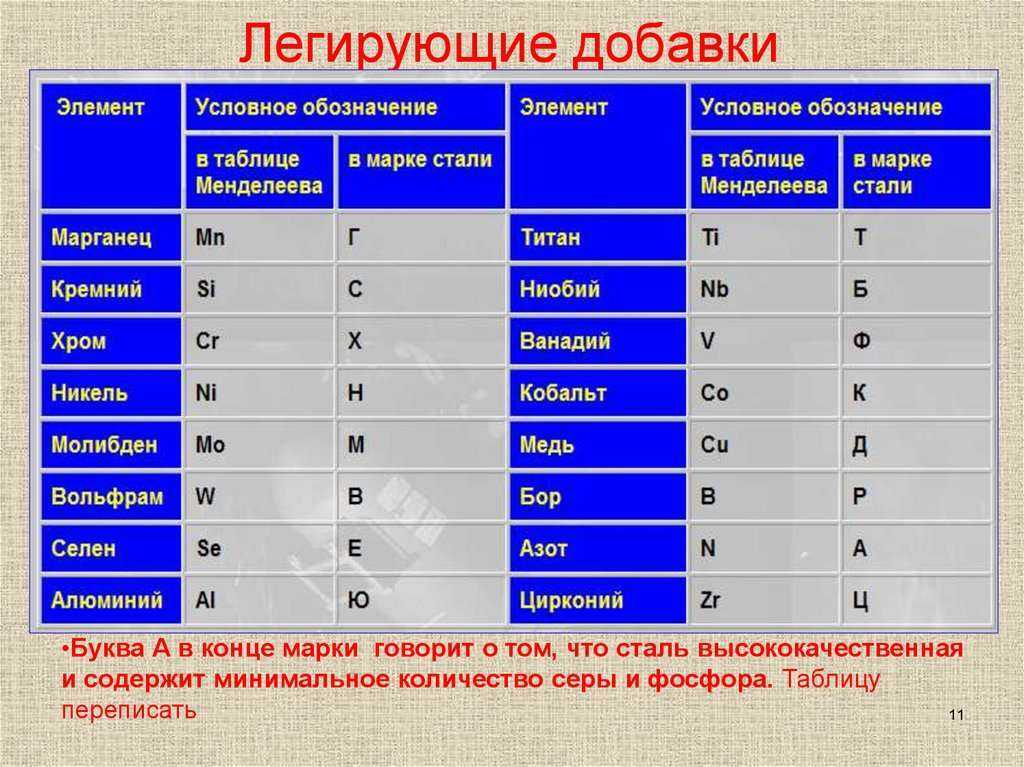 Мартеновская печь (рис. 1) по строению и принципу работы является регенеративною печью. Топливо и воздух, проходя через насадки регенераторов 1 и 2, где они нагреваются до температуры 1000…1200 С, по вертикальным каналам 3 и 4 подаются в “головку” печи 9 и из нее в рабочее пространство печи 5. При сгорании топлива образуется факел с температурой 1800…19000 С. Как топливо для мартеновских печей применяется природный газ, мазут и смешанный газ (смесь коксового и доменного газа). Это топливо имеет сравнительно невысокую теплоту сгорания и мартеновские печи в этом случае должны регенераторы для газа и воздуха (рис. 1).
Мартеновская печь (рис. 1) по строению и принципу работы является регенеративною печью. Топливо и воздух, проходя через насадки регенераторов 1 и 2, где они нагреваются до температуры 1000…1200 С, по вертикальным каналам 3 и 4 подаются в “головку” печи 9 и из нее в рабочее пространство печи 5. При сгорании топлива образуется факел с температурой 1800…19000 С. Как топливо для мартеновских печей применяется природный газ, мазут и смешанный газ (смесь коксового и доменного газа). Это топливо имеет сравнительно невысокую теплоту сгорания и мартеновские печи в этом случае должны регенераторы для газа и воздуха (рис. 1).
- 1, 2 — топливные и воздушные регенераторы;
- 3, 4 — вертикальные каналы для подачи топлива и воздуха;
- 5 — рабочее пространство печи;
- 6 — под печи;
- 7 — своды печи;
- 8 — загрузочные окна;
- 9 — головка печи;
- 10 — перекидные клапаны.
Основная же масса стали выплавляется в печах, которые работают на высококалорийных топливах – природном газе и мазуте. В этих случаях достаточно иметь только одну пару регенераторов — для воздуха, что значительно упрощает конструкцию и эксплуатацию печей.
В этих случаях достаточно иметь только одну пару регенераторов — для воздуха, что значительно упрощает конструкцию и эксплуатацию печей.
Для визуального наблюдения за ходом плавки внутреннее пространство печи должно быть хорошо освещено, что обеспечивается светом факела пламени. Факел природного газа плохо светится, поэтому для подсветки факела одновременно с газом в печь вводят до 30…40% мазута. Примесь мазута также делает факел более тяжелым и настилочным.
Масса плавки мартеновских печей на металлургических заводах составляет 300…500 т с размерами ванны до 120 м.
Мартеновская плавка черного металла: последовательность, технология
Подавляющее большинство металла выплавляется в основных мартеновских печах. В основных мартеновских печах осуществляется как скрап-процесс и скрап-рудный процесс. Шихта состоит из стального лома (55…75%) и чугуна в чушках (25…45%). Соотношение между стальным ломом и чушковым чугуном рассчитывают из таких соображений, что во время загрузки и плавления выгорает из шихты 30…40% углерода. Флюсом является известняк (5…10% от массы металла). Для ускорения окисления примесей используют железную руду.
Флюсом является известняк (5…10% от массы металла). Для ускорения окисления примесей используют железную руду.
Загрузки (в завалку) мартеновской печи осуществляют через окна 8 (рис. 2): сначала стальной лом, затем чугун. После расплавления металлической шихты начинается энергичное окисление углерода, то есть начинается период «кипения». На данный момент ванна покрывается шлаком, источником которого являются продукты окисления составляющих металла, продукты разъедание футеровки, загрязнения, внесенные шихтой, ржавчина на металлоломе.
Преимущества:
- Можно выплавлять любые углеродистые легированные стали.
- При выплавке можно использовать дорогие материалы (чугун, металлолом, руду).
Недостатки:
- Большой расход топлива.
- Длительный процесс выплавки.
Этапы выплавки стали | Металлургический портал MetalSpace.ru
Первый этап
На этом этапе идет расплавление шихты и нагрев жидкого металла. Температура металла невысока. Начинается интенсивное окисление железа, так как оно содержится в наибольшем количестве в чугуне и по закону действующих масс окисляется в первую очередь. Одновременно начинает окис-лятся примеси Si, P, Mn. Образующийся оксид железа (FeO) при высоких температурах растворяется в железе и отдает свой кислород более активным элементом (примесям в чугуне), окисляя их. Чем больше оксида железа содержится в жидком металле, тем активнее окисляются примеси. Для ускорения окисления примесей в сталеплавильную печь добавляют железную руду, окалину, содержащие оксиды же-леза.
Температура металла невысока. Начинается интенсивное окисление железа, так как оно содержится в наибольшем количестве в чугуне и по закону действующих масс окисляется в первую очередь. Одновременно начинает окис-лятся примеси Si, P, Mn. Образующийся оксид железа (FeO) при высоких температурах растворяется в железе и отдает свой кислород более активным элементом (примесям в чугуне), окисляя их. Чем больше оксида железа содержится в жидком металле, тем активнее окисляются примеси. Для ускорения окисления примесей в сталеплавильную печь добавляют железную руду, окалину, содержащие оксиды же-леза.
Скорость окисления примесей зависит не только от их концентрации, но и от температуры металла и подчиняется принципу, в соответствии с которым хи-мические реакции, выделяющие теплоту, протекают интенсивнее при более низких температурах, а реакции поглощающие теплоту, протекают активнее при высоких температурах. Поэтому в начале плавки, когда температура металла невысока, интенсивнее идут процессы окисления кремния, фосфора, марганца, протекающие с выделением теплоты, а углерод интенсивно окисляется только при высокой температуре металла.
Наиболее важной задачей этого этапа является удаление фосфора. Для этого необходимо проведение плавки в основной печи, в которой можно использовать основной шлак, содержащий СаО, применяемый для удаления фосфора. В ходе плавки фосфорный ангидрид Р2О5 образует с оксидом железа нестойкое соединение (FeO)3⋅Р2О5. Оксид кальция СаО более сильное основание, чем оксид железа. Поэтому при невысоких температурах он связывает ангидрид Р2О5 в прочное соединение , (CaO)⋅Р2О5 переводя его в шлак. Для удаления фосфора из металла шлак должен содержать достаточное количество оксида железа FeO. Для повышения содержания FeO в шлаке в сталеплавильную печь в этот период плавки добавляют железную руду, окалину, наводя железистый шлак. По мере удаления фосфора из металла в шлак содержание его в шлаке возрастает. В соответствии с законом распределения, когда вещество растворяется в двух несмешивающихся жидкостях, распределение его между этими жидкостями происходит до установления определенного соотношения постоянного для данной температуры. Поэтому удаление фосфора из металла замедляется и для более полного удаления фосфора из металла шлак, содержащий фосфор удаляют, и наводят новый со свежими добавками (CaO).
Поэтому удаление фосфора из металла замедляется и для более полного удаления фосфора из металла шлак, содержащий фосфор удаляют, и наводят новый со свежими добавками (CaO).
Второй этап
Этап начинается по мере прогрева металлической ванны до более высоких температур, чем на первом этапе. При повышении температуры более интенсивно протекает реакция окисления углерода, проходящая с поглощением тепла. Для окисления углерода на этом этапе в металл вводят зна-чительное количество руды, окалины или вдувают кислород.
Образующийся в металле оксид железа реагирует с углеродом и пузырьки оксида углерода СО выделяются из жидкого металла, вызывая кипение ванны. При кипении ванны:
- уменьшается содержание углерода в металле;
- выравнивается температура и состав ванны;
- удаляются частично неметаллические включения в шлак.
- Все это способствует повышению качества металла.
В этот же период создаются условия для удаления серы из металла. Сера в ванне находится в виде сульфида железа, растворенного в металле [FeS] и шла-ке (FeS). Чем выше температура, тем большее количество FeS растворяется в шлаке или больше серы переходят из металла в шлак. Сульфид железа, раство-ренный в шлаке, взаимодействует с оксидом кальция СаО, также растворенным в шлаке, образуя соединение CaS, которое растворимо в шлаке, но не растворя-ется в металле. Таким образом сера удаляется в шлак.
Сера в ванне находится в виде сульфида железа, растворенного в металле [FeS] и шла-ке (FeS). Чем выше температура, тем большее количество FeS растворяется в шлаке или больше серы переходят из металла в шлак. Сульфид железа, раство-ренный в шлаке, взаимодействует с оксидом кальция СаО, также растворенным в шлаке, образуя соединение CaS, которое растворимо в шлаке, но не растворя-ется в металле. Таким образом сера удаляется в шлак.
Третий этап
Этот этап является завершающим, в котором производится раскисление и, если требуется, легирование стали. Раскисление представляет собой технологическую операцию, при которой растворенный в металле кислород переводится в нерастворимое соединение и удаляется из металла. При плавке повышенное содержание кислорода в металле необходимо для окисления примесей. В готовой же стали кислород является нежелательной примесью, так как понижает механические свойства стали, особенно при высоких температурах.
Для раскисления стали используют элементы-ракислители, обладающие большим сродством к кислороду, чем железо.
- осаждающий способ;
- диффузионный.
Осаждающий способ
Раскисление по этому способу осуществляют введением в жидкую сталь раскислителей (ферромарганца, ферросилиция, алю-миния), содержащих Mn, Si, Al. В результате раскисления образуются оксиды MnO, SiO2, Al2O3, которые имеют меньшую плотность, чем сталь, и удаляются в шлак. Однако часть оксидов не успевает всплыть и удалится из металла, что понижает его свойства. Этот способ называют иногда глубинным, так как рас-кислители вводятся в глубину металла.
Диффузионный способ
По этому способу раскисление осуществляют раскислением шлака. Ферромарганец, ферросилиций и другие раскислители загружают в мелкоизмельченном виде на поверхность шлака. Раскислители, восстанавливая оксид железа, уменьшают его содержание в шлаке. В соответс-твии с законом распределения оксид железа, растворенный в стали, начнет пе-реходить в шлак. Образующиеся при таком способе раскисления оксиды остаю-тся в шлаке, а восстановленное железо переходит в сталь, что уменьшает в ней содержание неметаллических включений повышает ее качество.
В соответс-твии с законом распределения оксид железа, растворенный в стали, начнет пе-реходить в шлак. Образующиеся при таком способе раскисления оксиды остаю-тся в шлаке, а восстановленное железо переходит в сталь, что уменьшает в ней содержание неметаллических включений повышает ее качество.
Ввиду того, что скорость процесса перемещения кислорода из металла в шлак определяется скоростью его диффузии в металле, этот способ имеет и не-которые недостатки. Из-за малой скорости диффузии кислорода в металле про-цесс удаления кислорода идет медленно, возрастает продолжительность плавки. В зависимости от степени раскисленности различают стали:
- кипящие;
- спокойные;
- полуспокойные.
Кипящая сталь
Это сталь, выплавленная без проведения операции рас-кисления. При разливке такой стали и при ее постепенном охлаждении в излож-нице будет протекать реакция между растворенными в металле кислородом и углеродом
[O]+[C]=COг
Образующиеся при этом пузырьки оксида углерода СО будут выделятся из кристаллизующегося слитка, и металл будет бурлить. Такую сталь называют кипящей. Кипящая сталь практически не содержит неметаллических включений, представляющих продукты раскисления. Поэтому она обладает хорошей пластичностью.
Такую сталь называют кипящей. Кипящая сталь практически не содержит неметаллических включений, представляющих продукты раскисления. Поэтому она обладает хорошей пластичностью.
Спокойная сталь
Это сталь, полученная после проведения операции рас-кисления. Такая сталь при застывании в изложнице ведет себя спокойно, из нее не выделяются газы. Такую сталь называют спокойной.
Полуспокойная сталь. Сталь имеет промежуточную раскисленность между спокойной и кипящей. Раскисление ее проводят частично, удаляя из нее не весь кислород. Оставшийся кислород вызывает кратковременное кипение металла в начале его кристаллизации. Такую сталь называют полуспокойной.
Легированные стали
Легированием называют процесс присадки в сталь специальных (легирующих) элементов с целью получить так называемую леги-рованную сталь с особыми физико-химическими или механическими свойствами. Легирование осуществляют введением ферросплавов или чистых металлов в необходимом количестве в сплав. Легирующие элементы, сродство к кислороду которых меньше, чем у же-леза (Ni, Cu, Co, Mo), при плавке и разливке практически не окисляются и по-этому их вводят в печь в любое время плавки. Легирующие элементы, у которых сродство к кислороду больше, чем у железа (Si, Mn, Al и др.), вводят в металл после или одновременно с раскислением.
Легирующие элементы, у которых сродство к кислороду больше, чем у железа (Si, Mn, Al и др.), вводят в металл после или одновременно с раскислением.
ПОДЕЛИСЬ ИНТЕРЕСНОЙ ИНФОРМАЦИЕЙ
Урок Химическая промышленность России
Химическая промышленность России. (9 класс)
Цель урока: изучить состав химической промышленности, особенности размещения, основные проблемы и перспективы развития отрасли.
Образовательные: рассмотреть особенности химической промышленности России; показать ее значение в экономике России; раскрыть особенности размещения химической промышленности.
Развивающие:
продолжить формирование умений анализировать, выявлять причинно – следственные связи, работать со статистическим материалом, самостоятельно находить материал по теме и грамотно его оформлять; заполнить таблицу «Химическая промышленность»; находить отрасли, выпускаемую продукцию, центры, факторы размещения химической промышленности;Воспитательные: на примере развития химической промышленности формировать
убеждение о необходимости бережного отношения к окружающей среде.
Тип урока: комбинированный
Методы обучения: частично-поисковый, проблемный, картографический (сопоставление и наложение карт атласа).
Оборудование: учебник «География России. Население и хозяйство» 9 класс В. П. Дронов В. Я. Ром, атлас для 9 класса «Дрофа», презентация.
Ход урока:
1.Оргмомент
Учитель здоровается с обучающимися, мотивирует на плодотворную творческую работу на уроке.
2.Проверка домашнего задания. – 8 мин.
Учащиеся получают карточки с вопросами (одна карточка на парту).
После выполнения — проверка заданий и самооценка (ответы и критерии оценки на слайде)
Тест по теме металлургия:
1. Какие факторы размещения предприятий черной металлургии являются более важными?
1). Экологический
4). Близость потребителя
Близость потребителя
2). Сырье (уголь, железная руда) 5). Источники энергии
3). Наличие водоемов
2. Выберите из перечисленных, центры черной металлургии с доменной выплавкой стали
1) Братск 4). Норильск
2) Липецк 5). Магнитогорск
3) Старый Оскол
3. Центр металлургии Череповец расположен на..
1) Пересечении потоков угля и железа
2) В районе добычи руд
3) В районе добычи коксующих углей или производства дешевой энергии
4. Сибирская металлургия развивается на месторождениях железной руды:
1) КМА
2) Руде Кольского п-ва
3) Руде Горной Шории и Приангарья
5. Укажите правильную последовательность плавки черного металла:
1) прокатный цех – доменный – сталеплавильный
2) сталеплавильный цех – прокатный — доменный
3) доменный — прокатный цех – сталеплавильный
4) доменный – сталеплавильный — прокатный цех
6. Выберите из перечисленных центры цветной
металлургии:
Выберите из перечисленных центры цветной
металлургии:
1) Магнитогорск
2) Саяногорск
3) Норильск
4 Кузнецк
7. Производство легких цветных металлов приурочено к..
1) районам производства дешевой электроэнергии
2) потребителю
3) районам добычи руды
8. В каком городе металл производится по бездоменной технологии – электроконверторным способом?
1) Череповец
2) Старый Оскол
3) Новокузнецк
9. Производство тяжелых цветных металлов приурочено к..
1) районам производства дешевой электроэнергии2) районам добычи руды
3) к потребителю
10. ( Задание № 23 КИМ – 9)
В городе Шахты (Ростовская область) с 2007 г. работает Ростовский электрометаллургический завод – новое современное
предприятие, имеющее производственную мощность 730 тыс. тонн стального проката
в год. В 2008 г. рядом с этим заводом начато строительство
«Южнорусского электрометаллургического завода». Сталеплавильные мощности нового
завода составят 960 тыс. тонн в год. Наличие крупных потребителей металла как в
Ростовской области, так и в соседних регионах позволит компании, управляющей
заводами, быстро окупить затраты.
работает Ростовский электрометаллургический завод – новое современное
предприятие, имеющее производственную мощность 730 тыс. тонн стального проката
в год. В 2008 г. рядом с этим заводом начато строительство
«Южнорусского электрометаллургического завода». Сталеплавильные мощности нового
завода составят 960 тыс. тонн в год. Наличие крупных потребителей металла как в
Ростовской области, так и в соседних регионах позволит компании, управляющей
заводами, быстро окупить затраты.
Какие особенности хозяйства Ростовской области, кроме упомянутых в тексте, делают экономически целесообразным размещение в ней электрометаллургических производств? Укажите две особенности.
( Ответ 1. Ростовская область расположена к югу от месторождения железных руд КМА т. е. – рядом с источником сырья.
2. В области работает Ростовская АЭС, обеспечивающая данное производство электроэнергией). (Слайд 2) Ответы на тесты и критерии оценивания.
3. Изучение нового материала.
Изучение нового материала.
Учитель: — Мы изучаем с вами отрасли, входящие в состав комплекса по производству конструкционных материалов.
— Назовите какие ещё отрасли, кроме металлургии, входят в состав данного комплекса.
Химико – лесной комплекс состоит из двух отраслей: химической и лесной промышленности. (слайд 3). Цели отрасли (слайд 4).
Химическая промышленность выпускает разнообразные изделия.
По производству серной кислоты Россия занимает второе место в мире; по производству минеральных удобрений – пятое место; по производству синтетических смол – четырнадцатое место.
Химическая промышленность наряду с машиностроением и электроэнергетикой влияет на развитие НТР путём химизации.
По учебнику « География. Население и хозяйство» для 9 класса В. Я. Ром, В. П. Дронов и параграф 21, стр. 153 определите, что такое химизация?
( Химизация – широкое применение технологий и химических материалов во всех хозяйственных отраслях. ) (слайд 5,6)
) (слайд 5,6)
Химическая промышленность имеет три особенности, которые влияют на размещение предприятий.
Самостоятельная работа с учебником, Используя 153 страницу учебника, перечислите особенности химической промышленности. (слайд 7)
1. Создаёт новые материалы, которых нет в природе. По своим качествам они часто превосходят натуральные продукты. Их применение экономит труд людей и сырьё. Поэтому предприятия химической промышленности часто создают уже в сложившихся районах, центрах производства и потребления традиционных конструкционных материалов ( машиностроительных центрах и металлургических базах).
2. У химической промышленности почти
неограниченная сырьевая база:
нефть, газ, древесина, вода, воздух и пр. При этом один и тот же продукт можно
получить из разных видов сырья. Например, азотные удобрения можно производить
на основе коксования угля, электролиза воды, переработки нефти и природного
газа. Поэтому теоретически предприятия химической промышленности можно
создавать повсеместно. Но на сегодняшний день основным химическим сырьём
являются продукты нефте- и газопереработки, т. е. специально подготовленное
сырьё. В результате современная химия в значительной мере тяготеет к районам
добычи и переработки этих видов сырья ( Поволжье, Европейский Центр).
Поэтому теоретически предприятия химической промышленности можно
создавать повсеместно. Но на сегодняшний день основным химическим сырьём
являются продукты нефте- и газопереработки, т. е. специально подготовленное
сырьё. В результате современная химия в значительной мере тяготеет к районам
добычи и переработки этих видов сырья ( Поволжье, Европейский Центр).
Химические технологии очень разнообразны. Это открывает возможности для комплексной переработки сырья. (слайд 8)
В химической промышленности и, при её взаимодействии с
другими отраслями широко развито комбинирование. Оно способствует формированию разнообразных комбинатов: химических, нефтехимических, коксохимических, лесохимических и др.
Некоторые особенности химической
промышленности ограничивают потенциальную повсеместность её размещения. К ним
относятся высокая энерго – и водоёмкость многих её отраслей, особенно
современных. В последние годы нарастает влияние экологического фактора, так
как большая часть химических производств является сильным загрязнителем окружающей
среды.
Релаксация (зарядка для глаз) – 1 минута (слайд 9)
Запишите в тетрадь: Отраслевой состав и факторы размещения химической промышленности.
Используя Атлас для 9 класса стр 14 «Химическая промышленность» составить таблицу: Состав отраслей ХП и какую продукцию производит каждая из этих отраслей? (слайд10,11).
Отраслевой состав | Продукция | Факторы размещения | Центры |
Горно-химическая | апатиты Фосфориты сера калийная соль поваренная соль глауберовая соль
| У мест добычи сырья. | Хибины, Рудничный Оренбург Соликамск, Березняки
|
Основная химия | калийные удобрения фосфорные удобрения азотные удобрения
серная кислота | у сырья, потребителя и сернокислотных заводов у газопроводов на металлургических комбинатах у потребителя | Соликамск, Березняки г.Воскресенск Новомосковск. Щекино, Тольятти, Новгород, Магнитогорск.
Волгоград, Челябинск |
Химия органического синтеза | Пластмассы
химические волокна синтетический каучук
шины
| к потребителю и к НПЗ
водоемкое, энергоемкое у сырья, нефтепроводы
к производству каучука | Тюмень, Казань, Орехово-Зуево, Буденновск,
Саянск. Тверь, Клин, Энгельс, Саратов, Барнаул. Ефремов, Тольятти, Казань, Воронеж, Нижнекамск, Первоуральск. Ярославль, Киров, Курск Воронеж, Омск. |
Базы химической промышленности. (слайд 12)
В России существуют 4 базы химической промышленности:
1. Северо – Европейская
2. Центральная
3. Урало – Поволжская
4. Сибирская
Проблемы развития: (слайд 13)
1.Особенностью экологического воздействия предприятий химического комплекса является многообразие источников и видов выделяющихся вредных веществ. Ряд загрязняющих веществ выбрасывается в атмосферный воздух или сбрасывается в природные водоемы в относительно небольших по массе количествах, но характеризуется высокой токсичностью.
2. Сильный износ оборудования. Он составляет
57%, а 65% техники устарело морально и физически. Более 2/3 производств
эксплуатируется свыше 25 лет.
Сильный износ оборудования. Он составляет
57%, а 65% техники устарело морально и физически. Более 2/3 производств
эксплуатируется свыше 25 лет.
Перспективы развития: (слайд 14)
· Технологическая модернизация производства, внедрение ресурсо- и энергосберегающих технологий;
· снижение удельных расходов сырьевых, топливно-энергетических и трудовых ресурсов (на 12-15%) на производство химической и нефтехимической продукции;
· углубление переработки углеводородного и минерального сырья на основе новейших технологий, в том числе за счет эффективного использования попутного нефтяного газа;
· максимальное внедрение результатов отечественных разработок и использование новейшего оборудования отечественных машиностроительных предприятий при реконструкции, техническом перевооружении и строительстве новых производств;
·
концентрация инновационной
деятельности в химическом комплексе на разработке и внедрении технологических
процессов нового уровня, характеризующихся ограниченным количеством операций,
безотходностью, глубоким переделом исходного сырья.
4.Закрепление изученного материала. (слайд 15)
1.Особенностью химической промышленности является…
1). Тяготение к источникам дешевой электроэнергии
2). Производство материалов, не существующих в природе
3) Комплексность сырья
2.Какие из перечисленных производств химической промышленности тяготеют к потребителю?
1). Производство серной кислоты
2). Производство апатитов
3). Производство азотных и фосфорных удобрений
3. В каких районах химическая промышленность развита наиболее пропорционально в связи с наличием разнообразного сырья, воды, электроэнергии
1). В Сибири
2). В Поволжье и на Урале
3). В Центральной России
5. Итоги урока -2 мин
Выставляются оценки за работу на уроке наиболее активным учащимся.
6.Домашнее задание – 2мин. (слайд 16)
Задание на дом дается дифференцированно:
Ключ: Критерии:
1 — 2,4,5 6 – 2,3 9 — 10 баллов оценка «5»
2 – 2,5 7 — 1 7 — 8 баллов оценка «4»
3 – 1 8 – 2 6 — 7 баллов оценка «3»
4 – 3 9 – 2 4 — 5 баллов оценка «2»
5 – 4
Температура плавления черных и цветных металлов (полная таблица)
Какова температура плавления металла?
Какова самая высокая и самая низкая температура плавления металла?
Важной проблемой, о которой следует помнить при обработке металлических материалов, является температура плавления.
Во-первых, давайте посмотрим, что такое температура плавления.
Температура плавления вещества – это температура, при которой твердая и жидкая фазы чистого вещества уравновешиваются при определенном давлении.
То есть при давлении и температуре плавления химический потенциал чистого вещества равен химическому потенциалу жидкости.
Для чисто материальной твердой системы (наносистемы) с большой дисперсией нельзя игнорировать поверхностную часть, и ее химический потенциал зависит не только от температуры и давления, но также связан с размером твердых частиц, который принадлежит термодинамический процесс фазового перехода первого рода.
Проще говоря, только определенная температура плавления может изменить форму металла, таким образом, ковка различных изделий.
Таким образом, мы должны сначала понять температуру плавления различных металлов перед обработкой.
Давайте погрузимся в температуру плавления различных черных и цветных металлов. №
№
 0053 7
0053 7 0053 29
0053 29 0045
0045 In В периодической таблице элементов есть два неметаллических материала: кремний и бор, и их температура плавления составляет 1420°C и 2300°C соответственно.
Какая самая высокая и самая низкая температура плавления?
Из таблицы мы смогли ясно понять температуру плавления различных металлов.
Для металла с самой высокой и самой низкой температурой плавления я также дам вам краткое введение.
Существует разновидность металла, называемого цезием, серебристо-белого цвета.
Основан в 1860 году.
За исключением ртути, имеет самую низкую температуру плавления 29 °C.
Среди всех чистых металлов вольфрам имеет самую высокую температуру плавления.
В 1783 году два испанца обнаружили, что температура плавления вольфрама составляет 3417 ± 10 °C.
Наиболее устойчивы к высоким температурам карбиды ниобия (ТГ 0,88) и карбиды ниобия (HfG 0,95).
Температуры плавления двух материалов составляли 4010±75 °C и 3960±20 °C соответственно.
Чтение EAP
Чтение EAPМеталлургия: изготовление сплавов
Большинство сплавов получают смешиванием металлов в расплавленном состоянии;
затем смесь заливают в металлические или песчаные формы и дают затвердеть. Обычно основной ингредиент плавится первым; затем добавляются остальные
он и должен полностью раствориться. Например, если сантехник делает припой, он
может расплавить свинец, добавить олово, перемешать и отлить сплав в виде палочки. Некоторые пары
металлы так не растворяются. Когда это так, маловероятно, что
образуется полезный сплав. Таким образом, если бы сантехник добавил алюминий, вместо
от олова до свинца два металла не растворились бы — они вели бы себя как
масло и вода. При литье металл разделялся на два слоя: тяжелый
внизу свинец, вверху алюминий.
Обычно основной ингредиент плавится первым; затем добавляются остальные
он и должен полностью раствориться. Например, если сантехник делает припой, он
может расплавить свинец, добавить олово, перемешать и отлить сплав в виде палочки. Некоторые пары
металлы так не растворяются. Когда это так, маловероятно, что
образуется полезный сплав. Таким образом, если бы сантехник добавил алюминий, вместо
от олова до свинца два металла не растворились бы — они вели бы себя как
масло и вода. При литье металл разделялся на два слоя: тяжелый
внизу свинец, вверху алюминий.
Одна из трудностей при изготовлении сплавов заключается в том, что металлы имеют разные температуры плавления.
Так, медь плавится при 1083°С, а цинк плавится при 419°С и кипит при 907°С.
при изготовлении латуни, если мы просто положим кусочки меди и цинка в тигель и
нагреть их выше 1083°С, оба металла обязательно расплавятся. Но при этом
при высокой температуре жидкий цинк также выкипал бы, а пар окислялся бы
в воздухе. Метод, принятый в этом случае, состоит в том, чтобы сначала нагреть металл, имеющий
более высокая температура плавления, а именно медь. Когда это расплавлено, твердое
добавляется цинк, который быстро растворяется в жидкой меди до очень
цинк выкипел. Тем не менее, при изготовлении латуни необходимо делать поправку.
за неизбежную потерю цинка, которая составляет около одной двадцатой части цинка.
Следовательно, при взвешивании металлов перед легированием лишнее количество
необходимо добавить цинка.
Когда это расплавлено, твердое
добавляется цинк, который быстро растворяется в жидкой меди до очень
цинк выкипел. Тем не менее, при изготовлении латуни необходимо делать поправку.
за неизбежную потерю цинка, которая составляет около одной двадцатой части цинка.
Следовательно, при взвешивании металлов перед легированием лишнее количество
необходимо добавить цинка.
Иногда изготовление сплавов осложняется тем, что более тугоплавкие
точечный металл находится в меньшей пропорции. Например, один легкий сплав содержит
92 % алюминия (температура плавления 660°C) с 8 % меди (температура плавления
точка 1083°С). Для изготовления этого сплава нежелательно плавить
несколько фунтов меди и почти в двенадцать раз больше веса алюминия.
металл пришлось бы так сильно нагревать, чтобы убедить большой объем алюминия
растворить, что газы будут поглощены, что приведет к нездоровью. В этом, как
во многих других случаях легирование проводят в два этапа. Первый промежуточный
изготовлен «сплав-отвердитель», содержащий 50% меди и 50% алюминия,
этот сплав имеет температуру плавления значительно ниже, чем у меди и,
на самом деле, ниже, чем у алюминия. Затем алюминий расплавляется и правильный
количество добавленного отвердителя; таким образом, чтобы сделать 100 фунтов алюминиево-медного сплава
сплав мы должны потребовать 84lb. алюминия, который нужно расплавить первым, и 16 фунтов отвердителя
сплав, который нужно добавить к нему.
Затем алюминий расплавляется и правильный
количество добавленного отвердителя; таким образом, чтобы сделать 100 фунтов алюминиево-медного сплава
сплав мы должны потребовать 84lb. алюминия, который нужно расплавить первым, и 16 фунтов отвердителя
сплав, который нужно добавить к нему.
В некоторых случаях температуру плавления сплава можно определить примерно
по арифметике. Например, если медь (температура плавления 1083°С) сплавляется с
никель (температура плавления 1454 °C) сплав пятьдесят на пятьдесят будет плавиться примерно на полпути
между двумя температурами. Даже в этом случае поведение сплава на
плавить не просто. Медно-никелевый сплав не плавится и не замерзает при одном
фиксированная и определенная температура, но постепенно затвердевает в диапазоне
температура. Таким образом, если медно-никелевый сплав поровну сжижается, а затем
постепенно охлаждаясь, он начинает замерзать при 1312°С, а по мере понижения температуры
все больше и больше сплава становится твердым, пока, наконец, при 1248°C он полностью не затвердеет. затвердевший. За исключением некоторых особых случаев, этот «диапазон замораживания» возникает в
все сплавы, но не встречается в чистых металлах, металлических или химических соединениях,
и в некоторых специальных составах сплавов, упомянутых ниже, все из которых плавятся
и заморозить при одной определенной температуре.
затвердевший. За исключением некоторых особых случаев, этот «диапазон замораживания» возникает в
все сплавы, но не встречается в чистых металлах, металлических или химических соединениях,
и в некоторых специальных составах сплавов, упомянутых ниже, все из которых плавятся
и заморозить при одной определенной температуре.
Легирование олова и свинца представляет собой пример одного из этих особых
случаи. Свинец плавится при 327°С, а олово при 232°С. Если в расплавленное олово добавить свинец
и затем сплав охлаждают, температура замерзания сплава оказывается равной
ниже температуры замерзания как свинца, так и олова (см. рис. 1). Например,
если расплавленный сплав, содержащий 90 % олова и 10 % свинца, охлаждают,
смесь достигает температуры 217°С, прежде чем она начинает затвердевать. Затем,
по мере дальнейшего охлаждения сплав постепенно переходит из полностью жидкого состояния в
через стадию, когда он похож на кашу, пока не станет густым, как каша,
и, наконец, уже при температуре 183°С весь сплав стал полностью
твердый. Из рисунка 1 видно, что при содержании олова 80 %
сплав начинает затвердевать при 203°С и заканчивает затвердевание только при температуре
упал до 183°С (обратите внимание на повторение 183°С).
Из рисунка 1 видно, что при содержании олова 80 %
сплав начинает затвердевать при 203°С и заканчивает затвердевание только при температуре
упал до 183°С (обратите внимание на повторение 183°С).
Что происходит на другом конце ряда, когда к свинцу добавляется олово? Один раз
снова температура замерзания снижается. Сплав, содержащий только 20 процентов олова и
оставшийся свинец начинает замерзать при 279°С и завершает затвердевание при
привычная теперь температура 183°C. Один конкретный сплав, содержащий 62%
% олова и 38 % свинца, плавится и полностью затвердевает при 183°С. Очевидно
эта температура 183°С и состав 62/38% важны в
система оловянно-свинцового сплава. Подобные эффекты возникают во многих других системах сплавов.
и специальный состав, который имеет самую низкую температуру замерзания в серии
и который полностью замерзает при этой температуре, получил специальное название.
Конкретный сплав известен как «9».0713 эвтектический сплав ‘ и замерзание
температура (183°С в случае оловянно-свинцовых сплавов) называется эвтектикой температура.
Путем тщательного подбора компонентов можно получить сплавы с необычайно низкие температуры плавления. Такой легкоплавкий сплав представляет собой сложную эвтектику из четырех или пяти металлы, смешанные так, чтобы температура плавления была понижена до самой низкой точки плавления можно получить из любой смеси выбранных металлов. знакомый легкоплавкий сплав, известный как металл Вуда, имеет состав:
Висмут | 4 части |
Свинец | 2 части |
Олово | 1 часть |
Кадмий | 1 часть |
и его температура плавления около 70°С; то есть ниже температуры кипения
воды. Юмористы часто развлекались, бросая этот
легкоплавкий сплав в форме чайной ложки, который плавится при перемешивании
чашка горячего чая.
Юмористы часто развлекались, бросая этот
легкоплавкий сплав в форме чайной ложки, который плавится при перемешивании
чашка горячего чая.
Эти сплавы с низкой температурой плавления регулярно используются для более серьезных целей, как, например, в автоматических противопожарных оросителях, установленных в потолках зданий. Каждая форсунка спринклерной системы снабжена плавким предохранителем. сплава, так что если произойдет пожар и температура поднимется достаточно высоко, сплав плавится и вода выбрасывается через форсунки спринклера.
(из Metals in Service of Man W. Alexander & A. Street.)
Какова температура плавления алюминия?
Температура плавления является важным физическим свойством. Температура, при которой вещество переходит из твердого состояния в жидкое, напрямую влияет на то, как с этим веществом обращаются и наносят. Алюминий имеет температуру плавления приблизительно 1220°F. По сравнению с другими металлами это примерно в два раза выше температуры плавления цинка и вдвое ниже температуры плавления нержавеющей стали. Примечательно, что температура плавления алюминия изменяется в зависимости от состава сплава. Это жизненно важная информация, когда речь идет о производстве алюминия.
Примечательно, что температура плавления алюминия изменяется в зависимости от состава сплава. Это жизненно важная информация, когда речь идет о производстве алюминия.
Загрузить технические характеристики алюминия
Kloeckner Metals — поставщик полного ассортимента алюминия и сервисный центр. Загрузите нашу спецификацию алюминия и узнайте, что Kloeckner Metals регулярно поставляет на склад.
Технические характеристики алюминия
Производственные процессы часто требуют нагрева металлов до их температуры плавления. Для плавки, сварки плавлением и литья металлы должны быть жидкими. Алюминий и алюминиевые сплавы можно плавить и переплавлять по мере необходимости. Это включает в себя плавку для литья слитков или заготовок, а также для последующих производственных процессов, таких как прокатка, экструзия, волочение, ковка и переработка.
Во-первых, понимание того, как производится первоклассный алюминий
Алюминий всегда встречается в виде соединения, а не в чистом виде. Чистые формы металла должны быть сначала химически очищены до глинозема (оксида алюминия), а затем переплавлены в алюминий с помощью процесса электролитического восстановления Холла-Эру, обычно называемого первичным производственным процессом. По данным Алюминиевой ассоциации, первичный производственный процесс стал более эффективным, улучшив его на 20% за последние 20 лет.
Чистые формы металла должны быть сначала химически очищены до глинозема (оксида алюминия), а затем переплавлены в алюминий с помощью процесса электролитического восстановления Холла-Эру, обычно называемого первичным производственным процессом. По данным Алюминиевой ассоциации, первичный производственный процесс стал более эффективным, улучшив его на 20% за последние 20 лет.
Получение алюминия начинается с добычи бокситов, основного сырья, из которого производится металлический алюминий. Затем примеси из боксита удаляются отстаиванием и фильтрацией. Эта химическая обработка делает глинозем. Бокситы измельчают, смешивают с раствором гидроксида натрия, а затем нагревают паром под давлением для растворения оксида алюминия.
Температура плавления оксида алюминия выше, чем у алюминия, и составляет около 3762°F. Вот почему извлечение алюминия из оксида алюминия осуществляется электролизом до расплавления металла. Электролиз, метод, с помощью которого элементы могут быть разделены, происходит в восстановительных емкостях или ячейках восстановительной установки. Этот процесс восстановления удаляет кислород из оксида алюминия, который состоит из почти равных частей алюминия и кислорода. Только после всех этих шагов у нас есть чистый, первоклассный алюминий.
Этот процесс восстановления удаляет кислород из оксида алюминия, который состоит из почти равных частей алюминия и кислорода. Только после всех этих шагов у нас есть чистый, первоклассный алюминий.
Факторы, влияющие на температуру плавления алюминия
Соединение сплава
Диапазон температур плавления немного зависит от состава сплава. Диапазоны плавления некоторых распространенных сплавов указаны ASM International:
- 1100: 1190 – 1215°F
- 2024: 935–1180°F
- 3003: 1190–1210°F
- 5052: 1125 -1200°F
- 5456: 1055-1180°F
- 6061: 1080–1205°F
- 7075: 890–1175°F
Химические примеси
Обычный алюминий и его сплавы неизбежно содержат примеси. Примесью можно назвать любые химические элементы, не введенные намеренно в состав сплава.
Химические примеси изменят температуру плавления. Это называется депрессией точки плавления. Если температура плавления изменяется более чем на 41 градус по Фаренгейту, это доказывает наличие примесей.
Примеси могут появляться в различных точках процесса плавки. Загрязнение шихты в процессе плавки и разливки или взаимодействие с металлической футеровкой и флюсами. Растворение элементов литейного оборудования и литейного инструмента.
Примеси могут поступать при переплавке алюминиевых отходов во вторичное производство.
Состав молекул
Молекулам с сильными связями требуется больше энергии для разрыва. Алюминий имеет ковалентные связи, что приводит к более высокой температуре плавления.
Сила притяжения
Алюминий имеет прочные полярные связи, обеспечивающие низкую летучесть, высокие температуры плавления и кипения и высокую плотность.
Давление
Приложение давления в процессе нагревания может изменить температуру плавления. Для алюминия давление около 3500 гигапаскалей вызовет повторный нагрев или когда температура плавления действительно начнет снижаться выше определенного критического давления.
Плавка металлов: основы литья
Процессы литья известны уже тысячи лет. Металлы отливают в формы путем их плавления в жидкости, заливки металла в форму и удаления материала формы после того, как металл затвердеет при охлаждении.
Металлы отливают в формы путем их плавления в жидкости, заливки металла в форму и удаления материала формы после того, как металл затвердеет при охлаждении.
Высокотехнологичные отливки используются в 90% товаров длительного пользования, включая автомобили, грузовые автомобили, аэрокосмическую промышленность, поезда, горнодобывающее и строительное оборудование, нефтяные скважины, приборы, трубы, гидранты, ветряные турбины, атомные электростанции, медицинские устройства, изделия оборонного назначения, игрушки , и более.
Существует множество различных методов литья, которые относятся к методам литья одноразового или многоразового использования. Одноразовое литье предполагает использование временных, одноразовых форм. При многоразовом литье формы используются повторно без необходимости переформирования после каждого производственного цикла. Для получения дополнительной информации о каждом из процессов литья посетите базу данных металлов Total Materia.
Процесс литья алюминия
Миллионы фунтов расплавленного алюминия отливаются каждый день, что делает его одним из наиболее часто отливаемых металлов. Вероятно, это связано с тем, что алюминий является одним из немногих металлов, которые можно отливать всеми способами, используемыми для литья металлов. Но есть различия в типе литого алюминия.
Вероятно, это связано с тем, что алюминий является одним из немногих металлов, которые можно отливать всеми способами, используемыми для литья металлов. Но есть различия в типе литого алюминия.
Разница между первичным алюминием, ломом и отвердителями
При вопросе о том, как плавить алюминий, важно понимать разницу между первичным алюминием, ломом и отвердителями. Каждый играет ключевую роль в процессе кастинга.
- Алюминий Prime на 99,9% состоит из алюминия. Он проявляется в трех формах: Т-образные стержни, свиноматки и свиньи. Первичный алюминий добавляется в печь первым.
- Лом представляет собой переработанный алюминий. Брак может появляться непосредственно либо в процессе производства, либо в продуктах, собранных после использования и утилизации потребителем. После того, как весь первичный алюминий расплавится, добавляют лом для удаления влаги.
- Отвердители – это дополнительные элементы, предназначенные для упрочнения алюминия.
 Назначение отвердителей – повысить прочность и придать конечному изделию желаемые свойства. Это включает отделку, прочность и измельчение зерна. Силикон и магний являются двумя основными отвердителями в процессе литья алюминия. Как правило, они добавляются в ванну с алюминием последними, чтобы довести концентрацию легирующих добавок до спецификации отливаемого сплава.
Назначение отвердителей – повысить прочность и придать конечному изделию желаемые свойства. Это включает отделку, прочность и измельчение зерна. Силикон и магний являются двумя основными отвердителями в процессе литья алюминия. Как правило, они добавляются в ванну с алюминием последними, чтобы довести концентрацию легирующих добавок до спецификации отливаемого сплава.
Литейные печи для плавки алюминия
Алюминиевые печи используются для плавки алюминия и литья бревен. Как правило, в печах могут использоваться разные технологии для плавки материала, но каждая печь стремится минимизировать потребление тепла и топлива. Энергоэффективные печи помогают контролировать условия плавки, что увеличивает выход металла.
Алюминиевые печи проектируются с открытым колодцем. Эта конструкция учитывает этапы процесса литья алюминия, описанные ниже, поскольку, как только основной алюминий плавится, через это отверстие добавляется металлолом.
Какие этапы процесса литья?
Сначала готовится шихта, в которой смесь сырья расплавляется для получения сплава. Добавляется первичный алюминий, и как только весь первичный алюминий расплавится, добавляется металлолом для удаления влаги.
Добавляется первичный алюминий, и как только весь первичный алюминий расплавится, добавляется металлолом для удаления влаги.
Методы и приемы обработки расплавленного алюминия для повышения и проверки его чистоты. Это обработка флюсов, продувка инертными газами, фильтрация и отстаивание.
После подтверждения чистоты добавляются отвердители. Опять же, какие элементы добавляются в смесь и в каких количествах, полностью зависит от спецификации отливаемого сплава.
Последний шаг — отливка и охлаждение.
Экструдирование алюминия начинается с нагрева твердого куска алюминиевой пластины, трубы, листа или бруска до тех пор, пока он не станет мягким. Затем размягченный алюминий прессуется через меньшее отверстие матрицы. Алюминиевые профили могут быть сплошными, полупустыми или полыми и служат для облегчения одних потребительских товаров, а других — более прочных.
Безопасная плавка алюминия
Любой расплавленный материал несет в себе опасность. Несоблюдение надлежащих процедур при плавке и литье алюминия может быть опасным.