Изопропиловый спирт (изопропанол)
Изопропиловый спирт (изопропанол), CH₃CH(OH)CH₃
Простейший спирт алифатического ряда. Представляет собой бесцветную жидкость с характерным запахом. Плотность: 786,00 кг/м³. Температура кипения: 82,5 °C. Температура плавления: -89 °C. Молярная масса: 60,1 г/моль.
Фасовка:
канистра 10 л, канистра 20 л, бочка 200 л.
Техника безопасности:
Это горючее летучее соединение, как следствие – взрывоопасное. При работе с ним желательно использовать респиратор, чтобы исключить отравления при вдыхании его паров. Помещение должно иметь хорошую вентиляцию. Вдыхание паров растворителя может вызвать галлюцинации, токсические отравления организма, тяжелого типа нервные и психические расстройства. Образует с воздухом взрывоопасные смеси и обладает низкой температурой вспышки, следовательно, необходимо соблюдать особую осторожность при работе с ним.
Транспортировка:
Транспортировка любым видом транспорта. При доставке этого химического вещества необходимо следовать правилам перевозок опасных грузов. Выбор тары будет зависеть от объема и фасовки поставляемой партии. Само химическое соединение является горючим летучим соединениям, и естественно является взрывоопасным.
Применение:
Изопропиловый спирт применяется в аналитической химии и фундаментальной науке в процессе высокоэффективной жидкостной хроматографии. Также популярен в качестве органического растворителя. Ещё одно применение — в оффсетной печати и полиграфии, в составе ряда растворов. 70-процентный водный раствор изопропилового спирта часто используют для дезинфекции.
В химической промышленности изопропанол применяют в производстве ацетона, перекиси водорода и других веществ. В качестве более дешёвого заменителя этанола он входит в состав косметики, бытовой химии, средств для дезинфекции, антифриза и стеклоомывателя для авто, репеллентов.
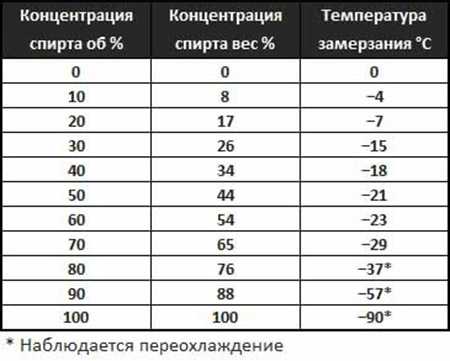
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице:
| Концентрация спирта об % | Концентрация спирта вес % | Температура замерзания °C |
| 0 | 0 | 0 |
| 10 | 8 | — 4 |
| 20 | 17 | — 7 |
| 30 | 26 | — 15 |
| 40 | 34 | — 18 |
| 50 | 44 | — 21 |
| 60 | 54 | — 23 |
| 70 | 65 | — 29 |
| 80 | 76 | — 37* |
| 90 | 88 | — 57* |
| 100 | 100 | — 90* |
(*Наблюдается переохлаждение)
Характеристики Основные
| Производитель | Завод синтетического спирта |
| Страна производитель | Польша |
1 л.-225 грн.
ukr-himiya.net
Температура замерзания спирта
Свойства спиртных напитков всегда интересовали человека, ведь из-за особого состава они непохожи на все остальные жидкости, предназначенные для питья. Для того чтобы понять это, даже не нужно было знать формулы веществ. Как пример, историки знают об особенно холодных зимах в Европе по сохранившимся документам, где указано, что в погребах даже замерзало вино. Какова температура замерзания спирта и содержащих его напитков, тогда не было известно. В наши дни наука продвинулась вперёд и этот вопрос можно прояснить.
Этиловый спирт
Так как в алкогольных напитках (и прошлых столетий, и современных) содержится именно этиловый спирт, его свойства наиболее интересны не только химикам и физикам, но и всем остальным людям. Зная соотношение спирта и воды в напитке, можно рассчитать, при какой температуре он превратится в лёд и возможно ли это в бытовых условиях.
Этанол – он же этиловый, винный спирт, метилкарбинол или же просто спирт – в стандартных условиях представляет собой бесцветную прозрачную жидкость. Он горюч и выделяет летучие пары. Вкус и запах продукта примерно представляют себе все. Одноатомный насыщенный спирт со знакомой со школьной скамьи формулой C2H5(OH) используется не только в производстве алкоголя, но и как топливо, растворитель, компонент дезинфицирующих средств и лекарств, в парфюмерии, пищевой и химической промышленности. В медицине применяется раствор спирта 96-ти или 70%, который должен быть предварительно очищен.
Как замерзает этиловый спирт
Замерзание – это тот момент, когда вещество меняет агрегатную форму, переходя из жидкой формы в твёрдую, кристаллическую. На этот процесс оказывают влияние состав и молекулярные свойства вещества, наличие в нём примесей, уровень атмосферного давления в момент охлаждения и другие факторы.
Что касается этилового спирта, то достигнуть этого состояния в естественных природных условиях на планете Земля ему не суждено: абсолютная температура замерзания спирта равна -117°C. По другим данным это показатель составляет -114 или 115°C. Вот какой продукт не боится никаких морозов, может, поэтому прочно ассоциируется с согреванием.
Спиртовые растворы
Спиртосодержащие напитки тоже устойчивы к холоду, но заморозить их всё же возможно – как вино из европейских погребов, которое фактом своего замерзания ясно говорило об экстремальных для тех широт и времени температурах. Всё дело в воде и других добавках, которые делают из чистого спирта раствор, разбавляя его концентрацию.
Раствор, в котором спирта в 2 раза меньше, чем воды, замерзает при -17°C. Если соотношение спирта и воды составляет 1:3, то его температура замерзания будет уже -11 градусов ниже нуля.
Водка представляет собой 40%-ный раствор спирта, то есть в ней 6 частей воды и 4 части спирта. Она замерзает при 25–29° ниже нуля. Если же напиток превратился в лёд при более высокой температуре, например, -20 градусах, это уже серьёзный повод усомниться в его качестве и составе. Водка, разбавленная пополам с водой, переходит в твёрдое состояние уже при -7,5°C.
При этом водка замерзает постепенно, но не так, как вода. Сначала она становится вязкой, желеобразной, а потом индевеет отдельными пластинами. Это связано с тем, что по мере замерзания в растворе увеличивается концентрация этанола, процесс отвердевания протекает неравномерно. Загустевшая водка не имеет характерного вкуса и запаха, за счёт чего пьётся легко, а потому очень просто увлечься экспериментом, перебрать с её количеством и получить серьёзное отравление.
Пиво относится к слабоалкогольным напиткам, так как содержит мало этанола. И замерзает оно уже при -2 градусах, о чём знают все, кто хоть раз забывал пиво в морозилке, надеясь охладить его быстрее. Пить такой напиток не опасно, однако он может потерять во вкусовых качествах. То же самое относится и ко всем слабо- и среднеалкогольным напиткам: вину, вермуту, коктейлям.
Интересно, что сильное охлаждение играет существенную роль в приготовления ряда алкогольных напитков. Некоторые разновидности бренди и метаксу по технологии специально подвергают выдержке при -6°C в течение нескольких месяцев.
Другие разновидности спирта
Изопропиловый спирт используют в качестве заменителя этанола в косметике, парфюмерии, для производства растворителя, антифриза, для сварки оптических волокон и так далее. Замерзает при -90°C. 70%-ный изопропанол применяется в качестве антисептика, пропитывающего медицинские салфетки. Его температура замерзания выше, примерно -29 градусов.
Метиловый спирт (метанол, древесный спирт, метилгидрат) имеет формулу CH₃OH. Сильный растворитель, в основном используется для производства формальдегида. Метанол – опаснейший яд, причём даже в малых количествах. 60%-ный раствор метилового спирта замерзает при температуре -75,7°C, 20%-ный – при -15°C, 10%-ный – при 5,6°C.
Нашатырный спирт – это водный раствор гидроксида аммония. Известен своим резким запахом и способностью приводить в чувство при обморочном состоянии. Также его применяют для того, чтобы вызвать рвоту при отравлении алкоголем: нужно выпить раствор нашатыря, 5-10 капель на 100 мл воды. Чаще всего в медицинских и бытовых целях нам помогает 10% раствор аммиачной воды, который обладает свойством замерзать уже при -12 градусах по Цельсию. 25%-ный раствор затвердевает при температуре -56°C.
alkolife.ru
Изопропиловый спирт — WiKi
Изопропи́ловый спирт (пропано́л-2, втор-пропанол, изопропано́л, диметилкарбино́л, ИПС) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует изомер изопропанола — пропанол-1.
| Изопропанол | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Пропан-2-ол |
| Традиционные названия | Изопропиловый спирт |
| Хим. формула | C3H8O |
| Рац. формула | CH3CH(OH)CH3 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 60,09 г/моль |
| Плотность | 0,7851 г/см³ |
| Динамическая вязкость | 0,00243 Па·с |
| Энергия ионизации | 10,1 ± 0,1 эВ[1] |
| Термические свойства | |
| Т. плав. | -89,5 °C |
| Т. кип. | 82,4 °C |
| Т. всп. | 11,7 °C |
| Т. свспл. | 400 °C |
| Пр. взрв. | 2 ± 1 об.%[1] |
| Мол. теплоёмк. | 155,2 Дж/(моль·К) |
| Давление пара | 4,4 кПа при 20 °C |
| Химические свойства | |
| pKa | 16,5 |
| Растворимость в бензоле | хорошо растворим |
| Растворимость в ацетоне | растворим |
| Оптические свойства | |
| Показатель преломления | 1,3776 (nD, 20°C) |
| Структура | |
| Дипольный момент | 1,66 Д |
| Классификация | |
| Рег. номер CAS | 67-63-0 |
| PubChem | 3776 |
| Рег. номер EINECS | 200-661-7 |
| SMILES | |
| InChI | |
| RTECS | NT8050000 |
| ChEBI | 17824 и 43588 |
| Номер ООН | 1219 |
| ChemSpider | 3644 |
| Безопасность | |
| ЛД50 | 12800 мг/кг (кролик) |
| Токсичность | Класс опасности 3 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
При нормальных условиях прозрачная, бесцветная жидкость с резким запахом и мягким горьким вкусом[2].
Изопропиловый спирт используется в качестве заменителя этилового спирта в косметике, парфюмерии, бытовой химии, жидкостей для автомобилей, медицинских целях, в средствах для очистки стёкол, оргтехники и как растворитель органических веществ промышленности.
В развитых странах изопропанол широко используется в товарах личной гигиены и в медицине, благодаря своей относительно низкой токсичности[3].
75 % водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь клеточные мембраны бактерий, таким образом обеспечивает более высокую эффективность и лучшее обеззараживание[4].
Изопропиловый спирт также используется в медицине в качестве вспомогательного компонента профилактического средства от наружного отита[5].
Эффективен при лечении дерматита протиранием пораженных участков кожи, с малым вредным влиянием на кожу.
Как и все летучие спирты, огнеопасен. Умеренно токсичен, требует осторожного обращения.
Свойства
Химические свойства
Рациональная химическая формула изопропилового спирта Ch4CH(OH)Ch4{\displaystyle {\ce {Ch4CH(OH)Ch4}}} .
Изопропанол обладает всеми свойствами вторичных спиртов жирного ряда, образует простые и сложные эфиры.
Гидроксильная группа может быть вытеснена галогенами.
С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол.
При дегидрировании превращается в ацетон[6].
Реагирует с сильными окислителями.
В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения.
Растворяет некоторые виды пластмасс и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резким, чем у этанола, по запаху их можно в некоторых случаях отличить.
Коэффициент преломления nD = 1,3776 при 20 °C. Динамическая вязкость при стандартных условиях 2,43 мПа·с — немного более вязкий, чем вода . Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К). Удельная теплота сгорания 34,1 МДж/кг.
Пар хорошо смешивается с воздухом, в диапазоне взрывоопасных концентраций образует взрывчатые смеси. Давление насыщенного пара при 20 °C — 4,4 кПа. Относительная плотность пара по воздуху — 2,1, относительная плотность смеси насыщенный пар/воздух — 1,05 при 20 °C.
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях.
С водой образует азеотропную смесь 87,9 % изопропилового спирта с температурой кипения 80,2 °C.
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице, при замерзании концентрированных растворов наблюдается переохлаждение[7]:
| Концентрация спирта, об % | Концентрация спирта, вес. % | Температура замерзания, °C |
|---|---|---|
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Получение
Применяются два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена[8][9].
Основным способом получения изопропанола в российской промышленности является сернокислотная гидратация пропилена
- Ch4CH=Ch3+h3SO4⟶(Ch4)2CHOSO2OH+h3O⟶(Ch4)2CHOH{\displaystyle {\ce {Ch4CH=Ch3 + h3SO4 ->(Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH}}} .
Сырьем может служить, в том числе кроме пропилена, пропан-пропиленовая фракция с содержанием пропилена 30—90 % (фракция получаемая при пиролизе и крекинге нефти). Сейчас начинают чаще использовать чистый пропилен, так как в этом случае процесс можно вести при невысоких давлениях, при этом существенно снижается образование побочных продуктов реакции — полимеров и ацетона.
На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (Ch4)2CHOSO2OH{\displaystyle {\ce {(Ch4)2CHOSO2OH}}} , серной кислоты h3SO4{\displaystyle {\ce {h3SO4}}} и воды h3O{\displaystyle {\ce {h3O}}} . На второй стадии процесса — сернокислотный экстракт нагревается с водой и отгоняется образующийся изопропиловый спирт.
Прямую гидратацию пропилена осуществляют в основном в присутствии катализатора — (в скобках указаны условия процессов): ортофосфорной кислоты h4PO4{\displaystyle {{\ce {h4PO4}}}} на твёрдом неорганическом носителе при 240—260°С и 2,5—6,5 МПа) или на носителе из катионообменной смолы при 130—160°С и 8,0—10,0 МПа.
Изопропиловый спирт получают также окислением алканов воздухом, а также и другими способами[6].
Современный способ гидрирования ацетона водородом:
- Ch4COCh4+h3→katCh4CH(OH)Ch4{\displaystyle \mathrm {CH_{3}COCH_{3}+H_{2}{\xrightarrow {kat}}CH_{3}CH(OH)CH_{3}} }
Гидрирование ацетона впаровой фазе в присутствии твёрдого медно-никельхромитного катализатора[10][11].
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск)[12] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)[11][13].
Применение
Изопропиловый спирт используют для получения:
По причине особого государственного регулирования этанола, изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием.
Медицина
70 % изопропиловый спирт применяется вместо этилового спирта в качестве антисептика для пропитки медицинских салфеток.
Влияние на человека
- Ингаляционное
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест 0,6 мг/м³ (ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает[14].
Изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству изопропиловый спирт заменяет этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пламя, полностью разлагается на простые составляющие — воду и углекислый газ, которые не вызывают раздражений и иных побочных эффектов. При горении с достаточным избытком воздуха изопропанол не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости с площадью менее 20 см² в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций у людей[15].
- Пероральное
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко[2].
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола, если только не выпил единовременно от 500 мл.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов[2].
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием[14], наркотический эффект от приёма изопропанола почти в 2 раза превышает аналогичный эффект этанола[16]. Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов вызывает состояние глубокого наркоза и смерть[15].
При длительном воздействии больших концентраций паров в воздухе вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта человеку потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Длительное вдыхание воздуха с концентрацией, значительно превышающем ПДК, может вызвать потерю сознания. Тяжёлое отравление изопропиловым спиртом происходит редко.
Примечания
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0359.html
- ↑ 1 2 3 R. J. Slaughter, R. W. Mason, D. M. G. Beasley, J. A. Vale, L. J. Schep. Isopropanol poisoning // Clinical Toxicology (Philadelphia, Pa.). — 2014-06-01. — Т. 52, вып. 5. — С. 470–478. — ISSN 1556-9519. — DOI:10.3109/15563650.2014.914527.
- ↑ Papa, A. J. «Propanols» // Ullmann’s Encyclopedia of Industrial Chemistry : Weinheim: Wiley-VCH. — 2005.
- ↑ «Guide to Local Production: WHO-recommended Handrub Formulations» (англ.) // World Health Organization. — 2009. — Август.
- ↑ Otitis Externa (Swimmer’s Ear) (26 февраля 2010). Проверено 21 февраля 2016. Архивировано 26 февраля 2010 года.
- ↑ 1 2 ХиМиК.Ру — Изопропиловый спирт
- ↑ Ссылка один (англ.),Ссылка два
- ↑ «Isopropyl Alcohol, by John E. Logsdon and Richard A. Loke», Kirk‑Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc, Article Online Posting Date: December 4, 2000
- ↑ A. J. Papa (2005), «Propanols», Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_173
- ↑ СПОСОБ ПОЛУЧЕНИЯ ПРОПАНОЛА-2 — Патент РФ 2047590
- ↑ 1 2 ООО Синтез Ацетон (недоступная ссылка — история). Проверено 26 ноября 2011. Архивировано 21 марта 2012 года.
- ↑ О заводе | Завод синтетического спирта
- ↑ ПРОИЗВОДСТВО ИЗОПРОПИЛОВОГО СПИРТА В РОССИИ
- ↑ 1 2 ГОСТ 9805-84. Спирт изопропиловый. Технические условия[1]
- ↑ 1 2 Review of Inhalants: Euphoria to Dysfunction Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.,National Institute on Drug Abuse (недоступная ссылка — история). Проверено 10 августа 2011. Архивировано 15 октября 2011 года.
- ↑ «Достоинства и недостатки современных кожных антисептиков» С. В. Волкова, Е. В. Клементенок
ru-wiki.org
Низкотемпературная стекломоющая жидкость
Изобретение относится к моющим составам, предназначенным для очистки твердых поверхностей, в том числе стекол. Сущность: жидкость содержит, мас.%: изопропиловый спирт 10-30, этилкарбитол 2-10, неионогенное поверхностно-активное 0,01-0,10, многоатомный спирт 0,02-0,10, вещество, вода — остальное. В качестве многоатомного спирта жидкость предпочтительно содержит гликоль, а в качестве аминоспирта триэтаноламин. Технический результат — снижение температуры замерзания водных растворов изопропилового спирта до минус 40°С, повышение чистящей способности, снижение суммарного содержания низкотемпературных ингредиентов и, соответственно, стоимости продукции. 2 з.п. ф-лы, 2 табл.
Изобретение относится к моющим составам, предназначенным для очистки твердых поверхностей, в том числе стекол.
В продукции бытовой химии последнее время, в связи с введением акцизов на технические и денатурированные этиловые спирты, стали использовать изопропиловый спирт. Несмотря на то, что изопропиловый спирт уступает этиловому спирту по токсичности (3 класс опасности), коррозионной безопасности (коррозионная активность выше, чем у этилового спирта), имеет неприятный запах, на сегодня он является единственно доступным растворителем для использования в автомобильных стекломоющих низкотемпературных жидкостях и в другой продукции бытовой химии.
Однако по сравнению с этиловым спиртом, для обеспечения одинаковой температуры замерзания водного раствора, требуется более высокая концентрация изопропилового спирта. Для обеспечения температуры замерзания от минус 25°С до минус 30°С, изопропилового спирта потребуется примерно на 10-15% больше.
С целью понижения температуры замерзания водных растворов изопропилового спирта целесообразно введение низкотемпературных компонентов.
Известен состав для чистки стекол (RU 2051957 С1, 1992), включающий неионогенное поверхностно-активное вещество (НПАВ), многоатомный спирт, изопропиловый спирт и воду при следующем соотношении компонентов, мас.%:
| НПАВ | 1-10 |
| Многоатомный спирт | 25-40 |
| Изопропиловый спирт | 10-25 |
| Вода | остальное |
В качестве многоатомного спирта используют этиленгликоль или диэтиленгликоль.
Для обеспечения низкой температуры замерзания данного состава с содержанием изопропилового спирта в количестве 10-25 мас.% требуется введение большого количества (25-40 мас.%) многоатомного спирта (этиленгликоля или диэтиленгликоля), то есть суммарное содержание низкотемпературных компонентов составляет 35-65 мас.%.
Данный состав является эффективным чистящим средством. Однако использование его в качестве стеклоомывающей жидкости для автомобильных стекол связано с таким недостатком, как закрывание видимости через стекло вследствие образования большого количества пены и жирных натеков на стекле, обусловленных наличием в составе значительного содержания НПАВ и многоатомного спирта.
Задачей настоящего изобретения является разработка низкотемпературной стекломоющей жидкости на основе изопропилового спирта, лишенной недостатков прототипа благодаря дополнительному содержанию этилкарбитола, что позволяет существенно уменьшить содержание в составе НПАВ и многоатомного спирта и расширить возможности применения данной жидкости.
Согласно изобретению предлагается низкотемпературная стекломоющая жидкость, включающая изопропиловый спирт, многоатомный спирт, неионогенное поверхностно-активное вещество и воду, дополнительно содержит этилкарбитол при следующем соотношении ингредиентов, мас.%:
| изопропиловый спирт | 10-30 |
| этилкарбитол | 2,0-10,0 |
| неионогенное поверхностно-активное вещество | 0,01-0,10 |
| многоатомный спирт | 0,02-0,10 |
| вода | остальное. |
Преимущественно жидкость дополнительно содержит аминоспирт в количестве 0,01-0,03 мас.%, отдушку в количестве 0,02-0,20 мас.% и краситель в количестве 0,0002-0,0006 мас.%. В качестве многоатомного спирта целесообразно применять гликоль (этиленгликоль, диэтиленгликоль, пропиленгликоль и др.), в качестве аминоспирта — триэтаноламин.
При приведенном суммарном содержании изопропилового спирта и этилкарбитола (12-40 мас.%) температура замерзания стекломоющей жидкости составляет от минус 7°С до минус 40°С. Для обеспечения указанной температуры замерзания жидкости без этилкарбитола потребовалось бы от 14 до 68 мас.% изопропилового спирта.
Неионогенное ПАВ повышает смачивающую и чистящую способность жидкости. При концентрациях НПАВ выше 0,1% эффективность действия НПАВ не повышается. Следовательно, повышение концентрации НПАВ более 0,1% мас.% нецелесообразно.
Многоатомный спирт в данном составе выполняет функцию мягчителя, устраняющего скрип щеток.
Аминоспирт способствует устранению коррозионного воздействия изопропилового спирта на лакокрасочные покрытия, резиновые детали и металлические части кузова автомобиля.
Известно использование этилкарбитола в хладоносителях (Баранник В.П., Маринюк Б.Т., Овчаренко B.C., Афонский В.П. Новый хладоноситель, особенности и перспективы применения. Холодильный бизнес, 2001, №1. Этилкарбитол).
При этом этилкарбитол в водных растворах с концентрацией до 10 мас.% не эффективен; при концентрации этилкарбитола 30 мас.% температура замерзания воды понижается всего на 5°, то есть температура замерзания водного раствора этилкарбитола с концентрацией 30% мас. составляет всего минус 5°С.
Неожиданно выявлено, что в водных растворах изопропилового спирта эффективность действия этилкарбитола по понижению температуры замерзания существенно выше.
При введении в водный раствор изопропилового спирта (с концентрацией 10-30 мас.%) этилкарбитола в количестве всего 5 мас.% температура замерзания раствора понижается на 2-10°С, при введении 10% этилкарбитола — на 5-15°С (в том же интервале концентраций изопропилового спирта).
Введение в водный раствор изопропилового спирта этилкарбитола в количестве менее 5 мас.% малоэффективно, более 10 мас.% — нецелесообразно, так как эффективность понижения температуры замерзания растворов с повышением содержания этилкарбитола падает.
Понижение температуры замерзания водных растворов изопропилового спирта при введении этилкарбитола до 10% более эффективно, чем при введении в таком же количестве других низкотемпературных жидкостей: этилового, метилового спиртов, глицерина, гликолей (этиленгликоля, диэтиленгликоля, пропиленгликоля).
Температура плавления этилкарбитола (минус 78°С) выше, чем у изопропилового спирта (минус 89,5°С). Следовательно, действие этилкарбитола можно объяснить снижением взаимодействия между молекулами изопропилового спирта, что и приводит к понижению температуры замерзания.
Для достижения одной и той же температуры замерзания с введением этилкарбитола снижается суммарная концентрация низкозамерзающих ингредиентов в водном растворе (таблица 1).
| Таблица 1 | |||||
| Температура замерзания водного раствора, °С | Массовая доля в водном растворе изопропилового спирта с этилкарбитолом, % | Суммарная массовая доля в водном растворе изопропилового спирта с этилкарбитолом, % | |||
| Массовая доля этилкарбитола. % | |||||
| 2,5 | 5,0 | 7,5 | 10,0 | ||
| Минус 15 | 24 | 24 | 24 | 26,5 | 27 |
| Минус 16 | 27 | 25,5 | 25 | 26,5 | 28 |
| Минус 20 | 34 | 28,5 | 28 | 30 | 30 |
| Минус 25 | 45 | 34 | 32 | 33,5 | 34 |
| Минус 28 | 49 | 37 | 35 | 36 | 36 |
В таблице 2 приведена температура замерзания водных растворов изопропилового спирта при введении этилкарбитола от 2,0 мас.% до 10 мас.%.
| Таблица 2 | |||||
| Массовая доля изопропилового спирта в растворе, % | Температура замерзания раствора, °С, при содержании в растворе этилкарбитола, мас.% | ||||
| 0 | 2,5 | 5,0 | 7,5 | 10,0 | |
| 10 | минус 4,5 | минус 6 | минус 6,5 | минус 7 | минус 9 |
| 15 | минус 8 | минус 9 | минус 10 | минус 11 | минус 12 |
| 20 | минус 11 | минус 13 | минус 16 | минус 17 | минус 20 |
| 22 | минус 13 | — | — | — | — |
| 25 | минус 15 | минус 19 | минус 23 | минус 25 | минус 27 |
| 27,5 | минус 17 | — | — | — | — |
| 30 | минус 18 | минус 24 | минус 28 | минус 30 | минус 40 |
| 34 | минус 20 | — | — | — | — |
| 40 | минус 24 | — | — | — | — |
Как следует из результатов, приведенных в таблице 2, с введением этилкарбитола суммарная концентрация изопропилового спирта и этилкарбитола (для достижения одной и той же температуры замерзания) меньше концентрации изопропилового спирта в растворе без добавления этилкарбитола.
Коррозионная активность стекломоющей жидкости за счет уменьшения концентрации изопропилового спирта также понижается.
Наиболее оптимальной является концентрация этилкарбитола 5 мас.%, обеспечивающая минимальное суммарное содержание низкозамерзающих компонентов в водном растворе.
В других случаях количество введения в раствор этилкарбитола будет определяться соотношением цен на изопропиловый спирт и этилкарбитол.
Низкотемпературная стекломоющая жидкость не выделяет токсичных продуктов, безопасна для окружающей среды.
Чистящая способность низкотемпературной стекломоющей жидкости не ниже 98%.
Низкотемпературная стекломоющая жидкость не пенится при обмывании стекол, не оставляет на стекле разводов, пленок.
Смешение ингредиентов производится при комнатной температуре.
Пример 1. Для приготовления 500 кг низкотемпературной стекломоющей жидкости в 389,7 кг (77,94 мас.%) воды приливают 100 кг (20 мас.%) изопропилового спирта, 10 кг (2 мас.%) этилкарбитола, вводят 0,05 кг (0,01 мас.%) НПАВ (неонол), 0,1 кг (0,02 мас.%) этиленгликоля, 0,05 кг 90,01 мас.%) триэтаноламина, 0,1 кг (0,02 мас.%) отдушки и 1 г (0,0002 мас.%) красителя. Раствор перемешивают в течение 10-15 мин. Раствор однородный, прозрачный. Температура замерзания минус 14°С. Чистящая способность 98%. На стеклах автомобилей не оставляет разводов, пленок и т.п.
Пример 2. Для приготовления 500 кг низкотемпературной стекломоющей-жидкости в 298 кг (59,6 мас.%) воды приливают 150 кг (30 мас.%) изопропилового спирта, 50 кг (10 мас.%) этилкарбитола, вводят по 0,5 кг (0,1 мас.%) неонола (НПАВ) и этиленгликоля, 0,15 кг (0,03 мас.%) триэтаноламина, 1 кг (0,2 мас.%) отдушки и 3 г красителя. Раствор перемешивают в течение 10-15 мин. Раствор однородный, прозрачный. Температура замерзания минус 32°С. Чистящая способность 99,8%. На стеклах автомобилей не оставляет разводов, пленок и т.п.
Аналогичные результаты получаются при использовании в качестве многоатомных спиртов других гликолей: диэтиленгликоля, пропиленгликоля, а также в отсутствии целевых добавок — аминоспирта, отдушки и красителя.
Низкотемпературная стекломоющая жидкость экологически безопасна, обладает высокими чистящими свойствами, не оставляет на стекле разводов и пленок, не образует пены при обмывании стекол, не повреждает лакокрасочное покрытие кузова автомобиля, не вызывает коррозии металлических и резиновых деталей и может использоваться как стекломоющая жидкость, так и чистящее средство.
Наличие в составе этилкарбитола приводит к понижению температуры замерзания водного раствора изопропилового спирта, снижению суммарного содержания низкотемпературных ингредиентов в составе и удешевлению продукции.
1. Низкотемпературная стекломоющая жидкость, включающая изопропиловый спирт, многоатомный спирт, неионогенное поверхностно-активное вещество и воду, отличающаяся тем, что она дополнительно содержит этилкарбитол при следующем соотношении ингредиентов, мас.%:
| изопропиловый спирт | 10-30 |
| этилкарбитол | 2,0-10,0 |
| неионогенное поверхностно-активное вещество | 0,01-0,10 |
| многоатомный спирт | 0,02-0,10 |
| вода | остальное |
2. Жидкость по п.1, отличающаяся тем, что она дополнительно содержит аминоспирт в количестве 0,01-0,03 мас.%, отдушку в количестве 0,02-0,20 мас.% и краситель в количестве 0,0002-0,0006 мас.%.
3. Жидкость по п.2, отличающаяся тем, что в качестве многоатомного спирта она содержит гликоль, а в качестве аминоспирта — триэтаноламин.
www.findpatent.ru
Изопропиловый спирт — Википедия (с комментариями)
Материал из Википедии — свободной энциклопедии
| Изопропанол | |
 | |
| Isopropanol-3D-vdW.png | |
| Общие | |
|---|---|
| Систематическое наименование | Пропан-2-ол |
| Традиционные названия | Изопропиловый спирт |
| Хим. формула | C3H8O |
| Рац. формула | CH3CH(OH)CH3 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 60,09 г/моль |
| Плотность | 0,7851 г/см³ |
| Динамическая вязкость | 0,00243 Па·с |
| Термические свойства | |
| Т. плав. | -89,5 °C |
| Т. кип. | 82,4 °C |
| Т. всп. | 11,7 °C |
| Т. свспл. | 400 °C |
| Мол. теплоёмк. | 155,2 Дж/(моль·К) |
| Давление пара | 4,4 кПа при 20 °C |
| Химические свойства | |
| pKa | 16,5 |
| Растворимость в бензоле | хорошо растворим |
| Растворимость в ацетоне | растворим |
| Оптические свойства | |
| Показатель преломления | 1,3776 |
| Структура | |
| Дипольный момент | 1,66 Д |
| Классификация | |
| Рег. номер CAS | 67-63-0 |
| SMILES |
[chemapps.stolaf.edu/jmol/jmol.php?model=CC%28O%29C CC(O)C] |
| Безопасность | |
| Токсичность | довольно высокая |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Изопропиловый спирт, пропанол-2 (2-пропанол), изопропанол, диметилкарбинол, ИПС — простейший вторичный одноатомный спирт алифатического ряда. Существует изомер изопропанола — пропанол-1.
Прозрачная, бесцветная жидкость с фруктовым запахом и мягким горьким вкусом.[1]
Изопропиловый спирт используется в качестве заменителя этилового спирта в косметике, парфюмерии, бытовой химии, автохимии, медицинских изделиях, в средствах для очистки стёкол, оргтехники и как растворитель в промышленности.
В развитых странах пропанол-2 широко используется в товарах личной гигиены и в медицине, благодаря низкой токсичности.[2] 75 % Водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь мембраны пор бактерий, таким образом обеспечивая высокую эффективность и более качественное обеззараживание[3]. Изопропиловый спирт используется в качестве вспомогательного компонента профилактического средства от наружного отита.[4]
Как и все спирты, огнеопасен, токсичен, требует осторожного отношения. Оказывает раздражающее действие на кожу.
Свойства
Химические свойства
Химическая формула (рациональная) изопропилового спирта: CH3CH(OH)CH3.
Изопропанол обладает свойствами вторичных спиртов жирного ряда, в том числе образует простые и сложные эфиры. Гидроксильная группа может быть вытеснена представителями ряда галогенов. С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол. В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения. При дегидрировании превращается в ацетон.[5]
Реагирует с сильными окислителями. Агрессивен в отношении некоторых видов пластика и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резковатым по сравнению с этанолом (по чему их можно в некоторых случаях отличить), tплавления −89,5 °C, tкипения 82,4 °C, плотность 0,7851 г/см³ (при 20 °C), tвспышки 11,7 °C. Нижний предел взрываемости в воздухе 2,5 % по объёму (при 25 °C). Температура самовоспламенения 456 °C. Коэффициент преломления 1,3776 (в жидком состоянии, при 20 °C). Динамическая вязкость при стандартных условиях 2,43 мПа·с. Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К).
Пар хорошо смешивается с воздухом, легко образует взрывчатые смеси. Давление паров — 4,4 кПа (при 20 °C). Относительная плотность пара — 2,1, относительная плотность смеси пар/воздух — 1,05 (при 20 °C).
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях. С водой образует азеотропную смесь (87,9 % изопропилового спирта, tкипения 80,2 °C).
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице[6]:
| Концентрация спирта об % | Концентрация спирта вес % | Температура замерзания °C |
|---|---|---|
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Получение
Существует два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена.[7][8]
Основным способом получения изопропанола в Российской промышленности является сернокислотная гидратация пропилена
- CH3CH=CH2 + H2SO4 → (CH3)2CHOSO3H + H2O → (CH3)2CHOH.
Сырьем может служить пропан-пропиленовая фракция с содержанием пропилена 30-90 % (фракция пиролиза и крекинга нефти). Однако наблюдается тенденция к использованию чистого пропилена, так как в этом случае процесс можно вести при невысоких давлениях, резко снижается образование побочных продуктов реакции — полимеров и ацетона. На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (Ch4)2CHOSO2OH, H2SO4 и Н2О, на второй — сернокислотный экстракт нагревается с водой и удаляется образующийся изопропиловый спирт. Прямую гидратацию пропилена осуществляют в основном в присутствии твердого катализатора (в скобках указаны условия процессов): Н3РО4 на носителе (240—260°С; 2,5-6,5 МПа) или катионообменной смолы (130—160°С; 8,0-10,0 МПа). Изопропиловый спирт получают также окислением парафинов воздухом и другими способами.[5]
Современный способ:
- <math>\mathrm{CH_3COCH_3 +H_2\xrightarrow{kat} CH_3CH(OH)CH_3}</math>
Гидрирование ацетона водородом (в фазе пара) в присутствии стационарного медно-никельхромитного катализатора.[9][10]
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск)[11] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)[10][12]
Применение
Изопропиловый спирт используют для получения:
По причине особого государственного регулирования этанола, изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием.
Медицина
70 % изопропиловый спирт применяется вместо этилового спирта как антисептик для пропитки медицинских салфеток.
Влияние на человека
Ингаляционное. Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе составляет 10 мг/м³. Не накапливается в организме, то есть укумулятивными свойствами не обладает[13]. Необходимо отметить, что изопропиловый спирт значительно менее летуч чем, например, этанол и для достижения больших концентраций его паров, необходима значительно большая площадь разлива и испарения. Благодаря этому свойству, изопропиловый спирт заменил этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пышное пламя, полностью разлагается на простые составляющие — воду и углекислый газ, не вызывая раздражений и иных побочных эффектов. Горение изопропанола не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости с площадью менее 20 см² в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций.[14]
Пероральное.
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко.[1]
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза больше, чем у этанола, но при этом опьяняющее действие его также выше в 10 раз. По этой причине смертельных отравлений изопропанолом не зафиксировано, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8,0 часов.[1]
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием.[13] Наркотический эффект изопропанола почти в 2 раза превышает аналогичный эффект этанола.[15] Концентрация 1,2 %, воздействующая в течение 4 часов, оказывает опьяняющее действие.[14]
При длительном воздействии больших концентраций паров вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта потребуется находиться в течении длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Воздействие на уровне, значительно превышающем ПДК, может вызвать потерю сознания. Отравление изопропиловым спиртом возникает нечасто.
Напишите отзыв о статье «Изопропиловый спирт»
Примечания
- ↑ 1 2 3 R. J. Slaughter, R. W. Mason, D. M. G. Beasley, J. A. Vale, L. J. Schep [www.ncbi.nlm.nih.gov/pubmed/24815348 Isopropanol poisoning] // Clinical Toxicology (Philadelphia, Pa.). — 2014-06-01. — Т. 52, вып. 5. — С. 470–478. — ISSN [www.sigla.ru/table.jsp?f=8&t=3&v0=1556-9519&f=1003&t=1&v1=&f=4&t=2&v2=&f=21&t=3&v3=&f=1016&t=3&v4=&f=1016&t=3&v5=&bf=4&b=&d=0&ys=&ye=&lng=&ft=&mt=&dt=&vol=&pt=&iss=&ps=&pe=&tr=&tro=&cc=UNION&i=1&v=tagged&s=0&ss=0&st=0&i18n=ru&rlf=&psz=20&bs=20&ce=hJfuypee8JzzufeGmImYYIpZKRJeeOeeWGJIZRrRRrdmtdeee88NJJJJpeeefTJ3peKJJ3UWWPtzzzzzzzzzzzzzzzzzbzzvzzpy5zzjzzzzzzzzzzzzzzzzzzzzzzzzzzzzzzzztzzzzzzzbzzzzzzzzzzzzzzzzzzzzzzzzzzzvzzzzzzyeyTjkDnyHzTuueKZePz9decyzzLzzzL*.c8.NzrGJJvufeeeeeJheeyzjeeeeJh*peeeeKJJJJJJJJJJmjHvOJJJJJJJJJfeeeieeeeSJJJJJSJJJ3TeIJJJJ3..E.UEAcyhxD.eeeeeuzzzLJJJJ5.e8JJJheeeeeeeeeeeeyeeK3JJJJJJJJ*s7defeeeeeeeeeeeeeeeeeeeeeeeeeSJJJJJJJJZIJJzzz1..6LJJJJJJtJJZ4….EK*&debug=false 1556-9519]. — DOI:10.3109/15563650.2014.914527.
- ↑ Papa, A. J. [dx.doi.org/10.1002%2F14356007.a22_173 «Propanols»] // Ullmann’s Encyclopedia of Industrial Chemistry : Weinheim: Wiley-VCH. — 2005.
- ↑ [www.who.int/gpsc/5may/Guide_to_Local_Production.pdf «Guide to Local Production: WHO-recommended Handrub Formulations»] (англ.) // World Health Organization. — 2009. — Август.
- ↑ [web.archive.org/web/20100226215757/www.mcw.edu/pediatricoto/CommonHealthProblems/OtitisExternaSwimmersEar.htm Otitis Externa (Swimmer’s Ear)] (26 февраля 2010). Проверено 21 февраля 2016.
- ↑ 1 2 [www.xumuk.ru/encyklopedia/1625.html ХиМиК.Ру — Изопропиловый спирт]
- ↑ [www.engineeringtoolbox.com/ispropanol-water-d_988.html Ссылка один] (англ.),[www.chemport.ru/forum/viewtopic.php?f=4&t=40177&start=20 Ссылка два]
- ↑ «Isopropyl Alcohol, by John E. Logsdon and Richard A. Loke», Kirk‑Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc, Article Online Posting Date: December 4, 2000
- ↑ A. J. Papa (2005), «Propanols», Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_173
- ↑ [ru-patent.info/20/45-49/2047590.html СПОСОБ ПОЛУЧЕНИЯ ПРОПАНОЛА-2 — Патент РФ 2047590]
- ↑ 1 2 [sintez-aceton.ru/izopropilovyy-spirt/ ООО Синтез Ацетон]
- ↑ [isopropanol.ru/ru/about.html О заводе | Завод синтетического спирта]
- ↑ [www.newchemistry.ru/letter.php?n_id=8058 ПРОИЗВОДСТВО ИЗОПРОПИЛОВОГО СПИРТА В РОССИИ]
- ↑ 1 2 [www.himtrade.ru/g_9805-84.htm#3 ГОСТ 9805-84. Спирт изопропиловый. Технические условия][protect.gost.ru/document.aspx?control=7&id=143685]
- ↑ 1 2 [archives.drugabuse.gov/pdf/monographs/15.pdf Review of Inhalants: Euphoria to Dysfunction Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.,National Institute on Drug Abuse]
- ↑ [www.poliklin.ru/imagearticle/201103/148-149.pdf «Достоинства и недостатки современных кожных антисептиков» С. В. Волкова, Е. В. Клементенок]
Отрывок, характеризующий Изопропиловый спирт
Из трех назначений масонства Пьер сознавал, что он не исполнял того, которое предписывало каждому масону быть образцом нравственной жизни, и из семи добродетелей совершенно не имел в себе двух: добронравия и любви к смерти. Он утешал себя тем, что за то он исполнял другое назначение, – исправление рода человеческого и имел другие добродетели, любовь к ближнему и в особенности щедрость.Весной 1807 года Пьер решился ехать назад в Петербург. По дороге назад, он намеревался объехать все свои именья и лично удостовериться в том, что сделано из того, что им предписано и в каком положении находится теперь тот народ, который вверен ему Богом, и который он стремился облагодетельствовать.
Главноуправляющий, считавший все затеи молодого графа почти безумством, невыгодой для себя, для него, для крестьян – сделал уступки. Продолжая дело освобождения представлять невозможным, он распорядился постройкой во всех имениях больших зданий школ, больниц и приютов; для приезда барина везде приготовил встречи, не пышно торжественные, которые, он знал, не понравятся Пьеру, но именно такие религиозно благодарственные, с образами и хлебом солью, именно такие, которые, как он понимал барина, должны были подействовать на графа и обмануть его.
Южная весна, покойное, быстрое путешествие в венской коляске и уединение дороги радостно действовали на Пьера. Именья, в которых он не бывал еще, были – одно живописнее другого; народ везде представлялся благоденствующим и трогательно благодарным за сделанные ему благодеяния. Везде были встречи, которые, хотя и приводили в смущение Пьера, но в глубине души его вызывали радостное чувство. В одном месте мужики подносили ему хлеб соль и образ Петра и Павла, и просили позволения в честь его ангела Петра и Павла, в знак любви и благодарности за сделанные им благодеяния, воздвигнуть на свой счет новый придел в церкви. В другом месте его встретили женщины с грудными детьми, благодаря его за избавление от тяжелых работ. В третьем именьи его встречал священник с крестом, окруженный детьми, которых он по милостям графа обучал грамоте и религии. Во всех имениях Пьер видел своими глазами по одному плану воздвигавшиеся и воздвигнутые уже каменные здания больниц, школ, богаделен, которые должны были быть, в скором времени, открыты. Везде Пьер видел отчеты управляющих о барщинских работах, уменьшенных против прежнего, и слышал за то трогательные благодарения депутаций крестьян в синих кафтанах.
Пьер только не знал того, что там, где ему подносили хлеб соль и строили придел Петра и Павла, было торговое село и ярмарка в Петров день, что придел уже строился давно богачами мужиками села, теми, которые явились к нему, а что девять десятых мужиков этого села были в величайшем разорении. Он не знал, что вследствие того, что перестали по его приказу посылать ребятниц женщин с грудными детьми на барщину, эти самые ребятницы тем труднейшую работу несли на своей половине. Он не знал, что священник, встретивший его с крестом, отягощал мужиков своими поборами, и что собранные к нему ученики со слезами были отдаваемы ему, и за большие деньги были откупаемы родителями. Он не знал, что каменные, по плану, здания воздвигались своими рабочими и увеличили барщину крестьян, уменьшенную только на бумаге. Он не знал, что там, где управляющий указывал ему по книге на уменьшение по его воле оброка на одну треть, была наполовину прибавлена барщинная повинность. И потому Пьер был восхищен своим путешествием по именьям, и вполне возвратился к тому филантропическому настроению, в котором он выехал из Петербурга, и писал восторженные письма своему наставнику брату, как он называл великого мастера.
«Как легко, как мало усилия нужно, чтобы сделать так много добра, думал Пьер, и как мало мы об этом заботимся!»
Он счастлив был выказываемой ему благодарностью, но стыдился, принимая ее. Эта благодарность напоминала ему, на сколько он еще больше бы был в состоянии сделать для этих простых, добрых людей.
Главноуправляющий, весьма глупый и хитрый человек, совершенно понимая умного и наивного графа, и играя им, как игрушкой, увидав действие, произведенное на Пьера приготовленными приемами, решительнее обратился к нему с доводами о невозможности и, главное, ненужности освобождения крестьян, которые и без того были совершенно счастливы.
Пьер втайне своей души соглашался с управляющим в том, что трудно было представить себе людей, более счастливых, и что Бог знает, что ожидало их на воле; но Пьер, хотя и неохотно, настаивал на том, что он считал справедливым. Управляющий обещал употребить все силы для исполнения воли графа, ясно понимая, что граф никогда не будет в состоянии поверить его не только в том, употреблены ли все меры для продажи лесов и имений, для выкупа из Совета, но и никогда вероятно не спросит и не узнает о том, как построенные здания стоят пустыми и крестьяне продолжают давать работой и деньгами всё то, что они дают у других, т. е. всё, что они могут давать.
В самом счастливом состоянии духа возвращаясь из своего южного путешествия, Пьер исполнил свое давнишнее намерение заехать к своему другу Болконскому, которого он не видал два года.
Богучарово лежало в некрасивой, плоской местности, покрытой полями и срубленными и несрубленными еловыми и березовыми лесами. Барский двор находился на конце прямой, по большой дороге расположенной деревни, за вновь вырытым, полно налитым прудом, с необросшими еще травой берегами, в середине молодого леса, между которым стояло несколько больших сосен.
Барский двор состоял из гумна, надворных построек, конюшень, бани, флигеля и большого каменного дома с полукруглым фронтоном, который еще строился. Вокруг дома был рассажен молодой сад. Ограды и ворота были прочные и новые; под навесом стояли две пожарные трубы и бочка, выкрашенная зеленой краской; дороги были прямые, мосты были крепкие с перилами. На всем лежал отпечаток аккуратности и хозяйственности. Встретившиеся дворовые, на вопрос, где живет князь, указали на небольшой, новый флигелек, стоящий у самого края пруда. Старый дядька князя Андрея, Антон, высадил Пьера из коляски, сказал, что князь дома, и проводил его в чистую, маленькую прихожую.
Пьера поразила скромность маленького, хотя и чистенького домика после тех блестящих условий, в которых последний раз он видел своего друга в Петербурге. Он поспешно вошел в пахнущую еще сосной, не отштукатуренную, маленькую залу и хотел итти дальше, но Антон на цыпочках пробежал вперед и постучался в дверь.
– Ну, что там? – послышался резкий, неприятный голос.
– Гость, – отвечал Антон.
– Проси подождать, – и послышался отодвинутый стул. Пьер быстрыми шагами подошел к двери и столкнулся лицом к лицу с выходившим к нему, нахмуренным и постаревшим, князем Андреем. Пьер обнял его и, подняв очки, целовал его в щеки и близко смотрел на него.
– Вот не ждал, очень рад, – сказал князь Андрей. Пьер ничего не говорил; он удивленно, не спуская глаз, смотрел на своего друга. Его поразила происшедшая перемена в князе Андрее. Слова были ласковы, улыбка была на губах и лице князя Андрея, но взгляд был потухший, мертвый, которому, несмотря на видимое желание, князь Андрей не мог придать радостного и веселого блеска. Не то, что похудел, побледнел, возмужал его друг; но взгляд этот и морщинка на лбу, выражавшие долгое сосредоточение на чем то одном, поражали и отчуждали Пьера, пока он не привык к ним.
При свидании после долгой разлуки, как это всегда бывает, разговор долго не мог остановиться; они спрашивали и отвечали коротко о таких вещах, о которых они сами знали, что надо было говорить долго. Наконец разговор стал понемногу останавливаться на прежде отрывочно сказанном, на вопросах о прошедшей жизни, о планах на будущее, о путешествии Пьера, о его занятиях, о войне и т. д. Та сосредоточенность и убитость, которую заметил Пьер во взгляде князя Андрея, теперь выражалась еще сильнее в улыбке, с которою он слушал Пьера, в особенности тогда, когда Пьер говорил с одушевлением радости о прошедшем или будущем. Как будто князь Андрей и желал бы, но не мог принимать участия в том, что он говорил. Пьер начинал чувствовать, что перед князем Андреем восторженность, мечты, надежды на счастие и на добро не приличны. Ему совестно было высказывать все свои новые, масонские мысли, в особенности подновленные и возбужденные в нем его последним путешествием. Он сдерживал себя, боялся быть наивным; вместе с тем ему неудержимо хотелось поскорей показать своему другу, что он был теперь совсем другой, лучший Пьер, чем тот, который был в Петербурге.
– Я не могу вам сказать, как много я пережил за это время. Я сам бы не узнал себя.
– Да, много, много мы изменились с тех пор, – сказал князь Андрей.
– Ну а вы? – спрашивал Пьер, – какие ваши планы?
– Планы? – иронически повторил князь Андрей. – Мои планы? – повторил он, как бы удивляясь значению такого слова. – Да вот видишь, строюсь, хочу к будущему году переехать совсем…
Пьер молча, пристально вглядывался в состаревшееся лицо (князя) Андрея.
– Нет, я спрашиваю, – сказал Пьер, – но князь Андрей перебил его:
– Да что про меня говорить…. расскажи же, расскажи про свое путешествие, про всё, что ты там наделал в своих именьях?
Пьер стал рассказывать о том, что он сделал в своих имениях, стараясь как можно более скрыть свое участие в улучшениях, сделанных им. Князь Андрей несколько раз подсказывал Пьеру вперед то, что он рассказывал, как будто всё то, что сделал Пьер, была давно известная история, и слушал не только не с интересом, но даже как будто стыдясь за то, что рассказывал Пьер.
Пьеру стало неловко и даже тяжело в обществе своего друга. Он замолчал.
– А вот что, душа моя, – сказал князь Андрей, которому очевидно было тоже тяжело и стеснительно с гостем, – я здесь на биваках, и приехал только посмотреть. Я нынче еду опять к сестре. Я тебя познакомлю с ними. Да ты, кажется, знаком, – сказал он, очевидно занимая гостя, с которым он не чувствовал теперь ничего общего. – Мы поедем после обеда. А теперь хочешь посмотреть мою усадьбу? – Они вышли и проходили до обеда, разговаривая о политических новостях и общих знакомых, как люди мало близкие друг к другу. С некоторым оживлением и интересом князь Андрей говорил только об устраиваемой им новой усадьбе и постройке, но и тут в середине разговора, на подмостках, когда князь Андрей описывал Пьеру будущее расположение дома, он вдруг остановился. – Впрочем тут нет ничего интересного, пойдем обедать и поедем. – За обедом зашел разговор о женитьбе Пьера.
– Я очень удивился, когда услышал об этом, – сказал князь Андрей.
Пьер покраснел так же, как он краснел всегда при этом, и торопливо сказал:
– Я вам расскажу когда нибудь, как это всё случилось. Но вы знаете, что всё это кончено и навсегда.
– Навсегда? – сказал князь Андрей. – Навсегда ничего не бывает.
– Но вы знаете, как это всё кончилось? Слышали про дуэль?
– Да, ты прошел и через это.
– Одно, за что я благодарю Бога, это за то, что я не убил этого человека, – сказал Пьер.
– Отчего же? – сказал князь Андрей. – Убить злую собаку даже очень хорошо.
– Нет, убить человека не хорошо, несправедливо…
– Отчего же несправедливо? – повторил князь Андрей; то, что справедливо и несправедливо – не дано судить людям. Люди вечно заблуждались и будут заблуждаться, и ни в чем больше, как в том, что они считают справедливым и несправедливым.
– Несправедливо то, что есть зло для другого человека, – сказал Пьер, с удовольствием чувствуя, что в первый раз со времени его приезда князь Андрей оживлялся и начинал говорить и хотел высказать всё то, что сделало его таким, каким он был теперь.
– А кто тебе сказал, что такое зло для другого человека? – спросил он.
– Зло? Зло? – сказал Пьер, – мы все знаем, что такое зло для себя.
– Да мы знаем, но то зло, которое я знаю для себя, я не могу сделать другому человеку, – всё более и более оживляясь говорил князь Андрей, видимо желая высказать Пьеру свой новый взгляд на вещи. Он говорил по французски. Je ne connais l dans la vie que deux maux bien reels: c’est le remord et la maladie. II n’est de bien que l’absence de ces maux. [Я знаю в жизни только два настоящих несчастья: это угрызение совести и болезнь. И единственное благо есть отсутствие этих зол.] Жить для себя, избегая только этих двух зол: вот вся моя мудрость теперь.
– А любовь к ближнему, а самопожертвование? – заговорил Пьер. – Нет, я с вами не могу согласиться! Жить только так, чтобы не делать зла, чтоб не раскаиваться? этого мало. Я жил так, я жил для себя и погубил свою жизнь. И только теперь, когда я живу, по крайней мере, стараюсь (из скромности поправился Пьер) жить для других, только теперь я понял всё счастие жизни. Нет я не соглашусь с вами, да и вы не думаете того, что вы говорите.
Князь Андрей молча глядел на Пьера и насмешливо улыбался.
– Вот увидишь сестру, княжну Марью. С ней вы сойдетесь, – сказал он. – Может быть, ты прав для себя, – продолжал он, помолчав немного; – но каждый живет по своему: ты жил для себя и говоришь, что этим чуть не погубил свою жизнь, а узнал счастие только тогда, когда стал жить для других. А я испытал противуположное. Я жил для славы. (Ведь что же слава? та же любовь к другим, желание сделать для них что нибудь, желание их похвалы.) Так я жил для других, и не почти, а совсем погубил свою жизнь. И с тех пор стал спокойнее, как живу для одного себя.
wiki-org.ru
Изопропиловый спирт — Википедия
| Изопропанол | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Пропан-2-ол |
| Традиционные названия | Изопропиловый спирт |
| Хим. формула | C3H8O |
| Рац. формула | CH3CH(OH)CH3 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 60,09 г/моль |
| Плотность | 0,7851 г/см³ |
| Динамическая вязкость | 0,00243 Па·с |
| Энергия ионизации | 10,1 ± 0,1 эВ[1] |
| Термические свойства | |
| Т. плав. | -89,5 °C |
| Т. кип. | 82,4 °C |
| Т. всп. | 11,7 °C |
| Т. свспл. | 400 °C |
| Пр. взрв. | 2 ± 1 об.%[1] |
| Мол. теплоёмк. | 155,2 Дж/(моль·К) |
| Давление пара | 4,4 кПа при 20 °C |
| Химические свойства | |
| pKa | 16,5 |
| Растворимость в бензоле | хорошо растворим |
| Растворимость в ацетоне | растворим |
| Оптические свойства | |
| Показатель преломления | 1,3776 (nD, 20°C) |
| Структура | |
| Дипольный момент | 1,66 Д |
| Классификация | |
| Рег. номер CAS | 67-63-0 |
| PubChem | 3776 |
| Рег. номер EINECS | 200-661-7 |
| SMILES | |
| InChI | |
| RTECS | NT8050000 |
| ChEBI | 17824 и 43588 |
| Номер ООН | 1219 |
| ChemSpider | 3644 |
| Безопасность | |
| ЛД50 | 12800 мг/кг (кролик) |
| Токсичность | Класс опасности 3 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Изопропи́ловый спирт (пропано́л-2, втор-пропанол, изопропано́л, диметилкарбино́л, ИПС) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует изомер изопропанола — пропанол-1.
При нормальных условиях прозрачная, бесцветная жидкость с резким запахом и мягким горьким вкусом[2].
Изопропиловый спирт используется в качестве заменителя этилового спирта в косметике, парфюмерии, бытовой химии, жидкостей для автомобилей, медицинских целях, в средствах для очистки стёкол, оргтехники и как растворитель органических веществ промышленности.
В развитых странах изопропанол широко используется в товарах личной гигиены и в медицине, благодаря своей относительно низкой токсичности[3].
75 % водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь клеточные мембраны бактерий, таким образом обеспечивает более высокую эффективность и лучшее обеззараживание[4].
Изопропиловый спирт также используется в медицине в качестве вспомогательного компонента профилактического средства от наружного отита[5].
Эффективен при лечении дерматита протиранием пораженных участков кожи, с малым вредным влиянием на кожу.
Как и все летучие спирты, огнеопасен. Умеренно токсичен, требует осторожного обращения.
Свойства
Химические свойства
Рациональная химическая формула изопропилового спирта Ch4CH(OH)Ch4{\displaystyle {\ce {Ch4CH(OH)Ch4}}}.
Изопропанол обладает всеми свойствами вторичных спиртов жирного ряда, образует простые и сложные эфиры.
Гидроксильная группа может быть вытеснена галогенами.
С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол.
При дегидрировании превращается в ацетон[6].
Реагирует с сильными окислителями.
В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения.
Растворяет некоторые виды пластмасс и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резким, чем у этанола, по запаху их можно в некоторых случаях отличить.
Коэффициент преломления nD = 1,3776 при 20 °C. Динамическая вязкость при стандартных условиях 2,43 мПа·с — немного более вязкий, чем вода . Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К). Удельная теплота сгорания 34,1 МДж/кг.
Пар хорошо смешивается с воздухом, в диапазоне взрывоопасных концентраций образует взрывчатые смеси. Давление насыщенного пара при 20 °C — 4,4 кПа. Относительная плотность пара по воздуху — 2,1, относительная плотность смеси насыщенный пар/воздух — 1,05 при 20 °C.
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях.
С водой образует азеотропную смесь 87,9 % изопропилового спирта с температурой кипения 80,2 °C.
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице, при замерзании концентрированных растворов наблюдается переохлаждение[7]:
| Концентрация спирта, об % | Концентрация спирта, вес. % | Температура замерзания, °C |
|---|---|---|
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Видео по теме
Получение
Применяются два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена[8][9].
Основным способом получения изопропанола в российской промышленности является сернокислотная гидратация пропилена
- Ch4CH=Ch3+h3SO4⟶(Ch4)2CHOSO2OH+h3O⟶(Ch4)2CHOH{\displaystyle {\ce {Ch4CH=Ch3 + h3SO4 ->(Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH}}}.
Сырьем может служить, в том числе кроме пропилена, пропан-пропиленовая фракция с содержанием пропилена 30—90 % (фракция получаемая при пиролизе и крекинге нефти). Сейчас начинают чаще использовать чистый пропилен, так как в этом случае процесс можно вести при невысоких давлениях, при этом существенно снижается образование побочных продуктов реакции — полимеров и ацетона.
На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (Ch4)2CHOSO2OH{\displaystyle {\ce {(Ch4)2CHOSO2OH}}}, серной кислоты h3SO4{\displaystyle {\ce {h3SO4}}} и воды h3O{\displaystyle {\ce {h3O}}}. На второй стадии процесса — сернокислотный экстракт нагревается с водой и отгоняется образующийся изопропиловый спирт.
Прямую гидратацию пропилена осуществляют в основном в присутствии катализатора — (в скобках указаны условия процессов): ортофосфорной кислоты h4PO4{\displaystyle {{\ce {h4PO4}}}} на твёрдом неорганическом носителе при 240—260°С и 2,5—6,5 МПа) или на носителе из катионообменной смолы при 130—160°С и 8,0—10,0 МПа.
Изопропиловый спирт получают также окислением алканов воздухом, а также и другими способами[6].
Современный способ гидрирования ацетона водородом:
- Ch4COCh4+h3→katCh4CH(OH)Ch4{\displaystyle \mathrm {CH_{3}COCH_{3}+H_{2}{\xrightarrow {kat}}CH_{3}CH(OH)CH_{3}} }
Гидрирование ацетона впаровой фазе в присутствии твёрдого медно-никельхромитного катализатора[10][11].
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск)[12] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)[11][13].
Применение
Изопропиловый спирт используют для получения:
По причине особого государственного регулирования этанола, изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием.
Медицина
70 % изопропиловый спирт применяется вместо этилового спирта в качестве антисептика для пропитки медицинских салфеток.
Влияние на человека
- Ингаляционное
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест 0,6 мг/м³ (ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает[14].
Изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству изопропиловый спирт заменяет этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пламя, полностью разлагается на простые составляющие — воду и углекислый газ, которые не вызывают раздражений и иных побочных эффектов. При горении с достаточным избытком воздуха изопропанол не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости с площадью менее 20 см² в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций у людей[15].
- Пероральное
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко[2].
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола, если только не выпил единовременно от 500 мл.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов[2].
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием[14], наркотический эффект от приёма изопропанола почти в 2 раза превышает аналогичный эффект этанола[16]. Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов вызывает состояние глубокого наркоза и смерть[15].
При длительном воздействии больших концентраций паров в воздухе вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта человеку потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Длительное вдыхание воздуха с концентрацией, значительно превышающем ПДК, может вызвать потерю сознания. Тяжёлое отравление изопропиловым спиртом происходит редко.
Примечания
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0359.html
- ↑ 1 2 3 R. J. Slaughter, R. W. Mason, D. M. G. Beasley, J. A. Vale, L. J. Schep. Isopropanol poisoning // Clinical Toxicology (Philadelphia, Pa.). — 2014-06-01. — Т. 52, вып. 5. — С. 470–478. — ISSN 1556-9519. — DOI:10.3109/15563650.2014.914527.
- ↑ Papa, A. J. «Propanols» // Ullmann’s Encyclopedia of Industrial Chemistry : Weinheim: Wiley-VCH. — 2005.
- ↑ «Guide to Local Production: WHO-recommended Handrub Formulations» (англ.) // World Health Organization. — 2009. — Август.
- ↑ Otitis Externa (Swimmer’s Ear) (26 февраля 2010). Проверено 21 февраля 2016. Архивировано 26 февраля 2010 года.
- ↑ 1 2 ХиМиК.Ру — Изопропиловый спирт
- ↑ Ссылка один (англ.),Ссылка два
- ↑ «Isopropyl Alcohol, by John E. Logsdon and Richard A. Loke», Kirk‑Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc, Article Online Posting Date: December 4, 2000
- ↑ A. J. Papa (2005), «Propanols», Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_173
- ↑ СПОСОБ ПОЛУЧЕНИЯ ПРОПАНОЛА-2 — Патент РФ 2047590
- ↑ 1 2 ООО Синтез Ацетон (недоступная ссылка — история). Проверено 26 ноября 2011. Архивировано 21 марта 2012 года.
- ↑ О заводе | Завод синтетического спирта
- ↑ ПРОИЗВОДСТВО ИЗОПРОПИЛОВОГО СПИРТА В РОССИИ
- ↑ 1 2 ГОСТ 9805-84. Спирт изопропиловый. Технические условия[1]
- ↑ 1 2 Review of Inhalants: Euphoria to Dysfunction Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.,National Institute on Drug Abuse (недоступная ссылка — история). Проверено 10 августа 2011. Архивировано 15 октября 2011 года.
- ↑ «Достоинства и недостатки современных кожных антисептиков» С. В. Волкова, Е. В. Клементенок
wikipedia.green
Изопропиловый спирт — Gpedia, Your Encyclopedia
| Изопропанол | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Пропан-2-ол |
| Традиционные названия | Изопропиловый спирт |
| Хим. формула | C3H8O |
| Рац. формула | CH3CH(OH)CH3 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 60,09 г/моль |
| Плотность | 0,7851 г/см³ |
| Динамическая вязкость | 0,00243 Па·с |
| Энергия ионизации | 10,1 ± 0,1 эВ[1] |
| Термические свойства | |
| Т. плав. | -89,5 °C |
| Т. кип. | 82,4 °C |
| Т. всп. | 11,7 °C |
| Т. свспл. | 400 °C |
| Пр. взрв. | 2 ± 1 об.%[1] |
| Мол. теплоёмк. | 155,2 Дж/(моль·К) |
| Давление пара | 4,4 кПа при 20 °C |
| Химические свойства | |
| pKa | 16,5 |
| Растворимость в бензоле | хорошо растворим |
| Растворимость в ацетоне | растворим |
| Оптические свойства | |
| Показатель преломления | 1,3776 (nD, 20°C) |
| Структура | |
| Дипольный момент | 1,66 Д |
| Классификация | |
| Рег. номер CAS | 67-63-0 |
| PubChem | 3776 |
| Рег. номер EINECS | 200-661-7 |
| SMILES | |
| InChI | |
| RTECS | NT8050000 |
| ChEBI | 17824 и 43588 |
| Номер ООН | 1219 |
| ChemSpider | 3644 |
| Безопасность | |
| ЛД50 | 12800 мг/кг (кролик) |
| Токсичность | Класс опасности 3 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Изопропи́ловый спирт (пропано́л-2, втор-пропанол, изопропано́л, диметилкарбино́л, ИПС) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует изомер изопропанола — пропанол-1.
При нормальных условиях прозрачная, бесцветная жидкость с резким запахом и мягким горьким вкусом[2].
Изопропиловый спирт используется в качестве заменителя этилового спирта в косметике, парфюмерии, бытовой химии, жидкостей для автомобилей, медицинских целях, в средствах для очистки стёкол, оргтехники и как растворитель органических веществ промышленности.
В развитых странах изопропанол широко используется в товарах личной гигиены и в медицине, благодаря своей относительно низкой токсичности[3].
75 % водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь клеточные мембраны бактерий, таким образом обеспечивает более высокую эффективность и лучшее обеззараживание[4].
Изопропиловый спирт также используется в медицине в качестве вспомогательного компонента профилактического средства от наружного отита[5].
Эффективен при лечении дерматита протиранием пораженных участков кожи, с малым вредным влиянием на кожу.
Как и все летучие спирты, огнеопасен. Умеренно токсичен, требует осторожного обращения.
Свойства
Химические свойства
Рациональная химическая формула изопропилового спирта Ch4CH(OH)Ch4{\displaystyle {\ce {Ch4CH(OH)Ch4}}}.
Изопропанол обладает всеми свойствами вторичных спиртов жирного ряда, образует простые и сложные эфиры.
Гидроксильная группа может быть вытеснена галогенами.
С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол.
При дегидрировании превращается в ацетон[6].
Реагирует с сильными окислителями.
В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения.
Растворяет некоторые виды пластмасс и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резким, чем у этанола, по запаху их можно в некоторых случаях отличить.
Коэффициент преломления nD = 1,3776 при 20 °C. Динамическая вязкость при стандартных условиях 2,43 мПа·с — немного более вязкий, чем вода . Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К). Удельная теплота сгорания 34,1 МДж/кг.
Пар хорошо смешивается с воздухом, в диапазоне взрывоопасных концентраций образует взрывчатые смеси. Давление насыщенного пара при 20 °C — 4,4 кПа. Относительная плотность пара по воздуху — 2,1, относительная плотность смеси насыщенный пар/воздух — 1,05 при 20 °C.
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях.
С водой образует азеотропную смесь 87,9 % изопропилового спирта с температурой кипения 80,2 °C.
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице, при замерзании концентрированных растворов наблюдается переохлаждение[7]:
| Концентрация спирта, об % | Концентрация спирта, вес. % | Температура замерзания, °C |
|---|---|---|
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Получение
Применяются два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена[8][9].
Основным способом получения изопропанола в российской промышленности является сернокислотная гидратация пропилена
- Ch4CH=Ch3+h3SO4⟶(Ch4)2CHOSO2OH+h3O⟶(Ch4)2CHOH{\displaystyle {\ce {Ch4CH=Ch3 + h3SO4 ->(Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH}}}.
Сырьем может служить, в том числе кроме пропилена, пропан-пропиленовая фракция с содержанием пропилена 30—90 % (фракция получаемая при пиролизе и крекинге нефти). Сейчас начинают чаще использовать чистый пропилен, так как в этом случае процесс можно вести при невысоких давлениях, при этом существенно снижается образование побочных продуктов реакции — полимеров и ацетона.
На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (Ch4)2CHOSO2OH{\displaystyle {\ce {(Ch4)2CHOSO2OH}}}, серной кислоты h3SO4{\displaystyle {\ce {h3SO4}}} и воды h3O{\displaystyle {\ce {h3O}}}. На второй стадии процесса — сернокислотный экстракт нагревается с водой и отгоняется образующийся изопропиловый спирт.
Прямую гидратацию пропилена осуществляют в основном в присутствии катализатора — (в скобках указаны условия процессов): ортофосфорной кислоты h4PO4{\displaystyle {{\ce {h4PO4}}}} на твёрдом неорганическом носителе при 240—260°С и 2,5—6,5 МПа) или на носителе из катионообменной смолы при 130—160°С и 8,0—10,0 МПа.
Изопропиловый спирт получают также окислением алканов воздухом, а также и другими способами[6].
Современный способ гидрирования ацетона водородом:
- Ch4COCh4+h3→katCh4CH(OH)Ch4{\displaystyle \mathrm {CH_{3}COCH_{3}+H_{2}{\xrightarrow {kat}}CH_{3}CH(OH)CH_{3}} }
Гидрирование ацетона впаровой фазе в присутствии твёрдого медно-никельхромитного катализатора[10][11].
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск)[12] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)[11][13].
Применение
Изопропиловый спирт используют для получения:
По причине особого государственного регулирования этанола, изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием.
Медицина
70 % изопропиловый спирт применяется вместо этилового спирта в качестве антисептика для пропитки медицинских салфеток.
Влияние на человека
- Ингаляционное
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест 0,6 мг/м³ (ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает[14].
Изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству изопропиловый спирт заменяет этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пламя, полностью разлагается на простые составляющие — воду и углекислый газ, которые не вызывают раздражений и иных побочных эффектов. При горении с достаточным избытком воздуха изопропанол не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости с площадью менее 20 см² в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций у людей[15].
- Пероральное
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко[2].
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола, если только не выпил единовременно от 500 мл.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов[2].
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием[14], наркотический эффект от приёма изопропанола почти в 2 раза превышает аналогичный эффект этанола[16]. Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов вызывает состояние глубокого наркоза и смерть[15].
При длительном воздействии больших концентраций паров в воздухе вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта человеку потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Длительное вдыхание воздуха с концентрацией, значительно превышающем ПДК, может вызвать потерю сознания. Тяжёлое отравление изопропиловым спиртом происходит редко.
Примечания
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0359.html
- ↑ 1 2 3 R. J. Slaughter, R. W. Mason, D. M. G. Beasley, J. A. Vale, L. J. Schep. Isopropanol poisoning // Clinical Toxicology (Philadelphia, Pa.). — 2014-06-01. — Т. 52, вып. 5. — С. 470–478. — ISSN 1556-9519. — DOI:10.3109/15563650.2014.914527.
- ↑ Papa, A. J. «Propanols» // Ullmann’s Encyclopedia of Industrial Chemistry : Weinheim: Wiley-VCH. — 2005.
- ↑ «Guide to Local Production: WHO-recommended Handrub Formulations» (англ.) // World Health Organization. — 2009. — Август.
- ↑ Otitis Externa (Swimmer’s Ear) (26 февраля 2010). Проверено 21 февраля 2016. Архивировано 26 февраля 2010 года.
- ↑ 1 2 ХиМиК.Ру — Изопропиловый спирт
- ↑ Ссылка один (англ.),Ссылка два
- ↑ «Isopropyl Alcohol, by John E. Logsdon and Richard A. Loke», Kirk‑Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc, Article Online Posting Date: December 4, 2000
- ↑ A. J. Papa (2005), «Propanols», Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_173
- ↑ СПОСОБ ПОЛУЧЕНИЯ ПРОПАНОЛА-2 — Патент РФ 2047590
- ↑ 1 2 ООО Синтез Ацетон (недоступная ссылка — история). Проверено 26 ноября 2011. Архивировано 21 марта 2012 года.
- ↑ О заводе | Завод синтетического спирта
- ↑ ПРОИЗВОДСТВО ИЗОПРОПИЛОВОГО СПИРТА В РОССИИ
- ↑ 1 2 ГОСТ 9805-84. Спирт изопропиловый. Технические условия[1]
- ↑ 1 2 Review of Inhalants: Euphoria to Dysfunction Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.,National Institute on Drug Abuse (недоступная ссылка — история). Проверено 10 августа 2011. Архивировано 15 октября 2011 года.
- ↑ «Достоинства и недостатки современных кожных антисептиков» С. В. Волкова, Е. В. Клементенок
www.gpedia.com


