Изопропиловый спирт, его характеристики и применение
Изопропиловый спирт или изопропанол – вещество, широко востребованное во многих областях промышленности. Простая химическая формула, доступная цена и отличные свойства, значимые для различных сфер производства и областей человеческой деятельности – вот что отличает изопропиловый спирт.
В химическом отношении он представляет собой бесцветную жидкость с характерным запахом, это простейший вторичный спирт алифатического ряда, его формула — Ch4CH(OH)Ch4; температура плавления составляет 89,5С, температура кипения — 82,4С, плотность 0,7851 г/куб.см, нижний предел взрываемости в воздухе 2,5% по объёму (при 25С). Смешивается с водой и органическими растворителями во всех соотношениях и обладает всеми свойствами вторичных спиртов жирного ряда.
В промышленности изопропиловый спирт получают главным образом сернокислотной или прямой гидратацией пропилена. Сырьем служит пропан-пропиленовая фракция газов крекинга, а также пропиленовые фракции газов пиролиза нефти.
Изопропанол востребован в химической, нефтяной, медицинской, мебельной, пищевой, лесохимической, парфюмерной промышленности, поскольку является хорошим растворителем для многих эфирных масел, восков, эфиров, алкалоидов, синтетических смол.
В лакокрасочной промышленности этот спирт используется в качестве вспомогательного растворителя нитроцеллюлозы, ацетилцеллюлозы, этилцеллюлозы, он является одним из важнейших вспомогательных растворителей для нитролаков.
Изопропиловый спирт может применяться для денатурации этилового спирта, при приготовлении тормозной и стеклоомывающей жидкости, в качестве антифриза для автомобильных радиаторов.
Изопропиловый спирт применяется также для синтеза ацетона и пластмасс, в частности, производство полиэтилена низкого давления и полипропилена.
В нефтеперерабатывающей промышленности изопропанол применяется как растворитель карбамида, как экстрагент в процессе селективной экстракции нафтеновых кислот и в качестве добавки к маслам для повышения их качества в части антикоррозийных свойств и температуры застывания.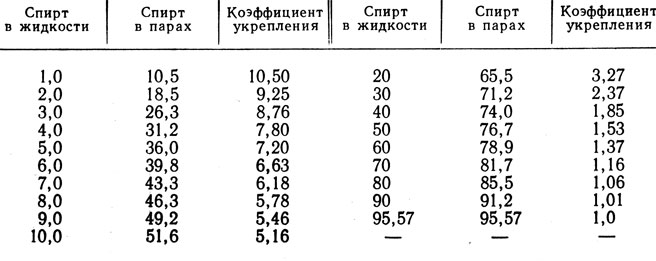
Если Вы заинтересованы в покупке изопропилового спирта, мы готовы предложить Вам купить нефтехимию высокого качества от ведущих российских производителей по привлекательным ценам. Фасовку и доставку мы также готовы взять на себя.
Изопропиловый спирт, азеотропная смесь — Справочник химика 21
Для получения безводного изопропилового спирта азеотропную смесь обезвоживают бензолом или диизопропиловым эфиром, реже — [c.57] Изопропиловый спирт (вторичный) ( Hg j HOH получают путем прямой или сернокислотной гидратации пропилена примерно по тем же схемам, что и этиловый спирт из этилена. Так как пропилен значительно легче, чем этилен, реагирует с серной кислотой, режим процесса в этом случае устанавливают более мягкий давление газа (при высоком содержании пропилена) 4—5 ат, температура 25—30°, концентрация серной кислоты 75—80%.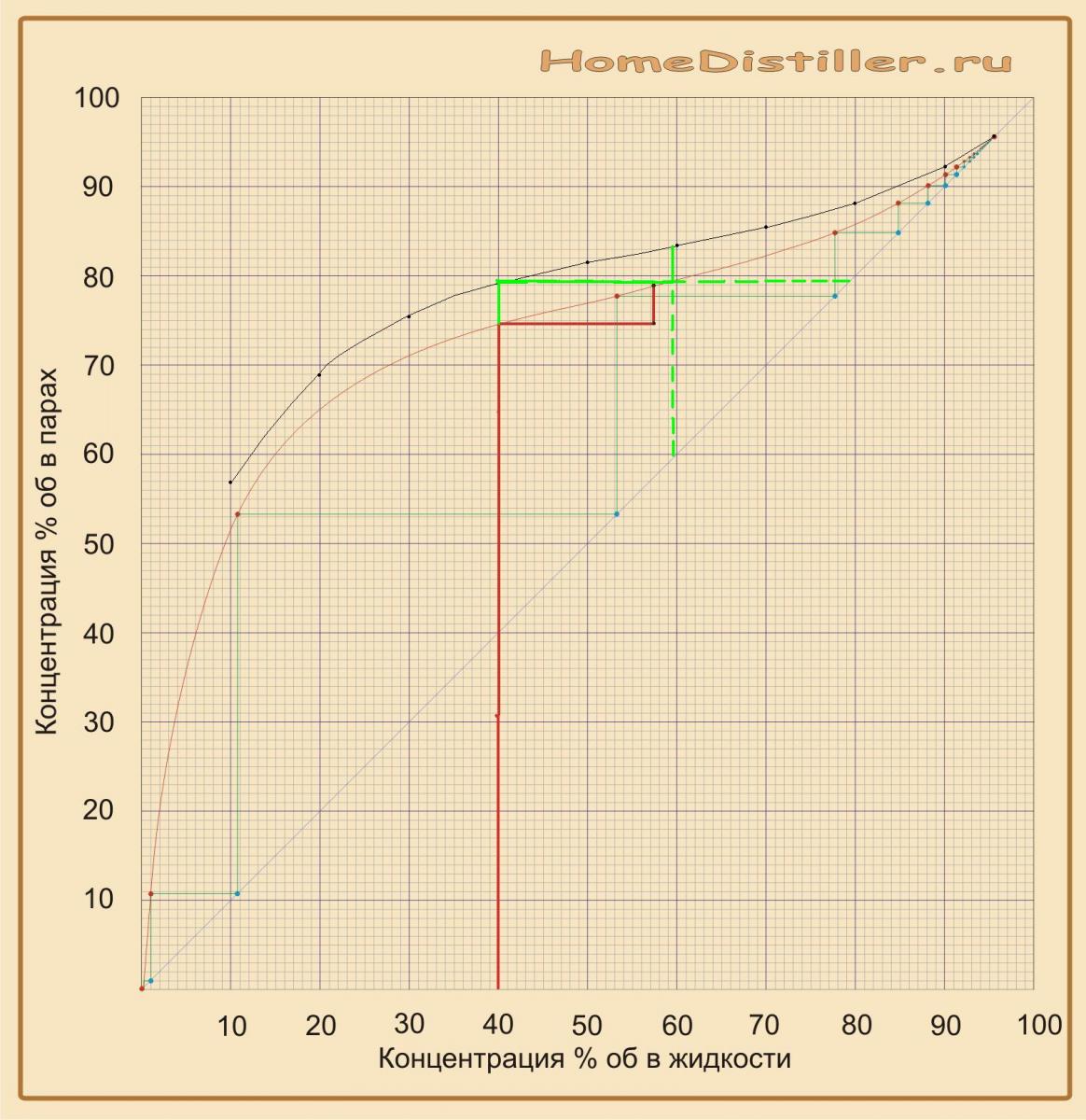
Водный раствор изопропилового спирта можно сконцентрировать встряхиванием с хлористым натрием верхний слой содержит около 87% пропанона-2 и 2 — 3% хлористого натрия. Перегонка дает 91%-нУю азеотропную смесь. (Относительно осущки [c.316]
Производство абсолютированного изопропилового спирта (ИПС). В результате простой дистилляции получают азеотропную смесь ИПС с водой (87,7% ИПС, 12,3% НаО т. кип. 80,3°С). Таким образом, в ИПС-сырце на 1 г спирта приходится 155 кг воды, в то время как в тройной смеси ИПС —бензол на 1 т спирта приходится 40 кг воды. Чтобы удалить из смеси всю воду, надо добавить 10т бензола на 1 т воды (или 660кг бензола на 1 т ИПС).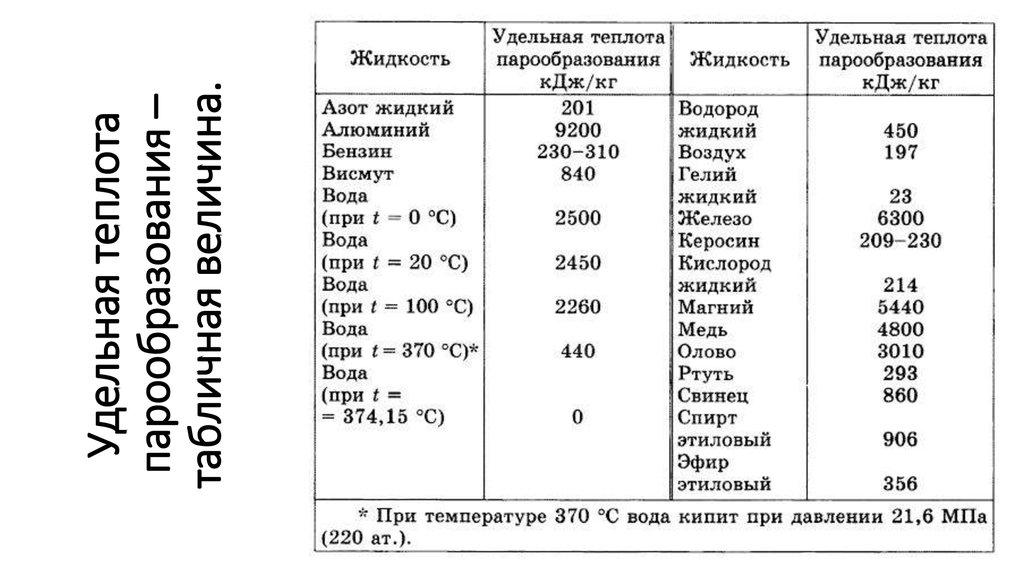 Абсолютирование спирта проводят в тарельчатой колонне с 68— 70 тарелками. Бензол подают на верхнюю тарелку, технический ИПС на 50—66-ю. [c.242]
Абсолютирование спирта проводят в тарельчатой колонне с 68— 70 тарелками. Бензол подают на верхнюю тарелку, технический ИПС на 50—66-ю. [c.242]
Этиловый спирт-ректификат содержит 4—5% воды. В последнее время в качестве заменителя этилового спирта применяют весьма доступный изопропиловый спирт, который по температуре кипения (82,4°) и растворяющей способности довольно близок к этиловому спирту. Надо, однако, помнить, что изопропиловый спирт образует с водой азеотропную смесь (12,1 % воды), кипящую при почти той же температуре (80,4°), что и безводный изопропиловый спирт. Различать водный и безводный изопропиловый спирт
После ректификации образующегося разбавленного спиртового раствора получают 88%-ный изопропиловый спирт (азеотропная смесь, кипящая при 80,4 °С). Технологическая схема синтеза изопропилового спирта из пропилена примерно такая же, что и этилового спирта из этилена. [c.214]
Опыт проводят в приборе, изображенном на рис. 7. Газообразный хлористый водород [5] пропускают через предохранительную ловушку и реометр (не обязательно) в литровую колбу Клайзена, содержащую 125 мл 6,5 н. раствора соляной кислоты и 5 г двуокиси германия . Смесь нагревают до слабого кипения. Хлорид германия (4) и азеотропная соляная кислота поступают в охлаждаемый водой холодильник, над которым расположена колонка, наполненная стеклянными бусами (для устранения разбрызгивания капель). Смесь газообразного хлористого водорода и паров хлорида германия (4) проходит через сушильную колонку, наполненную слоями безводного хлористого кальция (8 меш), и стеклянной ваты, и собирается в приемнике, охлаждаемом до —78° смесью порошкообразного сухого льда и изопропилового спирта. Хлорид германия застывает (температура замерзания —49,5°) на стенках приемника, а хлористый водород (температура кипения —85°) через центральную трубку уходит в атмосферу (вытяжной шкаф ) после про- [c.108]
7. Газообразный хлористый водород [5] пропускают через предохранительную ловушку и реометр (не обязательно) в литровую колбу Клайзена, содержащую 125 мл 6,5 н. раствора соляной кислоты и 5 г двуокиси германия . Смесь нагревают до слабого кипения. Хлорид германия (4) и азеотропная соляная кислота поступают в охлаждаемый водой холодильник, над которым расположена колонка, наполненная стеклянными бусами (для устранения разбрызгивания капель). Смесь газообразного хлористого водорода и паров хлорида германия (4) проходит через сушильную колонку, наполненную слоями безводного хлористого кальция (8 меш), и стеклянной ваты, и собирается в приемнике, охлаждаемом до —78° смесью порошкообразного сухого льда и изопропилового спирта. Хлорид германия застывает (температура замерзания —49,5°) на стенках приемника, а хлористый водород (температура кипения —85°) через центральную трубку уходит в атмосферу (вытяжной шкаф ) после про- [c.108]
Изопропиловый спирт СПз—СНОН—СНз — жидкость (т.
 кип. 32,5 °С), смешивающаяся с водой. Его пары дают с воздухом взрывоопасные смеси в пределах концентраций 2—12% (об.). Образует е водой азеотропную смесь, содержащую 88% спирта и кипящую при 80,3 °С. Изопропиловый спирт нашел применение в качестве растворителя, заменяющего во многих случаях этиловый спирт. Кроме того, из него получают сложные эфиры, ацетон и т. д. Изопропиловый спирт получают исключительно синтетическим путем, а именно гидратацией пропилена.
кип. 32,5 °С), смешивающаяся с водой. Его пары дают с воздухом взрывоопасные смеси в пределах концентраций 2—12% (об.). Образует е водой азеотропную смесь, содержащую 88% спирта и кипящую при 80,3 °С. Изопропиловый спирт нашел применение в качестве растворителя, заменяющего во многих случаях этиловый спирт. Кроме того, из него получают сложные эфиры, ацетон и т. д. Изопропиловый спирт получают исключительно синтетическим путем, а именно гидратацией пропилена. Смесь паров, выходящую из гидролизера, конденсируют. Конденсат состоит из воды и изопропилового спирта и содержит около 5% диизопропилового эфира (считая на спирт). Эфир отделяется и экстрагируется водой для извлечения изопропилового спирта. Концентрирование и очистка изопропилового спирта достигаются прямой перегонкой с последующей азеотропной дистилляцией с бензолом для получения безводного продукта. [c.401]
В Германии существовал только один завод (в Мерзе), где осуществлялась гидратация пропилена и н-бутиленов.
С. Смешивается с водой, эфиром и бензолом. Образует с водой азеотропную смесь, кипящую при 80,4 °С, содержащую 87,9 % изопропилового спирта. Легко воспламеняется. Образует с воздухом взрывоопасные смеси, нижний предел 2,8 % [c.246]
Образует с водой азеотропную смесь, кипящую при 80,4 °С, содержащую 87,9 % изопропилового спирта. Легко воспламеняется. Образует с воздухом взрывоопасные смеси, нижний предел 2,8 % [c.246]
С фурфуролом смешиваются ацетон, бензол, нормальный и изопропиловый спирты, хлороформ, этиленгликоль, уксусная, масляная, муравьиная, молочная, олеиновая, пропионовая и нафтеновые кислоты, а также другие органические соединения, в том числе высокомолекулярные. Фурфурол и вода при нормальных температурах обладают ограниченной растворимостью. Критическая температура растворимости фурфурола в воде отвечает температуре 121°С и концентрации фурфурола в растворе 50,3% (масс,). Фурфурол с водой образует азеотронную смесь. Содержание фурфурола в азеотропной смеси 35% (масс.), температура кипения смеси 97,45°С. [c.26]
Имеет т. кип. 82,4°, с водой образует азеотропную смесь с т. кип. 80°, содержащую 87,4% изопропилового спирта. С водой смешивается во всех отношениях. При большом содержании воды изопропиловый спирт предварительно подсушивают углекислым натрием или поташом и окончательно абсолютируют его хлористым кальцием [62]. При небольшом содержании воды хорошим осушителем является окись кальция, которая снижает содержание воды до 0,1% для окончательного обезвоживания рекомендуется перегонка над безводным сульфатом меди [3]. Кроме того, для сушки изопропилового спирта можно использовать все методы, указанные выше для этилового спирта. [c.610]
При большом содержании воды изопропиловый спирт предварительно подсушивают углекислым натрием или поташом и окончательно абсолютируют его хлористым кальцием [62]. При небольшом содержании воды хорошим осушителем является окись кальция, которая снижает содержание воды до 0,1% для окончательного обезвоживания рекомендуется перегонка над безводным сульфатом меди [3]. Кроме того, для сушки изопропилового спирта можно использовать все методы, указанные выше для этилового спирта. [c.610]
Выделение ацетона из газа, выходящего из реактора дегидрирования, чрезвычайно просто. Выходящий поток охлаждается водой и конденсируется. Остаточный газ промывается в водяном скруббере. Смесь конденсата и промывной жидкости подвергается обычному фракционированию и азеотропной перегонке для получения технического ацетона и безводного изопропилового спирта.
Азеотропная смесь изопропилового спирта с водой кинит нри 80,4° и содержит 91% спирта. Во многих случаях эта азеотропная смесь может подвергаться дальнейшей переработке.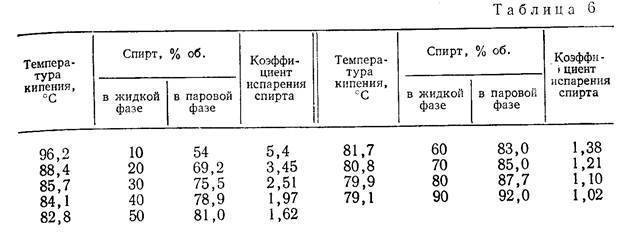 [c.204]
[c.204]
Дистиллят из ректификационной колонны /, представляющий собой азеотропную смесь изопропилового спирта и воды, при конденсации образует два жидких слоя. Органический слой используют в качестве флегмы, а водный слой вместе с рафинатом (после экстракции) подают в ректификационную колонну 3. [c.673]
Этиловый спирт-ректификат содержит 4—5% воды. Безводный этанол имеет темп. кип. 78,3° С, =0,7936. Нередко в качестве заменителя этилового спирта применяют весьма доступный изопропиловый спирт, который по температуре кипения (82,4°) и растворяющей способности довольно близок к этиловому спирту. Надо, однако, помнить, что изопропиловый спирт образует с водой азеотропную смесь (12,1% воды), кипящую при почти той же температуре (80,4° С), что и безводный изопропиловый спирт. Различать водный и безводный изопропиловый спирт проще всего по плотности (плотность безводного спирта 1 = =0,789, плотность водного «=0,821). [c.56]
На серебряных катализаторах вполне удовлетворительно протекает окислительное дегидрирование и других первичных спиртов в альдегиды, в том числе дегидрирование этилового спирта в ацетальдегид [92].
 Путем окислительного дегидрирования изопропилового спирта получают ацетон [93], а из вгор-бутилового спирта метилэтилкетон [94]. Этот метод до сего времени остается основным в производстве метилэтилкетона. Процесс обычно проводят на серебряных катализаторах при 530—560 °С и объемной скорости по сырью (азеотропная смесь спирта с водой) 8—12 ч в аппаратах адиабатического типа с закалочным холодильником продуктов реакции. При этом степень конверсии спирта составляет 79—81%, а селективность по метилэтилкетону 90—92%. [c.55]
Путем окислительного дегидрирования изопропилового спирта получают ацетон [93], а из вгор-бутилового спирта метилэтилкетон [94]. Этот метод до сего времени остается основным в производстве метилэтилкетона. Процесс обычно проводят на серебряных катализаторах при 530—560 °С и объемной скорости по сырью (азеотропная смесь спирта с водой) 8—12 ч в аппаратах адиабатического типа с закалочным холодильником продуктов реакции. При этом степень конверсии спирта составляет 79—81%, а селективность по метилэтилкетону 90—92%. [c.55]После азеотропной перегонки с изопропиловым спиртом и последующей ректификации получают смесь безводных кислот i—Сз, направляемую на разделение. [c.169]
Процесс протекает в жидкой и в паровой фазе в качестве инициатора применяют перекись водорода или какую-нибудь другую перекись, дающую щелочную реакцию. Жидкофазное окисление нужно вести так, чтобы между количествами абсорбированного кислорода и полученной перекисью водорода поддерживалось равновесие. Процесс идет непрерывно его осуществляют при температурах 100—105° С и давлении 2—3 ат, несколько большем, чем необходимо для поддержания изопропилового спирта в жидком состоянии. В этих условиях получается перекись водорода концентрацией 15—25% вес. В качестве стабилизатора перекиси водорода применяется метастанат натрия или ацетанилид. В качестве сырья применяется технический изопропиловый спирт (азеотропная смесь, содержащая 88% спирта и 12% воды) и кислород концентрацией не менее 95%. [c.450]
Процесс идет непрерывно его осуществляют при температурах 100—105° С и давлении 2—3 ат, несколько большем, чем необходимо для поддержания изопропилового спирта в жидком состоянии. В этих условиях получается перекись водорода концентрацией 15—25% вес. В качестве стабилизатора перекиси водорода применяется метастанат натрия или ацетанилид. В качестве сырья применяется технический изопропиловый спирт (азеотропная смесь, содержащая 88% спирта и 12% воды) и кислород концентрацией не менее 95%. [c.450]
Как и при получении этилового спирта, кислый раствор, содержащий изопропилсерную кислоту, необходимо разбавить водой и затем нагреть, чтобы осуществить гидролиз. Раствор разбавляют до концентрации серной кислоты не свыше 50% (обычно до 35—40%). При фракционированной разгонке водного изопропилового спирта отгоняется азеотропная смесь, кипящая при 80,35° (температура кипения чистого изопропанола 82,4°) и содержащая 87,7% изопропилового спирта и 12,3% воды. Чтобы получить безводный изопропиловый спирт, эту азеотропную смесь перегоняют с толуолом, дихлорэтаном или ксилолом, образующими с водой и изопропанолом тройные азеотропные смеси. [c.149]
[c.149]
Из куба ректификационной колонны вытекает снирто-водная смесь, которую разгоняют на колонне с 50-ю тарелками нри флегмовом числе 2—3, получая чистый 91 %-ный изопропиловый спирт (азеотропная смесь с водо11). Выход изопропилового спирта составляет 85—90% от теории (считая на израсходованный пропилен). Чтобы дать представление о расходе энергии в этом процессе, следует указать, что при получении 10 л чистого (91%-пого) изопропилового спирта нужно затратить около 17,5 кг пара для отгонки спирта от кислоты и около 22 кг пара для обоих последующих разгонок. В абсорбционной колонне необходимо отводить на каждые 10 л 91%-ного изопропилового спирта приблизительно 38 ккалЫас. Количество 91 %-ной серной кислоты, необходимое для получения 10 л изопропилового спирта, достигает 11,8 кг. Потери серной кислоты в процессе принимают равными 12-15%. [c.464]
Изопропиловый спирт был первым спиртом, который получили гидратацией олефина. Его производят трех степеней чистоты спирт-сырец, применяющийся для денатурирования этилового спирта, 91 %-ный изопропиловый спирт (азеотропная смесь с водой) и 100%-ный абсолютный изопронанол. Обезвоживание изопрэпилового спирта легко осуществляется перегонкой над твердым едким натром. Абсолютный спирт кипит при 82,4°. Ниже приведены важнейшие физические свойства изопропилового спирта. [c.470]
Обезвоживание изопрэпилового спирта легко осуществляется перегонкой над твердым едким натром. Абсолютный спирт кипит при 82,4°. Ниже приведены важнейшие физические свойства изопропилового спирта. [c.470]
И одфенилметилкарбинол. В круглодонную колбу емкостью 5 л, снабженную ректификационной колонкой высотой 1 м с насадкой из спиралей, помещают 235 г (0,96 моля) 4-иодацетофенона и 2900 мл сухого изопропилового спирта, в котором растворено 40 г (1,48 г-атома) алюминия. Смесь нагревают так, чтобы при этом происходила медленная перегонка. Через несколько часов, когда дистиллят уже не будет давать положительной пробы на ацетон с 2,4-динитрофенилгидразином, отгоняют избыток изопропилового спирта. После охлаждения остаток разлагают добавлением 350 мл концентрированной соляной кислоты и 1000 г льда. На другой день смесь экстрагируют бензолом, бензольный раствор сушат азеотропной перегонкой и отгоняют бензол. Затем, применяя колонку Вигре высотой 15 см, остаток перегоняют в вакууме при 2 мм.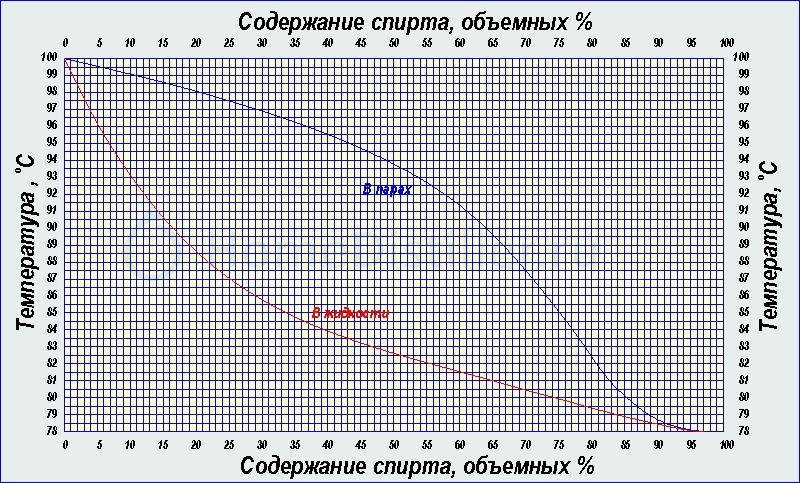 После отгонки первой низкокипящей фракции перегонку продолжают без [c.32]
После отгонки первой низкокипящей фракции перегонку продолжают без [c.32]
Фрежакё [651] получал безводный изопропиловый спирт, насыщая водную смесь аммиаком и двуокисью углерода. При этом образовывались два слоя. Слой, содержащий большее количество воды, перегоняли, получая аммиак, двуокись углерода и азеотропную смесь. Слой с меньшим содержанием воды также подвергали фракционированной перегонке, в результате чего получали азеотроп и безводный спирт. [c.316]
Получаемый водный раствор серной кислоты и изопропилового спирта отстаивают от всплывающих полимеров, а затем подвергают ректификации. При перегонке с перегретым паром в колонне, орошаемой азеотропной смесью спирта и воды отгоняются спирт и вода. Полученный водный раствор спирта подвергают перегонке в присутствии бензола или толуола, образующих с водой азеотрапную смесь, кипящую при более низкой температуре, чем смесь спирта и воды остаток ректификации — безводный изопропиловый спирт — служит для получения ацетона- Отгоняемые пары азеотропной смеси воды и бензола подвергают конденсации конденсат расслаивается на воду, содержащую спирт, отделяемый от воды, и на бензол, используемый повторно в качестве компонента при азеотропной перегонке. [c.203]
[c.203]
Первым синтетическим спиртом, полученным сернокислотной гидратацией пропилена, был изопропиловый спирт. Процесс абсорбции пропилена серной кислотой может быть осуществлен в двух вариантах либо 92%-ной кислотой без давления при 20 °С, либо 80%-ной кислотой при 60 °С под давлением 25 ат. При работе по второму методу в абсорбере одновременно идег и гидролиз изопропилсульфата. Из реакционной смеси во второй колонне отгоняют изопропиловый спирт и диизопропиловый эфир, а серную кислоту возвращают в абсорбер. Регенерация серной кислоты не требуется. Изопропиловый спирт образует с водой азеотропную смесь, содержащую 12,3 вес. % воды и кипящую при 80,4 °С (чистый изопропиловый спирт кипит при 82,4°С). При поступлении реакционной смеси из абсорбера в колонну к ней добавляют такое количество воды, чтобы концентрация серной кислоты была 60%. При отгонке азеотропной смеси изопропиловый спирт — вода концентрация серной кислоты увеличивается до 70%. [c.215]
Joung нашел, что температура кипения азеотропной смеси изопропилового спирта с водой равна 80,37°. В этой смеси содержится 87,90% (весовых) изопропилового- спирта. Смеои, содержащие спирта больше, чем азеотропная iwe b, при кипении образуют пар, более богатый спиртом, чем жидкость. Омеси с низшими концентрациями спирта образуют при кипении пар, более бедный, чем жидкость состав пара имеет тенденцию приближаться к составу постоянно-кипящей смеси. Lebo исследовал температуры кипения различных смесей изопропилового спирта с водой и нашел, что азеотропная смесь имеет темп. кип. 80,4 , содержит 87,7% (весовых) спирта (или 91,1% по объему) и обладает удельным весом — 0,8158. [c.392]
В этой смеси содержится 87,90% (весовых) изопропилового- спирта. Смеои, содержащие спирта больше, чем азеотропная iwe b, при кипении образуют пар, более богатый спиртом, чем жидкость. Омеси с низшими концентрациями спирта образуют при кипении пар, более бедный, чем жидкость состав пара имеет тенденцию приближаться к составу постоянно-кипящей смеси. Lebo исследовал температуры кипения различных смесей изопропилового спирта с водой и нашел, что азеотропная смесь имеет темп. кип. 80,4 , содержит 87,7% (весовых) спирта (или 91,1% по объему) и обладает удельным весом — 0,8158. [c.392]
Схема установки для обезвоживания смеси изопропилового и этилового спиртов приведена на рис. У1-46. Азеотропная смесь изопропиловый спирт — этиловый спирт —вода, аолучаемая в результате ректификации и содержащая воду в количестве >0,5%, поступает в диффузионную камеру. Обогащенный водой поток направляется в исходную систему, обезвоженная смесь (содержание воды собой готовый продукт. Устройство аппарата, предназначенного для разделения легких углеводородов (материал пленки—полиэтилен), показано на рис. 1-47. [c.512]
Азеотропная смесь, образуемая 1,1-дихлорпропаном с изопропиловым спиртом, кипит при 30 °С и содержит 71% (моль) 1,1-дихлорпропана. [c.226]
температура кипения, описание вещества, использование
Изопропиловый спирт (пропанол-2, изопропанол, i-propanol, isopropyl alcohol) – химическое соединение, получившее широкое распространение благодаря растворяющей способности, дезинфицирующим и консервирующим свойствам. Этот спирт используют во многих видах промышленности, а также автомобилисты и медики.
Изопропиловый спирт – что это такое?
Изопропиловый спирт – вторичный одноатомный спирт. Химическая формула изопропанола СН3 – СН (ОН) – СН3. Изопропанол можно рассматривать как производное насыщенного углеводорода пропана СН3 – СН2 – СН3, в молекуле которого один атом водорода замещен на спиртовую — гидроксильную группу (-ОН).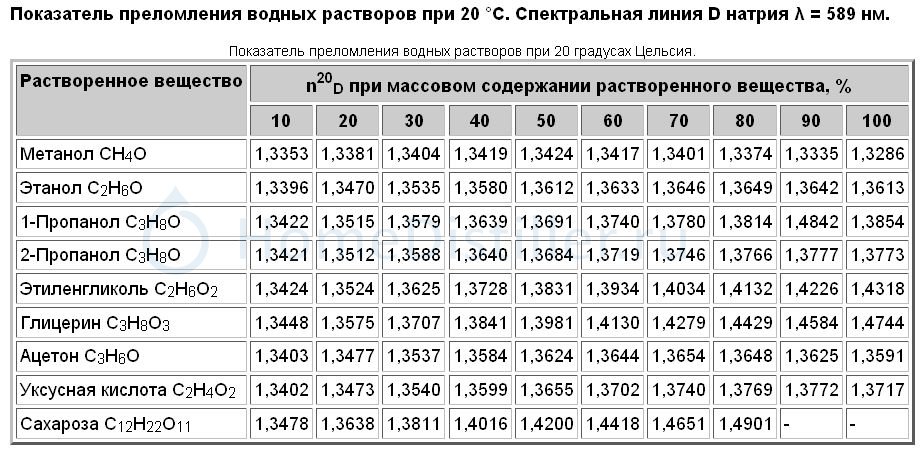 Поскольку гидроксильная группа в молекуле одна, то спирт называют одноатомным. Как видно из химической формулы изопропилового спирта, углерод, связанный с гидроксильной группой, соединен с двумя группами СН3. Поэтому спирт называют вторичным.
Поскольку гидроксильная группа в молекуле одна, то спирт называют одноатомным. Как видно из химической формулы изопропилового спирта, углерод, связанный с гидроксильной группой, соединен с двумя группами СН3. Поэтому спирт называют вторичным.
Структурная формула изопропилового спирта, а также формулы некоторых других одноатомных спиртов приведены на рисунке.
Физические свойства
Многие свойства изопропанола, температура кипения например, обусловлены наличием спиртовой группы (-ОН). Эта группа обладает высокой полярностью. В результате чего группа –ОН одной молекулы изопропанола образует связь с группой –ОН другой молекулы изопропанола. Таким образом, молекулы ассоциируются, то есть соединяются между собой. Такую связь называют водородной. Она слабая, но имеет большое значение в природе.
Благодаря водородным связям вода H2O при обычных условиях — жидкость, а не газ, как, например, похожее по строению вещество H2S сероводород. Именно наличие водородных связей приводит к тому, что твердая фаза воды – лед — имеет меньшую плотность в природе, чем жидкая фаза, в результате чего лед не тонет.
Именно наличие водородных связей приводит к тому, что твердая фаза воды – лед — имеет меньшую плотность в природе, чем жидкая фаза, в результате чего лед не тонет.
Образование водородных связей объясняет высокую температуру кипения изопропилового спирта и других низкомолекулярных спиртов в сравнении с соединениями схожего строения. Например, температура кипения пропана -42 °С, то есть пропан при любых температурах выше -42°С находится в газообразном состоянии. Температура кипения изопропилового спирта намного выше и составляет 82,4 °С. Это означает, что изопропанол при обычной температуре находится в жидком состоянии.
Если сравнить температуру кипения изопропилового спирта и метилового, то у первого она несколько выше: 82 градуса против 65. Это означает, что при обычных условиях изопропиловый спирт меньше испаряется, чем метиловый.
Температура плавления и температура кипения изопропилового спирта и некоторых других соединений представлены в таблице.
| Вещество | Температура кипения, оС | Температура плавления, оС |
| Метанол | 65 | -98 |
| Этанол | 78 | -117 |
| Пропанол | 97 | -127 |
| Изопропанол | 82 | -88 |
| Пропан | -42 | -190 |
Образование водородных связей между спиртовыми группами изопропанола и молекулами воды обуславливает растворимость этого спирта в воде.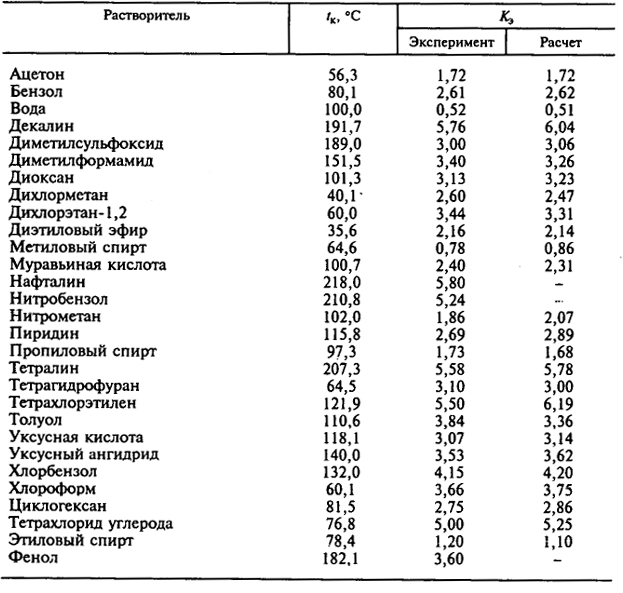 Растворимость зависит от количества углеродных атомов в цепи, чем их меньше, тем лучше растворяется спирт. Поэтому среди спиртов наибольшей растворимостью в воде обладает метанол, который можно смешать с водой в любом соотношении. Этанол растворяется в воде чуть хуже метанола, а изопропанол — хуже этанола.
Растворимость зависит от количества углеродных атомов в цепи, чем их меньше, тем лучше растворяется спирт. Поэтому среди спиртов наибольшей растворимостью в воде обладает метанол, который можно смешать с водой в любом соотношении. Этанол растворяется в воде чуть хуже метанола, а изопропанол — хуже этанола.
Основные характеристики изопропилового спирта
Растворяется в ацетоне, в бензоле хорошо растворяется, смешивается с водой, эфиром, этанолом.
Плотность 0,7851 г/см3 (20 °С).
Нижний предел взрываемости — 2,5% (по объему).
Температура плавления -89,5 °С.
Температура кипения +82,4°С.
Зависимость температуры кипения изопропилового спирта от давления представлена в таблице.
| Давление паров, мм рт.ст. | Температура кипения, оС |
| 1 | -26,1 |
| 10 | 2,4 |
| 40 | 23,8 |
| 100 | 39,5 |
| 400 | 67,8 |
| 1020,7 | 90 |
Химические свойства
Изопропиловый спирт представляет собой бесцветную жидкость. Обладает характерным запахом, не похожим на запах этилового спирта. Не проводит электрический ток.
Обладает характерным запахом, не похожим на запах этилового спирта. Не проводит электрический ток.
Вступает в многочисленные химические реакции, что используется для промышленных синтезов. Большая часть произведенного изопропилового спирта идет на производство ацетона. Для получения ацетона изопропанол необходимо окислить сильным окислителем – смесью K2Cr2O7 + H2SO4 или KMnO4 + H2SO4.
Получение
В России в 2017 году произведено около 40 тыс. тонн изопропилового спирта, почти на 20% меньше, чем в 2016 году. Объем производства достаточно мал — за этот же период метанола произведено почти 4 млн тонн.
Производят изопропиловый спирт в России два предприятия: ЗАО «Завод синтетического спирта» в городе Орске Оренбургской области и ООО «Синтез Ацетон» в городе Дзержинске Нижегородской области.
В Орске производят изопропанол методом сернокислотной гидратации пропилена или пропан-пропиленовой фракции, полученной из газов термического или каталитического крекинга.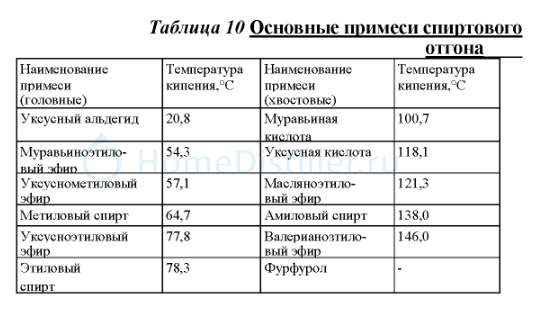 Получают два вида изопропанола, отличающихся степенью очистки: технический (87%) и абсолютизированный (99,95%). В Дзержинске изопропанол получают гидрированием ацетона.
Получают два вида изопропанола, отличающихся степенью очистки: технический (87%) и абсолютизированный (99,95%). В Дзержинске изопропанол получают гидрированием ацетона.
Побочным продуктом при получении изопропилового спирта гидратацией пропилена является диизопропиловый спирт, который представляет особую ценность как вещество, имеющее высокое октановое число, равное 98.
Применение
Изопропиловый спирт – отличный растворитель, поэтому имеет широкую сферу применения. Его используют в основном в химической промышленности, а также в нефтеперерабатывающей, лесохимической, мебельной, медицинской, пищевой, парфюмерной отраслях промышленности, в полиграфии, домашнем хозяйстве. Направления применения:
- растворитель,
- консервант,
- обезвоживающее средство,
- экстрагент примесей,
- стабилизатор,
- антиобледенитель.
Применение изопропанола в химической и автомобильной промышленности
Применение в химической промышленности следующее:
- сырье для производства ацетона,
- производство пластмасс – полиэтилена низкого давления и полипропилена,
- синтез изопропилацетата,
- производство инсектицидов,
- растворитель при производстве этилцеллюлозы, ацетилцеллюлозы, нитроцеллюлозы в лакокрасочной промышленности,
- безопасная транспортировка нитроцеллюлозы (в нее добавляют 30% изопропанола),
- экстрагент в тонкой химической технологии.
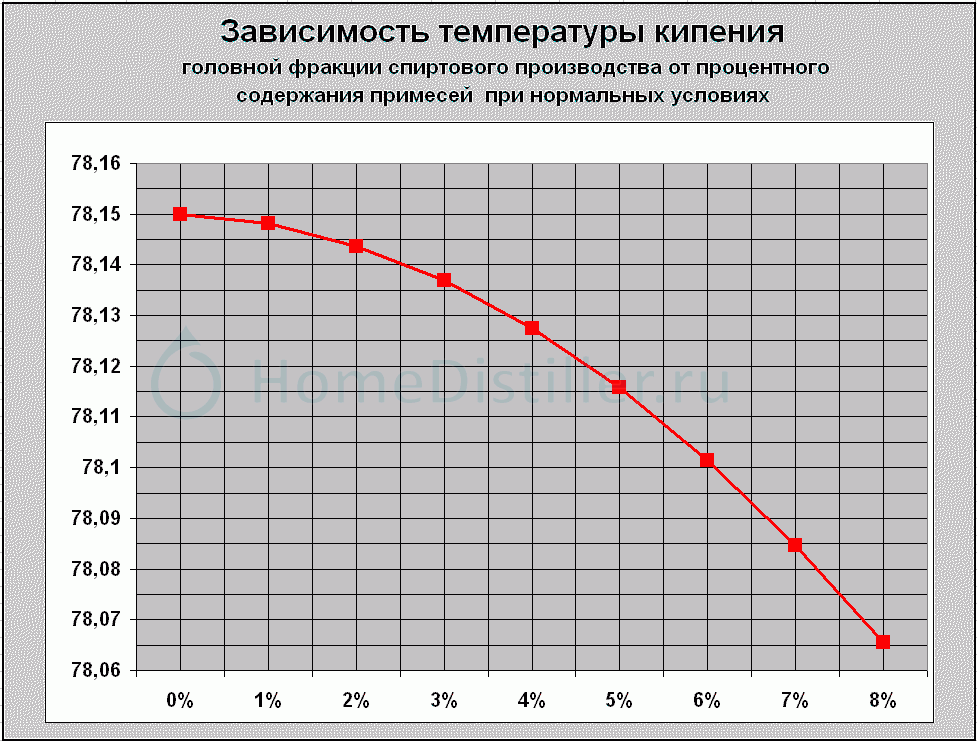
- применение в нефтеперерабатывающей промышленности:
- растворитель карбамида, применяемого для депарафинизации дизельного топлива,
- добавка к маслам, усиливающая их антикоррозионные свойства и понижающая температуру застывания,
- «удаление» воды из бензиновых баков.
Вода попадает в топливные магистрали и баки нефтебаз путем конденсации из влажного воздуха. При низких температурах она замерзает и может образовать ледяную пробку. При добавлении абсолютированного изопропанола вода в нем растворяется и не замерзает.
В автомобильной промышленности:
- «удаление» воды из бензобаков путем ее растворения,
- как компонент топлива для повышения октанового числа и уменьшения токсичных выбросов,
- антиобледенитель ветрового стекла,
- антифриз для радиаторов,
- удаление тормозной жидкости с гидравлических тормозных систем.
Применение изопропанола в других видах хозяйственной деятельности
Применение в мебельной и лесохимической промышленности:
- экстракция смол из древесины в смеси с другими растворителями,
- снятие старого лакового покрытия, растворитель французской полировки, клеев, масел,
- связующее вещество в полиролях и очистителях.

В полиграфии изопропанол применяют для увлажнения в печатных процессах. В электронике — в качестве растворителя для очистки контактных разъемов, магнитных лент, головок дисков, лазерных линз, для удаления термопасты, очистки клавиатуры, ЖК-мониторов, стеклянных экранов. Нельзя применять его только для очистки винила, так как изопропанол вступает с ним в реакцию.
Применение в медицинской промышленности и медицине:
- входит в состав антисептических растворов, пропитывающих жидкостей для салфеток,
- обеззараживающее средство для протирания места инъекции,
- 75% водный раствор используют как дезинфицирующее средство для рук,
- дезинфицирующие тампоны,
- осушитель для профилактики отита,
- консервирующее средство для сохранения генетического материала и анализов (менее токсичен, чем формальдегид).
Изопропанол имеет преимущества перед этанолом: более выраженное антисептическое действие и низкую цену. Поэтому в тех случаях, когда раньше применяли этанол, сейчас используют изопропанол.
В косметической и парфюмерной промышленностях изопропанол применяют в производстве:
- косметических средств,
- средств личной гигиены,
- духов, одеколонов, лаков.
В пищевой промышленности изопропанол используют при производстве замороженных продуктов в качестве хладоносителя.
В домашнем хозяйстве:
- для очищения различных поверхностей, кроме резиновых и виниловых,
- для удаления пятен с тканей, древесины,
- для удаления клея от наклеек (на бумажные изопропанол не действует).
Токсичность
Изопропанол применяется в медицине в качестве местного антисептика. При местном использовании быстро испаряется и не оказывает негативного влияния.
При вдыхании паров раздражает дыхательные пути, может вызвать головную боль. Высокая концентрация изопропанола в воздухе тормозит работу ЦНС, приводит к потере сознания. Поэтому работать с изопропанолом можно только в хорошо проветриваемом помещении.
Внутрь изопропанол не применяется, поскольку он токсичен. Попадая в печень, превращается в ядовитое вещество — ацетон, поражающий печень, почки и головной мозг. 200 мл изопропанола являются смертельной дозой.
Попадая в печень, превращается в ядовитое вещество — ацетон, поражающий печень, почки и головной мозг. 200 мл изопропанола являются смертельной дозой.
перегонка, процесс очистки в самогоноварении
Давно люди заметили, что жидкости начинают испаряться с разными температурами. Спустя время, этим свойством научились пользоваться. Для чего используют это знание? Как применяется техника? Какова температура кипения чистого спирта? На эти вопросы ответит статья.
Самогоноварение когда-то было промыслом, но сейчас это увлечение не больше, чем хобби. Причём, мастера своего хобби поднимаются до невообразимых уровней. Как же это получается и с какой стороны подступиться к этому не самому простому увлечению?
При правильном самогоноварении
Немного теории
Спирт, имеет отличную от воды плотность, а, следовательно, и температура его испарения будет иной. Используют это познание шире всего при перегонке браги.
Сбродивший компот или варенье перегоняют, получая на выходе самогон.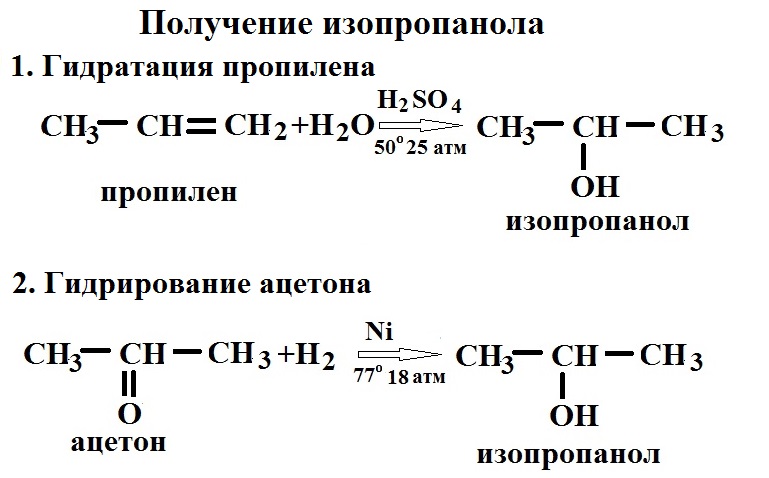 Это не магия превращения воды в вино, это обычное физическое явление.
Это не магия превращения воды в вино, это обычное физическое явление.
При нагревании браги в первую очередь начинают испаряться наиболее летучие спирты, которые и являются самыми ядовитыми для организма.
Следующим испаряется спирт этиловый, а за ним – тяжёлые спирты, употребление которых тоже нередко доводит до летального исхода с малых доз.
До того как начать заниматься перегоном, необходимо знать:
- Температуры кипения спиртов. Для каждой фракции свой градус.
- Чем чище получается конечный продукт, тем более качественно выполнена перегонка.
- Основной залог качества конечного продукта состоит в качестве исходной браги.
Полагаясь на это знание и основан процесс перегонки. Таким образом, из сахарной, ягодной, зерновой, плодовой и любой другой браги получают дистиллят спирта. Для начала нужно разобраться, при какой температуре гонят самогон?
Температуры кипения спиртов
Чистый идеализированный спирт имеет градус кипения равный семидесяти восьми.
Как только брага нагревается до определённой температуры, первыми начинают испаряться самые летучие части. В первую очередь выпариваются метанол, уксусный альдегид и прочие особо опасные яды. Это происходит уже при температуре кипения 64–67 градусов.
Второй этап – отделяется этиловый спирт – огонь нагрева убавляют до минимального. Таким образом, поддерживается температура около 62–64 градусов. Именно эту температуру необходимо поддерживать на протяжении всей перегонки. Однако, температура перегонки самогона в ёмкости постепенно растёт по мере испарения спирта.
Когда температура поднимается до 85 градусов, начинается третий этап. Сейчас весь возможный этиловый спирт уже отделился, и за ним выпариваются сивушные масла. Это тоже ядовитые вещества, которые не употребляют для питьевых целей.
Нельзя допустить поднятия температуры до 95 градусов и выше. Такой перегрев приведёт к выбросу браги в остужающий элемент самогонного аппарата. Это заметно ухудшит качество конечного напитка, его цвет и вкус.
Это заметно ухудшит качество конечного напитка, его цвет и вкус.
Источник: http://vse-vino.ru/vodka-i-samogon/temperatura-kipeniya-spirta-pri-pravilnom-samogonovarenii
Чему равна температура кипения спирта?
Этанол – это главный компонент алкогольных напитков. Обычная водка на 40% стоит из него. В быту его называют спиртом. Хотя на самом деле этот термин характеризует огромный класс органических веществ. Температура кипения спирта при нормальном давлении составляет 78,3 градуса по шкале Цельсия.
Это касается только неразбавленного этанола. Температура кипения раствора спирта обычно несколько меньше. В этой статье мы разберемся, что такое этанол. Также обсудим его физические и химические свойства, особенности производства и применения.
Не обойдем мы стороной и основной вопрос относительно того, какая температура кипения спирта.
Общие сведения
Этанол является одним из самых известных спиртов. В состав его молекулы входят такие элементы, как углерод, водород и кислород.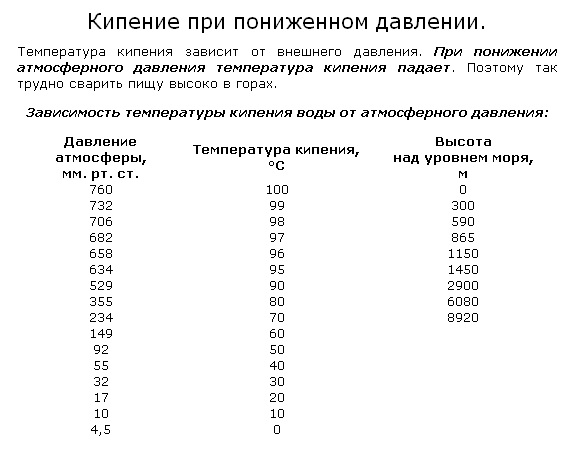 Химическая формула этанола — С2Н6О. Он представляет собой бесцветную жидкость со специфическим алкогольным запахом. Он легче воды.
Химическая формула этанола — С2Н6О. Он представляет собой бесцветную жидкость со специфическим алкогольным запахом. Он легче воды.
Температура кипения спирта – 78,39 градуса по шкале Цельсия. Но это при нормальном давлении. Температура кипения спирта-ректификата составляет 78,15 градусов по шкале Цельсия. Он содержит 4,43% воды.
Температура кипения этилового спирта тем меньше, чем более разбавленным он является.
Применение в быту и промышленности
Этиловый спирт является прекрасным растворителем. Его производят методом ферментации сахара дрожжами. Во многих селах постсоветских стран его по-прежнему делают в домашних условиях.
Получаемый алкогольный напиток называют самогоном. Этиловый спирт является самым древним рекреационным наркотиком, использованным человеком.
Он может вызвать алкогольную интоксикацию при употреблении в значительном объеме.
Этанол является летучим легковоспламеняющимся веществом. Он используется в быту и промышленности в качестве антисептика, растворителя, топлива и активной жидкости в нертутных термометрах (он замерзает при -114 градусах по шкале Цельсия).
Он используется в быту и промышленности в качестве антисептика, растворителя, топлива и активной жидкости в нертутных термометрах (он замерзает при -114 градусах по шкале Цельсия).
От давления
Когда в справочниках указываются физические свойства веществ, то нужно понимать, что все эти замеры делались в так называемых нормальных условиях. С увеличением давления температура кипения этилового спирта уменьшается.
Сегодня можно найти множество таблиц, в которых указаны справочные данные по этому вопросу.
При 780 мм ртутного столба этанол кипит при 78,91 градусов по шкале Цельсия, при 770 – 78,53ºC, при 760 – 78,15ºC, при 750 – 77,77ºC, при 740 – 77,39ºC, при 720 – 76,63ºC.
Метилового спирта
Ch4OH изначально производили как побочный продукт деструктивной перегонки древесины. На сегодняшний день его получают непосредственно из диоксида углерода и водорода. По запаху он очень похож на этанол.
Однако метанол очень токсичен и может привести к смерти человека. Температура кипения спирта – 64,7 градуса по шкале Цельсия. Его используют в качества антифриза и растворителя.
Температура кипения спирта – 64,7 градуса по шкале Цельсия. Его используют в качества антифриза и растворителя.
Также он применяется для производства биодизельного топлива.
История изготовления
Ферментация сахара для получения этанола – это одна из самых ранних биотехнологий на службе у человечества. Опьяняющее действие напитков на его основе было известно с давних времен. Людям всегда нравилось то состояние измененного сознания, которое он вызывает.
Еще 9000 лет назад китайцы знали алкогольные напитки. Дистилляция, как процесс, была хорошо известна арабам и грекам, но им хватало вина. Алхимики научились производить из него спирт только в 12 веке.
Синтетически этанол был впервые изготовлен только в 1825 году Майклом Фарадеем.
Химия и медицина
Этанол применяется в основном в качестве сырья для получения других веществ и растворителя. Он является одним из компонентов многих товаров бытовой химии, которые ежедневно употребляются в быту. Этанол входит в состав стеклоочистителей и антифризов.
Этанол входит в состав стеклоочистителей и антифризов.
В медицине его используют в качестве самого простого антисептика. Он хорошо обеззараживает и подсушивает раны. Также его применяют для изготовления всевозможных настоек и экстрактов. Кроме того, он хорошо охлаждает и согревает.
В условиях отсутствия других медикаментов его использовали в качестве анестезии.
Общество и культура
В исследовании, опубликованном в 2002 году, было установлено, что 41% смертей в автомобильных авариях происходит из-за вождения в нетрезвом виде. Чем больше содержание алкоголя в крови водителя, тем больше риск. Употребление спиртных напитков имеет давнюю историю. Этому социальному явлению посвящены множество исследований.
Процесс распития алкогольных напитков и опьянение описаны во множестве художественных произведений. Известный новогодний фильм «Ирония судьбы, или С легким паром!» посвящен как раз последствиям злоупотребления спиртными напитками, пусть и в комедийной форме.
Многие творческие люди использовали алкоголь как необходимый элемент генерации новых идей или легкий способ преодоления стресса.
Умеренное употребление алкоголя является приемлемым и даже желательным явлением в большинстве современных культур. Распитие спиртных напитков – это традиция на многих торжественных мероприятиях.
Исключение составляет Ислам. По правилам этой религии, употребление любых спиртных напитков – это страшный грех.
Алкоголизм и его последствия
Чрезмерное употребление спиртных напитков – это заболевание. Оно характеризуется физической и психической зависимостью от водки или других крепких напитков, является разновидностью токсикомании. Алкоголики теряют контроль над количеством выпитого.
Им требуется все большая доза для получения удовольствия. Считается, что улучшение благосостояния населения приводит только к росту объемов употребления спиртных напитков. Впервые изучением хронического алкоголизма занялся шведский врач М. Гусс в 1849 году.
Он выделял ряд патологических изменений, которые появляются у человека при систематическом употреблении спиртного. Сейчас ученые проводят четкую границу между пьянством и алкоголизмом. Второе – это болезнь, с которой сам человек справиться не в состоянии. Она проходит в своем развитии несколько стадий.
Сейчас ученые проводят четкую границу между пьянством и алкоголизмом. Второе – это болезнь, с которой сам человек справиться не в состоянии. Она проходит в своем развитии несколько стадий.
На каждом новом этапе происходит постепенно увеличение зависимости. Больному требуется все большая доза. Постепенно хроническая интоксикация алкоголя приводит к соматическим нарушениям. К начальным признакам физической и психической зависимости относят утрату контроля за употреблением и появление запоев.
Лиц с выраженным алкоголизмом отличают сбои в работе внутренних органов и психические расстройства.
Лечение и профилактика
Для борьбы с алкогольной зависимостью требуются медикаменты. Во-первых, лекарства нужны для устранения сбоев в работе организма. Во-вторых, обязательны медикаменты, которые не совместимы с употреблением алкоголя. До сведения пациента доводится то, что запой во время лечения может привести к его смерти.
К тому же с больными обязательно должны работать психологи. Их задача – закрепить эффект от лечения и сформировать негативное представление о пьянстве. Также обязательным является социальная реабилитация бывших алкоголиков. Важно помочь найти человеку свое место в обществе, вернуть семью. Счастливые люди не уходят в запой.
Их задача – закрепить эффект от лечения и сформировать негативное представление о пьянстве. Также обязательным является социальная реабилитация бывших алкоголиков. Важно помочь найти человеку свое место в обществе, вернуть семью. Счастливые люди не уходят в запой.
Поэтому лечение алкоголизма в большей мере зависит от умений психолога.
Источник: https://www.syl.ru/article/228952/new_chemu-ravna-temperatura-kipeniya-spirta
Дистилляция спирта
Подготовительные работы завершены, сусло сбродило, переходим к процессу перегонки.
Итак, мы имеем жидкость (брага, вино) в бродильной емкости, в состав которой входят большое количество различных компонентов, в том числе этанол или этиловый спирт, ради которого мы проделали всю предварительную работу (для справки: даже в хорошей водке, как показывает хроматографический анализ, содержится до 170 различных составляющих).
Метод дистилляции или ректификации подразумевает нагрев этой жидкости, в результате чего некоторые компоненты доходят до точки кипения и переходят в парообразное состояние, эта масса взвешенных частиц попадает в конденсатор-холодильник, где принудительно охлаждается и переходит обратно в жидкое состояние.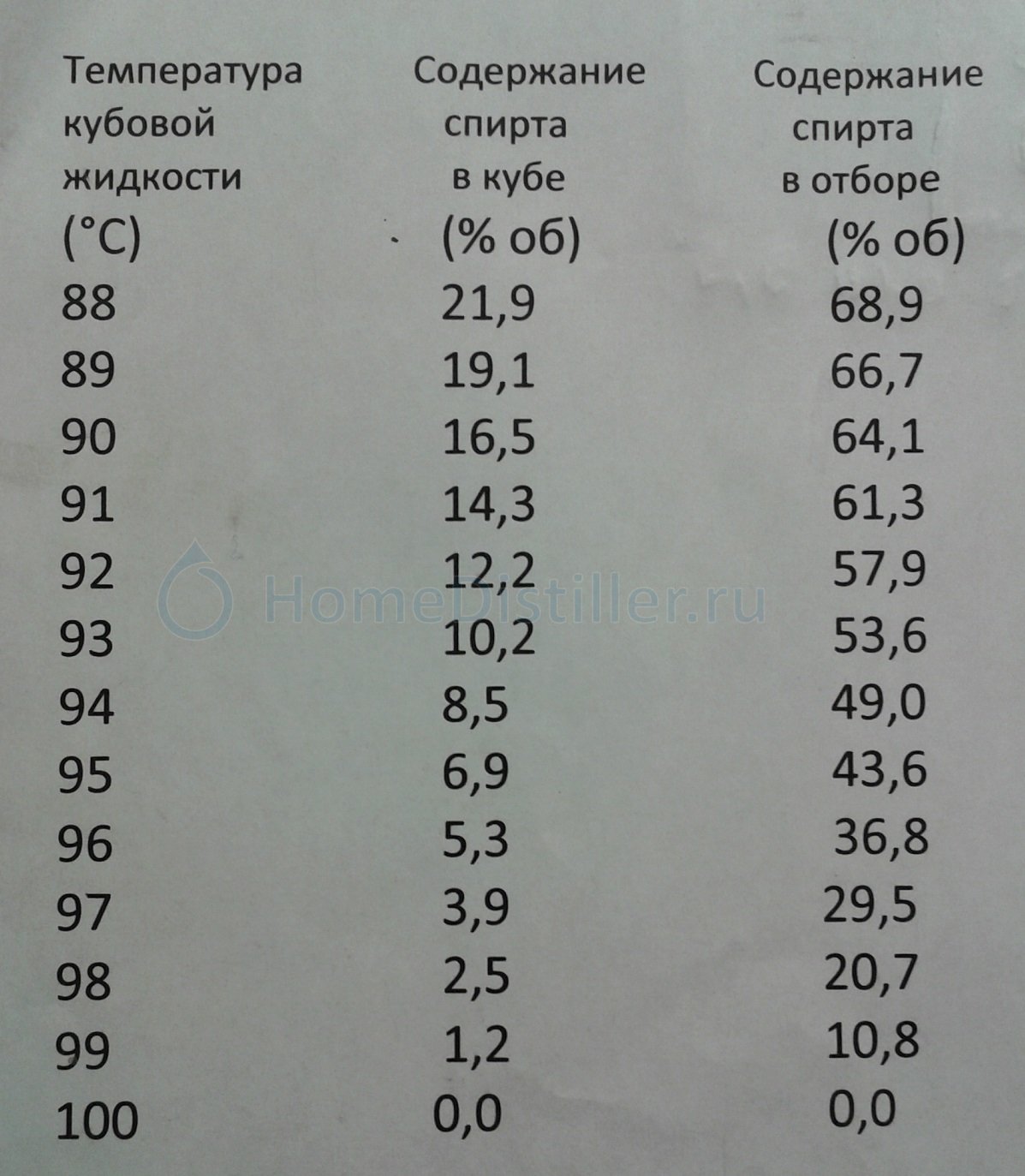 Эта жидкость называется дистиллят. Различные температуры кипения компонентов составляющих брагу позволяют, поддерживая определённые температурные режимы, выделить из общего состава в большей концентрации требуемые вещества, например, этиловый спирт.
Эта жидкость называется дистиллят. Различные температуры кипения компонентов составляющих брагу позволяют, поддерживая определённые температурные режимы, выделить из общего состава в большей концентрации требуемые вещества, например, этиловый спирт.
| Вещество | Температура кипения, °C |
| Ацетон | 56,5 |
| Метанол (древесный спирт) | 64 |
| Этил ацетат | 77,1 |
| Этанол | 78 |
| 2-пропанол (спирт для растирания) | 82 |
| 1-пропанол | 97 |
| Вода | 100 |
В таблице показаны не все, а только наиболее «летучие» составляющие брагу (вино) компоненты.
Многие вещества знакомы многим и более того вызывают опасения. Но давайте по порядку. Метанол или древесный спирт, самый, наверное, пугающий. Он образуется в браге благодаря пектину.
Он образуется в браге благодаря пектину.
«Пектин» — природный полимер Д- галактуроновой кислоты, входящий в состав всех зеленых растений планеты, является неотъемлемой частью пищи человека на всех этапах его эволюции. В результате сбраживания пектин трансформируется в метанол (это естественный процесс!!!).
Количественно образование метанола хорошо изучено, ниже приведен график, который наглядно показывает, сколько образуется этого «страшного» вещества в вишнёвой браге.
Сведения взяты из книги «Ремесло Дистилляции» написанной профессором мичеганского государственного университета (MSU) Крисом Арвидом Берглунд.
Кстати по ГОСТу этиловый спирт типа «Экстра» допускает содержание метанола 0,03% (0,05% — не допускается к продаже, но исследования показывают, что содержание такого уровня в напитках произведённых методом дистилляции натурального сырья встречается крайне редко). В большей концентрации метанол может содержаться в фальсифицированных спиртных напитках, в составе которых присутствуют технические спирты, полученные синтетическим путём из нефти или гидролизом целлюлозы.
К тому же температура кипения метанола ниже температуры кипения этанола (этилового спирта), поэтому при обычной дистилляции, весь дистиллят, собранный до выхода на температурный уровень 78–80°C.
При работе с домашними ректификационными колоннами, сначала выводят установку на режим 78°C, и далее, открыв кран отвода дистиллята медленно, капля за каплей, отводят порядка 3-5% от расчётного количества этанола в отдельную ёмкость.
Весь метанол мы, конечно, не выведем, но после вторичной перегонки, количество его будет минимально. Подобная ситуация и с ацетоном и этил ацетатом…
Помните, что все эти вещества образуются естественным путём в процессе сбраживания сусла, и, если не было грубых нарушений в технологической цепочке производства, эти компоненты попадут в готовый продукт в минимальной концентрации.
А вообще, количество, микропримесей регламентировано только в водке, в виски, к примеру, количество сивушных масел никто никогда не ограничивал, и по факту превышение может составить до 4000 раз (относительно традиционного русского напитка). А может быть в этом и есть очарование этого продукта? Помните опасаться надо не натуральных продуктов, а технических суррогатов (подделок), которые и в наше время можно легко найти в розничной продаже!!!
А может быть в этом и есть очарование этого продукта? Помните опасаться надо не натуральных продуктов, а технических суррогатов (подделок), которые и в наше время можно легко найти в розничной продаже!!!
В мировой практике принято делить отводимый дистиллят на фракции:
- Первая фракция: головная, «heads» — первые 3-5% от расчетного количества дистиллята;
- Средняя, пищевая фракция, «hearts» — вторая часть после отбора головы, собирают до 85–87°C в колонне;
- Хвостовая фракция, «tails» — третья часть дистиллята после 87–90°C в колонне.
«Головная» фракция отличается резким, неприятным запахом, её окончание определяют следующим образом: каплю дистиллята растирают на ладони, если резкий запах ушёл, то пора ставить емкость под пищевую фракцию.
«Пищевую» фракцию собирают в отдельную емкость, далее разбавляют до 35–40% об. и употребляют по назначению, либо перегоняют ещё раз, если не в полном объеме была отобрана «голова» или были упущены «хвосты».
«Хвост» собирают экономные, для последующих перегонок. Но обычно по окончании пищевой фракции дистилляцию останавливают. «Хвост» характеризуется большим количеством сивушных масел (активно выделяются при повышении температуры дистилляции свыше 85–87°C).
Источник: https://www.doctorguber.ru/book/samogonovarenie/tehnologiya-proizvodstva/article-distillation/
При какой температуре гнать самогон: таблица и рекомендации
Действительно, такие вопросы появляются у большинства начинающих винокуров.
Данная статья посвящена работе на классическом самогонном аппарате, состоящем из бака и охладителя. Ну или еще сухопарника между баком и дистиллятором. Термометр установлен в перегонном кубе.
- Возможность точно определить начало перегонки, следовательно сэкономить на воде, включив ее подачу только тогда, когда это необходимо.
- Определить начальную крепость браги.
- Определить текущую крепость самогона на выходе из холодильника, следовательно отпадает необходимость использования ареометров при перегонке.
- Вовремя перейти с отбора тела на отбор хвостов.
- Вовремя закончить отбор хвостов и всю перегонку.
- Рассчитать остаток спирта в кубе.
Как контролировать процесс перегонки по температуре
Как известно, этиловый спирт кипит при температуре 78,4 °C (при атмосферном давлении 760 мм.рт.ст).
Но брага или спирт-сырец являются водно-спиртовым раствором (примесями пренебрегаем), а следовательно и температура кипения этого раствора иная и зависит от содержания в нем этанола.
Причем определенное количество спирта в браге соответствует определенному количеству спирта в парах, поступающих в охладитель.
- Допустим, вы залили 10 литров браги.
- Брага закипела и отбор пошел при 92 градусах, следовательно крепость жидкости приблизительно равна 12%. Только ориентироваться надо не на самые первые капли, а когда пойдет веселая струйка и температура стабилизируется. У меня вчера первые капли появились на 88-89 градусах, но температура очень быстро добралась до 93 и потом стала повышаться очень медленно — на 0,1 градуса. Вот на эту цифру и надо ориентироваться.
- Гоним самогон до 98-99 °C в зависимости от вашей жадности и терпения. Я обычно гоню до 98. До 100 градусов все же не советую — потери продукта будут незначительными, а время потратите много и при этом соберете много ненужных примесей.
При перегонке спирта-сырца:
- Залили, скажем, 20% сортировку.
- По таблице определяем, что температура закипания смеси 88-89 градусов. Следовательно раньше 80 °C воду включать необходимости нет и ее можно поберечь.
- В большинстве методик, да и у меня в статье про дистилляцию, рекомендуется отбирать тело до 40% в струе (или пока горит). Это соответствует температуре 95-96 °C. Т.е. при таком нагреве можно переходить к отбору хвостов. Забегая вперед хочу сказать, что по моим последним данным, переходить к хвостам лучше при 93-94 °C. Да, так мы отправляем большое количество спирта в хвосты, но из этих хвостов потом можно будет отжать еще приличное количество самогона хорошего качества. Почему надо заканчивать отбор тела при 93 °C я расскажу в одной из следующих статей, когда упорядочу полученную информацию.
- Отбираем хвосты до 98-99 градусов.
Источник: http://vinodela.ru/kak-kontrolirovat-process-peregonki-po-temperature.html
Большая Энциклопедия Нефти и Газа
Температура кипения спирта при нормальном давлении равна 78 3 С. Температура кипящего спирта остается постоянной, несмотря на непрерывный подвод тепла. Это происходит потому, что для превращения жидкости в пар необходимо затратить определенное количество тепла, которое называется теплотой испарения.
Температура кипения спиртов повышается в гомологическом ряду с увеличением длины цепи.
Температуры кипения спиртов значительно, можно сказать, аномально, выше температур кипения соответствующих алканов. С увеличением массы спиртов температуры кипения возрастают, причем у разветвленных спиртов температуры кипения ниже, чем у нормальных.
Температура кипения спиртов возрастает с увеличением молекулярного веса; при этом разность между точками кипения двух соседних членов ряда от этилового до деЦнлового спирта составляет 18 — 20; для высших спиртов эта разность меньше.
Температуры кипения спиртов значительно выше, чем температуры кипения эфиров или углеводородов, имеющих ту же молекулярную массу.
Температура кипения спиртов значительно выше температуры кипения соответствующих углеводородов и даже галогенопроиз-водных.
Температура кипения спиртов значительно выше температуры кипения соответствующих углеводородов и даже галогенопроизвод-ных. Например, этан кипит при — 88 3 С, бромистый этил С2Н5Вг — при 38 0 С, а этиловый спирт — при 78 3 С.
Температура кипения спиртов значительно выше температуры кипения соответствующих углеводородов и даже галогенопроизводных. Например, этан кипит при — 88 3 С, бромистый этил С2Н5Вг — при 38 0 С, а этиловый спирт — при 78 3 С.
Температуры кипения спиртов и фенолов значительно выше, чем соответствующих углеводородов. Это вызвано тем, что в спиртах имеет место ассоциация молекул, обусловленная наличием гидроксильных групп.
Температуры кипения спиртов значительно, можно сказать, аномально, выше температур кипения соответствующих алканов. С увеличением массы спиртов температуры кипения возрастают, причем у разветвленных спиртов температуры кипения ниже, чем у нормальных.
Температура кипения спиртов возрастает с увеличением молекулярного веса; при этом разность между точками кипения двух соседних членов ряда от этилового до децилового спирта — составляет 18 — 20; для высших спиртов эта разность меньше.
Температуры кипения спиртов и фенолов значительно выше, чем соответствующих углеводородов. Это вызвано тем, что в спиртах имеет место ассоциация молекул, обусловленная наличием гидроксильных групп.
Температура кипения спиртов зависит от их строения. По общей закономерности, чем больше отклоняется данное вещество от нормального строения, тем ниже температура его кипения.
Источник: http://www.ngpedia.ru/id503619p1.html
Температура браги при перегонке — правильные температурные режимы
При изготовлении самогона температура браги при перегонке имеет первостепенное значение.
От того, насколько правильно соблюдён температурный режим, без преувеличения, зависит качество самогона и целостность самогонного аппарата. Слишком быстрое доведение браги до кипения может даже взорвать перегонный куб.
Можно добиться нужного результата путём проб и ошибок. Но более разумно воспользоваться уже собранной информацией и готовыми советами.
Состав браги
Брага представляет собой водно-спиртовой раствор, который, кроме спирта и воды, содержит примеси эфирных масел, альдегидов и прочих соединений.
Смысл дистилляции заключается в извлечении как можно большего количества этилового спирта из этого раствора. Максимально полно выделить этиловый спирт из браги позволяет перегонка с разделением на фракции.
Есть несколько методов дробной перегонки. Оптимальным и проверенным является правильный температурный контроль.
Температура перегонки браги
Разделение самогона на фракции основывается на разнице температур кипения входящих в брагу соединений. При давлении 760 мм рт. ст. температура кипения этилового спирта — 78,3°C, воды — 100°C. Остальные, входящие в брагу вещества, закипают раньше спирта либо позже. Рассмотрим на подробном примере, при какой температуре гнать самогон.
Диапазон 0—68°C
В начале перегонки самогонный аппарат выводится на рабочую мощность 63°C. Затем нагрев снижается, чтобы температура браги плавно вышла на 65–68°C. При умеренном нагреве брага задержится на некоторое время на этом уровне, а не проскочит его. На данном этапе закипают следующие жидкие соединения:
- уксусный альдегид — 20°C;
- муравьино-этиловый эфир — 54°C;
- муравьино-метиловый эфир — 57°C;
- метиловый спирт — 65°C.
Эти вредные и ядовитые соединения принято называть «головами», а процесс их отделения — отбором голов. Не рекомендуется использовать их даже для технических нужд.
Диапазон 78—85°C
После отбора голов рекомендуется заменить или почистить сухопарник. Ставим новую ёмкость и начинаем сбор «тела» самогона. Это цель всей перегонки, собственно, этиловый спирт.
Для его выгона постепенно повышаем температуру браги до 78°C, приближаясь к началу кипения этила. Чем выше концентрация спирта в браге, тем быстрее произойдёт его испарение. Выход тела продолжается до 85°C.
Стараемся как можно дольше удержать брагу в этом температурном диапазоне.
Выше 85°C
Нагрев перегонный куб до 85 градусов, можно усиливать подогрев и быстро отделять «хвосты». В самогонном аппарате ещё осталось небольшое содержание алкоголя.
Но он растворён в смеси из уксусной и муравьиной кислот, масляно-этилового эфира, амилового спирта и других сивушных соединений с температурой кипения выше 100°C. Часто их называют просто «сивухой».
Единственный вариант их дальнейшего использования — добавить в новую брагу к следующей перегонке.
Конструкции перегонных кубов
Перегонные кубы промышленного изготовления могут различаться конструкцией и схемой сборки. Стандартный самогонный аппарат состоит из перегонного куба, сухопарника, водяного охладителя и крана для слива готового продукта. Обычно в корпус встраиваются биметаллические термометры. Благодаря их показаниям температура перегонки самогона известна с точностью до градуса.
Другой способ переработки браги — колонна для ректификации. Термометр не монтируется заранее. В корпусе предусматривается отверстие для внешнего термометра. Он может быть биметаллическим или электронным. В сравнении друг с другом электронный выигрывает в точности, а биметаллический — в прочности.
Для более точных показаний колонна требует небольшой доработки. Нужно смазать пространство под термометром растительным маслом. Это улучшит реакцию термометра на теплоту испаряющихся водных, спиртовых и эфирных паров.
Перегонка браги в самогон без термометра
В условиях, если дистиллятор изготовлен собственноручно и не оборудован термометром, можно обойтись и без показаний температуры.
Отбор голов
В данном случае обязательна двойная перегонка. Первый перегон осуществляется без дробления на фракции. По его окончании измерить объем спирта-сырца в литрах и крепость в градусах. Чтобы рассчитать, сколько в браге чистого спирта, нужно умножить эти данные друг на друга. 12—15% от количества чистого спирта занимают головы, которые нужно отобрать в отдельную тару при второй перегонке.
Второй процесс расчёта голов основывается на содержании сахара в браге. Замеры осуществляются ещё на стадии приготовления сусла перед внесением дрожжей. На каждый внесённый килограмм сахарного песка нужно отобрать 100 мл голов.
Сбор тела самогонки
Следующим шагом после выхода голов будет сбор спиртового дистиллята. Он продолжается до падения крепости сырца до 40°C. Технология без использования спиртомера предлагает поджигать самогон. До тех пор, пока реакция горения сопровождается синим пламенем, идёт основная фракция. Хвосты гореть перестанут.
Источник: https://alcoplace.ru/samogon/temperatura-peregonki-bragi.html
Физика — Ректификация спирта
Чтобы понять «физику» ректификации спирта рассмотрим основные свойства абсолютизированного 100%-ного этилового спирта:
- температура кипения = 78,3°C при 760 мм рт.ст.
- плотность жидкости = 790 кг/м3 при 20°С
Известно, что этиловый спирт прекрасно растворяется в воде, образуя бинарную водно-спиртовую смесь с любым количеством спирта. Здесь нужно обозначить разницу между массовой и объёмной концентрацией этанола в водно-спиртовом растворе. Массовая концентрация спирта — это масса спирта в массе раствора (обозначается как г/г или %масс.).
Чаще применяется понятие объёмной концентрации — это объем спирта в объеме смеси (обозначается как мл/мл или %об.). Величины объёмной и массовой концентраций из-за значительной разницы в плотности спирта (0,79 г/мл) и воды (1 г/мл) могут существенно различаться. В дальнейшем здесь будет использоваться только понятием объёмной концентрации.
Понятно, что температура кипения раствора двух жидкостей должна находиться между их индивидуальными температурами кипения — 100°C для воды и 78,3°C для этилового спирта (при 760 мм рт. ст.). Зависимость температуры кипения (парообразования) этого раствора, или, что то же самое, температуры насыщенного водно-спиртового пара от концентрации спирта в парах показана на рис. 1.
Особого внимания на этом графике заслуживает точка А с концентрацией 96,4% и с температурой кипения меньше температуры кипения 100%-ного этилового спирта.
Нагляднее всего процессы дистилляции и ректификации этанола объяснить по кривой равновесия фаз бинарной водно-спиртовой смеси.
Практически вся кривая равновесия находится выше диагонали Y=X, то есть при испарении водно-спиртового раствора концентрация спирта в парах получается большей, чем в исходной жидкости. Именно это и лежит в основе процессов дистилляции и ректификации этанола.
Большое значение имеет точка (А, X=Y=97,2% объёмных) пересечения кривой равновесия фаз с диагональю. Это особая «точка азеотропа» — нераздельно кипящая жидкая смесь двух чистых компонентов, которую путём перегонки или ректификации невозможно разделить на составляющие. Максимально приближенная к точке азеотропа водно-спиртовая смесь и называется спирт-ректификат.
Используя кривую равновесия и диагональ Y=X (см. рис. 2), можно увидеть, что при простой перегонке 10%-ной бражки сначала получается самогон с концентрацией примерно 53%об. Далее, после ступеньки 10-53, можно построить следующие — 53-82, 82-88, 88-92 и т.д.
Вертикальная составляющая ступеньки показывает повышение процента этанола в паровой фазе вплоть до наступления равновесия фаз (точка А). Горизонтальная составляющая ступеньки показывает конденсацию этих паров (точка пересечения горизонтали с диагональю Y=X).
По диаграмме видно, что для получения спирта-ректификата из бражки с начальной концентрацией 10% теоретически должно пройти более десятка таких последовательных перегонок. На практике их должно быть намного больше, так по мере уменьшения концентрации спирта в перегонном кубе соответственно уменьшается и концентрация дистиллята. Например, на первой ступеньке 53%об. соответствует только начальному моменту перегонки.
По прошествии какого-то времени концентрация спирта в бражке уменьшается и мы имеем в ней уже меньше, чем 10% спирта, в результате чего к концу первой перегонки отобранный самогон имеет среднюю крепость не 53%об., а 35-40%об.
Стоит отметить, что температура кипения этанола зависит от атмосферного давления. Причём эта зависимость достаточно существенна для процесса ректификации, когда каждая десятая доля градуса имеет значение.
В очень-очень упрощенной постановке, описанные выше «ступеньки» отдельных перегонок, но осуществляемые не по отдельности, а собранные вместе в одном аппарате и составляют процесс ректификации спирта.
Такая ректификационная установка имеет еще один огромный «плюс» — параллельно с задачей получения спирта-ректификата она решает еще и задачу очистки его от примесей, имеющих отличную от спирта температуру кипения.
Выходя за рамки нашей цели — получения спирта, с помощью ректификационной колонны можно выделить в чистом виде любое вещество (это будет особенно легко, если вы знаете температуру его кипения).
Например, перегоняя настой еловых иголок, можно попробовать выделить составляющую, заведующую запахом хвои, или из настоя лепестков розы выделить вещество, отвечающее за этот цветочный запах.
От самогонщика до парфюмера один шаг.
На самом деле ректификационные колонны бывают разных типов и имеют порой весьма сложное устройство.
Источник: http://www.home-alco.ru/teoriya/fizika-rektifikatsiya-spirta-detail
Температура дистилляции
Проблема температурной стабилизации не редко обсуждается на просторах интернета, люди задают вопросы почему температура не соответствует теории или наблюдается т.н. «пила».. скачки температуры.
Если у людей возникают подобные вопросы, за них можно искренне порадоваться, так как подобные «проблемы» возникают только на правильно сконструированных аппаратах и правильном выходе на режим дистилляции или ректификации. На самом деле это не проблема, а лишнее доказательство правильного пути…
Давайте разберемся почему так происходит.
Допустим, температура кипения спирта не соответствует теории… Все уважающие себя винокуры прекрасно знают, что температура кипения спирта зависит от атмосферного давления, но не редко об этом забывают..
При атмосферном давлении 760мм.рт.ст. температура кипения 78,15ºC, а при 740мм.рт.ст. уже – 77,35ºC. Заметили существенную разницу? Таким образом, при проведении ректификации или дистилляции не будет лишним взглянуть на барометр.. Так что можно смело продолжать работать и не переживать.
Еще одна проблема, т.н. «пила», скачки температуры. Тут все еще проще — это обычные капли флегмы (дистиллята) попадающие из дефлегматора на датчик температуры. Проблема решается обычным «надеванием козырька» на датчик.
Если не нравится, что термометр показывает скачки, нужно прикрыть его датчик сверху небольшой пластинкой металла защищающей от брызг.
Сильные скачки температуры говорят о том, что флегма переохлаждена, необходимо отрегулировать подачу охлаждения в дефлегматор.
Немного информации про атмосферное давление
Дефлегматоры ректификационных колонн обязательно имеют связь с атмосферой для свободного «выдоха» колонны. Связь с атмосферой необходима на всех режимах работы колонны.
Если атмосферное давление меняется в допустимых пределах, это никак не сказывается на работе за исключением вышеописанных «проблем».
Достаточно уточнить температуру кипения спирта для соответствующего уровня давления и работать дальше.
Допустим, в процессе ректификации, находясь на спиртовой полке 77,35ºC (740мм.рт.ст.), будет зафиксирована температура 77,6ºC, достаточно перекрыть кран отбора и подождать пару минут. Если температура осталась 77,6ºC, значит атмосферное давление выросло. Посмотрите на барометр, убедитесь, что давление действительно поднялось до 746мм.рт.ст., верните отбор на прежний уровень, и продолжайте работать.
Если давление упадет ниже допустимого предела заложенного в технологические особенности вашего аппарата, допустим.. 720…730мм.рт.ст., колонна скорее всего, захлебнется.
Причина захлеба в уменьшении плотности паров из-за падения давления.
Дальше работает такая цепочка причин: массовая производительность пара осталась прежней, но из-за падения плотности спиртового пара возрастает его скорость, что и приводит к захлебыванию насадки в колонне.
Источник: https://alcodistillers.ru/distill2.html
Температура кипения сивушного масла
Согласно Большому Энциклопедическому Словарю, «СИВУШНОЕ МАСЛО — ядовитая маслянистая жидкость с неприятным запахом; смесь одноатомных спиртов, альдегидов, кислот и др. Образуется как примесь при производстве этилового спирта методом брожения. Из сивушного масла получают амиловые и некоторые др. спирты.»
Так вот, основную часть сивушного масла составляет изоамиловый спирт. Именно ему люди обязаны самогонным букетом и головной болью на следующее утро.
Выделенный в чистом виде (это можно сделать только путем технологических ухищрений на РК с высокой степенью разделения) изоамиловый спирт (другое название — изоамилол) имеет удушающий химический запах растворителя масляной краски. Собственно из изоамилола этот растворитель и делают.
Если же эту блаженную жидкость размазать по водно-спиртовому раствору, мы получим неопознаваемый, но весьма противный букет той самой «сивухи», запах которой знаком многим поколениям. Нужно оговориться, что там не только изоамилол, но и другие «жирные» спирты. Просто амилового гораздо больше.
Нет никакого особого смысла «ковырятся» в этих других компонентах сивушного масла так как, во-первых, ведут они себя в основном схожим образом и честно отсиживаются в хвостовой фракции, а во-вторых, есть смысл двигаться от простого к сложному. Т.е. сначала нужно избавиться от самых крупных и противных, а уж потом думать, стоит ли дальше заморачиваться. И эта-то задача не то, чтобы была нерешаемой, но не такая уж простая.
Итак, изоамилол. Температура кипения у него 132,1ºС. Казалось бы чего морочиться, даже вода отойдет раньше. Ан нет, оказывается поведение изоамилола очень зависит от количества этанола в растворе. При низкой спиртуозности раствора, он ведет себя как головная фракция, дистиллируясь в начале погона.
Как показали замеры, при обычной дистилляции низкоспиртуозного раствора, изоамилол в значительных концентрациях присутствует только в первой трети продукта возгонки. Оставшаяся часть (2/3 от общего количества продукта) содержит лишь незначительные следы.
Скорость возгонки при этом не играет особой роли, скорее важна именно спиртуозность, чем она меньше — тем быстрее и легче изоамилол покидает раствор. При дистиллировании высокоспиртуозных растворов, до крепости 40º он упорно сидит в кубе, начиная отбираться при переходе через 40º и менее.
Такое его поведение связано с тем, что изоамиловый спирт практически нерастворим в воде, зато хорошо растворяется в этаноле.
Ихсодя из этого интересного механизма возгонки изоамилола, родилась своя технология дробного перегона на обычных дистилляторах. При перегоне браги первая треть погона отбирается в отдельную партию. Вторые две трети перегоняются повторно для достижения нужной крепости с небольшим отбором головы. Хвосты — по вкусу.
Затем первая партия вновь разбавляется и снова дробится, но теперь уже пополам. Первая половина или выливается или передается на колонну для ректификации. Вторая половина перегоняется повторно для достижения нужной крепости. Вновь немного головы и хвостов по вкусу. Затем можно смешать с питьевой частью, полученной из вторых двух третей самого первого погона.
Отходов будет больше по сравнению с традиционной методикой, но и качество выше.
Теперь, отдельно пару слов о пропаноле-2 или изопропиловом спирте.
Изопропиловый спирт конечно отличается по органолептике от этанола, но отличия эти в более резком запахе и вкусе. Относится он к веществам третьей группы опасности, т.е. умеренно опасен.
Даже употребление его в химически чистом виде не способно убить человека просто потому, что он вызывает опьянение в 10 раз более сильное, чем этанол (продуктом его окисления печенью является ацетон) да еще и более стойкое.
Человек теряет сознание задолго до того как сможет без посторонней помощи употребить сколь-нибудь значимое его количество. На сегодняшний день не зафиксировано ни одного случая смертельного отравления пропанолом.
Так вот, в плане ответа на вопрос о температуре кипения сивухи, правильно будет сказать :
Вопрос о температуре кипения сивушного масла не имеет практического смысла так как состав его сложен, вещества в него входящие имеют очень разные свойства и механизмы поведения.
Для уменьшения их количества в конечном продукте нужно применять правильные технологические схемы дистилляции.
Для их полного удаления необходимо использовать еще и правильное ректификационное оборудование.
Источник: http://moi.12ruk.ru/2014/11/22/temperatura-kipeniya-sivushnogo-masla/
Головы, тело и хвосты
Физика и химия
Для отделения спирта в классических самогонных аппаратах используют различные физические свойства воды, спиртов и масел. Разница в температурах кипения позволяет «выпарить» сначала легкие метиловые спирты, затем получить этиловый спирт и отделить его от сивушных масел и воды.В браге все компоненты «сцеплены» друг с другом. В обычном самогонном аппарате нельзя полностью их разделить, поэтому мы можем говорить только про этапы перегонки, когда в испарениях содержится наибольшее количество этилового спирта. Также мы не можем точно ориентироваться и по температурам кипения спиртов и воды, так как в исходных жидкостях спирт зачастую находится в связанном состоянии с различными минералами и другими спиртами.
Головы
Первым при температуре 64,7 °C закипает метиловый спирт (метанол). Метанол ядовит и токсичен, однако этиловый спирт нейтрализует его действие на организм. Жидкость, полученную при перегонке на температурах от 65° до 80 °C, в народе называют “первачом” или “головами”. От основного продукта «первач» отличается характерным резким запахом. Такой продукт непригоден для потребления.Телo
При температуре 75-78 °C после выхода метанола и других легких примесей в испарениях преобладает этиловый спирт. Температура кипения этилового спирта — 78,4 °C. Жидкость, полученную при перегонке на температурах от 80 до 95 °C, самогонщики называют «тело». С ростом температуры в перегонном кубе концентрация этилового спирта снижается. Полученный самогон можно пить, облагораживать или перегнать во второй раз.Хвосты
При температуре выше 95 °C начинают испаряться тяжелые примеси и сивушные масла. Крепость конденсата сильно падает и он перестает гореть. На этом этапе следует прекратить перегонку, а остатки браги вылить или оставить до следующего перегона. Чтобы определить, когда пошли «хвосты», используйте ареометр (спиртомер) или попробуйте поджечь ватку, смоченную в дистилляте. Помните про соблюдение пожарной безопасности.Чтобы контролировать содержание спирта в перегонном кубе по термометру, советуем ориентироваться по таблице:
Таблица
| Температура кубовой жидкости, ℃ | Содержание спирта в кубе, % об. | Содержание спирта в отборе, % об. |
| 88 | 21,9 | 68,9 |
| 89 | 19,1 | 66,7 |
| 90 | 16,5 | 64,1 |
| 91 | 14,3 | 61,3 |
| 92 | 12,2 | 57,9 |
| 93 | 10,2 | 53,6 |
| 94 | 8,5 | 49,0 |
| 95 | 6,9 | 43,6 |
| 96 | 5,3 | 36,8 |
| 97 | 3,9 | 29,5 |
| 98 | 2,5 | 2,7 |
| 99 | 1,2 | 10,8 |
| 100 | 0,0 | 0,0 |
СВОЙСТВА ИЗОПРОПИЛОВОГО СПИРТА
Химия и технология пропилена
Ниже приведены свойства изопропилового спирта [103]:
Температура плавления, °С Температура кипения, РС.
Плотность р|°…………………………
Показатель преломления п|°
TOC \o «1-3» \h \z Вязкость при 20 9С, сП………………………………………………………………. 2,43
Поверхностное натяжение при 20 °С, дпн/см. . . 21,7
Критическая температура, °С………………………………………….. 234,9
Критическое давление, кгс/см2 …………………………………………………….. 53
Теплота плавления при температуре текучести
Кал/г………………………………………………………………………. 21,08
Ккал/моль……………………………………………………………….. 1,284
Теплота испарения при температуре кипения, кал/г 160
Теплота испарения при 25 °С, ккал/моль…………………………… 11,05
Теплота образования, ккал/моль………………………………………. 76,4
Теплота сгорания,
Кал/г…………………………………………………………………………………. 7970
Ккал/моль………………………………………………………………… 478,9
Удельная теплоемкость, кал/(г ■ °С)…………………………………. 0,563
При 30 рС…………………………………………………………………………. 0,677
50 °С…………………………………………………………… ‘ . 13,740
Коэффициент теплопроводности при 09С,
Кал ■ см/(сек • см2 ■ °С)…………………………………………………… 3,683 ■ 10~4
Коэффициент теплового расширения, 1/°С……………………….. 0,001075
Нижний предел взрываемости в смеси с воздухом,
Объемн. % …………………………………………………………………. 2,5
Температура вспышки (в закрытой аппаратуре), РС 15
Температура самовоспламенения, РС……………………………….. 456
Диэлектрическая проницаемость при 20 °С…. 26
В литературе [104] приведен обзор двойных и тройных азеотроп — ных смесей.
Изопрен [1—12] был впервые получе-н в 1860 г. в результате сухой перегонки каучука [13]. Вскоре после того как стало известно, что изопрен является основным элементом структуры натурального каучука, были предприняты …
Третий метод [188—190] разработан Bataaf Petroleum Maats — chappij. Очищенный кислотой кумол окисляется кислородом в медных башнях при 120—130 °С. Медь (в форме колец) при специальных условиях протравливается азотной кислотой. …
Первые опыты по термической полимеризации пропилена [1] были проведены Ипатьевым [2], который показал, что при высоком давлении и 330—370 °С образуется полимер следующего состава в %): TOC \o «1-3» \h …
| Изопропиловый спирт представляет собой бесцветную жидкость с характерным спиртовым запахом, более резковатым по сравнению с этанолом. Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях. С водой образует азеотропную смесь (87,9% изопропилового спирта, температура кипения 80,2° C). Является простейшим вторичным одноатомным спиртом алифатического ряда, обладает свойствами вторичных спиртов жирного ряда, в том числе образует простые и сложные эфиры. В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения. При дегидрировании превращается в ацетон. Реагирует с сильными окислителями. Агрессивен в отношении некоторых видов пластика и резины. Плотность 0,785 г/см³. Температура плавления -89,5° C, температура кипения 82,4° C, температура вспышки 11,7° C, температура самовоспламенения 456° C. Химическая формула: C3H8O. Изопропиловый спирт получают гидрированием ацетона водородом (в фазе пара) или сернокислотной гидратацией пропилена. Во втором случае, сырьем служит пропан-пропиленовая фракция с содержанием пропилена 30-90% (фракция пиролиза и крекинга нефти). Изопропиловый спирт имеет очень широкую сферу применения:
Требование безопасности. Упаковка, транспортировка и хранение. ООО “ФАСТЕХ” осуществляет поставки химической продукции со склада в Белгороде в сроки и по доступным ценам, на выгодных для Вас условиях. | ||
Точка кипения спирта
Температура кипения спирта зависит от того, какой спирт вы используете, а также от атмосферного давления. Температура кипения снижается с понижением атмосферного давления, поэтому она будет немного ниже, если вы не находитесь на уровне моря. Вот посмотрите на температуру кипения различных видов алкоголя.
Температура кипения этанола или зернового спирта (C 2 H 5 OH) при атмосферном давлении (14,7 фунтов на кв. Дюйм, 1 бар абс.) Составляет 173.1 F (78,37 ° C).
- Метанол (метиловый спирт, древесный спирт): 66 ° C или 151 ° F
- Изопропиловый спирт (изопропанол): 80,3 ° C или 177 ° F
Последствия различных точек кипения
Одним из практических применений различных температур кипения спиртов и спирта по отношению к воде и другим жидкостям является то, что их можно использовать для их разделения с помощью дистилляции. В процессе перегонки жидкость тщательно нагревается, чтобы более летучие соединения выкипали.Их можно собрать, как метод перегонки спирта, или этот метод можно использовать для очистки исходной жидкости путем удаления соединений с более низкой температурой кипения. Различные типы спирта имеют разные точки кипения, поэтому их можно использовать для отделения друг от друга и от других органических соединений. Дистилляция также может использоваться для разделения спирта и воды. Температура кипения воды составляет 212 F или 100 C, что выше, чем у спирта. Однако перегонку нельзя использовать для полного разделения двух химических веществ.
Миф о приготовлении алкоголя из еды
Многие люди считают, что алкоголь, добавленный в процессе приготовления, выкипает, добавляя аромат без удержания алкоголя. В то время как приготовление пищи при температуре выше 173 F или 78 C имеет смысл избавиться от алкоголя и оставить воду, ученые из Департамента сельского хозяйства Университета Айдахо измерили количество алкоголя, остающегося в продуктах питания, и обнаружили, что большинство методов приготовления на самом деле не влияют на содержание алкоголя, сколько вы думаете.
- Наибольшее количество спирта остается, когда спирт добавляют в кипящую жидкость, а затем снимают с огня. Осталось около 85 процентов алкоголя.
- Обжиг жидкости для сжигания спирта все еще позволял удерживать 75%.
- Хранение спиртосодержащих продуктов на ночь без нагрева привело к задержке на 70%. Здесь потеря спирта произошла из-за того, что у него более высокое давление пара, чем у воды, поэтому часть его испарилась.
- Выпечка по рецепту, содержащему спирт, привела к удержанию алкоголя в диапазоне от 25 процентов (время выпекания 1 час) до 45 процентов (25 минут, без перемешивания).Рецепт нужно было выпекать 2 часа или дольше, чтобы содержание алкоголя снизилось до 10 процентов или ниже.
Почему нельзя приготовить алкоголь из еды? Причина в том, что спирт и вода связываются друг с другом, образуя азеотроп. Компоненты смеси нелегко разделить с помощью тепла. По этой же причине дистилляции недостаточно для получения 100-процентного или абсолютного спирта. Единственный способ полностью удалить спирт из жидкости — это полностью выкипеть или дать ему испариться, пока он не высохнет.
Свойства изопропилового спирта | Sciencing
Изопропиловый спирт или 2-пропанол продается как медицинский спирт во многих супермаркетах и аптеках. Он принадлежит к классу органических соединений, называемых спиртами, все из которых отличаются группой -ОН, присоединенной к их углеродной цепи. Многие физические свойства изопропилового спирта напоминают свойства других подобных короткоцепочечных спиртов.
Физические свойства
Благодаря группе -ОН молекулы изопропилового спирта могут образовывать слабые связи, называемые водородными связями, которые помогают удерживать молекулы вместе.Следовательно, он имеет гораздо более высокую температуру кипения и плавления, чем пропан, который также содержит три атома углерода и восемь атомов водорода. Температура кипения изопропилового спирта составляет 82 градуса Цельсия; его температура плавления -89 C. Его температура кипения ниже, чем у 1-пропанола (пропилового спирта). Плотность чистого изопропилового спирта при комнатной температуре составляет около 78,6% от плотности воды при той же температуре.
Поведение в растворе
Изопропиловый спирт очень хорошо смешивается с водой; медицинский спирт, продаваемый в аптеках, например, представляет собой смесь 2-пропанола и воды.Кислотность соединения часто измеряется с помощью его pKa, в котором более низкие числа обозначают более высокую кислотность. Изопропиловый спирт имеет pKa 17,1. Это чрезвычайно слабая кислота — более слабая, чем вода, у которой pKa составляет 15,7.
Химия
Изопропиловый спирт легко воспламеняется как в жидкой, так и в парообразной форме. Воздействие окислителей, таких как хромовая кислота, превращает изопропиловый спирт в ацетон, в то время как воздействие тепла и концентрированной серной кислоты может дегидратировать изопропиловый спирт с образованием пропена.Сильные основания могут отщеплять ион водорода от изопропилового спирта с образованием изопропоксидов, которые являются сильными основаниями и могут быть полезны в некоторых органических синтезах. Взаимодействие изопропилового спирта с трибромидом фосфора приведет к замене спиртовой группы на атом брома.
Соображения растворимости
Изопропиловый спирт имеет более низкую диэлектрическую проницаемость, чем вода или этанол, что означает, что он имеет меньшую способность экранировать противоположные заряды и удерживать их разделенными. Следовательно, добавление изопропилового спирта к раствору соли, содержащему ДНК или РНК, поможет осаждать ДНК или РНК, потому что положительно заряженные ионы из соли и молекулы ДНК могут объединиться, чтобы образовать агрегаты и выпасть из раствора.Изопропиловый спирт также менее растворим в соленой воде, чем в чистой воде.
Свойства растворителя изопропилового спирта
Свойства растворителя изопропилового спирта
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Заявление о доступности Оставить отзыв о веб-сайте
90% изопропиловый спирт | Инструменты для дома
Есть вопросы? Обратитесь в службу поддержки клиентов.406-256-0990 или Живой чат в
- Возраст 14+
- На складе, готово к отправке
- Это нужно быстро? Смотрите варианты доставки в корзине.
Этот флакон на 30 мл содержит 90% изопропиловый спирт, который можно использовать в качестве топлива для спиртовых ламп. Посмотрите ниже, чтобы узнать о формуле изопропилового спирта, температуре кипения изопропилового спирта, других применениях изопропилового спирта и многом другом! Читать Подробнее
My Science Perks получают не менее $ 0,07 обратно на этот предмет. Войдите или создайте Бесплатный HST Аккаунт, чтобы начать зарабатывать сегодня
Ограничения на доставку:ОПИСАНИЕ
Бутылка на 30 мл содержит 90% изопропиловый спирт.Изопропиловый спирт можно использовать для:
Посмотрите на таблицу ниже, чтобы узнать формулу изопропилового спирта, точку кипения изопропилового спирта, использование изопропилового спирта, плотность изопропилового спирта и многое другое.
| Формула | C 3 H 8 O |
| Форма | Решение |
| Номер CAS | Смесь |
| Классификация DOT | UN1219, раствор изопропанола |
| Плотность | 786 кг / м³ |
| Код хранения | Красный |
| Обычное использование | Спиртовая лампа топливная Эксперименты по хроматографии и экстракции ДНК Часто встречается в медицинском спирте, который можно использовать в антисептических целях. |
| Опасность | Легковоспламеняющиеся и горючие жидкости |
| Температура кипения чистого изопропанола | 82 ° С (179.6 ° F) |
| Точка плавления для чистого изопропанола | -90 ° C (-130 ° F) |
БЛОК ДОПОЛНИТЕЛЬНОЙ ИНФОРМАЦИИ
ВКЛАДКА С СОДЕРЖАНИЕМ
ТАБЛИЦА ТЕХНИЧЕСКИХ ХАРАКТЕРИСТИК
- Описание
- ООН-ИЗОПАЛК
- Технические характеристики
- СОДЕРЖАНИЕ
Ограничение на доставку: Этот товар доставляется только эконом-классом или UPS на почтовые адреса в 50 штатах США.
Предупреждение: ОПАСНОЕ ХИМИЧЕСКОЕ ВЕЩЕСТВО — Легковоспламеняющаяся жидкость; внимательно прочтите предупреждающие надписи.
Мы хотим, чтобы этот предмет был живым, когда вы его получите! Следовательно, нам необходимо знать, когда вы будете дома, чтобы получить его (минимизируя воздействие стихии). Пожалуйста, укажите дату доставки, среда — Пятница, это минимум 7 дней с сегодняшнего дня.
Химия / Химия
/ химия /, / химия / химия /
Понятно. Наука может быть беспорядочной. Но продукты и услуги Home Science Tools справятся с этим.
Наша продукция долговечна, надежна и доступна по цене, позволяя вам перемещаться из полевых условий в лабораторию и на кухню. Они не подведут вас, с чем бы они ни боролись. Будь то (чрезмерно) нетерпеливые молодые ученые из года в год или строгие требования, которые возникают раз в жизни.
И если ваш научный запрос идет не так, как ожидалось, вы можете рассчитывать на помощь нашей службы поддержки клиентов. Рассчитывайте на дружеские голоса на другом конце телефона и советы экспертов в вашем почтовом ящике. Они не будут счастливы, пока вы не станете счастливыми.
Итог? Мы гарантируем, что наши продукты и услуги не испортят ваше научное исследование, каким бы беспорядочным оно ни было.
Вопросы? Свяжитесь с нашей службой поддержки клиентов.
MSDS: 70% изопропиловый спирт
% PDF-1.6 % 1 0 объект > эндобдж 14 0 объект > эндобдж 5 0 obj > эндобдж 81 0 объект > поток 2007-03-19T12: 41-05: 002007-03-19T12: 40: 55-05: 002007-03-19T12: 41-05: 00application / pdf
Разница между изопропиловым и этиловым спиртом
Разница — изопропиловый спирт и этиловый спирт
Основное различие между изопропиловым и этиловым спиртом заключается в разнице в длине их цепи.
Изопропил и этиловый спирт — два органических соединения. Первичная функциональная группа этих спиртов — группа –ОН. Названия этих спиртов соответствуют количеству содержащихся в них атомов углерода. Этиловый спирт имеет два атома углерода, тогда как изопропиловый спирт имеет три атома углерода.
Основные зоны покрытия
1. Что такое этиловый спирт
— Структура, молекулярная формула, свойства, применение
2. Что такое изопропиловый спирт
— Структура, молекулярная формула, свойства, области применения
3. В чем разница между изопропилом и этиловым спиртом
— Сравнение основных различий
Ключевые термины
2-пропанол, этанол, этиловый спирт, изопропиловый спирт, медицинский спирт
Что такое этиловый спирт
Этиловый спирт, также называемый этанолом , имеет молекулярную формулу CH 3 CH 2 OH.Он имеет два атома углерода, шесть атомов водорода и один кислород. Это бесцветная жидкость с приятным запахом. Кроме того, температура плавления составляет -115 ̊C, а температура кипения составляет 78 C. Этанол хорошо растворяется в воде из-за своей полярности. Поэтому он часто доступен в виде азеотропной смеси с водой. Кроме того, абсолютный этанол относится к этанолу, который на 100% не содержит воды. Еще одним свойством этанола является то, что он легко воспламеняется, поэтому при нагревании в любых экспериментальных целях приходится использовать водяную баню.
Более того, его получают либо путем спиртовой ферментации, либо путем реакции этана с паром. Для получения сахара из растений ферментируют фермент зимазу. Учитывая его использование, во всем мире его обычно используют как опьяняющий напиток. Однако, если уровень этанола в кровотоке превышает 5%, это может вызвать вредные последствия. Эти вредные эффекты включают ухудшение зрения, изменения поведения или потерю сознания. Важно отметить, что этанол — это первичный спирт. Таким образом, группа –ОН присоединена к 1 st углерода цепи.Благодаря этому при окислении он превращается в альдегид. Итак, аналогичный процесс происходит и в печени. Следовательно, этанол в печени превращается в ацетальдегид, что весьма вредно.
В дополнение к вышеупомянутому использованию, он также работает как растворитель для духов, консервант биологических образцов и дезинфицирующее средство в дополнение к его использованию в производстве лаков. Кроме того, это биотопливо, которое часто используют в качестве добавки к бензину.
Рисунок 1: Структурная формула этилового спирта
Что такое изопропиловый спирт
Изопропиловый спирт, также известный как 2-пропанол или медицинский спирт , является изомером пропанола.В его структуре три атома углерода, 8 атомов водорода и один кислород. Его молекулярная формула: CH 3 CHOHCH 3 . Кроме того, это вторичный спирт, так как группа –ОН присоединена к 2 ому атому углерода цепи. Кроме того, при окислении образуется ацетон. Его получают путем непрямой гидратации пропилена и сильнокислотным способом. Судя по их свойствам, его температура плавления составляет -89,5 C, а температура кипения составляет 82,4 C. Будучи полярным соединением, он смешивается с водой.И этот спирт тоже легковоспламеняющаяся жидкость.
Принимая во внимание использование, изопропиловый спирт используется во многих случаях. В больших количествах он используется для производства ацетона. Кроме того, он является хорошим растворителем для натуральных продуктов, таких как масла, воск, пектин, водоросли и десны. Кроме того, это хорошее дезинфицирующее средство; таким образом, используется для лечебных чистящих целей. Из-за его растворяющих свойств и высокой летучести люди хорошо используют его для очистки электрооборудования.
Более того, изопропиловый спирт может быть вредным при проглатывании в достаточных количествах.Проглатывание происходит в основном путем вдыхания. Кратковременное воздействие также может вызвать раздражение глаз и носа и депрессию в центральной нервной системе, вызывая тошноту или потерю сознания.
Рисунок 2: Шариковая модель изопропила
Разница между изопропилом и этиловым спиртом
Молекулярная формула
Изопропил имеет молекулярную формулу CH 3 CHOHCH 3 .
Этиловый спирт имеет молекулярную формулу CH 3 CH 2 OH.
Категория
Изопропил представляет собой вторичный спирт, поскольку -ОН присоединен к 2-му углероду nd .
Этиловый спирт является первичным спиртом, так как -ОН присоединен к 1 st атому углерода.
Физические свойства
Изопропил: Точка кипения -82,4 ̊C и точка плавления -89,5 C.
Этиловый спирт: Температура кипения 78 C и точка плавления -115 C.
Питьевая способность
Изопропил: Непить.
Этиловый спирт: Обычно используется в качестве напитка.
использует
Изопропил: растворитель, дезинфицирующее и чистящее средство .
Этиловый спирт: Растворитель, дезинфицирующее средство, биологический консервант для образцов и т. Д.
Заключение
Разница между изопропиловым спиртом и этиловым спиртом в основном связана с их различной химической структурой — этиловый спирт имеет 2 атома углерода, тогда как изопропиловый спирт имеет 3 атома углерода.Группа -ОН этилового спирта присоединена к первому атому углерода цепи и, следовательно, является первичным спиртом. Напротив, группа –OH изопропилового спирта присоединена ко второму атому углерода и, таким образом, является вторичным спиртом. Кроме того, температуры кипения и плавления спиртов немного различаются. Кроме того, из-за различий в структуре оба спирта после окисления дают разные продукты. Этиловый спирт дает ацетальдегид, тогда как изопропиловый спирт дает ацетон. Это связано с разным положением групп –ОН.Более того, люди употребляют этиловый спирт в качестве напитка, но изопропиловый спирт явно не годится для питья.
Ссылка:
1. «Этанол». Infoplease. N.p., n.d. Интернет. 16 февраля 2017 г.
2. «Изопропанол | (Ch4) 2CHOH. ” Национальный центр биотехнологической информации. Национальная медицинская библиотека США, без даты. Интернет. 16 февраля 2017 г.
3. «Для чего используется изопропанол?» Reference.Com. N.p., n.d. Интернет. 16 февраля 2017 г.
Изображение предоставлено:
1. «Этанол-2D-плоский» Автор Benjah-bmm27 — собственная работа (общественное достояние) через Commons Wikimedia
2.«Пропан-2-ол-3D-шары» Автор Jynto (доклад) — Собственная работа — Этот химический образ был создан с помощью Discovery Studio Visualizer. (CC0) через Commons Wikimedia
Безопасность и качество пищевых продуктов | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

