Пламя: строение, описание, схема, температура
В процессе горения образуется пламя, строение которого обусловлено реагирующими веществами. Его структура поделена на области в зависимости от температурных показателей.
Определение
Пламенем называют газы в раскаленном виде, в которых присутствуют составляющие плазмы или вещества в твердой дисперсной форме. В них осуществляются преобразования физического и химического типа, сопровождающиеся свечением, выделением тепловой энергии и разогревом.
Наличие же в газообразной среде ионных и радикальных частичек характеризует его электрическую проводимость и особое поведение в электромагнитном поле.
Что такое языки пламени
Обычно так называют процессы, связанные с горением. По сравнению с воздухом, газовая плотность меньше, но высокие температурные показатели обуславливают поднятие газа. Так и образуются языки пламени, которые бывают длинными и короткими. Часто происходит и плавный переход одних форм в другие.
Пламя: строение и структура
Для определения внешнего вида описываемого явления достаточно зажечь газовую горелку. Появившееся несветящееся пламя нельзя назвать однородным. Визуально можно выделить три его основные области. Кстати, изучение строения пламени показывает, что различные вещества горят с образованием различного типа факела.
При горении смеси из газа и воздуха вначале происходит формирование короткого факела, цвет которого имеет голубые и фиолетовые оттенки. В нем просматривается ядро — зелено-голубое, напоминающее конус. Рассмотрим это пламя. Строение его разделяется на три зоны:
- Выделяют подготовительную область, в которой происходит нагревание смеси из газа и воздуха при выходе из отверстия горелки.
- За ней следует зона, в которой происходит горение. Она занимает верхушку конуса.
- Когда имеется недостаток воздушного потока, газ сгорает не полностью. Выделяется углерода двухвалентный оксид и водородные остатки. Их догорание протекает в третьей области, где есть кислородный доступ.
Теперь отдельно рассмотрим разные процессы горения.
Горение свечи
Горение свечи подобно горению спички или зажигалки. А строение пламени свечи напоминает раскаленный газовый поток, который вытягивается вверх за счет выталкивающих сил. Процесс начинается с нагревания фитиля, за которым следует испарение парафина.
Самую нижнюю зону, находящуюся внутри и прилегающую к нити, называют первой областью. Она обладает небольшим свечением синего цвета из-за большого количества топлива, но малого объема кислородной смеси. Здесь осуществляется процесс неполного сгорания веществ с выделением угарного газа, который в дальнейшем окисляется.

Первую зону окружает светящаяся вторая оболочка, характеризующая строение пламени свечи. В нее поступает больший кислородный объем, что обуславливает продолжение окислительной реакции с участием топливных молекул. Температурные показатели здесь будут выше, чем в темной зоне, но недостаточные для конечного разложения. Именно в первых двух областях при сильном нагревании капелек несгоревшего топлива и угольных частичек появляется светящийся эффект.
Вторая зона окружена слабозаметной оболочкой с высокими температурными значениями. В нее заходит много кислородных молекул, что способствует полному догоранию топливных частичек. После окисления веществ, в третьей зоне светящийся эффект не наблюдается.
Схематическое изображение
Для наглядности представляем вашему вниманию изображение горения свечи. Схема пламени включает:
- Первую или темную область.
- Вторую светящуюся зону.
- Третью прозрачную оболочку.
Нить свечи не подвергается горению, а только происходит обугливание загнутого конца.

Горение спиртовки
Для химических экспериментов часто используют небольшие резервуары со спиртом. Их называют спиртовками. Фитиль горелки пропитывается залитым через отверстие жидким топливом. Этому способствует давление капиллярное. При достижении свободной верхушки фитиля, спирт начинает испаряться. В парообразном состоянии он поджигается и горит при температуре не более 900 °C.
Пламя спиртовки имеет обычную форму, оно практически бесцветное, с небольшим оттенком голубого. Его зоны не так четко видны, как у свечки.
У спиртовой горелки, названной в честь ученого Бартеля, начало огня располагается над калильной сеткой горелки. Такое заглубление пламени приводит к уменьшению внутреннего темного конуса, а из отверстия выходит средний участок, который считается самым горячим.

Цветовая характеристика
Излучения различных цветов пламени, вызывается электронными переходами. Их еще называют тепловыми. Так, в результате горения углеводородного компонента в воздушной среде, синее пламя обусловлено выделением соединения H-C. А при излучении частичек C-C, факел окрашивается в оранжево-красный цвет.
Трудно рассмотреть строение пламени, химия которого включает соединения воды, углекислого и угарного газа, связь OH. Его языки практически бесцветны, так как вышеуказанные частички при горении выделяют излучения ультрафиолетового и инфракрасного спектра.
Окраска пламени взаимосвязана с температурными показателями, с наличием в нем ионных частиц, которые относятся к определенному эмиссионному или оптическому спектру. Так, горение некоторых элементов приводит к изменению цвета огня в горелке. Отличия в окрашивании факела связаны с расположением элементов в разных группах системы периодической.
Огонь на наличие излучений, относящихся к видимому спектру, изучают спектроскопом. При этом было установлено, что простые вещества из общей подгруппы оказывают и подобное окрашивание пламени. Для наглядности используют горение натрия в качестве теста на данный металл. При внесении его в пламя, языки становятся ярко-желтыми. На основании цветовых характеристик выделяют натриевую линию в эмиссионном спектре.
Для щелочных металлов характерно свойство быстрого возбуждения светового излучения атомарных частиц. При внесении труднолетучих соединений таких элементов в огонь горелки Бунзена происходит его окрашивание.
Спектроскопическое исследование показывает характерные линии в области, видимой для глаза человека. Быстрота возбуждения светового излучения и простое спектральное строение тесно взаимосвязаны с высокой электроположительной характеристикой данных металлов.
Характеристика
В основе классификации пламени лежат следующие характеристики:
- состояние агрегатное сгорающих соединений. Они бывают газообразной, аэродисперсной, твердой и жидкой формы;
- тип излучения, которое может быть бесцветным, светящимся и окрашенным;
- распределительная скорость. Существует быстрое и медленное распространение;
- высота пламени. Строение может быть коротким и длинным;
- характер передвижения реагирующих смесей. Выделяют пульсирующее, ламинарное, турбулентное перемещение;
- визуальное восприятие. Вещества горят с выделением коптящего, цветного или прозрачного пламени;
- температурный показатель. Пламя может быть низкотемпературным, холодным и высокотемпературным.
- состояние фазы топливо – окисляющий реагент.
Возгорание происходит в результате диффузии или при предварительном перемешивании активных компонентов.
Окислительная и восстановительная область
Процесс окисления протекает в слабозаметной зоне. Она самая горячая и располагается вверху. В ней топливные частицы подвергаются полному сгоранию. А наличие в кислородного избытка и горючего недостатка приводит к интенсивному процессу окисления. Этой особенностью следует пользоваться при нагревании предметов над горелкой. Именно поэтому вещество погружают в верхнюю часть пламени. Такое горение протекает намного быстрее.
Восстановительные реакции проходят в центральной и нижней части пламени. Здесь содержится большой запас горючих веществ и малое количество O2 молекул, осуществляющих горение. При внесении в эти области кислородсодержащих соединений осуществляется отщепление O элемента.
В качестве примера восстановительного пламени используют процесс расщепления железа двухвалентного сульфата. При попадании FeSO4 в центральную часть факела горелки, происходит вначале его нагревание, а затем разложение на оксид трехвалентного железа, ангидрид и двуокись серы. В данной реакции наблюдается восстановление S с зарядом от +6 до +4.
Сварочное пламя
Данный вид огня образуется в результате сгорания смеси из газа или пара жидкости с кислородом чистого воздуха.
Примером служит формирование пламени кислородно-ацетиленового. В нем выделяют:
- зону ядра;
- среднюю область восстановления;
- факельную крайнюю зону.
Так горят многие газокислородные смеси. Различия в соотношении ацетилена и окислителя приводят к разному типу пламени. Оно может быть нормального, науглероживающего (ацетиленистого) и окислительного строения.
Теоретически процесс неполного сгорания ацетилена в чистом кислороде можно охарактеризовать следующим уравнением: HCCH + O2 → H2 + CO +CO (для реакции необходима одна моль O2).
Полученный же молекулярный водород и угарный газ реагируют с воздушным кислородом. Конечными продуктами является вода и оксид четырехвалентного углерода. Уравнение выглядит так: CO + CO + H2 + 1½O2 → CO2 + CO2 +H2O. Для этой реакции необходимо 1,5 моля кислорода. При суммировании O2 получается, что 2,5 моль затрачивается на 1 моль HCCH. А так как на практике трудно найти идеально чистый кислород (часто он имеет небольшое загрязнение примесями), то соотношение O2 к HCCH будет 1,10 к 1,20.
Когда значение пропорции кислорода к ацетилену меньше 1,10, возникает науглероживающее пламя. Строение его имеет увеличенное ядро, очертания его становятся расплывчатыми. Из такого огня выделяется копоть, вследствие недостатка кислородных молекул.
Если же соотношение газов больше 1,20, то получается окислительное пламя с кислородным избытком. Лишние его молекулы разрушают атомы железа и другие компоненты стальной горелки. В таком пламени ядерная часть становится короткой и имеет заострения.
Температурные показатели
Каждая зона огня свечи или горелки имеет свои значения, обусловленные поступлением кислородным молекул. Температура открытого пламени в разных его частях колеблется от 300 °C до 1600 °C.
Примером служит пламя диффузионное и ламинарное, которое образовано тремя оболочками. Конус его состоит из темного участка с температурой до 360 °C и недостатком окисляющего вещества. Над ним располагается зона свечения. Ее температурный показатель колеблется от 550 до 850 °C, что способствует разложению термическому горючей смеси и ее горению.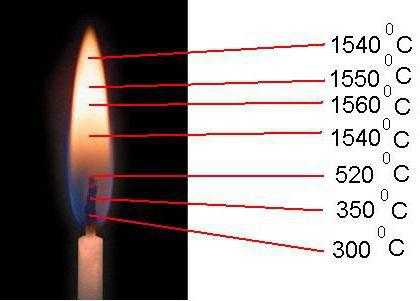
Внешняя область едва заметная. В ней температура пламени доходит до 1560 °C, что обусловлено природными характеристиками топливных молекул и быстротой поступления окисляющего вещества. Здесь горение наиболее энергичное.
Вещества воспламеняются при разных температурных условиях. Так, металлический магний горит только при 2210 °С. Для многих твердых веществ температура пламени около 350 °С. Возгорание спичек и керосина возможно при 800 °С, тогда как древесины – от 850 °С до 950 °С.
Сигарета горит пламенем, температура которого варьируется от 690 до 790 °С, а в пропан-бутановой смеси – от 790 °С до 1960 °С. Бензин воспламеняется при 1350 °С. Пламя горения спирта имеет температуру не более 900 °С.
fb.ru
Температура сгорания элементов в кислороде
| Рис. ХУ-40. Температуры сгорания элементов в кислороде (°К 103). |  |
Термодинамический расчет равновесного состава продуктов сгорания и конверсии. Применяемые в промышленности углеводородные топлива и окислители (воздух или кислород) состоят в основном из углерода С, водорода Н, кислорода О и азота N. Расчеты показывают, что в области умеренно высоких температур (800—1800 °С) при близких к атмосферному давлениях в термодинамически равновесной смеси в заметных количествах могут присутствовать лишь СО2, СО, Н2О, Н2, N2, СН4, О2 (при коэффициенте расхода воздуха ав > 1) и сажистый углерод С (при определенных, достаточно малых значениях ав). Диссоциация Н2О, СО2, а тем более СО, Н2 и N2 при этих температурах еще незаметна, в то время как все углеводороды (кроме СН4) диссоциируют практически нацело. Одновременное присутствие в равновесной смеси заметных количеств горючих элементов и кислорода невозможно при ав 1 — горючих газов.
Натрий довольно широко применяется в качестве теплоносителя в различных энергетических установках. Он обладает достаточно хорошими физическими и теплофизическими свойствами, позволяющими осуществлять интенсивный теплосъем в различных теплообменных аппаратах (теплотворная способность 2180ккал/кг коэффициент теплопроводности, кал (см-с-град), 0,317 при 21 °С и 0,205 при 100 °С). Вместе с тем натрий характеризуется и существенными недостатками. Он обладает высокой химической активностью, благодаря которой он реагирует со многими химическими элементами и соединениями. При его горении выделяется большое количество тепла, что приводит к росту температуры и давления в помещениях. Он обладает большой реакционной способностью [температура горения около 900 °С, температура самовоспламенения в воздухе 330—360 °С, температура самовоспламенения в кислороде 118°С, минимальное содержание кислорода, необходимое для горения, 5 % объема, скорость выгорания 0,7—0,9 кг/ /(м2-мин)]. При сгорании в избытке кислорода образуется перекись NaaOa, которая с легкоокисляющимися веществами (порошками алюминия, серой, углем и др.) реагирует очень энергично, иногда со взрывом. Карбиды щелочных металлов обладают большой химической активностью в атмосфере углекислого и сернистого газов они самовоспламеняются энергично и взаимодействуют с водой со взрывом. Твердая углекислота взрывается с расплавленным натрием при температуре 350 °С. Реакция с водой начинается при температуре —98 °С с выделением водорода. Азотистое соединение NaNa взрывается при температуре, близкой к плавлению. В хлоре и фторе натрий воспламеняется при обычной температуре, с бромом взаимодействует при темпера- [c.115]
Теплота сгорания топлива. Важнейшей характеристикой топлива является теплота сгорания. Теплотой сгорания вещества называют тепловой эффект реакции окисления кислородом элементов, входящих в состав этого вещества до образования высших оксидов. Теплоту сгорания обычно относят к стандартному состоянию (давление 101 кПа), одному молю топлива и температуре 298,15 К и назначают стандартной теплотой сгорания.
Продуктами сгорания называются газообраз- ые, жидкие и твердые вещества, образующиеся в результате процесса горения. Состав их зависит от состава горящего вещества и условий его горения. Органические и неорганические горючие вещества состоят главным образом из углерода, водорода, кислорода, серы, фосфора и азота. Из них углерод, водород, сера и фосфор способны окисляться при горе-иии и образовывать продукты СО2, СО, Н2О, ЗОг и РгОа. Азот при температуре горения не способен окисляться и выделяется в свободном состоянии, а кислород расходуется на окисление горючих элементов вещества. [c.27]
Несколько иной механизм действия органических растворителей в случае комбинированных горелок-распылителей з . Здесь увеличение интенсивности излучения для некоторых металлов доходит до 10-кратного, а увеличение поглощения света (для линии никеля с длиной волны 341,5 ммк) до 36-кратного . При введении в пламя органического растворителя значительно увеличивается объем пламени . Температура пламени снижается на 90—250° С при введении в пламя водных растворов (в отдельных случаях отмечалось снижение до 2600° С для пламени дициан-кислород и до 900° С для кислородно-водородного пламени з). При введении органических растворителей температура пламени снижается меньше. Таким образом, температура пламени при использовании органических растворителей выше, чем при использовании водных растворов (для кислородно-водородного пламени она составляет 2810° С с первыми и 2700° С со вторыми). К этому следует добавить более эффективное использование вещества в капельках аэрозоля за счет теплового эффекта сгорания орх анического растворителя. Все эти факторы следует рассматривать как дополнительно увеличивающие концентрацию атомов определяемого элемента в пламени и их свечение. При введении в пламя смесей водород — кислород или ацетилен — кислород растворов солей и элементов в органических
Детектор по теплоте сгорания (термохимический). Основан на измерении теплового эффекта при сгорании компонентов анализируемой пробы в присутствии катализатора. Катализатором служит платиновое проволочное сопротивление, являющееся одновременно и чувствительным элементом детектора. По конструкции этот детектор во многом аналогичен детектору по теплопроводности. В качестве газа-носителя используются только воздух или кислород, обеспечивающие горение газов. Температура нагревательных элементов достигает 800—900° С. Оба нагревательных элемента являются плечевыми сопротивлениями схемы моста Уитстона. За счет большого выделения тепла происходит большое изменение температуры нити. Отсюда чувствительность этого детектора выше в десятки раз, чем у катарометра. [c.247]
К однокомпонентным топливам относятся вещества, молекула которых содержит в своем составе горючие элементы и необходимый для горения кислород, а также устойчивые смеси (растворы) горючих и окислителей, не вступающих в химическое взаимодействие друг с другом при обычных температурах. Такие топлива при сгорании не нуждаются в подаче окислителя в камеру сгорания. [c.676]
Так как парциальные давления вводимых в пламя соединений определяемых элементов пренебрежимо малы, можно считать, что газовая смесь пламени состоит в основном из соединений, образующихся в ходе реакции горения, и продуктов диссоциации воды. Примерный состав газов пламен наиболее часто употребляемых горючих смесей представлен в табл. 2.2. Как это видно из таблицы, помимо продуктов полного сгорания, т. е. СОг и НгО, в газовой смеси присутствуют СО и продукты диссоциации воды свободный гидроксил ОН, Ог, Нг, О, Н, а также N2, молекулы которого при температуре пламени практически не диссоциируют. Из всех соединений, образуемых ме таллами, при этих температурах наиболее устойчивы молекулы монооксидов типа МеО, а иногда и молекулы типа МеОН. Поэтому в условиях относительно высокой концентрации свободного кислорода и гидроксила образованием молекул других соединений можно пренебречь.
Определение углерода в черных металлах основано на следующем принципе. Пробу анализируемого металла сжигают при высокой температуре в атмосфере кислорода, а полученный при этом СОг определяют с помощью газометрических, весовых или титрометрических методов. Для этого взвешенную пробу тонких металлических стружек или порошка (предварительно очищенных органическим растворителем от возможного загрязнения маслом) помещают в специальную лодочку из высококачественного фарфора, кварца или оксида алюминия. Лодочку вводят в керамическую огнеупорную трубу электрической печи и нагревают до 1200 °С. Через трубу пропускают струю кислорода, предварительно очищенного от следов СОг, восстанавливающих примесей или твердых частиц. Для сталей с высоким содержанием легирующих элементов в лодочку добавляют (менее 0,005%) более легкоплавкие металлы, такие, как медь, свинец или олово, не содержащие углерод. Пропущенный через трубу газ очищается от увлеченных частиц оксидов железа и ЗОз, полученного при сгорании содержащейся в пробе серы. Определить СОг в газе можно различными методами. [c.474]
В расчетах методом суммирования широко используются термодинамические характеристики реакций образования веществ. Свободная энергия образования вещества в стандартных условиях, АРf, представляет собой изменение свободной энергии, происходящее при образовании этого вещества в его обычном состоянии (твердое тело, жидкость или газ) из составляющих элементов, находящихся в стандартном состоянии. За стандартное состояние элемента обычно принимается его наиболее стабильная форма при комнатной температуре. Стандартное состояние углерода — графит, водорода или кислорода — двухатомные газы. Изменение свободной энергии в стандартных условиях можно легко рассчитать, складывая стандартные свободные энергии образования индивидуальных компонентов реакции. Так, например, АР° для сгорания бутадиена (первая реакция в (УП-4) рассчитывается по выражению
Особенно агрессивная локальная коррозия элементов печи наблюдается при сжигании серосодержащего газа. На хромоникелевых сплавах это проявляется при температуре на 100—150°С ниже предела его окалиностойкости, а для сплавов на никелевой основе такие явления наблюдаются при 650—750 °С, если при сжигании топлива создается восстановительная среда. При достаточном избытке кислорода в продуктах сгорания серосодержащего топлива образующиеся сернистые соединения не проявляют агрессивности вплоть до 850 °С. Если же создаются условия восстановительной среды в результате неполного сгорания газа в печи и при наличии в газе SO2, то скорость коррозии резко возрастает (в 6—25 раз). [c.174]
Таким образом, в конце прошлого столетия точка зрения, предполагающая, что пламенное сгорание углеводородов — это процесс непосредственного распада горючего на элементы с последующим их взаимодействием с кислородом, должна была вступить в противоречие с повседневным опытом химиков, наблюдавших внедрение кислорода в молекулу углеводорода без разрыва углеродного скелета. Первым отражением этого противоречия явились прогрессивные для того времени представления Армстронга [4], высказанные им еще в 1874 г. Он предположил, что промежуточные стадии пламенного сгорания углеводородов представляют собой преходящее образование неустойчивых гидроксилированных молекул, получающихся внедрением кислорода в исходную молекулу горючего. Такие окисленные образования способны при высокой температуре распадаться на стабильные кислородсодержащие промежуточные продукты, так что весь процесс может быть изображен как последовательное гидроксилирование углеводорода.
Из неметаллических элементов наиболее тугоплавки углерод и бор, т. е. элементы П1—IV групп с ковалентной связью. К сожалению, не все перечисленные элементы сохраняют достаточный уровень свойств при высоких температурах. Причина тому — состав окружающей среды. Так, например, алмаз, имеющий самую высокую температуру плавления (4200° С) из всех существующих на земле элементов, при отсутствии защитной атмосферы сгорает при 850—1000° С, а в атмосфере кислорода — при 700—850° С. Пленка окисла на молибдене появляется при 250° С, а при температурах выше 700° С окисел начинает так быстро испаряться, что кусок молибдена буквально тает на глазах. Например, молибденовый стержень диаметром 13 мм при 1100° С через 6 ч будет полностью уничтожен . Среди окислов тугоплавких металлов самую меньшую температуру плавления имеет окисел рения. Он плавится при 300° С и кипит при несколько большей температуре. Кроме безвозвратных потерь (окалина и продукты сгорания или испарения), при длительном воздействии высоких температур происходит своего рода химико-термическая обработка поверхностных слоев, газонасыщение с образованием хрупких соединений. [c.215]
Сплавы на никелевой основе используют для изготовления элементов камер сгорания. Эти сплавы проявляют высокую жаростойкость при температурах 1000—1200°С в условиях окисления кислородом (воздух, продукты сгорания природного газа и др.) и подвергаются, как правило, интенсивной коррозии в средах. [c.238]
В ВРД кислород воздуха, используемый для сжигания горючего, в значительной мере разбавлен азотом — балластным элементом, не участвующим в горении. Содержание кислорода в жидких окислителях значительно выше, чем в воздухе, и достигает 75—100% веса окислителя. В связи с этим концентрация химической энергии на единицу веса топлива для ЖРД (горючее — — окислитель) намного больше, чем в реактивных топливах. При сгорании топлива для ЖРД выделяется очень большое количество тепла и достигаются высокие температуры и скорости истечения продуктов сгорания, что обеспечивает получение высоких мощностей двигателя. [c.592]
С увеличением температуры, воздействию которой подвергаются топлива и особенно масла, в составе осадков н отложений все больше обнаруживается соединений, обогащенных гетероатомами, преимущественно кислородом, и углеродом. В застойных зонах двигателя, где не происходит достаточного кислородного обмена, скапливается повышенное количество нагара или продуктов неполного сгорания. В составе этих сажистых плотных образований наряду с большим содержанием углерода обнаруживается значительное количество кислорода, серы, азота, а также зольных элементов. Механизм образования таких обуглероженных соединений мало изучен. Одна из теорий сгорания вещества (капельная) исходит из того, что в зонах с пониженной температурой протекает дегидрогенизация и конденсация свободных радикалов вначале до простых ароматических соеди-ний, а затем до сложных высокомолекулярных соединений с низкой упругостью паров даже при температуре пламени. [c.183]
Проблема охлаждения кислородных двигателей несколько упрощается, если в качестве горючего компонента применяются вещества с повыщенньим содержанием в молекуле водородных атомов. Водород — один из наиболее теплопроизводительныл горючих элементов, но температура сгорания его в атмосфере кислорода гораздо ниже, чем других распространенных горючих. Сгорание водорода в кислороде сопровождается выделением тепла в количестве 3210 ккал/кг при идеальной температуре сгорания 4120°С, а углеродно-кислородное топливо имеет теплопроизводительность 2130 ккал/кг при идеальной температуре сгорания 5950° С. [c.40]
Принципы современной калориметрии. В немногих случаях, например для газообразных НС1, HjO и Oj, можно определить теплоту образования соединения, измеряя тепло, выделяющееся при непосредственном их синтезе из элементов. Однако в большинстве случаев необходимо измерять теплоту тех реакций, для которых известны теплоты образования всех исходных веществ и продуктов реакции, за исключением интересующего нас вещества. Теплоты образования большинства органических соединений получены измерением теплоты, выделяющейся при сжигании в кислороде под давлением в бомбе при постоянном объеме. В случае НС1, как упомянуто выше, возможно измерить теплоту образования из Hj и lj при постоянном давлении около 1 атм», поэтому, если не считать второстепенных поправок, то наблюдаемый тепловой эффект представляет собой непосредственно величину АН образования. С другой стороны, результаты, получаемые при сжигании в бомбе постоянного объема под повышенным давлением, дают изменение внутренней энергии, соответствующее этому давлению эти данные должны быть подвергнуты обработке с помощью весьма тонких методов расчета для получения величины ДН при 1 атм и комнатной температуре [1]. Кроме того, вычисление теплот образования из теплот сгорания требует знания теплот образования HjO, Oj и других соединений, образующихся в бомбе следовательно, если эти термохимические постоянные не будут определены с высокой степенью точности, то и точность вычисляемой теплоты образования будет недостаточной. Надежность определения каждой термохимической величины в значительной мере зависит от методов анализа, применявшихся для определения качественного и количественного состава образовавшихся продуктов. [c.43]
Теьшература и положение второго и третьего элементов печи в течение всего, опыта не меняется. Положение первого элемента печи по отношению к лодочке и его температура определяются в соответствии с данными, приведенными в табл. 7. В процессе сгорания навески угля скорость тока кислорода в поглотительных сосудах резко снижается. В этот период следует усилить подачу кислорода, доводя ее в поглотительной цепи до 1—2 пузырьков в 1 сек. После окончания этого периода вновь устанавливают первоначальную скорость 2—3 пузырька в 1 сек., одинаковую в очистительной и поглотительной цени. [c.40]
Наиболее прямой путь получения сведений об энергиях связи — использование термохимических данных, т. е. сведений о тепловых эффектах реакций. Практически чаще всего эти данные получают в виде теплот сгорания, т. е. теплового эффекта, которым сопровождается полное сгорание органического соединения до оксидов составляющих его элементов (СОг, НгО, SO2), азот, бром и иод выделяются в свободном виде, хлор образует НС1. Сжигание проводят в калориметрах — приборах, состоящих из прочных металлических сосудов для сожжения вещества под давлением кислорода, причем по повышению температуры в специальной водяной рубашке сосуда учитывают количество выделившегося тепла. Полученные данные используют для расчета теплот образования сое-динений из атомов составляющих их элементов от теплот образования переходят к энергиям связей. Так, например, теплота образования метана равна 1660 кДж/моль. Поскольку при образовании метана возникают четыре С—Н-связи, на долю каждой из них приходится энергия 1660 4 = 415 кДж/моль. Разность между теплотами образования двух соседних членов ряда парафинов составляет около 1180 кДж/моль это значение соответствует теплоте образования группы СНг, т. е. созданию дополнительной С—С-связи и двух С—Н-связей. Вычитая из приведенного выше значения энергию двух С—Н-связей, можно получить энергию [c.34]
Малые длины связей между кайносимметричными и немногослойными атомами С позволяют совершаться перекрыванию облаков л-электронов, а потому для химии углерода весьл а характерны кратные связи в отличие от химии кремния. Углерод можно назвать полидесмогеном , т. е. элементом — образователем двойных и тройных связей. Эти связи настолько прочны (этому способствует заметно и энергия корреляции) и вместе с тем в отсутствие катализаторов и высоких температур настолько мало реакционноспособны (достаточно вспомнить необходимость платинового катализатора при гидрировании этиленовых производных), что органическая химия богата мономерами даже среди класса ненасыщенных соединений, молекулы которых могли бы полимеризоваться с разрывом кратных связей, если бы при помощи катализаторов была преодолена их инертность. Напомним, что и молекулы СО для своего сгорания в кислороде требуют катализаторов. Этилен полимеризуется при низких давлениях и температурах лишь в присутствии катализаторов, например, смеси триэтилалюминия и четыреххлористого титана. [c.358]
При иснользовании детектора по теплоте сгорания с платиновой нитью температура чувствительного элемента поддерживается в пределах 700 — 800 С. Как показывают зависимости, приведенные на рис. 5-23, при этой рабочей температуре коэффициент теплопроводности кислорода превышает значение коэффициента теплопроводности воздуха Ядозд, в то время как теплопроводность азота Я меньше Явозд- В связи [c.153]
Воспламенение струи пылевоздушной смеси, вдуваемой в топочную камеру, имеет характер вынужденного воспламенения (иначе зажигания) подобно рассмотренному выше для гомогенной газовоздушной смеои. Начинаясь по периферийной поверхности струи, воспламенение постепенно развивается в глубь ее сечения. Первоначальным источником тепла для зажигания струи пылевоздушной смеси служат эжектируемые ею высокотемпературные топочные газы, окружающие вдуваемую струю. Подмешиваясь к внешним слоям струи, топочные газы доводят их до воспламенения. В свою очередь воспламенившиеся элементы потока иылевоздушной смеси служат источником тепла для дальнейшего развития воспламенения в глубь сечения струи. В итоге при зажигании пылевоздушной струи, подобно тому как это наблюдается в струе газовоздушной, возникает фронт воопламенения. Однако следует отметить весьма существенное различие в развитии этого процесса между газо- и пылевоздушными струями. В первом случае при наличии в смеси достаточного для ее сгорания количества кислорода горение (и тепловыделение) завершается в тонком фронте пламени, разделяющем исходную невоопламененную омесь и продукты горения. Во втором случае горение и тепловыделение, начинаясь по франту воопламенения, значительно растягиваются по времени и в пространстве. Вследствие этого существенно замедляется и развитие высоких температур в зоне воспламенения, а скорость распространения фронта воспламенения резко падает по сравнению с гомогенной газовой смесью. В особенности это относится к твердым топливам, бедным летучими. Сгорание летучих, сосредоточенное в зоне фронта воспламенения, сравнительно быстро повышает температуру воспламеняющейся смеси. При большом выходе летучих развивающаяся от их сгорания температура существенно выше уровня воспламенения [c.27]
Если результаты измерений теплоты сгорания органического соединения, не содержащего иных элементов, кроме углерода, водорода и кислорода, были правильно рассчитаны, то величина Qe представляет собой тепло, выделяющееся при комнатной температуре и постоянном давлении в 1 атм при сгорании в кислороде вещества в форме, стабильной при комнатной температурё, с образованием газо разной углекислоты и жидкой воды. Например, теплота сгорания этилового спирта Qтop. представляет собой величину — ДЯ процесса, изображаемого уравнением [c.46]
Все описанные соотношения справедливы не только для кислородсодержащих соединений. Так, для углеводородов применимы те же соотношения, но число атомов кислорода принимается равным нулю. Для соединений, содержащих серу, азот, фосфор, в уравнении (VI,1) постоянство суммы теплот образования и теплот сгорания сохраняется, но в правую часть уравнения входит новый член, представляющий теплоту сгорания перечисленных элементов (точнее говоря — соответствующих простых веществ). Конечное состояние продуктов сгорания в этом случае принимается иногда условно. Здесь важно лишь, чтобы это состояние было одинаковым конечным состоянием, принятым при определении теплоты сгорания данного соединения. Одинаковыми должны быть и исходные состояния данного элемента в реакции, к которой относится теплота сгорания простого вещества, и в реакции образования рассматриваемого соединения нз простых веществ. Практически это замечание относится главным образом к сере, так как для нее параметры реакций образования и, в частности, теплоту образования -в настоящее время часто относят к исходному состоянию ее в виде газа с двухатомными молекулами, 5г(г). Хотя стандартное состояние такого газа в обычных условиях физически нереализуемо, термодинамически оно определено достаточно хорошо, а использование параметров его в качестве вспомогательных расчетнь1х величин дает возможность при выражении влияния температуры на параметры реакций образования избежать искажающего влия ния изменений агрегатного состояния серы при повышенных температурах. К тому же при сопоставлении серусодержащих соединений с аналогичными кислородными соединениями параметры реакций образования с участием 5г(г), естественно, показывают более закономерные соотношения, чем параметры реакций образования с участием серы ромбической. [c.210]
Термохимический детектор устроен аналогично катарометру, юднако изменение электрического сопротивления нити в нем происходит за счет тепла, выделяющегося при сгорании анализируемых веществ на нагретой до высокой температуры платиновой нити, -являющейся одновременно чувствительным элементом детектора и катализатором реакции горения. Поэтому в качестве материала яити применяется только платина. Термохимический детектор прост ш удобен в обращении, достаточно чувствителен для обычной газовой хроматографии, сравнительно недорог. Однако его применение ограничено анализом только горючих веществ и необходимостью применения воздуха или даже кислорода в качестве газа-носителя. Кроме того, его чувствительность изменяется со временем, а продолжительность работы нити невелика. [c.106]
В свободном состоянии элементы У1В группы — тугоплавкие металлы, вольфрам имеет максимальную для метал.л)н температуру плавления +3387 С. При сгорании металлов на воздухе образуются оксиды СггОз, МоОз и М Оз. 0ста, ьн1,и известные оксиды термически неустойчивы и после прокалмна-ния также переходят в СгдОз и МоОз ( 0з), выделяя либо из-быток кислорода (в случае разложения СгОз, СгОз). либо из-быток металла (для СгО, М0О2), [c.237]
В табл. 1.14 приведена высшая теплотворная способность элементов при взаимодействии их с различными реагентами, отнесенная к единице массы продуктов сгорания. Теплотворная способность элементов при взаимодействии с хлором, азотом (кроме образования ВезН2 и ВЫ), бором, углеродом, кремнием, серой и фосфором значительно меньше теплотворной способности элементов при взаимодействии с кислородом и фтором. Большое разнообразие требований, предъявляемых к процессам горения и реагентам (по температуре, составу, состоянию продуктов сгорания и др.), делает целесообразным использование данных табл. 1.14 при практической разработке топливных смесей того или иного назначения. [c.69]
Наличие в молекуле спиртов атомов кислорода может ра ссматри-ваться как частичное сгорание горючих элементов этих соединений. Поэтому теплота сгорания у спиртов ниже, чем у углеводородов. Вследствие этого при сгорании спиртов развивается меньшая температура, что облегчает создание надежно работающего двигателя. Кроме того, спирты имеют более высокую теплоемкость и скрытую теплоту испарения, чем нефтепродукты (табл. 189). Это обстоятельство, а также высокое относительное содержание спиртов в готовых ТШ1ЛИВНЫХ смесях (до 40—50%) дает возможность с успехом использовать спирты для охлаждения стенок камеры двигателя. Достаточно [c.612]
Одной из наиболее харак гедных особенностей кислорода является его способность соединяться с большинством элементов с выделением, тенла и света. Чтобы вызвать такое соединение, сгорание, часто требуется нагревание до определенной тёвшературы — температуры воспламенения, так как при обычной температуре кислород является довольно инертным веществом. Однако в присутствии влаги медленное соединение с кислородом медленное сгорание) происходит уже при обычных температурах. Важнейшим примером такого процесса является дыхание живых организмов. Но и другие нротекаюш,ие при обычных температурах процессы медленного горения в природе весьма многочисленны (см также стр, 821 и сл.). [c.743]
Этот детектор использует эффект теплоты сгорания компонентов анализируемой пробы в присутствии катализатора — платинового проволочного сопротивления, являющегося одновременно и чувствительным элементом детектора. По конструкции детектор по теплоте сгорания во многом аналогичен детектору по теплопроводности. В качестве газа-носителя может применяться только воздух или кислород, обеспечивающие горение газов. Платиновые проволоки, иногда называемые филаментами, накаливаются до температуры 800—900° С. Они также находятся в сравнительной и измерительной камерах и являются плечевыми сопротивлепиями схемы моста Уитстона. [c.25]
Горючим в ракетных двигателях могут быть те элементы или соединения, которые в сочетании с окислителями обеспечивают высокую теплопроизводительность топливной смеси (не менее 1500—2000 ккал кг). Элементарный фтор и некоторые фторсодержащие соединения отвечают этим требованиям из всех известных элементов, способных быть окислителями, только кислород и фтор образуют топливные смеси с высокой теплопроизводительностью. Здесь показатели фтора как окислителя в сочетании с большинством элементов (за исключением углерода) значительно превосходят показатели кислорода. Это объясняется рядом причин, в частности малым молекулярным весом фтора, низкой энергией диссоциации (38 ккал молъ), экзо-термичностью реакций со многими элементами. Высокая реакционная способность фтора, ведущая к воспламенению в его среде большинства горючих веществ, обусловлена, с одной стороны, малой величиной энергии, требуемой для разрыва связей в его молекуле, а с другой, большим количеством тепла, выделяющегося при образовании связи между атомом фтора и атомом какого-либо другого элемента (например, энергия связи С — Г равна 104 ккал моль), и, следовательно, высокой стабильностью многих соединений фтора. Например, фтористый водород, образующийся при окислении водорода или водородсодержащего горючего фтором, может существовать в молекулярной форме даже при очень высокой температуре. После молекулы азота молекула НГ — одна из самых термически стабильных. Таким образом, продукт сгорания водорода во фторе — фтористый водород—по стойкости к диссоциации и термодинамическим свойствам значительно превосходит [c.35]
В опыте с брикетами на токопроводящей графитовой основе при отсутствии в газовой среде кислорода продолжительное обыскрива-ние ведет к снижению аналитического сигнала. Это обстоятельство объясняется неблагоприятными условиями для сгорания графита как основы и затруднением выхода частиц в облако разряда. Другим фактором, объясняющим это снижение, являются процессы кар-бидообразования, поскольку наиболее ярко оно проявляется для РЗЭ и других элементов, склонных к карбидообразованию,— циркония, титана. Термодинамические исследования [8] возможных химических реакций для РЗЭ при температурах процессов выше 2000°С подтверждают высказанную точку зрения. [c.39]
Основным топочным процессом, идущим и в камере сгорания газовой турбины, является процесс окисления горючего в среде кислорода воздуха. При этом развиваются довольно значительные температуры факела (порядка 1500—1600°С). В химическом смысле можно сказать, что процесс горения приводит к полной минерализации вещества, так как продуктами сгорания являются простейшие окислы СОг, НгО и т. д. Агрессивные элементы также окисляются сера до 50г и частично до 80з ванадий до высшего окисла УгОб. Таким образом, в камере сгорания происходит окисление с получением из сложных молекул исходного маэута простых окислов. [c.33]
Все описанные соотношения справедливы не только для кисло-родсодержаших соединений. Так, для углеводородов применимы те же соотношения, но число атомов кислорода принимается равным нулю. Для соединений, содержащих серу, азот, фосфор, в уравнении (VI, 1) постоянство суммы теплот образования и теплот сгорания сохраняется, но в правую часть уравнения входит новый член, представляющий теплоту сгорания перечисленных элементов (точнее говоря — соответствующих простых веществ). Конечное состояние продуктов сгорания в этом случае принимается иногда условно. Здесь важно лишь, чтобы это состояние было одинаковым конечным состоянием, принятым при определени-и теплоты сгорания данного соединения. Одинаковыми должны быть и исходные состояния данного элемента в реакции, к которой относится теплота сгорания простого вещества, и в реакции образования рас-, сматриваемого соединения из простых веществ. Практически это замечание относится главным образом к сере, так как для нее па- раметры реакций образования и, в частности, теплоту образования в настоящее время часто относят к исходному состоянию ее в виде газа -с двухатомными молекулами, 5г(г). Хотя стандартное состояние такого газа в обычных условиях физически нереализуемо, термодинамически оно определено достаточно хорошо, а использование параметров его в качестве вспомогательных расчетных величин дает возможность при выражении влияния температуры [c.213]
За исключением газов VIH группы, все элементы соединяются с кислородом экзотермически, но лишь некоторые из них можно резать струей кислорода. Данные о способности ряда чистых металлов разрезаться кислородом приведены в табл. VIII.2. Тот факт, что образующаяся при сгорании окись имеет иногда более низкую температуру плавления, чем основной металл (см. табл. VIII.2), не может дать исчерпывающего объяснения способности данного элемента поддаваться резке, хотя этот критерий наиболее часто используется [3] для объяснения поведения железных сплавов при резке. [c.600]
Случай (а)—недостаток кислорода. При расчете исходят из 1 г топлива, содержащего (С), (Н), (N) и (О) грамматомов соответствующих элементов. Теплоту образования твердого метательного вещества принимают равной к. Ставится задача рассчитать состав продуктов реакции, образующихся при температуре и общем давлении Р . При наличии каких-либо неорганических элементов определяют сначала их продукты сгорания и вычитают необходимое количество грамматомов из исходного числа грамматомов различных элементов. [c.27]
chem21.info
Обогреватель, не сжигающий кислород: правильный выбор для дома
Сжечь кислород невозможно. Горение – окисление веществ с повышенной скоростью под действием воздуха. Воздух — кислород на 20%. Азот (остальные 80%) не окисляется при нормальных условиях. Кислород не горит, но пыль на спирали нагревательного элемента может сгорать. Этот запах слышится при включении не работавшего прибора. Частички, постоянно витающие в воздухе, станут сгорать при высокой температуре. Обогреватель, не сжигающий кислород, работает по-особому. Посмотрим, что имеется в виду!
Почему «горит» спираль
Не измерялось, при какой температуре в точности начинается горение пыли. Из опыта видно, что подошва утюга неспособна воспламенить пыль, а спираль это делает. Потому при включении стареньких моделей утюгов слышится неприятный запах. Внутри оседает пыль, загорающаяся при включении. Считается, чем ниже температура нагревательного элемента, тем меньше жжет прибор воздух.
Окисляются пыль и материал спирали. Порой прибор перегорает. Это заметили, появились технологии, ограничивающие доступ воздуха к поверхности. К примеру, нашумевшее керамическое покрытие выполняет одновременно две функции:
- Снижает наружную температуру спирали.
- Защищает нихром от контакта с кислородом.
Температура уменьшается, так как площадь поверхности элемента становится больше. Керамика в качестве покрытия выбрана в силу двух особенностей:
- Инертность.
- Жаропрочность.
- Дешевизна.
- Доступность.
- Простота изготовления.
Материал, получаемый при температуре 1200 ºС (порой выше), не боится 300 ºС, встречающихся в типичном обогревателе. Одновременно керамическое покрытие гладкое, мало подвержено оседанию пыли в сравнении с металлом. Обогреватель, не сжигающий кислород, снабжается защитным покрытием из керамического материала.
Найден альтернативный способ защиты — воздушные фильтры. Приспособления уже применяются в керамических обогревателях (ветродувках) и конвекторах. В результате воздух на входе очищается от механических загрязнений, от запахов и микробов. Так функционируют конвекторные обогреватели Электролюкс Air Gate. В созданные Ворота проходит чистый воздух, не оставляющий на нагревательном элементе следа.
Эффект сжигания кислорода
Пользователи замечали, что масляный обогреватель после включения вызывает эффект духоты. Становится трудно дышать. Ситуацию тоже причислили к явлению сжигания кислорода, хотя процесс близко не стоит с химическими реакциями. На деле начинает стремительно понижаться влажность воздуха. Это физиологически чувствуется как удушье. Нормальная влажность в помещении укладывается в диапазон 40 — 60%. В противном случае человеку некомфортно. В случае нагревания влажность опускается ниже 40%.
Вдобавок подобные эффекты вызывают постепенное снижение иммунитета, что приводит к резкому росту заболеваемости. Врачи советуют поддерживать в комнате естественный режим:
- температуру 20 ºС;
- влажность в пределах 40 — 60%.
Это возвращает человеку нормальное самочувствие, поднимает иммунитет, блокирует размножение большинства грибков и вирусов. Для паразитов создаются неприемлемые условия – слишком холодно. И влажность не подходит. Обогреватель для детской комнаты не ухудшает микроклимат.
Эффект высушивания воздуха получается из-за повышения температуры. Молекулы пара приобретают энергии, чтобы покинуть помещение через бетонные плиты. Стены дышат, слой пароизоляции не блокирует проникновение воды напрочь. Просто процесс обмена пара с окружающей средой сильно замедляется. Придавая молекулам дополнительную энергию, заставляем жидкость стремительно покидать комнату. На этом основывается привычка размещения вещи на батарее для сушки. В последнем случае процесс очевиден.
При повышении температуры концентрация пара снижается. Масляные обогреватели ругают за нежелательный эффект. Чем выше температура и больше площадь, тем сильнее прибор сушит воздух. У масляного обогревателя оба критерия в сумме дают максимум, отсюда и мнение, что жжет кислород. Правдоподобности добавляет запах гари, витающий вокруг. Инфракрасное излучение прогревает стены, потолок, пол. Отсутствие движения воздуха создает благоприятные условия для осаждения паров на поверхность бетона, способствуя проникновению влаги в поры плит, кирпича.
Меры устранения сжигания кислорода нагревателем
Уже назвали косвенно два условия, когда обогреватель жжет кислород:
- Малая площадь рабочего элемента.
- Высокая температура.

На указанные два параметра направлено противодействие сжиганию кислорода.
- К примеру, в ламповых инфракрасных обогревателях стекло прозрачно для рабочего диапазона, не греется слишком сильно, вдобавок площадь мала. 90% энергии уходит в виде излучения и не трогает пыль. Однако лампу требуется периодически обмахивать щеткой, иначе гарь не отступит.
- Гораздо дальше идут пленочные инфракрасные обогреватели систем Теплый пол и Теплый потолок. Греются до 60 ºС. При такой температуре кислород не сгорает, воздух сушится гораздо меньше. Пленочные обогреватели ПЛЭН не пропускают пар, применяются совместно с ПЕНОФОЛ, который является изолятором тепла. Получается, через потолок молекулы воды уже не пройдут.
- В керамических обогревателях ТЭН покрывается защитным слоем.
- В конвекторах увеличивается площадь нагревательного элемента при снижении температуры, но с ухищрением: применяется специальное покрытие, отталкивающее пыль. Это увеличивает КПД, устраняет запах гари.
- Настенные инфракрасные обогреватели в виде плит из камня и тканых панно не горячие, не вызывают значительных эффектов в осушении и сжигании воздуха.
Чтобы избежать осушения воздуха часто в обогреватели добавляют функции увлажнения. Это позволит удержать параметры микроклимата на нормальном уровне. Микробы убиваются ионизатором или ультрафиолетовым излучением. Подобные приборы выпускает шведская фирма Timberk.

Какие обогреватели не жгут кислород
Поговорим, какие обогреватели не сжигают кислород.
Конвекторы
Лучшими считают конвекторы. Добавим, что полезны обогреватели фирмы Электролюкс, снабжённые специальными фильтрами. Timberk выпускает конвекторы с увлажнителями в виде дополнительной опции. Это нормализует микроклимат, больше подходит для юга России, чем для средней полосы, заросшей лесами.
Инфракрасные обогреватели
Хвалят электрические инфракрасные обогреватели потолочного типа. Создаются двух разновидностей:
- Ламповые.
- Керамические.
Первые не отличаются от ламп дневного света. Внутри за решеткой находится длинная стеклянная колба со спиралью. По науке перед работой указанного обогревателя нужно смахнуть пыль с лампы и рефлектора, на практике это делается реже, процесс затрудняется решеткой.
На этом фоне керамические инфракрасные обогреватели смотрятся выгоднее. Напоминают лампы дневного света, вместо решеток защитные панели, но не стекло. Гладкая поверхность представляет сталь, покрытую керамикой. Конструкция ведет себя по свойствам как абсолютно черное тело. Максимум излучения приходится на инфракрасный диапазон. К указанному классу относятся изделия Пион, Билюкс и Иколайн.
Газовые инфракрасные обогреватели для помещений являются неплохим решением. К примеру, камины, работающие по инфракрасному принципу. Внутри за жаропрочным стеклом горит пламя, докрасна разогревая керамическую решетку. Начинается излучение тепла. Газ подводится снаружи, придется пробурить стену под желтую трубу, вдобавок требуется забрать с улицы воздух и выбросить продукты сгорания. Это требует наличия дополнительного отверстия под коаксиал. Это двойная труба – певая внутри второй. Подобный прием позволит обойтись единсвтенной дырой в стене (вместе с желтой трубой получается две).
Подумайте, стоит ли так стараться, только чтобы получить хороший камин. Это дорогое устройство, красивое. Газовый камин называют прибором, обладающим декоративным эффектом и работоспособным в качестве нагревателя.
Для справки. Электрокамины являются устройствами, имитирующими горение очага и не дающими тепла. В лучшем случае внутри спрятана спираль с вентилятором. В наличии маломощная ветродувка. Огромные деньги, уплаченные за оборудование, отдаются за внешнее оформление и спецэффекты.
Имеются газовые конвекторы, не слишком сильно сушат воздух, однако по красоте (и цене) уступают каминам, а дыры в стене все равно делать придется. Если уж задумались о вопросах климата, не стоит брать модели. Обратите внимание, что избранные газовые камины с баллоном забирают воздух из помещения и выкидывают обратно. Такие обогреватели жгут и сушат воздух. Однако! При сгорании газа образуется водяной пар, потери восполняются. Вдобавок образуется четырехвалентный оксид серы, образуя во влажном воздухе серную кислоту. Подобные приборы хороши на даче, на природе, куда выезжает толпа людей повеселиться и отдохнуть.
vashtehnik.ru
Химические свойства кислорода
Кислород вступает в соединения почти со всеми элементами периодической системы Менделеева.
Реакция соединения любого вещества с кислородом называется окислением.
Большинство таких реакций идет с выделением тепла. Если при реакции окисления одновременно с теплом выделяется свет, ее называют горением. Однако не всегда удается заметить выделяющиеся тепло и свет, так как в некоторых случаях окисление идет чрезвычайно медленно. Заметить тепловыделение удается тогда, когда реакция окисления происходит быстро.
В результате любого окисления — быстрого или медленного — в большинстве случаев образуются окислы: соединения металлов, углерода, серы, фосфора и других элементов с кислородом.
Вам, вероятно, не раз приходилось видеть, как перекрывают железные крыши. Перед тем как покрыть их новым железом, старое сбрасывают вниз. На землю вместе с железом падает бурая чешуя — ржавчина. Это гидрат окиси железа, который медленно, в течение нескольких лет, образовывался на железе под действием кислорода, влаги и углекислого газа.
Ржавчину можно рассматривать как соединение окиси железа с молекулой воды. Она имеет рыхлую структуру и не предохраняет железо от разрушения.
Для предохранения железа от разрушения — коррозии — его обычно покрывают краской или другими коррозионно устойчивыми материалами: цинком, хромом, никелем и другими металлами. Предохранительные свойства этих металлов, как и алюминия, основаны на том, что они покрываются тонкой устойчивой пленкой своих окислов, предохраняющих покрытие от дальнейшего разрушения.
Предохранительные покрытия значительно замедляют процесс окисления металла.
В природе постоянно происходят процессы медленного окисления, сходные с горением.
При гниении дерева, соломы, листьев и других органических веществ происходят процессы окисления углерода, входящего в состав этих веществ. Тепло при этом выделяется чрезвычайно медленно, и поэтому обычно оно остается незамеченным.
Но иногда такого рода окислительные процессы сами по себе ускоряются и переходят в горение.
Самовозгорание можно наблюдать в стоге мокрого сена.
Быстрое окисление с выделением большого количества тепла и света можно наблюдать не только при горении дерева, керосина, свечи, масла и других горючих материалов, содержащих углерод, но и при горении железа.
Налейте в банку немного воды и наполните ее кислородом. Затем внесите в банку железную спираль, на конце которой укреплена тлеющая лучинка. Лучинка, а за ней и спираль загорятся ярким пламенем, разбрасывая во все стороны звездообразные искры.
Это идет процесс быстрого окисления железа кислородом. Он начался при высокой температуре, которую дала горящая лучинка, и продолжается до полного сгорания спирали за счет тепла, выделяющегося при горении железа.
Тепла этого так много, что образующиеся при горении частицы окисленного железа накаляются добела, ярко освещая банку.
Состав окалины, образовавшейся при горении железа, несколько иной, чем состав окисла, образовавшегося в виде ржавчины при медленном окислении железа на воздухе в присутствии влаги.
В первом случае окисление идет до закиси-окиси железа (Fe3O4), входящей в состав магнитного железняка; во втором — образуется окисел, близко напоминающий бурый железняк, который имеет формулу 2Fe2O3 ∙ Н2O.
Таким образом, в зависимости от условий, в которых протекает окисление, образуются различные окислы, отличающиеся друг от друга содержанием кислорода.
Так, например, углерод в соединении с кислородом дает два окисла — окись и двуокись углерода. При недостатке кислорода происходит неполное сгорание углерода с образованием окиси углерода (СО), которую в общежитии называют угарным газом. При полном сгорании образуется двуокись углерода, или углекислый газ (СO2).
Фосфор, сгорая в условиях недостатка кислорода, образует фосфористый ангидрид (Р2O3), а при избытке — фосфорный ангидрид (Р2O5). Сера в различных условиях горения также может дать сернистый (SO2) или серный (SO3) ангидрид.
В чистом кислороде горение и другие реакции окисления идут быстрее и доходят до конца.
Почему же в кислороде горение идет энергичнее, чем в воздухе?
Обладает ли чистый кислород какими-то особыми свойствами, которых нет у кислорода воздуха? Конечно, нет. И в том и в другом случае мы имеем один и тот же кислород, с одинаковыми свойствами. Только в воздухе кислорода содержится в 5 раз меньше, чем в таком же объеме чистого кислорода, и, кроме того, в воздухе кислород перемешан с большими количествами азота, который не только сам не горит, но и не поддерживает горение. Поэтому, если непосредственно около пламени кислород воздуха уже израсходован, то другой его порции необходимо пробиваться через азот и продукты горения. Следовательно, более энергичное горение в атмосфере кислорода можно объяснить более быстрой подачей его к месту горения. При этом процесс соединения кислорода с горящим веществом идет энергичнее и тепла выделяется больше. Чем больше в единицу времени подается к горящему веществу кислорода, тем пламя ярче, тем температура выше и тем сильнее идет горение.
А горит ли сам кислород?
Возьмите цилиндр и опрокиньте его вверх дном. Подведите под цилиндр трубку с водородом. Так как водород легче воздуха, он полностью заполнит цилиндр.
Зажгите водород около открытой части цилиндра и введите в него сквозь пламя стеклянную трубку, через которую вытекает газообразный кислород. Около конца трубки вспыхнет огонь, который будет спокойно гореть внутри цилиндра, наполненного водородом. Это горит не кислород, а водород в присутствии небольшого количества кислорода, выходящего из трубки.
Что же образуется в результате горения водорода? Какой при этом получается окисел?
Водород окисляется до воды. Действительно, на стенках цилиндра постепенно начинают осаждаться капельки конденсированных паров воды. На окисление 2 молекул водорода идет 1 молекула кислорода, и образуются 2 молекулы воды (2Н2 + O2 → 2Н2O).
Если кислород вытекает из трубки медленно, он весь сгорает в атмосфере водорода, и опыт проходит спокойно.
Стоит только увеличить подачу кислорода настолько, что он не успеет сгореть полностью, часть его уйдет за пределы пламени, где образуются очаги смеси водорода с кислородом, появятся отдельные мелкие вспышки, похожие на взрывы.
Смесь кислорода с водородом — это гремучий газ. Если поджечь гремучий газ, произойдет сильный взрыв: при соединении кислорода с водородом получается вода и развивается высокая температура. Пары воды и окружающие газы сильно расширяются, создается большое давление, при котором может легко разорваться не только стеклянный цилиндр, но и более прочный сосуд. Поэтому работа с гремучей смесью требует особой осторожности.
Кислород обладает еще одним интересным свойством. Он вступает в соединение с некоторыми элементами, образуя перекисные соединения.
Приведем характерный пример. Водород, как известно, одновалентен, кислород двухвалентен: 2 атома водорода могут соединиться с 1 атомом кислорода. При этом получается вода. Строение молекулы воды обычно изображают Н — О — Н. Если к молекуле воды присоединить еще 1 атом кислорода, то образуется перекись водорода, формула которой Н2O2.
Куда же входит второй атом кислорода в этом соединении и какими связями он удерживается? Второй атом кислорода как бы разрывает связь первого с одним из атомов водорода и становится между ними, образуя при этом соединение Н—О—О—Н. Такое же строение имеет перекись натрия (Na—О—О—Na), перекись бария.
Характерным для перекисных соединений является наличие 2 атомов кислорода, связанных между собой одной валентностью. Поэтому 2 атома водорода, 2 атома натрия или 1 атом бария могут присоединить к себе не 1 атом кислорода с двумя валентностями (—О—), а 2 атома, у которых в результате связи между собой также остается только две свободные валентности (—О—О—).
Перекись водорода можно получить действием разбавленной серной кислоты на перекись натрия (Na2O2) или перекись бария (ВаO2). Удобнее пользоваться перекисью бария, так как при действии на нее серной кислотой образуется нерастворимый осадок сернокислого бария, от которого перекись водорода легко отделить путем фильтрования (ВаO2 + H2SO4 → BaSO4 + Н2O2).
Перекись водорода, как и озон, — соединение неустойчивое и разлагается на воду и атом кислорода который в момент выделения обладает большой окислительной способностью. При низких температурах и в темноте разложение перекиси водорода идет медленно. А при нагревании и на свету оно происходит значительно быстрее. Песок, порошок двуокиси марганца, серебра или платины также ускоряют разложение перекиси водорода, а сами при этом остаются без изменения. Вещества, которые только влияют на скорость химической реакции, а сами остаются неизмененными, называются катализаторами.
Если налить немного перекиси водорода в склянку, на дне которой находится катализатор — порошок двуокиси марганца, разложение перекиси водорода пойдет с такой быстротой, что можно будет заметить выделение пузырьков кислорода.
Способностью окислять различные соединения обладает не только газообразный кислород, но и некоторые соединения, в состав которых он входит.
Хорошим окислителем является перекись водорода. Она обесцвечивает различные красители и поэтому применяется в технике для отбеливания шелка, меха и других изделий.
Способность перекиси водорода убивать различные микробы позволяет применять ее как дезинфицирующее средство. Перекись водорода употребляется для промывания ран, полоскания горла и в зубоврачебной практике.
Сильными окислительными свойствами обладает азотная кислота (HNO3). Если в азотную кислоту добавить каплю скипидара, образуется яркая вспышка: углерод и водород, входящие в состав скипидара, бурно окислятся с выделением большого количества тепла.
Бумага и ткани, смоченные азотной кислотой, быстро разрушаются. Органические вещества, из которых сделаны эти материалы, окисляются азотной кислотой и теряют свои свойства. Если смоченную азотной кислотой бумагу или ткань нагреть, процесс окисления ускорится настолько, что может произойти вспышка.
Азотная кислота окисляет не только органические соединения, но и некоторые металлы. Медь при действии на нее концентрированной азотной кислотой окисляется сначала до окиси меди, выделяя из азотной кислоты двуокись азота, а затем окись меди переходит в азотнокислую соль меди.
Не только азотная кислота, но и некоторые ее соли обладают сильными окислительными свойствами.
Азотнокислые соли калия, натрия, кальция и аммония, которые в технике получили название селитры, при нагревании разлагаются, выделяя кислород. При высокой температуре в расплавленной селитре тлеющий уголек сгорает так энергично, что появляется яркобелый свет. Если же в пробирку с расплавленной селитрой вместе с тлеющим угольком бросить кусочек серы, горение пойдет с такой интенсивностью и температура повысится настолько, что стекло начнет плавиться. Эти свойства селитры давно были известны человеку; он воспользовался этими свойствами для приготовления пороха.
Черный, или дымный, порох приготовляется из селитры, угля и серы. В этой смеси уголь и сера являются горючими материалами. Сгорая, они переходят в газообразный углекислый газ (СO2) и твердый сернистый калий (K2S). Селитра, разлагаясь, выделяет большое количество кислорода и газообразный азот. Выделившийся кислород усиливает горение угля и серы.
В результате горения развивается такая высокая температура, что образовавшиеся газы могли бы расшириться до объема, который в 2000 раз больше объема взятого пороха. Но стенки замкнутого сосуда, где обычно производят сжигание пороха, не позволяют газам легко и свободно расширяться. Создается огромное давление, которое разрывает сосуд в его наиболее слабом месте. Раздается оглушительный взрыв, газы с шумом вырываются наружу, унося с собой в виде дыма размельченные частицы твердого вещества.
Так из калийной селитры, угля и серы образуется смесь, обладающая огромной разрушительной силой.
К соединениям с сильными окислительными свойствами относятся и соли кислородосодержащих кислот хлора. Бертолетова соль при нагревании распадается на хлористый калий и атомарный кислород.
Еще легче, чем бертолетова соль, отдает свой кислород хлорная, или белильная, известь. Белильной известью отбеливают хлопок, лен, бумагу и другие материалы. Хлорная известь употребляется и как средство против отравляющих веществ: отравляющие вещества, как и многие другие сложные соединения, разрушаются под действием сильных окислителей.
Окислительные свойства кислорода, его способность легко вступать в соединение с различными элементами и энергично поддерживать горение, развивая при этом высокую температуру, уже давно обратили на себя внимание ученых различных областей науки. Особенно этим заинтересовались химики и металлурги. Но использование кислорода было ограничено, так как не было простого и дешевого способа получения его из воздуха и воды.
На помощь химикам и металлургам пришли физики. Они нашли очень удобный способ выделения кислорода из воздуха, а физико-химики научились получать его в огромных количествах из воды.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
www.activestudy.info
Краткие сведения о кислороде, пропан-бутане и ацетилене
Кислород — это газ без вкуса, запаха и цвета, не горючий, но активно поддерживает горение, немного тяжелее воздуха. При нормальном атмосферном давлении (760 мм ртутного столба) при температуре 0° С масса 1 м куб. кислорода равна 1.43 кг, а при нормальном атмосферном давлении и температуре 20° С, масса 1 м куб. кислорода равна 1.33 кг, масса 1 м куб воздуха равна 1.29 кг.
Кислород — это газ без вкуса, запаха и цвета, не горючий, но активно поддерживает горение, немного тяжелее воздуха. При нормальном атмосферном давлении (760 мм ртутного столба) при температуре 0° С масса 1 м куб. кислорода равна 1.43 кг, а при нормальном атмосферном давлении и температуре 20° С, масса 1 м куб. кислорода равна 1.33 кг, масса 1 м куб воздуха равна 1.29 кг.
В промышленности кислород получают из атмосферного воздуха методом глубокого охлаждения и ректификации.
Технический кислород для газопламенных работ получают в специальных установках из атмосферного воздуха в жидком состоянии. Жидкий кислород — это легко подвижная, голубоватая жидкость. Температура кипения (начало испарения) жидкого кислорода минус 183° С.
При нормальных условиях и температуре минус 183° С. легко испаряется, превращаясь в газообразное состояние. При повышении температуры интенсивность испарении увеличивается. Из 1 литра жидкого кислорода, образуется около 860 литров газообразного.
Кислород обладает большой химической активностью. Реакция соединения его с маслами, жирами, угольной пылью, ворсинками ткани и т.д., приводит их к мгновенному окислению, самовоспламенению и взрыву при обычных температурах.
Кислород в смеси с горючими газами и парами горючих жидкостей образует в широких пределах взрывчатые смеси.
«Кислород газообразный технический» согласно ГОСТ 5583- 78 выпускается для сварки и резки трех сортов: 1-й — чистотой не менее 99,7%, 2-й — не менее 99,5%, 3-й — не менее 99,2% по объёму. Чем меньше в кислороде газовых примесей, тем выше скорость реза, чище кромки и меньше расход кислорода. На предприятие поставляется в газообразном состоянии, в стальных кислородных баллонах «голубого» цвета ёмкостью 40 дм. куб. и давлением 150 кгс/см2. Сжатый кислород хранят и транспортируют в баллонах по ГОСТ 949-73.
Пропан — технический, бесцветный газ с резким запахом, состоящий из пропана С3Н8 или из пропана и пропилена С3Н6, суммарное содержание которых должно быть не менее 93%. Получают пропан при переработке нефтепродуктов. Пропанобутановая смесь – это смесь газов главным образом технического пропана и бутана. Эти газы относятся к группе тяжёлых углеводородов. Сырьём для их получения являются природные нефтяные газы, отходящие газы нефтеперерабатывающих заводов. Эти газы в чистом виде или в виде смесей при нормальной температуре и на большом повышении давления могут быть переведены из газообразного состояния в жидкое состояние.Хранится и транспортируется пропанобутановая смесь в жидком состоянии, а используется в газообразном.
Газообразная пропанобутановая смесь — это горючий газ без вкуса, запаха и цвета, тяжелее воздуха в 2 раза, поэтому при утечке газа он не рассеивается в атмосфере, а опускается вниз и заполняет углубления пола или местности.
При содержании газа пропан-бутана в воздухе или кислороде до нижнего предела взрываемости и внесении открытого огня происходит горение газа вокруг источника открытого огня.
При содержании газа пропан-бутана в воздухе или кислороде свыше нижнего предела взрываемости и внесении открытого огня или искры происходит пожар, т.е. интенсивное горение газа.
Газообразная пропанобутановая смесь при атмосферном давлении не обладает токсичным (отравляющим) воздействием на организм человека, так как мало растворяется в крови. Но, попадая в воздух, смешивается с ним, вытесняет и уменьшает содержание кислорода в воздухе. Человек, находящийся, а такой атмосфере испытывает кислородное голодание, а при значительных концентрациях газа в воздухе может погибнуть от удушья.
Предельно допустимая концентрация пропан-бутана в воздухе рабочей зоны должна быть не более 300 мг/м3(в пересчёте на углерод).При попадании жидкого пропан-бутана на кожные покровы тела, нормальная температура которого 36,6 град. С, происходит быстрое его испарение и интенсивный отбор тепла с поверхности тела, затем наступает обморожение.
По ГОСТ 20448-80 промышленность выпускает пропанобутановую смесь 3 марок:
- пропан технический, с содержанием пропана более 93%, бутана — менее 3 процентов;
- бутан технический, с содержанием бутана менее 93%, пропана не более 4 процентов;
- пропанобутановая смесь, 2-х типов: зимняя и летняя.
На предприятия для газопламенной обработки металлов поставляется пропанобутановая смесь в стальных баллонах зимняя и летняя.
Зимняя пропанобутановая смесь содержит 15% пропана, 25% бутана и прочих компонентов.
Летняя пропанобутановая смесь содержит 60% бутана, 40% пропана и прочих компонентов.
Для сжигания I куб. м газообразной пропано-бутановой смеси требуется 25-27 куб. м воздуха или 3,58 — 3,63 кг кислорода.
Температура воспламенения с воздухом:
- пропана — 510 град. С;
- бутана — 540 град. С
Температура воспламенения пропанобутановой смеси:
- с воздухом 490-510 град. С;
- с кислородом — 465-480 град. С.
Температура пламени пропанобутановой смеси с кислородом зависит от её состава и равна 2200-2680 град. С. При окислительном пламени (избыток кислорода) температура повышается.
Теплотворная способность пропанобутановой смеси равна 93000 Дж/м куб. (22000 ккал/м куб.).
Скорость горения пропанобутановой смеси:
- при обычном горении 0,8 – 1,5 м/сек.;
- при дистанционном (со взрывом) 1,5 — 3,5 км/сек.
Пределы взрывоопасности пропан-бутана при нормальном давлении составляют:
- в смеси с воздухом:
- нижний – 1,5%;
- верхний – 9,5%.нижний – 2%;
- в смеси с кислородом:
- верхний – 46%.
Пропанобутановые смеси в жидком виде разрушают резину, поэтому необходимо тщательно следить за резиновыми изделиями, применяемыми в газопламенной аппаратуре, и в случае необходимости производить их своевременную замену.
Наибольшая опасность разрушения резины существует зимой, вследствие большей вероятности попадания жидкой фазы пропанобутановой смеси в рукава.
Ацетилен — это горючий газ, без цвета, вкуса, с резким специфическим чесночным запахом, он легче воздуха. Его плотность по отношению к воздуху 0,9.
При нормальном атмосферном давлении (760 мм ртутного столба) и температуре плюс 20 град. С 1 м куб. имеет массу 1,09 кг, воздух 1,20 кг.
При нормальном атмосферном давлении и температуре от — 82,4 градуса до — 84 градусов С ацетилен переходит из газообразного в жидкое состояние, а при температуре минус 85 град. С затвердевает.
Ацетилен — единственный широко применяемый в промышленности газ, горение и взрыв которого возможны в отсутствии кислорода или других окислителей.
При газопламенной обработке металлов ацетилен используют либо в газообразном состоянии, получая его в передвижных или стационарных ацетиленовых генераторах, либо растворённым в ацетиленовых баллонах. Растворенный ацетилен по ГОСТ 5457-75 представляет собой раствор газообразного ацетилена в ацетоне, распределённый в пористом наполнителе под давлением до 1,9 МПА (19 кгс/см2). В качестве пористых наполнителей используются насыпные – берёзовый активированный уголь (БАЦ) и литые пористые массы.
Основным сырьём для получения ацетилена является карбид кальция. Это твёрдое вещество тёмно-серого или коричневатого цвета. Ацетилен получается в результате разложения (гидролиза) кусков, карбида кальция водой. Выход ацетилена на 1 кг карбида кальция составляет 250 дм куб. Для разложения 1 кг карбида кальция требуется от 5 до 20 дм куб. воды. Карбид кальция транспортируется в герметически закрытых барабанах. Масса карбида в одном барабане от 50 до 130 кг.
При нормальном атмосферном давлении ацетилен с воздухом и кислородом образуют взрывоопасные смеси. Пределы взрывоопасности ацетилена с воздухом:
- нижний – 2,2%;
- верхний – 81%.
Пределы взрывоопасности ацетилена с кислородом:
- нижний – 2,3%;
- верхний – 93%.
Наиболее взрывоопасные концентрации ацетилена с воздухом и кислородом составляют:
- нижний – 7%;
- верхний – 13%.
gazresyrs.ru
описание и условия реакции, применение в технике
Одной из актуальных проблем является загрязнение окружающей среды и ограниченность энергетических ресурсов органического происхождения. Многообещающим способом решения этих проблем является использование водорода в качестве источника энергии. В статье рассмотрим вопрос горения водорода, температуру и химию этого процесса.
Что такое водород?

Прежде чем рассматривать вопрос, какая температура сгорания водорода, необходимо вспомнить, что собой представляет это вещество.
Водород — это самый легкий химический элемент, состоящий всего из одного протона и одного электрона. При нормальных условиях (давление 1 атм., температура 0 oC) он присутствует в газообразном состоянии. Его молекула (H2) образована 2 атомами этого химического элемента. Водород является 3-м по распространенности элементом на нашей планете, и 1-м во Вселенной (около 90 % всей материи).
Водородный газ (H2) не имеет запаха, вкуса и цвета. Он не токсичен, однако, когда содержание его в атмосферном воздухе составляет несколько процентов, то человек может испытывать удушье, по причине недостатка кислорода.
Любопытно отметить, что хотя с химической точки зрения все молекула H2 идентичны, физические свойства их несколько отличаются. Дело все в ориентации спинов электронов (они ответственны за появление магнитного момента), которые могут быть параллельными и антипараллельными, такую молекулу называют орто- и параводородом, соответственно.
Химическая реакция горения

Рассматривая вопрос, температуры горения водорода с кислородом, приведем химическую реакцию, которая описывает этот процесс: 2H2 + O2 => 2H2O. То есть в реакции участвуют 3 молекулы (две водорода и одна кислорода), а продуктом являются две молекулы воды. Эта реакция описывает горение с химической точки зрения, и по ней можно судить, что после ее прохождения остается только чистая вода, которая не загрязняет окружающую среду, как это происходит при сгорании органического топлива (бензина, спирта).
С другой стороны, эта реакция является экзотермической, то есть помимо воды она выделяет некоторое количества тепла, которое можно использовать для приведения в движение машин и ракет, а также для его перевода в другие источники энергии, например, в электричество.
Механизм процесса горения водорода
Описанная в предыдущем пункте химическая реакция известна любому школьнику старших классов, однако она является очень грубым описанием того процесса, который происходит в действительности. Отметим, что до середины прошлого века человечество не знало, как происходит горение водорода в воздухе, а в 1956 году за ее изучение была присуждена Нобелевская премия по химии.
В действительности, если столкнуть молекулы O2 и H2, то никакой реакции не произойдет. Обе молекулы являются достаточно устойчивыми. Чтобы горение происходило, и образовывалась вода, необходимо существование свободных радикалов. В частности, атомов H, O и групп OH. Ниже приводится последовательность реакций, которые происходят в действительности при горении водорода:
- H + O2 => OH + O;
- OH + H2 => H2O + H;
- O + H2 = OH + H.
Что видно из этих реакций? При горении водорода образуется вода, да, верно, но происходит это только, когда группа из двух атомов OH встречается с молекулой H2. Кроме того, все реакции происходят с образованием свободных радикалов, это означает, что запускается процесс самоподдержания горения.
Таким образом, ключевой момент в запуске этой реакции заключается в образовании радикалов. Они появляются, если поднести к кислород-водородной смеси горящую спичку, либо если нагреть эту смесь выше определенной температуры.
Инициация реакции
Как было отмечено, сделать это можно двумя способами:
- С помощью искры, которая должна предоставить всего 0,02 мДж теплоты. Это очень маленькое значение энергии, для сравнения скажем, что аналогичное значение для бензиновой смеси составляет 0,24 мДж, а для метановой — 0,29 мДж. С уменьшением давления энергия инициации реакции растет. Так, при 2 кПа она составляет уже 0,56 мДж. В любом случае, это очень маленькие значения, поэтому водород-кислородная смесь считается легко воспламеняющейся.
- С помощью температуры. То есть кислород-водородную смесь можно просто нагревать, и выше некоторой температуры она сама воспламенится. Когда это произойдет, зависит от давления и процентного соотношения газов. В широком интервале концентраций при атмосферном давлении реакция самовозгорания происходит при температурах выше 773-850 К, то есть выше 500-577 oC. Это достаточно высокие значения по сравнению с бензиновой смесью, которая начинает самовоспламеняться уже при температурах ниже 300 oC.
Процентное содержание газов в горючей смеси

Говоря о температуре горения водорода в воздухе, следует отметить, что не всякая смесь этих газов будет вступать в рассматриваемый процесс. Экспериментально установлено, что если количество кислорода меньше 6% по объему, либо если количество водорода меньше 4% по объему, то никакой реакции не будет. Тем не менее, пределы существования горючей смеси являются достаточно широкими. Для воздуха процентное содержание водорода может составлять от 4,1 % до 74,8 %. Отметим, что верхнее значение как раз соответствует необходимому минимуму по кислороду.
Если же рассматривается чистая кислород-водородная смесь, то здесь пределы еще шире: 4,1-94 %.
Уменьшение давления газов приводит к сокращению указанных пределов (нижняя граница поднимается, верхняя — опускается).
Также важно понимать, что в процессе горения водорода в воздухе (кислороде), возникающие продукты реакции (вода) приводят к уменьшению концентрации реагентов, что может привести к прекращению химического процесса.
Безопасность горения

Это важная характеристика воспламеняющейся смеси, поскольку она позволяет судить о том, происходит реакция спокойно, и можно ее контролировать, либо процесс имеет взрывной характер. От чего зависит скорость горения? Конечно же, от концентрации реагентов, от давления, а также от количества энергии «затравки».
К большому сожалению, водород в широком интервале концентраций способен к взрывному горению. В литературе приводятся следующие цифры: 18,5-59 % водорода в воздушной смеси. Причем на краях этого предела в результате детонации выделяется наибольшее количество энергии на единицу объема.
Отмеченный характер горения представляет большую проблему для использования этой реакции в качестве контролируемого источника энергии.
Температура реакции горения
Теперь мы подошли непосредственно к ответу на вопрос, какая низшая температура сгорания водорода. Она составляет 2321 К или 2048 oC для смеси с 19,6 % H2. То есть температура горения водорода в воздухе выше 2000 oC (для других концентраций она может достигать 2500 oC), и в сравнении с бензиновой смесью — это огромная цифра (для бензина около 800 oC). Если сжигать водород в чистом кислороде, то температура пламени будет еще выше (до 2800 oC).
Столь высокая температура пламени представляет еще одну проблему в использовании этой реакции в качестве источника энергии, поскольку не существует в настоящее время сплавов, которые могли бы работать длительное время в таких экстремальных условиях.
Конечно, эта проблема решается, если использовать хорошо продуманную систему охлаждения камеры, где происходит горение водорода.
Количество выделяемой теплоты
В рамках вопроса температуры горения водорода любопытно также привести данные о количестве энергии, которая выделяется во время этой реакции. Для разных условий и составов горючей смеси получили значения от 119 МДж/кг до 141 МДж/кг. Чтобы понять, насколько это много, отметим, что аналогичное значение для бензиновой смеси составляет около 40 МДж/кг.
Энергетический выход водородной смеси намного выше, чем для бензина, что является огромным плюсом для ее применения в качестве топлива для двигателей внутреннего сгорания. Однако, и здесь не все так просто. Все дело в плотности водорода, она слишком низка при атмосферном давлении. Так, 1 м3 этого газа весит всего 90 грамм. Если сжечь этот 1 м3 H2, то выделится около 10-11 МДж теплоты, что уже в 4 раза меньше, чем при сжигании 1 кг бензина (чуть больше 1 литра).
Приведенные цифры говорят о том, что для использования реакции горения водорода необходимо научиться хранить этот газ в баллонах с высоким давлением, что создает уже дополнительные сложности, как в технологическом вопросе, так и с точки зрения безопасности.
Применение водородной горючей смеси в технике: проблемы

Сразу необходимо сказать, что в настоящее время водородная горючая смесь уже используется в некоторых сферах человеческой деятельности. Например, в качестве дополнительного топлива для космических ракет, в качестве источников для выработки электрической энергии, а также в экспериментальных моделях современных автомобилей. Однако масштабы этого применения являются мизерными, по сравнению с таковыми для органического топлива и, как правило, носят экспериментальных характер. Причиной этому являются не только трудности в контроле самой реакции горения, но также в хранении, транспортировке и добыче H2.
Водород на Земле практически не существует в чистом виде, поэтому его необходимо получать из различных соединений. Например, из воды. Это достаточно популярный способ в настоящее время, который осуществляется с помощью пропускания электрического тока через H2O. Вся проблема заключается в том, что при этом расходуется больше энергии, чем потом можно получить путем сжигания H2.
Еще одна важная проблема — транспортировка и хранение водорода. Дело в том, что этот газ, ввиду маленьких размеров его молекул, способен «вылетать» из любых контейнеров. Кроме того, попадая в металлическую решетку сплавов, он вызывает их охрупчивание. Поэтому наиболее эффективным способом хранения H2 является использование атомов углерода, способных прочно связывать «неуловимый» газ.

Таким образом, применение водорода в качестве топлива в более-менее широких масштабах возможно, только если его использовать в качестве «сохранения» электричества (например, переводить ветровую и солнечную энергию в водород с помощью электролиза воды), либо если научиться доставлять H2 из космоса (где его очень много) на Землю.
fb.ru
Какова максимальная температура огня при горении дерева (любого)?
при нагревании до 105°С из древесины испаряется вода; при нагревании до 150°С из древесины удаляются остатки влаги и начинается разложение и выделение газообразных продуктов; при нагревании 270—280°С начинается экзотермическая реакция с выделением тепла, т. е. созданы условия для самоподдержания необходимой температуры, при • которой идёт разложение древесины с образованием пламени и дальнейшим повышением температуры; при температуре 450°С и более пламенное горение переходит в беспламенное горение угля (тление) с температурой до 900°С.
Думаю градусов 500-600
При температуре 275° на открытом воздухе начинается горение древесины, т. е. соединение ее с кислородом воздуха, сопровождающееся светящимся пламенем. При этом в толстых кусках древесина из-за малой теплопроводности не прогревается; начавшееся горение переходит в тление и прекращается совсем. Поэтому практически точкой воспламенения древесины можно считать (для сосны) 300—330°.
Температура воспламенения для большинства твердых материалов — 300°С. Температура пламени в горящей сигарете — 700-800°С. В спичке температура пламени 750-850 °С, при этом 300°С — температура воспламенения дерева, А ТЕМПЕРАТУРА ГОРЕНИЯ ДЕРЕВА РАВНЯЕТСЯ ПРИМЕРНО 800 — 1000 °С. Температура горения пропан-бутана колеблется от 800 до 1970 °С. Температура горения бензина — 1300-1400 °С. Температура пламени керосина — 1100 °С. Температура пламени спирта не превышает 900 °С. Температура горения магния — 2200 °С.
Ответ зависит от того, что и как греть. Большие температуры за 1000 С для нагрева крупных тел можно получить лишь с подогревом воздуха, в прогретых печах, где тепло не рассеивается в стороны. Хотя верхняя часть пламени имеет выше 1500 С, но никто не расплавит в ней железо.
По моему подробней не получится открыть тему, чем здесь: <a rel=»nofollow» href=»http://fas.su/page-510″ target=»_blank»>http://fas.su/page-510</a>
touch.otvet.mail.ru
