Сравните крахмал и целлюлозу Вопрос 3 Параграф 15 Химия 10 класс О.С.Габриелян – Рамблер/класс
Сравните крахмал и целлюлозу Вопрос 3 Параграф 15 Химия 10 класс О.С.Габриелян – Рамблер/классИнтересные вопросы
Школа
Подскажите, как бороться с грубым отношением одноклассников к моему ребенку?
Новости
Поделитесь, сколько вы потратили на подготовку ребенка к учебному году?
Школа
Объясните, это правда, что родители теперь будут информироваться о снижении успеваемости в школе?
Школа
Когда в 2018 году намечено проведение основного периода ЕГЭ?
Новости
Будет ли как-то улучшаться система проверки и организации итоговых сочинений?
Вузы
Подскажите, почему закрыли прием в Московский институт телевидения и радиовещания «Останкино»?
Даров! Помощи прошу вашей, ибо я честно говорю, ну не знаю как ответить правильно.
Сравните крахмал и целлюлозу, т. е. назовите признаки
общего и отличного в их составе, строении, свойствах и
применении.
ответы
Привет) Отвечать буду таблицей, так понятней будет, вот ответ….
Сравнительная характеристика крахмала и целлюлозы:
ваш ответ
Можно ввести 4000 cимволов
отправить
дежурный
Нажимая кнопку «отправить», вы принимаете условия пользовательского соглашения
похожие темы
ЕГЭ
9 класс
11 класс
Физика
похожие вопросы 5
Приготовление раствора сахара и расчёт его массовой доли в растворе. Химия. 8 класс. Габриелян. ГДЗ. Хим. практикум № 1. Практ. работа № 5.
Попробуйте провести следующий опыт. Приготовление раствора
сахара и расчёт его массовой доли в растворе.
 ..)
..)ГДЗШкола8 классХимияГабриелян О.С.
Почему сейчас школьники такие агрессивные ?
Читали новость про 10 классника который растрелял ? как вы к этому относитесь
Новости10 классБезопасность
Здравствуйте.
(Подробнее…)
Химия
Это правда, что будут сокращать иностранные языки в школах?
Хочется узнать, когда собираются сократить иностранные языки в школе? Какой в итоге оставят? (Подробнее…)
ШколаНовостиИностранные языки
ЕГЭ-2017 Цыбулько И. П. Русский язык ГДЗ. Вариант 13. 18. Расставьте все знаки препинания: укажите цифру(-ы), на месте которой(-ых)…
18.
Расставьте все знаки препинания: укажите цифру(-ы), на месте которой(-ых)
в предложении должна(-ы) стоять запятая(-ые). (Подробнее…)
ГДЗЕГЭРусский языкЦыбулько И.П.
Microsoft Word — _№ 6_титул.
 docx
docx%PDF-1.6 % 1 0 obj > endobj 5 0 obj >/Font>>>/Fields[]>> endobj 2 0 obj >stream 2021-06-29T11:37:18+07:002021-06-29T11:37:18+07:002021-06-29T11:37:18+07:00PScript5.dll Version 5.2.2application/pdf

6.2b Целлюлоза | EGEE 439: Альтернативные виды топлива из источников биомассы
6.2b Целлюлоза
Целлюлоза является наиболее распространенным полисахаридом, а также самой распространенной биомассой на Земле. Связи немного отличаются от крахмальных, называемых β-1,4-гликозидными связями (см. рис. 6.7C), поскольку связь имеет немного другую конфигурацию или форму. Как показано на рис. 6.7А и 6.7В, эта связь приводит к тому, что нити целлюлозы становятся более прямыми (а не спиральными). Водород одной цепи полимера может взаимодействовать с ОН другой цепи; это взаимодействие известно как водородная связь (H-связь), хотя это не настоящая связь, а просто сильное взаимодействие.
Рисунок 6.7a: Изображение целлюлозы в различных формах.
Предоставлено: The McGraw-Hill Companies
Рисунок 6.7b: Структура целлюлозы — одна цепь и волокна.
Авторы и права: CHEMIK 2013, 67, 3, 242-249
В таблице 6.1 показано сравнение двух типов крахмала и целлюлозы. Целлюлоза образует удлиненные волокна, которые вытягиваются; он не скручивается, как амилоза (помните о спиральной структуре), и не разветвляется и не скручивается, как амилопектин. Из-за своей химической структуры он образует большую сеть, в которой Н-связи стабилизируют саму нить, а также группу нитей, из которых состоят волокна. Н-связь придает волокнам целлюлозы несколько важных структурных особенностей. Это невероятно сложно. Он непроницаем для воды из-за водородных связей и, таким образом, не пропускает воду. Таблица 6.1: Сравнение свойств двух компонентов крахмала и целлюлозы.
Из-за своей химической структуры он образует большую сеть, в которой Н-связи стабилизируют саму нить, а также группу нитей, из которых состоят волокна. Н-связь придает волокнам целлюлозы несколько важных структурных особенностей. Это невероятно сложно. Он непроницаем для воды из-за водородных связей и, таким образом, не пропускает воду. Таблица 6.1: Сравнение свойств двух компонентов крахмала и целлюлозы.
| Тип полисахарида | Крахмал (амилопектин) | Крахмал (амилоза) | Целлюлоза |
|---|---|---|---|
| Типы соединений |
| α-1,4-глюкозид | β-1,4-глюкозид |
| Функция | Сохраняет энергию | Сохраняет энергию | Поддерживает и укрепляет |
Молекулярная масса (а. е.м.) е.м.) | 300 000 | 10 000–50 000 | 50 000–500 000 |
| Размер единиц глюкозы | 1800 единиц глюкозы | 6-300 единиц глюкозы | 300-2500 единиц глюкозы |
‹ 6.2a Крахмал вверх 6.2c Гемицеллюлоза ›
О конформационных свойствах олигомеров амилозы и целлюлозы в растворе
На этой странице
АннотацияВведениеМетодыРезультатыОбсуждениеБлагодарностиСсылкиАвторские праваСтатьи по теме
конформация двухцепочечной и одноцепочечной амилозы и одноцепочечной
олигомеры целлюлозы, содержащие 9 фрагментов сахара в растворе, в зависимости от растворителя
состав, ионная сила, температура и степень метилирования. Это исследование наряду
с другими предыдущими исследованиями предполагает, что водородные связи имеют решающее значение для гарантии
стабильность двойной спирали амилозы. Одноцепочечная амилоза образует спираль
структура, а целлюлоза остается сильно вытянутой на протяжении всего времени моделирования,
поведение, которое также наблюдалось экспериментально. С точки зрения координации растворенного вещества
гидроксильные группы с ионами, амилоза демонстрирует энтропийную координацию кальция
и сульфат-ионы, тогда как координация ионов целлюлозы, по-видимому, зависит от энтальпии.
Это указывает на то, что соображениями энтропии нельзя пренебрегать при объяснении
структурные различия между амилозами и целлюлозами.
С точки зрения координации растворенного вещества
гидроксильные группы с ионами, амилоза демонстрирует энтропийную координацию кальция
и сульфат-ионы, тогда как координация ионов целлюлозы, по-видимому, зависит от энтальпии.
Это указывает на то, что соображениями энтропии нельзя пренебрегать при объяснении
структурные различия между амилозами и целлюлозами.
1. Введение
Амилоза и целлюлоза представляют собой линейные полимеры глюкозы, связанные 1,4-связями. Основное отличие заключается в аномерной конфигурации: глюкозные звенья амилозы связаны гликозидными связями, тогда как мономерные звенья целлюлозы связаны гликозидными связями. Этот другой тип связывания заставляет амилозу образовывать спиральные структуры, а целлюлозу — прямые полимерные цепи.
Амилоза встречается в различных формах: A, B, V и других формах [1]. Обе формы A и B имеют левые спирали с шестью единицами глюкозы на виток и, по-видимому, различаются только упаковкой спиралей крахмала. V-форму амилозы получают путем сокристаллизации с такими соединениями, как йод, ДМСО, спирты или жирные кислоты [2, 3].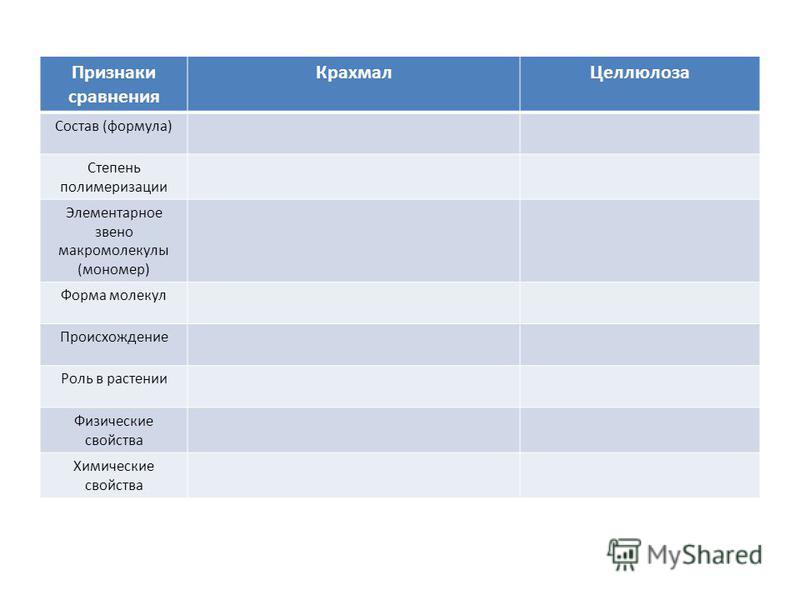 Спиральные конформации B- и V-амилозы различаются [4–6].
Спиральные конформации B- и V-амилозы различаются [4–6].
Целлюлоза представляет собой линейный полимер и самый распространенный природный полимер на земле. Структура и свойства целлюлозы были тщательно исследованы, но до сих пор существуют неопределенности в отношении кристаллической структуры целлюлозы [7–9]. Эксперименты по рассеянию рентгеновских лучей и дифракции электронов показывают, что целлюлоза образует агрегаты в листообразные структуры с молекулами целлюлозы в удлиненной конформации.
Эти структурные различия являются причиной того, что амилозы и целлюлозы имеют очень разные физические и биологические свойства [10]. Амилоза плохо растворяется в воде и образует суспензии, в которых сохраняется ее спиральность. Целлюлозные волокна нерастворимы в воде.
Можно выполнить компьютерное моделирование этих систем, чтобы получить представление о поведении этих молекул на атомном уровне и выполнить компьютерные исследования их свойств. Компьютерное моделирование двойной спирали амилозы в воде методом Монте-Карло Эйзенхабером и Шулером [11] предполагает, что левосторонняя антипараллельная двойная спираль лучше всего соответствует структуре жидкой воды. Наблюдались регулярные водные мостики, образующие сеть вокруг дуплекса.
Наблюдались регулярные водные мостики, образующие сеть вокруг дуплекса.
Предыдущие исследования молекулярной динамики (МД) амилозы и целлюлозы были проведены Yu et al. [12]. Фрагменты этих молекул метилировали в разных положениях и контролировали их стабильность. Авторы пришли к выводу, что одиночные спирали в большей степени дестабилизируются при метилировании остатков O-2 и O-3 амилозы, чем при метилировании O-6, но метилирование O-6 сильнее дестабилизирует двойные спирали.
В настоящей работе анализируются модели двухцепочечных и одноцепочечных амилоз и одноцепочечных олигомеров целлюлозы, состоящих из 9 фрагментов сахара, и изучается стабильность конкретных структур этих молекул в зависимости от типа растворителя, ионной прочность, температура и состояние метилирования.
2. Методы
2.1. Молекулярно-динамическое моделирование
МД-моделирование выполняли с помощью пакета программ GROMOS [13–15] с использованием набора параметров силового поля 53A6 [16], который рассматривает алифатические углероды как объединенные атомы. Параметры сахара были оптимизированы для силового поля GROMOS Линсом и Хюненбергером [17]. Моделирование МД, выполненное для молекул, состоящих из 9единицы сахара приведены в таблице 1. Исходные координаты амилозы и целлюлозы были сгенерированы с помощью программного пакета INSIGHTII (Accelerys Inc., Сан-Диего, Калифорния, США). Амилоза была смоделирована в виде двойной спирали. Исходными растворенными конформациями двойной спирали амилозы были правильные спирали, построенные по данным Imberty et al. [18]. Эта модель характеризуется углами закручивания и . Для дальнейшего исследования роли водородных связей в стабильности спирали было проведено моделирование с отключением всех несвязанных взаимодействий между атомами растворенного вещества, участвующими в водородных связях (метка: noHB), а также моделирование с метилированными гидроксигруппами, участвующими в водородных связях (метка: встретились). В топологиях моделирования с исключенными водородными связями взаимодействия Леннарда-Джонса между атомами, связанными водородными связями, были установлены равными нулю.
Параметры сахара были оптимизированы для силового поля GROMOS Линсом и Хюненбергером [17]. Моделирование МД, выполненное для молекул, состоящих из 9единицы сахара приведены в таблице 1. Исходные координаты амилозы и целлюлозы были сгенерированы с помощью программного пакета INSIGHTII (Accelerys Inc., Сан-Диего, Калифорния, США). Амилоза была смоделирована в виде двойной спирали. Исходными растворенными конформациями двойной спирали амилозы были правильные спирали, построенные по данным Imberty et al. [18]. Эта модель характеризуется углами закручивания и . Для дальнейшего исследования роли водородных связей в стабильности спирали было проведено моделирование с отключением всех несвязанных взаимодействий между атомами растворенного вещества, участвующими в водородных связях (метка: noHB), а также моделирование с метилированными гидроксигруппами, участвующими в водородных связях (метка: встретились). В топологиях моделирования с исключенными водородными связями взаимодействия Леннарда-Джонса между атомами, связанными водородными связями, были установлены равными нулю. Для моделирования одноцепочечной амилозы одна цепь была удалена из исходной двойной спиральной структуры. Моделирование с участием олигомеров целлюлозы начиналось с расширенной конформации с углами и . Модель воды с простым точечным зарядом (SPC) [19] использовался для описания молекул растворителя. В некоторых моделях в качестве растворителя использовали ДМСО [20] (обозначение: ДМСО). При моделировании молекулы растворителя добавлялись вокруг растворенного вещества внутри прямоугольной коробки для (двухцепочечной) амилозы и целлюлозы с минимальным расстоянием 1,4 нм между атомами растворенного вещества и стенками периодической коробки. В моделировании использовались вращательно-поступательные ограничения [21]. В некоторых моделях в водном растворе были включены ионы ( и ) (таблица 1). Первоначальное размещение ионов было случайным. Все связи и валентные углы молекул растворителя были ограничены геометрическим допуском алгоритма SHAKE [22]. Минимизация энергии методом наискорейшего спуска без каких-либо ограничений всех систем выполнялась для релаксации контактов растворенное вещество-растворитель.
Для моделирования одноцепочечной амилозы одна цепь была удалена из исходной двойной спиральной структуры. Моделирование с участием олигомеров целлюлозы начиналось с расширенной конформации с углами и . Модель воды с простым точечным зарядом (SPC) [19] использовался для описания молекул растворителя. В некоторых моделях в качестве растворителя использовали ДМСО [20] (обозначение: ДМСО). При моделировании молекулы растворителя добавлялись вокруг растворенного вещества внутри прямоугольной коробки для (двухцепочечной) амилозы и целлюлозы с минимальным расстоянием 1,4 нм между атомами растворенного вещества и стенками периодической коробки. В моделировании использовались вращательно-поступательные ограничения [21]. В некоторых моделях в водном растворе были включены ионы ( и ) (таблица 1). Первоначальное размещение ионов было случайным. Все связи и валентные углы молекул растворителя были ограничены геометрическим допуском алгоритма SHAKE [22]. Минимизация энергии методом наискорейшего спуска без каких-либо ограничений всех систем выполнялась для релаксации контактов растворенное вещество-растворитель. Минимизация энергии прекращалась, когда изменение энергии на шаг становилось меньше 0,1 кДж . Для невалентных взаимодействий использовался трехдиапазонный метод с радиусами отсечки 0,8/1,4 нм. Короткодействующие ван-дер-ваальсовы и электростатические взаимодействия оценивались на каждом (временном) шаге на основе списка пар заряд-группа. Среднедействующие ван-дер-ваальсовы и электростатические взаимодействия между парами на расстоянии более 0,8 нм и менее 1,4 нм оценивались на каждом пятом (временном) шаге, в который (временной) момент обновлялся список пар. Вне большего радиуса отсечки использовалось приближение поля реакции [23] с относительной диэлектрической проницаемостью 66 [24]. Начальные скорости атомов были заданы по распределению Максвелла при 50 K. Для амилозы были проведены четыре периода 50 пс МД-моделирования с гармоническим ограничением положения атомов растворенного вещества с силовыми константами кДж , кДж , кДж и 5,0 кДж , чтобы уравновесить далее системы при 50 К, 100 К, 200 К и 278/313 К соответственно.
Минимизация энергии прекращалась, когда изменение энергии на шаг становилось меньше 0,1 кДж . Для невалентных взаимодействий использовался трехдиапазонный метод с радиусами отсечки 0,8/1,4 нм. Короткодействующие ван-дер-ваальсовы и электростатические взаимодействия оценивались на каждом (временном) шаге на основе списка пар заряд-группа. Среднедействующие ван-дер-ваальсовы и электростатические взаимодействия между парами на расстоянии более 0,8 нм и менее 1,4 нм оценивались на каждом пятом (временном) шаге, в который (временной) момент обновлялся список пар. Вне большего радиуса отсечки использовалось приближение поля реакции [23] с относительной диэлектрической проницаемостью 66 [24]. Начальные скорости атомов были заданы по распределению Максвелла при 50 K. Для амилозы были проведены четыре периода 50 пс МД-моделирования с гармоническим ограничением положения атомов растворенного вещества с силовыми константами кДж , кДж , кДж и 5,0 кДж , чтобы уравновесить далее системы при 50 К, 100 К, 200 К и 278/313 К соответственно. Для целлюлозы было проведено пять периодов МД моделирования по 50 пс с гармоническим ограничением положения атомов растворенного вещества с силовыми константами кДж , кДж , кДж , кДж и 5,0 кДж для дальнейшего уравновешивания систем при 50 7 0K, 8, 1002 /313 К и 278/313 К соответственно. Во время уравновешивания степени свободы растворителя и растворенного вещества были независимо слабо связаны с температурной баней при заданной температуре с временем релаксации 0,1 пс [25]. В дальнейшем моделировании движение центра масс всей системы устанавливалось равным нулю каждые 1000 временных шагов. Системы также были слабо связаны с ванной под давлением из 1 атома со временем релаксации 0,5 пс и изотермической сжимаемостью . Координаты траектории и энергии сохранялись каждые 0,5 пс для анализа.
Для целлюлозы было проведено пять периодов МД моделирования по 50 пс с гармоническим ограничением положения атомов растворенного вещества с силовыми константами кДж , кДж , кДж , кДж и 5,0 кДж для дальнейшего уравновешивания систем при 50 7 0K, 8, 1002 /313 К и 278/313 К соответственно. Во время уравновешивания степени свободы растворителя и растворенного вещества были независимо слабо связаны с температурной баней при заданной температуре с временем релаксации 0,1 пс [25]. В дальнейшем моделировании движение центра масс всей системы устанавливалось равным нулю каждые 1000 временных шагов. Системы также были слабо связаны с ванной под давлением из 1 атома со временем релаксации 0,5 пс и изотермической сжимаемостью . Координаты траектории и энергии сохранялись каждые 0,5 пс для анализа.
2.2. Анализ
Анализы проводились с помощью пакетов программного обеспечения для анализа GROMOS++ [15] и esra [26]. Радиусы вращения были рассчитаны для наблюдения за уровнем компактности моделируемых молекул. Структурная информация об ионных растворах была получена из функций радиального распределения. Для амилозы проценты меж- и внутримолекулярных водородных связей были рассчитаны с использованием критерия максимального расстояния 0,25 нм между атомом водорода и акцепторным атомом и критерия минимального угла для угла донор-водород-акцептор.
Структурная информация об ионных растворах была получена из функций радиального распределения. Для амилозы проценты меж- и внутримолекулярных водородных связей были рассчитаны с использованием критерия максимального расстояния 0,25 нм между атомом водорода и акцепторным атомом и критерия минимального угла для угла донор-водород-акцептор.
3. Результаты
3.1. Двухцепочечная амилоза в чистом растворителе
Радиусы вращения амилозы в различных растворителях и состояниях метилирования показаны на рис. 1. Исключение взаимодействий между атомами, образующими водородные связи, не оказывает существенного влияния на поведение радиусов вращения. Процентное содержание водородных связей показано в таблице 2. Исключение взаимодействия водородных связей в моделировании приводит к тому, что анализируемые водородные связи исчезают. Моделирование в ДМСО увеличивает водородные связи между растворенными веществами, и можно наблюдать более высокие проценты. Метилирование структуры сводит к нулю водородные связи между растворенными веществами. Тем не менее, структуры метилированных и неметилированных случаев дают сходные радиусы вращения (рис. 1). Однако их структуры различаются по сравнению с окончательными структурами (рис. 2). Амилоза с гидроксильными группами сохраняет спиральную структуру (рис. 2(а) и 2(б)), тогда как метоксилированная структура распадается (рис. 2(а) и 2(б)).
Тем не менее, структуры метилированных и неметилированных случаев дают сходные радиусы вращения (рис. 1). Однако их структуры различаются по сравнению с окончательными структурами (рис. 2). Амилоза с гидроксильными группами сохраняет спиральную структуру (рис. 2(а) и 2(б)), тогда как метоксилированная структура распадается (рис. 2(а) и 2(б)).
3.2. Двухцепочечная амилоза в ионном растворе
Амилоза принимает меньшие радиусы вращения при 313 К, чем при 278 К (рис. 1). Анализ водородных связей (таблица 3) показывает более низкий процент водородных связей при более высокой температуре, но, с другой стороны, более благоприятную координацию сульфата с гидроксильными группами растворенного вещества, чем при более низкой температуре. На рис. 3 показаны функции радиального распределения для различных пар атомов. Сродство сульфата к кальцию выше при более высокой температуре, по крайней мере, для первой сольватной оболочки (рис. 3, а). Это говорит о том, что координация кальция и сульфата управляется энтропией. И кальций, и сульфат координируются с гидроксильными группами растворенного вещества, которые не находятся на внутренней стороне спирали ( и ), но сульфат координируется в несколько большей степени, чем кальций. Координация сульфата с гидроксильными группами растворенного вещества, по-видимому, также имеет энтропийный вклад; во всех сольватных оболочках наблюдается более высокая координация при более высокой температуре. Вода имеет большее сродство к ионам кальция, чем к ионам сульфата.
И кальций, и сульфат координируются с гидроксильными группами растворенного вещества, которые не находятся на внутренней стороне спирали ( и ), но сульфат координируется в несколько большей степени, чем кальций. Координация сульфата с гидроксильными группами растворенного вещества, по-видимому, также имеет энтропийный вклад; во всех сольватных оболочках наблюдается более высокая координация при более высокой температуре. Вода имеет большее сродство к ионам кальция, чем к ионам сульфата.
3.3. Одноцепочечная амилоза и целлюлоза в ионном растворе
На рис. 4 показаны радиусы вращения для моделирования одноцепочечной амилозы и целлюлозы. Радиусы вращения целлюлозы показывают более высокие значения, чем у одноцепочечной амилозы. Согласно этому наблюдению, целлюлоза остается сильно вытянутой во время моделирования, тогда как одноцепочечная амилоза образует компактные структуры, которые, однако, демонстрируют значительные колебания. Это отражено в окончательных структурах двух молекул (рис. 2(e) и 2(f)). Ни одна из молекул существенно не меняет своего поведения при изменении температуры. Функции радиального распределения двух молекул изображены на рисунках 5 и 6. Сравнивая координацию кальция с сульфатом, можно наблюдать сходное поведение в обоих моделях для амилозы и целлюлозы. Оба графика показывают более высокое сродство к сульфату кальция при более высокой температуре. Сравнивая координацию ионов кальция и сульфата с растворенными гидроксильными группами, два сахара показывают довольно разную температурную зависимость: формы кривых на рисунках 5 и 6 аналогичны, но в случае амилозы ионная координация предпочтительнее при более высокой температуре. , а в случае целлюлозы при более низкой температуре.
2(e) и 2(f)). Ни одна из молекул существенно не меняет своего поведения при изменении температуры. Функции радиального распределения двух молекул изображены на рисунках 5 и 6. Сравнивая координацию кальция с сульфатом, можно наблюдать сходное поведение в обоих моделях для амилозы и целлюлозы. Оба графика показывают более высокое сродство к сульфату кальция при более высокой температуре. Сравнивая координацию ионов кальция и сульфата с растворенными гидроксильными группами, два сахара показывают довольно разную температурную зависимость: формы кривых на рисунках 5 и 6 аналогичны, но в случае амилозы ионная координация предпочтительнее при более высокой температуре. , а в случае целлюлозы при более низкой температуре.
4. Обсуждение
В этой работе моделировались двухцепочечные и одноцепочечные амилозы и одноцепочечная целлюлоза при различных условиях, касающихся состава растворителя, ионной силы и температуры. Чтобы проследить роль водородных связей в образовании спирали и формировании компактных структур двухцепочечной амилозы, использовались различные подходы для разрушения сети водородных связей, образованной двумя нитями амилозы. Во-первых, выключаются взаимодействия между донорными и акцепторными атомами; в другом подходе метилированы все гидроксигруппы, участвующие в водородных связях.
Во-первых, выключаются взаимодействия между донорными и акцепторными атомами; в другом подходе метилированы все гидроксигруппы, участвующие в водородных связях.
Из этого исследования можно сделать вывод, что водородные связи важны для стабильности двойной спирали амилозы. Введение метоксигрупп вместо гидроксигрупп препятствует образованию спирали. Замена растворителя с воды на ДМСО увеличивает стабильность межцепочечных водородных связей, что можно объяснить отсутствием конкуренции между водородными связями с молекулами воды и гидроксильными группами амилозы. При более высокой температуре двухцепочечная амилоза в растворе сульфата кальция проявляет меньше межцепочечных водородных связей и образует более компактные структуры. Другое наблюдение, сделанное в этой работе, заключается в том, что координация кальция с сульфатом управляется энтропией, и была обнаружена более высокая координация при более высоких температурах. Также такое поведение демонстрирует координация ионов с гидроксильными группами растворенного вещества.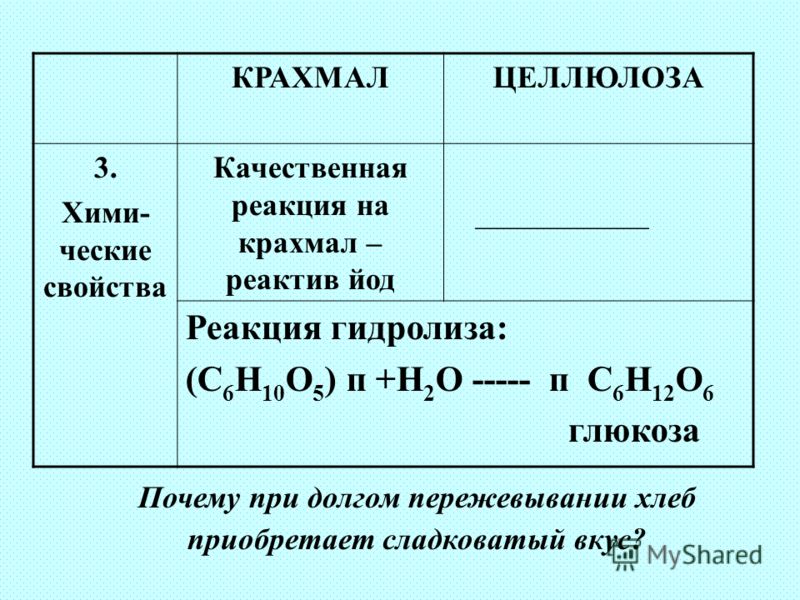
Одноцепочечные амилоза и целлюлоза представляют собой сходные молекулы, отличающиеся характером связывания их гликозидными связями. Было обнаружено, что целлюлоза остается в удлиненной конформации, тогда как одноцепочечная амилоза образует более компактные структуры. Еще одно поразительное различие между двумя молекулами заключается в чувствительности координации ионов к гидроксильным группам растворенного вещества к температуре. Координация ионов кальция и сульфата с растворенными гидроксильными группами, по-видимому, обусловлена энтропией в случае амилозы, тогда как в случае целлюлозы преобладает энтальпия. Это говорит о том, что при объяснении структурных различий между амилозами и целлюлозами нельзя пренебрегать соображениями энтропии.
Благодарности
Финансовая поддержка была получена от Национального центра компетенций в области исследований (NCCR) в области структурной биологии и от гранта №. 200021-109227 Швейцарского национального научного фонда, за что мы выражаем благодарность.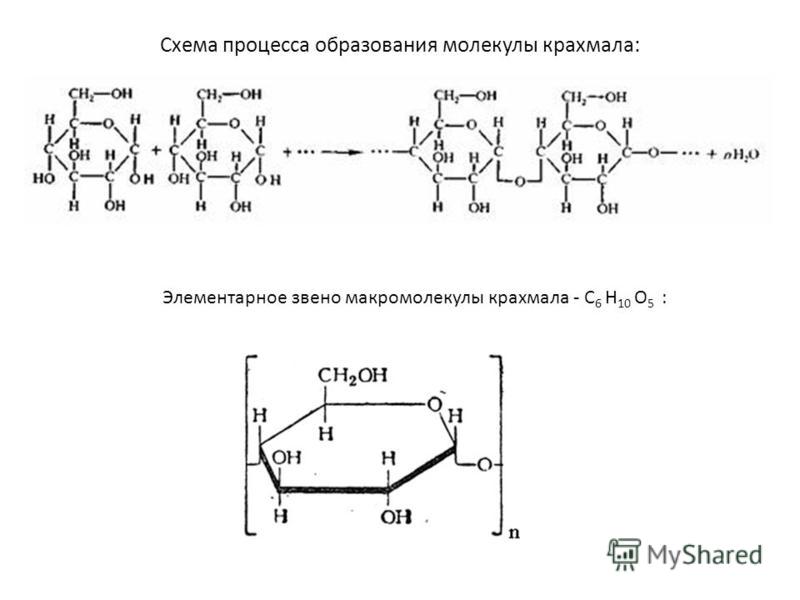 Авторы благодарят Кристину Перейру и Филиппа Хюненбергера за плодотворные и вдохновляющие дискуссии.
Авторы благодарят Кристину Перейру и Филиппа Хюненбергера за плодотворные и вдохновляющие дискуссии.
Ссылки
A. Buléon, P. Colonna, V. Planchot и S. Ball, «Крахмальные гранулы: структура и биосинтез», Международный журнал биологических макромолекул , том. 23, нет. 2, стр. 85–112, 1998.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Г. Раппенекер и П. Цугенмайер, «Подробное уточнение кристаллической структуры Vh-амилозы», Carbohydrate Research , vol. 89, нет. 1, стр. 11–19, 1981.
Посмотреть по адресу:
Сайт издателя | Google Scholar
M. C. Godet, H. Bizot и A. Buléon, «Кристаллизация комплексов амилозы и жирных кислот, полученных с различной длиной цепи амилозы», Углеводные полимеры , vol. 27, нет. 1, стр. 47–52, 1995.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Х.
 Сайто, Дж. Ямада, Т. Юкумото, Х. Ядзима и Р. Эндо, «Конформационная стабильность V-амилоз и их преобразование, вызванное гидратацией, в форму B-типа.
по данным твердотельной C13 ЯМР-спектроскопии высокого разрешения», Bulletin of the Chemical Society of Japan , vol. 64, нет. 12, стр. 3528–3537, 1991.
Сайто, Дж. Ямада, Т. Юкумото, Х. Ядзима и Р. Эндо, «Конформационная стабильность V-амилоз и их преобразование, вызванное гидратацией, в форму B-типа.
по данным твердотельной C13 ЯМР-спектроскопии высокого разрешения», Bulletin of the Chemical Society of Japan , vol. 64, нет. 12, стр. 3528–3537, 1991.Посмотреть по адресу:
Сайт издателя | Google Scholar
А. Имберти, А. Булеон, В. Тран и С. Перес, «Последние достижения в изучении структуры крахмала», Starch-Stärke , vol. 43, нет. 10, стр. 375–384, 1991.
Посмотреть по адресу:
Сайт издателя | Google Scholar
М. Б. Кардосо, Ж.-Л. Putaux, Y. Nishiyama et al., «Монокристаллы V-амилозы в комплексе с α-нафтолом», Biomacromolecules , vol. 8, нет. 2007. Т. 4. С. 1319–1326.
Посмотреть по адресу:
Сайт издателя | Google Scholar
A.
 C. O’Sullivan, «Целлюлоза: структура медленно распутывается», Cellulose , vol. 4, нет. 3, стр. 173–207, 1997.
C. O’Sullivan, «Целлюлоза: структура медленно распутывается», Cellulose , vol. 4, нет. 3, стр. 173–207, 1997.Посмотреть по адресу:
Сайт издателя | Google Scholar
П. Цугенмайер, «Конформация и упаковка различных волокон кристаллической целлюлозы», Progress in Polymer Science , vol. 26, нет. 9, стр. 1341–1417, 2001.
Посмотреть по адресу:
Сайт издателя | Академия Google
Y. Nishiyama, H. Chanzy, M. Wada et al., «Синхротронные рентгеновские исследования и нейтронная дифракция волокон полиморфных модификаций целлюлозы», Advances in X-Ray Analysis , vol. 45, pp. 385–390, 2002.
View по адресу:
Google Scholar
J. F. Robyt, Основы углеводной химии , Springer, New York, NY, USA, 1998.

- 9
. F. F. F. F. F. F. F. F. F. F. F. F. F. F. F. F. F. F. F. Frings, NY, USA, 1998.
- 9
. F. F. F. Fr Эйзенхабер и В. Шульц, «Моделирование методом Монте-Карло гидратной оболочки двойной спирали амилозы: левосторонняя антипараллельная двойная спираль лучше всего вписывается в структуру жидкой воды», Биополимеры , том. 32, нет. 12, стр. 1643–1664, 1992.
Посмотреть по адресу:
Сайт издателя | Google Scholar
H. Yu, M. Amann, T. Hansson, J. Köhler, G. Wich и W. F. van Gunsteren, «Влияние метилирования на стабильность и свободную энергию сольватации фрагментов амилозы и целлюлозы: молекулярный исследование динамики», Carbohydrate Research , vol. 339, нет. 10, стр. 1697–1709, 2004.
Посмотреть по адресу:
Сайт издателя | Академия Google
W.F. Van Gunsteren, S.
 R. Billeter, A. A. Eising et al., Биомолекулярное моделирование: Gromos96 Manual and Guide , Verlag der Fachvereine, Zürich, Switzerland, 1996.
R. Billeter, A. A. Eising et al., Биомолекулярное моделирование: Gromos96 Manual and Guide , Verlag der Fachvereine, Zürich, Switzerland, 1996.W… P. P. P. P. Тирони и др., «Пакет программ биомолекулярного моделирования GROMOS», The Journal of Physical Chemistry A , vol. 103, нет. 19, стр. 3596–3607, 1999.
Посмотреть по адресу:
Сайт издателя | Академия Google
М. Кристен, П. Х. Хюненбергер, Д. Баковис и др., «Программное обеспечение GROMOS для биомолекулярного моделирования: GROMOS05», Journal of Computational Chemistry , vol. 26, нет. 16, стр. 1719–1751, 2005.
Посмотреть по адресу:
Сайт издателя | Google Scholar
К. Остенбринк, А. Вилла, А. Э. Марк и В. Ф. ван Гюнстерен, «Биомолекулярное силовое поле, основанное на свободной энтальпии гидратации и сольватации: Наборы параметров силового поля GROMOS 53A5 и 53A6», Журнал вычислительной химии , том.
 25, нет. 13, стр. 1656–1676, 2004.
25, нет. 13, стр. 1656–1676, 2004.Посмотреть по адресу:
Сайт издателя | Google Scholar
Р. Д. Линс и П. Х. Хюненбергер, «Новое силовое поле GROMOS для углеводов на основе гексопиранозы», Journal of Computational Chemistry , vol. 26, нет. 13, стр. 1400–1412, 2005.
Посмотреть по адресу:
Сайт издателя | Google Scholar
А. Имберти, Х. Чанзи, С. Перес, А. Булеон и В. Тран, «Двойная спиральная природа кристаллической части А-крахмала», Журнал молекулярной биологии , том. 201, нет. 2, стр. 365–378, 1988.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Х. Дж. К. Берендсен, Дж. П. М. Постма, В. Ф. ван Гюнстерен и Дж. Херманс, «Модели взаимодействия воды по отношению к гидратации белка», в Межмолекулярные силы , Б.
 Пуллман, изд., стр. 331– 342, Reidel, Dordrecht, The Netherlands, 1981.
Пуллман, изд., стр. 331– 342, Reidel, Dordrecht, The Netherlands, 1981.Просмотр по адресу:
Google Scholar
H. Liu, F. Müller-Plathe, and W. F. van Gunsteren, «Силовое поле для жидкого диметилсульфоксида и физические свойства жидкого диметилсульфоксида, рассчитанного с помощью молекулярно-динамического моделирования», Журнал Американского химического общества , том. 117, нет. 15, стр. 4363–4366, 1995.
Посмотреть по адресу:
Сайт издателя | Google Scholar
A. Amadei, G. Chillemi, M.A. Ceruso, A. Grottesi, and A. Di Nola, «Моделирование молекулярной динамики с ограниченными вращательно-поступательными движениями: теоретическая основа и статистическая механическая согласованность», The Journal of Химическая физика , вып. 112, нет. 1, стр. 9–23, 2000.
Посмотреть по адресу:
Сайт издателя | Академия Google
Ж.
 -П. Рикарт, Г. Чиккотти и Х. Дж. К. Берендсен, «Численное интегрирование декартовых уравнений движения системы с ограничениями: молекулярные
динамика н-алканов», Journal of Computational Physics , vol. 23, нет. 3, стр. 327–341, 1977.
-П. Рикарт, Г. Чиккотти и Х. Дж. К. Берендсен, «Численное интегрирование декартовых уравнений движения системы с ограничениями: молекулярные
динамика н-алканов», Journal of Computational Physics , vol. 23, нет. 3, стр. 327–341, 1977.Посмотреть по адресу:
Сайт издателя | Google Scholar
И. Г. Тирони, Р. Сперб, П. Э. Смит и В. Ф. ван Гюнстерен, «Обобщенный метод реакционного поля для моделирования молекулярной динамики», Журнал химической физики , том. 102, нет. 13, стр. 5451–5459, 1995.
Посмотреть по адресу:
Сайт издателя | Google Scholar
A. Glättli, X. Daura и WF van Gunsteren, «Вывод улучшенной модели простого точечного заряда для жидкой воды: SPC/A и SPC/L», Journal of Chemical Physics , vol. 116, нет. 22, стр. 9811–9828, 2002.
Посмотреть по адресу:
Сайт издателя | Google Scholar
Х.

