2.2 Характерные химические свойства и получение простых веществ
Видеоурок 1: Неорганическая химия. Металлы: щелочные, щелочноземельные, алюминий
Видеоурок 2: Переходные металлы
Лекция: Характерные химические свойства и получение простых веществ — металлов: щелочных, щелочноземельных, алюминия; переходных элементов (меди, цинка, хрома, железа)
Химические свойства металловВсе металлы в химических реакциях проявляют себя, как восстановители. Они легко расстаются с валентными электронами, окисляясь при этом. Вспомним, что, чем левее располагается металл в электрохимическом ряду напряженности, тем более сильным восстановителем он является. Следовательно, самый сильный — это литий, самый слабый — золото и наоборот, золото — самый сильный окислитель, а литий — самый слабый.
Li→Rb→K→Ba→Sr→Ca→Na→Mg→Al→Mn→Cr→Zn→Fe→Cd→Co→Ni→Sn→Pb→H→Sb→Bi→Cu→Hg→Ag→Pd→Pt→Au
Все металлы вытесняют из раствора солей другие металлы, т.е. восстанавливают их. Все, кроме щелочных и щелочноземельных, так как они взаимодействуют с водой. Металлы, расположенные до Н, вытесняют его из растворов разбавленных кислот, а сами растворяются в них.
Рассмотрим некоторые общие химические свойства металлов:
- Взаимодействие металлов с кислородом образует основные (СаО, Na2O, 2Li2O и др.) или амфотерные (ZnO, Cr2O3, Fe2O3 и др.) оксиды.
- Взаимодействие металлов с галогенами (главная подгруппа VII группы) образует галогеноводородные кислоты (HF — фтороводород, HCl — хлороводород и др.).
- Взаимодействие металлов с неметаллами образует соли (хлориды, сульфиды, нитриды и др.).
- Взаимодействие металлов с металлами образует интерметаллиды (MgB2, NaSn, Fe3Ni и др.).
- Взаимодействие активных металлов с водородом образует гидриды (NaH, CaH 2, KH и др.).
- Взаимодействие щелочных и щелочноземельных металлов с водой образует щелочи (NaOH, Ca(OH)2, Cu(OH)2 и др.).
- Взаимодействие металлов (только, стоящих в электрохимическом ряду до Н) с кислотами образует соли (сульфаты, нитриты, фосфаты и др.). Следует иметь ввиду, что металлы реагируют с кислотами достаточно неохотно, тогда как с основаниями и солями взаимодействуют практически всегда. Для того, чтобы реакция металла с кислотой прошла нужно, чтобы металл был активным, а кислота сильной.
Химические свойства щелочных металлов
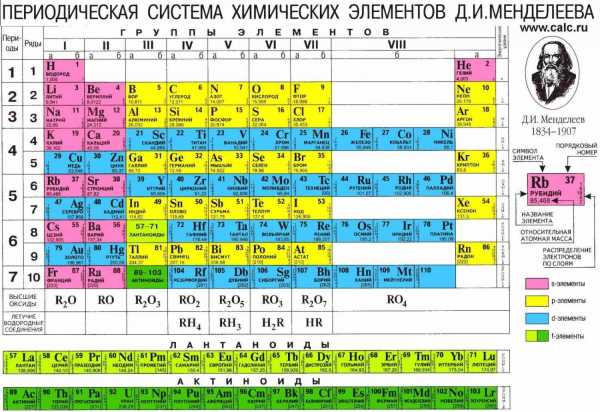
К группе щелочных металлов относятся следующие химические элементы: литий (Li), натрий (Na), калий (К), рубидий (Rb), цезий (Cs), франций (Fr). С перемещением сверху вниз по группе I Периодической таблицы их атомные радиусы увеличиваются, а значит возрастают металлические и восстановительные свойства.
Рассмотрим химические свойства щелочных металлов:
- Не имеют признаков амфотерности, так как обладают отрицательными значениями электродных потенциалов.
- Самые сильные восстановители среди всех металлов.
- В соединениях проявляют только степень окисления +1.
- Отдавая единственный валентный электрон, атомы данных химических элементов преобразуются в катионы.
- Образуют многочисленные ионные соединения.
- Практически все растворяются в воде.
Взаимодействие щелочных металлов с другими элементами:
1. С кислородом, образуя индивидуальные соединения, так оксид образует только литий (Li2O), натрий образует пероксид (Na2O2), а калий, рубидий и цезий — надпероксиды (KO2, RbO2, CsO2).
2. С водой, образуя щелочи и водород. Помните, эти реакции взрывоопасны. Без взрыва с водой реагирует только литий:
3.
С галогенами, образуя галогениды (NaCl — хлорид натрия, NaBr — бромид натрия, NaI — йодид натрия и др.).4. С водородом при нагревании, образуя гидриды (LiH, NaH и др.)
5. С серой при нагревании, образуя сульфиды (Na2S, K2S и др.). Они бесцветны и хорошо растворимы в воде.
6. С фосфором при нагревании, образуя фосфиды (Na3P, Li3P и др.), очень чувствительны к влаге и воздуху.
7. С углеродом при нагревании карбиды образуют только литий и натрий (Li2CO3, Na2CO3), тогда как калий, рубидий и цезий не образуют карбидов, они образуют бинарные соединения с графитом (C8Rb, C8Cs и др).
8. С азотом при обычных условиях реагирует только литий, образуя нитрид Li3N, с остальными щелочными металлами реакция возможна только при нагревании.
9. С кислотами реагируют со взрывом, поэтому проведение таких реакций очень опасно. Данные реакции проходят неоднозначно, потому что щелочной металл активно реагирует с водой, образуя щелочь, которая потом нейтрализуются кислотой. Таким образом создается конкуренция между щелочью и кислотой.
10. С аммиаком, образуя амиды — аналоги гидроксидов, но более сильные основания (NaNH2 — амид натрия, KNH2 — амид калия и др.).
11. Со спиртами, образуя алкоголяты.
Франций — радиоактивный щелочной металл, один из редчайших и наименее устойчивых среди всех радиоактивных элементов. Его химические свойства изучены недостаточно.
Получение щелочных металлов:
Для получения щелочных металлов используют в основном электролиз расплавов их галогенидов, чаще всего — хлоридов, образующих природные минералы:
Натрий также можно получить, прокаливая соду с углем в закрытых тиглях:
- Na2CO3 + 2C → 2Na + 3CO.
- 2Li2O + Si + 2CaO → 4Li + Ca2SiO4.
Химические свойства щелочноземельных металлов
К щелочноземельным металлам относятся элементы главной подгруппы II группы: кальций (Ca), стронций (Sr), барий (Ba), радий (Ra). Химическая активность данных элементов растет также, как и у щелочных металлов, т.е. с увеличением вниз по подгруппе.
Химические свойства щелочноземельных металлов:
Взаимодействие щелочноземельных металлов с другими элементами:
1. С кислородом все щелочноземельные металлы, кроме бария образуют оксиды, барий образует пероксид BaO2. Из данных металлов берилий и магний, покрытые тонкой защитной оксидной пленкой взаимодействуют с кислородом только при очень высоких t. Основные оксиды щелочноземельных металлов реагируют с водой, за исключением оксида берилия BeO, обладающего амфотерными свойствами. Реакция оксида кальция и воды называется реакцией гашения извести. Если реагентом является CaO образуется негашенная известь, если Ca(OH)
- 3CaO + P2O5 → Ca3(PO4)2.
2. С водой щелочноземельные металлы и их оксиды образуют гидроксиды — белые кристаллические вещества, которые в сравнении с гидроксидами щелочных металлов хуже растворяются в воде. Гидроксиды щелочноземельных металлов являются щелочами, кроме амфотерного Be(OH)2 и слабого основания Mg(OH)2. Поскольку берилий не реагирует с водой, Be(OH)2 может быть получен другими способами, например гидролизом нитрида:
- Be3N2 + 6Н2О → 3Be(OH)2 + 2NН3.
3. С галогенами при обычных условиях реагирую все, кроме бериллия. Последний вступает в реакцию только при высоких t. Образуются галогениды (MgI2 – иодид магния, CaI2 – иодид кальция, СаBr2 – бромид кальция и др.).
4. С водородом реагируют при нагревании все щелочноземельные металлы, кроме берилия. Образуются гидриды (BaH2, CaH2 и др.). Для реагирования магния с водородом помимо высокой t требуется еще и повышенное давление водорода.
5. С серой образуют сульфиды. К примеру:
Сульфиды служат для получения серной кислоты и соответствующих металлов.
6. С азотом образуют нитриды. К примеру:
7. С кислотами образуя соли соответствующей кислоты и водород. К примеру:
- Ве + Н2SO4(разб.) → BeSO4 + H2↑.
Эти реакции протекают также, как и в случае щелочных металлов.
Получение щелочно-земельных металлов:
Бериллий получают восстановлением фторида:
- BeF2 + Mg –tо→ Be + MgF2
- 3BaO + 2Al –tо→ 3Ba + Al2O3
Химические свойства алюминия
Алюминий – активный, легкий металл, под порядковым номером 13 в таблице. В природе самый распространенный из всех металлов. А из химических элементов занимает третью позицию по распространению. Высокий тепло- и электропроводник. Устойчив к коррозии, поскольку покрывается оксидной пленкой. Температура плавления равна 6600 С.
Рассмотрим химические свойства и взаимодействие алюминия с другими элементами:
1. Во всех соединениях алюминий находится в степени окисления +3.
2. Практически во всех реакциях проявляет восстановительные свойства.
3. Амфотерный металл, проявляет как кислотные, так и основные свойства.
4. Восстанавливает многие металлы из оксидов. Этот метод получения металлов получил название алюмотермии. Пример получения хрома:
5. Взаимодействует со всеми разбавленными кислотами, образуя соли и выделяя водород. К примеру:
В концентрированных HNO3 и H2SO4 алюминий пассивируется. Благодаря этому, возможно хранить и транспортировать данные кислоты в емкостях, изготовленных из алюминия.
6. Взаимодействует со щелочами, так как они растворяют оксидную пленку.
7. Взаимодействует со всеми неметаллами, кроме водорода. Для проведения реакции с кислородом нужен мелкораздробленный алюминий. Реакция возможна только при высокой t:
- 4Al + 3O2 → 2Al2O3.
По своему тепловому эффекту данная реакция относится к экзотермическим. Взаимодействие с серой образует сульфид алюминия Al
8. Взаимодействует с другими металлами, образуя алюминиды (FeAl3 CuAl2, CrAl7 и др.).
Получение алюминия:Металлический алюминий получают электролизом раствора глинозема Al2O3 в расплавленном криолите Na2AlF6 при 960–970°С.
К переходным относятся элементы побочных подгрупп Периодической таблицы. Рассмотрим химические свойства меди, цинка, хрома и железа.
Химические свойства меди
1. В электрохимическом ряду находится правее Н, поэтому данный металл малоактивен.
2. Слабый восстановитель.
3. В соединениях проявляет степени окисления +1 и +2.
4. Взаимодействует с кислородом при нагревании, образуя:
- оксид меди (I) 2Cu + O2 → 2CuO (при t 4000C)
- или оксид меди (II): 4Cu + O2 → 2Cu2O (при t 2000C).
Оксиды обладают основными свойствами. При нагревании в инертной атмосфере Cu2O диспропорционируется: Cu2O → CuO + Cu. Оксид меди (II) CuO в реакциях со щелочами образует купраты, к примеру: CuO + 2NaOH → Na2CuO2 + H2O.
5. Гидроксид меди Си(ОН)2 амфотерен, основные свойства в нем преобладают. В кислотах он растворяется легко:
- Сu(OH)2 + 2HNO3 → Cu(NO3)2 + 2H2O,
а в концентрированных растворах щелочей с трудом:
- Сu(OH)2 + 2NaOH → Na2[Cu(OH)4].
6. Взаимодействие меди с серой при различных температурных условиях, также образует два сульфида. При нагревании до 300-4000С в вакууме образуется сульфид меди (I):
При комнатной t, растворив серу в сероводороде, можно получить сульфид меди (II):
7. Из галогенов взаимодействует со фтором, хлором и бромом, образуя галогениды (CuF2, CuCl2, CuBr2), йодом, образуя йодид меди (I) CuI; не взаимодействует с водородом, азотом, углеродом, кремнием.
8. С кислотами — неокислителями не реагирует, потому как они окисляют только металлы, расположенные до водорода в электрохимическом ряду. Данный химический элемент реагирует с кислотами — окислителями: разбавленной и концентрированной азотной и концентрированной серной:
3Cu + 8HNO3(разб) → 3Cu(NO3)2 + 2NO↑ + 4H2O;
Cu + 4HNO3(конц) → Cu(NO3)2 + 2NO2 + 2H2O;
Cu + 2H2SO4(конц) → CuSO4 + SO2↑ + 2H2O.
9. Взаимодействуя с солями, медь вытесняет из их состава металлы, расположенные правее неё в электрохимическом ряду. К примеру,
Здесь мы видим, что медь перешла в раствор, а железо (III) восстановилось до железа (II). Данная реакция имеет важное практическое значение и применяется для удаления меди, напыленной на пластмассу.
Химические свойства цинка
1. Самый активный после щелочноземельных металлов.2. Обладает выраженными восстановительными свойствами и амфотерными свойствами.
3. В соединениях проявляет степень окисления +2.
4. На воздухе покрывается оксидной пленкой ZnO.
5. Взаимодействие с водой возможно при температуре красного каления. В результате образуется оксид цинка и водород:
6. Взаимодействует с галогенами, образуя галогениды (ZnF2 — фторид цинка, ZnBr2 — бромид цинка, ZnI2 — йодид цинка, ZnCl2 — хлорид цинка).
7. С фосфором образует фосфиды Zn3P2 и ZnP2.
8. С серой халькогенид ZnS.
9. Непосредственно не реагирует с водородом, азотом, углеродом, кремнием и бором.
10. Взаимодействует с кислотами — неокислителями, образуя соли и вытесняя водород. К примеру:
- H2SO4 + Zn → ZnSO4 + H2↑
- Zn + 2HCl → ZnCl2 + H2↑.
С кислотами — окислителями тоже реагирует: с конц. серной кислотой образует сульфат цинка и сернистый газ:
- Zn + 2H2SO4 → ZnSO4 + SO2↑ + 2H2O.
11. Активно реагирует со щелочами, так как цинк — амфотерный металл. С растворами щелочей образует тетрагидроксоцинкаты и выделяя водород:
- Zn + 2NaOH + 2H2O → Na2[Zn(OH)4] + H2↑.
На гранулах цинка, впоследствии реакции, появляются пузырьки газа. С безводными щелочами при сплавлении образует цинкаты и выделяет водород:
- Zn + 2NaOH → Na2ZnO2 +H2↑.
Химические свойства хрома
1. В обычных условиях инертен, при нагревании активен.
2. Обладает амфотерными свойствами.
3. Образует окрашенные соединения.
4. В соединениях проявляет степени окисления +2 (основный оксид CrO черного цвета), +3 (амфотерный оксид Cr2O3 и гидроксид Cr(OH)3 зеленого цвета) и +6 (кислотный оксид хрома (VI) CrO3 и кислоты: хромовая H2CrO4 и двухромовая H2Cr2O7 и др.).
5. Со фтором взаимодействует при t 350-4000C, образуя фторид хрома (IV):
6. C кислородом, азотом, бором, кремнием, серой, фосфором и галогенами при t 6000C:
- соединение с кислородом образует оксид хрома(VI) CrO3 (тёмно-красные кристаллы),
- соединение с азотом — нитрид хрома CrN (черные кристаллы),
- соединение с бором — борид хрома CrB (желтые кристаллы),
- соединение с кремнием — силицид хрома CrSi,
- соединение с углеродом — карбид хрома Cr3C2.
7. С водяным паром реагирует, находясь в раскалённом состоянии, образуя оксид хрома (III) и водород:
- 2Cr + 3H2O → Cr2O3 + 3H2.
8. С растворами щелочей не реагирует, однако медленно реагирует с их расплавами, образуя хроматы:
- 2Cr + 6KOH → 2KCrO2 + 2K2O + 3H2.
9. В разбавленных сильных кислотах растворяется, образуя соли. Если реакция проходит на воздухе образуются соли Cr3+, например:
- 2Cr + 6HCl + O2 → 2CrCl3 + 2H2O + H2.
Если же без воздуха, то соли Cr2+, например:
- Cr + 2HCl → CrCl2 + H2.
10. С концентрированными серной и азотной кислотами, а также с царской водкой, реагирует только при нагревании, т.к. при низких t эти кислоты пассивируют хром. Реакции с кислотами при нагревании выглядят так:
Оксид хрома(II) CrO — твердое вещество черного или красного цвета, не растворяющееся в воде.
Химические свойства:
- Обладает основными и восстанавливающими свойствами.
- При нагревании до 1000С на воздухе окисляется до Cr2O3 — оксида хрома (III).
- Возможно восстановление хрома водородом из данного оксида: CrO + Н2 → Cr + H2O или коксом: CrO + С → Cr + СO.
- Реагирует с соляной кислотой, при этом выделяя водород: 2CrO + 6HCl → 2CrCl3 + H2↑ + 2H2O.
- Не реагирует со щелочами, разбавленными серной и азотной кислотами.
Оксид хрома (III) Cr2O3 — тугоплавкое вещество, темно-зеленого цвета, нерастворяющееся в воде.
Химические свойства:
- Обладает амфотерными свойствами.
- Как основный оксид взаимодействует с кислотами: Cr2O3 + 6HCl → CrCl3 + 3H2O.
- Как кислотный оксид взаимодействует со щелочами: Cr2O3 + 2КОН → 2КCrО3 + H2O.
- Сильные окислители окисляют Cr2O3 до хромата H2CrO4.
- Сильные восстановители восстанавливают Cr из Cr2O3.
Гидроксид хрома(II) Cr(OH)2 — твердое вещество желтого или коричневого цвета, плохо растворяющееся в воде.
Химические свойства:
- Слабое основание, проявляет основные свойства.
- В присутствии влаги на воздухе окисляется до Cr(OH)3 — гидроксида хрома (III).
- Реагирует с концентрированными кислотами, образуя соли хрома (II) синего цвета: Cr(OH)2 + H2SO4 → CrSO4 + 2H2O.
- Не реагирует со щелочами и разбавленными кислотами.
Гидроксид хрома (III) Cr(OH)3 — вещество серо-зеленого цвета, нерастворяющееся в воде.
Химические свойства:
- Обладает амфотерными свойствами.
- Как основный гидроксид взаимодействует с кислотами: Cr(OH)3 + 3HCl → CrCl3 + 3H2O.
- Как кислотный гидроксид взаимодействует со щелочами: Cr(OH)3 + 3NaОН → Na3[Cr(OH)6].
Химические свойства железа
1. Активный металл, обладающий высокой реакционной способностью.
2. Обладает восстановительными свойствами, а также ярко выраженными магнитными свойствами.
3. В соединениях проявляет основные степени окисления +2 (со слабыми окислителями: S, I, HCl, растворами солей ), +3 (с сильными окислителями: Br и Cl) и менее характерную +6 (с О и H2O). У слабых окислителей железо принимает степень окисления +2, у более сильных +3. Степени окисления +2 соответствуют чёрный оксид FeO и зелёный гидроксид Fe(OH)2, обладающие основными свойствами. Степени окисления +3 соответствуют красно-коричневый оксид Fe2O3 и коричневый гидроксид Fe(OH)3, обладающие слабо выраженными амфотерными свойствами. Fe (+2) — слабый восстановитель, а Fe (+3) — чаще слабый окислитель. При изменении окислительно — восстановительных условий, степени окисления железа могут меняться друг с другом.
4. На воздухе при t 2000C покрывается оксидной пленкой. В обычных атмосферных условиях легко подвергается коррозии. При пропускании кислорода через расплав железа образуется оксид FeО. При сгорании железа на воздухе образуется оксид Fe2О3. При сгорании в чистом кислороде образуется оксид — железная окалина:5. C галогенами реагирует при нагревании:
- соединение с хлором образует хлорид железа(III) FeCl3,
- соединение с бромом — бромид железа (III) FeBr3,
- соединение с йодом — йодид железа (II,III) Fe3I8,
- соединение со фтором — фторид железа (II) FeF2, фторид железа(III) FeF3.
6. С серой, азотом, фосфором, кремнием и углеродом также реагирует при нагревании:
- соединение с серой образует сульфид железа(II) FeS,
- соединение с азотом — нитрид железа Fe3N,
- соединение с фосфором — фосфиды FeP, Fe2P и Fe3P,
- соединение с кремнием — силицид железа FeSi,
- соединение с углеродом — карбид железа Fe3C.
7. При высокой t взаимодействует с водой:
- 3Fe + 4Н2О → Fe3O4 + 4Н2.
8. Не реагирует с концентрированными серной и азотной кислотами, так как покрыто оксидной пленкой, пассивирующее данный металл. Если же концентрированную серную кислоту нагреть, реакция пойдет:
- 2Fe + 6Н2SО4(конц) → Fe2(SО4)3 + 3SО2↑ + 6Н2О
Реакции с соляной и разбавленной 20-% серной кислотами образуют соли железа (II):
Реакция с разбавленной 70-% серной кислотой образует сульфат железа (III):
- 2Fe + 4H2SO4 → Fe2 (SO4)3 + SO2 + 4H2O
9. С растворами щелочей не реагирует, однако медленно реагирует с расплавами щелочей, являющихся сильными окислителями:
- Fe + KClO3 + 2KOH → K2FeO4 + KCl + H2O.
10. Восстанавливает металлы, расположенные в электрохимическом ряду правее:
- Fe + SnCl2 → FeCl2 + Sn.
- 3Fe2O3 + CO → CO2 + 2Fe3O4,
- Fe3O4 + CO → CO2 + 3FeO,
- FeO + CO → CO2 + Fe.
Оксид железа (II) FeO — кристаллическое вещество черного цвета (вюстит), не растворяющееся в воде.
Химические свойства:
- Обладает основными свойствами.
- Реагирует с разбавленной соляной кислотой: FeO + 2HCl → FeCl2 + H2O.
- Реагирует с концентрированной азотной кислотой: FeO + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O.
- Не реагирует с водой и солями.
- С водородом при t 3500C восстанавливается до чистого металла: FeO +H2 → Fe + H2O.
- Также восстанавливается до чистого металла при соединении с коксом: FeO +C → Fe + CO.
- Получить данный оксид можно различными способами, один из них нагревание Fe при низком давлении О: 2Fe + O2 → 2FeO.
Оксид железа (III) Fe2O3 — порошок бурового цвета (гематит), нерастворяющееся в воде вещество. Другие названия: окись железа, железный сурик, пищевой краситель E172 и пр.
Химические свойства:
- Обладает слабовыраженными амфотерными свойствами с преобладанием основных.
- Легко взаимодействует с кислотами: Fe2O3 + 6HCl → 2 FeCl3 + 3H2O.
- С растворами щелочей не реагирует, реагирует с их расплавами, образуя ферриты: Fe2O3 + 2NaOH → 2NaFeO2 + H2O.
- При нагревании с водородом проявляет окислительные свойства: Fe2O3 + H2 → 2FeO + H2O.
- В щелочной среде с сильными окислителями проявляет восстановительные свойства: Fe2O3 + 3KNO3 + 4KOH → 2K2FeO4 + 3KNO2 + 2H2O.
Оксид железа (II, III) Fe3O4 или FeO•Fe2O3 — серовато-черное твердое вещество (магнетит, магнитный железняк), нерастворяющееся в воде вещество.
Химические свойства:
- Разлагается при нагревании более 15000С: 2Fe3O4 → 6FeO + O2.
- Реагирует с разбавленными кислотами: Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O.
- С растворами щелочей не реагирует, реагирует с их расплавами: Fe3O4 + 14NaOH → Na3FeO3 + 2Na5FeO4 + 7H2O.
- При реакции с кислородом окисляется: 4Fe3O4 + O2 → 6Fe2O3.
- С водородом при нагревании восстанавливается: Fe3O4 + 4H2 → 3Fe + 4H2O.
- Также восстанавливается при соединении с оксидом углерода: Fe3O4 + 4CO → 3Fe +4CO2.
Гидроксид железа(II) Fe(OH)2 — белое, редко зеленоватое кристаллическое вещество, нерастворяющееся в воде.
Химические свойства:
- Обладает амфотерными свойствами с преобладанием основных.
- Вступает в реакции нейтрализации кислоты-неокислителя, проявляя основные свойства: Fe(OH)2 + 2HCl → FeCl2 + 2H2O.
- При взаимодействии с азотной или концентрированной серной кислотами проявляет восстановительные свойства, образуя соли железа (III): 2Fe(OH)2 + 4H2SO4 → Fe2(SO4)3 + SO2 + 6H2O.
- При нагревании вступает в реакции с концентрированными растворами щелочей: Fe(OH)2 + 2NaOH → Na2[Fe(OH)4].
Гидроксид железа (III) Fe(OH)3 — бурое кристаллическое или аморфное вещество, нерастворяющееся в воде.
Химические свойства:
- Обладает слабовыраженными амфотерными свойствами с преобладанием основных.
- Легко взаимодействует с кислотами: Fe(OH)3 + 3HCl → FeCl3 + 3H2O.
- С концентрированными растворами щелочей образует гексагидроксоферраты (III): Fe(OH)3 + 3NaOH → Na3[Fe(OH)6].
- С расплавами щелочей образует ферраты: 2Fe(OH)3 + Na2CO3 → 2NaFeO2 + CO2 + 3H2O.
- В щелочной среде с сильными окислителями проявляет восстановительные свойства: 2Fe(OH)3 + 3Br2 + 10KOH → 2K2FeO4 + 6NaBr + 8H2O.
cknow.ru
1. Общая характеристика и химические свойства щелочных металлов.
Особенности соединений лития по сравнению с соединениями других щелочных металлов.
Гидриды, оксиды, пероксиды, гидроксиды щелочных металлов : химическая связь в соединениях, получение и свойства.
Получение натрия, гидроксида натрия и карбоната натрия в промышленности.
Взаимодействие с растворами щелочей: а)амфотерных металлов; б)неметаллов; в)кислотных оксидов; г)амфотерных оксидов.
Металлы подгруппы IA периодической системы элементов I. И. Менделеева Li, Na, К, Rb, Cs и Fr называются щелочными.
Щелочные, щелочноземельные металлы, Be и Mg относятся к наиболее электроположительным, элементам. В соединениях с другими элементами для металлов подгруппы IA типична степень окисления + 1, а для металлов подгруппы ПА +2. С ростом числа электронных слоев и увеличением радиусов энергия ионизации атомов уменьшается. Вследствие этого химическая активность элементов в подгруппах увеличивается с ростом их порядкового номера. С малой энергией ионизации связан характерный для них фотоэффект, а также окрашивание их солями пламени» газовой горелки. Благодаря легкой отдаче наружных электронов щелочные и щелочноземельные металлы образуют соединения преимущественно с ионной связью.
Щелочные и щелочноземельные металлы проявляют высокую
химическую активность. При нагревании в водороде они образуют
гидриды — солеподобные соединения, в которых водород находится
а виде отрицательно заряженного иона. На воздухе щелочные
металлы быстро окисляются, образуя в зависимости от их активности
оксиды, пероксиды, надпероксиды или озониды.
При этом Ci, Na и К’загораются на воздухе или в атмосфере сухого кислорода только
при нагревании, a, Rb и Cs самовоспламеняются без нагревания.
Образование при горении оксида состава М2О характерно только
для лития. Натрий образует пероксид состава М2O2, калий, рубидий
и цезий — надпероксиды состава МО2.
Щелочные металлы энергично взаимодействуют с водой, вытес-из нее водород и образуя соответствующие гидроксиды. Активность взаимодействия этих металлов с водой возрастает по мере увеличения порядкового номера элемента. Так,- литий реагирует с водой без плавления, натрий — плавится, калий — самовозгорает-ся , взаимодействие рубидия и цезия протекает еще более энергично. Щелочные металлы энергично взаимодействуют с галогенами, а при нагревании — с серой.
Гидроксиды щелочных металлов — соединения с преимуществен-
но ионной связью. В водных растворах они нацело диссоциируют
ным характером связи объясняется и их высокая термическая
устойчнвость:они не, отщепляют воду дажепри нагревании до температуры кипения (выше 1300 °С) Исключение составляет, гидроксид лития, который при нагревании разлагается с отщепле-нием ,воды. Поведение лития отличается и в других отношениях от поведения остальных щелочных металлов. Это объясняется его неполной электронной аналогией с остальными элементами группы.
Из щелочных металлов только литий при сравнительно небольшом нагревании взаимодействует с азотом, углеродом и крем-нием, образуя соответственно нитрид Li3N, карбид Li2С2 и силицид Li6Si2. В присутствии влаги образование нитрида идёт уже при комнатной температуре.
В отличие от щелочных металлов, почти все соли которых хорошо растворимы в воде, литий образует малорастворимый фторид LiF карбонат Li2CO3 и фосфат Li3PO4.
Кальций, стронций и барий по отношению к кислороду и воде ведут себя подобно щелочным металлам. Они разлагают воду с выделением водорода и образованием гидроксидов М(ОН)2. Взаимодействуя с кислородом, образуют оксиды (СаО) и пероксиды (SrO2, ВаО2), которые реагируют с водой подобно аналогичным соединениям щелочных металлов.
Магний также существенно отличается от щелочноземельных металлов. Например, из-за малой растворимости его гидроксида он не взаимодействует с холодной водой. При нагревании процесс облегчается.
В целом металлы подгруппы ПА химически активны: при нагревании они взаимодействуют с Галогенами и серой с .образованием соответствующих солей, соединяются с молекулярным азотом.
Соли щелочноземельных металлов, как и соли щелочных металлов, состоят из ионов. Соли этих металлов окрашивают пламя горелки в характерные цвета, для соединений Be и Mg этого не наблюдается.
В отличие от солей щелочных металлов многие соли металлов подгруппы ПА малорастворимы, в частности фториды (кроме BeF2). сульфаты (кроме BeSО4 и MgSO4), карбонаты. Из водных раствороэ Ве2+ осаждается в виде основных карбонатов перемен-.ного состава, Mg2+— в виде 4MgCO3-Mg(OH)2-5H2O, а Са2+, Sr2+ и Ва2+ осаждаются в виде средних карбонатов МСОз.
А) Be+2NaOH= Na2BeO2+h3
Al+NaOH+h3O=NaAlO2+h3
Б) Неметаллы, за исключением галогенов, не реагируют с растворами щелочей
Cl2+NaOH=NaClO3+NaCl+h3O
В) кислотные оксиды растворяются только в щелочах с образование соли и воды
SO3+2NaOH=Na2So4+h3o
Г) Амф ме реагируют с сильными щелочами, проявляя этим свои кислотные свойства, например:
ZnO + 2NaOH → Na2ZnO2 + H2O Амфотерные оксиды могут реагировать с щелочами двояко: в растворе и в расплаве.
При реакции с щёлочью в расплаве образуется обычная средняя соль(как показано на примере выше).
При реакции с щёлочью в растворе образуется комплексная соль.
Al2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4] (В данном случае образуется тетрагидроксоаллюминат натрия)
studfiles.net
Щелочные металлы — реферат
Щелочные металлы.
Щелочные металлы — элементы главной подгруппы I группы Периодической системы химических элементов Д. И. Менделеева: литий Li, натрий Na, калий K, рубидий Rb, цезий Cs и франций Fr. Эти металлы получили название щелочных, потому что большинство их соединений растворимо в воде. По-славянски «выщелачивать» означает «растворять», это и определило название данной группы металлов. При растворении щелочных металлов в воде образуются растворимые гидроксиды, называемые щёлочами.
Основная характеристика
щелочных металлов: В Периодической системе они
следуют сразу за инертными газами, поэтому
особенность строения атомов щелочных
металлов заключается в том, что они содержат
один электрон на новом энергетическом
уровне: их электронная конфигурация ns1.
Очевидно, что валентные электроны щелочных
металлов могут быть легко удалены, потому
что атому энергетически выгодно отдать
электрон и приобрести конфигурацию инертного
газа. Поэтому для всех щелочных металлов
характерны восстановительные свойства.
Это подтверждают низкие значения их потенциалов
ионизации (потенциал ионизации атома
цезия — один из самых низких) и электроотрицательности
(ЭО).
Все металлы этой
подгруппы имеют серебристо-
Щелочные металлы
встречаются в природе в форме
соединений, содержащих однозарядные
катионы. Многие минералы содержат в
своём составе металлы главной подгруппы
I группы. Например, ортоклаз, или полевой
шпат, состоит из алюмюсиликата калия
K2[Al2Si6O16], аналогичный минерал, содержащий
натрий — альбит — имеет состав Na2[Al2Si6O16].
В морской воде содержится хлорид натрия
NaCl, а в почве — соли калия — сильвин KCl,
сильвинит NaCl • KCl, карналлит KCl • MgCl2 •
6h3O, полигалит K2SO4 • MgSO4 • CaSO4 • 2h3O.
Химические свойства щелочных металлов
Из-за высокой химической активности щелочных
металлов по отношению к воде, кислороду,
азоту их хранят под слоем керосина. Чтобы
провести реакцию со щелочным металлом,
кусочек нужного размера аккуратно отрезают
скальпелем под слоем керосина, в атмосфере
аргона тщательно очищают поверхность
металла от продуктов его взаимодействия
с воздухом и только потом помещают образец
в реакционный сосуд.
1. Взаимодействие
с водой. Важное свойство
При проведении аналогичной
реакции натрий горит жёлтым пламенем
и происходит небольшой взрыв. Калий
ещё более активен: в этом случае
взрыв гораздо сильнее, а пламя
окрашено в фиолетовый цвет.
2. Взаимодействие с кислородом. Продукты
горения щелочных металлов на воздухе
имеют разный состав в зависимости от
активности металла.
Только литий сгорает на воздухе с образованием оксида стехиометрического состава:
При горении натрия в основном образуется пероксид Na2O2 с небольшой примесью надпероксида NaO2:
В продуктах горения калия, рубидия и цезия содержатся в основном надпероксиды:
Для получения оксидов
натрия и калия нагревают смеси
гидроксида, пероксида или надпероксида
с избытком металла в отсутствие кислорода:
Для кислородных соединений щелочных
металлов характерна следующая закономерность:
по мере увеличения радиуса катиона щелочного
металла возрастает устойчивость кислородных
соединений, содержащих пероксид-ион О22-и
надпероксид-ион O2-.
Для тяжёлых щелочных металлов характерно образование довольно устойчивых озонидов состава ЭО3. Все кислородные соединения имеют различную окраску, интенсивность которой углубляется в ряду от Li до Cs:
Формула | Цвет |
Li2O | Белый |
Na2O | Белый |
K2O | Желтоватый |
Rb2O | Жёлтый |
Cs2O | Оранжевый |
Na2O2 | Светло- |
KO2 | Оранжевый |
RbO2 | Тёмно- |
CsO2 | Жёлтый |
Оксиды щелочных металлов обладают всеми свойствами, присущими основным оксидам: они реагируют с водой, кислотными оксидами и кислотами:
Пероксиды и надпероксиды проявляют свойства сильных окислителей:
Пероксиды и надпероксиды интенсивно взаимодействуют с водой, образуя гидроксиды:
3. Взаимодействие с другими веществами. Щелочные металлы реагируют со многими неметаллами. При нагревании они соединяются с водородом с образованием гидридов, с галогенами, серой, азотом, фосфором, углеродом и кремнием с образованием, соответственно, галогенидов, сульфидов, нитридов, фосфидов, карбидов и силицидов:
При нагревании щелочные металлы способны реагировать с другими металлами, образуя интерметаллиды. Активно (со взрывом) реагируют щелочные металлы с кислотами.
Щелочные металлы растворяются в жидком аммиаке и его производных — аминах и амидах:
При растворении в жидком аммиаке щелочной металл теряет электрон, который сольватируется молекулами аммиака и придаёт раствору голубой цвет. Образующиеся амиды легко разлагаются водой с образованием щёлочи и аммиака:
Щелочные металлы
4. Качественное определение щелочных металлов. Поскольку потенциалы ионизации щелочных металлов невелики, то при нагревании металла или его соединений в пламени атом ионизируется, окрашивая пламя в определённый цвет:
Окраска пламени щелочными металлами | |
Li | Карминно-красный |
Na | Жёлтый |
K | Фиолетовый |
Rb | Беловато-розовый |
Cs | Фиолетово-красный |
Получение щелочных металлов
1. Для получения щелочных металлов используют
в основном электролиз расплавов их галогенидов,
чаще всего — хлоридов, образующих природные
минералы:
катод: Li+ + e → Li
анод: 2Cl- — 2e → Cl2
2. Иногда для получения щелочных металлов
проводят электролиз расплавов их гидроксидов:
катод: Na+ + e → Na
анод: 4OH- — 4e → 2h3O + O2
Поскольку щелочные металлы в электрохимическом
ряду напряжений находятся левее водорода,
то электролитическое получение их из
растворов солей невозможно; в этом случае
образуются соответствующие щёлочи и
водород.
Соединения щелочных
металлов. Гидроксиды
Для получения гидроксидов щелочных
металлов в основном используют электролитические
методы. Наиболее крупнотоннажным является
производство гидроксида натрия электролизом
концентрированного водного раствора
поваренной соли:
ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ
Общая характеристика
К щелочноземельным металлам относятся следующие элементы главной подгруппы II-ой группы Периодической системы: кальций, стронций, барий и радий. Магний имеет ряд сходных со щелочными металлами свойств, бериллий по химическим свойствам ближе к алюминию.Щелочноземельные металлы являются электронными аналогами, внешний электронный уровень имеет строение ns2, в соединениях наиболее характерная степень окисления +2. В соединениях с неметаллами основой тип связи – ионный. Соединения щелочноземельных металлов окрашивают бесцветное пламя газовой горелки: кальция – в оранжево-красный, стронция – в темно-красный, бария – в светло-зеленый цвет. В природе щелочноземельные металлы встречаются только в виде соединений, основные минералы кальция –кальцит (извесковый шпат, известняк, мрамор, мел) СаСО3, доломит CaMg(CO3)2, гипс CaSO4 2H2O, флюорит CaF2, гидроксиапатит (фосфорит) Ca5(PO4)3(OH), апатит Ca5(PO4)3F,Cl. Основные минералы стронция – стронцианит SrCO3 и целестин SrSO4, бария – витерит BaCO3 и барит BaSO4.
Физические свойства
Внешне – серебристо-белые блестящие металлы, твердость значительно выше, чем у щелочных металлов. Твердость по группе уменьшается сверху вниз, барий по твердости близок к свинцу. Температуры плавления щелочноземельных металлов выше, чем у щелочных и составляют: для кальция 851оС, стронция 770оС, бария 710оС. Плотности щелочноземельных металлов в подгруппе сверху вниз увеличиваются и равны для Са, Sr и Ва, соответственно 1,54, 2,63 и 3,76 г/см3.
Химические свойства щелочноземельных металлов
Щелочноземельные металлы химически весьма активны, в реакциях проявляют свойства восстановителей. Взаимодействуют с
1. Кислородом (горят на воздухе)
2Са + О2 = 2СаО
2Sr + O2 = 2SrO
2Ba + O2 = 2BaO
При этом образуются и нитриды состава Me3N2. При контакте щелочноземельных металлов с воздухом при комнатной температуре на поверхности металлов образуетсяжелтоватая пленка, состоящая из оксидов, гидроксидов и нитридов.
Оксид бария при нагреваии до 500оС образуeт пероксид:
2BaO + O2 = 2BaO2
который разлагается при температуре выше 800оС:
2BaO2 = 2BaO + O2
2. С водородом при нагревании образуют гидриды
Ca + H2 = CaH2
Ba + H2 = BaH2
3. С серой реагируют в обычных условиях, образуя сульфиды
Ca + S = CaS
и полисульфиды
CaS + nS = CaSn+1
4. С азотом – при нагревании образуют нитриды
3Ca + N2 = Ca3N2
5. C фосфором – фосфиды
3Ca + 2Р = Ca3Р2
6. С углеродом – при
нагревании образуются карбиды,
Са + 2С = СаС2
7. С водой – растворяются с выделением водорода, реакция протекает спокойнее, чем со щелочными металлами:
Са + 2Н2О = Са(ОН)2 + Н2
8. Восстанавливают другие металлы из их соединений, например:
UF4 + 2Ca = U + 2CaF2
Активность взаимодействия с водой возрастает от кальция к барию.
Получение щелочноземельных металлов
Кальций получают электролизом расплaва хлорида кальция СаCl2, к которому добавляют 5-7% CaF2 для снижения температуры плавления:
СаCl2 = Са(катод) + Cl2(анод)
Стронций и барий получают методом алюмотермии из оксидов:
3BaO + 2Al = 3Ba + Al2O3
Применение щелочноземельных металлов
Металлический кальций применяется как восстановитель и легирующая добавка к сплавам.
referat911.ru
Проверяемые элементы: Характерные химические свойства простых веществ- металлов: щелочных, щелочноземельных, алюминия; переходных металлов: меди,
52bc3c62.png» NAME=»Рисунок 1″ ALIGN=BOTTOM WIDTH=96 HEIGHT=88 BORDER=0>Часть 1. Задание А8.Проверяемые элементы: Характерные химические свойства простых веществ-
металлов: щелочных, щелочноземельных, алюминия; переходных металлов: меди,
цинка, хрома, железа. Характерные химические свойства простых веществ-
неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода,
кремния.
Теория:
Химические свойства — свойства веществ (химических элементов, простых веществ и химических соединений), имеющие отношение к химическим процессам, то есть проявляемые в процессе химической реакции.
Металлы:
Химические свойства металлов:
В химическом отношении все металлы характеризуются сравнительной легкостью отдачи валентных электронов и способностью образовывать положительно заряженные ионы. Следовательно, металлы в свободном состоянии являются восстановителями.
Восстановительная способность различных металлов неодинакова и определяется положением в электрохимическом ряду напряжения металлов:
Li K Rb Cs Ca Na Mg Al Mn Zn Cr Cr Fe Ni Sn Pb Cu Hg Ag Pt Ag Pt Au
Металлы размещены в порядке убывания их восстановительных свойств и усиления окислительных свойств их ионов. Этот ряд характеризует химическую активность металлов только в окислительно-восстановительных реакциях, протекающих в водной среде.
Характерными свойствами для металлов являются следующие:
Восстановление неметаллов Реакции с галогенами и кислородом воздуха протекают с различными скоростями и при различных температурах с разными металлами. Так, щелочные металлы легко окисляются кислородом воздуха и взаимодействуют с простыми веществами, железо и медь взаимодействуют с простыми веществами только при нагревании, золото и платиновые металлы не окисляются вообще. Многие металлы образуют на поверхности оксидную пленку, которая защищает их от дальнейшего окисления. 2Мg + О2 = 2МgО 4Аl + ЗО2 = 2А12О3 2К + Сl2 = 2КСl
Менее энергично металлы взаимодействуют с серой: Сu + S = СuS Fе + S = FеS
Трудно вступают в реакцию с азотом и фосфором: ЗМg + N2 = Мg3N2 (нитрид магния)
ЗСа + 2Р = Са3Р2 (фосфид кальция) Активные металлы взаимодействуют с водородом:
Са + Н2 = СаН2 (гидрид кальция)
Взаимодействие с водой Активные металлы (щелочные металлы) взаимодействуют с водой при обычных условиях с образованием гидроксидов и выделением водорода: 2Nа + 2Н2О == 2NаОН + Н2 Са + 2Н2О = Са(ОН)2 + Н2 2Аl + 6Н2O = 2Аl(ОН)3 + ЗН2.
^
К щелочным металлам относятся элементы первой группы, главной подгруппы: литий Li, натрий Na, калий K, рубидий Rb, цезий Cs и франций Fr. При растворении щелочных металлов в воде образуются растворимые гидроксиды, называемые щёлочами.
^
| 1. | С кислородом (Rb, Cs — самовоспламеняются) | 2Na+O2=Na2O2; 2K+2O2=K2O4 (пероксиды) 4Li+O2=2Li2O (оксид лития) |
| 2. | С галогенами | 2Na+Cl2=2NaCl |
| 3. | С серой при нагревании | 2Li+S=Li2S (сульфид) |
| 4. | Литий взаимодействует с азотом | 6Li+N2=2Li3N ( нитрид) |
| 5. | С водородом при нагревании | 2Na+h3=2NaH (гидрид) |
| 6. | С водой | 2Na+2h3O=2NaOH+h3 |
^
К щелочноземельным металлам относятся элементы главной подгруппы второй группы: бериллий, магний, кальций, стронций, барий, радий.
^
Щелочноземельные металлы легко реагируют с кислородом, галогенами, неметаллами, водой и кислотами, особенно при нагревании:
— особенно легко эта реакция протекает для кальция и бария, поэтому их хранят в особых условиях
— персульфид бария BaS – люминофор
— при гидролизе ацетиленидов образуется ацетилен:
Алюминий
Химические свойства алюминия:
| 1. | С кислородом | 4Al+3O2=2Al2O3 |
| 2. | С галогенами | 2Al+3Cl2=2AlCl3 |
| 3. | С серой при нагревании | 2Al+3S=Al2S3 |
| 4. | С углеродом | 4Al+3C=Al4C3 |
| 5. | Алюминотермия | 8Al+3Fe3O4=4Al2O3+9Fe |
| 6. | С водой (после разрушения оксидной пленки) | 2Al+6h3O=2Al(OH)3+3h3 |
| 7. | Растворяется в щелочах | 2Al+2NaOH+6h3O=2Na[Al(OH)4]+3h3 |
| 8. | Реагирует с кислотами | 2Al+6HCl=2AlCl3+3h3 |
| 9. | С азотной и концентрированной серной кислотами на холоду не реагируют. При нагревании | Al+6h3SO4(конц.)=Al2(SO4)3+3SO2+6h3O Al+6HNO3=Al(NO3)3+3NO2+3h3O |
^
Химические свойства меди:
| 1. | Взаимодействует с неметаллами при высоких температурах | 2Cu + O2 = 2CuO Cu + Cl2 = CuCl2 |
| 2. | Медь стоит в ряду напряжений правее водорода, поэтому не реагирует с разбавленными соляной и серной кислотами, но растворяется в кислотах – окислителях | 3Cu + 8HNO3(разб.) = 3Cu(NO3)2 + 2NO + 2h3O Cu + 4HNO3(конц.) = Cu(NO3)2 + 2NO2 + 2h3O Cu + 2h3SO4(конц.) = CuSO4 + SO2+2h3O |
Сплавы меди с оловом — бронзы, с цинком — латуни.
^
Химические свойства цинка:
| 1. | На воздухе цинк покрывается тонкой пленкой оксида ZnO. При сильном нагревании сгорает с образованием амфотерного белого оксида ZnO | 2Zn + O2 = 2ZnO. |
| 2. | Оксид цинка реагирует с растворами кислот | ZnO + 2HNO3 = Zn(NO3)2 + h3O |
| 3. | С щелочами | ZnO + 2NaOH = Na2ZnO2 + Н2О |
| 4. | Цинк обычной чистоты активно реагирует с растворами кислот | Zn + 2HCl = ZnCl2 + h3↑, Zn + h3SO4(разб.) = ZnSO4 + h3↑ |
| 5. | С растворами щелочей | Zn + 2NaOH + 2h3O = Na2[Zn(OH)4] + h3↑, образуя гидроксоцинкаты |
С растворами кислот и щелочей очень чистый цинк не реагирует. Взаимодействие начинается при добавлении нескольких капель раствора сульфата меди CuSO4.
При нагревании цинк реагирует с галогенами с образованием галогенидов ZnHal2. С фосфором цинк образует фосфиды Zn3P2 и ZnP2. С серой и её аналогами — селеном и теллуром — различные халькогениды, ZnS, ZnSe, ZnSe2 и ZnTe.
С водородом, азотом, углеродом, кремнием и бором цинк непосредственно не реагирует. Нитрид Zn3N2 получают реакцией цинка с аммиаком при 550—600 °C.
В водных растворах ионы цинка Zn2+ образуют аквакомплексы [Zn(h3O)4]2+ и [Zn(h3O)6]2+.
^
Химические свойства хрома:
В ряду Cr – Mo – W химическая активность падает.
С увеличением степени окисления элементов у их оксидов и гидроксидов законо-мерно происходит ослабление основных свойств и усиление кислотных. Высшим оксидам RO3 соответствуют кислоты h3RO4.
В том же направлении происходит усиление окислительных свойств соединений.
Железо
| 1. | На воздухе железо легко окисляется в присутствии влаги (ржавление) | 4Fe + 3O2 + 6h3 O = 4Fe(OH)3 |
| 2. | Накалённая железная проволока горит в кислороде, образуя окалину — оксид железа (II,III) | 3Fe + 2O2 = Fe3O4 |
| 3. | При высокой температуре (700–900C) железо реагирует с парами воды | 3Fe + 4h3O = Fe3O4 + 4h3 |
| 4. | Железо реагирует с неметаллами при нагревании | 2Fe + 3Br2 = 2FeBr3 Fe + S = FeS |
| 5. | Железо легко растворяется в соляной и разбавленной серной кислотах | Fe + 2HCl = FeCl2 + h3 Fe + h3SO4(разб.) = FeSO4 + h3 |
| 6. | В концентрированных кислотах–окислителях железо растворяется только при нагревании | 2Fe + 6h3SO4(конц.) = Fe2(SO4)3 + 3SO2 + 6h3O Fe + 6HNO3(конц.) = Fe(NO3)3 + 3NO2 + 3h3O |
| 7. | (На холоде концентрированные азотная и серная кислоты пассивируют железо). Железо вытесняет металлы, стоящие правее его в ряду напряжений из растворов их солей. | Fe + CuSO4 = FeSO4 + Cu |
Неметаллы
Химические свойства неметаллов:
Химические элементы-неметаллы могут проявлять как окислительные, так и восстановительные свойства, в зависимости от химического превращения, в котором они принимают участие.
Атомы самого электроотрицательного элемента – фтора – не способны отдавать электроны, он всегда проявляет только окислительные свойства, другие элементы могут проявлять и восстановительные свойства, хотя намного в меньшей степени, чем металлы. Наиболее сильными окислителями являются фтор, кислород и хлор, преимущественно восстановительные свойства проявляют водород, бор, углерод, кремний, фосфор, мышьяк и теллур. Промежуточные окислительно-восстановительные свойства имеют азот, сера, йод.
| Взаимодействие с металлами | 2Na + Cl2 = 2NaCl, Fe + S = FeS, 6Li + N2 = 2Li3N, 2Ca + O2 = 2CaO |
Вэтих случаях неметаллы проявляют окислительные свойства, они принимают электроны, образуя отрицательно заряженные частицы.
| Взаимодействие с другими неметаллами | ||
| 1. | Взаимодействуя с водородом, большинство неметаллов проявляет окислительные свойства, образуя летучие водородные соединения – ковалентные гидриды | 3h3 + N2 = 2Nh4, h3 + Br2 = 2HBr; |
| 2. | взаимодействуя с кислородом , все неметаллы, кроме фтора, проявляют восстановительные свойства | S + O2 = SO2, 4P + 5O2 = 2P2O5; |
| 3. | при взаимодействии с фтором фтор является окислителем, а кислород – восстановителем | 2F2 + O2 = 2OF2 |
| 4. | неметаллы взаимодействуют между собой, более электроотрицательный металл играет роль окислителя, менее электроотрицательный – роль восстановителя | S + 3F2 = SF6, C + 2Cl2 = CCl4 |
^
Химические свойсва водорода:
| 1. | Молекулы водорода Н2 довольно прочны, и для того, чтобы водород мог вступить в реакцию, должна быть затрачена большая энергия | Н2 = 2Н − 432 кДж |
| 2. | При обычных температурах водород реагирует только с очень активными металлами, например с кальцием, образуя гидрид кальция | Ca + Н2 = СаН2 |
| 3. | с единственным неметаллом — фтором, образуя фтороводород | F2 + h3 = 2HF |
| 4. | С большинством же металлов и неметаллов водород реагирует при повышенной температуре или при другом воздействии, например при освещении | О2 + 2Н2 = 2Н2О |
| 5. | Он может «отнимать» кислород от некоторых оксидов | CuO + Н2 = Cu + Н2O |
| 6. | Восстановительные свойства водорода | N2 + 3h3 → 2Nh4 |
| 7. | С галогенами образует галогеноводороды | F2 + h3 → 2HF, реакция протекает со взрывом в темноте и при любой температуре, Cl2 + h3 → 2HCl, реакция протекает со взрывом, только на свету. |
| 8. | С сажей взаимодействует при сильном нагревании | C + 2h3 → Ch5 |
| 9. | При взаимодействии с активными металлами водород образует гидриды | 2Na + h3 → 2NaH Ca + h3 → Cah3 Mg + h3 → Mgh3 |
| 10. | Гидриды — солеобразные, твёрдые вещества, легко гидролизуются | Cah3 + 2h3O → Ca(OH)2 + 2h3↑ |
| 11. | Оксиды восстанавливаются до металлов | CuO + h3 → Cu + h3O Fe2O3 + 3h3 → 2Fe + 3h3O WO3 + 3h3 → W + 3h3O |
Галогены
Химические свойства галогенов:
Рассмотрим свойства галогенов на примере хлора:
| 1. | Взаимодействие с металлами | Mg + Cl2 = MgCl2 |
| 2. | Реакции с неметаллами | h3 + Cl2 = 2HCl |
| 3. | Взаимодействие со щелочами на холоду | 2NaOH + Cl2 = NaCl + NaClO + h3O |
| 4. | Взаимодействие со щелочами при нагревании | 6NaOH + 3Cl2 = 5NaCl + NaClO3 + 3h3O |
| 5. | Вытеснение менее активных галогенов из галогенидов | 2KBr + Cl2 = 2KCl + Br2 |
| 6. | С водой | h3O + Cl2 = HCl + HClO(хлорная вода) |
Кислород
Химические свойства кислорода:
| 1. | Взаимодействие с металлами | 2Cu + O2 = 2CuO |
| 2. | Горение неметаллов | S+O2 = SO2 |
| 3. | Горение сложных веществ | 2h3S + 3O2 = 2h3O + 2SO2 |
Сера
Химические свойства серы:
| 1. | Горение серы | 2h3S + 3O2 = 2h3O + 2SO2 |
| 2. | Взаимодействие с неметаллами | h3 + S = h3S S+O2 = SO2 |
| 3. | Окисление серной кислотой | S + 2h3SO4 = 2h3O + 3SO2 |
| 4. | Взаимодействие со щелочами при нагревании | S + 2h3SO4 = 2h3O + 3SO2 |
^
Химические свойства азота:
| 1. | Взаимодействие с кислородом | N2+O2=2NO (эл.дуга, 3000 C) |
| 2. | Взаимодействие с щелочными и щелочноземельными металлами | 6Li+N2=2Li3N |
| 3. | С водородом | 3N2+3h3 2Nh4 |
Фосфор
Химические свойства фосфора:
| 1. | Взаимодействие с кислородом | 4P+5O2=2P2O5 |
| 2. | С галогенами | 2P+5Cl5=2PCl5 |
| 3. | С активными металлами | 2P+3Mg=Mg3P2 (фосфид) |
| 4. | С сильными окислителями | 3P+5HNO3+2h3O=3h4PO4+5NO |
Углерод
Химические свойства углерода:
| 1. | Восстановитель | C+O2=CO2-ниже 500 0С С+h3O=CO+h3-выше 1200 0С CuO+C=Cu+CO-при нагревании 4HNO3+3C=3CO2+4NO+2h3O |
| 2. | Окислитель | Ca+2C=CaC2 карбид кальция 2h3+C=Ch5 |
^
Химические свойства кремния:
| 1. | Восстановитель | Si+2F2=SiF4 Si+O2=SiO2 Si+Cl2=SiCl4 Si+2NaOH+h3O=Na2SiO3+2h3-нагрев. Si+C=SiC 2N2+3Si=Si3N4 (> 1000 C) |
| 2. | Окислитель | 2Ca+Si=Ca2Si силицид кальция |
Запомнить:
1. Металлы реагируют с неметаллами.
2. Металлы, стоящие до водорода, реагируют с кислотами (кроме азотной и серной конц.) с выделением водорода
3. Активные металлы реагируют с водой с образованием щелочи и выделением водорода.
4. Металлы средней активности реагируют с водой при нагревании, образуя оксид металла и водород.
5. Металлы, стоящие после водорода, с водой и растворами кислот (кроме азотной и серной конц.) не реагируют
6. Более активные металлы вытесняют менее активные из растворов их солей.
7. Галогены реагируют с водой и раствором щелочи.
8 Активные галогены (кроме фтора) вытесняют менее активные галогены из растворов их солей.
9. Галогены не реагируют с кислородом.
10. Амфотерные металлы (Al, Be, Zn) реагируют с растворами щелочей и кислот.
11. Магний реагирует с углекислым газом и оксидом кремния.
12. Щелочные металлы (кроме лития) с кислородом образуют пероксиды.
Алгоритм выполнения задания в демонстрационном варианте:
Задание:
Решение:
Цинк — элемент побочной подгруппы второй группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 30. Обозначается символом Zn. При нормальных условиях — хрупкий переходный металл голубовато-белого цвета (тускнеет на воздухе, покрываясь тонким слоем оксида цинка).
Цинк более сильный Ме, чем Медь по ряду напряжений металлов.
Более активный металл вытесняет менее активный из растворов её соли.
Ответ: Цинк взаимодействует с раствором CuSO4. Вариант 1.
Различные формулировки задания А8:
1.Медь реагирует с разбавленным водным раствором кислоты
1)серной 2)соляной 3)азотной 4)фтороводородной
2.Верны ли следующие суждения о свойствах хлора
А.Хлор реагирует как с активными, так и с неактивными металлами.
Б.Хлор не растворяется в воде
1)верно только А 2)верно только Б 3)верны оба 4)оба неверны
3.С водой без нагревания реагирует
1)цинк 2)медь 3)железо 4)литий
4.Химическая реакция возможна между
1)Cu и HCl 2)Fe и Na3PO4 3)Ag и Mg(NO3)2 4)Zn и FeCl2
5. Верны ли следующие суждения о меди
А.Для медь характерны степени окисления +1 и +2.
Б.Медь вытесняет цинк из раствора сульфата цинка
1)верно только А 2)верно только Б 3)верны оба 4)оба неверны
6.При обычных условиях практически осуществима реакция между железом и
1)серой 2)серной к-той (конц.) 3)нитратом цинка (р-р) 4)нитратом меди (II) (р-р)
7.В разбавленной серной кислоте растворяется
1)Cu 2)Zn 3)Ag 4)Au
8.
9.
ignorik.ru
