Свойства алюминия и его сплавы
Алюминий — это самый распространенный металл на Земле. Хоть в чистом виде он не встречается, известно около 300 соединений и минералов алюминия. Этот легкий и прочный металл является отличным конструкционным материалом. Где бы мы не находились — в автомобиле, поезде, самолете, в офисе, дома — всюду нас окружают изделия, где присутствует алюминий. Он находит свое применение (самостоятельно или в составе сплавов) практически во всех областях человеческой деятельности:
- строительство;
- машиностроение;
- энергетика;
- электронная техника;
- пищевая промышленность;
- медицина;
- мебельное производство;
- дизайн и оформление интерьеров;
- рекламная отрасль…
Характеристики алюминия
Алюминий сочетает в себе уникальными качества, которые позволяют ему максимально востребованным.
- Небольшой удельный вес. Применение алюминия особенно оправдано в случаях, когда вес изделия имеет особенное значение, как например, в строительстве, авиа -, ракетостроении.
- Антикоррозийные свойства алюминия. Небольшая оксидная пленка, образующаяся на поверхности, защищает его от негативных воздействий окружающей среды.
- Пластичность материала дает возможность производить сверхтонкие изделия разными способами.
- Способность соединяться с другими металлами в сплавы.
- Электропроводность.
- Огнестойкость.
- Экологичность и не токсичность.
Сплавы алюминия, используемые
Алюминиевые сплавы по сравнению с чистым алюминием имеют лучшие физико-химические и механические качества. В зависимости от состава сплавы алюминия делятся на деформируемые, которые в дальнейшем используются для прокатки, ковки, прессования, и литейные, обладающие повышенной текучестью.
Для получения новых характеристик и новых эксплуатационных возможностей в состав сплавов в разных процентных соотношениях вводятся легирующие элементы: медь, магний, марганец, цинк, кремний, никель… Так, марганец повышает коррозионную стойкость; титан, никель, хром улучшают жаропрочность сплавов; кремний применяется для создания литейных сплавов.
Знакомые всем сплавы на основе алюминия:
- дюралюминий, в состав которого входит медь, магний и марганец;
- силумин — сплав алюминия с кремнием.
В состав сплавов могут входить и другие добавки в зависимости от свойств, которые ожидают от материала.
Виды обработки алюминия
Алюминий и алюминиевые сплавы поддаются всем видам обработки — ковке, прокатке, резке, электрическим способам. Ввиду пластичности алюминия он легко обрабатывается давлением, но при механической резке негативным фактором является налипание металла на режущий инструмент. Из-за механического воздействия инструмента и возможных вибраций, возникающих в ходе механической обработки, алюминиевую заготовку приходится надежно фиксировать к рабочей поверхности. А при жесткой фиксация упругого материала не исключены деформации детали в местах крепления. Обеспечить хорошее качество реза способны термические способы обработки — плазменная или лазерная резка алюминия, действующие бесконтактно.
Из-за механического воздействия инструмента и возможных вибраций, возникающих в ходе механической обработки, алюминиевую заготовку приходится надежно фиксировать к рабочей поверхности. А при жесткой фиксация упругого материала не исключены деформации детали в местах крепления. Обеспечить хорошее качество реза способны термические способы обработки — плазменная или лазерная резка алюминия, действующие бесконтактно.
Лазерная резка алюминия
Применение лазерной технологии для раскроя и резки алюминия — это точность, качество и производительность. Резка алюминия лазером позволяет получать изделия нужного размера и конфигурации любой сложности как при серийном производстве, так и при выполнении индивидуальных заказов.
Коротко суть обработки можно описать следующим образом. Лазер направляется вдоль линии реза и благодаря сконцентрированной энергии плавит металл заготовки в узкой зоне. Резка происходит без механического контакта инструмента с заготовкой, а значит всякие деформации исключены. Благодаря тому, что луч оказывает локальное воздействие, лазерная резка не вызывает изменений физико-химических свойств материала. Еще одним достоинством лазерной резки является получение гладких кромок, не требующих дополнительной обработки.
Благодаря тому, что луч оказывает локальное воздействие, лазерная резка не вызывает изменений физико-химических свойств материала. Еще одним достоинством лазерной резки является получение гладких кромок, не требующих дополнительной обработки.
Алюминий | Химические свойства
Алюминий
Химически алюминий — довольно активный металл. На воздухе его поверхность мгновенно покрывается плотной пленкой оксида Al2О3, которая препятствует дальнейшему доступу кислорода к металлу и приводит к прекращению реакции, что обусловливает высокие антикоррозионные свойства алюминия. Защитная поверхностная пленка на алюминии образуется также, если его поместить в концентрированную азотную кислоту.
Характерная степень окисления алюминия +3, но благодаря наличию незаполненных 3р- и 3d-орбиталей атомы алюминия могут образовывать дополнительные донорно-акцепторные связи. Поэтому ион Al3+ с небольшим радиусом весьма склонен к комплексообразованию, образуя разнообразные катионные и анионные комплексы: AlCl4—, AlF63-, [Al(H2O)6]3+, Al(OH)4—, Al(OH)63-, AlH4— и многие другие. Известны комплексы и с органическими соединениями.
Известны комплексы и с органическими соединениями.
Химическая активность алюминия весьма высока; в ряду электродных потенциалов он стоит сразу за магнием. На первый взгляд такое утверждение может показаться странным: ведь алюминиевая кастрюля или ложка вполне устойчивы на воздухе, не разрушаются и в кипящей воде. Алюминий, в отличие от железа, не ржавеет. Оказывается, на воздухе металл покрывается бесцветной тонкой, но прочной из оксида, которая защищает металл от окисления. Так, если внести в пламя горелки толстую алюминиевую проволоку или пластинку толщиной 0,5-1 мм, то металл плавится, но алюминий не течет, так как остается в мешочке из его оксида. Если лишить алюминий защитной пленки или сделать ее рыхлой (например, погружением в раствор ртутных солей), алюминий тут же проявит свою истинную сущность: уже при комнатной температуре начнет энергично реагировать с водой с выделением водорода: 2Al + 6H2O -> 2Al(OH)3 + 3H2. На воздухе лишенный защитной пленки алюминий прямо на глазах превращается в рыхлый порошок оксида: 2Al + 3O2 -> 2Al2O3.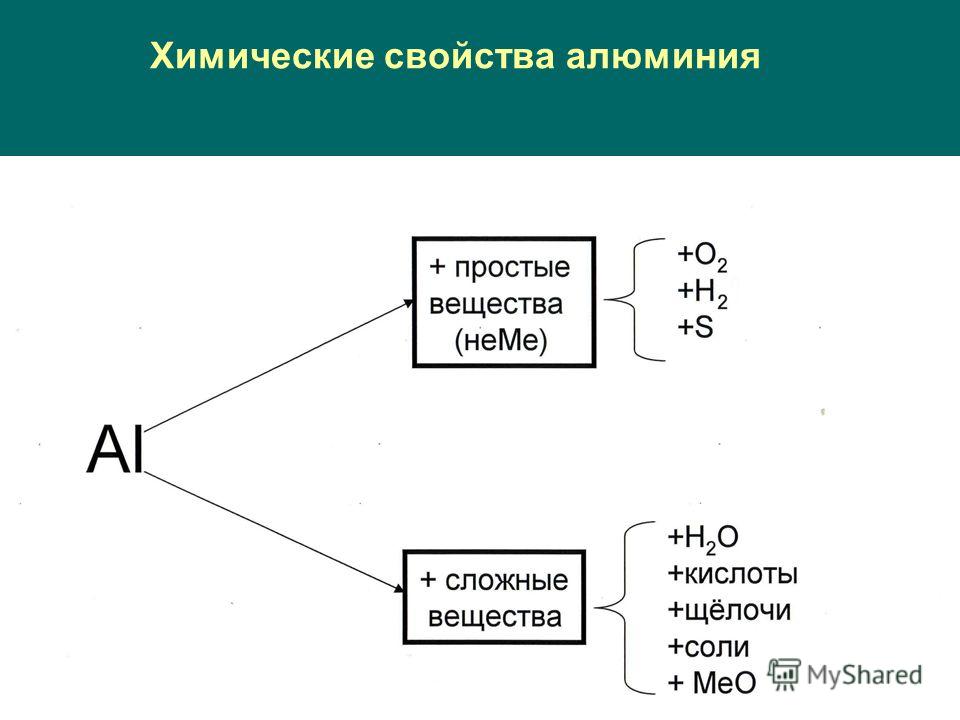 Особенно активен алюминий в мелкораздробленном состоянии; алюминиевая пыль при вдувании в пламя моментально сгорает. Если смешать на керамической пластинке алюминиевую пыль с пероксидом натрия и капнуть на смесь водой, алюминий также вспыхивает и сгорает белым пламенем.
Особенно активен алюминий в мелкораздробленном состоянии; алюминиевая пыль при вдувании в пламя моментально сгорает. Если смешать на керамической пластинке алюминиевую пыль с пероксидом натрия и капнуть на смесь водой, алюминий также вспыхивает и сгорает белым пламенем.
Очень высокое сродство алюминия к кислороду позволяет ему отнимать кислород от оксидов ряда других металлов, восстанавливая их (метод алюминотермии). Самый известный пример — термитная смесь, при горении которой выделяется так много тепла, что полученное железо расплавляется: 8Al + 3Fe3O4 -> 4Al2O3 + 9Fe. Эта реакция была открыта в 1856 Н.Н.Бекетовым. Таким способом можно восстановить до металлов Fe2O3, CoO, NiO, MoO3, V2O5, SnO2, CuO, ряд других оксидов. При восстановлении же алюминием Cr2O3, Nb2O5, Ta2O5, SiO2, TiO2, ZrO2, B2O3 теплоты реакции недостаточно для нагрева продуктов реакции выше их температуры плавления.
Алюминий легко растворяется в разбавленных минеральных кислотах с образованием солей. Концентрированная азотная кислота, окисляя поверхность алюминия, способствует утолщению и упрочнению оксидной пленки (так называемая пассивация металла). Обработанный таким образом алюминий не реагирует даже с соляной кислотой. С помощью электрохимического анодного окисления (анодирования) на поверхности алюминия можно создать толстую пленку, которую нетрудно окрасить в разные цвета.
Вытеснение алюминием из растворов солей менее активных металлов часто затруднено защитной пленкой на поверхности алюминия. Эта пленка быстро разрушается хлоридом меди, поэтому легко идет реакция 3CuCl2 + 2Al -> 2AlCl3 + 3Cu, которая сопровождается сильным разогревом. В крепких растворах щелочей алюминий легко растворяется с выделением водорода: 2Al + 6NaOH + 6Н2О -> 2Na3[Al(OH)6] + 3H2 (образуются и другие анионные гидроксо-комплексы). Амфотерный характер соединений алюминия проявляется также в легком растворении в щелочах его свежеосажденного оксида и гидроксида. Кристаллический оксид (корунд) весьма устойчив к действию кислот и щелочей. При сплавлении со щелочами образуются безводные алюминаты: Al2O3 + 2NaOH -> 2NaAlO2 + H2O. Алюминат магния Mg(AlO2)2 — полудрагоценный камень шпинель, обычно окрашенный примесями в самые разнообразные цвета.
Кристаллический оксид (корунд) весьма устойчив к действию кислот и щелочей. При сплавлении со щелочами образуются безводные алюминаты: Al2O3 + 2NaOH -> 2NaAlO2 + H2O. Алюминат магния Mg(AlO2)2 — полудрагоценный камень шпинель, обычно окрашенный примесями в самые разнообразные цвета.
Бурно протекает реакция алюминия с галогенами. Если в пробирку с 1 мл брома внести тонкую алюминиевую проволоку, то через короткое время алюминий загорается и горит ярким пламенем. Реакция смеси порошков алюминия и иода инициируется каплей воды (вода с иодом образует кислоту, которая разрушает оксидную пленку), после чего появляется яркое пламя с клубами фиолетовых паров иода. Галогениды алюминия в водных растворах имеют кислую реакцию из-за гидролиза: AlCl3 + H2O -> Al(OH)Cl2 + HCl.
Реакция алюминия с азотом идет только выше 800° С с образованием нитрида AlN, с серой — при 200° С (образуется сульфид Al2S3), с фосфором — при 500° С (образуется фосфид AlP). При внесении в расплавленный алюминий бора образуются бориды состава AlB2 и AlB12 — тугоплавкие соединения, устойчивые к действию кислот. Гидрид (AlH)х (х = 1,2) образуется только в вакууме при низких температурах в реакции атомарного водорода с парами алюминия. Устойчивый в отсутствие влаги при комнатной температуре гидрид Alh4 получают в растворе безводного эфира: AlCl3 + LiH -> AlH3 + 3LiCl. При избытке LiH образуется солеобразный алюмогидрид лития LiAlH4 — очень сильный восстановитель, применяющийся в органических синтезах. Водой он мгновенно разлагается: LiAlH4 + 4H2O -> LiOH + Al(OH)3 + 4H2.
При внесении в расплавленный алюминий бора образуются бориды состава AlB2 и AlB12 — тугоплавкие соединения, устойчивые к действию кислот. Гидрид (AlH)х (х = 1,2) образуется только в вакууме при низких температурах в реакции атомарного водорода с парами алюминия. Устойчивый в отсутствие влаги при комнатной температуре гидрид Alh4 получают в растворе безводного эфира: AlCl3 + LiH -> AlH3 + 3LiCl. При избытке LiH образуется солеобразный алюмогидрид лития LiAlH4 — очень сильный восстановитель, применяющийся в органических синтезах. Водой он мгновенно разлагается: LiAlH4 + 4H2O -> LiOH + Al(OH)3 + 4H2.
Свойства, характеристики и использование алюминия
Алюминий является основным продуктом в домашних хозяйствах по всему миру, которые используют этот универсальный материал для изготовления фольги, нагревательных приборов и кухонной утвари. Из-за долговечности алюминия и разнообразия применений, которые он предлагает, алюминий также стал важной частью производственной и строительной отраслей. Хотя алюминий не встречается в природе, процесс его обнаружения и создания проложил путь для домов и компаний к использованию алюминия или алюминиевого сплава для создания перерабатываемых и экономичных продуктов.
Хотя алюминий не встречается в природе, процесс его обнаружения и создания проложил путь для домов и компаний к использованию алюминия или алюминиевого сплава для создания перерабатываемых и экономичных продуктов.
Об алюминии
Алюминий — легкий металл, известный своим серебристо-белым цветом. Этот ковкий металл является одним из самых распространенных элементов и встречается в магматических породах или присутствует в различных драгоценных камнях, таких как топаз и гранат. Хотя алюминий никогда не встречается в природе в виде металла, его можно получить в сочетании с кислородом или другими элементами.
Где найти алюминий
Бокситы часто используются в качестве источника алюминия. Материал можно измельчить и обдать водой, чтобы удалить глину и кремнезем, присутствующие в материале. Затем его сушат в печи и смешивают с кальцинированной содой или дробленой известью. После обработки боксит восстанавливают под давлением и удаляют различные примеси. После различных фильтров, процессов и методов нагрева создается глинозем или оксид алюминия. Этот материал представляет собой порошкообразное вещество и получается из кислорода, смешанного с алюминием.
Этот материал представляет собой порошкообразное вещество и получается из кислорода, смешанного с алюминием.
История алюминия
Жители Месопотамии в 5000 г. до н.э. делали глиняную посуду из глины, содержащей алюминий. Было также обнаружено, что египтяне и вавилоняне использовали алюминий в химикатах и лекарственных средствах. Еще одно раннее появление алюминия можно найти еще в Китае третьего века, где анализ гробницы военачальника обнаружил следы алюминия, украшающие украшения.
Ганс Христиан Эрстед был первым, кто получил образец нечистого алюминия в 1825 году. Немецкий химик Фридрих Вёлер окончательно усовершенствовал эту технику примерно в 1827 году.0003
В 1855 году алюминий впервые был представлен публике на Парижской выставке. Современные методы производства алюминия были позже открыты такими людьми, как Шарль Мартин Холл и Поль-Луи-Туссен Эру в 1886 году. В 1960-х годах алюминий стал самым популярным цветным металлом в производстве, основным продуктом в домах и широко используется в современном оборудовании. .
.
Свойства алюминия
Алюминий имеет много преимуществ по сравнению с различными металлами, доступными для потребителей или производственных компаний. Благодаря своей прочности и пластичности алюминий используется в различных продуктах по всему миру для создания машин, теплопроводности или изготовления контейнеров и предметов домашнего обихода. Несколько важных свойств алюминия отличают его от других металлов:
- Легкий вес: Алюминий весит меньше, чем другие металлы, такие как медь, сталь или железо. Из-за этого его часто используют в транспортном или аэрокосмическом дизайне.
- Прочность: Металл устойчив к любым погодным условиям, включая экстремальную жару или холод. Его можно использовать чрезмерно, и он все еще сохраняет свою первоначальную прочность.
- Устойчивость к коррозии: Алюминий можно поцарапать или помять, но он остается прочным. Сопротивление материалов может быть усилено краской или отделкой.

- Электропроводность: Алюминий с низкой плотностью проводит электричество лучше, чем другие металлы, такие как железо или медь. Различные алюминиевые сплавы обладают различной проводимостью и могут использоваться в таких изделиях, как линии электропередач.
- Теплопроводность: Алюминий также хорошо проводит тепло или холод и может оставаться прочным при различных температурах. Из-за этого он часто используется в двигателях, обогревателях или деталях холодильников.
- Немагнитная природа: Поскольку в обычных условиях алюминий не обладает магнитными свойствами, компании могут использовать его в различных электронных устройствах.
- Отражающая способность: Из-за своей отражающей способности алюминий часто используется в качестве отражателя ламп или для защиты продуктов от радиоволн или света.
- Пригодность для вторичной переработки: Алюминий хорошо поддается вторичной переработке.
 Из-за долговечности алюминия он быстро обрабатывается, не теряя своих свойств и прочности.
Из-за долговечности алюминия он быстро обрабатывается, не теряя своих свойств и прочности. - Универсальность: Алюминий — один из самых пластичных сплавов. Его пластичность, долговечность и перечисленные выше свойства делают алюминий чрезвычайно универсальным материалом. Его можно использовать как для предметов домашнего обихода, так и для деталей самолетов.
Что такое алюминиевый сплав?
Когда алюминиевый слиток помещают в печь для легирования, он расплавляется и смешивается с легирующими металлами, такими как медь, кремнезем или магний. Это формирует алюминиевый сплав. Смешивание материалов с алюминием придает сплавам различную прочность и свойства.
Например, при смешивании с марганцем алюминиевый сплав устойчив к коррозии. В сочетании с цинком материал очень прочный и долговечный. Часто сплавы отливают в твердые пластины, называемые бревнами или заготовками, а затем отправляют в экструдер для экструзии алюминия.
Для чего используется алюминий?
Алюминий используется в различных отраслях промышленности и в различных предметах домашнего обихода. В зависимости от сорта металла и типа произведенного алюминия или алюминиевого сплава он может иметь различную прочность, электрические характеристики или коррозионную стойкость.
В зависимости от сорта металла и типа произведенного алюминия или алюминиевого сплава он может иметь различную прочность, электрические характеристики или коррозионную стойкость.
Типы алюминиевых металлов
Наиболее часто используемые марки алюминия — 1100, 3003 и 6061. Различные номера обозначают их использование и возможности:
- 1100: Алюминий марки 1100 — это ковкий металл, из которого легко формуются различные изделия. Он чаще всего используется в химическом оборудовании, циферблатах, цистернах, шильдиках и плавниках. В таких отраслях, как освещение или сантехника, будет использоваться сорт 1100, а также его можно использовать для изготовления посуды или строительных целей.
- 3003: 3003 Алюминий — универсальный сплав, используемый для изготовления кухонной посуды, столовых приборов, кастрюль и крышек для сковородок. Хотя это универсальный сорт, он не может выдерживать очень высокие температуры.
- 6061: Алюминий марки 6061 часто используется для изделий, которые со временем изнашиваются.
 Это могут быть водосточные желоба или части мебели. Прочность марки 6061 также важна, что делает ее отличным вариантом для продуктов, подверженных воздействию влаги.
Это могут быть водосточные желоба или части мебели. Прочность марки 6061 также важна, что делает ее отличным вариантом для продуктов, подверженных воздействию влаги.
Алюминий обычно используется в различных продуктах по всему миру. Некоторые распространенные примеры включают пивные кеги, детали самолетов, оконные рамы, посуду, банки и фольгу. Алюминий также встречается в электрических линиях или в виде алюминиевых покрытий, например, в упаковках, декоративной бумаге и игрушках.
Узнайте больше об алюминиевых сплавах на литейном заводе Warner Brothers
На литейном заводе Warner Brothers наша команда стремится помочь вам или вашей компании с вашими потребностями в алюминиевом, латунном и бронзовом литье. Мы предоставляем отличный сервис нашим клиентам в литейной промышленности, которые ищут прототипы или производственный материал. Литейный завод Warner Brothers использует отвержденный воздухом песок для производства отливок из цветных металлов. Этот метод уменьшит нашу стоимость производства и вашу окончательную цену.
Этот метод уменьшит нашу стоимость производства и вашу окончательную цену.
Ознакомьтесь с нашими техническими характеристиками алюминиевых сплавов, чтобы узнать больше об алюминиевых сплавах, и свяжитесь с Warner Brothers Foundry по всем вопросам, связанным с литьем металлов.
- 29955 Groesbeck Hwy Roseville, Мичиган 48066
- Позвоните нам сегодня: 586-773-0858
- [email protected]
- Коды государственной сертификации:
- Код клетки: 9E499
- JCP: 0084451
- ДУНС: 005371604
Наверх
Warner Brothers Foundry гарантирует, что ваша алюминиевая деталь на 100 % произведена в Соединенных Штатах, как и все наши инструменты. Это алюминиевые отливки американского производства, лучшие в мире.
Это алюминиевые отливки американского производства, лучшие в мире.
Вернуться к началу
Свойства алюминия | bartleby
Что такое алюминий?Алюминий (или алюминий) — металл серебристо-белого цвета. Химическим символом алюминия является Al, и он имеет атомный номер (Z) 13 в периодической таблице. Название алюминия для этого металла происходит от латинского слова «alumen», что означает «горькая соль». Алюминий был открыт в 1825 году Гансом Эрстедом, а позже Фридрих Вёлер выделил алюминий. Это наиболее часто встречающийся металл в ядре Земли, который составляет около 8% от общей массы ядра. Более того, это третий по распространенности элемент на Земле после кислорода и кремния. Электронное распределение алюминия на оболочку составляет 2, 8 и 3 с валентностью 3. Атомный вес составляет около 26,9.815 у.е.
Промышленное производство алюминия впервые началось в 1856 году, а позже, в 1954 году, алюминий, обогнав медь, стал самым производимым цветным искробезопасным металлом. Алюминий встречается в изверженных породах в виде полевого шпата и слюды. В результате выветривания образуется гидратированный оксид алюминия, боксит, который является основной рудой алюминия. Глинозем не растворяется в воде, но растворяется в расплавленном криолите.
Алюминий встречается в изверженных породах в виде полевого шпата и слюды. В результате выветривания образуется гидратированный оксид алюминия, боксит, который является основной рудой алюминия. Глинозем не растворяется в воде, но растворяется в расплавленном криолите.
Плотность алюминия 2710 кг/м 3 с удельным весом 2,71. Алюминий в чистом виде имеет серебристо-белый цвет. Элемент чистого алюминия (Al) находится в p-блоке периодической таблицы. Чистый алюминий — очень мягкий, ковкий металл, а также отражает свет. Алюминий легко связывается с другими элементами и, следовательно, не встречается в чистом виде. Сульфаты алюминия являются наиболее распространенной формой алюминия в природе.
Алюминий легкий и немагнитный. Это второй по пластичности и шестой по пластичности металл. Ковкость – это свойство металла, которое позволяет его ковать или раскатывать в тонкие листы. С другой стороны, пластичность — это свойство, указывающее на способность металла деформироваться в тонкие проволоки. Другими словами, податливость — это способность деформироваться под действием сжимающих напряжений, а пластичность — под действием растягивающих напряжений.
Другими словами, податливость — это способность деформироваться под действием сжимающих напряжений, а пластичность — под действием растягивающих напряжений.
Алюминий имеет следующие химические свойства, а именно, он имеет температуру плавления 660,323°С (933,47 К и 1220,58°F) и температуру кипения 2470°С (2743 К и 4478°F). Следовательно, при стандартной температуре 20°С в природе он находится в твердом состоянии. Модуль Юнга, модуль сдвига и объемный модуль алюминия составляют 70 ГПа, 26 ГПа и 76 ГПа соответственно.
Алюминий естественным образом обладает хорошей коррозионной стойкостью ко многим химическим веществам, но имеет большое сродство к кислороду, что приводит к образованию оксидного слоя на поверхности металла при воздействии атмосферы. Этот оксидный слой образует защитное покрытие, предотвращающее дальнейшую коррозию.
Алюминий имеет стабильную кубическую структуру, которая остается стабильной до тех пор, пока не будет нагрета до температуры плавления. Поверхность этого металла менее блестящая и хорошо отражает свет. Коэффициент расширения алюминия при нагреве равен 23,2.
Поверхность этого металла менее блестящая и хорошо отражает свет. Коэффициент расширения алюминия при нагреве равен 23,2.
Механические свойства алюминия также заслуживают внимания. Его эластичность составляет около 10 000 фунтов на квадратный дюйм, а прочность на растяжение составляет около 13 000 фунтов на квадратный дюйм. Предел текучести алюминия составляет 5000 фунтов на квадратный дюйм, а предел текучести его подшипников составляет около 23 100 фунтов на квадратный дюйм. Прочность алюминия на сдвиг составляет около 9000 фунтов на квадратный дюйм, а усталостная прочность имеет значение 5000 фунтов на квадратный дюйм. Коэффициент Пуассона алюминия равен 0,35.
Различное промышленное использование алюминия Наиболее важным применением алюминия является строительство самолетов, в которых используется алюминий, легированный медью, марганцем, магнием и кремнием, что делает сплав легким, но прочным, как чистый алюминий, который не отличается особой силой.
Алюминий — легкий металл с плотностью 2,71 г/см 3 , что составляет всего 1/3 rd от стали, а также намного ниже, чем у других металлов. Он выделяется как большой потенциал для применения в местах, где необходимы легкие детали, например, в самолетах.
Кроме того, алюминий также используется в строительстве кораблей из-за его коррозионной стойкости. Он также используется в оконных рамах, высотных зданиях, поездах, компонентах космических кораблей и так далее. Кровельные листы для домов состоят из алюминия.
Алюминиевый сплав Алюминий также сплавляется с другими металлами, которые еще больше улучшают свойства алюминия. В алюминиевом сплаве алюминий сочетается с магнием, марганцем, оловом, кремнием и цинком с преобладанием самого алюминия (около 85%). Термообрабатываемые алюминиевые сплавы состоят из чистого алюминия, нагретого до определенной температуры. При повышенных температурах алюминиевые сплавы становятся все слабее и слабее.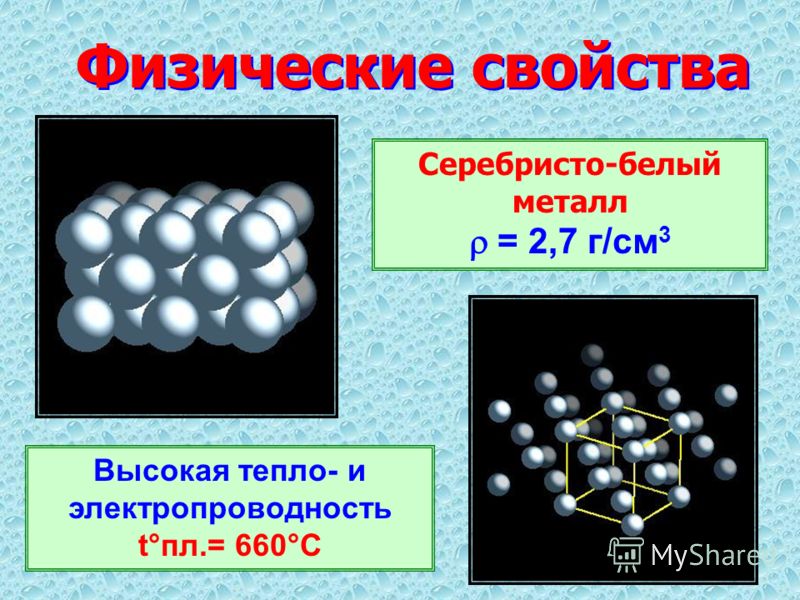
Алюминиевые сплавы легче по сравнению с медью, латунью, никелем и сталью. Он также обладает хорошей коррозионной стойкостью. Благодаря хорошей теплопроводности и электропроводности он находит применение в кухонной технике, а также для электропроводки электронных приборов. Электропроводность алюминия примерно равна 36,9× 106 Сименс/метр. Алюминий также дешевле меди и почти так же хорош в электропроводности, как медь, поэтому он используется в линиях электропередачи.
Дюралюминий представляет собой сплав алюминия и меди и имеет широкое применение. Химический состав дюралюминия, алюминия 94%, меди 4%, марганца и магния 0,4 — 0,7%. Алюминий в смеси с магнием обеспечивает легкий сплав с более высокой огнестойкостью. Другими алюминиевыми сплавами являются Al-Li (сочетание алюминия и лития), альнико (алюминий + никель + медь), магналий (алюминий + магний), силумин (алюминий + кремний) и так далее.
Алюминиевая фольга Одним из основных применений алюминия является изготовление алюминиевой фольги, которая используется для упаковки пищевых продуктов. Металлический алюминий прокатывается под большим давлением на фольгопрокатных станах для получения тонкой и очень тонкой фольги толщиной почти с бумагу (толщина > 25 мкм).
Металлический алюминий прокатывается под большим давлением на фольгопрокатных станах для получения тонкой и очень тонкой фольги толщиной почти с бумагу (толщина > 25 мкм).
Алюминий обладает высокой пластичностью и не пропускает свет, кислород, влагу и бактерии, дополнительно выступая в качестве барьера. Эти характеристики алюминия делают его пригодным для использования в фольге для упаковки пищевых продуктов, а также для фармацевтической упаковки таблеток и пилюль. Алюминиевая фольга, будучи блестящей, также используется в художественных и декоративных целях.
Контекст и приложенияЭта концепция актуальна для различных дипломов, курсов для студентов и аспирантов, таких как
- Бакалавр наук в области машиностроения
- Магистр наук в области машиностроения
- Обучение литью металлов Американским литейным обществом
- 6,894 × 10-9 мкм
- 3,447 × 10-6 мкм
- 4,447 × 10-5 мкм
- 4,447 × 10-6 мкм
Ответ-Вариант B
. 6,894 × 10-9 мкм. Таким образом, 5000 фунтов на квадратный дюйм становится 3,447 × 10-6 мкм.
6,894 × 10-9 мкм. Таким образом, 5000 фунтов на квадратный дюйм становится 3,447 × 10-6 мкм.
2. Как ведет себя алюминий при высоких температурах?
- В целом слабое
- Самое плотное
- Самое сильное
- Никаких изменений не наблюдается
Ответ- Вариант а
Пояснение- Температура плавления алюминия составляет около 1,260 o F и он теряет свою прочность на 50% при нагревании до 600 o F. Более того, можно сделать вывод, что как повышается температура, прочность алюминия снижается.
3. Какова температура плавления алюминия?
- 100 °C
- 550,323 °C
- 660,323 °C 90 2
- хрупкая
- Soft
- Hard
- Магнитный
24
Ответ- Вариант c
Пояснение- Температура плавления алюминия около 1,260 o F, то есть 660 o C.
4 . Какое химическое свойство алюминия является наиболее важным?
Ответ- Вариант B
Объяснение.
