Строение молекулы ацетилена (C2h3), схема и примеры
Общие сведения о строении молекулы ацетилена
Формула C2H2. Структурная формула HC ≡ CH. Молярная масса равна 26 г/моль.
В свободном виде представляет собой газ без цвета и запаха, обладающий слабым наркотическим действием. Температура кипения равна (-84oС).
Ацетилен мало растворим в воде и очень хорошо растворим в ацетоне. В виде ацетонового раствора его хранят в стальных баллонах, заполненных каким-нибудь инертным пористым материалом. Смеси ацетилена с воздухом взрывоопасны.
Электронное строение молекулы ацетилена
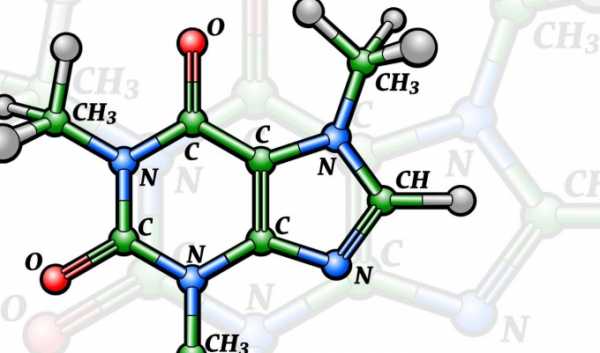
Структурная формула ацетилена имеет вид HC ≡ CH. Два атома углерода, связанные тройной связью, находятся в состоянии sp-гибридизации. Каждый такой атом имеет две sp-гибридные орбитали, расположенные под углом 180o. За счет осевого перекрывания одной из этих орбиталей атом углерода образует σ-связь с другим атомом углерода, а за счет второй sp-гибридной орбитали — σ-связь с атомом водорода. σ-Скелет молекулы имеет линейное строение (рис. 1).
Рис. 1. Строение молекулы ацетилена.
Оставшиеся негибридизованными две p-орбиталикаждого атома углерода расположены под углом 90o одна к другой. При боковом перекрывании этих орбиталей с соответствующими p-орбиталями другого sp-гибридизованного атома углерода образуются две π-связи, расположенные в двух взаимно перпендикулярных плоскостях.
Таким образом, тройная связь образуется из трех пар обобществленных электронов, т.е. это шестиэлектронная связь. Она представляет собой сочетание одной σ- и двух π-связей. π-Электронное облако тройной связи имеет вид цилиндра, охватывающего оба атома углерода.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
Формула воды в химии
Химическая и структурная формула воды
Химическая формула: Н2O
Структурная формула:
Молярная масса: 18,01528 г/моль.
Альтернативные названия: оксид водорода, гидроксид водорода, гидроксильная кислота, монооксид дигидрогена, оксидан, дигидромонооксид.
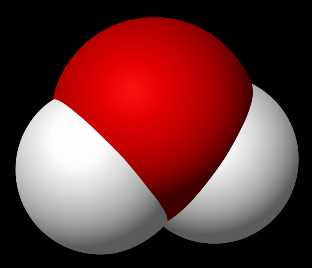
В молекуле воды атом кислорода находится в состоянии sp3–гибридизации, поскольку в образовании гибридных орбиталей участвуют не только валентные электроны, но и неподеленные электронные пары. Гибридные орбитали направлены к вершинам тетраэдра:
Вследствие большой разницы электроотрицательностей кислорода и водорода связи в молекуле сильно поляризованы, и происходит смещение электрон ной плотности в сторону кислорода. Молекула воды обладает большим дипольным моментом, поскольку полярные связи расположены несимметрично.
С сильной поляризацией связи О – Н связано образование водородных связей между молекулами воды. Каждая молекула воды может образовывать до четырёх водородных связей – две из них образует атом кислорода, а еще две – атомы водорода:
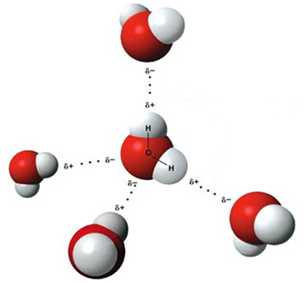
Образование водородных связей определяет более высокую температуру кипения, вязкость и поверхностное натяжение воды по сравнению с гидридами аналогов (серы селена и теллура).
Изотопные модификации воды
В зависимости от типа изотопов водорода, входящих в состав молекулы, выделяют следующие изотопные модификации воды:
| Название | Формула |
|---|---|
|
Легкая вода (основной компонент природной воды) |
H2 O |
|
Тяжёлая вода (дейтериевая) |
D2O |
|
Сверхтяжёлая вода (тритиевая) |
T2O |
|
Тритий-дейтериевая вода |
TDO |
|
Тритий-протиевая вода |
THO |
|
Дейтерий-протиевая вода |
DHO |
С учетом того, что у кислорода три стабильных изотопа (16O, 17O и 18O), можно составить 18 формул молекул воды, различающихся изотопным составом. Как правило, природная вода содержит все эти разновидности молекул.
Примеры решения задач по теме «формула воды»
Как написать структурную формулу 🚩 Составление формул комплексных соединений 🚩 Естественные науки
Автор КакПросто!
Структурная формула — это графическое изображение химического строения молекулы вещества, в котором показывается порядок связи атомов, их геометрическое расположение. Кроме того, она наглядно показывает валентность атомов входящих в ее состав.
Вам понадобится
- — ручка;
- — бумага;
- — периодическая система элементов.
Инструкция
Для правильного написания структурной формулы того или иного химического вещества вы должны хорошо знать и представлять, что такое способность атомов образовывать определенное количество электронных пар с другими атомами. Ведь именно валентность поможет вам нарисовать химические связи. Например, дана молекулярная формула аммиака Nh4. Вы должны написать структурную формулу. Учитывайте то, что водород всегда одновалентен, поэтому его атомы не могут быть связаны между собой, следовательно, они будут соединены с азотом. Чтобы правильно написать структурные формулы органических соединений, повторите основные положения теории А.М. Бутлерова, согласно которой существуют изомеры – вещества с одинаковым элементарным составом, но с разными химическими свойствами. Например, изобутан и бутан. Молекулярная формула у них одинаковая: C4h20, а структурные – отличаются.
Чтобы правильно написать структурные формулы органических соединений, повторите основные положения теории А.М. Бутлерова, согласно которой существуют изомеры – вещества с одинаковым элементарным составом, но с разными химическими свойствами. Например, изобутан и бутан. Молекулярная формула у них одинаковая: C4h20, а структурные – отличаются. 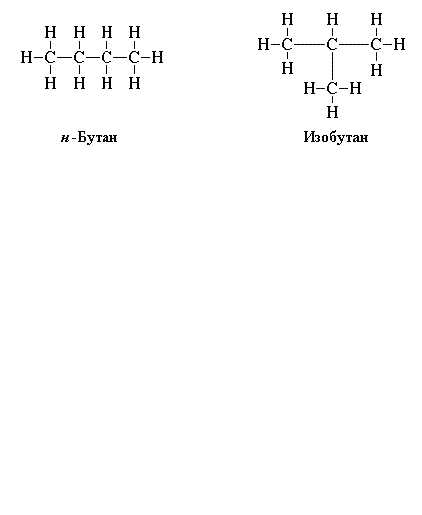
В линейной формуле каждый атом записывается отдельно, поэтому такое изображение занимает много места. Однако при составлении структурной формулы, вы можете указать общее число атомов водорода при каждом атоме углерода. А между соседними углеродами нарисуйте химические связи в виде линий.

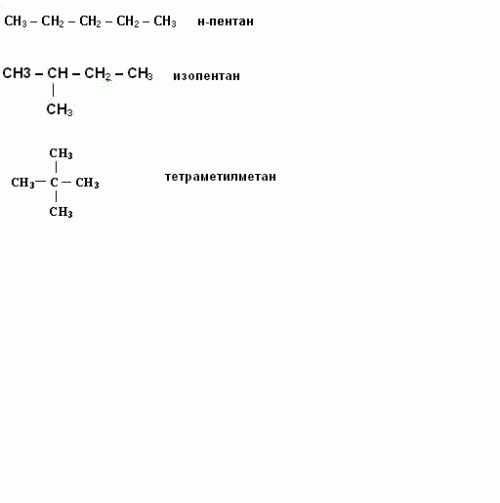
Написание изомеров начните с углеводорода нормального строения, то есть с неразветвленной цепью углеродных атомов. Затем сократите на один атом углерода, который присоедините к другому, внутреннему углероду. Исчерпав все варианты написания изомеров с данной длиной цепи, сократите ее еще на один углеродный атом. И опять присоедините его к внутреннему углеродному атому цепи. Например, структурные формулы н-пентана, изопентана, тетраметилметана. Таким образом, углеводород с молекулярной формулой C5h22 имеет три изомера.
Полезный совет
Для определения валентности атомов при составлении структурных формул используйте периодическую систему. Показать точно расстояние атомов в молекуле поможет трехмерная структурная формула.
Источники:
- структурная формула веществ
- Составление формул комплексных соединений
Некоторые до сих пор с содроганием вспоминают школьные уроки химии, на которых нужно было составлять структурные формулы углеводородов и их изомеров. А между тем, ничего сверхсложного в этом нет. Достаточно руководствоваться при составлении формул определенным алгоритмом.
Инструкция
Ознакомьтесь с молекулярной формулой углеводорода. Исходя из нее, составьте формулу сначала неразветвленного углеродного скелета (углеродную цепь).
Над каждым атомом углерода надпишите его порядковый номер. Далее расставьте атомы водорода в цепи. Не забудьте: углерод четырехвалентен. Уменьшите углеродную цепь на один атом. Расположите его как боковое ответвление углеродной цепи. Не забудьте, что атомы, которые располагаются у крайних атомов цепи, не могут являться боковыми ответвлениями. Определите, к какому краю ближе боковое ответвление. Пронумеруйте заново углеродную цепь, начиная с этого края. Расставьте атомы водорода в соответствии с валентностью углерода.Определите, можно ли располагать боковое ответвление у прочих атомов углерода в цепи. В случае положительных выводов составьте формулы изомеров. Если же такая возможность отсутствует, уменьшите основную углеродную цепь еще на атом и расположите его в качестве еще одного бокового ответвления. Обратите внимание: возле одного атома углерода можно располагать не больше 2-х боковых ответвлений.
Расставьте порядковые номера над атомами углерода с того края, к которому ближе всего располагается боковое ответвление. Расположите возле каждого атома атомы водорода с учетом валентности углерода.
Снова проверьте, есть ли возможность расположить боковые ответвления у прочих атомов углерода в основной цепи. Если такая возможность существует, то составьте формулы возможных изомеров, если нет — уменьшите углеродную цепь еще на атом и расположите его как боковое ответвление. Теперь пронумеруйте всю цепь атомов и снова попробуйте составить формулы изомеров. В том случае, если уже два боковых ответвления находятся на одинаковом удалении от краев цепи, начинайте нумерацию с края, у которого боковых ответвлений больше.
Продолжайте выполнять эти действия до тех пор, пока не исчерпаете все возможности для расположения боковых ответвлений.
Умение решать задачи по химии может пригодиться не только школьнику и студенту, но и рабочему на производстве, домохозяйке на кухне, садоводу на приусадебном участке. Существует простой алгоритм, который позволяет решить стандартные химические задачи.

Вам понадобится
- теоретические знания по химии на школьном уровне.
Инструкция
К решению химической задачи необходимо подходить планомерно. Внимательно разберите ее условие, запишите в столбик все данные. Переведите все величины в единую систему измерения. Отдельно запишите искомую величину. На рисунке 1 представлены величины, которые используются в стандартных школьных задачах и их единицы измерения. Самый просто тип задач — задачи, решаемые при помощи одних расчетных формул. В таких задачах нет необходимости составлять уравнения реакции. Достаточно внимательно посмотреть на таблицу стандартных химических формул (рисунок 2), и выбрать те формулы, которые будут необходимы, чтобы найти искомую величину по известным данным. Более сложными являются задачи, в которых указаны реагирующие вещества, в этом случае вам необходимо составить уравнение реакции.Вам понадобятся теоретические знания об основных химических реакциях и соединениях для того, чтобы правильно установить продукты реакции. Кроме того, вам будет необходимо уравнять коэффициенты в уравнении.
Для уравнивания коэффициентов надо помнить, что количество каждого вещества, вступившего в реакцию и общее количество вещества остаются постоянными.
После того, как вы составите уравнение реакции, вам будет необходимо найти количество известного вещества, а потом с его помощью количество неизвестного вещества. Дальнейшее решение опять сводится к подбору формулы для нахождения искомой величины.
Существует тип химических задач на избыток/недостаток. В этих задачах необходимо вычислить количества реагирующих веществ и, учитывая коэффициенты реакции, выяснить, какого вещества больше. Дальнейший расчет необходимо вести по веществу, которого меньше, так как оно прореагирует полностью, а вот вещество, находящееся в избытке, частично останется непрореагировавшим.
Научиться решать стандартные химические задачи может каждый, педагоги говорят, что необходимо прорешать около 15 задач каждого типа самостоятельно для того, чтобы решать их уверенно.
Источники:
- Интерактивный учебник химии
Химическая формула – это запись, сделанная с использованием общепринятых символов, которая характеризует состав молекулы какого-либо вещества. Например, формула всем известной серной кислоты – h3SO4. Легко можно увидеть, что каждая молекула серной кислоты содержит два атома водорода, четыре атома кислорода и один атом серы. Надо понимать, что это – лишь эмпирическая формула, она характеризует состав молекулы, но не ее «структурность», то есть расположение атомов относительно друг друга.
Вам понадобится
- — Таблица Менделеева.
Инструкция
Сначала узнайте элементы, входящие в состав вещества, и их валентность. Например: какова будет формула оксида азота? Очевидно, что в состав молекулы этого вещества входят два элемента: азот и кислород. Оба они – газы, то есть ярко выраженные неметаллы. Так какую же валентность имеют азот и кислород в этом соединении?Запомните очень важное правило: неметаллы имеют высшую и низшую валентности. Высшая соответствует номеру группы (в данном случае, 6 для кислорода и 5 для азота), а низшая – разнице между 8 и номером группы (то есть низшая валентность для азота равна 3, а для кислорода — 2). Единственное исключение их этого правила – фтор, который во всех своих соединениях проявляет одну валентность, равную 1.
Так какую же валентность – высшую или низшую имеют азот и кислород? Еще одно правило: в соединениях двух элементов, низшую валентность проявляет тот, которых находится в Таблице Менделеева правее и выше. Совершенно очевидно, что в вашем случае это – кислород. Следовательно, в соединении с азотом кислород имеет валентность, равную 2. Соответственно, азот в этом соединении имеет высшую валентность, равную 5.
А теперь вспомните само определение валентности: это способность атома какого-либо элемента присоединить к себе определенное количество атомов другого элемента. Каждый атом азота в этом соединении «притягивает» 5 атомов кислорода, а каждый атом кислорода – 2 атома азота. Какова же формула оксида азота? То есть, какие индексы имеет каждый элемент?
Ответить на этот вопрос поможет еще одно правило: сумма валентностей элементов, входящих в соединение, должна быть равной! Какое наименьшее общее кратное для чисел 2и 5? Естественно, 10! Поделив его на величины валентностей азота и кислорода, вы найдете индексы и итоговую формулу соединения: N2O5.
Видео по теме
Вам необходимо составить химическую формулу, но вы абсолютно забыли основы школьной химии? Поверьте, не стоит переживать. На сегодняшний день известно более 20 миллионов химических соединений, и, поверьте, никто не держит их формулы у себя в голове. Достаточно знать простой принцип их написания.
Вам понадобится
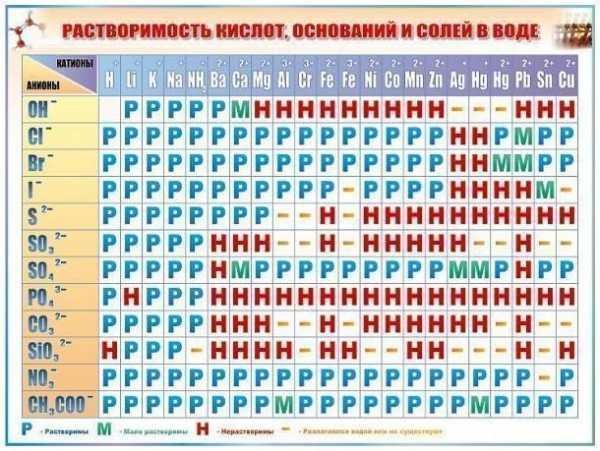
- периодическая таблица Менделеева, таблица растворимости солей
Инструкция
Задача составления химической формулы вещества сводится к созданию электронейтральной системы. Поэтому вам необходимо будет подобрать некоторое число электронов для каждого элемента соединения так, чтобы оно было уравновешено.Однако перед тем, как это сделать, вам следует вспомнить некоторые теоретические основы. Любой элемент периодической таблицы Менделеева обладает своей валентностью (степенью окисления), то есть способностью отдавать или принять некоторое количество электронов, с учетом своей валентности, не более восьми электронов. Валентность каждого химического элемента соответствует номеру группы в периодической таблице (верхняя строка, написанная римскими цифрами). Стоит заметить, что все элементы таблицы Менделеева можно условно разделить на два класса: окислители и восстановители. Первые, как правило, только забирают электроны, вторые – отдают.Для составления химической формулы также необходимо знать, с каким типом соединений вы имеете дело. Их можно разделить на следующие группы:1. Бинарные;2. Основания, соли, кислоты.
Для составления формулы бинарных соединений вам потребуется таблица Менделеева, а для остальных групп – таблица растворимости солей. В формулах бинарных соединений на первом месте принято писать металл или элемент с меньшей валентностью, на втором – неметалл или элемент с большей валентностью. Допустим, необходимо составить формулу оксида тантала. Запишите рядом обозначения этих элементов и проставьте их валентность: Та5О6. Тантал, соответственно, способен отдать 3 электрона, а кислород – принять два, то есть: Та3+О2-. Таким образом, для создания уравновешенной системы методом «крест-на-крест» (меняя индексы химических элементов местами и отбрасывая их знаки) вы получаете следующую формулу: Та2О3.Для составления формул оснований, солей и кислот необходимо воспользоваться таблицей растворимости солей. В верхней ее строке указаны катионы – вещества, отдающие электроны, а в левом столбце – анионы, то есть соединения, способные принимать электроны. Пользуясь таблицей растворимости солей, можно получить следующую формулу для сульфата алюминия: Al3+ SO42-. Используя принцип «крест-на-крест», окончательная формула вещества будет иметь вид: Аl2(SO4)3.Как видите, алгоритм составления химических формул очень прост. Он остается неизменным для любых других соединений.
Для удобства записи химического состава и структуры химического вещества были созданы определенные правила составления химических формул с помощью специальных символов-обозначений, чисел и вспомогательных знаков.
Инструкция
Химические формулы участвуют в написании уравнений химических реакций, схематичного изображения химических процессов, связей. Для их написания используется так называемый язык химии, который представляет собой набор условных обозначений, таких как символы химических элементов, количество атомов каждого элемента в описываемом веществе и пр.Символы химических элементов – одна или несколько букв латинского алфавита, из которых первая заглавная. Это схематичная запись полного называния элемента, например, Ca – это кальций или лат. Calcium.
Количество атомов выражается математическими числами, например, H_2 – это два атома водорода.
Существует несколько способов записи химической формулы: простейшая, эмпирическая, рациональная и структурная. Простейшая формула записи отражает соотношение химических элементов с указанием атомной массы, которая указывается после знака химического элемента в виде нижнего индекса. Например, H_2O – простейшая формула молекулы воды, т.е. два атома водорода и один атом кислорода.Эмпирическая химическая формула отличается от простейшей тем, что отражает состав вещества, но не структуру молекул. Формула показывает количество атомов в одной молекуле, которое также изображается в виде нижнего индекса.
Различие между простейшей и эмпирической формулами показывает запись формулы бензола: CH и C_6H_6 соответственно. Т.е. простейшая формула показывает прямое соотношение атомов углерода и водорода, в то время как эмпирическая говорит, что в молекуле вещества содержится 6 атомов углерода и 6 – водорода.
Рациональная формула четко показывает наличие групп атомов элементов в соединении. Такие группы выделяются круглыми скобками, а их количество указывается нижним индексом после скобок. В формуле используются также квадратные скобки, в которые заключаются комплексные соединения атомов (соединений с нейтрально заряженной молекулой, ионом).
Структурная формула изображается графически в двух- или трехмерном пространстве. Химические связи между атомами изображаются в виде линий, при этом атомы указываются столько раз, сколько их участвует в соединении. Наиболее наглядно формулу вещества выражает трехмерное изображение, которые показывают взаимное расположение атомов и расстояния между ними.
Видео по теме
Распространенная программа Excel от Microsoft незаменима при составлении таблиц, диаграмм, проведении расчетов. Чтобы автоматизировать вычисление введенных в ячейки таблиц значений, в Excel применяются формулы. Существуют определенные правила для ввода формул в таблицы.

Вам понадобится
- — программа Excel, установленная на компьютер.
Инструкция
Установите купленную или скачайте и установите триальную версию Excel. Запустите программу. Рассмотрите интерфейс программы. Строка формул обозначается буквами fx. Для ввода простой формулы введите в ячейку необходимые значения, поставив перед ними знак равенства. Например, чтобы рассчитать сумму 1+1, в ячейку вам необходимо ввести «=1+1» без кавычек и нажать Enter. В ячейке появится результат суммирования — 2.
Воспользуйтесь другим способом ввода. Щелкните на пустую ячейку (А1) и вставьте в нее число, предварив его знаком «равно». В соседнюю ячейку (В1) вставьте другое число и так далее, в зависимости от того, сколько чисел вам необходимо. В последнюю пустую ячейку поставьте знак «равно».
Выберите ячейку А1. Затем вставьте арифметический знак (сложение, умножение, деление и другие) и выберите другую ячейку, например, В2. Нажмите Enter. Просмотрите исходную формулу, дважды кликнув по ячейке, нажав Ctrl+апостроф. Помимо этого формула отобразится в строке формул на панели инструментов после выделения ячейки. Нажмите F2 для изменения формулы и по завершении нажмите Enter. Добавьте в формулу круглые скобки, если необходимо задать порядок выполнения операции. Сначала програма выполняет вычисления внутри скобок. Если скобки не хватает, Excel выдаст ошибку — исправьте.Чтобы умножить, поставьте число, затем знак умножения * и иное число. Excel рассматривает произведение числа на другое число, стоящее справа. Если число слева или справа опустить, то программа выдаст ошибку. Чтобы сложить, вычесть или разделить числа, используйте знаки +, -, /.
Возведите число в степень с помощью знака ^, например, «=2^3». Степень можно записать иначе, к примеру, «=СТЕПЕНЬ(2;3)». Нажмите Enter. Результат будет равен восьми. Чтобы найти процент от числа, умножьте число на n% (n% — тот процент, который надо рассчитать).
Чтобы сложить все числа из какого-либо столбца, введите в строку формул формулу «=СУММ(А:А)» (в этом примере суммируются числа из столбца А). Чтобы вычислить значение в диапазоне, введите в строку формул «=СРЗНАЧ(А1:В4)» (в примере вычисляется среднее арифметическое значений в диапазоне от А1 до В4).Для просмотра сложных функций зайдите в меню на вкладку «Вставка» (там выберите «Функция» и функцию из категории) или на вкладку «Функция» в последних версиях Excel.
Видео по теме
Полезный совет
В Excel при вводе формулы в ячейку автоматически подставляется результат вычислений. Но бывает, что надо увидеть формулу, стоящую за значением конкретной ячейки и тогда приходится возвращаться к ней, а это не всегда удобно при сложных расчетах с большим количеством формул. Для переключения режима работы с формулами и с результатами вычислений нажмите на клавиатуре сочетание клавиш [Ctrl]+[~].
Источники:
- Правила вода формул в Excel
При выполнении заданий по химии, которые включают в себя тестирование, решение расчетных задач, практическую работу или лабораторный опыт могут понадобиться умения и навыки при написании формул солей. Таблица растворимости, в которой указаны значения зарядов ионов металлов и кислотных остатков, а также знание принципа ее использования поможет верно написать формулы и других веществ.

Вам понадобится
- — таблица растворимости солей, кислот, оснований
Инструкция
Карбонаты – это соли, состоящие из атомов металла и кислотного остатка, который имеет один атом углерода и три атома кислорода — СO3. Соли могут быть как средними — карбонаты, так и кислыми — гидрокарбонаты. Чтобы правильно написать формулу, необходимо воспользоваться таблицей растворимости кислот, солей и оснований, являющейся справочным материалом на всех видах контроля, включая даже ЕГЭ по химии. Карбонат-ион имеет заряд 2-. Чтобы формула соли была написана правильно, найдите, какой заряд имеет металл, который входит в состав карбоната. В любом случае, суммарное число положительных зарядов ионов должно равняться суммарному числу отрицательных. При этом необходимо обязательно учитывать индексы, стоящие внизу справа от химического символа. Значение заряда иона и индекса, стоящего у этого же иона, перемножаются.Пример № 1. Напишите формулу карбоната калия.
В таблице растворимости посмотрите на кислотный остаток и на металл, входящий в состав соли. Кислотный остаток — СO3 имеет заряд 2-, а ион калия имеет заряд + (считается +1, но единица не пишется).
Напишите формулу, учитывая, что металл всегда стоит на первом месте: КСO3.
Если сравнить количество зарядов, то отрицательных получилось два (2-), а положительных только один (+). Значит, в формуле должно быть 2 атома калия, которые дадут два положительных заряда (2+), так как значение заряда и индекса перемножается. Следовательно, и молекула будет электронейтральна: К2СO3. Полученная соль называется карбонат калия.
Кислотный остаток тот же, то есть — СO3 с зарядом (2-). В таблице растворимости найдите металл кальций и его заряд, который равен 2+ . Напишите формулу, имеющую вид: СаСO3. В итоге получилось одинаковое количество отрицательных (2-) и положительных 2(+) зарядов. Следовательно, формула написана правильно, так как в целом она электронейтральна. Полученная соль называется карбонат кальция, она знакома как мел или известняк.
Пример № 3. Напишите формулу гидрокарбоната калия.
Гидрокарбонат-иона в таблице растворимости нет, а потому следует запомнить, что он имеет вид — НСO3 и у него заряд, равный (-). Ион калия имеет противоположный заряд (+), поэтому формула будет выглядеть таким образом:
КНСO3.
Полученное соединение называется гидрокарбонат калия, которое представляет собой кислую соль.
Видео по теме
Источники:
- карбонат кальция формула
www.kakprosto.ru
Формула Воды структурная химическая
Структурная формула
 |
 |
Истинная, эмпирическая, или брутто-формула: H2O
Химический состав Воды
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| H | Водород | 1,008 | 2 | 11,2% |
| O | Кислород | 15,999 | 1 | 88,8% |
Молекулярная масса: 18,015
Вода́ (оксид водорода) — бинарное неорганическое соединение с химической формулой H2O. Молекула воды состоит из двух атомов водорода и одного — кислорода, которые соединены между собой ковалентной связью. При нормальных условиях представляет собой прозрачную жидкость, не имеет цвета (в малом объёме), запаха и вкуса. В твёрдом состоянии называется льдом (кристаллы льда могут образовывать снег или иней), а в газообразном — водяным паром. Вода также может существовать в виде жидких кристаллов (на гидрофильных поверхностях). Составляет приблизительно около 0,05 % массы Земли.
Является хорошим сильнополярным растворителем. В природных условиях всегда содержит растворённые вещества (соли, газы).
Вода при нормальных условиях находится в жидком состоянии, тогда как аналогичные водородные соединения других элементов являются газами (H2S, CH4, HF). Атомы водорода присоединены к атому кислорода, образуя угол 104,45° (104°27′). Из-за большой разности электроотрицательностей атомов водорода и кислорода электронные облака сильно смещены в сторону кислорода. По этой причине молекула воды обладает большим дипольным моментом (p = 1,84 Д, уступает только синильной кислоте). Каждая молекула воды образует до четырёх водородных связей — две из них образует атом кислорода и две — атомы водорода. Количество водородных связей и их разветвлённая структура определяют высокую температуру кипения воды и её удельную теплоту парообразования. Если бы не было водородных связей, вода, на основании места кислорода в таблице Менделеева и температур кипения гидридов аналогичных кислороду элементов (серы, селена, теллура), кипела бы при −80 °С, а замерзала при −100 °С.
При переходе в твёрдое состояние молекулы воды упорядочиваются, при этом объёмы пустот между молекулами увеличиваются, и общая плотность воды падает, что и объясняет меньшую плотность (больший объём) воды в фазе льда. При испарении, напротив, все водородные связи рвутся. Разрыв связей требует много энергии, отчего у воды самая большая удельная теплоёмкость среди прочих жидкостей и твёрдых веществ. Для того чтобы нагреть один литр воды на один градус, требуется затратить 4,1868 кДж энергии. Благодаря этому свойству вода нередко используется как теплоноситель. Помимо большой удельной теплоёмкости, вода также имеет большие значения удельной теплоты плавления (333,55 кДж/кг при 0 °C) и парообразования (2250 кДж/кг).
formula-info.ru
Структурная и молекулярная формула: ацетилен
Особенности строения ацетилена влияют на его свойства, получение и применение. Условное обозначение состава вещества — С2Н2 — это его простейшая и брутто-формула. Ацетилен образован двумя атомами углерода, между которыми возникает тройная связь. Ее наличие отражают разные виды формул и моделей молекулы этина, позволяющих разобраться в проблеме влияния строения на свойства вещества.
Алкины. Общая формула. Ацетилен
Углеводороды алкины, или ацетиленовые, являются ациклическими, непредельными. Цепочка атомов углерода — не замкнутая, в ней присутствуют простые и кратные связи. Состав алкинов отражает сводная формула CnH2n– 2. В молекулах веществ этого класса присутствует одна или несколько тройных связей. Ацетиленовые соединения относятся к ненасыщенным. Это означает, что только одна валентность углерода реализуется за счет водорода. Оставшиеся три связи используются при взаимодействии с другими атомами углерода.
Первый — и наиболее известный представитель алкинов — ацетилен, или этин. Тривиальное название вещества произошло от латинского слова «acetum» — «уксус» и греческого — «hyle» — «дерево». Родоначальник гомологического ряда был открыт в 1836 году в химических опытах, позже вещество синтезировали из угля и водорода Э. Дэви и М. Бертло (1862 год). При обычной температуре и нормальном атмосферном давлении ацетилен находится в газообразном состоянии. Это бесцветный газ, без запаха, малорастворимый воде. Этин легче растворяется в этаноле и ацетоне.
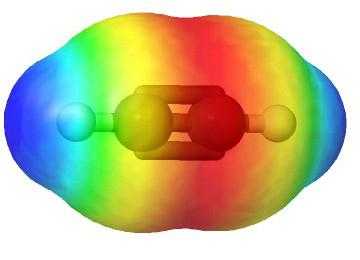
Молекулярная формула ацетилена
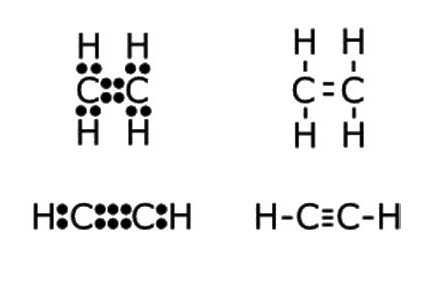
Этин — простейший член своего гомологического ряда, его состав и строение отражают формулы:
- С2Н2 — молекулярная запись состава этина, которая дает представление о том, что вещество образовано двумя углеродными атомами и таким же числом атомов водорода. По этой формуле можно рассчитать молекулярную и молярную массы соединения. Mr (С2Н2) = 26 а. е. м., М (С2Н2) = 26,04 г/моль.
- Н:С:::С:Н — электронно-точечная формула ацетилена. Подобные изображения, получившие название «структуры Льюиса», отражают электронное строение молекулы. При написании необходимо соблюдать правила: атом водорода стремится при образовании химической связи обладать конфигурацией валентной оболочки гелия, другие элементы — октетом внешних электронов. Каждое двоеточие означает общую для двух атомов или неподеленную пару электронов внешнего энергетического уровня.
- H—C≡C—H — структурная формула ацетилена, отражающая порядок и кратность связей между атомами. Одна черточка заменяет собой одну пару электронов.
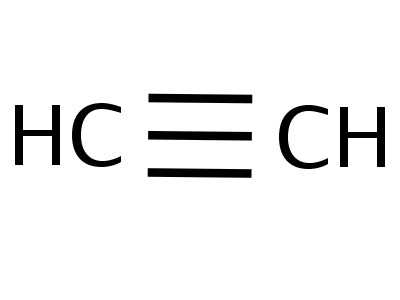
Модели молекулы ацетилена
Формулы, показывающие распределение электронов, послужили фундаментом для создания атомно-орбитальных моделей, пространственных формул молекул (стереохимических). Еще в конце XVIII века получили распространение шаростержневые модели — например, шарики разного цвета и размера, обозначающие углерод и водород, которые образуют ацетилен. Структурная формула молекулы представлена в виде стержней, символизирующих химические связи и их количество у каждого атома.
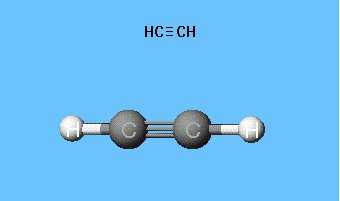
Шаростержневая модель ацетилена воспроизводит валентные углы, равные 180°, но межъядерные расстояния в молекуле отражаются приблизительно. Пустоты между шариками не создают представления о заполнении пространства атомов электронной плотностью. Недостаток устранен в моделях Дрейдинга, обозначающих ядра атомов не шариками, а точками присоединения стержней друг к другу. Современные объемные модели дают более яркое представление об атомных и молекулярных орбиталях.
Гибридные атомные орбитали ацетилена
Углерод в возбужденном состоянии содержит три р-орбитали и одну s с неспаренными электронами. При образовании метана (СН4) они принимают участие в создании равноценных связей с атомами водорода. Известный американский исследователь Л. Полинг разработал учение о гибридном состоянии атомных орбиталей (АО). Объяснение поведения углерода в химических реакциях заключается в выравнивании АО по форме и энергии, образовании новых облаков. Гибридные орбитали дают более прочные связи, становится устойчивее формула.
Атомы углерода в молекуле ацетилена, в отличие от метана, подвергаются sp-гибридизации. По форме и энергии смешиваются s- и р электроны. Появляются две sp-орбитали, лежащие под углом 180°, направленные по разные стороны от ядра.
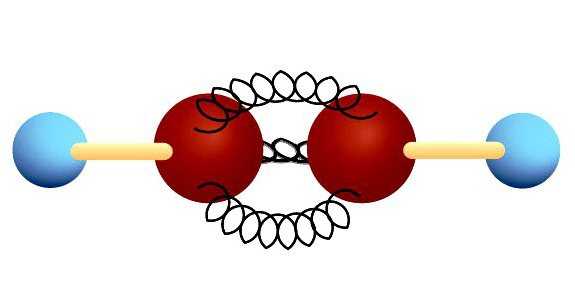
Тройная связь
В ацетилене гибридные электронные облака углерода участвуют в создании σ-связей с такими же соседними атомами и с водородом в парах С—Н. Остаются две перпендикулярные друг другу негибридные p-орбитали. В молекуле этина они участвуют в образовании двух π-связей. Вместе с σ возникает тройная связь, которую отражает структурная формула. Ацетилен отличается от этана и этилена расстоянием между атомами. Тройная связь короче двойной, но обладает большим запасом энергии, является более прочной. Максимальная плотность σ- и π-связей расположена в перпендикулярных областях, что приводит к образованию цилиндрического электронного облака.
Особенности химической связи в ацетилене
Молекула этина имеет линейную форму, что удачно отражает химическая формула ацетилена — H—C≡C—H. Атомы углерода и водорода находятся вдоль одной прямой, между ними возникают 3 σ- и 2 π-связи. Свободное движение, вращение вдоль оси C—C невозможно, этому препятствует наличие кратных связей. Другие особенности тройной связи:
- количество пар электронов, связывающих два атома углерода, — 3;
- длина — 0,120 нм;
- энергия разрыва — 836 кДж/моль.
Для сравнения: в молекулах этана и этилена длина одинарной и двойной химической связи — 1,54 и 1,34 нм соответственно, энергия разрыва С—С составляет 348 кДж/моль, C=C — 614 кДж/моль.
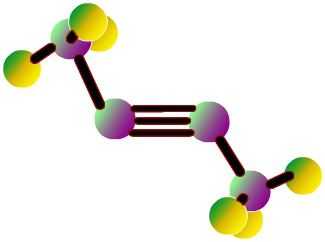
Гомологи ацетилена
Ацетилен — простейший представитель алкинов, в молекулах которых также присутствует тройная связь. Пропин СН3С≡СН — гомолог ацетилена. Формула третьего представителя алкинов — бутина-1 — СН3СН2С≡СН. Ацетилен — тривиальное название этина. Систематическая номенклатура алкинов подчиняется правилам ИЮПАК:
- в линейных молекулах указывается название основной цепи, возникшее от греческого числительного, к которому добавляется суффикс -ин и номер атома при тройной связи, например, этин, пропин, бутин-1;
- нумерацию главной цепочки атомов начинают с конца молекулы, ближайшего к тройной связи;
- для разветвленных углеводородов сначала идет наименование бокового ответвления, затем следует название главной цепочки атомов с суффиксом -ин.
- заключительная часть наименования — цифра, указывающая расположение в молекуле тройной связи, например, бутин-2.
Изомерия алкинов. Зависимость свойств от строения
Этин и пропин не имеют изомеров положения тройной связи, они появляются, начиная с бутина. Изомеры углеродного скелета есть у пентина и следующих за ним гомологов. Относительно тройной связи не проявляется пространственная изомерия ацетиленовых углеводородов.
Первые 4 гомолога этина — газы, плохо растворимые в воде. Ацетиленовые углеводороды C5 – C15 — жидкости. Твердыми веществами являются гомологи этина, начиная с углеводорода C17. Химическая природа алкинов испытывает значительное влияние тройной связи. Углеводороды этого типа активнее, чем этиленовые, присоединяют различные частицы. На этом свойстве основано широкое применение этина в промышленности и технике. При горении ацетилена выделяется большое количество теплоты, что находит применение в газовой резке и сварке металлов.
fb.ru
Непредельные углеводороды. Алкины
Строение алкинов
Первым и основным представителем гомологического ряда алкинов является ацетилен (этин) С2Н2. Строение его молекулы выражается формулами:
структурная формула
Н — С ≡ С — Н
или
электронная формула
Н:С:::С:Н
По названию первого представителя этого ряда — ацетилена — эти непредельные углеводороды называют ацетиленовыми.
В алкинах атомы углерода находятся в третьем валентном состоянии (sp-гибридизация). В этом случае между углеродными атомами возникает тройная связь, состоящая из одной σ — и двух π -связей. Длина тройной связи равна 0,12 нм, а энергия ее образования составляет 830 кДж/моль.
Номенклатура
Простейшим алкином является этин (ацетилен С2Н2). По номенклатуре IUPAC названия алкинов образуются от названий соответствующих алканов заменой суффикса «-ан» на «-ин»; положение тройной связи указывается арабской цифрой.
Углеводородные радикалы, образованные от алкинов имеют суффикс «-инил», так CH-C- называется «этинил».
Гомологический ряд
Этин:C2H2 Пропин: C3H4 Бутин: C4H6 Пентин: C5H8 Гексин: C6H10 Гептин: C7H12 Октин: C8H14 Нонин: C9H16 Децин: C10H 18
Изомерия
Изомерия алкиновых углеводородов (как и алкеновых) определяется строением цепи и положением в ней кратной (тройной) связи:
(такая же как у алканов и алкенов)
З-метилбутин-1
Н — С ≡ С — СН2 — СН2 — СН3 пентин-1
Н3С — С ≡ С — СН2 — СН3 пентин-2
Алкины являются изомерами с алкадиенами.
Физические свойства алкинов
Алкины по своим физическим свойствам напоминают соответствующие алкены. Низшие (до С4) — газы без цвета и запаха, имеющие более высокие температуры кипения, чем аналоги в алкенах. Алкины плохо растворимы в воде, лучше — в органических растворителях.
Плохо растворимы в воде.
Химические свойства
Химические свойства алкинов определяются тройной связью, особенностями ее строения. Алкины способны вступать в реакции присоединения, замещения, полимеризации и окисления.
Будучи непредельными соединениями, алкины вступают в первую очередь в реакции присоединения. Эти реакции протекают ступенчато: с присоединением одной молекулы реагента тройная связь вначале переходит в двойную, а затем, по мере дальнейшего присоединения, — в одинарную.
Казалось бы, алкины, обладая двумя π-связями, гораздо активнее должны вступать в реакции электрофильного присоединения. Но это не совсем так. Углеродные атомы в молекулах алкинов расположены ближе друг к другу, чем в алкенах, и обладают большей электроотрицательностью. Это связано с тем, что электроотрицательность атома углерода зависит от его валентного состояния. Поэтому p-электроны, находясь ближе к ядрам углерода, проявляют несколько меньшую активность в реакциях электрофильного присоединения. Кроме того, сказывается, близость положительно заряженных ядер атомов, способных отталкивать приближающиеся электрофильные реагенты (катионы). В то же время алкины могут вступать в реакции нуклеофильиого присоединения (со спиртами, аммиаком и др.).
Реакция протекает в тех же условиях, что и в случае алкенов (катализаторы Pt, Pd, Ni). При восстановлении алкинов вначале образуются алкены, а затем — алканы:
HC ≡ CH + H2 → H2C = CH2 + H2 → H3C—CH3
ацетилен → этилен → этан
Эта реакция протекает с меньшей скоростью, чем в ряду этиленовых углеводородов. Реакция также проходит ступенчато:
HC ≡ CH + Br2 → CHBr = CHBr + Br2 → CHBr2 — CHBr2
ацетилен → 1,2-дибромэтан → 1,1,2,2-тетрабромэтан
Качественная реакция; бромная вода обесцвечивается.
Реакции присоединения галогеноводородов, как и галогенов, идут в основном по механизму электрофильного присоединения:
HC ≡ CH + HCl → H2C = CHCl → H3C — CHCl2
ацетилен → хлорэтен → 1,1-дихлорэтан
Вторая молекула галогеноводорода присоединяется в соответствии с правилом Марковникова.
Образуется ацетальдегид в случае С2Н2 и кетоны — в случае гомологов ацетилена.
Катализатор — соль ртути: HgSO4
HC ≡ CH + HCN кат.→ H2C = CH — CN (акрилонитрил)
Акрилонитрил — ценный продукт. Он используется в качестве мономера для получения синтетического волокна — нитрон.
В результате этой реакции образуются простые виниловые эфиры (реакция А. Е.Фаворского):
HC ≡ CH + HO — C2H5KOH→ H2C = CH — O — C2H5 (этилвиниловый эфир)
Присоединение спиртов в присутствии алкоголятов — типичная реакция нуклеофильного присоединения.
Водородные атомы в ацетилене способны замещаться на металлы (реакция металлирования). В результате образуются металлические производные ацетилена — ацетилениды. Такую способность ацетилена можно объяснить следующим образом. Углеродные атомы ацетилена, находясь в состоянии sp-гибридизации, отличаются, как известно, повышенной электроотрицательностью (по сравнению с углеродами в других гибридных состояниях). Поэтому электронная плотность связи С-H несколько смещена в сторону углерода и атом водорода приобретает некоторую подвижность:
d+ d- d- d+
H→C≡C←H
Образуются нерастворимые соли — ацетилениды. Возможны только для алкинов, содержащих этинильную группу -С=СН (т. н. терминальные алкины).
HC ≡ CH + 2CuCl → Cu — C ≡ C — Cu↓ + HCl
этин → ацетиленид меди(I) двузамещенный
CH3 — C ≡ CH + CuCl → CH3 — C ≡ C- Cu↓ + HCl
пропин → метилацетиленид меди (I)
Образование темно-красных осадков ацетиленидов меди — качественная реакция на этинильную группу, позволяющая отличить терминальные алкины от других непредельных углеводородов.
С ацетиленидами в сухом виде следует обращаться очень осторожно: они крайне взрывоопасны.
Ацетиленовые углеводороды, как алканы и алкены, способны к изомеризации с перемещением тройной связи:
Н3С — СН2— С ≡ СН Na(спирт р-р)→ Н3С — С ≡ С — СН3
бутин-1 → бутин-2
Из винилацетилена присоединением HCl получают хлоропрен, при полимеризации которого образуется хлоропреновый каучук:
Полимеризация для алкинов малохарактерна.
Ацетилены легко окисляются. При этом происходит разрыв молекулы по месту тройной связи. Если ацетилен пропускать через окислитель (водный раствор перманганата калия), то раствор быстро обесцвечивается. Эта реакция является качественной на кратные (двойные и тройные) связи:
3НC ≡ СН + 10KMnO4 + 2H2O → 6CO2 + 10КОН + 10MnO2
Ацетилен горит коптящим пламенем.
При полном сгорании ацетилена на воздухе образуются два продукта оксид углерода (IV) и вода:
2НС ≡ СН + 5O2 → 4СO2 + 2Н2O
При неполном сгорании образуется углерод (сажа):
НС ≡ СН + O2 → С + СО + Н2О
Способы получения
Ацетилен в промышленности и в лаборатории можно получать следующими способами:
Разложением водой карбида кальция СаС2, который получают спеканием негашеной извести СаО с коксом:
СаО + 3C 2500°C→ CaC2 + CO
СаС2 + 2Н2O → НС ≡ СН + Са(ОН)2
2СН41500°C→ НС ≡ СН + 3Н2
или этана:
С2Н61200°C→ НС ≡ СН + 2Н2
Из дигапогеналканов, содержащих атомы галогена у двух соседних атомов углерода, например:
Из дигалогеналканов, содержащих два атома галогена у одного атома углерода, например:
Качественные реакции
Качественной реакцией на алкины с концевой тройной связью является взаимодействие с аммиакатом серебра или меди.
Для подтверждения наличия тройной связи в соединении используют методы спектроскопии.
Применение
Из всех ацетиленовых углеводородов серьёзное промышленное значение имеет только ацетилен, который является важнейшим химическим сырьём. Его применяют:
— для сварки и резки металлов;
— как источник очень яркого, белого света в автономных светильниках, где он получается реакцией карбида кальция и воды;
— в производстве взрывчатых веществ ацетиленидов (соли ацетилена и его производных, в котором один или два атома водорода замещены атомами элементов, более электроположительных, чем углерод;
Ацетилениды тяжелых металлов обладают значительной химической неустойчивостью, при незначительных внешних воздействиях (удар, трение) разлагаются со взрывом. Наиболее известны как инициирующие взрывчатые вещества (ВВ) ацетилениды серебра Ag2C2 и меди Cu2C2. Также следует отметить сильнейшие взрывчатые способности ацетеленида ртути. Очень сильными взрывчатыми свойствами обладает ацетеленид золота.
— для получения уксусной кислоты, этилового спирта;
— для получения растворителей — индивидуальное химическое соединение или их смесь, способная растворять различные вещества, то есть образовывать с ними однородные системы переменного состава двух или большего числа компонентов;
— для получения пластических масс — органические материалы, основой которых являются синтетические или природные высокомолекулярные соединения (полимеры). Исключительно широкое применение получили пластмассы на основе синтетических полимеров.
Название «пластмассы» означает, что эти материалы под действием нагревания и давления способны формироваться и сохранять после охлаждения или отвердения заданную форму. Процесс формования сопровождается переходом пластически деформируемого (вязкотекучего) состояния в стеклообразное состояние.
— для получения каучука — натуральные или синтетические эластомеры, характеризующиеся эластичностью, водонепроницаемостью и электроизоляционными свойствами, из которых путём вулканизации получают резины и эбониты.
Нахождение в природе и физиологическая роль алкинов
В природе алкины практически не встречаются. В некоторых видах грибов Basidiomycetes были обнаружены в крайне малом количестве соединения содержащие полиацетиленовые структуры.
Ацетилен обнаружен в атмосфере Урана, Юпитера и Сатурна.
Алкины обладают слабым наркозным действием. Жидкие алкины вызывают судороги.
examchemistry.com
Формула Пероксида водорода структурная химическая
Структурная формула
 |
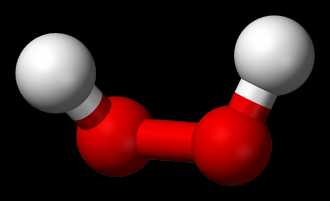 |
Истинная, эмпирическая, или брутто-формула: H2O2
Химический состав Пероксида водорода
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| H | Водород | 1,008 | 2 | 5,9% |
| О | Кислород | 15,999 | 2 | 94,1% |
Молекулярная масса: 34,014
Пероксид водорода (перекись водорода) H2O2 — простейший представитель пероксидов. Бесцветная жидкость с «металлическим» вкусом, неограниченно растворимая в воде, спирте и эфире. Концентрированные водные растворы взрывоопасны. Пероксид водорода является хорошим растворителем. Из воды выделяется в виде неустойчивого кристаллогидрата H2O2•2H2O. Вследствие несимметричности молекула H2O2 сильно полярна (μ = 0,7·10-29 Кл·м). Относительно высокая вязкость жидкого пероксида водорода обусловлена развитой системой водородных связей. Поскольку атомы кислорода имеют неподелённые электронные пары, молекула H2O2 также способна образовывать донорно-акцепторные связи.
Химические свойства
Оба атома кислорода находятся в промежуточной степени окисления −1, что и обусловливает способность пероксидов выступать как в роли окислителей, так и восстановителей. Наиболее характерны для них окислительные свойства. При взаимодействии с сильными окислителями пероксид водорода выступает в роли восстановителя, окисляясь до атомарного кислорода. Молекула пероксида водорода сильно полярна, что приводит к возникновению водородных связей между молекулами. Связь O—O непрочна, поэтому H2O2 — неустойчивое соединение, легко разлагается. Так же этому может поспособствовать присутствие ионов переходных металлов. В разбавленных растворах пероксид водорода тоже неустойчив и самопроизвольно диспропорционирует на H2O и O. Реакция диспропорционирования катализируется ионами переходных металлов, некоторыми белками. Однако очень чистый пероксид водорода вполне устойчив. Пероксид водорода проявляет слабые кислотные свойства (К = 1,4·10-12), и поэтому диссоциирует по двум ступеням. При действии концентрированного раствора H2O2 на некоторые гидроксиды в ряде случаев можно выделить пероксиды металлов, которые можно рассматривать как соли пероксида водорода (Li2O2, MgO2 и др.) Пероксид водорода может проявлять как окислительные, так и восстановительные свойства. Например, при взаимодействии с оксидом серебра он является восстановителем. Пероксидная группа [—O—O—] входит в состав многих веществ. Такие вещества называют пероксидами, или пероксидными соединениями. К ним относятся пероксиды металлов (Na2O2, BaO2 и др.). Кислоты, содержащие пероксидную группу, называют пероксокислотами, например, пероксомонофосфорная H3PO5 и пероксодисерная H2S2O8 кислоты.
Окислительно-восстановительные свойства
Пероксид водорода обладает окислительными, а также восстановительными свойствами. Он окисляет нитриты в нитраты, выделяет иод из иодидов металлов, расщепляет ненасыщенные соединения по месту двойных связей. Пероксид водорода восстанавливает соли золота и серебра, а также марганец при реакции с водным раствором перманганата калия в кислой среде. Окисление органических соединений пероксидом водорода (например, сульфидов и тиолов) целесообразно проводить в среде уксусной кислоты.
Биологические свойства
Пероксид водорода относится к реактивным формам кислорода и при повышенном образовании в клетке вызывает оксидативный стресс. Некоторые ферменты, например глюкозоксидаза, образуют в ходе окислительно-восстановительной реакции пероксид водорода, который может играть защитную роль в качестве бактерицидного агента. В клетках млекопитающих нет ферментов, которые бы восстанавливали кислород до перекиси водорода. Однако несколько ферментных систем (ксантиноксидаза, НАДФ•H-оксидаза, циклооксигеназа и др.) продуцируют супероксид, который спонтанно или под действием супероксиддисмутазы превращается в пероксид водорода.
Получение
Исторически первым промышленным методом синтеза пероксида водорода был электролиз серной кислоты или раствора сульфата аммония в серной кислоте, в ходе которого образуется надсерная кислота, с последующим гидролизом последней до пероксида и серной кислоты. С середины XX века персульфатный процесс синтеза пероксида водорода был вытеснен антрахиноновым процессом, разработанным компанией BASF в 1930-х. В этом процессе формально идет окисление водорода кислородом воздуха с катализом алкилпроизводными антрахинона. Процесс основан на автоокислении алкилантрагидрохинонов (обычно 2-этил-, 2-трет-бутил- и 2-пентилантрагидрохинонов) кислородом воздуха с образованием антрахинонов и пероксида водорода. Реакция проводится в растворе алкилантрагидрохинонов в бензоле с добавлением вторичных спиртов, по завершении процесса пероксид водорода экстрагируют из органической фазы водой. Для регенерации исходных антрагидрохинонов бензольный раствор антрахинонов восстанавливают водородом в присутствии каталитических количеств палладия. Пероксид водорода также может быть получен каталитическим окислением изопропилового спирта, при этом ценным побочным продуктом этой реакции является ацетон, однако в широких масштабах в промышленности этот метод в настоящее время не используется. Концентрирование и очистку пероксида водорода проводят осторожной перегонкой. В последнее время (кон. XX в.) удалось синтезировать H2O3 и H2O4. Эти соединения весьма неустойчивы. При обычных температурах (н.у.) они разлагаются за доли секунды, однако при низких температурах порядка −70 °C существуют часами. Спектро-химическое исследование показывает, что их молекулы имеют зигзагообразную цепную структуру (подобную сульфанам): H—O—O—O—H, H—O—O—O—O—H.
Применение
Благодаря своим сильным окислительным свойствам пероксид водорода нашёл широкое применение в быту и в промышленности, где используется, например, как отбеливатель на текстильном производстве и при изготовлении бумаги. Применяется как ракетное топливо, в качестве окислителя или как однокомпонентное (с разложением на катализаторе), в том числе для привода турбонасосных агрегатов.Используется в аналитической химии, в качестве пенообразователя при производстве пористых материалов, в производстве дезинфицирующих и отбеливающих средств. В промышленности пероксид водорода также находит своё применение в качестве катализатора, гидрирующего агента, как эпоксидирующий агент при эпоксидировании олефинов. Хотя разбавленные растворы перекиси водорода применяются для небольших поверхностных ран, исследования показали, что этот метод, обеспечивая антисептический эффект и очищение, также продлевает время заживления. Обладая хорошими очищающими свойствами, пероксид водорода на самом деле не ускоряет заживление ран. Достаточно высокие концентрации, обеспечивающие антисептический эффект, могут также продлевать время заживления из-за повреждения прилегающих к ране клеток. Более того, пероксид водорода может мешать заживлению и способствовать образованию рубцов из-за разрушения новообразующихся клеток кожи. Однако в качестве средства для очистки глубоких ран сложного профиля, гнойных затёков, флегмон и других гнойных ран, санация которых затруднена, пероксид водорода остаётся предпочтительным препаратом, так как он обладает не только антисептическим эффектом, но и создаёт большое количество пены при взаимодействии с ферментом каталазой. Это в свою очередь позволяет размягчить и отделить от тканей некротизированные участки, сгустки крови, гноя, которые будут легко смыты последующим введением в полость раны антисептического раствора. Без предварительной обработки пероксидом водорода антисептический раствор не сможет удалить эти патологические образования, что приведет к значительному увеличению времени заживления раны и ухудшит состояние больного. Пероксид водорода применяется также для обесцвечивания волос и отбеливания зубов, однако эффект в обоих случаях основан на окислении, а следовательно — разрушении тканей, и потому такое применение (особенно в отношении зубов) не рекомендуется специалистами. В пищевой промышленности растворы пероксида водорода применяются для дезинфекции технологических поверхностей оборудования, непосредственно соприкасающихся с продукцией. Кроме того, на предприятиях по производству молочной продукции и соков, растворы перекиси водорода используются для дезинфекции упаковки (технология «Тетра Пак»). Для технических целей пероксид водорода применяют в производстве электронной техники. В быту применяется также для выведения пятен MnO2, образовавшихся при взаимодействии перманганата калия («марганцовки») с предметами (ввиду его восстановительных свойств). 3%-ный раствор пероксида водорода используется в аквариумистике для оживления задохнувшейся рыбы, а также для очистки аквариумов и борьбы с нежелательной флорой и фауной в аквариуме.
Формы выпуска
Выпускается в виде водных растворов, стандартная концентрация 1-6 %, 30, 38, 50, 60, 85, 90 и 98 %. 30 % водный раствор пероксида водорода, стабилизированный добавлением фосфатов натрия, называется пергидролем. Выпускаемый в виде таблеток твёрдого клатрата с мочевиной пероксид водорода называется гидроперитом.
Опасность применения
Несмотря на то, что пероксид водорода нетоксичен, его концентрированные растворы при попадании на кожу, слизистые оболочки и в дыхательные пути вызывают ожоги. В больших концентрациях недостаточно чистый пероксид водорода может быть взрывоопасен. Опасен при приёме внутрь концентрированных растворов. Вызывает выраженные деструктивные изменения, сходные с действиями щелочей. Летальная доза 30%-го раствора пероксида водорода (пергидроля) — 50—100 мл.
formula-info.ru
