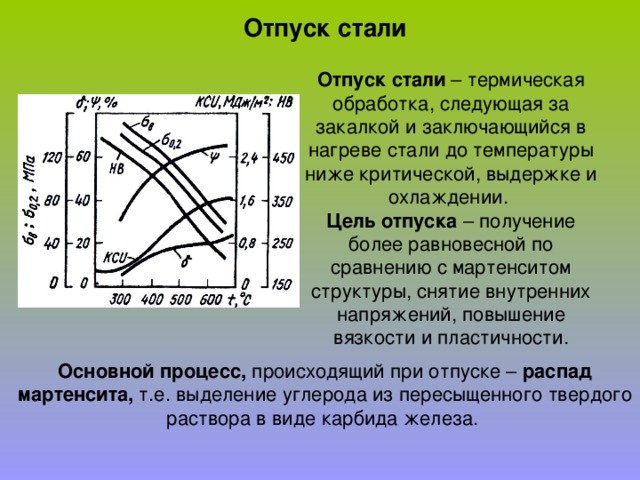
Тренировочные задачи по физике для 8 класса
Тренировочные задачи по физике для 8 класса.
Автор-составитель: учитель физики Трещина Екатерина Игоревна,
г. Таганрог, МОБУ СОШ № 24
Предлагаю вашему вниманию подборку задач для подготовки к ОГЭ по физике. Задачи можно использовать для подготовки к контрольным и зачетным работам, для индивидуальной работы с учениками. Варианты контрольной и зачетной работ (на выбор) представлены после подборки задач.
Теплопередача и работа
Задачи
Часть А
1. Какое количество теплоты потребуется для нагревания стального бруска массой 0,5 кг от 10⁰ до 40 °С?
2. Какое количество теплоты получила вода массой 200 г при нагревании от 10⁰С до 30 °С?
3. Какое количество теплоты необходимо для нагревания железного утюга массой 2 кг от 20⁰С до 320 °С?
4. Какое количество теплоты потребуется для нагревания на 10⁰С олова массой 500 г?
5. Какое количество теплоты потребуется для увеличения температуры латуни массой
0,2 т на 1 °С?
Какое количество теплоты потребуется для увеличения температуры латуни массой
0,2 т на 1 °С?
6. Кирпичная печь массой 1 т остывает от 20⁰С до 10 °С. Какое количество теплоты при этом выделяется?
7. Чугунная болванка массой 32 кг остывает от 1115⁰С до 15 °С. Какое количество теплоты при этом выделяется?
8. Какое количество теплоты выделится при охлаждении 100 г олова, взятого при температуре 82°С, на 50°С ?
9. Какое количество теплоты выделила вода массой 100 г при остывании от 45⁰С до 25 °С?
10. После обработки алюминиевой детали на станке температура ее понизилась от 420⁰С до 20 °С. На сколько при этом уменьшилась внутренняя энергия детали, если ее масса 0,5 кг?
11. Какое количество теплоты отдаст кирпичная печь массой 0,35 т, остывая с изменением температуры на 50 °С?
12. На сколько уменьшится внутренняя энергия латунной гири массой 200 г, если ее охладить на 10 °С?
13.
Для нагревания вещества массой 10 кг на 10 °С потребовалось 420 кДж энергии. Какое вещество нагрели?
Какое вещество нагрели?
14. Нагретый камень массой 5 кг, охлаждаясь в воде на 1 °С, передает ей количество теплоты 2,1 кДж. Чему равна удельная теплоемкость камня?
15. Для нагревания 100 г металла от 20⁰С до 40 °С потребовалось 260 Дж энергии. Что это за металл? (Определить удельную теплоемкость.)
16. При охлаждении жидкости массой 210 кг от 25⁰С до 15 °С выделилось 4,41 МДж теплоты. Что это за жидкость?
17. Стальное сверло при работе получило 5 кДж энергии и нагрелось от 15 до 115 °С. Какова масса этого сверла?
18. Мальчик вычислил, что при нагревании воды от 15°С до кипения внутренняя энергия ее увеличится на 178,5 кДж. Какова масса нагреваемой воды?
19. Стальной молоток был нагрет для закалки до температуры 720 °С, затем быстро охлажден до температуры 10°С. При этом он отдал окружающей среде 298,2 кДж энергии. Найти массу молотка.
20. Кирпичная печь, остыв на 50°С, отдала комнате 15400 кДж энергии. Какова масса
этой печи?
Какова масса
этой печи?
21. Какую массу воды можно нагреть от 15⁰С до 45 °С, затратив для этого 1260 кДж энергии?
22. Какое количество воды можно нагреть от 10⁰С до 60 °С, затратив для этого 210 кДж энергии?
23. На сколько нужно повысить температуру куска свинца массой 100 г, чтобы внутренняя энергия его увеличилась на 280 Дж?
24. При охлаждении куска олова массой 20 г. внутренняя энергия его уменьшилась на 1 кДж. На сколько изменилась температура олова?
25. На сколько градусов нагреется цинковая деталь массой 40 г, если ей сообщить 760 Дж энергии?
26. Какое количество теплоты выделяется при полном сгорании 2,5 кг природного газа?
27. Какое количество теплоты выделяется при полном сгорании бензина массой 5 кг?
28. Какое количество теплоты выделяется при полном сгорании 1,5 т каменного угля?
29. Сколько энергии выделится при полном сгорании древесного угля массой 15 кг?
30. Какое количество теплоты выделится при полном сгорании пороха массой 25 г?
Какое количество теплоты выделится при полном сгорании пороха массой 25 г?
31. Какое количество теплоты выделится при полном сгорании 50 кг сухих березовых дров?
32. Двигатель мопеда на пути 10 км расходует бензин массой 100 г. Какое количество теплоты выделяется при полном сгорании бензина?
33. Какое количество теплоты выделяется при полном сгорании 1,3 кг антрацита?
34. Сколько надо сжечь каменного угля, чтобы при этом выделилось 270 МДж теплоты?
35. Сколько надо сжечь дизельного топлива, чтобы при этом в36. Какую массу торфа надо сжечь для обогревания комнаты, если при сгорании топлива в печи должно выделяться не менее 224 МДж энергии?
37. Какую массу бензина надо сжечь, чтобы получить 230 МДж энергии?
38. Сколько керосина сожгли, если при этом выделилось 55,2 МДж энергии?
39. Чему равна масса сосновых дров, если при полном их сгорании получено 127,4 МДж теплоты?
40. Сколько древесного угля использовали для получения тепла, если получено было
1,27 МДж теплоты?
Сколько древесного угля использовали для получения тепла, если получено было
1,27 МДж теплоты?
41. На сколько уменьшилось количество спирта в спиртовке, если при его горении выделилось количество теплоты 243 кДж?
42. При полном сгорании кокса массой 10 кг выделяется 29 МДж энергии. Чему равна удельная теплота сгорания кокса?
43. При полном сгорании 3 кг топлива выделилось 11,4 МДж энергии. Какое топливо сожгли?
44. При полном сгорании 2 кг жидкости выделилось 92 МДж энергии. Какую жидкость сожгли?
45. При полном сжигании жидкого топлива массой 15 г получено 405 кДж энергии. Какую жидкость использовали как топливо?
46. При полном сгорании 0,5 кг топлива выделилось 7 МДж энергии. Найти удельную теплоту сгорания этого топлива.
47. При сжигании газа выделилось 132 МДж энергии. Чему равна удельная теплота сгорания газа, если его масса равна З кг?
48.
При сжигании 300 г каменного угля выделяется 9 МДж тепла. Найти его удельную
теплоту сгорания.
Найти его удельную
теплоту сгорания.
49. Найти удельную теплоту сгорания сосновых дров, если при сжигании 3 кг этих дров выделилось 39 МДж энергии.
50. Для обращения воды в пар при температуре кипения необходимо количество теплоты 65 МДж. Хватит ли для этого 6 кг сухих березовых дров?
Часть В
51. Какое количество теплоты потребуется для нагревания на 15°С воды объемом 0,5 л?
52. Какое количество теплоты получает при нагревании серебро объемом 2 см3 от 10⁰С до 60 ⁰С?
53. Какое количество теплоты необходимо для нагревания стали объемом 0,5 м3 от 10⁰С до 110 °С?
54. Какое количество теплоты получил нагретый от 10⁰С до 20 °С воздух комнаты, объем которой 60 м3?
55. Какое количество теплоты отдаст стакан кипятка, объемом 250 мл, остывая до температуры 15 °С?
56. Какое количество теплоты отдаст кирпичная печь, сложенная из 500 кирпичей, при
остывании от 70⁰С до 20 °С? Масса одного
кирпича равна 4 кг.
57. В порожнем закрытом металлическом баке вместимостью 60 м 3 под действием солнечного излучения воздух нагрелся от 5⁰С до 25 °С. Как и на сколько изменилась внутренняя энергия воздуха в баке?
58. При изменении температуры куска металла массой 0,08 кг от 20⁰С до 30 °С внутренняя энергия его увеличилась на 320 Дж. Что это заметалл? Найти его объем.
59. Найти объем металлического бруска массой 351 г, если при изменении его температуры от 20 до 24 °С его внутренняя энергия увеличивается на 1326,78 Дж.
60. Как уменьшилась температура кипятка в питьевом баке объемом 27 л, если он отдал окружающей среде 1500 кДж теплоты?
61. На сколько изменится температура воды в стакане, если ей сообщить количество теплоты, равное 109 Дж? Вместимость стакана принять равной 200 см3?
62. При охлаждении куска олова массой 100 г до температуры 32 °С выделилось 5 кДж
энергии. Найти температуру олова до охлаждения.
63. При охлаждении медного паяльника до 20°С выделилось 30,4 кДж энергии. До какой температуры был нагрет паяльник, если его масса 200 г?
64. До какой температуры остынут 5 л кипятка, взятого при температуре 100 °С, отдав в окружающее пространство 1680 кДж энергии?
65. Термос объемом 3 л заполнили кипятком. Через 20 часов температура воды в нем понизилась до 80 °С. На сколько изменилась внутренняя энергия воды?
66. Сколько теплоты выделится при полном сгорании сухихберезовых дров объемом 5 м³?
67. Сколько теплоты выделится при полном сгорании нефти объемом 250 л?
68. В каком случае выделится большее количество теплоты: при полном сгорании древесного угля массой 3 кг или при полном сгорании сухих дров массой 9 кг?
69. На сколько больше теплоты выделится при полном сгорании бензина массой 1,5 кг, чем при сгорании сухих березовых дров той же массы?
70. Во сколько раз больше выделится теплоты при полном сгорании водорода массой 2 кг, чем при полном сгорании сухих березовых дров той же массы?
71. В печи сгорели сухие сосновые дрова объемом 0,02 м3 и торф массой 2 кг. Сколько
теплоты выделилось в печи?
В печи сгорели сухие сосновые дрова объемом 0,02 м3 и торф массой 2 кг. Сколько
теплоты выделилось в печи?
72. Смешали бензин объемом 1,5 л и спирт объемом 0,5 л. Какое количество теплоты выделится при полном сгорании этого топлива?
73. К зиме заготовили сухие березовые дрова объемом 3 м3 и каменный уголь массой 1,5 т. Сколько теплоты выделится в печи при полном сгорании в ней заготовленного топлива?
74. Сколько каменного угля нужно сжечь, чтобы получить столько же энергии, сколько ее выделяется при полном сгорании бензина объемом 6 м3?
75. Какую массу каменного угля нужно сжечь, чтобы получить такое же количество теплоты .которое выделяется при сгорании керосина массой 20 т?
Часть С
76. Какое количество теплоты получила вода при нагревании от 15⁰С до 25 °С в бассейне, длина которого 100 м, ширина 6 м и глубина 20 дм?
77. Какое количество теплоты потребуется для того, чтобы в латунной бочке массой 12 кг нагреть воду объемом 9,5 л от температуры 20⁰С до 100⁰С
78. Алюминиевая фляга массой 12 кг вмещает 36 л молока. Какое количество теплоты
потребуется для нагревания молока во фляге от0 до 60 °С ?
Алюминиевая фляга массой 12 кг вмещает 36 л молока. Какое количество теплоты
потребуется для нагревания молока во фляге от0 до 60 °С ?
79. В железный душевой бак, масса которого 65 кг, налили холодной воды из колодца, объемом 200 л. В результате нагревания солнечным излучением температура воды повысилась от 4⁰С до 29 °С. Какое количество теплоты получили бак и вода?
80. Какое количество теплоты получили алюминиевая кастрюля массой 200 г и находящаяся в ней вода объемом 1,5 л при нагревании от 20 °С до кипения?
81. На сколько изменится температура куска меди массой 500 г, если ему сообщить такое же количество теплоты, которое пойдет на нагревание воды массой 200 г от 10 ⁰С до 60 °С?
82. До какой температуры нагрелась во время работы стальная фреза массой 1 кг, если после погружения ее в сосуд с водой, масса которой 1 кг, температура воды повысилась от 10⁰С до 30 °С?
83.
Двигатель мощностью 75 Вт в течение 5 мин вращает лопасти винта внутри
калориметра, в котором находится вода объемом 5 л. Вследствие трения о воду
лопастей винта вода нагрелась. Считая, что вся энергия пошла на нагревание
воды, определить, как изменилась ее температура?
Вследствие трения о воду
лопастей винта вода нагрелась. Считая, что вся энергия пошла на нагревание
воды, определить, как изменилась ее температура?
84. При работе машины внутренняя энергия одной из алюминиевых деталей массой 2 кг повысилась на столько, на сколько увеличивается внутренняя энергия воды массой 800 г. При нагревании ее от 0⁰С до 100°С. На сколько повысилась температура детали?
85. Как изменится температура воды массой 3 кг, если вся теплота, выделившаяся при полном сгорании спирта объемом 12,5 мм3, пошла на ее нагревание?
86. На сколько изменится температура воды объемом 100 л, если считать, что вся теплота, выделяемая при сжигании древесного угля массой 0,5 кг, пойдет на нагревание воды?
87. На сколько изменится температура воды, масса которой 22 кг, если ей передать всю энергию, выделившуюся при полном сгорании 10 г природного газа?
88. В ванну налили 40 л холодной воды температурой 6 °С. Затем долили горячую воду
температурой 96 °С. Температура воды после этого стала равной 36 °С. Найти массу
долитой воды. Нагреванием ванны и окружающей среды пренебречь.
Температура воды после этого стала равной 36 °С. Найти массу
долитой воды. Нагреванием ванны и окружающей среды пренебречь.
89. Мальчик налил в ведро 3 л воды, температура которой равна 10 °С. Сколько кипятка нужно долить в ведро, чтобы температура воды в нем стала равной 50 °С?
90. В воду объемом 1 л опустили кусок олова, нагретый до температуры 188 °С. Температура воды при этом увеличилась от 10⁰С до 20 °С. Чему равна масса куска олова?
91. В кувшин с водой, масса которой 100 г, а температура 20°С, влили воду при температуре 100 °С, после чего температура воды в кувшине стала равной 75 °С. Определить массу горячей воды. Потери энергии на нагревание кувшина не учитывать.
92. Сколько воды, взятой при температуре 10 «С, можно нагреть до 50 °С, сжигая керосин массой 15 г, считая, что вся выделяемая при горении керосина энергии идет на нагревание воды?
93. Сколько спирта надо сжечь, чтобы изменить температуру воды объемом 2 дм3 от 14⁰С до 50 °С, если вся теплота, выделенная спиртом, пойдет на нагревание воды?
94. Когда в бак с водой добавили еще 3 л воды при 100 °С и перемешали всю воду, то
температура воды в баке стала равна 35°С. Найти начальный объем воды в баке.
Когда в бак с водой добавили еще 3 л воды при 100 °С и перемешали всю воду, то
температура воды в баке стала равна 35°С. Найти начальный объем воды в баке.
95. В сосуд с водой, масса которой 150 г, а температура 16°С, добавили воду массой 50 г при температуре 80 °С. Определить температуру смеси.
96. В кастрюле с холодной водой, масса которой 3 кг, а температура 10°С, влили 2 кг кипятку. Какая установится температура воды? Нагреванием сосуда пренебречь.
97. На нагревание кирпича массой 4 кг на 63°С затрачено такое же количество теплоты, как и для нагревания воды той же массы на 13,2 °С. Определить удельную теплоемкость кирпича.
98. Металлическое тело массой 30 г нагрели в кипящей воде. После этого его перенесли в воду, масса которой 73,5 г и температура 20°С, налитую в калориметр. Вода от этого нагрелась до 23 °С. Из какого металла сделано тело?
99.
В стакан, содержащий 230 г кипятка, опустили ложку массой 150 г, имеющую
температуру 20 °С. Температура воды понизилась от этого до 97°С. Верно ли, что
эта ложка алюминиевая?
Температура воды понизилась от этого до 97°С. Верно ли, что
эта ложка алюминиевая?
100. Твердое тело массой 80 г опустили в кипяток. Затем его перенесли в калориметр, куда была налита вода массой 166,5 г при температуре 20 °С. Температура воды повысилась до 24°С. Найти удельную теплоемкость твердого тела. если выделилось 427 МДж теплоты?
Контрольная работа.
Вариант1
1. Кирпичная печь массой 1 т остывает от 20⁰С до 10 °С. Какое количество теплоты при этом выделяется?
2. Для нагревания вещества массой 10 кг на 10 °С потребовалось 420 кДж энергии. Какое вещество нагрели?
3. При охлаждении куска олова массой 100 г до температуры 32 °С выделилось 5 кДж энергии. Найти температуру олова до охлаждения.
4. Сколько спирта надо сжечь, чтобы изменить температуру воды объемом 2 дм3 от 14⁰С до 50 °С, если вся теплота, выделенная спиртом, пойдет на нагревание воды?
Вариант2
1. Какое количество теплоты получила вода
массой 200 г при нагревании от 10⁰С
до 30 °С?
Какое количество теплоты получила вода
массой 200 г при нагревании от 10⁰С
до 30 °С?
2. После обработки алюминиевой детали на станке температура ее понизилась от 420⁰С до 20 °С. На сколько при этом уменьшилась внутренняя энергия детали, если ее масса 0,5 кг?
3. До какой температуры остынут 5 л кипятка, взятого при температуре 100 °С, отдав в окружающее пространство 1680 кДж энергии?
4. В сосуд с водой, масса которой 150 г, а температура 16°С, добавили воду массой 50 г при температуре 80 °С. Определить температуру смеси.
Вариант3
1. Какое количество теплоты выделится при охлаждении 100 г олова, взятого при температуре 82°С, на 50°С ?
2. При охлаждении жидкости массой 210 кг от 25⁰С до 15 °С выделилось 4,41 МДж теплоты. Что это за жидкость?
3. Смешали бензин объемом 1,5 л и спирт объемом 0,5 л. Какое количество теплоты выделится при полном сгорании этого топлива?
4.
В воду объемом 1 л опустили кусок олова,
нагретый до температуры 188 °С. Температура воды при этом увеличилась от 10⁰С
до 20 °С. Чему равна масса куска олова?
Температура воды при этом увеличилась от 10⁰С
до 20 °С. Чему равна масса куска олова?
Зачет по теме
Вариант 1
1.Каким способом – совершением работы или теплопередачей – изменилась внутренняя энергия детали при ее нагревании в печи перед закалкой?
1) совершением работы 2) теплопередачей 3) совершением работы и теплопередачей
2. Удельная теплоемкость вещества показывает
1) какое количество теплоты необходимо передать телу для изменения его температуры на 1 градус
2) какое количество теплоты необходимо передать 1 кг вещества для изменения его температуры на 100 градусов
3) какое количество теплоты необходимо передать телу массой 1кг для изменения его температуры на 1 градус
3. Что потребует большего количества теплоты для нагревания на 10 С: 100 г воды или 100 г меди?
1) 100 г воды 2) 100 г меди 3) потребуется одинаковое количество теплоты
4. В каком случае кастрюля с горячей водой остынет быстрее, если ее поставить на
лед или если лед на крышку кастрюли положить сверху? Ответ пояснить
В каком случае кастрюля с горячей водой остынет быстрее, если ее поставить на
лед или если лед на крышку кастрюли положить сверху? Ответ пояснить
5. Чтобы нагреть 110 г алюминия на 90 0С требуется количество теплоты, равное 9,1 кДж. Вычислите удельную теплоемкость алюминия.
6. Смешали 39 л воды при температуре 20 0С и 21 л воды при температуре 60 0С. Определите температуру смеси.
Вариант 2
1. Каким способом изменялась внутренняя энергия детали при сверлении в ней отверстия
1) совершением работы 2) теплопередачей 3) совершением работы и теплопередачей
2. Количество теплоты зависит от
1) массы тела и его температуры
2) от рода вещества, из которого изготовлено тело и массы тела
3) от массы тела, начальной и конечной температур тела, рода вещества
3. Как называется величина, показывающая , какое количество теплоты необходимо для нагревания 1 кг железа на 10 С?
1) внутренняя энергия 2) количество теплоты 3) удельная теплоемкость вещества
4. Когда парусным судам легче заходить в гавань – днем или вечером? Ответ пояснить
Когда парусным судам легче заходить в гавань – днем или вечером? Ответ пояснить
5. Какова масса железной детали, если на ее нагревание от 20 0С до 200 0С потребовалось 20,7 кДж теплоты?
6. Вода массой 150 г имеет температуру 10 0С. Найти температуру воды после того, как в нее опустили железную деталь массой 0,5 кг, имеющую температуру 100 0С.
Вариант 3
1. Каким способом изменялась внутренняя энергия воды при ее нагревании в чайнике
1) совершением работы 2) теплопередачей 3) совершением работы и теплопередачей
2. Чугунную деталь массой 1 кг нагрели на 1 0С. На сколько при этом увеличилась ее внутренняя энергия?
1) на 540 Дж 2) на 540 Дж/ кг 0С 3) на 1 Дж
3. По куску свинца и куску стали одинаковой массы ударили молотком одинаковое число раз. Какой кусок нагрелся больше?
1) из стали 2) из свинца 3) невозможно определить
4.
В каком случае лед, внесенный в теплую комнату растает быстрее: если его просто
положить на стол , или, если сверху прикрыть шерстяным платком. Ответ пояснить
Ответ пояснить
5. На сколько градусов повысилась температура 4 кг воды, если она получила количество теплоты, равное 168 кДж?
6. Мальчик наполнил стакан кипятком, налив его 150 г, а затем добавил 50 г воды с температурой 20 0С. Определите температуру, которая установилась в стакане.
Литература
1) Р.А. Рахматуллин. Текстовые расчетные задачи, 8 кл. — Оренбург, 1997 – 59 с
2) Лукашева Е.В. Типовые тестовые задания. Физика. Изд-во «Экзамен», 2016 -126с
задачи для подготовки к контрольной работе | Материал для подготовки к ЕГЭ (ГИА) по естествознанию (8 класс) на тему:
Опубликовано 16.10.2014 — 23:01 — Дуденкова Галина Петровна
задачи для подготовки к контрольной работе в 8 классе.
Скачать:
Предварительный просмотр:
1 группа
- При остывании от 72°С до 22 °С кирпичная печь отдала окружающей среде 5250 кДж теплоты. Определите массу кирпичной печи.
- Какое количество теплоты выделится при полном сгорании 5 л бензина? Плотность бензина 800 кг/м3 .

- Длина прямоугольного бассейна 50 м, ширина 10 м и глубина 4 м. вода в бассейне нагрелась от 30 °С до 50 °С. Какое количество теплоты получила вода? Плотность воды 1000 кг/м3 .
- Удельная теплоёмкость льда равна 2100 Дж/кг °С, а воды 4200 Дж/кг °С. Какое вещество нагреется до большей температуры при сообщении им одинакового количества теплоты? Массы воды и льда равны 1 кг.
2 группа
- Сколько теплоты требуется для нагревания свинцовой детали массой 400 грамм на 60 °С?
- Брусок каменного угля с размерами 10 х 20 х 80 см сгорает в печи. Сколько теплоты при этом выделяется?
- Сколько воды можно нагреть на 70 °С, если сообщить ей 420 кДж теплоты?
- Во время работы стальное сверло нагрелось на 100 °С, а затем охладилось на воздухе до прежней температуры. За счёт чего увеличилась, а затем уменьшилась внутренняя энергия сверла?
3 группа
- На сколько градусов нагреется 300 г воды, если ей сообщить 6,3 кДж теплоты.

- Какое количество теплоты выделится при полном сгорании 2 м3 каменного угля? Плотность угля 1500 кг/м3
- Воду массой 200 грамм нагрели на 50 °С, а воду массой 400 грамм на 200 °С. Какая вода получила большее количество теплоты и во сколько раз?
- Почему при обработке детали напильником деталь и напильник нагреваются?
4 группа
- Стальной молоток был нагрет при закалке до 700 °С затем быстро охлаждён до 20 °С. При этом выделилось 550 кДж теплоты. Найдите массу молотка.
- Сколько дров нужно сжечь, чтобы выделилось 500 кДж теплоты? Найти массу и объём сгоревших дров.
- Температура стальной детали размерами 10 х 20 х 15 см изменилась от 50 до 150 °С. Какое количество теплоты передала при этом пластинка окружающим телам? Плотность стали 7800 кг/м3
- Почему весной снег тает быстрее в городе, чем в поле?
5 группа
- На сколько градусов нагреется 2 литра спирта, получив 168 кДж теплоты? Плотность спирта 790 кг/м3
- Сколько джоулей энергии выделится при полном сгорании 3 т дров?
- В баке размерами 2 х3 х 4 м находится вода.
 Сколько теплоты выделится при полном остывании воды на 40 °С? Плотность воды 1000 кг/м3
Сколько теплоты выделится при полном остывании воды на 40 °С? Плотность воды 1000 кг/м3
- Удельная теплота сгорания торфа 1,4 ∙ 107 Дж/кг, а керосина – 4,6 ∙ 107 Дж/кг. При сгорании, какого вещества выделится большее количество теплоты?
3 группа
- На сколько градусов нагреется 300 г воды, если ей сообщить 6,3 кДж теплоты.
- Какое количество теплоты выделится при полном сгорании 2 м3 каменного угля? Плотность угля 1500 кг/м3
- Воду массой 200 грамм нагрели на 50 °С, а воду массой 400 грамм на 200 °С. Какая вода получила большее количество теплоты и во сколько раз?
- Почему при обработке детали напильником деталь и напильник нагреваются?
По теме: методические разработки, презентации и конспекты
Решение задач методом Ключевых ситуаций. Контрольная работа №1. 7-ой класс.» Плотность характиеризует вещество». «Архимедова сила».
 .
.Дистанционный курс повышения квалификации «Как научиться решать задачи по физике (основная школа).Подготовка к ГИА». В школьном курсе огромное количество задач, которые можно сгруппировать вокруг неск…
Решение задач методом Ключевых ситуаций. Контрольная работа №1. 7-ой класс.» Плотность характиеризует вещество». «Архимедова сила»..
Дистанционный курс повышения квалификации «Как научиться решать задачи по физике (основная школа).Подготовка к ГИА». В школьном курсе огромное количество задач, которые можно сгруппировать вокруг неск…
Решение задач методом Ключевых ситуаций. Контрольная работа №1. 7-ой класс.» Плотность характиеризует вещество». «Архимедова сила»..
Дистанционный курс повышения квалификации «Как научиться решать задачи по физике (основная школа).Подготовка к ГИА». В школьном курсе огромное количество задач, которые можно сгруппировать вокруг неск…
Конспект урока, построенный по модульному принципу «Подготовка к контрольной работе по теме «Морфология».

Интегрирующая дидактическая цель: подготовить к контрольной работе.Целевой план действий для учащихся:· проверить знания, умения и навыки учащихся, степень ос…
Задачи для подготовки к контрольной работе «Начальные геометрические сведения»
Содержит подборку задач на смежные и вертикальные углы. Можно применять как для решения в классе, так и дать на домашнее задание….
задачи для самостоятельных и контрольных работ по физике для 10 класса
Данный материал разработан для контроля уровня усвоения предметных знаний по «Механике"…
Решение задач. Подготовка к контрольной работе по геометрии «Аксиомы стереометрии. Взаимное расположение прямых, прямой и плоскости. 10 класс
повторить аксиомы, признак параллельности прямой и плоскости, свойство транзитивности, угол между скрещивающимися прямыми…
Поделиться:
Краски для отпуска стали
Стали, содержащие более 0,3% углерода, предназначены для термической обработки. Низкое содержание углерода делает сталь более прочной, чем твердой, и подходит для применений, где важна прочность, например, пружины и высокопрочные болты. Стали с содержанием углерода более 0,7% могут быть закалены до более высокой степени и подходят для применений, где важна твердость, а не ударная вязкость. Инструментальные стали отлично подходят для резки и сверления, поскольку они содержат вольфрам, молибден, кобальт и ванадий для повышения термостойкости и долговечности.
Низкое содержание углерода делает сталь более прочной, чем твердой, и подходит для применений, где важна прочность, например, пружины и высокопрочные болты. Стали с содержанием углерода более 0,7% могут быть закалены до более высокой степени и подходят для применений, где важна твердость, а не ударная вязкость. Инструментальные стали отлично подходят для резки и сверления, поскольку они содержат вольфрам, молибден, кобальт и ванадий для повышения термостойкости и долговечности.
Закалка стали представляет собой двухэтапный процесс, при котором
1. Инструмент проковывается и закаляется
- Конец инструмента нагревается до ярко-красного цвета и проковывается
| Steel | ||
|---|---|---|
| ( o F) | ( o C) | |
| 2192 | 1200 | |
| 2012 | 1100 | |
| 1922 | 1050 | |
| 1796 | 980 | |
| 1706 | 930 | |
| 1598 | 870 | |
| 1490 | 810 | |
| 1400 | 760 | |
9 129239 | ||
| 1202 | 650 | |
| 1112 | 600 |
- tool quenched in cold water and cooled until touchable
- tool is sharpened and polished
2. The tool закален
The tool закален
- инструмент, нагретый до температуры отпуска, как указано ниже
| Температура | Цвет нагретой углеродистой стали | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ( o F) | ( o C) | |||||||||||||||||||||||||||||||||
| 600 | 316 | Scrapers, spokeshaves | ||||||||||||||||||||||||||||||||
| 560 | 293 | отвертки, Springs, Gears | ||||||||||||||||||||||||||||||||
| 540 | 282 | Холодные зубчатые зубцы, центральные удары | ||||||||||||||||||||||||||||||||
| 520 | 27191 | |||||||||||||||||||||||||||||||||
| 520 | 11919| 520 | 11919 900 | 520 | .0040 | Taps <= 1/4 inch | 500 | 260 | | Axes, wood chisels, drifts, taps >= 1/ inch, nut taps, thread dies, press tools | 480 | 249 | | Twist drills, large taps, knurls | 460 | 238 | | Dies, punches, bits, reamers | 450 | 232 | | Twist drills for hard use | 440 | 227 | | Turning tools, lathe tools, scrapers, milling, cutters, reamers | 430 | 221 | | Edge tools, reamers | 420 | 216 | | Ножи, молотки | |
- инструмент, закаленный в холодной воде
Применяются также свинцовые ванны и песочные ванны.
Если сталь нагревают в окислительной атмосфере, такой как воздух, на поверхности образуется пленка оксида, и цвет меняется при повышении температуры. На цвета в некоторой степени влияет состав стали, и метод может быть ненадежным.
Melting Points of Heat-Treating Baths
| Material | Melting Point | |
|---|---|---|
| ( o F) | ( o C) | |
| 35% lead, 65% tin | 358 | 181 |
| 50% sodium nitrate, 50% porassium nitrate | 424 | 218 |
| Tin | 450 | 232 |
| Sodium nitrate | 586 | 308 |
| Lead | 620 | 327 |
| Potassium nitrate | 642 | 339 |
| 45% sodium chloride, 50% sodium sulfate | 1154 | 623 |
| Sodium chloride | 1474 | 801 |
| Sodium sulfate | 1618 | 881 |
| Barium chloride | 1760 | 960 |
Что происходит при отпуске стали?
Спасибо Шону Хьюстону и Тайлеру Кристиану за то, что они стали сторонниками Knife Steel Nerds Patreon. Мы достигли нашей первой цели, и поэтому я возьму интервью у Девина Томаса и опубликую его в виде статьи на веб-сайте.
Мы достигли нашей первой цели, и поэтому я возьму интервью у Девина Томаса и опубликую его в виде статьи на веб-сайте.
В предыдущем посте я писал о том, что происходит во время быстрой закалки стали: Что делает закаленную сталь такой твердой?.
Несколько важных моментов из этого поста, которые следует запомнить для этого:
- Сталь приобретает высокую закалочную твердость за счет образования мартенсита при охлаждении высокотемпературного аустенита
- Больше углерода в мартенсите означает более высокую твердость
- Твердость/прочность увеличивается за счет затруднения движения «дислокаций» внутри материала, которые представляют собой линейные дефекты в атомной структуре
- Движение дислокаций в мартенсите предотвращается из-за твердорастворного упрочнения углерода, высокой плотности дислокаций, «тетрагональности» мартенсита и множества границ пакетов и блоков
- Когда превращение в мартенсит не завершено, любой оставшийся аустенит называется «остаточным аустенитом»
После закалки стали образуется мартенситная микроструктура с внедренными атомами углерода между атомами железа, что делает кристаллическую структуру «тетрагональной», а не кубической:
Процесс закалки, образование мартенсита и перенасыщение углеродом приводят к хрупкости стали.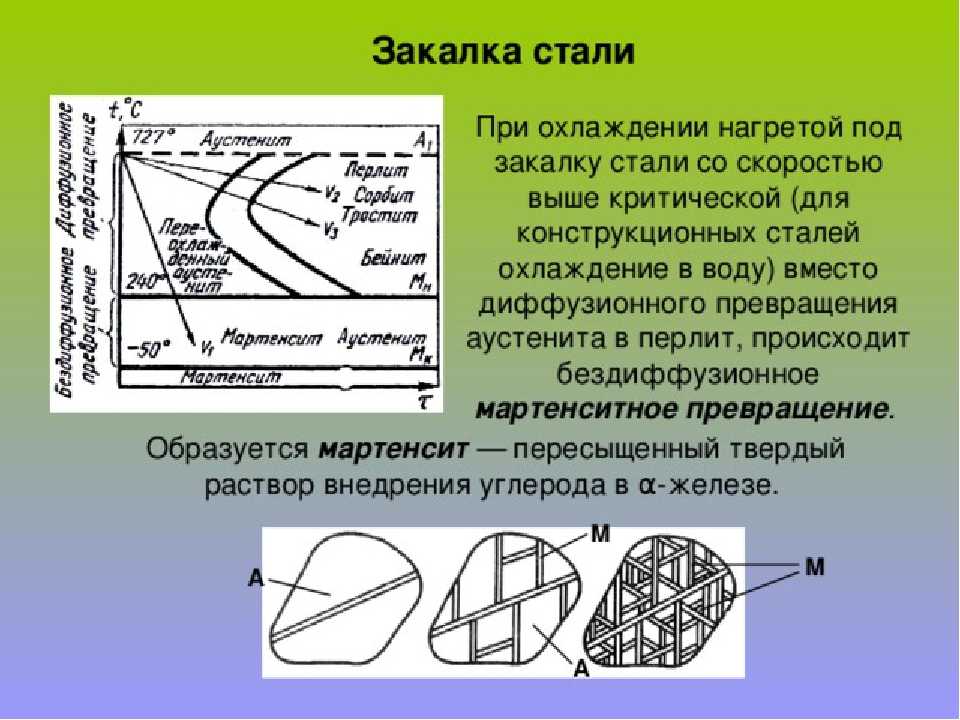 Основной причиной отпуска стали является снижение ее хрупкости или, другими словами, повышение ее ударной вязкости, как показано здесь для инструментальной стали L6 [1]:
Основной причиной отпуска стали является снижение ее хрупкости или, другими словами, повышение ее ударной вязкости, как показано здесь для инструментальной стали L6 [1]:
Отпуск не только повышает ударную вязкость, снижает твердость стали, как показано здесь из таблицы данных для стали 14-4CrMo (аналогично 154CM) [2]:
Потеря углерода
Если вы посмотрите на фазовую диаграмму железо-углерод при комнатной температуре, вы не увидите на ней мартенсита, но вместо этого увидите феррит + карбиды:
Карбиды
Карбиды твердые частицы, образованные между железом (или другими элементами) и углеродом. Причина, по которой мартенсит не превращается самопроизвольно в феррит и карбиды, заключается в том, что углерод не может легко диффундировать при комнатной температуре. Однако, если сталь нагрета, углерод может диффундировать из мартенсита. Эта потеря углерода означает, что прочность мартенсита снижается. Углерод покидает мартенсит, осаждаясь в виде карбидов.
Цементит и переходные карбиды
На приведенной выше диаграмме состояния равновесия эти карбиды представляют собой цементит (Fe 3 C), где на каждые три атома железа в структуре цементита приходится один атом углерода. Цементит иногда обозначается θ (тета). Однако сначала образуются «переходные» карбиды, представляющие собой неравновесные карбиды, меньшие по размеру, чем цементит. Существует два основных типа переходных карбидов, которые называются η- (эта) или ε- (эпсилон) карбидами. Эти карбиды имеют состав от Fe2C до Fe2,4C. Кристаллические структуры карбидов эта и эпсилон трудно различить, поэтому не всегда известно, какие формы (или и те, и другие), но это, вероятно, не важно для этой статьи; однако появляется все больше свидетельств того, что эта-карбиды являются основным переходным карбидом, особенно в высокоуглеродистых сталях [3]. Эти карбиды очень малы (2-4 нм), поэтому для их изображения требуется чрезвычайно высокое разрешение. С повышением температуры или времени переходные карбиды увеличиваются в размерах и в конечном итоге замещаются цементитом, который снова продолжает укрупняться с повышением температуры или времени. Здесь вы можете увидеть изображение переходных карбидов (ряды крошечных белых кругов) и цементита (линейные элементы несколько большего размера) в стали, отпущенной при 300°F [3]:
Здесь вы можете увидеть изображение переходных карбидов (ряды крошечных белых кругов) и цементита (линейные элементы несколько большего размера) в стали, отпущенной при 300°F [3]:
Переходные карбиды растворяются и замещаются большим количеством цементита, а мелкие частицы цементита со временем заменяются более крупными пластинами цементита. Затем процесс образования карбида можно резюмировать на следующих изображениях, где слева показан неотпущенный мартенсит, затем на среднем изображении показаны мелкие цементитные карбиды после отпуска при 375°F в течение 1 часа, а затем на правом изображении показаны более крупные пластины из цементит после отпуска при 790°F в течение 1 часа [4]:
Дисперсионное упрочнение
Если вы вспомните кривую отпуска для 14-4CrMo, вы, возможно, вспомните небольшое увеличение твердости при очень низких температурах: называется «осаждением». Другими словами, осадки или, в данном случае, карбиды увеличивают твердость стали. Как я уже говорил в предыдущем посте, упрочнение происходит за счет ограничения движения дислокаций: как измельчение зерна приводит к улучшению свойств? Карбиды могут ограничивать движение дислокаций, так как дислокации не могут легко пройти через них. С очень маленькими карбидами дислокации прорезают или сдвигают карбиды, а с более крупными карбидами дислокации должны обвиваться вокруг них [5]:
Как я уже говорил в предыдущем посте, упрочнение происходит за счет ограничения движения дислокаций: как измельчение зерна приводит к улучшению свойств? Карбиды могут ограничивать движение дислокаций, так как дислокации не могут легко пройти через них. С очень маленькими карбидами дислокации прорезают или сдвигают карбиды, а с более крупными карбидами дислокации должны обвиваться вокруг них [5]:
Таким образом, когда имеется массив карбидов, дислокации должны проходить через многие карбиды или вокруг них [6]: ]:
Существует оптимальный размер карбидов для упрочнения стали. Когда карбиды чрезвычайно малы, дислокации легко проходят сквозь них. Когда карбиды слишком велики, дислокации могут легко перемещаться вокруг них. В результате получается оптимальный размер карбидов для пикового упрочнения [8]:
В результате получается оптимальный размер карбидов для пикового упрочнения [8]:
Изменения в структуре мартенсита
Сам мартенсит также изменяется при отпуске. Одно изменение, которое происходит, заключается в том, что «тетрагональность» мартенсита уменьшается по мере того, как мартенсит становится все более и более похожим на кубический феррит по мере того, как углерод покидает мартенсит. Еще одно изменение заключается в том, что плотность дислокаций уменьшается при отпуске, как показано на этой схеме [9]:
мартенсит без отпуска. Затем (b) показывает небольшой черный линейный цементит внутри реек, окруженный дислокациями, который представляет собой мартенсит, отпущенный при температуре около 500 ° F. Изображение в (c) показывает, что дислокации стали восстановленными «ячейками» дислокаций, которые представляют собой малоугловые границы, которые представляют собой мартенсит, отпущенный при 1000 ° F. И, наконец, (d) показывает рекристаллизованный мартенсит, который полностью превратился в круглые зерна феррита, которые также содержат более крупные карбиды.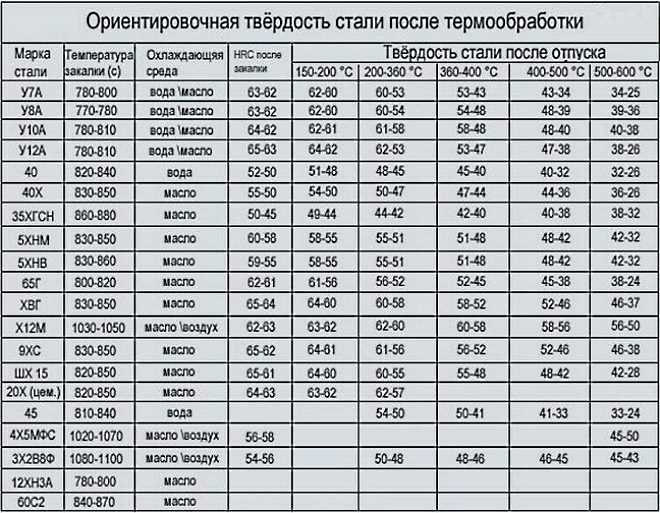
Эти изменения также видны на следующих микрофотографиях [10]:
Крайнее левое изображение показывает слабоотпущенный мартенсит, где рейки «темные» из-за высокой плотности дислокаций. На среднем изображении показана микроструктура восстановленного мартенсита после отпуска при 1290 °F в течение 2 часов, где мартенсит «чистый» и белый, что свидетельствует о низкой плотности дислокаций, но границы реек все еще видны. На правом изображении показана сталь, отпущенная при 1290°F в течение 12 часов, где видно начало рекристаллизации мартенсита, где круглые зерна феррита начали замещать мартенситные пластины.
Вторичная закалка
В некоторых видах сталей наблюдается вторичное повышение твердости при высоких температурах отпуска, ~800-1200°F. Это особенно заметно для сталей, легированных значительным количеством вольфрама или молибдена [4]:
Здесь все еще действуют описанные выше механизмы. Мартенсит все еще восстанавливается и в конечном итоге рекристаллизуется, и образуются переходные карбиды, которые замещаются цементитом. Однако при более высоких температурах цементит растворяется и выпадают в осадок новые карбиды, такие как Мо 2 C, W 2 C или V 4 C 3 карбиды. Это начинается с нового режима дисперсионного упрочнения, где наблюдается пик прочности от «идеального» размера карбидов. Это показано на следующей диаграмме [11]:
Однако при более высоких температурах цементит растворяется и выпадают в осадок новые карбиды, такие как Мо 2 C, W 2 C или V 4 C 3 карбиды. Это начинается с нового режима дисперсионного упрочнения, где наблюдается пик прочности от «идеального» размера карбидов. Это показано на следующей диаграмме [11]:
Таким образом, несмотря на восстановление самого мартенсита, которое обычно приводит к потере прочности, образование этих мелких карбидов приводит к увеличению прочности при высоких температурах. Это может позволить эксплуатировать стали при высоких температурах, потому что их можно «переотпускать» без потери прочности из-за образования этих карбидов. Я рассказал об открытии этого явления в следующей статье: История первой инструментальной стали.
Остаточный аустенит
С остаточным аустенитом во время отпуска может произойти несколько вещей [12]:
- Стабилизация остаточного аустенита таким образом, что он не может легко трансформироваться при дальнейшем отпуске или холодной обработке
- Разложение на бейнит или другие фазы «феррит плюс карбид»
- Дестабилизация, приводящая к образованию неотпущенного мартенсита после охлаждения от температуры отпуска
Стабилизация остаточного аустенита может происходить за счет диффузии углерода из мартенсита в аустенит, а не путем осаждения в виде карбидов.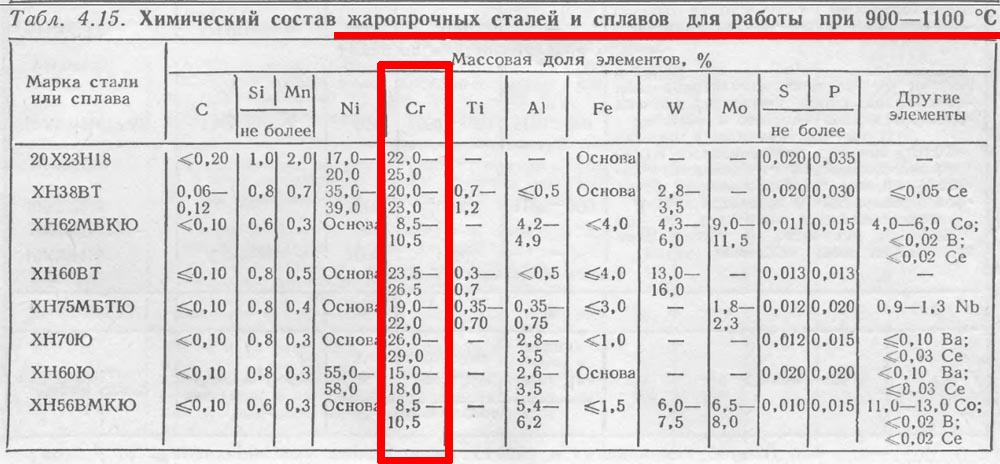 Более высокое содержание углерода в аустените стабилизирует его за счет снижения температуры начала мартенсита [13]. Стабилизация чаще всего происходит при отпуске при относительно низких температурах, когда не происходит распада аустенита.
Более высокое содержание углерода в аустените стабилизирует его за счет снижения температуры начала мартенсита [13]. Стабилизация чаще всего происходит при отпуске при относительно низких температурах, когда не происходит распада аустенита.
Разложение на феррит плюс карбиды или бейнит происходит аналогично аустенитному отпуску, когда сталь быстро охлаждают до промежуточной температуры и выдерживают для образования бейнита, а не охлаждают до комнатной температуры для образования мартенсита. Бейнит представляет собой промежуточную фазу, которая может выглядеть несколько похожей на мартенсит отпуска, поскольку представляет собой решетчатую фазу с карбидами внутри и между решетками. Таким образом, даже если сталь была охлаждена до комнатной температуры, оставшийся аустенит все еще ведет себя так же, как во время аустенитного отпуска, если сталь повторно нагревают до температуры, при которой образуется бейнит. Это превращение происходит с низколегированными сталями, но может быть подавлено достаточными добавками определенных легирующих элементов [12]. Вот график, показывающий распад аустенита во времени при трех разных температурах отпуска в простой стали 1,2С [14]:
Вот график, показывающий распад аустенита во времени при трех разных температурах отпуска в простой стали 1,2С [14]:
В большинстве высоколегированных инструментальных, быстрорежущих и нержавеющих сталей образование бейнита происходит очень медленно из-за высокого уровня легирования. Вместо этого сталь теряет аустенит из-за дестабилизации, когда аустенит превращается в мартенсит при охлаждении от температуры отпуска. Это работает за счет выделения карбидов из аустенита; потеря углерода из аустенита повышает температуру Ms выше комнатной температуры, так что при охлаждении образуется мартенсит. По этой причине рекомендуется несколько отпусков, так как этот вновь образованный мартенсит является хрупким и должен быть отпущен.
Более высокие количества легирующих добавок, таких как добавки хрома, повышают температуру, при которой аустенит разлагается или дестабилизируется, например, при сравнении стали с содержанием 1,25% Cr и стали с содержанием 5,0% Cr и 2,3% Mo [12][15]:
Однако даже в стали с 1,25% Cr все еще остается некоторое количество остаточного аустенита, когда сталь была отпущена при 400°F, поэтому отпуск не гарантирует преобразование всего остаточного аустенита, в зависимости от рассматриваемой стали, выбранного отпуска температура и т. д.
д.
Влияние легирующих добавок на прочность мартенсита
Различные легирующие элементы могут влиять на поведение стали при отпуске, например, как описано выше, с образованием карбида при вторичной закалке или сдвигом распада остаточного аустенита к более высоким температурам. Другой эффект возникает из-за «сопротивления отпуску», когда размягчение стали уменьшается при заданной температуре. Подводя итог эффектам, можно сказать, что добавки в сплав действуют через несколько основных механизмов:
- Подавляет образование и укрупнение переходных карбидов или цементита, чтобы углерод оставался в мартенсите
- Подавить восстановление мартенсита
- Упрочнение на твердый раствор
- Образование карбидов, ведущих к дисперсионному упрочнению
В результате некоторые стали могут быть отпущены при относительно высоких температурах с небольшой потерей прочности, как показано здесь [12]:
Класс 1 показывает потерю прочности при отпуске для типичной высокоуглеродистой стали, где стали класса 2-4 имеют различные легирующие элементы, которые приводят к различному поведению при отпуске.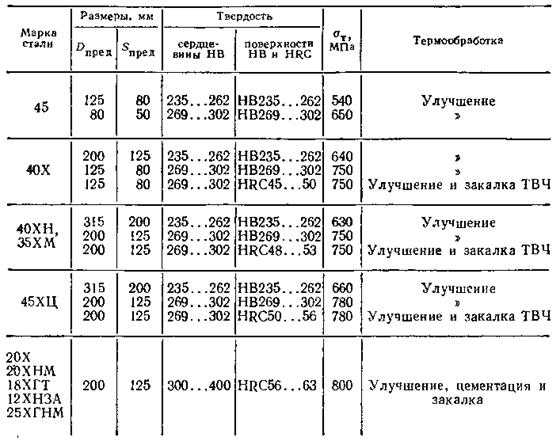 Класс 2 включает высоколегированные инструментальные стали, такие как D2, но без значительных добавок Mo, W или V для вторичной закалки. Класс 3 относится к быстрорежущим сталям со значительным вторичным упрочнением из-за добавок Mo и/или W. А класс 4 представляет собой среднеуглеродистую инструментальную сталь со значительными добавками Mo или W, которая изначально имеет более низкую твердость из-за более низкого содержания углерода, а также стойкость к отпуску и некоторую вторичную закалку.
Класс 2 включает высоколегированные инструментальные стали, такие как D2, но без значительных добавок Mo, W или V для вторичной закалки. Класс 3 относится к быстрорежущим сталям со значительным вторичным упрочнением из-за добавок Mo и/или W. А класс 4 представляет собой среднеуглеродистую инструментальную сталь со значительными добавками Mo или W, которая изначально имеет более низкую твердость из-за более низкого содержания углерода, а также стойкость к отпуску и некоторую вторичную закалку.
Общее влияние легирующих элементов на твердость после отпуска можно увидеть на этих двух рисунках с температурами отпуска 500°F или 1000°F [16]: дополнительную информацию см. в этой статье). При отпуске при температуре 500°F дисперсионное упрочнение не оказывает существенного влияния, поэтому большинство элементов вносят свой вклад в более высокую прочность мартенсита за счет упрочнения твердого раствора, подавления образования карбидов или восстановления мартенсита. Кремний способствует упрочнению твердого раствора и стойкости к отпуску. При 1000°F вклад вторичного упрочнения становится преобладающим, где V и Mo вносят очень сильный вклад в упрочнение мартенсита.
При 1000°F вклад вторичного упрочнения становится преобладающим, где V и Mo вносят очень сильный вклад в упрочнение мартенсита.
Подавление карбидообразования или укрупнение карбида происходит с добавками в сплав, такими как Mo, Cr или Mn, поскольку образуется более сложный цементитный карбид [16]. Другими словами, вместо цементита Fe 3 C имеется сложный карбид M 3 C, где M может относиться к Fe, Mo, Cr, Mn и т. д. Когда наряду с железом образуются другие легирующие элементы, тогда скорость диффузии этих элементов влияет на скорость отпуска, потому что все они диффундируют медленнее, чем малый межузельный углерод. Поэтому скорость образования карбидов (кинетика) замедляется за счет образования сложных карбидов. Это видно из расчетов JMatPro состава цементита с увеличением марганца, где углерод остается на уровне 25% атомного веса, но железо уменьшается и замещается марганцем:
Скорость восстановления мартенсита также частично контролируется влиянием этих легирующих элементов на образование и укрупнение карбидов [16]. Когда карбиды меньше и более равномерно распределены, карбиды «закрепляют» дислокации и малоугловые границы, поэтому они не могут двигаться так легко, и поэтому восстановление и рекристаллизация мартенсита подавляются.
Когда карбиды меньше и более равномерно распределены, карбиды «закрепляют» дислокации и малоугловые границы, поэтому они не могут двигаться так легко, и поэтому восстановление и рекристаллизация мартенсита подавляются.
Размер карбидов отпуска
Размер карбидов, образующихся во время отпуска, намного меньше, чем более крупные карбиды, которые мы наблюдаем в высокоуглеродистых сталях и инструментальных сталях. Инструментальные стали и нержавеющие стали с большим содержанием карбидов, такие как 154CM, часто имеют крупные «первичные» карбиды, которые образуются в расплаве, например, на следующей микрофотографии карбиды достигают размера 10–20 микрон:
В отличие от стали, такой как 13C26 или AEB-L, имеет намного меньше «вторичных» карбидов, которые образуются при более низких температурах по сравнению со 154CM, и этот факт в сочетании с меньшим общим количеством карбидов означает, что они больше порядка размером 1 микрон, как показано здесь:
Однако карбиды, которые образуются во время отпуска, намного меньше, чем даже эти маленькие карбиды. Микрофотографии ниже относятся к стали 440M [17], аналогичной стали AEB-L и 13C26, где вы можете видеть микроструктуру после закалки при большем увеличении с относительно крупными карбидами размером 1 микрон (а) после отпуска при 300 °C (б). ) и 500°С (в):
Микрофотографии ниже относятся к стали 440M [17], аналогичной стали AEB-L и 13C26, где вы можете видеть микроструктуру после закалки при большем увеличении с относительно крупными карбидами размером 1 микрон (а) после отпуска при 300 °C (б). ) и 500°С (в):
Карбиды после отпуска здесь относительно велики в пересчете на карбиды отпуска; при 300°C карбиды уже давно не вносят значительный вклад в дисперсионное упрочнение. Они, безусловно, намного больше, чем переходные карбиды размером 2-4 нм. Однако очевидно, что карбиды, образующиеся во время отпуска, все еще намного меньше, чем более крупные карбиды, образующиеся при более высоких температурах в высокоуглеродистых, инструментальных и нержавеющих сталях.
Температура в зависимости от времени
Поскольку отпуск является процессом, контролируемым диффузией, степень отпуска контролируется как температурой, так и временем. Чем выше температура, тем быстрее диффузия элементов и, следовательно, тем быстрее отпуск. Однако более низкие температуры при более длительном времени выдержки также могут привести к той же степени отпуска. Холломон и Джаффе исследовали этот путь еще в 1940-х годах [18] и обнаружили, что поведение выглядит следующим образом: Параметр Яффе, T — температура, t — время. C — константа, которая, как они обнаружили, меняется в зависимости от состава, и они определили, что она равна 19..5 для низкоуглеродистых сталей и 15 для высокоуглеродистых и инструментальных сталей. Следовательно, твердость в большей степени контролируется температурой, поскольку время находится в логарифмической шкале. Глядя на рисунок выше, достижение точки, обозначенной цифрой «16», занимает более 100 часов при 450°C и менее 15 минут при 550°C.
Однако более низкие температуры при более длительном времени выдержки также могут привести к той же степени отпуска. Холломон и Джаффе исследовали этот путь еще в 1940-х годах [18] и обнаружили, что поведение выглядит следующим образом: Параметр Яффе, T — температура, t — время. C — константа, которая, как они обнаружили, меняется в зависимости от состава, и они определили, что она равна 19..5 для низкоуглеродистых сталей и 15 для высокоуглеродистых и инструментальных сталей. Следовательно, твердость в большей степени контролируется температурой, поскольку время находится в логарифмической шкале. Глядя на рисунок выше, достижение точки, обозначенной цифрой «16», занимает более 100 часов при 450°C и менее 15 минут при 550°C.
Резюме
Хорошо, эта статья оказалась даже длиннее, чем я ожидал. Многое происходит во время закалки. Сначала мы начали с пересыщенного углеродом мартенсита, и сталь «хочет» достичь равновесного состояния феррит плюс карбиды, но этот процесс ограничивается диффузией. Когда сталь нагревается до достаточно высоких температур, углерод выделяется из мартенсита в виде карбидов, а мартенсит восстанавливается и рекристаллизуется, уменьшая свою тетрагональность и плотность дислокаций. Карбиды также могут способствовать повышению твердости за счет дисперсионного упрочнения. Изменения остаточного аустенита также происходят из-за того, что он разлагается до бейнита или дестабилизируется и превращается в мартенсит. Температура более важна, чем время при отпуске, поскольку время находится в логарифмической шкале, где при более низкой температуре требуется гораздо больше времени для достижения того же уровня твердости.
Когда сталь нагревается до достаточно высоких температур, углерод выделяется из мартенсита в виде карбидов, а мартенсит восстанавливается и рекристаллизуется, уменьшая свою тетрагональность и плотность дислокаций. Карбиды также могут способствовать повышению твердости за счет дисперсионного упрочнения. Изменения остаточного аустенита также происходят из-за того, что он разлагается до бейнита или дестабилизируется и превращается в мартенсит. Температура более важна, чем время при отпуске, поскольку время находится в логарифмической шкале, где при более низкой температуре требуется гораздо больше времени для достижения того же уровня твердости.
Будущие статьи
Я очень мало рассказал о влиянии отпуска на ударную вязкость; это будет в будущих статьях о закалке. Есть также некоторые практические аспекты отпуска, которые я не упомянул, такие как рекомендация некоторых закаливать после отпуска. После предыстории, изложенной в этой статье, я могу теперь коснуться некоторых других концепций, таких как образование бейнита, поскольку этот процесс имеет сходство с отпуском, и поэтому у нас есть основа для описания бейнита. Я мог бы написать статью о влиянии кремния на ударную вязкость, поскольку он в первую очередь влияет на ударную вязкость за счет своего воздействия на отпуск. Также есть статьи о криообработке стали, в которых утверждается, что крио способствует образованию эта-переходных карбидов для повышения износостойкости. Поэтому я могу писать статьи об этом аспекте криообработки, поскольку я могу ссылаться на эту статью для всех, кому необходимо понять, о каком типе карбидов говорится в этих статьях.
Я мог бы написать статью о влиянии кремния на ударную вязкость, поскольку он в первую очередь влияет на ударную вязкость за счет своего воздействия на отпуск. Также есть статьи о криообработке стали, в которых утверждается, что крио способствует образованию эта-переходных карбидов для повышения износостойкости. Поэтому я могу писать статьи об этом аспекте криообработки, поскольку я могу ссылаться на эту статью для всех, кому необходимо понять, о каком типе карбидов говорится в этих статьях.
[1] https://www.crucible.com/eselector/prodbyapp/tooldie/champloy.html
[2] https://www.alphaknifesupply.com/Pictures/Info/Steel/14- 4-DS.pdf
[3] Краусс, Джордж. Стали: обработка, структура и характеристики . Asm International, 2015.
[4] http://www.phase-trans.msm.cam.ac.uk/2004/Tempered.Martensite/tempered.martensite.html
[5] https://en. wikipedia.org/wiki/Укрепление_механизмов_материалов#/media/File:Particle_strengthening.svg
[6] Сян, Янсюнь, Минси Дэн и Фу-Чжэнь Сюань. «Характеристика повреждений при ползучести с использованием метода нелинейных ультразвуковых волноводов: мезомасштабная модель». Журнал прикладной физики 115, вып. 4 (2014): 044914.
«Характеристика повреждений при ползучести с использованием метода нелинейных ультразвуковых волноводов: мезомасштабная модель». Журнал прикладной физики 115, вып. 4 (2014): 044914.
[7] https://www.youtube.com/watch?v=BV1cxwxnhPs
[8] Гроте, Карл-Хайнрих и Эрик К. Антонссон, ред. Справочник Springer по машиностроению . Том. 10. Springer Science & Business Media, 2009 г.
[9] http://www.totalmateria.com/articles/Art12.htm
[10] Кэрон Р. Н. и Г. Краусс. «Отпуск реечного мартенсита Fe-C». Металлургические операции 3, вып. 9 (1972): 2381-2389.
[11] https://www.asminternational.org/web/hts/news/newswire/-/journal_content/56/10192/26120368/NEWS
[12] Roberts, GA, and Robert A. Cary. Инструментальная сталь . Бичвуд, Огайо: Американское общество металлов, 1980.
[13] https://www.bladeforums.com/threads/liquid-nitrogen-vs-dry-ice.1540810/
[14] Balliett, Thomas A. и Джордж Краусс. «Влияние первой и второй стадий отпуска на образование микротрещин в мартенсите сплава Fe-1,22 С».



 Сколько теплоты выделится при полном остывании воды на 40 °С? Плотность воды 1000 кг/м3
Сколько теплоты выделится при полном остывании воды на 40 °С? Плотность воды 1000 кг/м3