Спирт из древесины — Жизненные формы растений
А. А. Цветков
Вероятно, не один школьник, отвечая урок по химии, называл спирт из древесины древесным спиртом. Кто же, в самом деле, не скажет, что если спирт получен из древесины, значит это и есть древесный спирт?
Оказывается, однако, что спирт из древесины и древесный спирт — это два разных вещества.
Давно уже из дерева, путём сухой перегонки, наряду с другими веществами получают метиловый спирт СН3ОН. По способу получения ему дано было ещё название древесного спирта. И хотя этот спирт сейчас в промышленности получают преимущественно другим способом — синтезом из окиси углерода и водорода
СО + 2Н3 → СН3ОН
Его и теперь нередко называют древесным спиртом.
Но что же тогда подразумевают под «спиртом из древесины»? Здесь речь идёт о ближайшем гомологе метилового спирта-винном или этиловом спирте С2Н3ОН. И получают этот спирт не сухой перегонкой, а посредством совершенно других химических процессов — гидролиза древесины, т.
Что метиловый и этиловый спирты — два разных вещества, это можно видеть и по их составу (разное число атомов углерода и водорода в молекулах), и по разным температурам кипения и затвердевания, и по ряду других свойств. Но, пожалуй, самое разительное различие состоит в их физиологическом действии: метиловый спирт сильно ядовит и, будучи принят внутрь организма даже в небольших количествах, вызывает смертельный исход или потерю зрения.
Чтобы не путать названия веществ и точно знать, о каком спирте идёт речь, спирт из древесины (этиловый спирт) чаще называют гидролизным спиртом.
О производстве гидролизного спирта мы и хотим здесь рассказать.
Ещё в 1811 г. русский химик К. С. Кирхгоф установил, что крахмал при нагревании с раствором серной кислоты подвергается гидролизу, превращаясь в патоку или в глюкозу. Вскоре на использовании этой реакции возникла целая отрасль пищевой промышленности — крахмала-паточное производство’.
Клетчатка, или целлюлоза, имеет тот же состав, что и крахмал — (С6Н10О5). Естественно возникает вопрос: не обладает ли и она свойством подвергаться гидролизу?
Вскоре после открытия гидролиза крахмала почти одновременно русский химик Н. Фогель и французский учёный Г. Браконно сумели осуществить гидролиз клетчатки, нагревая её с раствором кислоты. Но лишь через много десятилетий, только в самые последние годы XIX в. появились первые полупромышленные установки по гидролизу древесины в Германии и в России. Впервые в мире крупное развитие гидролизная промышленность получила в нашей стране в годы пятилеток.
Техническое осуществление гидролиза древесины было сопряжено с большими трудностями.
Однако всё возраставший спрос на этиловый спирт, особенно со стороны промышленности синтетического каучука, и необходимость сбережения пищевых ресурсов требовали освоения новых источников сырья. Это сырьё в громадных количествах накапливалось на деревообрабатывающих заводах в виде отходов древесины — опилок, стружек, щепы и т. д., требовавших рационального использования их в целях экономии производства.
Это сырьё в громадных количествах накапливалось на деревообрабатывающих заводах в виде отходов древесины — опилок, стружек, щепы и т. д., требовавших рационального использования их в целях экономии производства.
Подобно тому, как бензин из бесполезного когда-то отхода нефтепереработки превратился в продукт первой необходимости или каменноугольная смола из неприятного отброса стала ценнейшим источником ароматических соединений, отходы лесопиления, загромождавшие заводы и часто сжигавшиеся без нужды, стали использоваться для химической переработки.
Открылись более широкие возможности и для использования минеральных кислот в гидролизном производстве, так как мощного развития достигла основная химическая промышленность. Гидролизный спирт стал более дешёвым, чем спирт из зерна и картофеля.
Как велико значение гидролизного производства в сбережении пищевых ресурсов, можно видеть из следующего. Производство миллиона литров спирта путём гидролиза древесины высвобождает 3 тыс.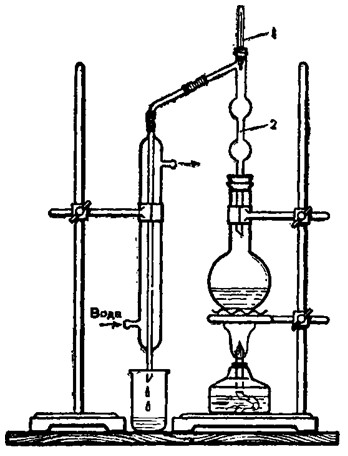 т хлеба или 10 тыс. т картофеля.
т хлеба или 10 тыс. т картофеля.
Для такой замены потребуется лишь 10 тыс. т опилок, что легко может дать за год работы один лесопильный завод. Иными словами, тонна опилок при производстве спирта заменяет тонну картофеля
Экономическое значение гидролизного производства
Особенно важно отметить получение кормовых дрожжей, богатых белками и представляющих огромную ценность для животноводства. Кормовых дрожжей может быть получено примерно до 200 т при производстве каждого миллиона литров спирта.
Проследим теперь, как же получают на гидролизном заводе спирт из древесины.
Весь производственный процесс слагается из трёх основных стадий:
а) гидролиз клетчатки (целлюлозы) до глюкозы, выражаемый, как известно, уравнением:
(С6H12О5)n + пН2О → nС6H12O6
б) сбраживание глюкозы в спирт в присутствии дрожжей:
С6Н12О6 — 2С2Н5ОН + 2СО2
в) выделение спирта из продуктов брожения.
Установлено, что первую стадию — гидролиз клетчатки – можно осуществлять достаточно быстро и полно, если для реакции применить в качестве катализатора разбавленную серную кислоту, а также нагревание до 180 — 185 ° и давление 10 — 12 атм. (Гидролиз может быть осуществлен и при других условиях. На некоторых заводах его ведут, например, в присутствии концентрированной соляной кислоты при,обычной температуре.)
Чтобы провести реакцию при таких «жёстких» условиях, применяют автоклав из толстой листовой стали, рассчитанный на повышенное давление’и выложенный внутри слоем бетона и керамическими плитками для защиты от кислоты. По типу реакции, осуществляемой в автоклаве, он называется ещё гидролизёром.
Гидролизёр по виду представляет собой высокий цилиндр с конической частью вверху и внизу. Емкость его до 50 м3. Через верхнюю горловину в гидролизёр загружаются при помощи транспортёра щепа и опилки. После загрузки горловина герметически закрывается крышкой.
Нагревание смеси до нужной температуры осуществляется перегретым паром, поступающим по трубопроводу снизу. Спуск избыточного давления из аппарата производится через особое отверстие в верхней горловине. Процесс «варки» одной загрузки в автоклаве длится несколько часов.
Образующийся при гидролизе раствор, с содержанием 3 — 4% сахара, называемый гидролизатом, выводится из аппарата снизу по трубопроводу.
Рис. 1. Гидролизёр.
Остаток неразложпвшейся массы — технического лигнина по окончании процесса «выстреливается» из аппарата под давлением 7 — 8 атм через нижнюю горловину, закрываемую задвижкой. После сушки лигнин может быть использован в производстве пластмасс, пористого кирпича (в смеси с глиной), сухой штукатурки, в качестве наполнителя при производстве резины или в виде топлива.
Интересно устроено в гидролизёре приспособление для фильтрования отводимого раствора. Так как в аппарат загружается измельчённая древесная масса, то она, не будучи задерживаемой, конечно, легко уносилась бы вместе с раствором и быстро засоряла бы жидкостные коммуникации. Приспособить в автоклаве какой-либо фильтр, который должен работать в условиях повышенного давления и действия горячей кислоты, дело нелёгкое. Проблема была разрешена следующим образом. В гидролизёре по нижней конусной его части проложены наклонные трубки с отверстиями, прикрытые снаружи чешуйками. Чешуйки, обращённые вниз, не дают возможности древесной массе (опилкам) попадать в отверстия, гидролизат же свободно проходит в них. Проникшая в трубки жидкость стекает по ним в общий кольцевой канал, из которого и выводится по трубопроводу наружу.
Общая схема гидролизного производства, в основных его частях, представлена на рис. 2
Рис. 2. Схема гидролизного производства
Из гидролизёра 1 лигнин поступает в циклон 2, а гидролизат — в испаритель 3. Назначение испарителя — выделить из раствора сахара летучие побочные продукты гидролиза. Так как давление в испарителе меньше, чем в автоклаве, гидролизат вскипает, и из него улетучиваются скипидар, метиловый спирт и другие вещества, которые затем улавливаются.
Назначение испарителя — выделить из раствора сахара летучие побочные продукты гидролиза. Так как давление в испарителе меньше, чем в автоклаве, гидролизат вскипает, и из него улетучиваются скипидар, метиловый спирт и другие вещества, которые затем улавливаются.
Следующей стадией производства должно быть получение спирта из сахара (глюкозы). Однако гидролизат даже после выделения из него летучих продуктов ещё нельзя пустить на сбраживание, так как в нём содержится много кислоты.
Поэтому, далее, он поступает в нейтрализатор 4, куда из мерника 5 подаётся известковое молоко. В результате взаимодействия серной кислоты с гидратом окиси кальция раствор становится нейтральным.
Н2SO4 + Са (ОН)2 = СаSO4 + 2Н2О
Для отвода выделяющихся при экзотермической реакции паров нейтрализатор имеет вытяжную трубу. Чтобы реакция нейтрализации шла быстрее и полнее использовался гидрат окиси кальция, в нейтрализатора вращается мешалка.
После нейтрализации возникает необходимость отделить гидролизат от осадка сернокислого кальция. Для этого он подается в отстойник 6, где выпадает основная часть соли, и, далее, после дополнительного охлаждения в градирне (на рисунке не показана) и в теплообменнике 7, — на фильтрпресс 8 для окончательной очистки.
После фильтрования раствор сахара подаётся в бродильный чан 9 ёмкостью 100 — 200 м3. Из сепаратора 10 сюда же поступает «дрожжевое молоко». Для нормальной жизнедеятельности дрожжей нужна температура 30°, поэтому раствор и подвергался ранее охлаждению. Процесс брожения сахара под действием фермента, вырабатываемого дрожжами, длится около 5 часов.
При больших масштабах производства реакция брожения одновременно является источником получения значительных количеств углекислого газа, из которого готовят «сухой лёд», широко применяющийся в качестве холодильного средства.
Раствор после брожения — бражка — с содержанием около 1,5% спирта поступает в сепаратор, где отделяется от дрожжей. Дрожжи снова идут на приготовление «дрожжевого молока» и вновь загружаются в бродильный чан (осуществляется циркуляционный процесс). Раствор же спирта после сепаратора собирается в сборник 11, откуда идёт на дальнейшую переработку-отделение его от примесей.
Дрожжи снова идут на приготовление «дрожжевого молока» и вновь загружаются в бродильный чан (осуществляется циркуляционный процесс). Раствор же спирта после сепаратора собирается в сборник 11, откуда идёт на дальнейшую переработку-отделение его от примесей.
Рис.3. Верхняя часть гидролизёра
Третья стадия производства — выделение спирта из бражки и очистка его — осуществляется в колонных аппаратах (на рисунке не показаны), напоминающих по устройству и действию ректификационные колонны нефтеперегонных заводов.
Сначала нагретая бражка поступает на верхние тарелки бражной колонны. Из бражки здесь испаряются спирт и другие летучие вещества, смесь их паров поступает далее в спиртовую колонну. В нижней части бражной колонны собирается барда, не содержащая спирта, но содержащая некоторое количество не пробродившего сахара, вследствие чего её используют как питательную среду для выращивания кормовых дрожжей, используемых в животноводстве.
В спиртовой колонне, благодаря многократно повторяющимся на тарелках процессам испарения и конденсации, спирт отделяется от таких примесей, как сивушные масла, альдегиды, эфиры.
Чтобы очистить этиловый спирт от наиболее трудно отделимой примеси — метилового спирта, — производят ещё дополнительную ректификационную перегонку.
Нетрудно заметить выше, что при общей непрерывности технологического процесса основной аппарат гидролизного производства (гидролизёр) — это аппарат периодического действия. Непрерывность всего производственного процесса достигается за счёт того, что на заводе работает несколько гидролизёров, в которых процесс гидролиза (а также загрузки и выгрузки) производится в разное время, так что всегда есть гидролизат для последующей переработки.
Таким образом, мы видим, что гидролизное получение спирта из древесины — большой и сложный процесс.
Источник: «Книга для чтения по химии, ч.2». Изд-во министерства просвещения РСФСР, 1956. , стр. 426-435
, стр. 426-435
Необычная обложка фантастического романа
Какой представляют читатели обложку фантастического романа? Космической с мириадами звёзд? Да, но это столь избитый приём, что он кажется уже скучным. Загадочной с мордами неизвестных существ? Да, но морды тоже не в новинку, а действительно оригинальных и при этом не вычурных существ в фантастике давно не встречалось. Волшебной с абстрактными образами? Да, но в романе Татьяны Латуковой «Небо в алмазах» нет волшебных сюжетов, это космическая опера в рамках логичной физики, без нарушений второго закона термодинамики.
Розетки на обложке
Стальная мебель
Огромные города и протяжённые трассы дорог через всю страну рождают спрос на ту сферу производства и услуг, что всегда была востребованной, однако её новые масштабы потребовали и новых стандартов качества, и новой культуры производства. Речь об общественном питании. Гигиеническая безопасность — первое и важнейшее условие работы любого продуктового цеха, любой кондитерской фабрики и пиццерии. Де-факто стандартом качества стали столешницы из шлифованной нержавеющей стали, обеспечивающие максимальную биобезопасность…
Де-факто стандартом качества стали столешницы из шлифованной нержавеющей стали, обеспечивающие максимальную биобезопасность…
Нейтральное оборудование из нержавеющей стали
Спирт из опилок рецепт. Спирт из древесины (гидролизный спирт)
Производство спирта из картофеля, зерна, мелассы, сахарной свеклы требует расхода больших количеств этих ценных видов сырья. Замена такого сырья более дешевым является одним из источников экономии пищевых продуктов и снижения себестоимости спирта. Поэтому в последнее время значительно увеличилось производство технического этилового спирта из непищевого сырья: древесины, сульфитных щелоков и синтетическим путем из этиленсодержащих газов.
Производство спирта из древесины
Гидролизная промышленность выпускает из растительных отходов, содержащих целлюлозу, в частности из древесных отходов, ряд продуктов: этиловый спирт, кормовые дрожжи, глюкозу и др.
На гидролизных заводах целлюлозу гидролизуют минеральными кислотами до глюкозы, которая используется для сбраживания в спирт, выращивания дрожжей и выпуска в кристаллическом виде. Существуют гидролизные заводы различного профиля: гидролизно-спиртовые, гидролизно-дрожжевые, гидролизно-глюкозные. Гидролизная промышленность имеет большое народнохозяйственное значение; оно обусловлено тем, что из малоценных растительных отходов получают ценные продукты. В частности, из 1 т абсолютно сухой хвойной древесины получают 170-200 л этилового спирта, для выработки которого потребовалось бы 0,7 т зерна или 2 т картофеля.
Существуют гидролизные заводы различного профиля: гидролизно-спиртовые, гидролизно-дрожжевые, гидролизно-глюкозные. Гидролизная промышленность имеет большое народнохозяйственное значение; оно обусловлено тем, что из малоценных растительных отходов получают ценные продукты. В частности, из 1 т абсолютно сухой хвойной древесины получают 170-200 л этилового спирта, для выработки которого потребовалось бы 0,7 т зерна или 2 т картофеля.
Гидролизная промышленность комплексно перерабатывает древесину, в результате чего на гидролизно-спиртовых заводах получают, кроме этилового спирта, и другие ценные продукты: фурфурол, лигнин, жидкую углекислоту, кормовые дрожжи.
Сырье гидролизного производства
Сырьем гидролизного производства служит древесина в виде различных отходов лесной и деревообрабатывающей промышленности: опилки, щепа, стружка и др. Влажность древесины колеблется от 40 до 60%. Опилки, перерабатываемые гидролизными заводами, обычно имеют влажность 40- 48%. В состав сухих веществ древесины входят целлюлоза, гемицеллюлозы, лигнин и органические кислоты.
Гемицеллюлозы древесины состоят из гексозанов: маннана, галактане и пентозанов: ксилана, арабана и их метилированных производных. Лигнин представляет собой сложное вещество ароматического ряда, химический состав и строение его еще не установлены.
Химический состав абсолютно сухой древесины приведен в таблице 1.
Кроме древесины, в качестве сырья для гидролизной промышленности применяются и растительные отходы сельского хозяйства: подсолнечная лузга, кукурузная кочерыжка, хлопковая шелуха, солома зерновых злаков.
Химический состав растительных отходов сельского хозяйства представлен в таблице 2.
Технологическая схема комплексной переработки древесины
Технологическая схема комплексной переработки древесины состоит из следующих стадий: гидролиз древесины, нейтрализация и очистка гидролизата; сбраживание гидролизного сусла, перегонка гидролизной бражки.
Измельченную древесину подвергают гидролизу разбавленной серной кислотой при нагревании под давлением. При гидролизе гемицеллюлозы и целлюлоза разлагаются. Гемицеллюлозы превращаются в гексозы: глюкозу, галактозу, маннозу и пентозы: ксилозу и арабинозу; целлюлоза — в глюкозу. Лигнин при гидролизе остается в виде нерастворимого остатка.
При гидролизе гемицеллюлозы и целлюлоза разлагаются. Гемицеллюлозы превращаются в гексозы: глюкозу, галактозу, маннозу и пентозы: ксилозу и арабинозу; целлюлоза — в глюкозу. Лигнин при гидролизе остается в виде нерастворимого остатка.
Гидролиз древесины осуществляют в гидролизном аппарате — стальном цилиндрическом сосуде. В результате гидролиза получают гидролизат, содержащий около 2-3% сбраживаемых моносахаридов и нерастворимый остаток-лигнин. Последний можно использовать непосредственно в производстве строительных плит, в кирпичном производстве, при помоле цемента, в качестве топлива; после соответствующей обработки лигнин может применяться в производстве пластмасс, резиновой промышленности и др.
Полученный гидролизат направляют в испаритель, где пар отделяется от жидкости. Выделяющийся пар конденсируют и используют для выделения из него фурфурола, скипидара и метилового спирта. Затем гидролизат охлаждают до 75-80°С, нейтрализуют в нейтрализаторе известковым молоком до pH 4-4,3 и добавляют питательные соли для дрожжей (сернокислый аммоний, суперфосфат). Полученный нейтрализат отстаивают для освобождения от выпавшего осадка сернокислого кальция и других взвешенных частиц. Осевший осадок сернокислого кальция отделяют, сушат, обжигают и получают алебастр, используемый в строительной технике. Нейтрализат охлаждают до 30-32°С и направляют на брожение. Подготовленный таким образом к брожению гидролизат называется суслом. Брожение гидролизного сусла производят непрерывным способом в бродильных чанах. При этом дрожжи непрерывно циркулируют в системе; дрожжи отделяют от бражки на сепараторах. Выделяющийся при брожении углекислый газ используют для выпуска жидкой или твердой углекислоты. Зрелую бражку, содержащую 1,0-1,5% спирта, направляют для перегонки и ректификации на брагоректификационный аппарат и получают этиловый спирт, метиловый спирт и сивушное масло. Барда, полученная после перегонки, содержит пентозы и ее используют для выращивания кормовых дрожжей.
Полученный нейтрализат отстаивают для освобождения от выпавшего осадка сернокислого кальция и других взвешенных частиц. Осевший осадок сернокислого кальция отделяют, сушат, обжигают и получают алебастр, используемый в строительной технике. Нейтрализат охлаждают до 30-32°С и направляют на брожение. Подготовленный таким образом к брожению гидролизат называется суслом. Брожение гидролизного сусла производят непрерывным способом в бродильных чанах. При этом дрожжи непрерывно циркулируют в системе; дрожжи отделяют от бражки на сепараторах. Выделяющийся при брожении углекислый газ используют для выпуска жидкой или твердой углекислоты. Зрелую бражку, содержащую 1,0-1,5% спирта, направляют для перегонки и ректификации на брагоректификационный аппарат и получают этиловый спирт, метиловый спирт и сивушное масло. Барда, полученная после перегонки, содержит пентозы и ее используют для выращивания кормовых дрожжей.
При переработке по указанной схеме из 1 т абсолютно сухой хвойной древесины можно получить следующие количества товарных продуктов:
- Спирта этилового, л ………………….
 . 187
. 187 - Жидкой углекислоты, кг …………….. 70
- или твердой углекислоты, кг ……… 40
- Дрожжей кормовых, кг…………….. .. 40
- Фурфурола, кг …………………………….9,4
- Скипидара, кг ……………………………0,8
- Термоизоляционных и строительных лигно-плит, м 2 …. 75
- Алебастра строительного, кг ……..225
- Сивушного масла, к г ………………..0,3
Производство спирта из сульфитных щелоков
При производстве целлюлозы из древесины по сульфитному способу в качестве отхода получают сульфитный щелок — коричневую жидкость с запахом сернистого газа. Химический состав сульфитного щелока (%): вода — 90, сухие вещества — 10, в том числе производные лигнина — лигносульфонаты — 6, гексозы — 2, пентозы -1 , летучие кислоты, фурфурол и другие вещества — около 1. Длительное время сульфитные щелока спускали в реки, они загрязняли воду и уничтожали рыбу в водоемах. В настоящее время у нас имеется ряд заводов по комплексной переработке сульфитного щелока на этиловый спирт, кормовые дрожжи и сульфитно-бардяные концентраты. Производство спирта из сульфитных щелоков состоит из следующих стадий: подготовка сульфитного щелока к брожению, сбраживание сульфитнощелокового сусла, перегонка зрелой сульфитной бражки.
Производство спирта из сульфитных щелоков состоит из следующих стадий: подготовка сульфитного щелока к брожению, сбраживание сульфитнощелокового сусла, перегонка зрелой сульфитной бражки.
Подготовку сульфитного щелока к сбраживанию осуществляют по непрерывной схеме. Щелок продувают воздухом для удаления летучих кислот и фурфурола, задерживающих процесс брожения. Продутый щелок нейтрализуют известковым молоком и затем выдерживают для укрупнения выпавших кристаллов сернокислого и сернистокислого кальция; при этом добавляют питательные соли для дрожжей (сернокислый аммоний и суперфосфат). Затем щелок отстаивают. Осевший осадок- шлам — спускают в канализацию, а осветленный щелок охлаждают до 30-32°С. Подготовленный таким образом щелок называется суслом. Сусло направляют в бродильное отделение и сбраживают так же, как гидролизаты древесины, или применяют метод с подвижной насадкой. Подвижной насадкой называются волокна целлюлозы, остающиеся в щелоке. Метод брожения с подвижной насадкой основан на свойстве некоторых рас дрожжей сорбироваться на поверхности целлюлозных волокон и образовывать хлопья волокнисто-дрожжевой массы, которая в зрелой бражке быстро и полно оседает на дно чана. Брожение проводят в бродильной батарее, которая состоит из головного и хвостового чанов. В бродящем сусле волокна целлюлозы с сорбированными дрожжами находятся в непрерывном движении под влиянием выделяющегося углекислого газа. Отбродившая бражка поступает из головного чана в хвостовой, где заканчивается процесс брожения, и волокна с дрожжами оседают на дно. Осевшую дрожжеволокнистую массу насосом возвращают в головной чан, куда одновременно подают сусло, а зрелую бражку, содержащую 0,5-1% спирта, направляют в брагоректификационный аппарат и получают этиловый спирт, метиловый спирт и сивушное масло. Полученная после перегонки барда содержит пентозы и служит питательной средой для выращивания кормовых дрожжей, которые затем отделяют, высушивают и выпускают в виде сухих дрожжей. Барду после отделения дрожжей, содержащую лигносульфонаты, упаривают до содержания сухих веществ 50-80%. Полученный продукт называется сульфитно-бардяным концентратом и применяется в производстве пластических масс, строительных материалов, синтетических дубителей для получения кожи, в литейном производстве и дорожном строительстве.
Брожение проводят в бродильной батарее, которая состоит из головного и хвостового чанов. В бродящем сусле волокна целлюлозы с сорбированными дрожжами находятся в непрерывном движении под влиянием выделяющегося углекислого газа. Отбродившая бражка поступает из головного чана в хвостовой, где заканчивается процесс брожения, и волокна с дрожжами оседают на дно. Осевшую дрожжеволокнистую массу насосом возвращают в головной чан, куда одновременно подают сусло, а зрелую бражку, содержащую 0,5-1% спирта, направляют в брагоректификационный аппарат и получают этиловый спирт, метиловый спирт и сивушное масло. Полученная после перегонки барда содержит пентозы и служит питательной средой для выращивания кормовых дрожжей, которые затем отделяют, высушивают и выпускают в виде сухих дрожжей. Барду после отделения дрожжей, содержащую лигносульфонаты, упаривают до содержания сухих веществ 50-80%. Полученный продукт называется сульфитно-бардяным концентратом и применяется в производстве пластических масс, строительных материалов, синтетических дубителей для получения кожи, в литейном производстве и дорожном строительстве.
Из сульфитно-бардяных концентратов можно получить ценное ароматическое вещество — ванилин.
Технологическая схема комплексной переработки сульфитных щелоков на этиловый спирт, кормовые дрожжи и сульфитно-бардяные концентраты показана на рисунке 2.
При переработке сульфитных щелоков получают в пересчете на 1т еловой древесины:
- Спирта этилового, л ……………….. 30-50
- Спирта метилового, л …………………… 1
- Жидкой углекислоты, л ………….. 19-25
- Сухих кормовых дрожжей, кг …. 15
- Сульфитно-бардяных концентратов влажностью 20%, кг …. 475
Производство спирта синтетическим методом
Сырьем для производства синтетического этилового спирта служат газы нефтеперерабатывающих заводов, которые содержат этилен. Кроме того, можно использовать и другие этиленсодержащие газы: коксовый газ, получаемый при коксовании угля, и попутные нефтяные газы.
В настоящее время синтетический этиловый спирт получают двумя способами: сернокислотной гидратацией и прямой гидратацией этилена.
Сернокислая гидратация этилена
Производство этилового спирта этим способом состоит из следующих процессов: взаимодействия этилена с серной кислотой, при котором образуются этилсерная кислота и диэтилсульфат; гидролиз полученных продуктов с образованием спирта; отделение спирта от серной кислоты и очистка его.
Сырьем для сернокислой гидратации служат газы, содержащие 47-50% вес. этилена, а также газы с меньшим содержанием этилена. Процесс осуществляется по схеме, приведенной ниже.
Этилен взаимодействует с серной кислотой в реакционной колонне, представляющей собой вертикальный цилиндр. Внутри колонны находятся колпачковые тарелки с переливными стаканами. В нижнюю часть колонны компрессором подают этиленосодержащий газ, сверху в колонну подводят для орошения 97-98%-ная серная кислота. Газ, поднимаясь вверх, на каждой тарелке барботирует через слой жидкости. Этилен с серной кислотой взаимодействует по реакциям:
Из реакционной колонны непрерывно вытекает смесь этилсерной кислоты, диэтилсульфата и непрореагировавшей серной кислоты. Эту смесь охлаждают в холодильнике до 50°С и направляют на гидролиз, при котором протекают такие реакции:
Эту смесь охлаждают в холодильнике до 50°С и направляют на гидролиз, при котором протекают такие реакции:
Моноэтилсульфат, полученный в результате второй реакции, подвергают дальнейшему разложению с образованием еще одной молекулы спирта.
Прямая гидратация этилена
Технологическая схема производства этилового спирта способом прямой гидратации этилена представлена ниже.
Сырьем для способа прямой гидратации служит газ с высоким содержанием этилена (94-96%). Этилен сжимают компрессором до 8-9 КПа. Сжатый этилен смешивают с водяным паром в определённых соотношениях. Взаимодействие этилена с водяным паром производят в контактном аппарате — гидрататоре, представляющим собой вертикальную стальную полую цилиндрическую колонну, в которой находится катализатор (фосфорная кислота, нанесенная на алюмосиликат).
Смесь этилена и водяного пара при 280-300°С под давлением около 8,0 КПа подают в гидрататор, в котором поддерживают такие же параметры. При взаимодействии этилена с водяным паром, кроме основной реакции образования этилового спирта, протекают побочные реакции, в результате которых получаются диэтиловый эфир, уксусный альдегид и продукты полимеризации этилена. Продукты синтеза уносят из гидрататора небольшое количество фосфорной кислоты, которая может в дальнейшем оказывать коррозийное действие на аппаратуру и трубопроводы. Чтобы избежать этого, кислоту, содержащуюся в продуктах синтеза, нейтрализуют щелочью. Продукты синтеза после нейтрализации пропускают через солеотделитель, а затем охлаждают в теплообменнике и производят конденсацию водно-спиртовых паров. Получают смесь водно-спиртовой жидкости и непрореагировавшего этилена. Непрореагировавший этилен отделяют от жидкости в сепараторе. Он представляет собой вертикальный цилиндр, в котором установлены перегородки, резко изменяющие скорость и направление газового потока. Этилен из сепаратора отводят во всасывающую линию циркуляционного компрессора и направляют на смешение со свежим этиленом. Водно-спиртовой раствор, вытекающий из сепаратора, содержит 18,5-19% об. спирта. Его концентрируют в отпарной колонне и в виде паров направляют для очистки в ректификационную колонну. Спирт получают крепостью 90,5% об.
Продукты синтеза уносят из гидрататора небольшое количество фосфорной кислоты, которая может в дальнейшем оказывать коррозийное действие на аппаратуру и трубопроводы. Чтобы избежать этого, кислоту, содержащуюся в продуктах синтеза, нейтрализуют щелочью. Продукты синтеза после нейтрализации пропускают через солеотделитель, а затем охлаждают в теплообменнике и производят конденсацию водно-спиртовых паров. Получают смесь водно-спиртовой жидкости и непрореагировавшего этилена. Непрореагировавший этилен отделяют от жидкости в сепараторе. Он представляет собой вертикальный цилиндр, в котором установлены перегородки, резко изменяющие скорость и направление газового потока. Этилен из сепаратора отводят во всасывающую линию циркуляционного компрессора и направляют на смешение со свежим этиленом. Водно-спиртовой раствор, вытекающий из сепаратора, содержит 18,5-19% об. спирта. Его концентрируют в отпарной колонне и в виде паров направляют для очистки в ректификационную колонну. Спирт получают крепостью 90,5% об.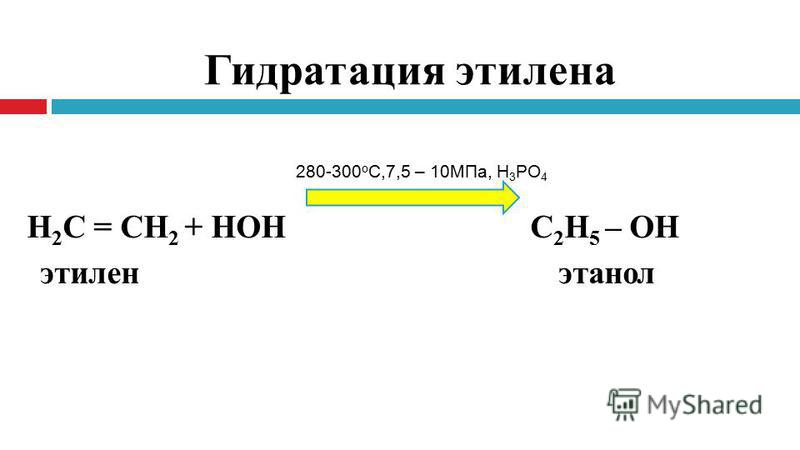 На заводах синтетического спирта применяется способ прямой гидратации этилена.
На заводах синтетического спирта применяется способ прямой гидратации этилена.
Производство синтетического спирта, независимо от способа его получения, значительно более эффективно, чем производство спирта из пищевого сырья. Для получения 1 т этилового спирта из картофеля или зерна необходимо затратить 160-200 чел -дней, из газов нефтепереработки только 10 чел -дней. Себестоимость синтетического спирта примерно в четыре раза меньше себестоимости спирта из пищевого сырья.
Статьи Рисунки Таблицы О сайте English
Ранее метанол получали при сухой перегонке дерева (отсюда его название древесный спирт). Он применяется как растворитель и для различных органических синтезов — получение формальдегида, некоторых красителей, фотореактивов, фармацевтических препаратов.
В гидролизном спирте, полученном из древесных опилок, может быть примесь метилового спирта. Эта примесь недопустима, так как метиловый спирт очень ядовит и в определенной концентрации может привести к тяжелому отравлению и слепоте. В качестве примеси в спирте могут быть дубильные вещества, если спирт хранился в дубовых бочках.
В качестве примеси в спирте могут быть дубильные вещества, если спирт хранился в дубовых бочках.
Метиловый спирт (метанол) в течение длительного времени получали из водного дистиллата, выделяющегося при сухой перегонке древесины (отсюда и название — древесный спирт). Выход спирта при этом зависит от породы древесины и колеблется в пределах от 3 до 6 кг на каждый кубометр сухой древесины. В 1933 г. в СССР была пущена первая установка по получению метилового спирта из синтез-газа, и в настоящее время более 90% его получают таким образом. Метиловый спирт является важным видом сырья для получения формальдегида, диметил-сульфата, антидетонационных смесей, ингибиторов, антифризов, метиламина, метилового эфира акриловой кислоты, лаков, красителей и других продуктов. В чистом виде применяется как добавка к моторному топливу и в качестве растворителя.
Гидролиз целлюлозы, иначе называемый осахариванием,-очень важное свойство целлюлозы, он позволяет получить из древесных опилок и стружек глюкозу, а сбраживанием последней — этиловый спирт. Этиловый спирт, полученный из древесины, называется гидролизным.
Этиловый спирт, полученный из древесины, называется гидролизным.
Поэтому большинство установок для перегонки дерева получают лишь часть содержащихся в сыром древесном спирте метилового спирта и ацетона в виде чистого метилового спирта и чистого ацетона. Остальную значительную часть в виде первых и средних погонов, полученных в колонках обычным способом, т. е. без введения воды и пара, смешивают вместе и получают древесный спирт для денатурации. Отделение метилового спирта от ацетона описанным здесь способом, посредством которого это отделение происходит почти количественно, дает значительное финансовое преимущество перед прочими установками, ра-
Метиловый спирт (метанол, древесный спирт) СНзОН — бесцветная жидкость с характерным запахом, смешивается с водой в любых соотношениях, хороши растворитель многих органических веществ, горит бледным пламенем. М. с. очень ядовит, вызывая в малых дозах слепоту, в больших — смерть. В промышленности метиловый спирт получают двумя способами присухой перегонке дерева (поэтому его называют древесным спиртом) и синтетически из СО и Нг в присутствии катализатора (напр. , оксид цинка ZnO), при 300-600 °С и давлении 5-10 Па (СО + Ц- 2Нг = СНзОН). М. с. применяют как сырье для получения муравьиного альдегида (формальдегида) и для синтеза других органических веществ, в производстве красителей и лаков.
, оксид цинка ZnO), при 300-600 °С и давлении 5-10 Па (СО + Ц- 2Нг = СНзОН). М. с. применяют как сырье для получения муравьиного альдегида (формальдегида) и для синтеза других органических веществ, в производстве красителей и лаков.
Метиловый спирт (метанол) СН3ОН, носящий еще название древесного спирта (по старому способу его получения — сухой перегонкой дерева), представляет собой бесцветную жидкость, кипящую при 64,7° С. Обладает характерным спиртовым запахом, горит бледным пламенем. Метиловый спирт сильно ядовит. При принятии внутрь вызывает тяжелое отравление, сопровождаемое потерей зрения может привести к смертельному исходу.
Первыми источниками получения органических веществ были животные и растительные организмы X, продукты их жизнедеятельности. Каждый живой организм представляет собой своеобразную химическую лабораторию, в которой осуществляются как процессы синтеза, так и распада. В растительных организмах из простых исходных веществ (диоксид углерода, вода) под воздействием солнечной энергии синтезируются сложные органические вещества (фотосинтез). В животных организмах, наоборот, сложные органические вещества (сахара, белки, жиры) распадаются на более простые, часть из них как бы сгорает, отдавая энергию и превращаясь в СО2 и Н2О, но в то же время в организме также синтезируются специфические белки, жиры и другие вещества. Растительный мир является главным производителем органических веществ. Особое место в этом отношении занимают деревья. Древесина и полученные из нее целлюлоза и лигнин являются ценным сырьем для химической переработки. Так, например, сухая перегонка древесины с давних времен применялась для получения органических соединений, таких, как уксусная кислота, метиловый спирт (древесный спирт), ацетон, фенолы.
В животных организмах, наоборот, сложные органические вещества (сахара, белки, жиры) распадаются на более простые, часть из них как бы сгорает, отдавая энергию и превращаясь в СО2 и Н2О, но в то же время в организме также синтезируются специфические белки, жиры и другие вещества. Растительный мир является главным производителем органических веществ. Особое место в этом отношении занимают деревья. Древесина и полученные из нее целлюлоза и лигнин являются ценным сырьем для химической переработки. Так, например, сухая перегонка древесины с давних времен применялась для получения органических соединений, таких, как уксусная кислота, метиловый спирт (древесный спирт), ацетон, фенолы.
До середины XIX в. практика переработки органических веществ не выходила за пределы извлечения из растительного и животного сырья содержащихся в нем ценных продуктов (например,- красителей, сахаров, дубителей и др.). Для выделения их использовались простейшие механические и тепловые процессы обработки сырья дробление, растворение, фильтрование, отжим, выпаривание, перегонка и т. д. При получении спирта, уксусной кислоты и некоторых других органических веществ использовались биохимические процессы (в частности, брожение). Некоторые органические продукты были выделены при термическом разложении природного сырья. Так, при сухой перегонке древесины наряду с древесным углем получали уксусную кислоту, древесный спирт, деготь.
д. При получении спирта, уксусной кислоты и некоторых других органических веществ использовались биохимические процессы (в частности, брожение). Некоторые органические продукты были выделены при термическом разложении природного сырья. Так, при сухой перегонке древесины наряду с древесным углем получали уксусную кислоту, древесный спирт, деготь.
Фракции сырой (неочищенной) смолы представляют собой сложные смеси, состоящие из легких и тяжелых масел, которые находят применение для пропитки древесины и медицинских целей. При перегонке смолы в остатке получают пек. Фракцию тяжелых масел перерабатывают на креозот. Основным компонентом этого продукта является гваякол, применяемый в фармацевтической промышленности как антисептическое средство. Фенольные компоненты пиролизной смолы можно также использовать при получении связующих для фанеры . Древесный спирт содержит около 60 % метанола и различных примесей (см. 12.5). Его используют в качестве растворителя и для денатурации этанола. Из фракции древесного уксуса (см. 12.5) можно получить чистую уксусную кислоту и пищевой уксус. Решение вопроса о том, следует или нет получать очищенные продукты, зависит от экономических соображений и требований экологии . Неконденсируемые газы, состоящие из диоксида и моноксида углерода, водорода, метана и других углеводородов (теплота сгорания около 8,9 МДж/м), применяют для предварительной сушки древесины и в качестве газа для продувки реторт .
Из фракции древесного уксуса (см. 12.5) можно получить чистую уксусную кислоту и пищевой уксус. Решение вопроса о том, следует или нет получать очищенные продукты, зависит от экономических соображений и требований экологии . Неконденсируемые газы, состоящие из диоксида и моноксида углерода, водорода, метана и других углеводородов (теплота сгорания около 8,9 МДж/м), применяют для предварительной сушки древесины и в качестве газа для продувки реторт .
В промышленности метиловый спирт раньше получали при сухой перегонке древесины, откуда и его название — древесный спирт. При нагревании древесины без доступа воздуха происходит разложение целлюлозы и других веществ, в частности сложного вещества, спутника целлюлозы — лигнина. В результате образуются различные газообразные, жидкие и твердые продукты, в том числе.и метиловый спирт. Полученный таким образом метиловый спирт всегда содержит примеси уксусной кислоты, ацетона и других органических веществ.
Метиловый спирт. Метиловый спирт (другие названия метанол, карбинол, древесный спирт) — простейший одноатомный спирт, бесцветная легкоподвижная жидкость. Сильный яд (прием внутрь вызывает слепоту, при больших дозах — смерть). Современный метод получения — каталитический синтез из окиси углерода и водорода (температура 300-400 С, давление 250-500 атм, катализатор — окись цинка)
Метиловый спирт (другие названия метанол, карбинол, древесный спирт) — простейший одноатомный спирт, бесцветная легкоподвижная жидкость. Сильный яд (прием внутрь вызывает слепоту, при больших дозах — смерть). Современный метод получения — каталитический синтез из окиси углерода и водорода (температура 300-400 С, давление 250-500 атм, катализатор — окись цинка)
Метиловый спирт прежде получали деструктивной перегонкой древесины и называли его поэтому иногда древесным спиртом. Это ядовитое вещество, и употребление его приводит к слепоте и смерти. Метиловый спирт применяют в качестве растворителя, а также используют для получения других органических соединений.
В табл. 38 приведены доли спирта от всего поступившего на ректификацию, в пересчете на 100%-ный, в отг льных сортах ректификованных спиртов, полученных ректификацией необработанного спирта-сырца и обработанного перед ректификацией древесным углем, едким натром либо перманганатом калия в табл. 39 — основные характеристики полученных при этом ректификованных спиртов I сорта. В представленных таблицах столбцы, пронумерованные цифрой 1, относятся к ректификованному спирту, полученному из необработанного спирта-сырца 2 — обработанного древесным углем 3 — обработанного едким натром 4 — обработанного перманганатом калия.
В представленных таблицах столбцы, пронумерованные цифрой 1, относятся к ректификованному спирту, полученному из необработанного спирта-сырца 2 — обработанного древесным углем 3 — обработанного едким натром 4 — обработанного перманганатом калия.
Некоторое количество метилового спирта получается методом сухой перегонки древесины отсюда и одно из названий метанола — древесный спирт. Это наиболее старый способ его получения.
Летучие компоненты отделяют перегонкой с получением сырых продуктов. Так, фракция древесного спирта состоит из воды, 45 % метанола, 7 ацетона, 5 метилацетата, 3 % ацетальдегида и небольших количеств аллилового спирта, метилформиата, фурана и фурфурола. Фракция древесного уксуса содержит в основном уксусную кислоту, а также пропионовую, масляную и другие кислоты. Главными компонентами фракции смолы являются крезол, гваякол, другие фенолы и простые эфиры фенолов .
Метилозый спирт образуется и при сухой перегонке дерева поэтому его называют также древесным спиртом. Применяется он как растворитель, а также для получения других органических веществ.
Применяется он как растворитель, а также для получения других органических веществ.
Первый представитель гомологического ряда предельных одноатомных спиртов — метиловый спирт (метанол) СН3ОН раньше часто называли древесным спиртом. Происхождение этого названия связано со старинным способом получения метилового спирта при сухой перегонке дерева. В настоящее время метанол получается исключительно синтетическим путем, при пропускании смеси окиси углерода и водорода при 350 °С и 250 атм над катализатором, состоящим из смеси цинка, хрома и других металлов
Метиловый спирт. Метило1 лй спирт (другие названия метанол, карбинол, древесный спирт) — простейший одноатомный спирт, бесцветная жидкость. Сильный яд (прием внутрь вызывает слепоту, при ббльших дозах — смерть). Сов >еменный метод получения — каталитический синтез из оксида углерэда (II) и водорода [томпература 250°С, давление 7 МПа, катализатор — смесь оксидов цинка и меди (II)]
При сухой перегонке древесины уксусная кислота, собирается в подсмольной воде. Для отделения уксусной кислоты от древесного спирта и ацетона ее нейтрализуют известью полученный уксуснокислый кальций, так называемый уксусный порошок, разлагают соляной кислотой или серной кислотой
Для отделения уксусной кислоты от древесного спирта и ацетона ее нейтрализуют известью полученный уксуснокислый кальций, так называемый уксусный порошок, разлагают соляной кислотой или серной кислотой
Кроме этих наименований некоторые спирты имеют еще эмпирические наименования, связанные с историей открытия в том или ином природном продукте, способом получения и т. д. Например, метиловый спирт часто называют древесным спиртом, т к как он получается при сухой перегонке дерева этиловый спирт называют винным спиртом, так как он был впервые обнаружен в виноградном вине, и т. д.
Метиловый спирт, или метанол, СН3ОН (также древесный спирт, или карбинол) получается любым из общих способов получения спиртов. Однако в течение многих лет единственным источником его являлись продукты сухой перегонки дерева. Водный слой, получаемый наряду с древесным дегтем при медленном нагревании дерева без доступа воздуха, содержит 1-2% метилового спирта и, кроме того, много уксусной кислоты (10%) и немного ацетона (0,5%). Уксусную кислоту отделяют обработкой известью, после чего метиловый спирт очищают дробной перегонкой и другими способами.
Уксусную кислоту отделяют обработкой известью, после чего метиловый спирт очищают дробной перегонкой и другими способами.
В течение длительного времени химики называли органические вещества по случайным признакам. Чаще всего эти названия отражали происхождение веществ (муравьиная, яблочная, винная кислоты, молочный сахар, винный и древесный спирты и др.), иногла- способ получения (пировиноградная кислота), а порой — имя исследователя (например, кетон Михлера). Эти случайные названия, не отражающие строения молекул органических веществ, получили название тривиальных, а система этих названий — тривиальной номенклатуры. Эти названия используются и сейчас, особенно когда речь идет о привычных и часто применяемых реактивах.
Метиловый спирт, метанол, древесный спирт. Бесцветная жидкость, т. кип, 64,5°, хорошо растворяется в воде. Широко применяется в лабораторной работе как растворитель, а также в ряде органических синтезов (получение формальдегида, реакция метилирования и др. ). Обладает высокой токсичностью и вызывает тяжелые отравления. При постоянной работе с метиловым спиртом опасно постепенное (комулятивное) нарастание его действия. Помимо наркотического действия метиловый спирт вызывает органическое поражение зрительного нерва и сетчатки глаз, в связи с чем при отравлении метиловым спиртом может наступить полная или частичная потеря зрения. Смертельная доза при приеме внутрь метилового спирта 30 г тяжелые отравления могут наступить при приеме 5-10 г .
). Обладает высокой токсичностью и вызывает тяжелые отравления. При постоянной работе с метиловым спиртом опасно постепенное (комулятивное) нарастание его действия. Помимо наркотического действия метиловый спирт вызывает органическое поражение зрительного нерва и сетчатки глаз, в связи с чем при отравлении метиловым спиртом может наступить полная или частичная потеря зрения. Смертельная доза при приеме внутрь метилового спирта 30 г тяжелые отравления могут наступить при приеме 5-10 г .
Как видно из представленных данных, ректификованные спирты I сорта, полученные из обработанного и необработанного спирта-сырца, имеют одинаковые или близкие показатели по вкусу и запаху, крепости, содержанию фурфурола, альдегидов и сивушного масла. (Понятно, что к характеристикам спирта, обозначенным словами нет и следы, небходимо относиться осторожно, с пониманием того, что анализ произведен в условиях промышленного производства исследования выполнены на Бах-мачском винокуренном заводе Черниговской губернии.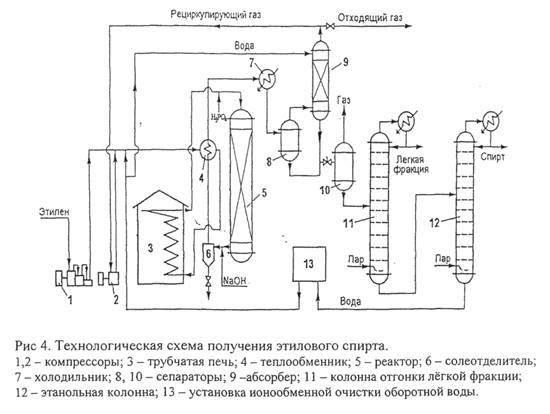 ) Но в спиртах, полученных перегонкой спирта-сырца, обработанного древесным углем и едким натром, содержание эфиров и кислот ниже, чем у двух других спиртов. Значительно лучше у них и показатель Ланга (см. с. 216-218). Выход ректификованных
) Но в спиртах, полученных перегонкой спирта-сырца, обработанного древесным углем и едким натром, содержание эфиров и кислот ниже, чем у двух других спиртов. Значительно лучше у них и показатель Ланга (см. с. 216-218). Выход ректификованных
Основной пирогенетический процесс был выбран с получением древесного угля, который является более дефицитным и нужным продуктом, чем древесный генераторный газ. Для получения наибольшей гаммы продуктов пиролиза, образующихся при НИЗКИХ и высоких температурах, процесс разложения ведется в две стадии. Сначала древесину подвергают предварительному пиролизу в среде жидкого теплоносителя (дизельное топливо) с температурой 275° и получают основную массу кислот, легкокипящих продуктов, входящих в так называемый древесный спирт, и смол. Образующуюся в результате предпиролиза бурую древесину (см. стр. 37) подвергают вторичному пиролизу при температуре 600-700° с твердым теплоносителем (древесный уголь) и Получают светильный газ и жижку, содержащую отстойную смолу с большим выходом низкокипящих фенолов, дополнительное количество кислот и древесный уголь. Последний отличается низким содержанием летучих и повышенной активностью.
Последний отличается низким содержанием летучих и повышенной активностью.
Осветленный сьфой древесный спирт должен быть и оставаться щелочным, прежде чем можно приступить к его иере-гоеке. Если он не щелочной, то полученный из него чистый метиловый спирт будет желтым, часто даже после нескольких перегонок. Если очистка известковым раствор ом проведена тщательно, то выделенный при взбалтывании 1 ч. отстоявшегося древесного спирта с 2 ч. раствора едкого натра уд. в. 1,3 ацетон
Номенклатура. Первый член гомологического ряда предельных одноатоммых спиртов в прошлом получали путем сухой перегонки древесины, а поэтому полученный спирт называли древесным спиртом или карбинолом. Следующий член — С2Н5ОН — был назван винным спиртом еще алхимиками.
По вопросу получения формальдегида из метана имеется обширная патентная литература. Процесс окисления начинается здесь при повышенной температуре (500-600°), которая поддерживается далее теплотой самой реакции для ее успешного течения некоторые авторы рекомендуют применение давления, а также катализаторов (Си, Ге, N1, Со). Формальдегид находит обширное применение в качестве дезинфе цирующего вещества и антисептика в химической технологии он широко применяется для изготовления органических красок (фуксин и др.), искусственных смол (бакелит и т. п.) и т. д. Технически формальдегид получается пока окислением древесного спирта.
Формальдегид находит обширное применение в качестве дезинфе цирующего вещества и антисептика в химической технологии он широко применяется для изготовления органических красок (фуксин и др.), искусственных смол (бакелит и т. п.) и т. д. Технически формальдегид получается пока окислением древесного спирта.
Смотреть страницы где упоминается термин Древесный спирт получение : Начала органической химии Кн 1 Издание 2 (1975) — [
Общая схема получения этилового спирта из гидролизной «черной патоки» такова. Сырье в измельченном виде загружают в многометровую стальную гидролизную колонну, изнутри облицованную химически стойкой керамикой. Туда подают под давлением горячий раствор соляной кислоты. В результате химической реакции из целлюлозы получается продукт, содержащий сахар, так называемая «черная патока». Этот продукт нейтрализуют известью и туда добавляют дрожжи — сбраживают патоку. После чего опять нагревают, и выделяющиеся пары конденсируются в виде этилового спирта (называть его «винным», не хочется).
Гидролизный способ — самый экономный способ производства этилового спирта. Если традиционным биохимическим способом сбраживания из одной тонны зерна можно получить 50 литров спирта, то из одной тонны древесных опилок, гидролизным способом преобразованных в «черную патоку», выгоняется 200 литров спирта. Как говориться: «Почувствуйте выгоду!» Весь вопрос, можно ли «черную патоку» как осаха-ренную целлюлозу называть «пищевым продуктом», наравне с зерном, картофелем и свеклой. Лица, заинтересованные в производстве дешевого этилового спирта, считают так: « А чё, почему нельзя? Ведь барда, как остаток «черной патоки», после ее перегонки идет на корм скоту, значит, она тоже пищевой продукт». Как тут не вспомнить слова Ф.М.Достоевского: «Образованный человек, когда это ему нужно, может словесно оправдать любую мерзость».
В 30-х годах прошлого века в осетинском поселке Беслан был построен крупнейший в Европе крахмалопа-точный комбинат, который с тех пор выпускает миллионы литров этилового спирта. Потом мощные заводы по производству этилового спирта были построены по всей стране, в том числе при Соликамском и Архангельском целлюлозо-бумажных комбинатах. И.В. Сталин, поздравляя строителей гидролизных заводов, которые во время войны, несмотря на трудности военного времени, досрочно ввели их в эксплуатацию, отметил, что это «дает возможность сэкономить государству миллионы пудов хлеба» (Газета «Правда» от 27 мая 1944 г.).
Потом мощные заводы по производству этилового спирта были построены по всей стране, в том числе при Соликамском и Архангельском целлюлозо-бумажных комбинатах. И.В. Сталин, поздравляя строителей гидролизных заводов, которые во время войны, несмотря на трудности военного времени, досрочно ввели их в эксплуатацию, отметил, что это «дает возможность сэкономить государству миллионы пудов хлеба» (Газета «Правда» от 27 мая 1944 г.).
Этиловый спирт, полученный из «черной патоки», а, по сути, из древесины (целлюлозы), осахаренной гидролизным способом, если, конечно, он хорошо очищен, не отличить от спирта, полученного из зерна или картофеля. По действующим стандартам такой спирт бывает «высшей очистки», «экстра» и «люкс», последний — самый лучший, то есть имеет самую высокую степень очистки. Водкой, приготовленной на основе такого спирта, не отравишься. На вкус такой спирт нейтрален, то есть «никакой» — безвкусный, в нем лишь одни «градусы», он только обжигает слизистую оболочку рта. Внешне распознать водку, сделанную на основе этилового спирта гидролизного происхождения, довольно трудно, а различные ароматизаторы, добавляемые к таким «водкам», придают им некоторое отличие друг от друга.
Внешне распознать водку, сделанную на основе этилового спирта гидролизного происхождения, довольно трудно, а различные ароматизаторы, добавляемые к таким «водкам», придают им некоторое отличие друг от друга.
Однако не все так хорошо, как кажется на первый взгляд. Генетики провели исследования: одной партии подопытных мышей в рацион добавляли настоящую (зерновую) водку, другой — гидролизную, из древесины. Мыши, которые употребляли «сучок» умирали гораздо быстрее, а их потомство вырождалось. Но результаты этих исследований не остановили выпуск псевдорусских водок. Это как в популярной песне: «Ведь если водку гнать не из опилок, то что б нам было с пяти бутылок…»
Растёт спрос на биотоплива — горючие жидкости, изготовленные из возобновляемых биологических ресурсов. Один из них — древесина. Можно ли из древесины получать топливо, не уступающее нефтяному?
Первое, что нужно уяснить — это то, что именно бензина или керосина из дерева сделать нельзя. Оно не поддаётся разложению на углеводороды с прямой цепью, из которых главным образом состоят нефтепродукты. Однако это не означает, что из него нельзя получать вещества, способные заменить нефтепродукты.
Однако это не означает, что из него нельзя получать вещества, способные заменить нефтепродукты.
Некоторые любят табуретовку
Первый в списке, конечно же, спирт. Из древесины можно получать два различных вида спирта. Первый, который так и называется древесным — по-научному метиловый спирт. Это вещество очень похоже на привычный этиловый спирт, как по горючести, так и по запаху и вкусу. Однако метиловый спирт отличается тем, что весьма ядовит, и приём его внутрь может привести к смертельному отравлению. Вместе с тем он является высококачественным моторным топливом, его октановое число даже выше, чем у этилового спирта, и намного выше, чем у обыкновенного бензина.
Технология получения метилового спирта из древесины очень проста. Он получается путём сухой перегонки, или пиролиза. Точнее, он является одной из составных частей жижки — смеси кислородсодержащих органических веществ, отделяющихся от свежевыгнанной древесной смолы. Однако выход полученного таким образом спирта слишком мал, чтобы он мог использоваться в качестве топлива. Это делает подобную технологию получения топлива бесперспективной.
Это делает подобную технологию получения топлива бесперспективной.
Однако из древесины можно получить и этиловый спирт, в намного больших количествах. Этот спирт — так называемый гидролизный — получается при разложении целлюлозы, основного компонента древесины, с помощью серной кислоты. Вернее, при разложении целлюлозы получаются сахара, которые в свою очередь могут быть переработаны в спирт обычным путём. Этот способ получения этилового спирта весьма распространён в промышленности, именно гидролизным способом получают практически весь технический спирт, применяемый в непищевых целях.
Этиловый спирт может быть использован как непосредственно вместо бензина, так и в качестве присадки к бензину. Путём таких присадок получаются различные сорта биотоплива, популярные, в частности, в таких странах, как Бразилия.
Получение этилового спирта путём гидролиза древесины экономически несколько менее выгодно, чем получение его из различных сельскохозяйственных культур. Однако выгодной стороной такого способа получения биотоплива является то, что он не требует отведения сельскохозяйственных площадей под «топливные» культуры, не дающие пищевых продуктов, а позволяет использовать для его производства территории, задействованные в лесном хозяйстве. Это делает получение биотопливного этанола из древесины достаточно практичной технологией.
Это делает получение биотопливного этанола из древесины достаточно практичной технологией.
И терпентин на что-нибудь полезен
Недостатком этанола как топлива является его низкая теплота сгорания. При использовании в двигателях в чистом виде он даёт или меньшую мощность, или больший расход, чем бензин. Решить эту проблему помогает смешивание спирта с веществами с высокой теплотой сгорания. И не обязательно это продукты из нефти: в качестве такой присадки вполне годится скипидар, или терпентин.
Скипидар — тоже продукт переработки древесины, а если конкретно — хвойной: сосен, елей, лиственниц и других. Он достаточно широко применяется как растворитель, а наиболее очищенные его сорта находят применение в медицине. Однако лесоперерабатывающая промышленность в качестве побочного продукта производит большое количество так называемого сульфатного скипидара — низшего сорта, содержащего ядовитые примеси, не только неприменимого в медицине, но и находит весьма ограниченное применение в химической и лакокрасочной промышленности.
Вместе с тем скипидар из всех продуктов переработки древесины более всего похож на нефтепродукт, точнее — на керосин. Он отличается весьма высокой теплотой сгорания, может использоваться как горючее в керосиновых примусах, лампах, керогазах. Пригоден он и в качестве моторного топлива, правда, непродолжительное время: если его заливать в баки в чистом виде, двигатели вскоре выходят из строя из-за засмоления.
Однако скипидар можно использовать в качестве топлива не в чистом виде, а в качестве присадки к этанолу. Такая присадка не сильно снижает октановое число этилового спирта, но повышает теплоту его сгорания. Ещё одна положительная сторона такой технологии изготовления биотоплива в том, что скипидар денатурирует спирт, делает его непригодным для употребления внутрь в качестве алкоголя. А социальные последствия широкого внедрения неденатурированного спирта в качестве топлива могут стать весьма тяжелыми.
Лигниновые отходы — в доходы!
Такой компонент древесины, как лигнин, считается малополезным. Его применение в промышленности значительно менее широкое, нежели у целлюлозы. Несмотря на то, что он находит применение в производстве строительных материалов и в химической промышленности, чаще его просто сжигают прямо на лесохимпроизводстве. Однако, как выясняется, при пиролизе лигнина можно получить более разнообразные продукты, чем при пиролизе целлюлозы.
Его применение в промышленности значительно менее широкое, нежели у целлюлозы. Несмотря на то, что он находит применение в производстве строительных материалов и в химической промышленности, чаще его просто сжигают прямо на лесохимпроизводстве. Однако, как выясняется, при пиролизе лигнина можно получить более разнообразные продукты, чем при пиролизе целлюлозы.
Лигнин состоит главным образом из ароматических циклов и коротких прямых углеводородных цепей. Соответственно, при его пиролизе получаются преимущественно углеводороды. Однако, в зависимости от технологии пиролиза, можно получать как продукт с высоким содержанием фенола и родственных ему веществ, так и жидкость, напоминающую нефтепродукты. Эта жидкость также пригодна в качестве присадки к этиловому спирту для получения биотоплива.
Разработаны технологии и установки для пиролиза, которые могут потреблять как лигнин из отвалов, так и неразделённые на лигнин и целлюлозу отходы древесины. Более высокие результаты получаются при смешивании лигнина или древесных отходов с мусором, состоящим из выброшенного пластика или резины: пиролизная жидкость получается более нефтеподобной.
Мирный атом и опилки
Ещё одна технология получения биотоплива из древесины разработана совсем недавно российскими учёными. Она относится к области радиохимии, то есть химических процессов, протекающих под воздействием радиоактивного излучения. В опытах учёных из ИФХЭ им. Фрумкина опилки и другие отходы древесины подвергались одновременному воздействию сильного бета-излучения и сухой перегонки, причём нагревание древесины проводилось именно с помощью сверхсильной радиации. Удивительно, но под воздействием радиации состав продуктов, получаемых при пиролизе, изменился.
В пиролизной жидкости, полученной «радиоактивным» способом, было обнаружено высокое содержание алканов и циклоалканов, то есть углеводородов, содержащихся главным образом в нефти. Эта жидкость получилась значительно легче нефти, сравнимой, скорее, с газоконденсатом. Причём экспертиза подтвердила пригодность этой жидкости для использования в качестве моторного топлива или переработки в высококачественные топлива, такие, как автомобильный бензин. Думаем, что это не заслуживает особого упоминания, но проясним ради успокоения страхов радиофобов: бета-излучение не способно вызывать наведённую радиоактивность, поэтому топливо, получаемое этим способом, безопасно и не проявляет радиоактивных свойств само.
Думаем, что это не заслуживает особого упоминания, но проясним ради успокоения страхов радиофобов: бета-излучение не способно вызывать наведённую радиоактивность, поэтому топливо, получаемое этим способом, безопасно и не проявляет радиоактивных свойств само.
Что пускать в переработку
Понятно, что предпочтительнее использовать для производства биотоплива не цельные стволы деревьев, а отходы переработки древесины, такие, как опилки, щепу, веточки, кору, да и тот же лигнин, который идёт в отвалы и печи. Выход этих отходов с гектара поваленного леса, конечно же, ниже, чем древесины в целом, но не следует забывать, что они получаются в качестве побочного продукта в производственных процессах, которые уже идут на многих предприятиях страны, соответственно, отходы производства дешевы и для их получения не нужно вырубать или засаживать под вырубку дополнительные площади леса.
В любом случае, древесина является ресурсом возобновляемым. Способы восстановления лесных площадей давно известны, а во многих регионах страны наблюдается даже и неконтролируемое зарастание лесом заброшенных сельскохозяйственных земель. Так или иначе, Российская Федерация не относится к странам, где к сбережению леса следует относиться со всем тщанием; площадей нашего леса и его потенциала к самовосстановлению вполне достаточно, чтобы загрузить полностью и лесоперерабатывающую промышленность, и производство биотоплив, и многие другие производства.
Так или иначе, Российская Федерация не относится к странам, где к сбережению леса следует относиться со всем тщанием; площадей нашего леса и его потенциала к самовосстановлению вполне достаточно, чтобы загрузить полностью и лесоперерабатывающую промышленность, и производство биотоплив, и многие другие производства.
Гидролиз полисахаридов растительной ткани в холодной воде практически не наблюдается. При повышении температуры воды выше 100° гидролиз полисахаридов протекает, но настолько медленно, что практического значения такой процесс не имеет. Удовлетворительные результаты получаются только при применении катализаторов, из которых производственное значение имеют лишь сильные минеральные кислоты: серная и реже соляная. Чем выше концентрация сильной кислоты в растворе и температура реакции, тем быстрее протекает гидролиз полисахаридов до моносахаридов. Однако присутствие таких катализаторов имеет и отрицательную сторону, так как они одновременно с реакцией гидролиза полисахаридов ускоряют и реакции распада моносахаридов, соответственно снижая этим их выход.
При распаде гексоз в этих условиях вначале образуется окси — метилфурфурол, который быстро разлагается далее с образованием конечных продуктов: левулиновой и муравьиной кислот. Пентозы в этих условиях превращаются в фурфурол.
В связи с этим, чтобы получить из полисахаридов растительной ткани моносахариды, необходимо обеспечить наиболее благоприятные условия для реакции гидролиза и максимально сократить возможности дальнейшего распада образующихся моносахаридов.
В этом заключается задача, которую решают исследователи и производственники при выборе оптимальных режимов гидролиза.
Из большого числа возможных вариантов концентрации кислоты и температуры реакции в настоящее время практически применяются только два: гидролиз разбавленными кислотами и гидролиз концентрированными кислотами. При гидролизе разбавленными кислотами температура реакции обычно составляет 160-190° и концентрация катализатора в водном растворе колеблется от 0,3 до 0,7% (h3S04, НС1).
Реакцию проводят в автоклавах под давлением 10-15 атм. При гидролизе концентрированными кислотами концентрация серной кислоты обычно составляет 70-80%, а соляной 37-42%. Температура реакции в этих условиях 15-40°.
При гидролизе концентрированными кислотами концентрация серной кислоты обычно составляет 70-80%, а соляной 37-42%. Температура реакции в этих условиях 15-40°.
Снизить потери моносахаридов легче при гидролизе концентрированными кислотами, вследствие чего выход сахара при этом методе может достигать почти теоретически возможного, т, е. 650-750 кг из 1 т абсолютно сухого растительного сырья.
При гидролизе разбавленными кислотами снизить потери моносахаридов вследствие их разложения значительно труднее и поэтому практически выход моносахаридов в этом случае обычно не превышает 450-500 кг из 1 г сухого сырья.
Ввиду малых потерь сахара при гидролизе концентрированными кислотами получающиеся водные растворы моносахаридов — гидролизаты отличаются повышенной чистотой, что имеет большое значение при их последующей переработке.
Серьезным недостатком методов гидролиза концентрированными кислотами до последнего времени был большой расход минеральной кислоты на тонну получаемого сахара, что приво дило к необходимости регенерации части кислоты или использования ее в других производствах; это осложняло и удорожало строительство и эксплуатацию таких заводов.
Большие трудности возникали также при подборе для аппаратуры материалов, стойких в агрессивных средах. По этой причине основная масса действующих в настоящее время гидролизных заводов была построена по методу гидролиза разбавленной серной кислотой.
Первый опытный гидролизно-спиртовый завод в СССР был пущен в январе 1934 г. в г. Череповце. Исходные показатели и технический проект этого завода были разработаны кафедрой гидролизных производств Ленинградской лесотехнической академии в 1931 -1933 гг. На основе данных эксплуатации опытного завода было начато строительство в СССР промышленных гид — ролизно-спиртовых заводов. Первый промышленный гидролизно — спиртовый завод был пущен в Ленинграде в декабре 1935 г. Вслед за этим заводом в период 1936-1938 гг. вошли в строй Бобруйский, Хорский и Архангельский гидролизно-спиртовые заводы. Во время второй мировой войны и после нее было построено много больших заводов в Сибири и на Урале. В настоящее время проектная мощность этих заводов в результате совершенствования технологии перекрыта в 1,5-2 раза.
Основным сырьем для этих заводов является хвойная древесина в виде опилок и щепы, поступающая с соседних лесопильных заводов, где ее получают путем измельчения в рубительных машинах отходов лесопиления — горбыля и рейки. В отдельных случаях измельчают и хвойные дрова.
Схема получения моносахаридов на таких заводах представлена на рис. 76.
Измельченная хвойная древесина со склада сырья по транспортеру 1 поступает в направляющую воронку 2 и далее в горло-
Вину гидролизаппарата 3. Это вертикальный стальной цилиндр с верхним и нижним конусами и горловинами. Внутреннюю поверхность такого гидролизаппарата покрывают кислотоупорными керамическими или графитовыми плитками или кирпичом, укрепленным на слое бетона толщиной 80-100 мм. Швы между плитками заполняются кислотоупорной замазкой. Верхняя и нижняя горловины гидролизаппарата с внутренней стороны защищены от действия горячей разбавленной серной кислоты слоем кислотоупорной бронзы. Полезный объем таких гидролизаппа — ратов обычно составляет 30-37 At3, но иногда применяются также гидролизаппараты объемом 18, 50 и 70 м3. Внутренний диаметр таких гидролизаппаратов составляет около 1,5, а высота 7-13 м. В верхний конус гидролизаппарата во время гидролиза по трубе 5 подается нагретая до 160-200° разбавленная серная кислота.
Полезный объем таких гидролизаппа — ратов обычно составляет 30-37 At3, но иногда применяются также гидролизаппараты объемом 18, 50 и 70 м3. Внутренний диаметр таких гидролизаппаратов составляет около 1,5, а высота 7-13 м. В верхний конус гидролизаппарата во время гидролиза по трубе 5 подается нагретая до 160-200° разбавленная серная кислота.
В нижнем конусе установлен фильтр 4 для отбора полученного гидролизата. Гидролиз в таких аппаратах производится периодически.
Как уже указывалось выше, гидролизаппарат загружают измельченным сырьем через направляющую воронку. При загрузке сырья через трубу 5 поступает нагретая до 70-90° разбавленная серная кислота, которая смачивает сырье, способствуя его уплотнению. При таком методе загрузки в 1 м3 гидролизаппарата помещается около 135 кг опилок или 145-155 кг Щепы, в пересчете на абсолютно сухую древесину. По окончании загрузки содержимое гидролизаппарата подогревается острым паром, поступающим в нижний конус его. Как только будет достигнута температура 150-170°, в гидролизаппарат по трубе 5 начинает поступать 0,5-0,7’%-пая серная кислота, нагретая до 170-200°. Одновременно образующийся гидролизат через фильтр 4 начинает выводиться в испаритель б. Реакция гидролиза в гидролизаппарате продолжается от 1 до 3 часов. Чем короче время гидролиза, тем выше температура и давление в гидролизаппарате.
Как только будет достигнута температура 150-170°, в гидролизаппарат по трубе 5 начинает поступать 0,5-0,7’%-пая серная кислота, нагретая до 170-200°. Одновременно образующийся гидролизат через фильтр 4 начинает выводиться в испаритель б. Реакция гидролиза в гидролизаппарате продолжается от 1 до 3 часов. Чем короче время гидролиза, тем выше температура и давление в гидролизаппарате.
В процессе гидролиза полисахариды древесины переходят в соответствующие моносахариды, растворяющиеся в горячей разбавленной кислоте. Для предохранения этих моносахаридов от разложения при высокой температуре содержащий их гидролизат непрерывно в течение всей варки выводят через фильтр 4 И быстро охлаждают в испарителе 6. Так как по условиям процесса гидролизуемое растительное сырье. в гидролизаппарат» все время должно быть залито жидкостью, заданный уровень е поддерживается горячей кислотой, поступающей по трубе 5,
Такой метод работы носит название перколяция. Чем быст рее идет перколяция, т. е. чем быстрее через гидролизаппарат протекает горячая кислота, тем быстрее образующийся сахар выводится из реакционного пространства и тем меньше он разлагается. С другой стороны, чем быстрее идет перколяция, тем больше расходуется на варку горячей кислоты и тем меньше получается концентрация сахара в гидролизате и соответственно больше расход пара и кислоты на варку.
е. чем быстрее через гидролизаппарат протекает горячая кислота, тем быстрее образующийся сахар выводится из реакционного пространства и тем меньше он разлагается. С другой стороны, чем быстрее идет перколяция, тем больше расходуется на варку горячей кислоты и тем меньше получается концентрация сахара в гидролизате и соответственно больше расход пара и кислоты на варку.
Практически для получения достаточно высоких выходов сахара (при экономически приемлемой концентрации его в гидролизате) приходится выбирать некоторые средние условия пер — коляции. Обычно останавливаются на выходе сахара в 45-50% от веса абсолютно сухой древесины при концентрации сахара в гидролизате 3,5-3,7 % — Эти оптимальные условия реакции соответствуют отбору через нижний фильтр из гидролизаппара — та 12-15 м3 гидролизата на 1 т абсолютно сухой древесины, загруженной в гидролизаппарат. Количество гидролизата, отбираемого за варку на каждую тонну гидролизуемого сырья, называют гидромодулем вытекания, и он является одним из основных показателей примененного на заводе режима гидролиза. бе 21. Для этой цели быстро открывают клапан 20, соединяющий внутреннее пространство гидролизаппарата с циклоном 22. Благодаря быстрому снижению давления между кусочками лигнина содержащаяся в нем перегретая вода мгновенно вскипает, образуя большие объемы пара. Последний рвет лигнин и увлекает его в виде взвеси по трубе 21 в циклон 22. Труба 21 подходит к циклону по касательной, благодаря чему струя пара с лигнином, врываясь в циклон, движется вдоль стенок, совер — шая вращательное движение. Лигнин центробежной силой отбрасывается к боковым стенкам и, теряя скорость, падает на дно циклона. Освобожденный от лигнина пар через центральную трубу 23 выбрасывается в атмосферу.
бе 21. Для этой цели быстро открывают клапан 20, соединяющий внутреннее пространство гидролизаппарата с циклоном 22. Благодаря быстрому снижению давления между кусочками лигнина содержащаяся в нем перегретая вода мгновенно вскипает, образуя большие объемы пара. Последний рвет лигнин и увлекает его в виде взвеси по трубе 21 в циклон 22. Труба 21 подходит к циклону по касательной, благодаря чему струя пара с лигнином, врываясь в циклон, движется вдоль стенок, совер — шая вращательное движение. Лигнин центробежной силой отбрасывается к боковым стенкам и, теряя скорость, падает на дно циклона. Освобожденный от лигнина пар через центральную трубу 23 выбрасывается в атмосферу.
Циклон 22 обычно представляет собой вертикальный сталь-‘ ной цилиндр объемом около 100 м3, снабженный боковой дверцей 31 и вращающейся мешалкой 25, которая помогает при выгрузке лигнина со дна циклона на ленточный или скребковый транспортер 24.
Для предохранения от коррозии внутренняя поверхность циклонов иногда защищается слоем кислотоупорного бетона Как уже указывалось выше, в процессе перколяции в верхний конус гидролизаппарата подается нагретая разбавленная серная кислота. Ее приготовляют путем смешивания в кислотоупорном смесителе 17 перегретой воды, подаваемой по трубе 28, с холодной концентрированной серной кислотой, поступающей из мерного бачка 19 через поршневой кислотный насос 18.
Поскольку холодная концентрированная серная кислота слабо корродирует железо и чугун, эти металлы широко используют для изготовления баков, насосов и трубопроводов, предназначенных для ее хранения и транспортировки к смесителю. Аналогичные материалы применяются и для подвода перегретой йоды к смесителю. Для защиты стенок смесителя от коррозии Применяют фосфористую бронзу, графит или пластическую массу — фторопласт 4. Последние два используются для внутренней футеровки смесителей и дают наилучшие результаты.
Готовый гндролизат из гидролизаппарата поступает в испаритель 6 высокого давления. Это — стальной сосуд, работающий под давлением и футерованный внутри керамическими плитками, как и гидролизаппарат. В верхней части испарителя емкостью 6-8 ж3 имеется крышка. В испарителе поддерживается давление на 4-5 атм ниже, чем в гидролизаппарате. Благодаря этому попадающий в него гидролизат мгновенно вскипает, частично испаряясь, и охлаждается до 130-140°. Образующийся пар отделяется от капель гидролизата и по трубе 10 поступает в решофер (теплообменник) 11, где конденсируется. Частично охлажденный гидролизат из испарителя 6 по трубе 7 поступает в испаритель 8 низкого давления, где охлаждается до 105-110° в результате вскипания при более низком давлении, обычно не превышающем одной атмосферы. Образующийся в этом испарителе пар по трубе 14 подается во второй решофер 13, где также конденсируется. Конденсаты из решоферов 11 и 13 содержат 0,2-0,3% фурфурола и используются для его выделения на специальных установках, которые будут рассмотрены ниже.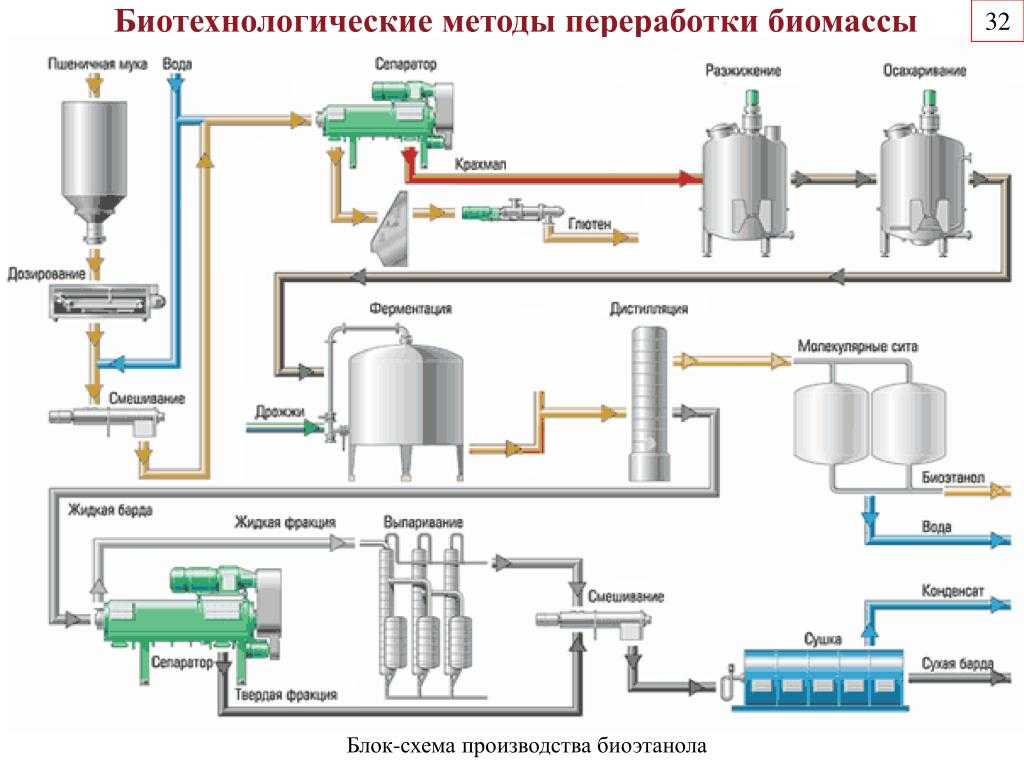
Тепло, содержащееся в паре, который выходит из испарителей 6 и 8, используется для нагрева воды, поступающей в смеситель 17. Для этой цели из бака 16 оборотной воды насосом 1Ь Теплую воду, полученную из ректификационного отделения гидролизного завода, подают в решофер низкого давления 13, где она нагревается с 60-80° до 100-110°. Затем по трубе 12 подогретая вода проходит решофер высокого давления 11, где паром при температуре 130-140° подогревается до 120-130°. Дальше температуру воды повышают до 180-200° в водогрейной колонне 27. Последняя представляет собой вертикальный стальной цилиндр с дном и верхней крышкой, рассчитанными на рабочее давление 13-15 атм.
Пар в водогрейную колонку подают по вертикальной трубе 26, на конце которой укреплены 30 горизонтальных дисков 2Ь. Пар из трубы 26 проходит через щели между отдельными дисками в колонну, заполненную водой. Последняя непрерывно подается в колонну через нижний штуцер, смешивается с паром, нагревается до заданной температуры и по трубе 28 поступает в смеситель 17.
Гидролизаппараты устанавливают на специальном фундаменте в ряд по 5-8 шт. На больших заводах число их удваивают и устанавливают их в два ряда. Трубопроводы для гидролизата изготовляют из красной меди или латуни. Арматура, состоящая из вентилей и клапанов, изготовляется из фосфористой или паспортной бронзы.
Описанный выше способ гидролиза является периодическим. В настоящее время испытываются новые конструкции гидролпз — аппаратов непрерывного действия, в которые при помощи специальных питателей непрерывно подается измельченная древесина, непрерывно удаляется лигнин и гидролизат.
Ведутся также работы по автоматизации гидролизаппаратов периодического действия. Это мероприятие позволяет более точно соблюдать заданный режим варки и одновременно облегчает труд варщиков.
Кислый гидролизат из испарителя низкого давления 8 (рис. 76) по трубе 9 подают в аппаратуру для его последующей переработки. Температура такого гидролизата 95-98°. В нем содержится (в %):
Серной кислоты. . . ……………………………………………………………………………………………….. 0,5 -0,7:
. . ……………………………………………………………………………………………….. 0,5 -0,7:
Гексоз (глюкоза, манноза, галактоза)………………………………………………………….. 2,5 -2,8;
Пентоз (ксилоза, арабиноза)…………………………………………………………………………. 0,8 -1,0;
Летучих органических кислот (муравьиная, уксусная) …………………………….. 0,24-0,30;
Нелетучих органических кислот (левулиновая) . . 0,2 -0,3;
Фурфурола………………………………………………………………………………………………………. 0,03-0,05;
Оксиметилфурфурола……………………………………………………………………………………. 0,13-0,16;
Метанола. ……………………………………………………………………………………………………….. 0,02-0,03
В гидролизатах присутствуют также коллоидные вещества (лигнин, декстрины), зольные вещества, терпены, смолы и т. д. Содержание моносахаридов в растительных гидролизатах при точных химических исследованиях устанавливают путем количественной бумажной хроматографии.
В заводских лабораториях при массовых экспрессных определениях Сахаров используется способность их в щелочной среде восстанавливать комплексные соединения окиси меди с образованием закиси меди:
2 Си (ОН)2 Си5 О + 2 Н2 О + 02.
По количеству образующейся закиси меди вычисляется со — i-фжание моносахаридов в растворе.
Такой метод определения Сахаров является условным, так Как одновременно с моносахаридами окись меди восстанавливают в закись также фурфурол, оксиметилфурфурол, декстрины, коллоидный лигнин. Эти примеси мешают определению истинного содержания сахара в гидролизатах. Общая ошибка здесь достигает 5-8%. Поскольку поправка на эти примеси требует большой затраты труда, ее обычно не делают, а полученные сахара в отличие от моносахаридов называют редуцирующими веществами или сокращено РВ. В заводских условиях учет количества вырабатываемого сахара в гидролизате учитывают в тоннах РВ.
Для получения этилового спирта гексозы (глюкоза, манноза и галактоза) сбраживают спиртообразующими дрожжами — сахаромицетами или шизосахаромицетами.
Суммарное уравнение спиртового брожения гексоз
C(i Hf, 06 — 2 С2 НГ) ОН + 2 С02 Гексоза этиловый спирт
Показывает, что при этом процессе теоретически на каждые 100 кг сахара должно получаться 51,14 кг, или около 64 л 100%-ного этилового спирта и около 49 кг углекислоты.
Таким образом, при спиртовом брожении гексоз получается почти в равных количествах два основных продукта: этанол и углекислота. Для осуществления этого процесса горячий кислый гидролизат должен быть подвергнут следующей обработке.:
1) нейтрализации; 2) освобождению от взвешенных твердых частиц; 3) охлаждению до 30°; 4) обогащению гидролизата необходимыми для жизнедеятельности дрожжей питательными веществами.
Кислый гидролизат имеет рН=1 -1,2. Среда, пригодная для брожения, должна иметь рН = 4,6-5,2. Чтобы придать гидро — лизату необходимую кислотность, содержащиеся в нем свободную серную и значительную часть органических кислот необходимо нейтрализовать. Если все кислоты, содержащиеся в гидролизате, условно выразить в серной кислоте, то ее концентрация составит около 1%. Остаточная кислотность гидролизата при рН = 4,6-5,2 составляет около 0,15%.
Поэтому для получения в гидролизате необходимой концентрации ионов водорода, в нем должно быть нейтрализовано 0,85% кислот. При этом полностью нейтрализуется свободная серная, муравьиная и часть уксусной. Остаются свободными левулиновая кислота и небольшая часть уксусной.
При этом полностью нейтрализуется свободная серная, муравьиная и часть уксусной. Остаются свободными левулиновая кислота и небольшая часть уксусной.
Нейтрализуют гидролизат известковым молоком, т. е. суспензией гидрата окиси кальция в воде с концентрацией 150-200 г СаО в литре.
Схема приготовления известкового молока представлена нм рис. 77.
Негашеную известь СаО непрерывно подают в загрузочную воронку вращающегося известегасительного барабана 34. Одновременно в барабан подают необходимое количество воды. При вращении барабана негашеная известь, связывая воду, переходит в гидрат окиси кальция. Последний диспергируется в воде, образуя суспензию. Не прореагировавшие куски извести отделяются в конце барабана от известкового молока и сбрасываются в вагонетку. Известковое молоко вместе с песком протекает по трубе в отделитель песка 35. Последний представляет собой горизонтально расположенное железное корыто с поперечными перегородками и продольным валом с лопастями.
Известковое молоко в этом аппарате медленно течет справа налево и далее по трубе 36 сливается в сборник 2.
Песок медленно оседает между перегородками отделителя песка и при помощи медленно вращающихся лопаток удаляется из аппарата. Перед поступлением известкового молока в нейтрализатор его смешивают с заданным количеством сернокислого аммония, раствор которого поступает из бачка 37. При смешении известкового молока с сернокислым аммонием протекает реакция
Са (ОН)3 + (Nh5)2 S04-> CaS04 + 2 NH, ОН, в результате которой часть извести связывается серной кислотой сернокислого аммония и образуются кристаллы плохо растворимого двухводного сернокислого кальция CaS04-2h30. Одновременно образуется аммиак, остающийся в известковом молоке в растворенном состоянии.
Присутствующие в известковом молоке мелкие кристаллы гипса при последующей нейтрализации являются центрами кристаллизации образующегося гипса и предохраняют от образования пересыщенных растворов его в нейтрализованном гидролизате. Это мероприятие имеет важное значение при последующей отгонке спирта из бражки, так как пересыщенные растворы гипса в бражке вызывают гипсацию бражных колонн и быстро выводят их из строя. Такой метод работы получил название нейтрализации с направленной кристаллизацией гипса.
Это мероприятие имеет важное значение при последующей отгонке спирта из бражки, так как пересыщенные растворы гипса в бражке вызывают гипсацию бражных колонн и быстро выводят их из строя. Такой метод работы получил название нейтрализации с направленной кристаллизацией гипса.
Одновременно с известковым молоком в нейтрализатор 5 Подаются слабокислый водный экстракт суперфосфата из мерника-бачка 38.
Соли даются в нейтрализатор из расчета 0,3 кг сернокислого аммония и 0,3 кг суперфосфата на 1 м3 гидролизата.
Нейтрализатор 5 (емкостью 35-40 м 3) представляет собой стальной бак, футерованный кислотоупорными керамическими плитками и снабженный вертикальными мешалками и тормозными лопатками, укрепленными неподвижно на стенках бака. Нейтрализация на гидролизных заводах ранее производилась периодически. В настоящее время она вытесняется более совершенной непрерывной нейтрализацией. На рис. 77 приведена последняя схема. Процесс осуществляется в двух последовательно соединенных нейтрализаторах 5 и 6, имеющих одинаковое устройство. Кислый гидролизат по трубе 1 непрерывно подается в первый нейтрализатор, куда одновременно поступают известковое молоко и питательные соли. Контроль за полнотой нейтрализации производят путем измерения концентрации ионов водорода при помощи потенциометра 3 с сурьмяным или стеклянным электродом 4. Потенциометр непрерывно записывает рН гидролизата и автоматически регулирует его в заданных пределах, посылая электрические импульсы реверсивному мотору, соединенному с запорной арматурой на трубе, подающей известковое молоко в первый нейтрализатор. В нейтрализаторах сравнительно быстро протекает реакция нейтрализации и относительно медленно — процесс кристаллизации гипса из пересыщенного раствора.
Процесс осуществляется в двух последовательно соединенных нейтрализаторах 5 и 6, имеющих одинаковое устройство. Кислый гидролизат по трубе 1 непрерывно подается в первый нейтрализатор, куда одновременно поступают известковое молоко и питательные соли. Контроль за полнотой нейтрализации производят путем измерения концентрации ионов водорода при помощи потенциометра 3 с сурьмяным или стеклянным электродом 4. Потенциометр непрерывно записывает рН гидролизата и автоматически регулирует его в заданных пределах, посылая электрические импульсы реверсивному мотору, соединенному с запорной арматурой на трубе, подающей известковое молоко в первый нейтрализатор. В нейтрализаторах сравнительно быстро протекает реакция нейтрализации и относительно медленно — процесс кристаллизации гипса из пересыщенного раствора.
Поэтому скорость протекания жидкости через нейтрализа — ционную установку обусловлена вторым процессом, требующим для своего окончания 30-40 мин.
По истечении этого времени нейтрализованный гидролизат, называемый «нейтрализатом», поступает в отстойник 7 полунепрерывного или непрерывного действия.
Полунепрерывный процесс состоит в том, что нейтрализат протекает через отстойник непрерывно, а оседающий на дно его гипс удаляется периодически, по мере накопления.
При непрерывной работе отстойника все операции производятся непрерывно. Перед спуском в канализацию шлам 8 в приемнике дополнительно промывается водой. Последний способ из-за некоторых производственных трудностей еще не получил широкого распространения.
Гипсовый шлам из отстойника обычно состоит наполовину из двухводного сернокислого кальция и наполовину из лигнина и гуминовых веществ, осевших из гидролизата. На некоторых гидролизных заводах гипсовый шлам обезвоживают, высушивают и обжигают, превращая в строительный алебастр. Обезвоживают на барабанных вакуум-фильтрах, а высушивают и обжигают во вращающихся барабанных печах, обогреваемых топочными газами.
Нейтрализат, освобожденный от взвешенных частиц, перед брожением охлаждается в холодильнике 10 (рис. 77) с 85 до 30°. Для этой цели обычно применяются спиральные или пластинчатые теплообменники, отличающиеся высоким коэффициентом теплопередачи и небольшими габаритами. При охлаждении из нейтрализата выделяются смолообразные вещества, которые оседают на стенках теплообменников и постепенно загрязняют их. Для чистки теплообменники периодически отключают и промывают 2-4%-ным горячим водным раствором едкого натра, который растворяет смолообразные и гуминовые вещества.
При охлаждении из нейтрализата выделяются смолообразные вещества, которые оседают на стенках теплообменников и постепенно загрязняют их. Для чистки теплообменники периодически отключают и промывают 2-4%-ным горячим водным раствором едкого натра, который растворяет смолообразные и гуминовые вещества.
Нейтрализованный, очищенный и охлажденный гидролизат.
Сбраживают древесное сусло специальными акклиматизированными в этой среде спнртообразующими дрожжами. Брожение идет по непрерывному методу в батарее последовательно соединенных бродильных чанов 11 и 12.
Дрожжевая суспензия, содержащая около 80-100 г прессованных дрожжей в литре, подается непрерывным потоком по трубе 15 в дрожжанку 44 и затем в верхнюю часть первого, или головного, бродильного чана 11. В дрожжанку одновременно’ с дрожжевой суспензией подается охлажденное древесное сусло. На каждый кубометр дрожжевой суспензии в бродильный чан поступает 8-10 м3 сусла.
Дрожжинки, содержащиеся в среде гексозных Сахаров, при помощи системы ферментов расщепляют сахара, образуя этиловый спирт и углекислоту. Этиловый спирт переходит в окружающую жидкость, а углекислый газ выделяется на поверхности дрожжинок в виде маленьких пузырьков, которые постепенно’ увеличиваются в объеме, затем постепенно всплывают на поверхность чана, увлекая приставшие к ним дрожжинки.
Этиловый спирт переходит в окружающую жидкость, а углекислый газ выделяется на поверхности дрожжинок в виде маленьких пузырьков, которые постепенно’ увеличиваются в объеме, затем постепенно всплывают на поверхность чана, увлекая приставшие к ним дрожжинки.
При соприкосновении с поверхностью пузырьки углекислоты лопаются, а дрожжинки, имеющие удельный вес 1,1, т. е. больший, чем у сусла (1,025), опускаются вниз, пока снова не будут подняты углекислотой на поверхность. Непрерывное движение дрожжинок вверх и вниз способствует перемещению потоков жидкости в бродильном чане, создавая перемешивание или «брожение» жидкости. Выделяющаяся на поверхности жидкости углекислота из бродильных чанов по трубе 13 поступает на установку для получения жидкой или твердой углекислоты, используется для получения химических продуктов (например, мочевины) или выпускается в атмосферу.
Частично сброженное древесное сусло вместе с дрожжами передается из головного бродильного чана в хвостовой чан 12, Где брожение и заканчивается. Поскольку концентрация сахарз в хвостовом чане небольшая, брожение в нем идет менее интенсивно, и часть дрожжей, не успевая образовать пузырьки углекислоты, оседает на дно чана. Чтобы не допустить этого, в хвостовом чане устраивают часто принудительное перемешивание жидкости мешалками или центробежными насосами .
Поскольку концентрация сахарз в хвостовом чане небольшая, брожение в нем идет менее интенсивно, и часть дрожжей, не успевая образовать пузырьки углекислоты, оседает на дно чана. Чтобы не допустить этого, в хвостовом чане устраивают часто принудительное перемешивание жидкости мешалками или центробежными насосами .
Бродящая или сброженная жидкость называется бражкой. По окончании брожения бражка передается в сепаратор 14, работающий по принципу центрифуги. Попадающая в него бражка вместе со взвешенными в ней дрожжами начинает вращаться со скоростью 4500-6000 оборотов в минуту. Центробежная сила вследствие разности удельных весов бражки и дрожжей разделяет их. Сепаратор делит жидкость на два потока: больший, не содержащий дрожжей, поступает в воронку 16 и меньший, содержащий дрожжи, поступает через воронку в трубу 15. Обычно первый поток в 8-10 раз больше, чем второй. По трубе 15 дрожжевая суспензия возвращается в головной бродильный чан 11 Через дрожжанку 44. Сброшенное и освобожденное от дрожжей сусло собирается в промежуточном сборнике бражки 17.
Сброшенное и освобожденное от дрожжей сусло собирается в промежуточном сборнике бражки 17.
При помощи сепараторов дрожжи постоянно циркулируют в замкнутой системе бродильной установки. Производительность сепараторов 10-35 м3/час.
Во время брожения и особенно при сепарации часть содержащихся в древесном сусле гуминовых коллоидов коагулируется, образуя тяжелые хлопья, медленно оседающие на дно бродильных чанов. В днищах чанов устроены штуцеры, через которые осадок периодически спускается в канализацию.
Как уже указывалось выше, теоретический выход спирта из 100 кг сброженных гексоз составляет 64 л. Однако практически вследствие образования за счет Сахаров побочных продуктов (глицерин, уксусный альдегид, янтарная кислота и т. д.), а также из-за присутствия в сусле вредных для дрожжей примесей выход спирта составляет 54-56 л.
Для получения хороших выходов спирта необходимо все время дрожжи поддерживать в активном состоянии. Для этого следует тщательно выдерживать заданную температуру брожения, концентрацию водородных ионов, необходимую чистоту сусла и оставлять в бражке перед поступлением ее на сепаратор небольшое количество гексоз, так называемый «недоброд» (обычно не более 0,1 %’ сахара в растворе). Благодаря наличию недоброда дрожжи все время остаются в активной форме.
Для этого следует тщательно выдерживать заданную температуру брожения, концентрацию водородных ионов, необходимую чистоту сусла и оставлять в бражке перед поступлением ее на сепаратор небольшое количество гексоз, так называемый «недоброд» (обычно не более 0,1 %’ сахара в растворе). Благодаря наличию недоброда дрожжи все время остаются в активной форме.
Периодически гидролизный завод останавливают на планово — предупредительный или капитальный ремонт. В это время дрожжи следует сохранять в живом виде. Для этого суспензию дрожжей при помощи сепараторов сгущают и заливают холодным древесным суслом. При низкой температуре брожение резко замедляется и дрожжи потребляют значительно меньше сахара.
Бродильные чаны емкостью 100-200 м3 обычно изготовляются из листовой стали или, реже, из железобетона. Продолжительность брожения зависит от концентрации дрожжей и составляет от 6 до 10 часов. Необходимо следить за чистотой производственной культуры дрожжей и предохранять ее от инфицирования посторонними вредными микроорганизмами. Для этой цели все оборудование необходимо содержать в чистоте и периодически подвергать стерилизации. Наиболее простым способом стерилизации является пропарка всего оборудования и особенно трубопроводов и насосов острым паром.
Для этой цели все оборудование необходимо содержать в чистоте и периодически подвергать стерилизации. Наиболее простым способом стерилизации является пропарка всего оборудования и особенно трубопроводов и насосов острым паром.
По окончании брожения и отделения дрожжей спиртовая бражка содержит от 1,2 до 1,6% этилового спирта и около 1% пентозных Сахаров.
Выделяют спирт из бражки, очищают и укрепляют его в трехколонном брагоректификационном аппарате, состоящем из браж — ной 18, ректификационной 22 и метанольной 28 колонн (рис.77).
Бражка из сборника 17 насосом подается через теплообменник 41 на питающую тарелку бражной колонны 18. Стекая по тарелкам исчерпывающей части бражной колонны вниз, бражка встречает на своем пути поднимающийся вверх пар. Последний, постепенно обогащаясь спиртом, переходит в верхнюю, укрепляющую часть колонны. Стекающая вниз бражка постепенно освобождается от спирта, а затем из кубовой царги колонны 18 по трубе 21 переходит в теплообменник 41, где нагревает поступающую в колонну бражку до 60-70е. Дальше бражку нагревают до 105° в колонне острым паром, поступающим по трубе 20. Освобожденная от спирта бражка называется «бардой». По трубе 42 Барда выходит из бардяного теплообменника 41 и направляется в дрожжевой цех для получения из пентоз кормовых дрожжей. Этот процесс в дальнейшем будет подробно рассмотрен.
Дальше бражку нагревают до 105° в колонне острым паром, поступающим по трубе 20. Освобожденная от спирта бражка называется «бардой». По трубе 42 Барда выходит из бардяного теплообменника 41 и направляется в дрожжевой цех для получения из пентоз кормовых дрожжей. Этот процесс в дальнейшем будет подробно рассмотрен.
Бражная колонна в верхней укрепляющей части заканчивается дефлегматором 19, в котором конденсируются пары ьод — носпиртовой смеси, поступающие с верхней тарелки колонны.
В 1 м3 бражки при температуре 30° растворяется около 1 мъ углекислого газа, образовавшегося при брожении. При нагревании бражки в теплообменнике 41 и острым паром в нижней части бражной колонны растворенная углекислота выделяется и вместе с парами спирта поднимается в укрепляющую часть колонны и далее в дефлегматор 19. Неконденсирующиеся газы отделяются через воздушники, установленные на трубопроводах спиртового конденсата после холодильников. Низкокипящие фракции, состоящие из спирта, альдегидов и эфиров, проходят через дефлегматор 19 и окончательно конденсируются в холодильнике 39у Откуда в виде флегмы стекают обратно в колонну через гидрозатвор 40. Неконденсирующиеся газы, состоящие из углекислого газа, перед выходом из холодильника 39 проходят дополнительный конденсатор или промываются в скруббере водой для улавливания последних остатков спиртовых паров.
Неконденсирующиеся газы, состоящие из углекислого газа, перед выходом из холодильника 39 проходят дополнительный конденсатор или промываются в скруббере водой для улавливания последних остатков спиртовых паров.
На верхних тарелках бражной колонны в жидкой фазе содержится 20-40% спирта.
Конденсат по трубе 25 поступает на питающую тарелку ректификационной колонны 22. Эта колонна работает аналогично бражной колонне, но на более высоких концентрациях спирта. В нижнюю часть этой колонны по трубе 24 подается острый пар, который постепенно вываривает спирт из спиртового конденсата, стекающего в низ колонны. Освобожденная от спирта жидкость, называемая лютером, по трубе 23 уходит в канализацию. Содержание спирта в барде и лютере составляет не более 0,02%.
Над верхней тарелкой ректификационной колонны устанавливается дефлегматор 26. Не сконденсировавшиеся в нем пары окончательно конденсируются в конденсаторе 26а и стекают обратно в колонну. Часть низкокипящих фракций отбирается по трубе 43 в виде эфироальдегидной фракции, которая возвращается в бродильные чаны, если она не имеет применения.
Часть низкокипящих фракций отбирается по трубе 43 в виде эфироальдегидной фракции, которая возвращается в бродильные чаны, если она не имеет применения.
Для освобождения этилового спирта от летучих органических кислот в колонну подается из бака 45 10%-ный раствор едкого натра, который нейтрализует кислоты на средних тарелках укрепляющей части колонны. В средней части ректификационной колонны, где крепость спирта составляет 45-50%, накапливаются сивушные масла, которые отбираются по трубе 46. Сивушные масла представляют собой смесь высших спиртов (бутиловый, пропиловый, амиловый), образовавшихся из аминокислот.
Этиловый спирт, освобожденный от эфиров и альдегидов, а также сивушных масел, отбирается при помощи гребенки с верхних тарелок укрепляющей части ректификационной колонны и по трубе 27 поступает на питающую тарелку метанольной колонны 28. Спирт-сырец, поступающий из ректификационной колонны, содержит около 0,7% метилового спирта, который образовался при гидролизе растительного сырья и вместе с моносахаридами попал в древесное сусло.
При брожении гексоз метиловый спирт не образуется. По техническим условиям на этиловый спирт, вырабатываемый гидролизными заводами, в нем должно содержаться не более 0,1% метилового спирта. Исследования показали, что легче всего метиловый спирт отделяется из спирта-сырца при минимальном содержании в нем воды. По этой причине в метанольную колонну подают спирт-сырец с максимальной крепостью (94-96% этанола). Выше 96%’ этиловый спирт получить на обычных ректификационных колоннах нельзя, так как этой концентрации отвечает состав нераздельнокипящей водоспиртовой смеси.
В метанольной колонне легкокипящей фракцией является метанол, который поднимается в верхнюю часть колонны, укрепляется в дефлегматоре 29 и по трубе 30 сливается в сборники метанольной фракции, содержащей около 80% метанола. Для выпуска товарного 100%-ного метанола устанавливается вторая метанольная колонна, не показанная на рис. 77.
Этиловый спирт, стекая по тарелкам, опускается в нижнюю часть метанольной колонны 28 и по трубе 33 сливается в приемники готовой продукции . Обогревают метанольную колонну глухим паром в выносном подогревателе 31, который установлен таким образом, что по принципу сообщающихся сосудов его межтрубное пространство залито спиртом. Поступающий в подогреватель водяной пар нагревает спирт до кипения и образующиеся спиртовые пары идут на обогрев колонны. Пар, поступающий в подогреватель 31, конденсируется в нем и в виде конденсата подается в сборники чистой воды или сливается в канализацию.
Обогревают метанольную колонну глухим паром в выносном подогревателе 31, который установлен таким образом, что по принципу сообщающихся сосудов его межтрубное пространство залито спиртом. Поступающий в подогреватель водяной пар нагревает спирт до кипения и образующиеся спиртовые пары идут на обогрев колонны. Пар, поступающий в подогреватель 31, конденсируется в нем и в виде конденсата подается в сборники чистой воды или сливается в канализацию.
Количество и крепость полученного этилового спирта измеряют в специальной аппаратуре (фонарь, контрольный снаряд, мерник спирта). Из мерника паровым насосом этиловый спирт подают за пределы главного корпуса — в стационарные цистерны, располженные в складе спирта. Из этих цистерн по мере необходимости товарный этиловый спирт переливают в железнодорожные цистерны, в которых отвозят его к местам потребления.
Описанный выше технологический процесс дает возможность получать из 1 т абсолютно сухой хвойной древесины 150-180 л 100%-ного этилового спирта. При этом на 1 дкл спирта расхо
При этом на 1 дкл спирта расхо
Абсолютно сухой древесины в кг. . . . . 55-66;
TOC o «1-3» h z серной кислоты — моаоидрата в кг … . 4,5;
Извести негашеной, 85%-ной в кг …………………………………………………. 4,3;
Пара технологического 3- и 16-атмосферного
В мегакалориях. ………………………………………………………………………….. 0,17-0,26;
Воды в м3……………………………………………………………………………………………. 3,6;
Элекгрознер в квт-ч. …………………………………………………………………….. 4,18
Годовая производительность гидролизно-спиртового завода средней мощности по спирту составляет 1 -1,5 млн. дал. На этих заводах основным продуктом является этиловый спирт. Как уже указывалось, одновременно с ним из отходов основного производства на гидролизно-спиртовом заводе вырабатывается твердая или жидкая углекислота, фурфурол, кормовые дрожжи, продукты переработки лигнина. Эти производства будут рассмотрены в дальнейшем.
На некоторых гидролизных заводах, получающих в качестве основного продукта фурфурол или ксилит, после гидролиза богатых пентозами гемицеллюлоз остается трудногидролизуемый остаток, состоящий из целлюлозы и лигнина и носящий название целлолигнина.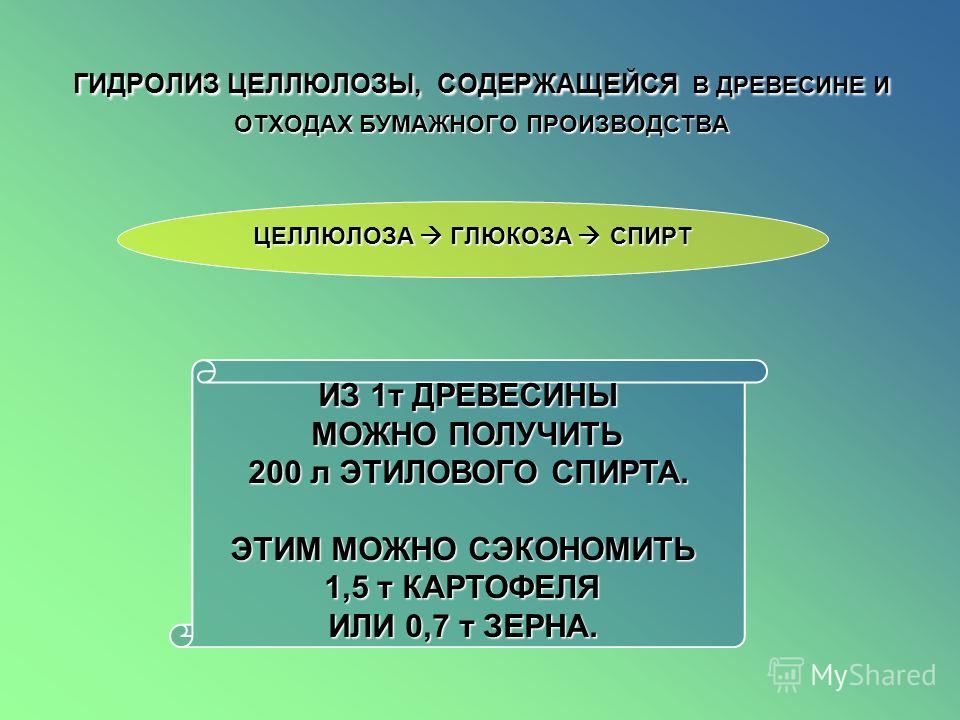
Целлолигнин может быть гидролизован перколяционным методом, как описано выше, и полученный гексозный гидролизат, обычно содержащий 2-2,5% Сахаров, может быть переработан по описанной выше методике в технический этиловый спирт или кормовые дрожжи. По этой схеме перерабатывается хлопковая шелуха, кукурузная кочерыжка, дубовая одубина, подсолнечная лузга и т. д. Такой производственный процесс является экономически выгодным только при дешевом сырье и топливе.
На гидролизно-спиртовых заводах обычно получается технический этиловый спирт, используемый для последующей химической переработки. Однако в случае необходимости этот спирт
сравнительно легко очищается путем дополнительной ректификации и окисления щелочным раствором перманганата. После такой очистки этиловый спирт вполне пригоден для пищевых целей.
способы получения. Производство этилового спирта из древесины Метиловый спирт из опилок
Общая схема получения этилового спирта из гидролизной «черной патоки» такова. Сырье в измельченном виде загружают в многометровую стальную гидролизную колонну, изнутри облицованную химически стойкой керамикой. Туда подают под давлением горячий раствор соляной кислоты. В результате химической реакции из целлюлозы получается продукт, содержащий сахар, так называемая «черная патока». Этот продукт нейтрализуют известью и туда добавляют дрожжи — сбраживают патоку. После чего опять нагревают, и выделяющиеся пары конденсируются в виде этилового спирта (называть его «винным», не хочется).
Сырье в измельченном виде загружают в многометровую стальную гидролизную колонну, изнутри облицованную химически стойкой керамикой. Туда подают под давлением горячий раствор соляной кислоты. В результате химической реакции из целлюлозы получается продукт, содержащий сахар, так называемая «черная патока». Этот продукт нейтрализуют известью и туда добавляют дрожжи — сбраживают патоку. После чего опять нагревают, и выделяющиеся пары конденсируются в виде этилового спирта (называть его «винным», не хочется).
Гидролизный способ — самый экономный способ производства этилового спирта. Если традиционным биохимическим способом сбраживания из одной тонны зерна можно получить 50 литров спирта, то из одной тонны древесных опилок, гидролизным способом преобразованных в «черную патоку», выгоняется 200 литров спирта. Как говориться: «Почувствуйте выгоду!» Весь вопрос, можно ли «черную патоку» как осаха-ренную целлюлозу называть «пищевым продуктом», наравне с зерном, картофелем и свеклой. Лица, заинтересованные в производстве дешевого этилового спирта, считают так: « А чё, почему нельзя? Ведь барда, как остаток «черной патоки», после ее перегонки идет на корм скоту, значит, она тоже пищевой продукт». Как тут не вспомнить слова Ф.М.Достоевского: «Образованный человек, когда это ему нужно, может словесно оправдать любую мерзость».
Как тут не вспомнить слова Ф.М.Достоевского: «Образованный человек, когда это ему нужно, может словесно оправдать любую мерзость».
В 30-х годах прошлого века в осетинском поселке Беслан был построен крупнейший в Европе крахмалопа-точный комбинат, который с тех пор выпускает миллионы литров этилового спирта. Потом мощные заводы по производству этилового спирта были построены по всей стране, в том числе при Соликамском и Архангельском целлюлозо-бумажных комбинатах. И.В. Сталин, поздравляя строителей гидролизных заводов, которые во время войны, несмотря на трудности военного времени, досрочно ввели их в эксплуатацию, отметил, что это «дает возможность сэкономить государству миллионы пудов хлеба» (Газета «Правда» от 27 мая 1944 г.).
Этиловый спирт, полученный из «черной патоки», а, по сути, из древесины (целлюлозы), осахаренной гидролизным способом, если, конечно, он хорошо очищен, не отличить от спирта, полученного из зерна или картофеля. По действующим стандартам такой спирт бывает «высшей очистки», «экстра» и «люкс», последний — самый лучший, то есть имеет самую высокую степень очистки. Водкой, приготовленной на основе такого спирта, не отравишься. На вкус такой спирт нейтрален, то есть «никакой» — безвкусный, в нем лишь одни «градусы», он только обжигает слизистую оболочку рта. Внешне распознать водку, сделанную на основе этилового спирта гидролизного происхождения, довольно трудно, а различные ароматизаторы, добавляемые к таким «водкам», придают им некоторое отличие друг от друга.
Водкой, приготовленной на основе такого спирта, не отравишься. На вкус такой спирт нейтрален, то есть «никакой» — безвкусный, в нем лишь одни «градусы», он только обжигает слизистую оболочку рта. Внешне распознать водку, сделанную на основе этилового спирта гидролизного происхождения, довольно трудно, а различные ароматизаторы, добавляемые к таким «водкам», придают им некоторое отличие друг от друга.
Однако не все так хорошо, как кажется на первый взгляд. Генетики провели исследования: одной партии подопытных мышей в рацион добавляли настоящую (зерновую) водку, другой — гидролизную, из древесины. Мыши, которые употребляли «сучок» умирали гораздо быстрее, а их потомство вырождалось. Но результаты этих исследований не остановили выпуск псевдорусских водок. Это как в популярной песне: «Ведь если водку гнать не из опилок, то что б нам было с пяти бутылок…»
Как из опилок получать спирт либо другое жидкое топливо?
- в германии в конце 2мир.войны все танки ездили на синтетич.
 топливе из опилок. а на спирте машины в Бразилии очень даже ездят, 20% машин там на спирту. так что и правда, можно воспользоваться брожением, перегнать и получить спирт и будет вам авто
топливе из опилок. а на спирте машины в Бразилии очень даже ездят, 20% машин там на спирту. так что и правда, можно воспользоваться брожением, перегнать и получить спирт и будет вам авто
может быть можно и метан с помощью бактерий получить? тогда еще лучше - Поделюсь опытом, так и быть! Вообщем, берешь 1КГ. опилок древесных или др. очень тчательно сушишь, затем добавляешь в колбу или еще что-то через холодильник (там будет возгонка) электролит (серную кислоту) 1/3 объема.. Советую, в Лабтехе купить холодильник 450 и не париться. нагреваешь, дотемпературы 150 градусов, и получаешь Метиловый Спирт, и там же его эфиры и др. ГОРЮЧИИ продукты реакции. жидкость может быть разных цветов. но обычно голубоватая, легколетучая. Да, будешь готовить не забудь добавить кусочки Корунда(оксид алюминия) ,- это катализатор. как только, жидкость в сосуде или колбе почернеет, до не узнаваемости, меняй и заливай следующию порцию. с 1 кг получишь где-то 470мл. спирта, а всего 700 с чем-то. Делай это в открытой местности, хорошо проветриваемой и в дали от еды.
 Да, маску и респиратор не забудь. Черную (отработавшую) жидкость процеди, и верхний слой после просушки очень хорошо горит. это тоже добавь в топливо.
Да, маску и респиратор не забудь. Черную (отработавшую) жидкость процеди, и верхний слой после просушки очень хорошо горит. это тоже добавь в топливо. - Из хвойных пород — плохо. Обычно гидролизный спирт получают из лиственных. Здесь, собственно, два варианта и оба практически не реализуемые в домашних условиях. А водка-табуретовка по большому счту — шутка, так как производство неэффективно и употребление конечного продукта может быть опасно для здоровья. Первый вариант. Надо сложить опилки в достаточно большую кучу на улице, намочить водой и оставить на пару лет (именно два года или больше). В центре кучи поселятся анаэробные микроорганизмы, которые будут постепенно осуществлять распад целлюлозы до мономеров (сахаров), которые уже можно сбродить. Далее — как обычный самогон. Или второй вариант, который реализуется в промышленности. Опилки варят со слабым раствором серной кислоты при повышенном давлении. В этом случае гидролиз целлюлозы осуществляется за несколько часов. Далее — перегонка как обычно.

Если рассматривать не только этиловый спирт, то можно пойти другим путм, но он, опять же, практически не реализуем в домашних условиях. Это — сухая перегонка опилок. Сырь необходимо нагреть в герметичной мкости до 800-900 град. и собирать выходящие газы. При охлаждении этих газов конденсируется креозот (основной продукт), метанол и уксусная кислота. Газы — смесь разнообразных углеводородов. Остаток- древесный уголь. Именно такой уголь в промышленности называют древесным, а не из костра. Он раньше применялся в металлургии вместо кокса. После его дополнительной обработки получают активированный уголь. Креозот — смола, которой смолят шпалы и телеграфные столбы. Газ можно использовать как обычный природный. Теперь жидкости. Метиловый, или древесный, спирт, отгоняют из жидкости при температуре до 75 град. Может сойти за топливо, но выход мал и он очень ядовит. Далее уксусная кислота. При е нейтрализации известью получается ацетат кальция, или, как раньше его называли, серый древесноуксусный порошок. При его прокаливании получается ацетон — чем не топливо? Правда, сейчас ацетон получают полностью синтетическим путм.
При его прокаливании получается ацетон — чем не топливо? Правда, сейчас ацетон получают полностью синтетическим путм.
Вроде ничего не забыл. Ну что, когда открываем креозотовую лавку? - «А если б водку гнать не из опилок, то че б нам было, с пяти бутылок?» (В.С. Высоцкий)
- сбраживание сахаристых веществ. например целлюлоза. только для ускорения нужен фермент-дрожжи. а по-поводу метилового спирта….ну вообщето при малых дозах, он смертельно опасен.
- Возгонкой.
- Надо целюлозу перебродить, потом перегнать
Сибирские ученые работают над технологией производства отечественного биоэтанола
В советское время, кто еще помнит, много шутили на тему спирта, приготовленного из опилок. Ходили слухи, будто после войны дешевую водку делали как раз на основе «опилочного» алкоголя. В народе этот напиток получил название – «сучок».
Вообще, разговоры о производстве спирта из опилок возникли, конечно же, не на пустом месте. Такой продукт действительно производился. Назывался он «гидролизным спиртом». Сырьем для его производства действительно были опилки, точнее – целлюлоза, извлекаемая из отходов лесной промышленности. Выражаясь строго научно – из непищевого растительного сырья. По приблизительным расчетам, из 1 тонны древесины можно было получить около 200 литров этилового спирта. Это будто бы позволяло заменить 1,5 тонны картофеля или 0,7 тонн зерна. Применялся ли такой спирт на советских лекеро-водочных заводах, неизвестно. Производился он, понятное дело, для сугубо технических целей.
Такой продукт действительно производился. Назывался он «гидролизным спиртом». Сырьем для его производства действительно были опилки, точнее – целлюлоза, извлекаемая из отходов лесной промышленности. Выражаясь строго научно – из непищевого растительного сырья. По приблизительным расчетам, из 1 тонны древесины можно было получить около 200 литров этилового спирта. Это будто бы позволяло заменить 1,5 тонны картофеля или 0,7 тонн зерна. Применялся ли такой спирт на советских лекеро-водочных заводах, неизвестно. Производился он, понятное дело, для сугубо технических целей.
Надо сказать, что производство технического этанола из органических отходов уже давно будоражит воображение ученых. Можно найти литературу XIX века, где обсуждаются возможности получения спирта из самого разнообразного сырья, в том числе и непищевого. В XX веке эта тема зазвучала с новой силой. В 1920-го годы ученые в Советской России даже предлагали делать спирт из… фекалий! Было даже шутливое стихотворение Демьяна Бедного:
Ну настали времена,
Что ни день, то чудо:
Водку гонят из говна –
По три литра с пуда!
Русский ум изобретет
В зависть всей Европы —
Скоро водка потечет
В рот из самой жопы…
Впрочем, идея с фекалиями так и осталась на уровне шутки. А вот к целлюлозе отнеслись серьезно. Помните, в «Золотом теленке» Остап Бендер рассказывает иностранцам о рецепте «табуреточного самогона». Дело в том, что с целлюлозой «химичили» уже тогда. Причем, надо заметить, извлекать ее можно не только из отходов лесной промышленности. Отечественное сельское хозяйство ежегодно оставляет огромные горы соломы – это тоже прекрасный источник целлюлозы. Не пропадать же добру. Солома – источник возобновляемый, можно сказать – даровой.
А вот к целлюлозе отнеслись серьезно. Помните, в «Золотом теленке» Остап Бендер рассказывает иностранцам о рецепте «табуреточного самогона». Дело в том, что с целлюлозой «химичили» уже тогда. Причем, надо заметить, извлекать ее можно не только из отходов лесной промышленности. Отечественное сельское хозяйство ежегодно оставляет огромные горы соломы – это тоже прекрасный источник целлюлозы. Не пропадать же добру. Солома – источник возобновляемый, можно сказать – даровой.
Есть только в этом деле одна загвоздка. Помимо нужной и полезной целлюлозы в одревесневших частях растений (а таковыми, в том числе, является и солома) содержится лигнин, который усложняет весь процесс. Из-за наличия в растворе этого самого лигнина практически невозможно получить нормальную «бражку», поскольку сырье не осахаривается. Лигнин тормозит развитие микроорганизмов. По этой причине требуется «подкормка» — добавление нормального пищевого сырья. Чаще всего в этой роли выступает мука, крахмал или патока.
От лигнина, конечно же, можно избавиться. В целлюлозо-бумажной промышленности это традиционно делается химическим путем, например, с помощью обработки кислотой. Вопрос только в том, куда его потом девать? В принципе, из лигнина можно получить неплохое твердое топливо. Горит он хорошо. Так, в Институте теплофизики СО РАН даже разработали соответствующую технологию сжигания лигнина. Но, к сожалению, тот лигнин, что остается от нашего целлюлозо-бумажного производства, в качестве топлива непригоден из-за содержащейся в нем серы (последствия химической обработки). Если его сжигать – получим кислотные дожди.
В целлюлозо-бумажной промышленности это традиционно делается химическим путем, например, с помощью обработки кислотой. Вопрос только в том, куда его потом девать? В принципе, из лигнина можно получить неплохое твердое топливо. Горит он хорошо. Так, в Институте теплофизики СО РАН даже разработали соответствующую технологию сжигания лигнина. Но, к сожалению, тот лигнин, что остается от нашего целлюлозо-бумажного производства, в качестве топлива непригоден из-за содержащейся в нем серы (последствия химической обработки). Если его сжигать – получим кислотные дожди.
Есть и другие способы – обрабатывать сырье перегретым паром (лигнин при высоких температурах плавится), проводить экстракцию органическими растворителями. Кое-где именно так и делают, однако эти способы очень затратные. В условиях плановой экономики, где все затраты брало на себя государство, можно было работать и таким способом. Однако в условиях рыночной экономики получается так, что овчинка, образно говоря, не стоит выделки. И при сопоставлении затрат выходит, что куда дешевле обходится производство технического спирта (по-современному – биоэтанола) из традиционного пищевого сырья. Все зависит от того, в каких количествах вы располагаете таким сырьем. У американцев, например, имеет место перепроизводство кукурузы. Куда проще и выгоднее излишки пустить на производство спирта, чем транспортировать ее на другой континент. В Бразилии, как мы знаем, излишки сахарного тростника также используются в качестве сырья для производства биоэтанола. В принципе, в мире не так уж мало стран, где спирт заливают не только в желудок, но и в бак автомобиля. И все было бы неплохо, если бы некоторые известные мировые деятели (в частности, кубинский лидер Фидель Кастро), не выступили против такого «несправедливого» использования сельхозпродукции в условиях, когда в некоторых странах люди страдают от недоедания, а то и вообще умирают с голоду.
И при сопоставлении затрат выходит, что куда дешевле обходится производство технического спирта (по-современному – биоэтанола) из традиционного пищевого сырья. Все зависит от того, в каких количествах вы располагаете таким сырьем. У американцев, например, имеет место перепроизводство кукурузы. Куда проще и выгоднее излишки пустить на производство спирта, чем транспортировать ее на другой континент. В Бразилии, как мы знаем, излишки сахарного тростника также используются в качестве сырья для производства биоэтанола. В принципе, в мире не так уж мало стран, где спирт заливают не только в желудок, но и в бак автомобиля. И все было бы неплохо, если бы некоторые известные мировые деятели (в частности, кубинский лидер Фидель Кастро), не выступили против такого «несправедливого» использования сельхозпродукции в условиях, когда в некоторых странах люди страдают от недоедания, а то и вообще умирают с голоду.
В общем, идя навстречу филантропическим пожеланиям, ученые, работающие в сфере производства биоэтанола, должны искать какие-то более рациональные, более совершенные технологии переработки непищевого сырья. Примерно десять лет назад специалисты Института химии твердого тела и механохимии СО РАН решили пойти другим путем – использовать для этих целей механохимический способ. Вместо известной химической обработки сырья или нагревания они стали применять особую механическую обработку. Для чего были сконструированы специальные мельницы и активаторы. Суть метода такова. Благодаря механической активации целлюлоза переходит из кристаллического состояния в аморфное. Это облегчает работу ферментов. Но главное здесь то, что сырье в процессе механической обработки разделяется на различные частички – с разным (большим или меньшим) содержанием лигнина. Потом уже – благодаря разным аэродинамическим характеристикам этих частичек – их легко отделить друг от друга с помощью специальных установок.
Примерно десять лет назад специалисты Института химии твердого тела и механохимии СО РАН решили пойти другим путем – использовать для этих целей механохимический способ. Вместо известной химической обработки сырья или нагревания они стали применять особую механическую обработку. Для чего были сконструированы специальные мельницы и активаторы. Суть метода такова. Благодаря механической активации целлюлоза переходит из кристаллического состояния в аморфное. Это облегчает работу ферментов. Но главное здесь то, что сырье в процессе механической обработки разделяется на различные частички – с разным (большим или меньшим) содержанием лигнина. Потом уже – благодаря разным аэродинамическим характеристикам этих частичек – их легко отделить друг от друга с помощью специальных установок.
На первый взгляд, все очень просто: размололи – и дело с концом. Но только на первый взгляд. Если бы действительно все было так просто, то уже во всех странах мололи бы солому и прочие растительные отходы. На самом деле здесь необходимо найти правильную интенсивность, чтобы сырье разделилось на отдельные ткани. В противном случае у вас получится однообразная масса. Задача ученых – как раз найти здесь необходимый оптимум. И оптимум этот, как показывает практика, достаточно узкий. Можно и перестараться. В том-то, надо сказать, и заключается работа ученого, чтобы выявить золотую середину. Причем, здесь необходимо учитывать и экономические аспекты – а именно, отработать технологию так, чтобы затраты на механихимическую обработку исходного сырья (каким бы дешевым оно ни было) не сказались на себестоимости производства.
На самом деле здесь необходимо найти правильную интенсивность, чтобы сырье разделилось на отдельные ткани. В противном случае у вас получится однообразная масса. Задача ученых – как раз найти здесь необходимый оптимум. И оптимум этот, как показывает практика, достаточно узкий. Можно и перестараться. В том-то, надо сказать, и заключается работа ученого, чтобы выявить золотую середину. Причем, здесь необходимо учитывать и экономические аспекты – а именно, отработать технологию так, чтобы затраты на механихимическую обработку исходного сырья (каким бы дешевым оно ни было) не сказались на себестоимости производства.
В лабораторных условиях уже получены десятки литров замечательного спирта. Самым впечатляющим выглядит тот момент, что спирт получен из обычной соломы. Причем – без применения кислоты, щелочей и перегретого пара. Главное подспорье тут – «чудо-мельницы», сконструированные спецами Института. В принципе, уже ничто не мешает перейти и к промышленным образцам. Но это уже – другая тема.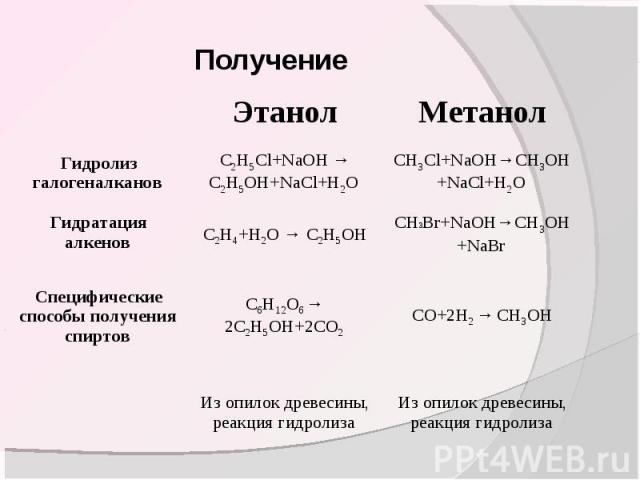
Вот он — первый отечественный биоэтанол из соломы! Пока еще в бутылях. Дождемся ли, когда его начнут производить цистернами?
Статьи Рисунки Таблицы О сайте English
Ранее метанол получали при сухой перегонке дерева (отсюда его название древесный спирт). Он применяется как растворитель и для различных органических синтезов — получение формальдегида, некоторых красителей, фотореактивов, фармацевтических препаратов.
В гидролизном спирте, полученном из древесных опилок, может быть примесь метилового спирта. Эта примесь недопустима, так как метиловый спирт очень ядовит и в определенной концентрации может привести к тяжелому отравлению и слепоте. В качестве примеси в спирте могут быть дубильные вещества, если спирт хранился в дубовых бочках.
Метиловый спирт (метанол) в течение длительного времени получали из водного дистиллата, выделяющегося при сухой перегонке древесины (отсюда и название — древесный спирт). Выход спирта при этом зависит от породы древесины и колеблется в пределах от 3 до 6 кг на каждый кубометр сухой древесины. В 1933 г. в СССР была пущена первая установка по получению метилового спирта из синтез-газа, и в настоящее время более 90% его получают таким образом. Метиловый спирт является важным видом сырья для получения формальдегида, диметил-сульфата, антидетонационных смесей, ингибиторов, антифризов, метиламина, метилового эфира акриловой кислоты, лаков, красителей и других продуктов. В чистом виде применяется как добавка к моторному топливу и в качестве растворителя.
Выход спирта при этом зависит от породы древесины и колеблется в пределах от 3 до 6 кг на каждый кубометр сухой древесины. В 1933 г. в СССР была пущена первая установка по получению метилового спирта из синтез-газа, и в настоящее время более 90% его получают таким образом. Метиловый спирт является важным видом сырья для получения формальдегида, диметил-сульфата, антидетонационных смесей, ингибиторов, антифризов, метиламина, метилового эфира акриловой кислоты, лаков, красителей и других продуктов. В чистом виде применяется как добавка к моторному топливу и в качестве растворителя.
Гидролиз целлюлозы, иначе называемый осахариванием,-очень важное свойство целлюлозы, он позволяет получить из древесных опилок и стружек глюкозу, а сбраживанием последней — этиловый спирт. Этиловый спирт, полученный из древесины, называется гидролизным.
Поэтому большинство установок для перегонки дерева получают лишь часть содержащихся в сыром древесном спирте метилового спирта и ацетона в виде чистого метилового спирта и чистого ацетона. Остальную значительную часть в виде первых и средних погонов, полученных в колонках обычным способом, т. е. без введения воды и пара, смешивают вместе и получают древесный спирт для денатурации. Отделение метилового спирта от ацетона описанным здесь способом, посредством которого это отделение происходит почти количественно, дает значительное финансовое преимущество перед прочими установками, ра-
Остальную значительную часть в виде первых и средних погонов, полученных в колонках обычным способом, т. е. без введения воды и пара, смешивают вместе и получают древесный спирт для денатурации. Отделение метилового спирта от ацетона описанным здесь способом, посредством которого это отделение происходит почти количественно, дает значительное финансовое преимущество перед прочими установками, ра-
Метиловый спирт (метанол, древесный спирт) СНзОН — бесцветная жидкость с характерным запахом, смешивается с водой в любых соотношениях, хороши растворитель многих органических веществ, горит бледным пламенем. М. с. очень ядовит, вызывая в малых дозах слепоту, в больших — смерть. В промышленности метиловый спирт получают двумя способами присухой перегонке дерева (поэтому его называют древесным спиртом) и синтетически из СО и Нг в присутствии катализатора (напр., оксид цинка ZnO), при 300-600 °С и давлении 5-10 Па (СО + Ц- 2Нг = СНзОН). М. с. применяют как сырье для получения муравьиного альдегида (формальдегида) и для синтеза других органических веществ, в производстве красителей и лаков.
Метиловый спирт (метанол) СН3ОН, носящий еще название древесного спирта (по старому способу его получения — сухой перегонкой дерева), представляет собой бесцветную жидкость, кипящую при 64,7° С. Обладает характерным спиртовым запахом, горит бледным пламенем. Метиловый спирт сильно ядовит. При принятии внутрь вызывает тяжелое отравление, сопровождаемое потерей зрения может привести к смертельному исходу.
Первыми источниками получения органических веществ были животные и растительные организмы X, продукты их жизнедеятельности. Каждый живой организм представляет собой своеобразную химическую лабораторию, в которой осуществляются как процессы синтеза, так и распада. В растительных организмах из простых исходных веществ (диоксид углерода, вода) под воздействием солнечной энергии синтезируются сложные органические вещества (фотосинтез). В животных организмах, наоборот, сложные органические вещества (сахара, белки, жиры) распадаются на более простые, часть из них как бы сгорает, отдавая энергию и превращаясь в СО2 и Н2О, но в то же время в организме также синтезируются специфические белки, жиры и другие вещества. Растительный мир является главным производителем органических веществ. Особое место в этом отношении занимают деревья. Древесина и полученные из нее целлюлоза и лигнин являются ценным сырьем для химической переработки. Так, например, сухая перегонка древесины с давних времен применялась для получения органических соединений, таких, как уксусная кислота, метиловый спирт (древесный спирт), ацетон, фенолы.
Растительный мир является главным производителем органических веществ. Особое место в этом отношении занимают деревья. Древесина и полученные из нее целлюлоза и лигнин являются ценным сырьем для химической переработки. Так, например, сухая перегонка древесины с давних времен применялась для получения органических соединений, таких, как уксусная кислота, метиловый спирт (древесный спирт), ацетон, фенолы.
До середины XIX в. практика переработки органических веществ не выходила за пределы извлечения из растительного и животного сырья содержащихся в нем ценных продуктов (например,- красителей, сахаров, дубителей и др.). Для выделения их использовались простейшие механические и тепловые процессы обработки сырья дробление, растворение, фильтрование, отжим, выпаривание, перегонка и т. д. При получении спирта, уксусной кислоты и некоторых других органических веществ использовались биохимические процессы (в частности, брожение). Некоторые органические продукты были выделены при термическом разложении природного сырья. Так, при сухой перегонке древесины наряду с древесным углем получали уксусную кислоту, древесный спирт, деготь.
Так, при сухой перегонке древесины наряду с древесным углем получали уксусную кислоту, древесный спирт, деготь.
Фракции сырой (неочищенной) смолы представляют собой сложные смеси, состоящие из легких и тяжелых масел, которые находят применение для пропитки древесины и медицинских целей. При перегонке смолы в остатке получают пек. Фракцию тяжелых масел перерабатывают на креозот. Основным компонентом этого продукта является гваякол, применяемый в фармацевтической промышленности как антисептическое средство. Фенольные компоненты пиролизной смолы можно также использовать при получении связующих для фанеры . Древесный спирт содержит около 60 % метанола и различных примесей (см. 12.5). Его используют в качестве растворителя и для денатурации этанола. Из фракции древесного уксуса (см. 12.5) можно получить чистую уксусную кислоту и пищевой уксус. Решение вопроса о том, следует или нет получать очищенные продукты, зависит от экономических соображений и требований экологии . Неконденсируемые газы, состоящие из диоксида и моноксида углерода, водорода, метана и других углеводородов (теплота сгорания около 8,9 МДж/м), применяют для предварительной сушки древесины и в качестве газа для продувки реторт .
В промышленности метиловый спирт раньше получали при сухой перегонке древесины, откуда и его название — древесный спирт. При нагревании древесины без доступа воздуха происходит разложение целлюлозы и других веществ, в частности сложного вещества, спутника целлюлозы — лигнина. В результате образуются различные газообразные, жидкие и твердые продукты, в том числе.и метиловый спирт. Полученный таким образом метиловый спирт всегда содержит примеси уксусной кислоты, ацетона и других органических веществ.
Метиловый спирт. Метиловый спирт (другие названия метанол, карбинол, древесный спирт) — простейший одноатомный спирт, бесцветная легкоподвижная жидкость. Сильный яд (прием внутрь вызывает слепоту, при больших дозах — смерть). Современный метод получения — каталитический синтез из окиси углерода и водорода (температура 300-400 С, давление 250-500 атм, катализатор — окись цинка)
Метиловый спирт прежде получали деструктивной перегонкой древесины и называли его поэтому иногда древесным спиртом. Это ядовитое вещество, и употребление его приводит к слепоте и смерти. Метиловый спирт применяют в качестве растворителя, а также используют для получения других органических соединений.
Это ядовитое вещество, и употребление его приводит к слепоте и смерти. Метиловый спирт применяют в качестве растворителя, а также используют для получения других органических соединений.
В табл. 38 приведены доли спирта от всего поступившего на ректификацию, в пересчете на 100%-ный, в отг льных сортах ректификованных спиртов, полученных ректификацией необработанного спирта-сырца и обработанного перед ректификацией древесным углем, едким натром либо перманганатом калия в табл. 39 — основные характеристики полученных при этом ректификованных спиртов I сорта. В представленных таблицах столбцы, пронумерованные цифрой 1, относятся к ректификованному спирту, полученному из необработанного спирта-сырца 2 — обработанного древесным углем 3 — обработанного едким натром 4 — обработанного перманганатом калия.
Некоторое количество метилового спирта получается методом сухой перегонки древесины отсюда и одно из названий метанола — древесный спирт. Это наиболее старый способ его получения.
Летучие компоненты отделяют перегонкой с получением сырых продуктов. Так, фракция древесного спирта состоит из воды, 45 % метанола, 7 ацетона, 5 метилацетата, 3 % ацетальдегида и небольших количеств аллилового спирта, метилформиата, фурана и фурфурола. Фракция древесного уксуса содержит в основном уксусную кислоту, а также пропионовую, масляную и другие кислоты. Главными компонентами фракции смолы являются крезол, гваякол, другие фенолы и простые эфиры фенолов .
Метилозый спирт образуется и при сухой перегонке дерева поэтому его называют также древесным спиртом. Применяется он как растворитель, а также для получения других органических веществ.
Первый представитель гомологического ряда предельных одноатомных спиртов — метиловый спирт (метанол) СН3ОН раньше часто называли древесным спиртом. Происхождение этого названия связано со старинным способом получения метилового спирта при сухой перегонке дерева. В настоящее время метанол получается исключительно синтетическим путем, при пропускании смеси окиси углерода и водорода при 350 °С и 250 атм над катализатором, состоящим из смеси цинка, хрома и других металлов
Метиловый спирт. Метило1 лй спирт (другие названия метанол, карбинол, древесный спирт) — простейший одноатомный спирт, бесцветная жидкость. Сильный яд (прием внутрь вызывает слепоту, при ббльших дозах — смерть). Сов >еменный метод получения — каталитический синтез из оксида углерэда (II) и водорода [томпература 250°С, давление 7 МПа, катализатор — смесь оксидов цинка и меди (II)]
Метило1 лй спирт (другие названия метанол, карбинол, древесный спирт) — простейший одноатомный спирт, бесцветная жидкость. Сильный яд (прием внутрь вызывает слепоту, при ббльших дозах — смерть). Сов >еменный метод получения — каталитический синтез из оксида углерэда (II) и водорода [томпература 250°С, давление 7 МПа, катализатор — смесь оксидов цинка и меди (II)]
При сухой перегонке древесины уксусная кислота, собирается в подсмольной воде. Для отделения уксусной кислоты от древесного спирта и ацетона ее нейтрализуют известью полученный уксуснокислый кальций, так называемый уксусный порошок, разлагают соляной кислотой или серной кислотой
Кроме этих наименований некоторые спирты имеют еще эмпирические наименования, связанные с историей открытия в том или ином природном продукте, способом получения и т. д. Например, метиловый спирт часто называют древесным спиртом, т к как он получается при сухой перегонке дерева этиловый спирт называют винным спиртом, так как он был впервые обнаружен в виноградном вине, и т. д.
д.
Метиловый спирт, или метанол, СН3ОН (также древесный спирт, или карбинол) получается любым из общих способов получения спиртов. Однако в течение многих лет единственным источником его являлись продукты сухой перегонки дерева. Водный слой, получаемый наряду с древесным дегтем при медленном нагревании дерева без доступа воздуха, содержит 1-2% метилового спирта и, кроме того, много уксусной кислоты (10%) и немного ацетона (0,5%). Уксусную кислоту отделяют обработкой известью, после чего метиловый спирт очищают дробной перегонкой и другими способами.
В течение длительного времени химики называли органические вещества по случайным признакам. Чаще всего эти названия отражали происхождение веществ (муравьиная, яблочная, винная кислоты, молочный сахар, винный и древесный спирты и др.), иногла- способ получения (пировиноградная кислота), а порой — имя исследователя (например, кетон Михлера). Эти случайные названия, не отражающие строения молекул органических веществ, получили название тривиальных, а система этих названий — тривиальной номенклатуры. Эти названия используются и сейчас, особенно когда речь идет о привычных и часто применяемых реактивах.
Эти названия используются и сейчас, особенно когда речь идет о привычных и часто применяемых реактивах.
Метиловый спирт, метанол, древесный спирт. Бесцветная жидкость, т. кип, 64,5°, хорошо растворяется в воде. Широко применяется в лабораторной работе как растворитель, а также в ряде органических синтезов (получение формальдегида, реакция метилирования и др.). Обладает высокой токсичностью и вызывает тяжелые отравления. При постоянной работе с метиловым спиртом опасно постепенное (комулятивное) нарастание его действия. Помимо наркотического действия метиловый спирт вызывает органическое поражение зрительного нерва и сетчатки глаз, в связи с чем при отравлении метиловым спиртом может наступить полная или частичная потеря зрения. Смертельная доза при приеме внутрь метилового спирта 30 г тяжелые отравления могут наступить при приеме 5-10 г .
Как видно из представленных данных, ректификованные спирты I сорта, полученные из обработанного и необработанного спирта-сырца, имеют одинаковые или близкие показатели по вкусу и запаху, крепости, содержанию фурфурола, альдегидов и сивушного масла. (Понятно, что к характеристикам спирта, обозначенным словами нет и следы, небходимо относиться осторожно, с пониманием того, что анализ произведен в условиях промышленного производства исследования выполнены на Бах-мачском винокуренном заводе Черниговской губернии.) Но в спиртах, полученных перегонкой спирта-сырца, обработанного древесным углем и едким натром, содержание эфиров и кислот ниже, чем у двух других спиртов. Значительно лучше у них и показатель Ланга (см. с. 216-218). Выход ректификованных
(Понятно, что к характеристикам спирта, обозначенным словами нет и следы, небходимо относиться осторожно, с пониманием того, что анализ произведен в условиях промышленного производства исследования выполнены на Бах-мачском винокуренном заводе Черниговской губернии.) Но в спиртах, полученных перегонкой спирта-сырца, обработанного древесным углем и едким натром, содержание эфиров и кислот ниже, чем у двух других спиртов. Значительно лучше у них и показатель Ланга (см. с. 216-218). Выход ректификованных
Основной пирогенетический процесс был выбран с получением древесного угля, который является более дефицитным и нужным продуктом, чем древесный генераторный газ. Для получения наибольшей гаммы продуктов пиролиза, образующихся при НИЗКИХ и высоких температурах, процесс разложения ведется в две стадии. Сначала древесину подвергают предварительному пиролизу в среде жидкого теплоносителя (дизельное топливо) с температурой 275° и получают основную массу кислот, легкокипящих продуктов, входящих в так называемый древесный спирт, и смол. Образующуюся в результате предпиролиза бурую древесину (см. стр. 37) подвергают вторичному пиролизу при температуре 600-700° с твердым теплоносителем (древесный уголь) и Получают светильный газ и жижку, содержащую отстойную смолу с большим выходом низкокипящих фенолов, дополнительное количество кислот и древесный уголь. Последний отличается низким содержанием летучих и повышенной активностью.
Образующуюся в результате предпиролиза бурую древесину (см. стр. 37) подвергают вторичному пиролизу при температуре 600-700° с твердым теплоносителем (древесный уголь) и Получают светильный газ и жижку, содержащую отстойную смолу с большим выходом низкокипящих фенолов, дополнительное количество кислот и древесный уголь. Последний отличается низким содержанием летучих и повышенной активностью.
Осветленный сьфой древесный спирт должен быть и оставаться щелочным, прежде чем можно приступить к его иере-гоеке. Если он не щелочной, то полученный из него чистый метиловый спирт будет желтым, часто даже после нескольких перегонок. Если очистка известковым раствор ом проведена тщательно, то выделенный при взбалтывании 1 ч. отстоявшегося древесного спирта с 2 ч. раствора едкого натра уд. в. 1,3 ацетон
Номенклатура. Первый член гомологического ряда предельных одноатоммых спиртов в прошлом получали путем сухой перегонки древесины, а поэтому полученный спирт называли древесным спиртом или карбинолом. Следующий член — С2Н5ОН — был назван винным спиртом еще алхимиками.
Следующий член — С2Н5ОН — был назван винным спиртом еще алхимиками.
По вопросу получения формальдегида из метана имеется обширная патентная литература. Процесс окисления начинается здесь при повышенной температуре (500-600°), которая поддерживается далее теплотой самой реакции для ее успешного течения некоторые авторы рекомендуют применение давления, а также катализаторов (Си, Ге, N1, Со). Формальдегид находит обширное применение в качестве дезинфе цирующего вещества и антисептика в химической технологии он широко применяется для изготовления органических красок (фуксин и др.), искусственных смол (бакелит и т. п.) и т. д. Технически формальдегид получается пока окислением древесного спирта.
Смотреть страницы где упоминается термин Древесный спирт получение : Начала органической химии Кн 1 Издание 2 (1975) — [
На сегодняшний день достаточно много людей занимается изготовлением домашней наливки, однако для некоторых напитков необходимо наличие спиртного элемента. Производство спирта в домашних условиях не является сильно трудоемким. Для этого необходимо знать и учитывать некоторые аспекты и принципы изготовления метилового спирта.
Производство спирта в домашних условиях не является сильно трудоемким. Для этого необходимо знать и учитывать некоторые аспекты и принципы изготовления метилового спирта.
В первую очередь для изготовления метанола требуется наличие зерна. В роли зерновых культур в данном случае могут выступать кукуруза, пшеница. Также можно использовать картофель и крахмал. Но, как известно, во взаимодействии с веществом крахмал не дает никакой реакции. С целью произвести химический элемент используется метод засахарения. А для того, чтобы его засахарить, необходимы определенные ферменты, они присутствуют в солоде. Делая этанол из зерна без химических примесей, наблюдается выход натурального продукта.
Технология производства метанола
Технология по производству спиртового химического вещества в домашних условиях может состоять из нескольких этапов.
Ниже представляются самые основные:
- Производство метанола с помощью солода. Зерна культурных растений необходимо проращивать в небольших посудинах, при этом их рассыпают в один слой, примерно до трех сантиметров.
 Помните, что предварительно пророщенные зерна необходимо обработать раствором марганцовки. После обработки семена помещаются в емкость и смачиваются водой. Следует учитывать, что наличие солнечных лучей, или достаточность света напрямую зависит от скорости прорастания зерна. Поверх емкости следует накрыть полиэтиленовый материал или тонкое стекло, то есть он должен быть достаточно прозрачным. Если наблюдается уменьшение количества воды, ее необходимо добавлять.
Помните, что предварительно пророщенные зерна необходимо обработать раствором марганцовки. После обработки семена помещаются в емкость и смачиваются водой. Следует учитывать, что наличие солнечных лучей, или достаточность света напрямую зависит от скорости прорастания зерна. Поверх емкости следует накрыть полиэтиленовый материал или тонкое стекло, то есть он должен быть достаточно прозрачным. Если наблюдается уменьшение количества воды, ее необходимо добавлять. - Следующий этап: обработка крахмала. Для начала добываем крахмал из продукта, который выбран для изготовления этанола. В данном случае это картофель. Слегка порченый картофель необходимо варить до тех пор, пока из воды начнет образовываться клейстер. Далее ждем, пока продукт остынет, тем временем измельчаем солод. Следом перемешиваем два продукта. Далее происходит процедура расщепления крахмала, ее необходимо производить при температуре не менее 60 ˚ С. Теперь смесь помещается в посуду с горячей водой и оставляется на 1 час.
 По истечении времени изделие полностью остужают.
По истечении времени изделие полностью остужают. - Этап брожения. Как известно, брожение характеризуется присутствием в алкоголе содержащих элементов. Однако брагу назвать алкогольным напитком невозможно. После остывания смеси добавляются дрожжи, которые способны вступить в реакцию даже при комнатной температуре. Однако если температура поднимается выше — брожение продукта естественно будет происходить быстрее. При значительной жаре процедура брожения закончится по истечении трех суток. При этом из продукта можно ощущать мягкий запах зерна.
- Следующий этап — это перегонка. С помощью чего она производится? Для этого используется специальный аппарат для производства спирта в домашних условиях.
- Заключительным этапом считается технология очистки. Можно сказать, что метиловый спирт готов, но замечается, что жидкость не прозрачная. Именно поэтому и делается очистка. Она проводится путем добавления раствора марганцовки. В таком виде оставляем метиловый спирт на одни сутки, затем фильтруем — продукт готов.

Как, видим, технология изготовления домашнего спирта довольно проста и не требует дополнительных усилий.
Производство этанолового вещества из опилок
В последние годы значительно снизилось ископаемое сырье, которое можно использовать для изготовления этилового спирта. Наблюдается нехватка зерна. Однако производство спирта из древесных опилок не самый худший вариант, так как этот сырьевой продукт постоянно обновляется по истечении годов.
Однако изготовление вещества из опилок требует некоторых навыков, и плюс ко всему изготовитель должен иметь специальное оборудование, без которого будет трудоемко изготавливать этанол. Производство спирта из опилок в домашних условиях пользуется высокой популярностью, так не требует высоких затрат.
Как известно, свой изготовленный этанол не сравнивается с заводским вариантом. Продукция, изготовленная в хозяйственных условиях, является более качественной, ведь каждый ингредиент отличается своей уникальностью.
Из опилок производить спирт значительно проще!
Как производить спиртной продукт дома?
Производство этилового спирта в домашних условиях ведется при использовании специального аппарата. Данный аппарат способен производить процедуру расщепления определенных элементов, а также проводить химические реакции между ними. Обычное оборудование для изготовления спиртной продукции может выглядеть как мини заводы. Изготавливать в них можно любые виды алкогольных напитков.
Изучить технологию приготовления этилового вещества довольно просто, при этом изделие получается высококачественным. Что из этого можно получить? Во-первых, это продукция алкогольного характера с высоким качеством, а во-вторых полностью происходит окупаемость собственных затрат, для этого требуется специальный аппарат.
Например, если используется сахар в количестве 20 кг, с него выходит до 12 литров алкоголя. При этом процент метанола достигает до 96%. Из этого расчета выходит 25 бутылок водки по пол литра.
Кроме того, электричества, которое потребляет аппарат, будет потрачено около 25 квт.
Такое оборудование способно использовать все загруженные продукты по назначению. Выход продукта, непригодного для питья, производимого при первой обработке, можно использовать как очиститель для стеклянных поверхностей и окон. Также такой аппарат можно установить самостоятельно, пользуясь необходимыми схемами и чертежами. Такое оборудование с легкостью справится с производством метилового спирта.
Оборудование по производство спиртных продуктов имеет некоторые принципы своей работы. Аппарат имеет специальную горловину, которая заполняет бак необходимой жидкостью. В виде такой жидкости может выступать брага. При помощи нагревательных горелок продукт нагревается до температуры кипения. После чего аппарат и оборудование необходимо перевести в обычный режим.
Далее происходит охлаждение через холодильное отделение с добавочной очисткой пара от ненужных примесей. Очищенное вещество попадает в бак, а пары в холодильник, в котором охлаждаются до состояния жидкости. Аппарат для производства спирта способен выработать установленный норматив. Результатом проведения данной процедуры выступает алкоголь высококачественного приготовления.
Аппарат для производства спирта способен выработать установленный норматив. Результатом проведения данной процедуры выступает алкоголь высококачественного приготовления.
Вторая жизнь гидролизной промышленности
Для России проблема переработки и дальнейшего использования отходов лесоперерабатывающей отрасли (которые, к слову сказать, составляют от 40 до 60% от заготавливаемой древесины в России) является крайне актуальной. А принимая во внимание наличие немалого количества ныне простаивающих гидролизных заводов, для которых отходы деревообработки и лесопиления являются основным сырьем, решение проблемы напрашивается само собой. Именно поэтому правительством РФ в 2012 году было принято решение наладить на базе бывших гидролизных заводов производство простых сахаров в форме, высоко усваиваемой клетками бактерий.
Немного истории
Первые опытно-промышленные заводы по получению спирта путем гидролиза древесины и растительных сельскохозяйственных отходов появились в СССР еще в 1930-х годах. В те годы строительство новых гидролизных заводов шло быстрыми темпами. Это было продиктовано все возрастающей потребностью в этиловом спирте, который, кроме всего прочего, использовался и в качестве сырья для расширяющегося производства синтетического каучука. В годы Великой Отечественной войны потребность в этиловом спирте возросла еще сильнее. Он применялся на предприятиях оборонной промышленности, в санитарных подразделениях и тыловых госпиталях. В годы острой нехватки продовольственного сырья гидролизный спирт полностью заменил спирт, производившийся из пищевого зерна. Сразу же после войны отрасль продолжала активно развиваться, были утверждены масштабные планы по строительству новых и модернизации уже существующих заводов. В те годы в СССР насчитывалось около 40 гидролизных заводов. Вплоть до начала 1990-х гг. гидролизное производство считалось крупной и высокорентабельной подотраслью. При этом многие гидролизные предприятия являлись градообразующими и выполняли социально значимые функции.
В те годы строительство новых гидролизных заводов шло быстрыми темпами. Это было продиктовано все возрастающей потребностью в этиловом спирте, который, кроме всего прочего, использовался и в качестве сырья для расширяющегося производства синтетического каучука. В годы Великой Отечественной войны потребность в этиловом спирте возросла еще сильнее. Он применялся на предприятиях оборонной промышленности, в санитарных подразделениях и тыловых госпиталях. В годы острой нехватки продовольственного сырья гидролизный спирт полностью заменил спирт, производившийся из пищевого зерна. Сразу же после войны отрасль продолжала активно развиваться, были утверждены масштабные планы по строительству новых и модернизации уже существующих заводов. В те годы в СССР насчитывалось около 40 гидролизных заводов. Вплоть до начала 1990-х гг. гидролизное производство считалось крупной и высокорентабельной подотраслью. При этом многие гидролизные предприятия являлись градообразующими и выполняли социально значимые функции. Однако вскоре положение стало меняться. На территории России осталось всего 17 действующих заводов, а к началу 2000-х годов эта цифра сократилась еще вдвое (А.П. Суходолов, В.А. Хаматаев «Развитие отечественной гидролизной промышленности»).
Однако вскоре положение стало меняться. На территории России осталось всего 17 действующих заводов, а к началу 2000-х годов эта цифра сократилась еще вдвое (А.П. Суходолов, В.А. Хаматаев «Развитие отечественной гидролизной промышленности»).
Наши дни
Ранее применявшаяся на гидролизных заводах технология с использованием серной кислоты влекла за собой образование большого количества шлама, борьба с которым продолжается и по сей день. А в условиях современного экологически ориентированного общества существующая технология получения этилового спирта из древесного сырья стала абсолютно неприемлемой.
К сожалению, лишь немногим заводам удалось перепрофилироваться и начать выпускать востребованную рынком продукцию. Большинство же из них пришло в упадок, а со временем было и вовсе закрыто. Прекращение деятельности биотехнологических предприятий привело к резкому падению производства не только технических спиртов и растворителей (АБЭ – ацетона, бутанола, этанола), но также микробиологического кормового дрожжевого белка. Сократилось и производство глюкозных сахаров – сырья для производства антибиотиков. И это лишь неполный перечень причин, по которым возрождение гидролизных заводов России является столь острой проблемой, требующей безотлагательного решения.
Сократилось и производство глюкозных сахаров – сырья для производства антибиотиков. И это лишь неполный перечень причин, по которым возрождение гидролизных заводов России является столь острой проблемой, требующей безотлагательного решения.
Имея положительный опыт сотрудничества с нашей компанией в реализации проекта по получению биобутанола, госкорпорация «РОСТЕХ» приняла решение вновь обратиться за помощью к ГК «БИОТЕХНО».
«На российском рынке довольно сложно выбрать организацию, которая имеет свою собственную производственную базу и высококвалифицированный инженерный состав. Ведь наши задачи не являются типовыми, а потому для нас было важно работать с людьми, которые способны произвести оборудование, удовлетворяющее именно нашим требованиям. Предыдущий опыт работы с ГК «БИОТЕХНО» значительно облегчил нам выбор партнера в данном проекте», – говорит г-н Ачильдиев Е.Р., директор по науке РТ-Биотехпром.
Перед специалистами нашей компании стояла очень сложная и ответственная задача – адаптировать имеющуюся технологию получения биобутанола под существующие мощности гидролизных заводов. Ведь итогом нашей работы должно было стать не просто получение высокорентабельного производства, а обеспечение сотен людей рабочими местами, которые оказались не у дел после развала гидролизной промышленности.
Ведь итогом нашей работы должно было стать не просто получение высокорентабельного производства, а обеспечение сотен людей рабочими местами, которые оказались не у дел после развала гидролизной промышленности.
При непосредственном участии специалистов нашей компании был осуществлен подбор производственной площадки, соответствующей всем необходимым требованиям для реализации пилотной части проекта, выполнена детальная проработка аппаратурного оформления проекта.
Особого внимания потребовал подбор оборудования для линии наработки ферментов с усиленной β-глюкозидазной активностью для осуществления процедуры ферментативного гидролиза. Идея состояла в том, чтобы наладить собственное производство ферментов с непрерывной их подачей на линию проведения ферментативного гидролиза целлюлозосодержащего сырья, с целью создания эффективного производства, как с технологической, так и с экономической точки зрения.
Используемые ферменты являлись уникальной разработкой российских ученых института биохимии им.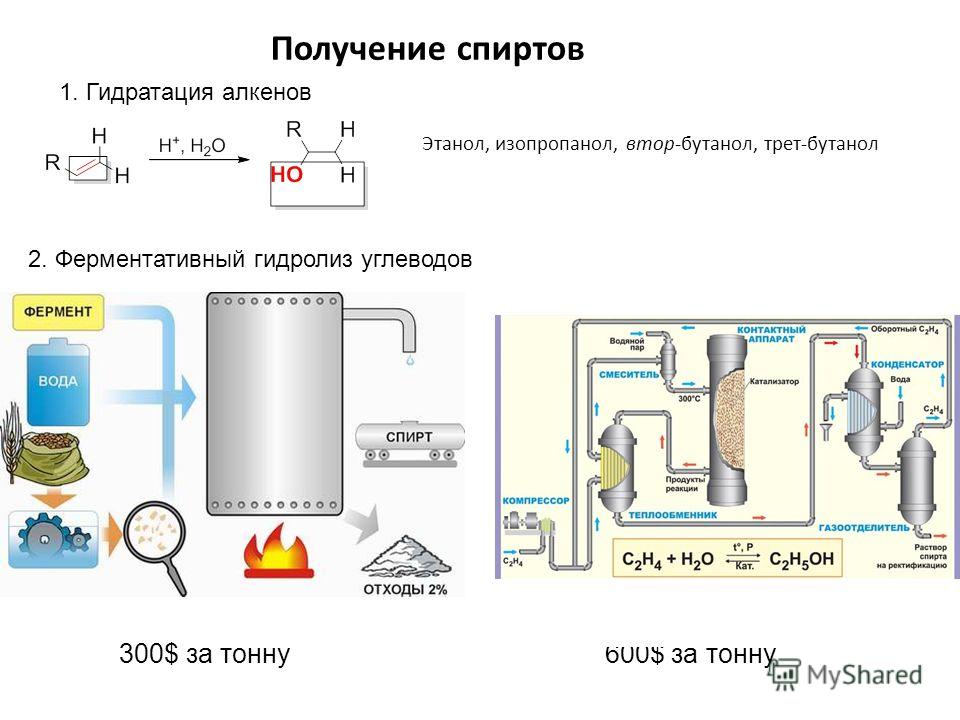 А. Н. Баха РАН и до сегодняшнего дня в масштабах промышленного производства получены не были.
А. Н. Баха РАН и до сегодняшнего дня в масштабах промышленного производства получены не были.
Специалистами ГК «БИОТЕХНО» было выполнено оснащение производственного цеха следующим оборудованием, а также произведен его монтаж и пуско-наладочные работы:
- Посевные ферментеры ферментной линии объемом 50 л и 500 л;
- Блок из двух ферментеров линии ферментативного гидролиза объемом 7,7 м3 каждый;
- Реакторы объемом 6,5 м3 – 2 шт;
- Импеллерная мельница – 1 шт;
- Вспомогательные емкости различного объема;
- Аналитическое оборудование.
Каждый из реализуемых нами проектов в своем роде уникален. Так было и здесь: нашим специалистам пришлось разработать и применить целый ряд оригинальных технических с решений с целью размещения всего требуемого оборудования на имеющихся площадях. Но наши инженеры успешно справились со всеми трудностями, и пилотная часть проекта завершилась получением требуемого количества сиропа простых сахаров с необходимым содержанием редуцирующих веществ.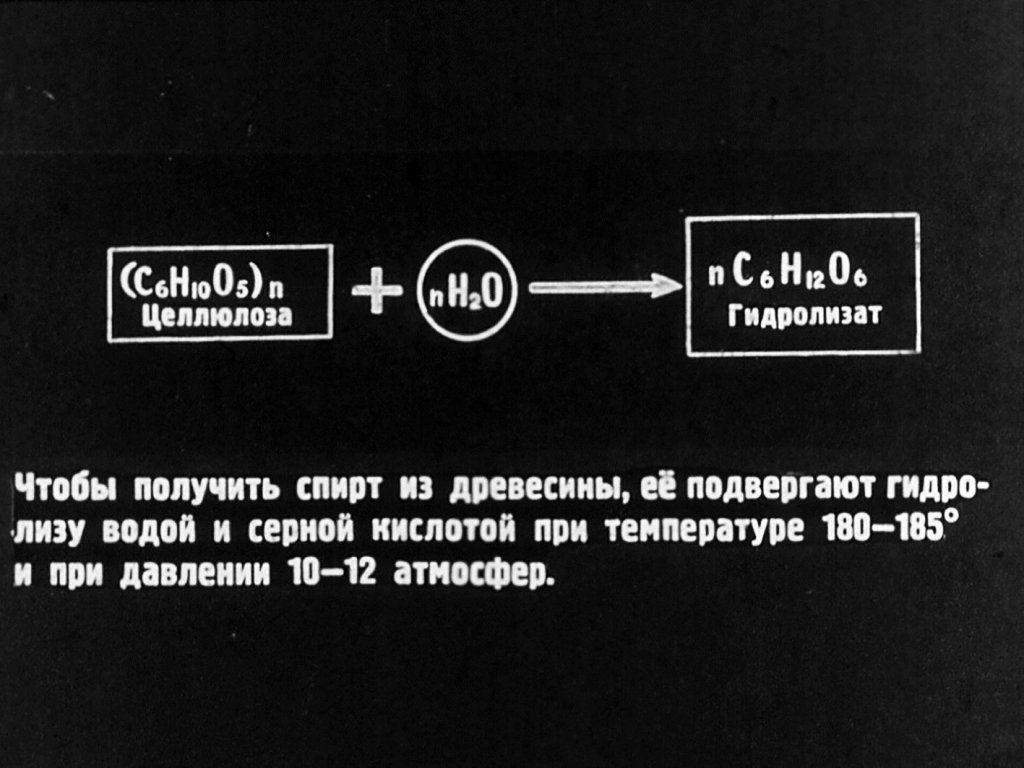 Следовательно, впереди нас ждала масштабная работа по запуску опытно-промышленного производства.
Следовательно, впереди нас ждала масштабная работа по запуску опытно-промышленного производства.
В данной части проекта перед нами стояла задача переноса части смонтированного ранее оборудования на площадку, подготовленную для реализации опытно-промышленного этапа проекта, и дооснащения производственного цеха всем необходимым оборудованием. Специалистами группы компаний «БИОТЕХНО» был произведен демонтаж и транспортировка ранее установленного оборудования, подбор всех недостающих единиц оборудования с последующей поставкой, монтажом и пуско-наладкой.
Группой компаний «БИОТЕХНО» дополнительно была произведена поставка следующего оборудования в рамках этого этапа проекта:
- Промышленные ферментеры ферментной линии объемом 2 м3, 10 м3 с емкостью для приготовления и подачи стерильной питательной среды
- Аппарат линии ферментативного гидролиза объемом 6,3 м3 – 6 шт
- Сепаратор Альфа Лаваль – 1шт
- Система микро- ультрафильтрации (UF)
- Пресс-фильтр – 1 шт
- Импеллерная мельница – 2 шт
- Дизельный парогенератор – 3 шт
- Система водоподготовки
- Компрессор
- On-line анализатор
- Вспомогательные емкости различного объема
Без сомнения данный проект является одним из сложнейших комплексных проектов, успешно выполненных группой компаний «БИОТЕХНО». Благодаря знаниям и накопленному опыту, а также тесному сотрудничеству с нашими партнерами специалистам группы компаний «БИОТЕХНО» удалось воплотить в жизнь масштабный проект по получению простых сахаров из непищевого (древесного) сырья, реализуемый правительством РФ при участии госкорпорации РОСТЕХ. Разработанная промышленная технология позволяет перерабатывать отходы древесины, в основном хвойных пород, в простые сахара (глюкозу, маннозу, арабинозу, ксилозу), лигнин и смолу с последующим производством из них путем микробиологического синтеза широкого спектра коммерчески привлекательных продуктов (кормовых добавок, сырья для фармпромышленности, различных видов биотоплива и компонентов моторного топлива).
Благодаря знаниям и накопленному опыту, а также тесному сотрудничеству с нашими партнерами специалистам группы компаний «БИОТЕХНО» удалось воплотить в жизнь масштабный проект по получению простых сахаров из непищевого (древесного) сырья, реализуемый правительством РФ при участии госкорпорации РОСТЕХ. Разработанная промышленная технология позволяет перерабатывать отходы древесины, в основном хвойных пород, в простые сахара (глюкозу, маннозу, арабинозу, ксилозу), лигнин и смолу с последующим производством из них путем микробиологического синтеза широкого спектра коммерчески привлекательных продуктов (кормовых добавок, сырья для фармпромышленности, различных видов биотоплива и компонентов моторного топлива).
Г-н Ачильдиев Е.Р.: «Хотелось бы отметить, что работать с ГК «БИОТЕХНО» было приятно с профессиональной точки зрения, подтверждением тому является высокое качество производимого оборудования, профессионализм инженерного состава и сервисной службы компании, а оптимальное соотношение стоимости оборудования и его качества является достойным подтверждением правильности нашего выбора».
Спирт из опилок своими руками. Производство этилового спирта из опилок
Растёт спрос на биотоплива — горючие жидкости, изготовленные из возобновляемых биологических ресурсов. Один из них — древесина. Можно ли из древесины получать топливо, не уступающее нефтяному?
Первое, что нужно уяснить — это то, что именно бензина или керосина из дерева сделать нельзя. Оно не поддаётся разложению на углеводороды с прямой цепью, из которых главным образом состоят нефтепродукты. Однако это не означает, что из него нельзя получать вещества, способные заменить нефтепродукты.
Некоторые любят табуретовку
Первый в списке, конечно же, спирт. Из древесины можно получать два различных вида спирта. Первый, который так и называется древесным — по-научному метиловый спирт. Это вещество очень похоже на привычный этиловый спирт, как по горючести, так и по запаху и вкусу. Однако метиловый спирт отличается тем, что весьма ядовит, и приём его внутрь может привести к смертельному отравлению. Вместе с тем он является высококачественным моторным топливом, его октановое число даже выше, чем у этилового спирта, и намного выше, чем у обыкновенного бензина.
Вместе с тем он является высококачественным моторным топливом, его октановое число даже выше, чем у этилового спирта, и намного выше, чем у обыкновенного бензина.
Технология получения метилового спирта из древесины очень проста. Он получается путём сухой перегонки, или пиролиза. Точнее, он является одной из составных частей жижки — смеси кислородсодержащих органических веществ, отделяющихся от свежевыгнанной древесной смолы. Однако выход полученного таким образом спирта слишком мал, чтобы он мог использоваться в качестве топлива. Это делает подобную технологию получения топлива бесперспективной.
Однако из древесины можно получить и этиловый спирт, в намного больших количествах. Этот спирт — так называемый гидролизный — получается при разложении целлюлозы, основного компонента древесины, с помощью серной кислоты. Вернее, при разложении целлюлозы получаются сахара, которые в свою очередь могут быть переработаны в спирт обычным путём. Этот способ получения этилового спирта весьма распространён в промышленности, именно гидролизным способом получают практически весь технический спирт, применяемый в непищевых целях.
Этиловый спирт может быть использован как непосредственно вместо бензина, так и в качестве присадки к бензину. Путём таких присадок получаются различные сорта биотоплива, популярные, в частности, в таких странах, как Бразилия.
Получение этилового спирта путём гидролиза древесины экономически несколько менее выгодно, чем получение его из различных сельскохозяйственных культур. Однако выгодной стороной такого способа получения биотоплива является то, что он не требует отведения сельскохозяйственных площадей под «топливные» культуры, не дающие пищевых продуктов, а позволяет использовать для его производства территории, задействованные в лесном хозяйстве. Это делает получение биотопливного этанола из древесины достаточно практичной технологией.
И терпентин на что-нибудь полезен
Недостатком этанола как топлива является его низкая теплота сгорания. При использовании в двигателях в чистом виде он даёт или меньшую мощность, или больший расход, чем бензин. Решить эту проблему помогает смешивание спирта с веществами с высокой теплотой сгорания. И не обязательно это продукты из нефти: в качестве такой присадки вполне годится скипидар, или терпентин.
И не обязательно это продукты из нефти: в качестве такой присадки вполне годится скипидар, или терпентин.
Скипидар — тоже продукт переработки древесины, а если конкретно — хвойной: сосен, елей, лиственниц и других. Он достаточно широко применяется как растворитель, а наиболее очищенные его сорта находят применение в медицине. Однако лесоперерабатывающая промышленность в качестве побочного продукта производит большое количество так называемого сульфатного скипидара — низшего сорта, содержащего ядовитые примеси, не только неприменимого в медицине, но и находит весьма ограниченное применение в химической и лакокрасочной промышленности.
Вместе с тем скипидар из всех продуктов переработки древесины более всего похож на нефтепродукт, точнее — на керосин. Он отличается весьма высокой теплотой сгорания, может использоваться как горючее в керосиновых примусах, лампах, керогазах. Пригоден он и в качестве моторного топлива, правда, непродолжительное время: если его заливать в баки в чистом виде, двигатели вскоре выходят из строя из-за засмоления.
Однако скипидар можно использовать в качестве топлива не в чистом виде, а в качестве присадки к этанолу. Такая присадка не сильно снижает октановое число этилового спирта, но повышает теплоту его сгорания. Ещё одна положительная сторона такой технологии изготовления биотоплива в том, что скипидар денатурирует спирт, делает его непригодным для употребления внутрь в качестве алкоголя. А социальные последствия широкого внедрения неденатурированного спирта в качестве топлива могут стать весьма тяжелыми.
Лигниновые отходы — в доходы!
Такой компонент древесины, как лигнин, считается малополезным. Его применение в промышленности значительно менее широкое, нежели у целлюлозы. Несмотря на то, что он находит применение в производстве строительных материалов и в химической промышленности, чаще его просто сжигают прямо на лесохимпроизводстве. Однако, как выясняется, при пиролизе лигнина можно получить более разнообразные продукты, чем при пиролизе целлюлозы.
Лигнин состоит главным образом из ароматических циклов и коротких прямых углеводородных цепей. Соответственно, при его пиролизе получаются преимущественно углеводороды. Однако, в зависимости от технологии пиролиза, можно получать как продукт с высоким содержанием фенола и родственных ему веществ, так и жидкость, напоминающую нефтепродукты. Эта жидкость также пригодна в качестве присадки к этиловому спирту для получения биотоплива.
Соответственно, при его пиролизе получаются преимущественно углеводороды. Однако, в зависимости от технологии пиролиза, можно получать как продукт с высоким содержанием фенола и родственных ему веществ, так и жидкость, напоминающую нефтепродукты. Эта жидкость также пригодна в качестве присадки к этиловому спирту для получения биотоплива.
Разработаны технологии и установки для пиролиза, которые могут потреблять как лигнин из отвалов, так и неразделённые на лигнин и целлюлозу отходы древесины. Более высокие результаты получаются при смешивании лигнина или древесных отходов с мусором, состоящим из выброшенного пластика или резины: пиролизная жидкость получается более нефтеподобной.
Мирный атом и опилки
Ещё одна технология получения биотоплива из древесины разработана совсем недавно российскими учёными. Она относится к области радиохимии, то есть химических процессов, протекающих под воздействием радиоактивного излучения. В опытах учёных из ИФХЭ им. Фрумкина опилки и другие отходы древесины подвергались одновременному воздействию сильного бета-излучения и сухой перегонки, причём нагревание древесины проводилось именно с помощью сверхсильной радиации. Удивительно, но под воздействием радиации состав продуктов, получаемых при пиролизе, изменился.
Удивительно, но под воздействием радиации состав продуктов, получаемых при пиролизе, изменился.
В пиролизной жидкости, полученной «радиоактивным» способом, было обнаружено высокое содержание алканов и циклоалканов, то есть углеводородов, содержащихся главным образом в нефти. Эта жидкость получилась значительно легче нефти, сравнимой, скорее, с газоконденсатом. Причём экспертиза подтвердила пригодность этой жидкости для использования в качестве моторного топлива или переработки в высококачественные топлива, такие, как автомобильный бензин. Думаем, что это не заслуживает особого упоминания, но проясним ради успокоения страхов радиофобов: бета-излучение не способно вызывать наведённую радиоактивность, поэтому топливо, получаемое этим способом, безопасно и не проявляет радиоактивных свойств само.
Что пускать в переработку
Понятно, что предпочтительнее использовать для производства биотоплива не цельные стволы деревьев, а отходы переработки древесины, такие, как опилки, щепу, веточки, кору, да и тот же лигнин, который идёт в отвалы и печи. Выход этих отходов с гектара поваленного леса, конечно же, ниже, чем древесины в целом, но не следует забывать, что они получаются в качестве побочного продукта в производственных процессах, которые уже идут на многих предприятиях страны, соответственно, отходы производства дешевы и для их получения не нужно вырубать или засаживать под вырубку дополнительные площади леса.
Выход этих отходов с гектара поваленного леса, конечно же, ниже, чем древесины в целом, но не следует забывать, что они получаются в качестве побочного продукта в производственных процессах, которые уже идут на многих предприятиях страны, соответственно, отходы производства дешевы и для их получения не нужно вырубать или засаживать под вырубку дополнительные площади леса.
В любом случае, древесина является ресурсом возобновляемым. Способы восстановления лесных площадей давно известны, а во многих регионах страны наблюдается даже и неконтролируемое зарастание лесом заброшенных сельскохозяйственных земель. Так или иначе, Российская Федерация не относится к странам, где к сбережению леса следует относиться со всем тщанием; площадей нашего леса и его потенциала к самовосстановлению вполне достаточно, чтобы загрузить полностью и лесоперерабатывающую промышленность, и производство биотоплив, и многие другие производства.
Общая схема получения этилового спирта из гидролизной «черной патоки» такова. Сырье в измельченном виде загружают в многометровую стальную гидролизную колонну, изнутри облицованную химически стойкой керамикой. Туда подают под давлением горячий раствор соляной кислоты. В результате химической реакции из целлюлозы получается продукт, содержащий сахар, так называемая «черная патока». Этот продукт нейтрализуют известью и туда добавляют дрожжи — сбраживают патоку. После чего опять нагревают, и выделяющиеся пары конденсируются в виде этилового спирта (называть его «винным», не хочется).
Сырье в измельченном виде загружают в многометровую стальную гидролизную колонну, изнутри облицованную химически стойкой керамикой. Туда подают под давлением горячий раствор соляной кислоты. В результате химической реакции из целлюлозы получается продукт, содержащий сахар, так называемая «черная патока». Этот продукт нейтрализуют известью и туда добавляют дрожжи — сбраживают патоку. После чего опять нагревают, и выделяющиеся пары конденсируются в виде этилового спирта (называть его «винным», не хочется).
Гидролизный способ — самый экономный способ производства этилового спирта. Если традиционным биохимическим способом сбраживания из одной тонны зерна можно получить 50 литров спирта, то из одной тонны древесных опилок, гидролизным способом преобразованных в «черную патоку», выгоняется 200 литров спирта. Как говориться: «Почувствуйте выгоду!» Весь вопрос, можно ли «черную патоку» как осаха-ренную целлюлозу называть «пищевым продуктом», наравне с зерном, картофелем и свеклой. Лица, заинтересованные в производстве дешевого этилового спирта, считают так: « А чё, почему нельзя? Ведь барда, как остаток «черной патоки», после ее перегонки идет на корм скоту, значит, она тоже пищевой продукт». Как тут не вспомнить слова Ф.М.Достоевского: «Образованный человек, когда это ему нужно, может словесно оправдать любую мерзость».
Как тут не вспомнить слова Ф.М.Достоевского: «Образованный человек, когда это ему нужно, может словесно оправдать любую мерзость».
В 30-х годах прошлого века в осетинском поселке Беслан был построен крупнейший в Европе крахмалопа-точный комбинат, который с тех пор выпускает миллионы литров этилового спирта. Потом мощные заводы по производству этилового спирта были построены по всей стране, в том числе при Соликамском и Архангельском целлюлозо-бумажных комбинатах. И.В. Сталин, поздравляя строителей гидролизных заводов, которые во время войны, несмотря на трудности военного времени, досрочно ввели их в эксплуатацию, отметил, что это «дает возможность сэкономить государству миллионы пудов хлеба» (Газета «Правда» от 27 мая 1944 г.).
Этиловый спирт, полученный из «черной патоки», а, по сути, из древесины (целлюлозы), осахаренной гидролизным способом, если, конечно, он хорошо очищен, не отличить от спирта, полученного из зерна или картофеля. По действующим стандартам такой спирт бывает «высшей очистки», «экстра» и «люкс», последний — самый лучший, то есть имеет самую высокую степень очистки. Водкой, приготовленной на основе такого спирта, не отравишься. На вкус такой спирт нейтрален, то есть «никакой» — безвкусный, в нем лишь одни «градусы», он только обжигает слизистую оболочку рта. Внешне распознать водку, сделанную на основе этилового спирта гидролизного происхождения, довольно трудно, а различные ароматизаторы, добавляемые к таким «водкам», придают им некоторое отличие друг от друга.
Водкой, приготовленной на основе такого спирта, не отравишься. На вкус такой спирт нейтрален, то есть «никакой» — безвкусный, в нем лишь одни «градусы», он только обжигает слизистую оболочку рта. Внешне распознать водку, сделанную на основе этилового спирта гидролизного происхождения, довольно трудно, а различные ароматизаторы, добавляемые к таким «водкам», придают им некоторое отличие друг от друга.
Однако не все так хорошо, как кажется на первый взгляд. Генетики провели исследования: одной партии подопытных мышей в рацион добавляли настоящую (зерновую) водку, другой — гидролизную, из древесины. Мыши, которые употребляли «сучок» умирали гораздо быстрее, а их потомство вырождалось. Но результаты этих исследований не остановили выпуск псевдорусских водок. Это как в популярной песне: «Ведь если водку гнать не из опилок, то что б нам было с пяти бутылок…»
В настоящее время многие люди умеют создавать метанол даже своими руками в домашних условиях. В том числе занимаются приготовлением спирта из опилок. Именно производство спирта из опилок считается самым простым и экономичным из всех других известных на сегодняшний день способов. При этом сложным и трудоемким он кажется лишь на первый взгляд. На самом деле повторить это процесс будет достаточно просто даже новичку. Главное, знать все основные принципы изготовления метилового спирта, а также учитывать некоторые хитрости процедуры, которые раскрывают всем желающим профессионалы. Стандартная технология по производству обсуждаемого химического вещества дома обычно состоит сразу из нескольких основных этапов. Для начала получается солод из зерновых культур, затем из слегка подпорченного картофеля варится клейстер, в результате чего происходит обработка крахмала.
Именно производство спирта из опилок считается самым простым и экономичным из всех других известных на сегодняшний день способов. При этом сложным и трудоемким он кажется лишь на первый взгляд. На самом деле повторить это процесс будет достаточно просто даже новичку. Главное, знать все основные принципы изготовления метилового спирта, а также учитывать некоторые хитрости процедуры, которые раскрывают всем желающим профессионалы. Стандартная технология по производству обсуждаемого химического вещества дома обычно состоит сразу из нескольких основных этапов. Для начала получается солод из зерновых культур, затем из слегка подпорченного картофеля варится клейстер, в результате чего происходит обработка крахмала.
Следующий этап — брожение. На нем к заранее подготовленной смеси уже добавляются дрожжи. Чем выше температура окружающей среды, тем быстрее удастся преодолеть обсуждаемый этап. Но он способен самостоятельно завершиться даже при обычных естественных условиях. Конечно, в том случае, если были выбраны качественные дрожжи. Предпоследний этап называется «перегонка». Его можно назвать самым трудоемким и продолжительным. Для данного этапа всегда требуется специальный аппарат, который, кстати, современные умельцы легко изготавливают своими руками. И, наконец, остается лишь очистка. Эта самый последний этап производства спирта в домашних условиях. Продукт практически готов, вот только ему не достает желаемой прозрачности. Добиться ее удастся при помощи самой обычной марганцовки, с которой жидкость настаивается в течении 24 часов. В завершение останется лишь профильтровать продукт.
Предпоследний этап называется «перегонка». Его можно назвать самым трудоемким и продолжительным. Для данного этапа всегда требуется специальный аппарат, который, кстати, современные умельцы легко изготавливают своими руками. И, наконец, остается лишь очистка. Эта самый последний этап производства спирта в домашних условиях. Продукт практически готов, вот только ему не достает желаемой прозрачности. Добиться ее удастся при помощи самой обычной марганцовки, с которой жидкость настаивается в течении 24 часов. В завершение останется лишь профильтровать продукт.
Так как в последнее время количество ископаемого сырья, которое подходит для производства спирта в домашних условиях, стало постепенно снижаться, то появилась необходимость найти новые варианты. Как известно, появляется нехватка зерна, поэтому потребовалось отыскать ему достойную альтернативу. И она была быстро найдена — это древесные опилки. Данное сырье на сегодняшний день является максимально доступным для всех желающих. Найти его не составляет никакого труда. И, что не менее важно, древесные опилки стоят недорого. А в некоторых случаях их и вовсе удается найти совершенно бесплатно. Неудивительно, что обсуждаемое сырье пользуется огромной популярностью среди всех, кто занимается производством спирта в домашних условиях. Правда, изготовление данного вещества требует от человека определенных навыков, а также приобретения некоторого дополнительного оборудования.
И, что не менее важно, древесные опилки стоят недорого. А в некоторых случаях их и вовсе удается найти совершенно бесплатно. Неудивительно, что обсуждаемое сырье пользуется огромной популярностью среди всех, кто занимается производством спирта в домашних условиях. Правда, изготовление данного вещества требует от человека определенных навыков, а также приобретения некоторого дополнительного оборудования.
В первую очередь потребуется заготовить древесные опилки. Например, 1 килограмм исходного продукта. Очень важно, чтобы опилки были тщательно измельчены. Их потребуется хорошенько просушить, прежде чем приступить к производству метанола. Лучше всего отказаться от использования для этой цели духового шкафа и других аналогичных вариантов. Достаточно будет высыпать опилки тонким слоем на чистую газету в темном хорошо проветриваемом помещении и оставить в таком виде на несколько дней. Конечно же, в сырье также не должно быть были, каких-либо примесей и грязи. Специалисты отмечают, что лучше всего для данного процесса подходят именно опилки лиственных пород. А вот сырье от хвойных лучше не использовать.
А вот сырье от хвойных лучше не использовать.
Через холодильник, в котором будет осуществляться возгонка и электролит, в качестве которого отлично подойдет серная кислота, тщательно просушенные опилки отправляются в удобную колбу или другую аналогичную емкость. Они должны заполнить ее на 2/3 от общего объема. Далее потребуется нагреть массу до 150 градусов. Готовая жидкость обычно имеет легкий голубоватый оттенок. Конечно, не стоит забывать и об использовании качественного катализатора. Например, можно применить оксид алюминия — части корунда. Заливать очередную порцию в используемый сосуд можно сразу после того, как жидкость в нем приобретет черный цвет. Очень важно защитить свои органы дыхания респиратором или специальной маской. Лучше всего также подумать о прочных перчатках. Помещение, в котором изготавливается спирт из опилок, должно быть просторным и тщательно проветриваемый. На кухне этого делать не стоит, так как вокруг находятся продукты.
Готовое вещество может использоваться в качестве топлива и для каких-либо других аналогичных целей. А вот употреблять получившийся спирт внутрь и использовать для дальнейшего приготовления из него алкогольных напитков не рекомендуется. Всего из одного килограмма просушенных опилок можно получить приблизительно пол литра (чуть меньше) готового метанола.
А вот употреблять получившийся спирт внутрь и использовать для дальнейшего приготовления из него алкогольных напитков не рекомендуется. Всего из одного килограмма просушенных опилок можно получить приблизительно пол литра (чуть меньше) готового метанола.
Вы в лесу… Вокруг теснятся толстые и тонкие стволы деревьев. Для химика все они состоят из одного и того же материала — древесины, основной частью которой является органическое вещество — клетчатка (C 6 H 10 O 5) х. Клетчатка образует стенки клеток растений, т. е. их механический скелет; довольно чистую мы её имеем в волокнах хлопчатой бумаги и льна; в деревьях она встречается всегда вместе с другими веществами, чаще всего с лигнином, почти такого же химического состава, но обладающего иными свойствами. Элементарная формула клетчатки C 6 H 10 O 5 совпадает с формулой крахмала, свекловичный сахар имеет формулу C 12 H 2 2O 11 . Отношение числа атомов водорода к числу атомов кислорода в этих формулах такое же, как и в воде: 2:1. Поэтому эти и им подобные вещества в 1844 г. были названы «углеводами», т. е. веществами, как бы (но не на самом деле) состоящими из углерода и воды.
были названы «углеводами», т. е. веществами, как бы (но не на самом деле) состоящими из углерода и воды.
Углевод клетчатка имеет большой молекулярный вес. Молекулы её представляют длинные цепи, составленные из отдельных звеньев. В отличие от белых зёрен крахмала, клетчатка представляет прочные нити и волокна. Это объясняется различным, теперь точно установленным, структурным строением молекул крахмала и клетчатки. Чистая клетчатка в технике зовётся целлюлозой.
В 1811 г. академик Кирхгоф сделал важное открытие. Он взял обыкновенный крахмал, полученный из картофеля, и подействовал на него разбавленной серной кислотой. Под действием H 2 SO 4 произошёл гидролиз крахмала и он превратился в сахар:
Эта реакция имела важное практическое значение. На ней основано крахмало-паточное производство.
Но ведь клетчатка имеет ту же самую эмпирическую формулу, что и крахмал! Значит, из неё тоже можно получить сахар.
Действительно, в 1819 г. было впервые осуществлено и осахаривание клетчатки с помощью разбавленной серной кислоты. Для этих целей можно применять и концентрированную кислоту; русский химик Фогель в 1822 г. получил сахар из обычной бумаги, действуя на неё 87-процентным раствором H 2 SO 4 .
Для этих целей можно применять и концентрированную кислоту; русский химик Фогель в 1822 г. получил сахар из обычной бумаги, действуя на неё 87-процентным раствором H 2 SO 4 .
В конце XIX в. получение сахара и спирта из дерева стало интересовать уже и инженеров-практиков. В настоящее время спирт из целлюлозы получают в заводских масштабах. Способ, открытый в пробирке учёного, стад осуществляться в больших стальных аппаратах инженера.
Посетим гидролизный завод… В огромные варочные котлы (перколяторы) загружают опилки, стружки или щепу. Это — отходы лесопильных или деревообрабатывающих предприятий. Раньше эти ценные отходы сжигались или просто выбрасывались на свалку. Через перколяторы непрерывным током проходит слабый (0,2-0,6%) раствор минеральной кислоты (чаще всего серной). Долго держать одну и ту же кислоту в аппарате нельзя: содержащийся в ней сахар, полученный из древесины, легко разрушается. В перколяторах давление 8-10 ат, а температура 170-185°. При этих условиях гидролиз целлюлозы идёт значительно лучше, чем при обычных условиях, когда процесс весьма затруднителен. Из перколяторов получают раствор, содержащий около 4% сахара. Выход сахаристых веществ при гидролизе достигает 85 % от теоретически возможного (по уравнению реакции).
Из перколяторов получают раствор, содержащий около 4% сахара. Выход сахаристых веществ при гидролизе достигает 85 % от теоретически возможного (по уравнению реакции).
Рис. 8. Наглядная схема получения гидролизного спирта из древесины.
Для Советского Союза, имеющего необозримые лесные массивы и неуклонно развивающего промышленность синтетического каучука, получение спирта из древесины представляет особый интерес. Ещё в 1934 г. XVII съезд ВКП(б) постановил всемерно развивать производство спирта из опилок и отходов бумажной промышленности. Первые советские гидролизно-спиртовые заводы начали регулярно работать с 1938 г. За годы второй и третьей пятилеток у нас были построены и пущены заводы по выработке гидролизного спирта — спирта из древесины. Этот спирт в настоящее время всё в больших количествах перерабатывается в синтетический каучук. Это — спирт из непищевого сырья. Каждый миллион литров гидролизного этилового спирта освобождает для питания около 3 тыс. тонн хлеба или 10 тыс. тонн картофеля и, следовательно, около 600 га посевной площади. Для получения этого количества гидролизного спирта нужно 10 тыс. тонн опилок с 45-процентной влажностью, что может дать за год работы один лесопильный завод средней производительности.
тонн картофеля и, следовательно, около 600 га посевной площади. Для получения этого количества гидролизного спирта нужно 10 тыс. тонн опилок с 45-процентной влажностью, что может дать за год работы один лесопильный завод средней производительности.
Гидролизный спирт — свойства, получение и применение
Гидролизный спирт — этанол, получаемый дрожжевым брожением сахароподобных веществ, полученных гидролизом целлюлозы, содержащейся в отходах лесной промышленности.
- C6H12O6 → 2C2H5OH + 2CO2
Целлюлоза состоит из остатков молекул глюкозы, которая и образуется при кислотном гидролизе целлюлозы:
На гидролизных заводах из 1 т древесины получают до 200 л этилового спирта, что позволяет заменить 1,5 т картофеля или 0,7 т зерна.
Кроме целлюлозы, в состав клеточных оболочек входят еще несколько других углеводов, известных под общим именем гемицеллюлоз, извлекаемых из клеточных оболочек 1% раствором соляной или серной кислоты при нагревании.
Гидролизный спирт можно производить с использованием различных технологий гидролиза.
Некоторые схемы гидролиза предусматривают получение смеси этилового и метилового спиртов.
История
В 1819 году французский химик Анри Браконно обнаружил, что целлюлоза может быть преобразована (гидролизована) в сахара с помощью серной кислоты. Этот сахар потом сбраживается до алкоголя.
В Соединенных Штатах Standard Alcohol Company открыла первый завод по производству целлюлозного этанола в Южной Каролине в 1910 году. Позже был открыт второй завод в Луизиане. Однако оба завода были закрыты после Первой мировой войны по экономическим причинам.
Первая попытка коммерциализации процесса получения этанола из древесины была предпринята в Германии в 1898 году. Она включала использование разбавленной кислоты для гидролиза целлюлозы до глюкозы и была способна производить 7,6 литра этанола на 100 кг древесных отходов. Вскоре немцы разработали промышленный процесс, оптимизированный для выработки около 190 л. на тонну биомассы. Этот процесс вскоре добрался до США, кульминацией которого стали две коммерческие установки, работавшие на юго-востоке во время Первой мировой войны. Эти установки использовали так называемый «американский процесс» — одностадийный гидролиз разбавленной серной кислоты. Хотя выходы были вдвое меньше, чем в оригинальном немецком процессе (25 галлонов США (95 л) этанола на тонну против 50), производительность американского процесса была намного выше. Падение производства пиломатериалов вынудило заводы закрыться вскоре после окончания Первой мировой войны. Тем временем в «Лаборатории лесной продукции USFS» продолжалось небольшое, но постоянное исследование гидролиза разбавленной кислоты. Во время Второй мировой войны США снова обратились к целлюлозному этанолу, на этот раз для преобразования в бутадиен для производства синтетического каучука. Компания Vulcan Copper and Supply Company заключила контракт на строительство и эксплуатацию завода по переработке опилок в этанол.
на тонну биомассы. Этот процесс вскоре добрался до США, кульминацией которого стали две коммерческие установки, работавшие на юго-востоке во время Первой мировой войны. Эти установки использовали так называемый «американский процесс» — одностадийный гидролиз разбавленной серной кислоты. Хотя выходы были вдвое меньше, чем в оригинальном немецком процессе (25 галлонов США (95 л) этанола на тонну против 50), производительность американского процесса была намного выше. Падение производства пиломатериалов вынудило заводы закрыться вскоре после окончания Первой мировой войны. Тем временем в «Лаборатории лесной продукции USFS» продолжалось небольшое, но постоянное исследование гидролиза разбавленной кислоты. Во время Второй мировой войны США снова обратились к целлюлозному этанолу, на этот раз для преобразования в бутадиен для производства синтетического каучука. Компания Vulcan Copper and Supply Company заключила контракт на строительство и эксплуатацию завода по переработке опилок в этанол. Завод был основан на модификациях оригинального немецкого «процесса Шоллера», разработанного «Лабораторией продукции USFS». Эта установка достигла выхода этанола в 50 галлонов США (190 л) на сухую тонну, но все еще не приносила прибыли и была закрыта после войны.
Завод был основан на модификациях оригинального немецкого «процесса Шоллера», разработанного «Лабораторией продукции USFS». Эта установка достигла выхода этанола в 50 галлонов США (190 л) на сухую тонну, но все еще не приносила прибыли и была закрыта после войны.
С быстрым развитием ферментных технологий в последние два десятилетия процесс кислотного гидролиза постепенно сменился ферментативным гидролизом. Химическая предварительная обработка исходного сырья необходима для предварительн. гидролиза (отделения) гемицеллюлозы, чтобы она могла более эффективно превращаться в сахара. Предварительная обработка разбавленной кислотой разработана на основе ранних работ по кислотному гидролизу древесины в «Лаборатории лесной продукции USFS» . Недавно Лаборатория лесной продукции USFS совместно с Университетом Висконсин-Мэдисон разработали предварительную обработку сульфитом для преодоления непроходимости лигноцеллюлозы для надежного ферментативного гидролиза древесной целлюлозы.
Биоэтанол из растительной биомассы
Биоэтанол — это этиловый спирт, полученный путем ферментации из сахаров с помощью микроорганизмов. Обычно для этой цели используют дрожжи (Saccharomyces cerevisiae). Сахар поступает из растений, которые используют энергию солнечного света в процессе фотосинтеза для создания своих органических компонентов из углекислого газа (СО2). Сахара могут храниться в форме крахмала (например у зерновых, картофеля) или сахарозы (например у сахарной свеклы, сахарного тростника), или они могут быть включены в структурные компоненты растений (например, целлюлоза).), которые придают растению его форму и устойчивость. В настоящее время биоэтанол в основном получают путем сбраживания сахарозы (бразильский сахарный тростник) или гидролизатов крахмала (кукуруза, другие злаки). После перегонки и сушки этанол можно использовать в качестве топлива. Однако этот вид технической культуры создает конкуренцию с продовольственным рынком. Кроме того, ограниченные доступные площади и экологические проблемы, связанные с необходимой интенсификацией сельского хозяйства, препятствуют крупномасштабному производству этанола на основе крахмала.
Обычно для этой цели используют дрожжи (Saccharomyces cerevisiae). Сахар поступает из растений, которые используют энергию солнечного света в процессе фотосинтеза для создания своих органических компонентов из углекислого газа (СО2). Сахара могут храниться в форме крахмала (например у зерновых, картофеля) или сахарозы (например у сахарной свеклы, сахарного тростника), или они могут быть включены в структурные компоненты растений (например, целлюлоза).), которые придают растению его форму и устойчивость. В настоящее время биоэтанол в основном получают путем сбраживания сахарозы (бразильский сахарный тростник) или гидролизатов крахмала (кукуруза, другие злаки). После перегонки и сушки этанол можно использовать в качестве топлива. Однако этот вид технической культуры создает конкуренцию с продовольственным рынком. Кроме того, ограниченные доступные площади и экологические проблемы, связанные с необходимой интенсификацией сельского хозяйства, препятствуют крупномасштабному производству этанола на основе крахмала. Таким образом, целью ученых является все более широкое использование дешевых растительных остатков, таких как солома, древесные отходы и, или энергетических культур, таких как Просо прутьевидное (Panicum virgatum) или мискантус, которые не требуют интенсивного ведения сельского хозяйства и зачастую растут на бросовых угодьях.
Таким образом, целью ученых является все более широкое использование дешевых растительных остатков, таких как солома, древесные отходы и, или энергетических культур, таких как Просо прутьевидное (Panicum virgatum) или мискантус, которые не требуют интенсивного ведения сельского хозяйства и зачастую растут на бросовых угодьях.
Растительные остатки или энергетические культуры содержат мало крахмала или сахарозы, но содержат углеводы, хранящиеся в виде лигноцеллюлоз в клеточных стенках. Лигноцеллюлозы состоят из целлюлозы, гемицеллюлозы и неферментируемого лигнина («древесная масса»). Целлюлоза, как и крахмал, представляет собой полимер из шестиуглеродных молекул сахара, глюкозы, связанных между собой длинными цепями. Оба отличаются только типом связей. Гемицеллюлозы в основном состоят из пятиуглеродных сахаров, ксилозы и арабинозы которые соседствуют в разветвленных цепях.
Как традиционный этанол целлюлозный этанол может быть добавлен к бензину и использоваться во всех бензиновых автомобилях сегодня. Его потенциал по снижению выбросов парниковых газов выше, чем у традиционного этанола, получаемого из зерновых. Производство целлюлозного этанола может стимулировать экономический рост в сельских районах, открыть новые рынки для фермеров и увеличить использование возобновляемых источников энергии.
Его потенциал по снижению выбросов парниковых газов выше, чем у традиционного этанола, получаемого из зерновых. Производство целлюлозного этанола может стимулировать экономический рост в сельских районах, открыть новые рынки для фермеров и увеличить использование возобновляемых источников энергии.
Wood Alcohol: The Poisoner’s Handbook
Имя:______________________________________ Дата:_______
В дни, предшествовавшие сухому закону, Нью-Йорк пытался обновить свой офис коронера, улучшая лабораторные методы и используя науку для определения причин смерти и раскрытия преступлений. Вплоть до 1917 года коронер был выборным должностным лицом, не имевшим ни научного, ни медицинского образования. Убийства всех видов списывались как самоубийства или «стихийные бедствия». Яды стали популярным способом избавиться от соперника или члена семьи, потому что маловероятно, что их действие будет обнаружено.
В 1918 году Чарльз Норрис был назначен главным судмедэкспертом и стал пионером в области судебной токсикологии. Он, в свою очередь, нанял химика по имени Александр Геттлер, которому было поручено разработать методы определения того, были ли яды причиной смерти. Геттлер потратил время на измельчение печени и тестирование различных веществ. В годы, предшествовавшие запрету, Геттлер отметил рост числа смертей, связанных с отравлением древесным спиртом.
Он, в свою очередь, нанял химика по имени Александр Геттлер, которому было поручено разработать методы определения того, были ли яды причиной смерти. Геттлер потратил время на измельчение печени и тестирование различных веществ. В годы, предшествовавшие запрету, Геттлер отметил рост числа смертей, связанных с отравлением древесным спиртом.
——- Выдержка из Справочника отравителя ——-
Древесный спирт — технически известный как метиловый спирт, но также как древесный спирт, гидроксиметан, карбино, колониальный спирт, колумбийский спирт и, несколько лет спустя, метанол — сам по себе не был чем-то новым. Древние египтяне использовали его в процессах бальзамирования. На протяжении веков он был основным ингредиентом домашнего виски. Его химическая формула была определена в 1661 году химиком, который назвал его «духом ящика», потому что он получил его путем перегонки самшита. Термин «метил» произошел от греческого слова «methy» (что означает «вино») и «hyle» (что означает «дерево» или, точнее, «тропа деревьев»).
Химическая структура древесного спирта проста: три атома водорода связаны с одним атомом углерода (в кластере, известном как метильная группа), с одним атомом кислорода и другим атомом водорода. Его также легко сделать, как поняли промышленники и самогонщики, требуя немного больше, чем дрова и тепло. Этот процесс получил название деструктивной дистилляции. Плиты и куски дерева помещались в закрытый контейнер и нагревались не менее чем до 400 градусов по Фаренгейту (204 градуса по Цельсию). Когда древесина превращалась в древесный уголь, ее естественные жидкости испарялись. Пар можно было охладить, сконденсировать и перегнать в довольно мутный суп, содержащий метиловый спирт, ацетон и уксусную кислоту. Вторая перегонка позволила отделить чистый метиловый спирт, жидкость прозрачную, как стекло, и без запаха, как лед, от других ингредиентов.
————————————————— ————————
«Промышленный» спирт представлял собой в основном зерновой спирт (этанол) с добавлением других химикатов, чтобы сделать его непригодным для питья, метанол был одним из них. из обычных добавок. Добавление этих химикатов требовалось по закону после введения запрета, чтобы предотвратить использование технического спирта в качестве напитка. По сути, правительство приказало добавить в алкоголь химические вещества, которые сделали бы его непригодным для питья. В результате было много бутлегеров, которые пытались сделать промышленный спирт пригодным для питья и менее токсичным, перегоняя, разбавляя или смешивая его с другими химическими веществами. Ни одна из этих процедур не была особенно эффективной, и люди, решившие употреблять алкоголь нелегально, рисковали своей жизнью.
из обычных добавок. Добавление этих химикатов требовалось по закону после введения запрета, чтобы предотвратить использование технического спирта в качестве напитка. По сути, правительство приказало добавить в алкоголь химические вещества, которые сделали бы его непригодным для питья. В результате было много бутлегеров, которые пытались сделать промышленный спирт пригодным для питья и менее токсичным, перегоняя, разбавляя или смешивая его с другими химическими веществами. Ни одна из этих процедур не была особенно эффективной, и люди, решившие употреблять алкоголь нелегально, рисковали своей жизнью.
Почему метиловый спирт так опасен, а другие алкогольные напитки — нет? Ликеры обычно содержат около 3% этанола, который часто получают путем ферментации зерна, фруктов и овощей. Чтобы заменить ныне запрещенные спиртные напитки в эпоху Сухого закона, люди обратились к сомнительным методам дистилляции и напиткам, которые представляли собой смесь этанола и метанола. Даже небольшое количество метанола может быть смертельным, но некоторых людей этот риск не останавливает.
Метанол токсичен при проглатывании, вдыхании или даже попадании на кожу. Метанол при попадании в организм распадается на еще более токсичные вещества, этот процесс называется 9.0026 отравление . Ферменты в печени сначала превращают метанол в формальдегид, который затем превращается в муравьиную кислоту. Этот процесс занимает до 30 часов с момента первоначального воздействия метанола и означает, что вы, возможно, не умрете изначально от его употребления, но у вас могут появиться симптомы через день. Обычно первым признаком отравления метанолом является потеря зрения. Если человек выздоравливает от токсинов, слепота остается постоянной, поскольку муравьиная кислота фактически повреждает зрительный нерв.
Как и предсказывал Геттлер, число случаев отравления увеличилось. В 1926 января только в Нью-Йорке 1200 человек заболели ядовитым алкоголем и 400 умерли. Бутлегерство алкоголя, большая часть которого содержала метанол, продолжалась, отравления стали проблемой общественного здравоохранения. Геттлер продолжал работать над этими случаями, публикуя сообщения о смерти от алкоголя, чтобы привлечь внимание к проблеме. В 1933 году была отменена 18-я поправка, а также прекращена программа, требовавшая сделать технический спирт токсичным.
Геттлер продолжал работать над этими случаями, публикуя сообщения о смерти от алкоголя, чтобы привлечь внимание к проблеме. В 1933 году была отменена 18-я поправка, а также прекращена программа, требовавшая сделать технический спирт токсичным.
____ 1. Согласно статье, что из следующего верно? (Стандарт 1: Приведите текстовое свидетельство)
а) чаще всего от отравления метанолом страдали дети б) Сухой закон узаконил употребление метилового спирта
в) структура метанола и этанола идентична г) метиловый спирт токсичен и может вызвать слепоту
____ 2. Выберите предложение the поддерживает центральную идею статьи. (Стандарт 2: Основные идеи)
а) Яды стали популярным способом избавиться от соперника или члена семьи, потому что было маловероятно, что их действие будет обнаружено.
b) В годы, предшествовавшие запрету, Геттлер отметил рост числа смертей, связанных с отравлением древесным спиртом.
c) В 1918 году Чарльз Норрис был назначен главным судебно-медицинским экспертом и был пионером в области судебной токсикологии.
d) Ликеры обычно содержат около 3% этанола, который часто получают путем ферментации зерна, фруктов и овощей.
____ 3. Что лучше всего описывает структуру статьи? (Стандарт 2: Основные идеи)
a) описание того, как медицинское обследование изменилось в 1900-х годах
b) убедительное эссе о том, почему сухой закон не был экономически обоснованной идеей
c) сравнение метилового спирта с этиловым спиртом и рассказ о том, почему метанол токсичен
d ) авторское мнение о том, какой была жизнь во время Сухого закона
____ 4. Почему так долго не умирал человек после приема смертельной дозы метанола? (Стандарт 1: Приведите текстовое свидетельство)
а) потребовалось некоторое время, чтобы яд распространился по всему телу и достиг головного мозга
б) яд накапливается в тканях человека и иногда требуются годы, чтобы его убить
в) только некоторые люди чувствительны к метанолу
г) метанол превращается печенью в еще более токсичное вещество (токсикология)
____ 5. Какая связь между запретом и метанолом? (Стандарт 5: Отношения)
Какая связь между запретом и метанолом? (Стандарт 5: Отношения)
a) запрет привел к тому, что метанол был признан незаконным
b) запрет привел к увеличению числа отравлений метанолом
c) запрет уменьшил количество смертей, связанных с алкоголем
d) запрет продвинул область токсикологии
____ 6. Какое из следующих определений термина «отравление» является лучшим? (Стандарт 4: Значения)
а) процесс, при котором одно вещество превращается в другое
б) ряд химических реакций, протекающих в крови
в) процесс, при котором одно вещество превращается в другое вещество, более токсичное, чем первое
г) а процедура, при которой ученый определяет, насколько сильным является токсин
____ 7. Какие из следующих данных подтверждают прогноз Геттлера о том, что отравления метанолом увеличатся после запрета? (Стандарт 8: Рассуждение)
а) сравнение количества смертей от отравления метанолом до и после введения запрета
б) токсикологический отчет о том, как быстро крысы умирают от отравления метанолом
в) перечень конфискованного количества спирта, содержащего метанол
г) больничные записи, показывающие, сколько людей лечились от болезней, связанных с алкоголем
____ 8. Завершите аналогию: Этанол относится к зерну так же, как метанол к… (Стандарт 4: Значения)
Завершите аналогию: Этанол относится к зерну так же, как метанол к… (Стандарт 4: Значения)
а) яд б) дерево в) плод г) слепота
____ 9. Есть два потенциальных источника получения человеком метанола, какие они — обведите 2? (Стандарт 4: Значения)
а) его можно получить непосредственно из горящей древесины
б) его можно получить из органов человека, умершего от отравления метанолом
c) его можно ферментировать с использованием гниющих фруктов
d) его можно полученный из промышленного спирта, который был загрязнен
10. Своими словами опишите отличие молекулы этанола от молекулы метанола. (Стандарт 8: Визуальная информация)
Многообразие применений метанола от одежды до топлива: основные продукты и технологии | Инновация
Универсальный возобновляемый ресурс
, помогающий людям
жить лучше
* По данным компании, использующей нашу технологию
Метанол, также известный как метиловый спирт, является универсальным химическим веществом, широко используемым в промышленных целях и в нашей повседневной жизни. Его эффективность в качестве энергоносителя сделала его все более распространенным в качестве топлива для заводов и для производства электроэнергии. Потенциал метанола в качестве экологически безопасного источника топлива огромен, и во всем мире растет спрос на него как на многообещающий ресурс для новой эры чистой энергии. MGC является единственным комплексным производителем метанола с полным спектром продуктов и технологий, поддерживаемых глобальной производственной сетью.
Его эффективность в качестве энергоносителя сделала его все более распространенным в качестве топлива для заводов и для производства электроэнергии. Потенциал метанола в качестве экологически безопасного источника топлива огромен, и во всем мире растет спрос на него как на многообещающий ресурс для новой эры чистой энергии. MGC является единственным комплексным производителем метанола с полным спектром продуктов и технологий, поддерживаемых глобальной производственной сетью.
Метанол — вездесущий в природе
Метанол — это разновидность спирта, изготавливаемая в основном из природного газа. Это основной материал в уксусной кислоте и формальдегиде, а в последние годы он также все чаще используется в этилене и пропилене. Смешивание метанола с подобными веществами позволяет использовать его в качестве промежуточного материала для производства буквально тысяч метанола и производных метанола, используемых практически во всех сферах нашей жизни. Метанол и его производные, такие как уксусная кислота и формальдегид, образующиеся в результате химических реакций, используются в качестве основных материалов в акриловом пластике; синтетические ткани и волокна, используемые для изготовления одежды; клеи, краски и фанера, используемые в строительстве; и в качестве химического агента в фармацевтике и агрохимикатах. Его бесконечное множество применений сделали метанол повсеместным в нашей жизни и во всем обществе.
Его бесконечное множество применений сделали метанол повсеместным в нашей жизни и во всем обществе.
Использование метанола
Mitsubishi Gas Chemical — единственный в мире комплексный производитель метанола
В 1952 году Mitsubishi Gas Chemical стала первой компанией в Японии, успешно синтезировавшей природный газ в метанол. Более десяти лет MGC производила метанол и производные продукты на одном заводе в Ниигате на севере Японии. В 1970-х годах мы увеличили наши производственные мощности и открыли заводы за границей, чтобы быть ближе к более дешевым исходным материалам, чтобы удовлетворить быстро растущий спрос и повысить нашу конкурентоспособность. Разработанные технологии производства и методы добычи природного газа вывели нас на передовые позиции в индустрии метанола, и мы начали работу по созданию глобальной сети производства и продаж.
Вскоре мы использовали нашу запатентованную технологию для производства и поставок метанола на месте и во все регионы мира с помощью специально спроектированных танкеров. За более чем 70 лет постоянного расширения и диверсификации нашей деятельности мы превратились в ведущего мирового поставщика метана с полностью интегрированной глобальной сетью, ежегодно производящей и поставляющей около 2,5 миллионов тонн метана. Зарубежные заводы MGC поставляют 60% всего метанола, ежегодно импортируемого Японией. Наши технологии, наши сети и наш опыт делают нас единственным в мире комплексным производителем метанола и производных метанола.
За более чем 70 лет постоянного расширения и диверсификации нашей деятельности мы превратились в ведущего мирового поставщика метана с полностью интегрированной глобальной сетью, ежегодно производящей и поставляющей около 2,5 миллионов тонн метана. Зарубежные заводы MGC поставляют 60% всего метанола, ежегодно импортируемого Японией. Наши технологии, наши сети и наш опыт делают нас единственным в мире комплексным производителем метанола и производных метанола.
Метанол — безопасный, чистый и универсальный источник энергии будущего
Универсальность метанола делает его распространенным топливным ресурсом в электроэнергетике. В MGC мы используем метанол в качестве источника топлива не только в жидком виде, но и в виде высокоэффективных аккумуляторов на топливных элементах. В местах и условиях, где нецелесообразно использовать коммерческую энергию, в настоящее время обычно используются перезаряжаемые батареи, солнечные элементы и генераторы, работающие на газе. Топливные элементы MGC с прямым метанолом (DMFC) предлагают еще одно решение, не имеющее себе равных по эффективности и универсальности.
Использование метанола
В отличие от стандартных водородных топливных элементов, которые используют газообразный водород в качестве источника топлива, DMFC использует уникальный метамикс концентрированного 54% сжиженного метанола. Концентрированное топливо обеспечивает стабильное производство электроэнергии в течение всего срока службы топлива, что делает его более стабильным, чем водород, а также более легким по весу и более компактным, что упрощает его хранение и транспортировку. Это делает его идеальным топливом для выработки электроэнергии в чрезвычайных ситуациях, например, после стихийного бедствия, в качестве резервного источника топлива и в качестве основного источника топлива для объектов, недоступных для электросетей. Портативные источники питания, использующие DMFC, также тише бензиновых генераторов и не выделяют вредных газов, таких как окись углерода или окись азота. Это делает DMFC подходящим для проектов и мероприятий, проводимых как снаружи, так и внутри. Снаружи генераторы DMFC практически бесшумны на расстоянии всего 2-3 метра, а всего четыре литра метамикса могут питать генератор мощностью 200 Вт более восьми часов. Его универсальность, безопасность, надежность и экологичность сделают метанол основным источником энергии в будущем.
Снаружи генераторы DMFC практически бесшумны на расстоянии всего 2-3 метра, а всего четыре литра метамикса могут питать генератор мощностью 200 Вт более восьми часов. Его универсальность, безопасность, надежность и экологичность сделают метанол основным источником энергии в будущем.
Дополнительный бонус! Питьевой этанол,
непригодный для питья метанол
Этанол (этиловый спирт) и метанол (метиловый спирт) очень похожи, но очень разные. Оба являются спиртами, но этанол создается из ферментированного крахмала и сахара, которые содержатся в зерне, а метанол создается из природного газа, угля и биомассы. Их молекулярные структуры отличаются всего на несколько молекул, но эта небольшая вариация придает им совершенно разные свойства. Самое главное отличие состоит в том, что этанол является питьевой формой алкоголя, а метанол при употреблении очень токсичен.
Разница между этанолом и метанолом
Подать заявку на получение лицензии на производство, распространение и/или продажу метилового или древесного спирта
Вы должны иметь лицензию Программы защиты пищевых продуктов на производство, распространение и/или продажу метилового или древесный спирт в Массачусетсе.
Программа защиты пищевых продуктов
Детали Подать заявку на получение лицензии на производство, распространение и/или продажу метилового или древесного спирта
Что вам нужно для Подать заявку на получение лицензии на производство, распространение и/или продажу метилового или древесного спирта
Чтобы подать заявку на лицензию, вам необходимо заполнить и подписать полностью двухстраничную форму заявки (находится в файлах для скачивания ниже).
Пожалуйста, подайте единую заявку на все места продажи.
Сборы для Подать заявку на получение лицензии на производство, распространение и/или продажу метилового или древесного спирта
Оплата чеком или денежным переводом на имя:
Содружество Массачусетса
| Имя | Плата | Блок |
|---|---|---|
| Плата за подачу заявления | 150 долларов | за каждое приложение лицензии |
Как подать заявку Подать заявку на получение лицензии на производство, распространение и/или продажу метилового или древесного спирта
Отправьте все необходимые материалы и оплату по почте:
Департамент общественного здравоохранения
Food Protection Program
305 South St.
Jamaica Plain, MA 02130-3597
Подробнее для Подать заявку на получение лицензии на производство, распространение и/или продажу метилового или древесного спирта
Эта лицензия соответствует Общему закону штата Массачусетс, глава 94, раздел 303B.
загрузок для Подать заявку на получение лицензии на производство, распространение и/или продажу метилового или древесного спирта
Контакт для Подать заявку на получение лицензии на производство, распространение и/или продажу метилового или древесного спирта
Обратная связь
Спасибо, ваше сообщение отправлено в Программу защиты пищевых продуктов!
Обследование
Расскажите нам больше о своем опытеНасколько вы согласны со следующими утверждениями по шкале от 1 (категорически не согласен) до 5 (полностью согласен)?
Категорически не согласен
Полностью согласен
Эта страница полезна.
Категорически не согласен
Полностью согласен
1 Категорически не согласен 2 3 4 5 Полностью согласен
Эта страница проста в использовании.Категорически не согласен
Полностью согласен
1 Категорически не согласен 2 3 3 4 5 Полностью согласен
Я уверен, что найду нужную мне информацию.
Категорически не согласен
Полностью согласен
1 Категорически не согласен 2 3 4 5 Полностью согласен
Что ты пришел сюда делать сегодня?
Вы используете Mass.gov по профессиональным или личным причинам? * требуетсяПерсональный
Профессиональный
Какие еще отзывы о Mass.gov у вас есть? (По желанию)
Если у нас возникнут дополнительные вопросы по поводу вашего отзыва, можем ли мы связаться с вами? Если это так, введите свой адрес электронной почты ниже. (По желанию)
Эл. адрес
(По желанию)
Эл. адресСпасибо, ваш опрос отправлен команде Mass.gov!
Присоединяйтесь к пользовательской панелиОбратная связь
Метанол 99%- 1 галлон
Продукт SDS Leate
Метанол 99%
Из Википедии, бесплатная энциклопедия
Метанол , также известная AS
Methanol , также известная AS
Methanol , также известная AS
Methanol . карбинол , древесный спирт , древесный бензин или древесный спирт , представляет собой химическое соединение с химической формулой Ch4OH. Это простейший спирт, представляющий собой легкую, летучую, бесцветную, легковоспламеняющуюся, ядовитую жидкость с характерным запахом, который несколько мягче и слаще этанола (этилового спирта). Он используется в качестве антифриза, растворителя, топлива и денатуранта для этилового спирта.
Он используется в качестве антифриза, растворителя, топлива и денатуранта для этилового спирта.Метанол естественным образом образуется в результате анаэробного метаболизма многих разновидностей бактерий. В результате в атмосфере присутствует небольшая доля паров метанола. В течение нескольких дней атмосферный метанол окисляется кислородом с помощью солнечного света до углекислого газа и воды.
Метанол сгорает на воздухе с образованием углекислого газа и воды:
2 Ch4OH + 3 O2 → 2 CO2 + 4 h3O
Пламя метанола почти бесцветно. Следует соблюдать осторожность при сжигании метанола, чтобы не обжечься почти невидимым огнем.
Из-за своих ядовитых свойств метанол часто используется в качестве денатурирующей добавки к этанолу, производимому для промышленных целей? это добавление яда экономически освобождает промышленный этанол от довольно значительных налогов на спиртные напитки, которые в противном случае взимались бы, поскольку он является сущностью всех питьевых алкогольных напитков. Метанол часто называют древесным спиртом, потому что когда-то он производился в основном как побочный продукт деструктивной перегонки древесины. В настоящее время он производится синтетическим путем в несколько этапов. Короче говоря, природный газ и пар преобразуются в печи для получения водорода и монооксида углерода; затем газы водорода и монооксида углерода реагируют под давлением в присутствии катализатора. Стадия риформинга является эндотермической, а стадия синтеза экзотермической.
Метанол часто называют древесным спиртом, потому что когда-то он производился в основном как побочный продукт деструктивной перегонки древесины. В настоящее время он производится синтетическим путем в несколько этапов. Короче говоря, природный газ и пар преобразуются в печи для получения водорода и монооксида углерода; затем газы водорода и монооксида углерода реагируют под давлением в присутствии катализатора. Стадия риформинга является эндотермической, а стадия синтеза экзотермической.
История
В процессе бальзамирования древние египтяне использовали смесь веществ, включая метанол, который они получали при пиролизе древесины. Однако чистый метанол был впервые выделен в 1661 году Робертом Бойлем, который назвал его спиртом коробки, потому что он получил его путем перегонки самшита. Позже он стал известен как пироксильный спирт. В 1834 году французские химики Жан-Батист Дюма и Эжен Пелиго определили его химический состав. Они также ввели слово метилен в органическую химию, образовав его от греческого methy = «вино» + h?l? = лес (участок деревьев). Его предполагаемое происхождение было «спирт, сделанный из дерева (вещества)», но в нем есть ошибки греческого языка. Термин «метил» был получен примерно в 1840 году путем обратного образования метилена и затем применялся для описания «метилового спирта». Это было сокращено до «метанола» в 189 г.2 Международной конференции по химической номенклатуре. Суффикс -ил, используемый в органической химии для образования названий радикалов, был выделен из слова «метил».
Его предполагаемое происхождение было «спирт, сделанный из дерева (вещества)», но в нем есть ошибки греческого языка. Термин «метил» был получен примерно в 1840 году путем обратного образования метилена и затем применялся для описания «метилового спирта». Это было сокращено до «метанола» в 189 г.2 Международной конференции по химической номенклатуре. Суффикс -ил, используемый в органической химии для образования названий радикалов, был выделен из слова «метил».
В 1923 году немецкий химик Матиас Пьер, работавший на BASF, разработал средство для преобразования синтез-газа (смесь оксидов углерода и водорода) в метанол. В этом процессе использовался катализатор на основе хромата цинка, и требовались чрезвычайно агрессивные условия: давление в диапазоне от 30 до 100 МПа (от 300 до 1000 атм) и температура около 400 °C. Современное производство метанола стало более эффективным за счет использования катализаторов (обычно медных), способных работать при более низких давлениях.
Использование метанола в качестве моторного топлива привлекло внимание во время нефтяного кризиса 1970-х годов из-за его доступности и низкой стоимости. Проблемы возникли на раннем этапе разработки смесей бензин-метанол. Из-за его низкой цены некоторые продавцы бензина переусердствовали. Другие использовали неправильные методы смешивания и обработки. Это привело к проблемам потребителей и средств массовой информации, а также к тому, что в последний раз закончились смеси метанола. Однако по-прежнему существует большой интерес к использованию метанола в качестве чистого (несмешанного) топлива. Автомобили с гибким топливом, которые в настоящее время производятся General Motors, Ford и Chrysler, могут работать на любой комбинации этанола, метанола и/или бензина. Чистое спиртовое топливо станет более распространенным по мере производства автомобилей с более гибким топливом.
Проблемы возникли на раннем этапе разработки смесей бензин-метанол. Из-за его низкой цены некоторые продавцы бензина переусердствовали. Другие использовали неправильные методы смешивания и обработки. Это привело к проблемам потребителей и средств массовой информации, а также к тому, что в последний раз закончились смеси метанола. Однако по-прежнему существует большой интерес к использованию метанола в качестве чистого (несмешанного) топлива. Автомобили с гибким топливом, которые в настоящее время производятся General Motors, Ford и Chrysler, могут работать на любой комбинации этанола, метанола и/или бензина. Чистое спиртовое топливо станет более распространенным по мере производства автомобилей с более гибким топливом.
В 2006 году астрономы с помощью массива радиотелескопов MERLIN в обсерватории Джодрелл-Бэнк обнаружили в космосе большое облако метанола диаметром 300 миллиардов миль.
Производство
В настоящее время синтез-газ чаще всего производится из метанового компонента природного газа, а не из угля. Коммерчески практикуются три процесса. При умеренном давлении от 1 до 2 МПа (10–20 атм) и высоких температурах (около 850 °С) метан реагирует с водяным паром на никелевом катализаторе с образованием синтез-газа по химическому уравнению:
Коммерчески практикуются три процесса. При умеренном давлении от 1 до 2 МПа (10–20 атм) и высоких температурах (около 850 °С) метан реагирует с водяным паром на никелевом катализаторе с образованием синтез-газа по химическому уравнению:
Ch5 + h3O → CO + 3 h3
Эта реакция, обычно называемая конверсией метана с паром или SMR, является эндотермической, и ограничения теплопередачи накладывают ограничения на размер используемых каталитических реакторов. Метан также может подвергаться частичному окислению молекулярным кислородом с образованием синтез-газа, как показывает следующее уравнение:
2 Ch5 + O2 → 2 CO + 4 h3
эта реакция является экзотермической, и выделяемое тепло может использоваться на месте для реакция парометанового риформинга. Когда два процесса объединяются, это называется автотермическим риформингом. Соотношение CO и h3 можно регулировать с помощью реакции конверсии водяного газа
CO + h3O → CO2 + h3,
, чтобы обеспечить соответствующую стехиометрию для синтеза метанола.
Окись углерода и водород затем реагируют на втором катализаторе с образованием метанола. Сегодня наиболее широко используемым катализатором является смесь меди, оксида цинка и оксида алюминия, впервые использованная ICI в 1966 году. При 5–10 МПа (50–100 атм) и 250 °C он может катализировать производство метанола из углерода. монооксид и водород с высокой селективностью
СО + 2 ч3 → Ch4OH
Стоит отметить, что при производстве синтез-газа из метана образуется 3 моля водорода на каждый моль оксида углерода, в то время как на синтез метанола расходуется всего 2 моля водорода на каждый моль оксида углерода. Одним из способов борьбы с избыточным водородом является подача диоксида углерода в реактор синтеза метанола, где он также вступает в реакцию с образованием метанола в соответствии с химическим уравнением 9.0003
CO2 + 3 h3 → Ch4OH + h3O
Хотя природный газ является наиболее экономичным и широко используемым сырьем для производства метанола, можно использовать и другое сырье. Там, где природный газ недоступен, вместо него можно использовать светлые нефтепродукты. Южноафриканская фирма Sasol производит метанол, используя синтез-газ из угля.
Там, где природный газ недоступен, вместо него можно использовать светлые нефтепродукты. Южноафриканская фирма Sasol производит метанол, используя синтез-газ из угля.
Применение
Метанол ограниченно используется в качестве топлива для двигателей внутреннего сгорания, главным образом в силу того факта, что он не так легко воспламеняется, как бензин. Смеси метанола являются предпочтительным топливом в гоночных трассах с открытыми колесами, таких как автомобили Champ, а также в радиоуправляемых моделях самолетов (требуется в двигателях со свечами накаливания, которые в основном их приводят в действие), легковых и грузовых автомобилях. Гоночные автомобили для грязных кругов, такие как автомобили Sprint, поздние модели и модификации, используют метанол в качестве топлива для своих двигателей. Дрэг-рейсеры и гонщики по грязи также используют метанол в качестве основного источника топлива. Метанол требуется для двигателя с наддувом в Top Alcohol Dragster, и до конца сезона 2005 года все автомобили в Indianapolis 500 должны были работать на метаноле. Гонщики по грязи смешивают метанол с бензином и закисью азота для получения большей мощности, чем только бензин и закись азота.
Гонщики по грязи смешивают метанол с бензином и закисью азота для получения большей мощности, чем только бензин и закись азота.
Помимо непосредственного использования в качестве топлива, метанол (или, реже, этанол) используется в качестве компонента при химическом образовании биодизельного топлива.
Метанол является традиционным ингредиентом метилового спирта или денатурата.
Во время Второй мировой войны метанол использовался в качестве топлива в нескольких немецких военных ракетах под названием M-Stoff и в смеси как C-Stoff.
Одним из недостатков метанола как топлива является его коррозионная активность по отношению к некоторым металлам, включая алюминий. Метанол, хотя и является слабой кислотой, разрушает оксидное покрытие, которое обычно защищает алюминий от коррозии:
6 Ch4OH + Al2O3 → 2 Al(OCh4)3 + 3 h3O
Полученные метоксидные соли растворимы в метаноле, в результате чего получается чистая поверхность алюминия, которая легко окисляется некоторым количеством растворенного кислорода. Также метанол может действовать как окислитель:
Также метанол может действовать как окислитель:
6 Ch4OH + 2 Al → 2 Al(OCh4)3 + 3 h3
Этот взаимный процесс эффективно подпитывает коррозию до тех пор, пока либо металл не будет съеден, либо концентрация Ch4OH станет незначительной.
При производстве из древесины или других органических материалов получаемый органический метанол (биоспирт) был предложен в качестве возобновляемой альтернативы углеводородам на основе нефти. Однако нельзя использовать ВА100 (100% биоспирт) в современных бензиновых автомобилях без модификации. Метанол также используется в качестве растворителя и антифриза в трубопроводах и жидкости для омывания ветрового стекла. Однако наибольшее использование метанола на сегодняшний день приходится на производство других химикатов. Около 40% метанола превращается в формальдегид, а оттуда в такие разнообразные продукты, как пластмассы, фанера, краски, взрывчатые вещества и ткани для перманентной печати.
На некоторых очистных сооружениях в сточные воды добавляют небольшое количество метанола, чтобы обеспечить источник углерода для денитрифицирующих бактерий, которые превращают нитраты в азот.
Также в начале 1970-х годов компания Mobil разработала процесс превращения метанола в бензин, который производит бензин, готовый для использования в автомобилях. Одно промышленное предприятие было построено в Новой Зеландии в 1980-х годах.
В 1990-х годах в США для производства присадки к бензину метил-трет-бутилового эфира (МТБЭ) использовалось большое количество метанола. 1990 Закон о чистом воздухе требовал, чтобы некоторые крупные города использовали МТБЭ в своем бензине для уменьшения фотохимического смога. Однако к концу 1990-х годов было обнаружено, что МТБЭ просочился из резервуаров для хранения бензина в грунтовые воды в количествах, достаточных для того, чтобы повлиять на вкус муниципальной питьевой воды во многих районах. Кроме того, в исследованиях на животных было обнаружено, что МТБЭ является канцерогеном. В результате несколько штатов запретили использование МТБЭ, и его будущее производство остается неопределенным.
Топливные элементы прямого действия на метаноле уникальны тем, что работают при низких температурах и атмосферном давлении, что позволяет их миниатюризировать до беспрецедентной степени. Это, в сочетании с относительно простым и безопасным хранением и обращением с метанолом, может открыть возможность для бытовой электроники на топливных элементах.
Это, в сочетании с относительно простым и безопасным хранением и обращением с метанолом, может открыть возможность для бытовой электроники на топливных элементах.
Другие химические производные метанола включают диметиловый эфир, который заменил хлорфторуглероды в качестве пропеллента для аэрозольных распылителей, и уксусную кислоту.
В настоящее время планируется использовать химическое вещество в экологически чистых топливных элементах для портативных компьютеров, элементы будут разлагать метанол с помощью электрохимического процесса.
Здоровье и безопасность
Метанол является опьяняющим, но не ядовитым. Он токсичен из-за его распада (токсичности) ферментом алкогольдегидрогеназой в печени с образованием муравьиной кислоты и формальдегида, которые вызывают слепоту из-за разрушения зрительного нерва. Проглатывание метанола также может быть смертельным из-за его депрессивных свойств ЦНС так же, как отравление этанолом. Он попадает в организм при проглатывании, вдыхании или всасывании через кожу. Ткань плода не переносит метанол. Опасные дозы будут накапливаться, если человек регулярно подвергается воздействию паров или работает с жидкостью без защиты кожи. Если метанол был проглочен, следует немедленно обратиться к врачу. Обычная смертельная доза составляет 100–125 мл (4 жидких унции). Токсические эффекты проявляются через несколько часов, и эффективные противоядия часто могут предотвратить необратимое повреждение. Это лечится этанолом или фомепизолом. Любой из этих препаратов замедляет действие алкогольдегидрогеназы на метанол посредством конкурентного ингибирования, так что он выводится почками, а не превращается в токсичные метаболиты.
Ткань плода не переносит метанол. Опасные дозы будут накапливаться, если человек регулярно подвергается воздействию паров или работает с жидкостью без защиты кожи. Если метанол был проглочен, следует немедленно обратиться к врачу. Обычная смертельная доза составляет 100–125 мл (4 жидких унции). Токсические эффекты проявляются через несколько часов, и эффективные противоядия часто могут предотвратить необратимое повреждение. Это лечится этанолом или фомепизолом. Любой из этих препаратов замедляет действие алкогольдегидрогеназы на метанол посредством конкурентного ингибирования, так что он выводится почками, а не превращается в токсичные метаболиты.
Начальными симптомами интоксикации метанолом являются симптомы угнетения центральной нервной системы: головная боль, головокружение, тошнота, нарушение координации, спутанность сознания, сонливость, а при достаточно больших дозах — потеря сознания и смерть. Начальные симптомы воздействия метанола обычно менее выражены, чем симптомы, возникающие при приеме внутрь такого же количества этилового спирта.
После исчезновения начальных симптомов через 10–30 часов после первоначального воздействия метанола возникает второй набор симптомов: нечеткость или полная потеря зрения вместе с ацидозом. Эти симптомы возникают в результате накопления токсичных уровней формиата в кровотоке и могут привести к смерти от дыхательной недостаточности. Эфирные производные метанола не обладают этой токсичностью.
Этанол иногда денатурируют (подделывают) и, таким образом, делают непригодным для питья путем добавления метанола. Результат известен как метилированный спирт или «мет» (используется в Великобритании). (Последнее не следует путать с метамфетамином, распространенным сокращением от метамфетамина.)
Чистый метанол использовался в гонках на открытых колесах с середины 1960-х годов. В отличие от нефтяных пожаров, возгорание метанола можно потушить простой водой (хотя плотность метанола меньше, чем у воды, они смешиваются, и добавление воды заставит огонь использовать свое тепло для кипячения воды). Кроме того, огонь на метаноле горит незаметно, в отличие от бензина, который горит густым черным дымом. Если на трассе возникнет пожар, дым не будет мешать обзору быстро приближающихся водителей. Решение навсегда перейти на метанол в американских гонках IndyCar стало результатом разрушительной аварии и взрыва на 19-й трассе.64 Индианаполис 500, в результате которого погибли водители Эдди Сакс и Дэйв Макдональд.
Кроме того, огонь на метаноле горит незаметно, в отличие от бензина, который горит густым черным дымом. Если на трассе возникнет пожар, дым не будет мешать обзору быстро приближающихся водителей. Решение навсегда перейти на метанол в американских гонках IndyCar стало результатом разрушительной аварии и взрыва на 19-й трассе.64 Индианаполис 500, в результате которого погибли водители Эдди Сакс и Дэйв Макдональд.
Одна проблема, связанная с добавлением метанола в автомобильное топливо, подчеркивается недавним воздействием на грунтовые воды топливной добавки метил-трет-бутилового эфира (МТБЭ). Протекающие подземные резервуары для хранения бензина создали шлейфы МТБЭ в грунтовых водах, которые в конечном итоге испортили колодезную воду. Высокая растворимость метанола в воде вызывает опасения, что аналогичное загрязнение колодезной воды может возникнуть в результате широкого использования метанола в качестве автомобильного топлива.
Метиловый спирт – обзор
ScienceDirectЗарегистрироватьсяВойти
Для метилового спирта он обнаружил, что весовое отношение водорода к углероду составляет 3,6:1.
Из: Encyclopedia of Analytical Science (Second Edition), 2005 г.
PlusAdd to Mendeley Greene Shepherd, in Encyclopedia of Toxicology (Second Edition), 2005 г. например, выбросы некоторых заводов как побочный продукт разложения органического материала), а также использование человеком метанола в качестве растворителя. Метанол имеет низкое давление паров и испаряется в воздух. При испарении в воздух метанол разлагается в результате реакции с переносимыми по воздуху гидроксильными радикалами, и его период полураспада составляет около 18 дней. Метанол можно удалить из воздуха с помощью осадков. Ожидается, что при попадании в воду разложение метанола будет происходить путем биодеградации. Предполагается, что при попадании в почву метанол разлагается и подвержен выщелачиванию. Из-за низкого давления паров метанола происходит быстрое испарение с сухих поверхностей. Просмотреть главуКнига покупок Прочитать главу полностью URL: https://www. Метанол может выделяться из природных источников (например, выбросы некоторых растений, как побочный продукт разложения органического материала), а также при использовании человеком метанола в качестве растворителя. Согласно Реестру токсичных выбросов Агентства по охране окружающей среды (EPA), в 2011 году компании из самых разных отраслей сообщили, что в воздух было выброшено 103 534 415 фунтов метанола, 13 987 379 фунтов было выпущено в виде подземных инъекций, 3 838 319 фунтов было выпущено в воду, а 2 255 595 фунтов было выпущено на сушу. Метанол является нормальной частью рациона человека (в небольших количествах содержится в свежих фруктах и овощах) и вырабатывается в организме в результате метаболического распада других продуктов. Пища является основным источником воздействия метанола на человека. Воздействие метанола на рабочем месте может происходить при вдыхании и кожном контакте с этим соединением. Наборы данных национального мониторинга содержания метанола в воздухе или воде не обнаружены. Было обнаружено, что в сельской местности уровни метанола в воздухе колеблются от 2 до 12 частей на миллиард. В готовой питьевой воде обнаружен метанол. Просмотреть главуКнига покупок Прочитать главу полностью URL: https://www.sciencedirect.com/science/article/pii/B978012386454300748X John Carroll, in Natural Gas Hydrates (Fourth Edition), 90 20920398 Метанол очень полезен для борьбы с образованием гидратов в трубопроводах и технологическом оборудовании. В качестве примера проблемы обработки, которая может возникнуть при использовании метанола, возможно, что метанол будет концентрироваться в потоке сжиженного нефтяного газа (СНГ). Сжиженный нефтяной газ состоит в основном из пропана и смешанных бутанов. Известно, что пропан + метанол и н-бутан + метанол образуют азеотропы (Leu et al., 19).92). Эти азеотропы означают, что разделить системы с помощью бинарной перегонки невозможно. С практической точки зрения, именно поэтому метанол может появляться в неприемлемом количестве в продукте LPG. Кроме того, метанол-углеводородные системы, как известно, трудно точно моделировать. Однако прикладная термодинамика добилась больших успехов в этой области. Инженер-конструктор должен с осторожностью относиться к моделям, выбранным для выполнения расчетов в таких системах. Еще одним интересным побочным эффектом использования метанола являются ингибиторы коррозии. Другой потенциальной проблемой коррозии, связанной с впрыском метанола, является растворенный воздух в метаноле. Метанол для ингибитора обычно хранится на месте в резервуарах, открытых для атмосферы. Это позволяет некоторому количеству воздуха растворяться в метаноле. Затем при впрыскивании в технологический процесс или трубопровод могут возникнуть проблемы с коррозией. Обычно количество растворенного кислорода невелико, но в долгосрочной перспективе это может вызвать проблемы. Просмотреть главуКнига покупок Прочитать главу 9 полностью0003 URL: https://www.sciencedirect.com/science/article/pii/B978012821771 Muhammet Kayfeci, Ali Keçebaş, in Solar Hydrogen Production, 2019 Methanol is obtained from hydrogen и CO жидкий при нормальных условиях и имеет высокое содержание водорода; благодаря этим свойствам метанол можно рассматривать как подходящее автомобильное топливо. Принцип использования гласит, что водород образуется при расщеплении метанола, и полученный водород расходуется в качестве топлива. Потери энергии в процессе фрагментации достаточно велики, поэтому КПД системы невысок. Чтобы преодолеть это отрицание, были разработаны высокоэффективные топливные элементы, работающие непосредственно на метаноле. Согласно проведенным исследованиям, транспортное средство, работающее на метанольном риформере, выбрасывает на 40–70 % больше CO 9 .0463 2 по сравнению с аналогичным бензиновым автомобилем. Кроме того, есть также выбросы CO и углеводородов. Метанол является токсичным, смешиваемым с водой и очень коррозионным веществом. Из-за этих особенностей необходимы более конкретные меры безопасности по сравнению с бензином при транспортировке и использовании. Посмотреть главуКнига покупок Прочитать главу полностью URL: https://www.sciencedirect.com/science/article/pii/B9780128148532000047 R. Muthudineshkumar, R. Anand, Advances in Eco-Fuels for the Sustainable Environment, 2019 sciencedirect.com/science/article/pii/B0123694000006037
sciencedirect.com/science/article/pii/B0123694000006037 Воздействие и мониторинг воздействия
 Население в целом может подвергаться воздействию метанола при вдыхании атмосферного воздуха, приеме пищи и питьевой воды, использовании продуктов, содержащих метанол (например, краски, жидкость для стеклоочистителей), и курении табачных изделий. В сигаретном дыме были обнаружены уровни мтанола 80–180 мкг на сигарету.
Население в целом может подвергаться воздействию метанола при вдыхании атмосферного воздуха, приеме пищи и питьевой воды, использовании продуктов, содержащих метанол (например, краски, жидкость для стеклоочистителей), и курении табачных изделий. В сигаретном дыме были обнаружены уровни мтанола 80–180 мкг на сигарету. 5.12 Предостережение
 Однако метанол может оказывать неблагоприятное воздействие на последующую обработку углеводородного потока.
Однако метанол может оказывать неблагоприятное воздействие на последующую обработку углеводородного потока. На одном участке в трубопровод был закачан метанол для предотвращения образования гидратов. Химические ингибиторы также были введены для предотвращения коррозии. Ингибиторы были на спиртовой основе, и метанол растворял ингибитор. Это привело к некоторым неожиданным проблемам с коррозией.
На одном участке в трубопровод был закачан метанол для предотвращения образования гидратов. Химические ингибиторы также были введены для предотвращения коррозии. Ингибиторы были на спиртовой основе, и метанол растворял ингибитор. Это привело к некоторым неожиданным проблемам с коррозией.57
4.
 10 Methanol
10 Methanol Его отрицательные свойства и высокие выбросы не позволяют метанолу быть очень предпочтительным топливом.
Его отрицательные свойства и высокие выбросы не позволяют метанолу быть очень предпочтительным топливом. характеристики горения. Его можно использовать в качестве топлива в основном в виде смеси 85% метанола и 15% углеводородов (M85) или в виде чистого метанола. Для этих детализированных топливных двигателей метанол предлагает потенциал для значительного повышения эффективности двигателя по сравнению с бензиновыми двигателями; оценки варьируются от 15% до 30% в зависимости от степени модификации существующих бензиновых двигателей. Выбросы также значительно улучшились. Дополнительное повышение энергоэффективности транспортных средств может быть достигнуто путем замены бензиновых двигателей меньшими, легкими двигателями эквивалентной мощности, разработанными для метанола.
 Меньшие двигатели сжигают меньше топлива напрямую и уменьшают вес автомобиля, тем самым обеспечивая дополнительную экономию топлива. Метанол можно использовать в качестве топлива для топливных элементов, поскольку его легко хранить, но его можно использовать и для портативных источников энергии.
Меньшие двигатели сжигают меньше топлива напрямую и уменьшают вес автомобиля, тем самым обеспечивая дополнительную экономию топлива. Метанол можно использовать в качестве топлива для топливных элементов, поскольку его легко хранить, но его можно использовать и для портативных источников энергии.
Просмотреть главуКнига покупок
Прочитать главу полностью
URL: https://www.sciencedirect.com/science/article/pii/B9780081027288000061
S.T. Coelho, José Goldemberg, Encyclopedia of Energy, 2004
2,5 Метанол
Метанол (или метиловый спирт) — это спирт (CH 3 OH), который использовался в качестве альтернативного топлива в транспортных средствах с гибким топливом, работающих на M85. (смесь 85% метанола и 15% бензина). Однако в настоящее время метанол широко не используется, потому что производители автомобилей больше не производят автомобили, работающие на метаноле. Метанол также можно использовать для получения метил- трет--бутиловый эфир (МТБЭ), оксигенат, который смешивают с бензином для повышения октанового числа и снижения выбросов загрязняющих веществ. Однако производство и использование МТБЭ сократились из-за того, что МТБЭ загрязняет грунтовые воды. В будущем метанол может стать важным топливом, помимо этанола, для производства водорода, необходимого для питания автомобилей на топливных элементах; такой процесс сейчас находится в стадии разработки.
Метанол также можно использовать для получения метил- трет--бутиловый эфир (МТБЭ), оксигенат, который смешивают с бензином для повышения октанового числа и снижения выбросов загрязняющих веществ. Однако производство и использование МТБЭ сократились из-за того, что МТБЭ загрязняет грунтовые воды. В будущем метанол может стать важным топливом, помимо этанола, для производства водорода, необходимого для питания автомобилей на топливных элементах; такой процесс сейчас находится в стадии разработки.
Метанол преимущественно получают путем паровой конверсии природного газа с получением синтез-газа, который затем подают в реактор в присутствии катализатора для получения метанола и водяного пара. Несмотря на то, что помимо природного газа могут использоваться различные виды сырья, сегодняшняя экономика отдает предпочтение природному газу. Синтез-газ представляет собой комбинацию монооксида углерода (CO) и водорода (H 2 ). Подобно транспортным средствам, работающим на этаноле, транспортные средства, работающие на метаноле, выделяют меньшее количество загрязнителей воздуха, таких как углеводороды, твердые частицы и NO x , чем автомобили, работающие на бензине. Однако обращение с метанолом гораздо более опасно по сравнению с этанолом из-за его сильного негативного воздействия на здоровье.
Однако обращение с метанолом гораздо более опасно по сравнению с этанолом из-за его сильного негативного воздействия на здоровье.
Мировой спрос на метанол составляет около 32 миллионов тонн в год и незначительно увеличивается примерно на 2–3 % в год, но со значительными изменениями в профиле отрасли. С начала 19В 80-х годах более крупные установки, использующие новые эффективные технологии низкого давления, заменили менее эффективные небольшие установки. Структура спроса в Европе меняется; Метанол когда-то подмешивался в бензин (когда его стоимость составляла примерно половину стоимости бензина), но теперь он не может конкурировать с более низкими ценами на нефть. Компенсацией этому стал поэтапный отказ от этилированного бензина в развитых странах, что потребовало использования бензина с измененным составом. Соединенные Штаты продвигали использование МТБЭ, полученного из метанола. Соединенные Штаты производят почти четверть мировых поставок метанола, но в мире наблюдается значительный избыток метанола. На Рисунке 2 показаны мировые поставки метанола, указывающие на этот значительный избыток мощностей.
На Рисунке 2 показаны мировые поставки метанола, указывающие на этот значительный избыток мощностей.
Рисунок 2. Предложение метанола в мире. Данные Института метанола (www.methanol.org).
Крупнейший рынок метанола в США – производство МТБЭ; в США около 50 заводов. По оценкам, в 1996 году 3,3 миллиарда галлонов МТБЭ было использовано для смешивания с чистым бензином с измененным составом, обслуживающим 30% рынка бензина США. МТБЭ вытесняет в 10 раз больше бензина, чем все другие альтернативные виды автомобильного топлива вместе взятые.
Цены на метанол в США значительно изменились с 1989; они удвоились к 1994 г. и вернулись к уровню 1993 г. к 1996 г. В 2002 г. цены на метанол достигли 64 центов/галлон, что немного выше европейских цен (61,7 центов/галлон) и азиатских цен (55,9 центов/галлон).
Просмотреть главуКнига покупок
Прочитать главу полностью
URL: https://www.sciencedirect.com/science/article/pii/B012176480X001777
R. J. Пирсон, Дж.В.Г. Turner, в Comprehensive Renewable Energy, 2012
J. Пирсон, Дж.В.Г. Turner, в Comprehensive Renewable Energy, 2012
5.16.3.4.3 Контакт с кожей/глазами
Метанол может попасть в организм через кожу или глаза; его действие отличается от действия бензина, которого также следует избегать, поскольку он особенно сильно сушит кожу из-за действия растворителя. Machiele [86] утверждает, что нечастые разбрызгивания метанола не вызывают особого беспокойства, но проблемы начинают возникать при постоянном или частом воздействии, когда накопление метанола в организме может достигать опасных уровней, так что возможно острое отравление; Утверждается, что это эквивалентно полному погружению руки в воду на 4 часа, чтобы смерть была возможной. Этот сценарий считается маловероятным, и его можно решить с помощью обычного подхода к охране здоровья и безопасности (что в настоящее время имеет место в случае промышленного использования метанола). В целом опасность биоаккумуляции метанола незначительна [9].1].
Просмотреть главуКнига покупок
Прочитать главу полностью
URL: https://www. sciencedirect.com/science/article/pii/B9780080878720005229
sciencedirect.com/science/article/pii/B9780080878720005229
Джеймс Дж. Спейт, доктор философии, доктор наук Природный газ (второе издание), 2019 г.
8.6 Процессы на основе метанола
Метанол, вероятно, является одним из самых универсальных растворителей в отрасли переработки природного газа. Исторически метанол был первым коммерческим органическим физическим растворителем и использовался для ингибирования образования гидратов, дегидратации, очистки газов и извлечения жидкостей (Kohl and Nielsen, 19).97). Большинство этих применений связаны с низкими температурами, когда физические свойства метанола выгодны по сравнению с другими растворителями, которые имеют проблемы с высокой вязкостью или даже образованием твердых частиц. Работа при низких температурах, как правило, устраняет наиболее существенный недостаток метанола, высокую потерю растворителя. Кроме того, метанол относительно недорог и прост в производстве, что делает этот растворитель очень привлекательной альтернативой для процессов обработки газа.
Метанол имеет благоприятные физические свойства по сравнению с другими растворителями, за исключением давления паров. Преимущества низкой вязкости метанола при низкой температуре проявляются в улучшении перепада давления в холодильной камере установок закачки и улучшении теплообмена. Метанол имеет гораздо более низкое поверхностное натяжение по сравнению с другими растворителями. Высокое поверхностное натяжение способствует возникновению проблем с пенообразованием в контакторах. Процессы с метанолом, вероятно, не подвержены пенообразованию. Однако основным недостатком метанола является высокое давление паров, которое в несколько раз больше, чем у гликолей или аминов. Чтобы свести к минимуму потери метанола и повысить абсорбцию воды и кислых газов, температура абсорбера или сепаратора обычно не превышает -20°F.
Высокое давление паров метанола вначале может показаться существенным недостатком из-за высоких потерь растворителя. Однако высокое давление пара также имеет значительные преимущества. Хотя это часто не учитывается, отсутствие тщательного смешивания газа и растворителя может создать серьезные проблемы. Из-за высокого давления паров метанол полностью смешивается с газовым потоком перед холодильной камерой. Гликоли, поскольку они не испаряются полностью, могут потребовать специальных насадок и их размещения в холодильной камере для предотвращения замерзания. Перенос растворителя в другие последующие процессы также может представлять серьезную проблему. Поскольку метанол более летуч, чем гликоли, амины и другие физические растворители, включая нежирное масло, метанол обычно не используется на стадии регенерации в этих последующих процессах. Отпарная колонна концентрирует метанол в верхнем конденсаторе, откуда его можно удалить и дополнительно очистить. К сожалению, если гликоли переносятся в аминные звенья, гликоль концентрируется в растворе и потенциально начинает разлагаться и, возможно, разбавлять раствор амина.
Хотя это часто не учитывается, отсутствие тщательного смешивания газа и растворителя может создать серьезные проблемы. Из-за высокого давления паров метанол полностью смешивается с газовым потоком перед холодильной камерой. Гликоли, поскольку они не испаряются полностью, могут потребовать специальных насадок и их размещения в холодильной камере для предотвращения замерзания. Перенос растворителя в другие последующие процессы также может представлять серьезную проблему. Поскольку метанол более летуч, чем гликоли, амины и другие физические растворители, включая нежирное масло, метанол обычно не используется на стадии регенерации в этих последующих процессах. Отпарная колонна концентрирует метанол в верхнем конденсаторе, откуда его можно удалить и дополнительно очистить. К сожалению, если гликоли переносятся в аминные звенья, гликоль концентрируется в растворе и потенциально начинает разлагаться и, возможно, разбавлять раствор амина.
Использование метанола в дальнейшем использовалось при разработке процесса Rectisol либо отдельно, либо в виде смесей толуола и метанола для более селективного удаления сероводорода и выделения углекислого газа в головной продукт (Ranke and Mohr, 1985). Толуол имеет дополнительное преимущество, поскольку карбонилсульфид более растворим в толуоле, чем в метаноле. Процесс Rectisol был в первую очередь разработан для удаления двуокиси углерода и сероводорода (наряду с другими серосодержащими соединениями) из газовых потоков, образующихся в результате частичного окисления угля, нефти и нефтяных остатков. Способность метанола поглощать эти нежелательные компоненты сделала его естественным растворителем. К сожалению, при низких температурах метанол также имеет высокое сродство к углеводородным компонентам газовых потоков. Например, пропан лучше растворяется в метаноле, чем в углекислом газе. Существует две версии процесса Rectisol — двухступенчатая и однократная. Первым этапом двухстадийного процесса является обессеривание перед конверсией сдвига; концентрации сероводорода и диоксида углерода составляют около 1% и 5% по объему соответственно. Регенерация метанола после десульфурации исходного газа дает сырье с высоким содержанием серы для извлечения серы.
Толуол имеет дополнительное преимущество, поскольку карбонилсульфид более растворим в толуоле, чем в метаноле. Процесс Rectisol был в первую очередь разработан для удаления двуокиси углерода и сероводорода (наряду с другими серосодержащими соединениями) из газовых потоков, образующихся в результате частичного окисления угля, нефти и нефтяных остатков. Способность метанола поглощать эти нежелательные компоненты сделала его естественным растворителем. К сожалению, при низких температурах метанол также имеет высокое сродство к углеводородным компонентам газовых потоков. Например, пропан лучше растворяется в метаноле, чем в углекислом газе. Существует две версии процесса Rectisol — двухступенчатая и однократная. Первым этапом двухстадийного процесса является обессеривание перед конверсией сдвига; концентрации сероводорода и диоксида углерода составляют около 1% и 5% по объему соответственно. Регенерация метанола после десульфурации исходного газа дает сырье с высоким содержанием серы для извлечения серы. Прямоточный процесс применим только для продуктов парциального окисления под высоким давлением. Прямоточный процесс также применим, когда соотношение содержания сероводорода и диоксида углерода неблагоприятно, около 1:50 (Esteban et al., 2000).
Прямоточный процесс применим только для продуктов парциального окисления под высоким давлением. Прямоточный процесс также применим, когда соотношение содержания сероводорода и диоксида углерода неблагоприятно, около 1:50 (Esteban et al., 2000).
Физический/химический комбинированный процесс очистки, в котором алканоламин (моно- или диэтаноламин) в смеси с метанолом более эффективен, чем один физический растворитель, используемый на многих газоочистных сооружениях. Основное преимущество этого растворителя заключается в хорошей физической абсорбции физического компонента растворителя в сочетании с химической реакцией амина. Комбинация химически активного амина с полярным физическим растворителем с низкой температурой кипения, таким как метанол, дает большие преимущества в абсорбции компонентов диоксида углерода и серы, поскольку: (1) низкое содержание серы в газообразном продукте, (2) низкое содержание углерода диоксида в очищенном газе, (3) удаление путем абсорбции следовых компонентов, таких как цианистый водород, карбонилсульфид, производные меркаптана и производные углеводородов с более высокой молекулярной массой, (4) относительно низкая температура регенерации, поскольку метанол имеет температуру кипения ниже температура кипения воды и (5) растворитель не вызывает коррозии, поэтому можно использовать оборудование из углеродистой стали.
Недавно был разработан процесс с использованием метанола, в котором одновременно возможно обезвоживание, удаление кислых газов и контроль точки росы по углеводородам (Rojey and Larue, 1988; Rojey et al., 1990). IFPEXOL-1 используется для удаления воды и контроля точки росы по углеводородам; процесс IFPEXOL-2 используется для удаления кислых газов. Новая концепция процесса IFPEXOL-1 заключается в использовании части насыщенного водой входного сырья для извлечения метанола из водной части низкотемпературного сепаратора. Такой подход решил основную проблему с закачкой метанола на крупных предприятиях, а именно получение метанола путем перегонки. Помимо этого очень простого открытия, холодная часть процесса удивительно похожа на основной процесс впрыска метанола. Модификации процесса включают промывку водой углеводородной жидкости из низкотемпературного сепаратора для увеличения извлечения метанола. Процесс IFPEXOL-2 для удаления кислых газов очень похож на процесс аминового типа, за исключением рабочих температур. Абсорбер работает при температуре ниже -20°F, чтобы свести к минимуму потери метанола, а регенератор работает при температуре около 9°С.0 фунтов на квадратный дюйм. Для извлечения метанола требуется охлаждение конденсатора регенератора. Этот процесс обычно следует за процессом IFPEXOL-1, поэтому чрезмерное поглощение углеводородов не представляет такой серьезной проблемы (Minkkinen and Jonchere, 1997).
Абсорбер работает при температуре ниже -20°F, чтобы свести к минимуму потери метанола, а регенератор работает при температуре около 9°С.0 фунтов на квадратный дюйм. Для извлечения метанола требуется охлаждение конденсатора регенератора. Этот процесс обычно следует за процессом IFPEXOL-1, поэтому чрезмерное поглощение углеводородов не представляет такой серьезной проблемы (Minkkinen and Jonchere, 1997).
Просмотреть главуКнига покупок
Прочитать главу полностью
URL: https://www.sciencedirect.com/science/article/pii/B9780128095706000084
John C.M. Браст, клиническая нейротоксикология, 2009 г.
Метанол
Метанол (метиловый спирт, древесный спирт) присутствует в промышленных растворителях, карбюраторной жидкости, антифризе, топливных баках и других продуктах. Заражение контрафактными спиртными напитками привело к эпидемиям отравления метанолом. 104, 105 По сравнению с этанолом метанол вызывает менее выраженное опьянение; у пациентов часто наблюдаются нарушения зрения, боль в животе и метаболический ацидоз с четким сенсорным контролем. Метанол метаболизируется алкогольдегидрогеназой (АДГ) до формальдегида и муравьиной кислоты. Муравьиная кислота, ингибируя митохондриальную цитохромоксидазу, токсична для нейронов, включая ганглиозные клетки сетчатки. Потеря зрения часто начинается через 12 и более часов после приема внутрь и прогрессирует до полной слепоты с нереактивными зрачками и гиперемией диска зрительного нерва. Возможны делирий, судороги, кома, угнетение дыхания, брадикардия и смерть. Лечение включает сердечную и респираторную поддержку и внутривенное введение этанола, который конкурирует с метанолом за АДГ, тем самым замедляя метаболизм метанола до токсичных продуктов. 4-Метилпиразол (фомепизол), ингибирующий АДГ, также может замедлять метаболизм метанола. 106 Фолат назначают, поскольку он ускоряет метаболизм муравьиной кислоты в углекислый газ. Гемодиализ рекомендуется пациентам с симптомами или значительным метаболическим ацидозом, концентрацией метанола в крови выше 25 мг/дл или почечной недостаточностью.
Метанол метаболизируется алкогольдегидрогеназой (АДГ) до формальдегида и муравьиной кислоты. Муравьиная кислота, ингибируя митохондриальную цитохромоксидазу, токсична для нейронов, включая ганглиозные клетки сетчатки. Потеря зрения часто начинается через 12 и более часов после приема внутрь и прогрессирует до полной слепоты с нереактивными зрачками и гиперемией диска зрительного нерва. Возможны делирий, судороги, кома, угнетение дыхания, брадикардия и смерть. Лечение включает сердечную и респираторную поддержку и внутривенное введение этанола, который конкурирует с метанолом за АДГ, тем самым замедляя метаболизм метанола до токсичных продуктов. 4-Метилпиразол (фомепизол), ингибирующий АДГ, также может замедлять метаболизм метанола. 106 Фолат назначают, поскольку он ускоряет метаболизм муравьиной кислоты в углекислый газ. Гемодиализ рекомендуется пациентам с симптомами или значительным метаболическим ацидозом, концентрацией метанола в крови выше 25 мг/дл или почечной недостаточностью. После лечения может восстановиться или не восстановиться зрение, а у выживших могут проявляться аномальные движения, такие как паркинсонизм или дистония. 107 Вскрытие показало некроз скорлупы и распространенное повреждение нейронов в коре головного мозга, мозжечке, стволе головного мозга и спинном мозге. 108
После лечения может восстановиться или не восстановиться зрение, а у выживших могут проявляться аномальные движения, такие как паркинсонизм или дистония. 107 Вскрытие показало некроз скорлупы и распространенное повреждение нейронов в коре головного мозга, мозжечке, стволе головного мозга и спинном мозге. 108
Просмотр книги Глава Черта
Читать полная глава
URL: https://www.sciendirect.com/science/article/pii/B9780323052603500356
95232603500356
95232603500356
в окружающей среде
in in in in in in in in in ormentiais Синтез метанола основан на ранней работе немецкой компании BASF по реакции между монооксидом углерода и водородом. В 1923 году было обнаружено, что синтез метанола является селективным, когда ZnO–Cr 2 O 3 используется катализатор. Компания Mobil Oil разработала цеолитный катализатор, способный с очень высокой эффективностью преобразовывать метанол в углеводороды. Этот процесс был испытан на экспериментальной установке, а в Новой Зеландии строится полномасштабная установка. Просмотреть главуКнига покупок Прочитать главу полностью URL: https://www.sciencedirect.com/science/article/pii/B9780080287348500127 Сухой закон предназначался для сдерживания употребления алкоголя, который считался вредным для здоровья и доставлял неудобства обществу. Мало того, что этого почти невозможно добиться, так еще и стремление правительства заблокировать потребление технического спирта приведет к непреднамеренным, но катастрофическим отравлениям, параличу и гибели тысяч пьющих от рук бутлегеров. Закон Волстеда содержит два существенных исключения из запрета на продажу алкоголя: спиртные напитки, отпускаемые врачами по рецепту (как правило, виски и другие крепкие напитки), и спиртные напитки, производимые и используемые для религиозных таинств (обычно вино) священниками, раввинами и министры. Раздел 7 Закона Волстеда разрешает употребление алкогольных напитков в качестве лечения врачом, который «добросовестно полагает, что употребление такого спиртного напитка в качестве лекарства таким лицом необходимо и принесет ему облегчение от какого-либо известного недуга». Закон также допускал злоупотребления, позволяя врачам назначать алкоголь, даже если они не могли физически осмотреть пациента, при условии, что их диагноз за пределами учреждения был основан «на наилучшей доступной информации». То, что Волстед сделал исключение для врачей, чтобы они прописывали, а фармацевты, чтобы распределять «лекарственный ликер», поскольку лечение больных противоречило даже преобладающим взглядам медицинской профессии в то время. Волстед уточнил, что врачи должны были получить разрешение от Министерства финансов США, чтобы выписывать алкоголь, который производился для аптек одобренными правительством винокурнями. Отделение выдавало врачам блокноты с пронумерованными формами и бланками с водяными знаками, которые затем могли подписывать рецепты, позволяющие пациентам выпивать до одной пинты спиртных напитков (обычно виски) каждые 10 дней. Лекарство было дорогостоящим — пациенту пришлось заплатить около 3 долларов (37,50 долларов в долларах 2016 года) врачу за диагностику и еще 3 доллара фармацевту. Врачи обычно прописывали одну унцию виски взрослым (меньше детям, которых также лечили ликером) каждые несколько часов при заболеваниях с формальными названиями, такими как «грипп» (грипп), «насморк» (простуда) и «фарингит» (боль в горле), но также и при серьезных заболеваниях, таких как высокое кровяное давление, болезни сердца, депрессия, туберкулез и рак, на том основании, что алкоголь способствует пищеварению и физической силе. Юридическое освобождение принесло непредвиденную прибыль врачам и фармацевтам. Даже АМА всего через два года после введения Сухого закона сняла свои возражения против лечебной ценности спиртных напитков, одобрив их как средство для лечения почти 30 болезней. Для чикагской фармацевтической компании Walgreens популярность медицинского алкоголя привела к колоссальным доходам — сеть выросла с 20 аптек за 19 лет. За годы до сухого закона промышленный (и непригодный для питья) спирт использовался на фабриках в качестве растворителя и чистящей жидкости, а также для производства моющих средств, ароматизирующих экстрактов и духи. Алкоголь облагался акцизным налогом как напиток в Соединенных Штатах до 1906, когда в процессе, заимствованном из Европы, добавлялись «денатуранты» или вещества, которые придавали зерновому (этиловому) спирту неприятный вкус или запах, чтобы предотвратить его использование в напитках. Затем «денатурированный» спирт можно было использовать в производстве без уплаты налогов. К началу действия сухого закона в 1920 году десятки миллионов галлонов денатурированного этилового спирта были произведены для промышленного использования, и правительство США считало его освобожденным от производства, поскольку он содержал токсичные добавки, делающие его опасным для питья. Спирт денатурировали, смешивая его с древесным (метиловым) спиртом, вредной жидкостью, которая могла вызвать слепоту или смерть при попадании внутрь. Но бутлегеры начали использовать денатурированный технический спирт, замаскированный под виски — который назвали бы «гнилой кишкой» из-за его воздействия на внутренние органы пьющего — еще за несколько месяцев до вступления в силу сухого закона. Журнал Literary Digest в выпуске от 10 января 1920 года сообщил, что десятки людей недавно умерли, в том числе 57 в Хартфорде, штат Коннектикут, и сотни других ослепли после употребления «предполагаемого виски», содержащего древесный спирт. Власти арестовали несколько бутлегеров после того, как отследили испорченный алкоголь до Нью-Йорка. Примерно к 1922 году запасы подлинного виски, произведенного до Сухого закона и предназначенного для кражи бутлегерами, закончились. Поскольку промышленный спирт производится в больших масштабах, бутлегеры начинают захватывать его, полагая, что они могут перегонять и продавать его как питьевой алкоголь. К 1923 января Запретное бюро министерства финансов уже было сосредоточено на недопущении того, чтобы организованная преступность перерабатывала промышленный спирт для продажи пьющим. Правительство поручило производителям жидкости для промышленного использования денатурировать ее, добавив четырехпроцентный древесный спирт, ядовитый для человека в очень малых количествах. Но бутлегерам, тем не менее, удалось украсть большое количество алкоголя, чтобы переработать его в дешевую выпивку для ничего не подозревающих пьющих, часто из низших классов, которые не могли позволить себе высококачественный ликер. Правительство сообщило, что к середине 1920-х годов около 90 миллионов галлонов спирта для промышленного использования было переработано в стране, из них около 6 миллионов зарезервировано для медицинских и исследовательских целей, а остальные предназначались для сотен коммерческих предприятий. В середине 1920-х годов бутлегеры в больших количествах продавали ядовитый алкоголь, смешанный с другими жидкостями, выдавали его за виски и другие напитки, и люди начали умирать. В 1926 году в Нью-Йорке около 750 человек погибли после употребления контрабандного ликера с добавлением древесного спирта. Критики, в том числе антисухой «мокрый», возложили ответственность за смерть и ранения на безрассудную политику правительства, такую как отсутствие предупредительных надписей на емкостях с техническим спиртом. Доктор Николас Мюррей Батлер из Колумбийского университета обвинил правительство США, которое одобрило денатурант древесного спирта, в «узаконенном убийстве». К 1930 году, когда доходы американских бутлегеров достигли примерно 3 миллиардов долларов, криминальные дистрибьюторы на какое-то время перешли от технического спирта к перегонке собственного спирта-сырца с сахаром, дрожжами и другими ингредиентами, производя урожай, который считался достаточно хорошим и безопасным для питья. . Но в том же году надвигалась еще одна национальная волна отравлений алкоголем, на этот раз без участия правительства. В 1928 году пара бостонских бутлегеров, шурины Гарри Гросс и Макс Рейзман, начали производство нелегального алкогольного напитка на основе экстракта ямайского имбиря, старого запатентованного лекарственного средства из порошка, смешанного со спиртом. Мужчины продавали смесь как «Джинджер Джейк», жидкий экстракт имбиря, используемый как лекарство от простуды, судорог и малярии. С 1929 по 1930 год они распространили около 1000 галлонов этого вещества. Тысячи бутылок Ginger Jake продавались как «жидкое лекарство» с подмигиванием и кивком в виде дешевого алкогольного напитка. Он был отправлен в Род-Айленд и Джорджию и в конечном итоге продан от побережья до побережья. Но линдол оказался токсичным для нервных клеток, вызывая паралич ниже пояса, в основном необратимый, включая импотенцию у мужчин. Это быстро произвело эпидемию поражения ног пьющих. От 35 000 до 100 000 человек страдали ярко выраженной медленной хромотой, называемой «джейк-нога» или «джейк-походка». Гросс и Райсман были привлечены к ответственности не по Закону Волстеда, а по законам Министерства сельского хозяйства о пищевых продуктах и лекарствах за производство поддельного продукта. Оба были признаны виновными в тяжких преступлениях и приговорены к двум годам лишения свободы. Гросс попал в тюрьму, но приговор Райзману был отложен. В последующие десятилетия людей с «неподвижной ногой» можно было увидеть хромающими и попрошайничающими на улицах крупных городов. Но они мало сочувствовали, так как многие считали, что с ними произошло по их собственной вине. Через несколько месяцев после трагедии в середине 1930-го года музыкальные группы начали писать песни о прискорбном длительном воздействии Джинджер Джейк. В июне 1930 года Allen Brothers, кантри-группа из Теннесси, записали «Jake Walk Blues», которая начиналась так: Я не могу есть, я не могу говорить, Господи, теперь я не могу ходить, Теперь мне нечего терять, Потому что я Джейк, гуляющий папа, с блюзом Джейк Уок. Метанол
 Требовалось очень высокое давление, 200–400 атм. В 1960-х ICI разработала катализатор Cu-ZnO, который позволил снизить давление до 50-100 атм. На сегодняшний день технология получения метанола из синтез-газа хорошо разработана, и по крайней мере пять процессов коммерчески доступны.
Требовалось очень высокое давление, 200–400 атм. В 1960-х ICI разработала катализатор Cu-ZnO, который позволил снизить давление до 50-100 атм. На сегодняшний день технология получения метанола из синтез-газа хорошо разработана, и по крайней мере пять процессов коммерчески доступны. Алкоголь как лекарство и яд. Запрет: интерактивная история алкоголя
901 и 2 Poison А в 1930 марта пара мужчин в Бостоне придумывала незаконный и токсичный алкогольный напиток «Джинджер Джейк», от которого пострадало до 100 000 человек по всей Америке.
А в 1930 марта пара мужчин в Бостоне придумывала незаконный и токсичный алкогольный напиток «Джинджер Джейк», от которого пострадало до 100 000 человек по всей Америке. В 1917 году Американская медицинская ассоциация выпустила декларацию, в которой говорилось, что алкоголь не имеет «научной ценности» как тонизирующее или стимулирующее средство для исцеления и «следует в дальнейшем не поощрять его употребление». Тем не менее, сомнительный и устаревший взгляд на алкоголь как на лекарство — тысячелетняя традиция — был закреплен в законе и оказался прибыльным как для врачей, так и для фармацевтов, а также поводом для «пациентов» набирать выпивку из 1920 до окончания сухого закона в 1933 году.
В 1917 году Американская медицинская ассоциация выпустила декларацию, в которой говорилось, что алкоголь не имеет «научной ценности» как тонизирующее или стимулирующее средство для исцеления и «следует в дальнейшем не поощрять его употребление». Тем не менее, сомнительный и устаревший взгляд на алкоголь как на лекарство — тысячелетняя традиция — был закреплен в законе и оказался прибыльным как для врачей, так и для фармацевтов, а также поводом для «пациентов» набирать выпивку из 1920 до окончания сухого закона в 1933 году. Волстед специально запретил повторные выписки (хотя и не отдельные рецепты) и заставил фармацевтов указывать дату, которая «отменяла» рецепт сразу после его выписки.
Волстед специально запретил повторные выписки (хотя и не отдельные рецепты) и заставил фармацевтов указывать дату, которая «отменяла» рецепт сразу после его выписки. от 20 до 525 магазинов по всей стране в 1929 году. Но Walgreens по сей день настаивает на том, что ее быстрый рост был связан с сочетанием эффективного управления, ее вкусного бренда мороженого, сделанного в Чикаго, который подается в автоматах с газированной водой в ее магазинах, и, в частности, изобретения солодового молочного коктейля, сделанного его сотрудником Иваром «Поп» Коулсоном в 1922 году.
от 20 до 525 магазинов по всей стране в 1929 году. Но Walgreens по сей день настаивает на том, что ее быстрый рост был связан с сочетанием эффективного управления, ее вкусного бренда мороженого, сделанного в Чикаго, который подается в автоматах с газированной водой в ее магазинах, и, в частности, изобретения солодового молочного коктейля, сделанного его сотрудником Иваром «Поп» Коулсоном в 1922 году.

 Однако, по оценкам правительства, бутлегеры захватили около 10 миллионов галлонов. Бутлегеры, прекрасно зная, что в нем содержится древесный спирт, пытались удалить токсины путем кипячения смеси зерна и древесного спирта в нелегальных перегонных кубах. Древесный спирт закипел и начал испаряться в конденсатор при температуре 151 градус по Фаренгейту, в то время как для закипания зерновой жидкости потребовалось 173 градуса. Часть ядовитой древесной жидкости испарилась, но, как позже узнала общественность, химически невозможно удалить весь древесный спирт. Даже небольшое количество оставшегося древесного спирта при приеме внутрь поражало нервную систему, например, зрительный нерв, вызывая слепоту.
Однако, по оценкам правительства, бутлегеры захватили около 10 миллионов галлонов. Бутлегеры, прекрасно зная, что в нем содержится древесный спирт, пытались удалить токсины путем кипячения смеси зерна и древесного спирта в нелегальных перегонных кубах. Древесный спирт закипел и начал испаряться в конденсатор при температуре 151 градус по Фаренгейту, в то время как для закипания зерновой жидкости потребовалось 173 градуса. Часть ядовитой древесной жидкости испарилась, но, как позже узнала общественность, химически невозможно удалить весь древесный спирт. Даже небольшое количество оставшегося древесного спирта при приеме внутрь поражало нервную систему, например, зрительный нерв, вызывая слепоту. В тот канун Нового года, когда люди пили в 1927 году, многие набились в больницу Бельвю в первый день Нового года, и 41 человек умер. Позже в том же году погибли еще сотни жителей Нью-Йорка. В январе того же года в Филадельфии умерло 307 человек, а в Чикаго — 163 человека. Сообщается, что только в одном округе Канзаса было отравлено около 15 000 человек. До 50 000 человек могли умереть от перепрофилированного технического спирта по всей стране, а тысячи других были поражены параличом. В 1927 только в Нью-Йорке, из 480 000 галлонов спиртных напитков, изъятых агентами министерства по запрету, 98 процентов содержали ядовитые добавки, а спиртные напитки, изъятые из 55 городских баров, содержали следы древесного спирта.
В тот канун Нового года, когда люди пили в 1927 году, многие набились в больницу Бельвю в первый день Нового года, и 41 человек умер. Позже в том же году погибли еще сотни жителей Нью-Йорка. В январе того же года в Филадельфии умерло 307 человек, а в Чикаго — 163 человека. Сообщается, что только в одном округе Канзаса было отравлено около 15 000 человек. До 50 000 человек могли умереть от перепрофилированного технического спирта по всей стране, а тысячи других были поражены параличом. В 1927 только в Нью-Йорке, из 480 000 галлонов спиртных напитков, изъятых агентами министерства по запрету, 98 процентов содержали ядовитые добавки, а спиртные напитки, изъятые из 55 городских баров, содержали следы древесного спирта. Правительство приняло новый закон, снизивший максимальное содержание древесного спирта в техническом спирте до двух процентов. Через несколько недель после катастрофы 1927 января Дж. М. Доран, главный химик Бюро по запрету, работал над совершенствованием нового, менее вредного, но все же неприятного запаха и вкуса денатуранта, такого как керосин. Позже федералы одобрили добавление таких ингредиентов, как йод, эфир, никотин и формальдегид, чтобы попытаться сделать промышленный спирт слишком ужасным для питья.
Правительство приняло новый закон, снизивший максимальное содержание древесного спирта в техническом спирте до двух процентов. Через несколько недель после катастрофы 1927 января Дж. М. Доран, главный химик Бюро по запрету, работал над совершенствованием нового, менее вредного, но все же неприятного запаха и вкуса денатуранта, такого как керосин. Позже федералы одобрили добавление таких ингредиентов, как йод, эфир, никотин и формальдегид, чтобы попытаться сделать промышленный спирт слишком ужасным для питья. Но чтобы скрыть алкоголь от агентов Сухого закона, мужчины добавили в качестве примеси химическое вещество три-орто-крезилфосфат, известное как линдол. Химикат без запаха и вкуса был пластификатором, используемым для изготовления целлулоидной пленки и взрывчатых веществ. Гросс и Рейзман заявили, что производитель заверил их в безопасности Линдола.
Но чтобы скрыть алкоголь от агентов Сухого закона, мужчины добавили в качестве примеси химическое вещество три-орто-крезилфосфат, известное как линдол. Химикат без запаха и вкуса был пластификатором, используемым для изготовления целлулоидной пленки и взрывчатых веществ. Гросс и Рейзман заявили, что производитель заверил их в безопасности Линдола. Многие из раненых были бедняками, иммигрантами и афроамериканцами.
Многие из раненых были бедняками, иммигрантами и афроамериканцами.
