Формиаты или соли муравьиной кислоты
Муравьиная кислота эффективнее других средств позволяет удалять лед с взлетно-посадочных полос и проезжей части дорог без вреда для окружающей среды.
Природа как крупнейший производитель
Муравьи и медузы используют это вещество для собственной защиты и для добывания пищи. Многим неоднократно доводилось испытать его действие на собственном опыте, случайно прикоснувшись к листьям крапивы. Речь идет о муравьиной кислоте – едкой пахучей жидкости природного происхождения, которая привлекает внимание людей уже на протяжении нескольких столетий.
Впервые эта простейшая карбоновая кислота в чистом виде была выделена английским естествоиспытателем Джоном Рэем в 1671 году. Он поместил рыжих лесных муравьев в стеклянную колбу с водой, довел сосуд до кипения, и в полученном дистилляте обнаружил кислую жидкость, которую назвал муравьиной кислотой. Первый успешный лабораторный синтез этого вещества датируется 1855 годом. Его осуществил французский химик Марселен Бертло. Концерн BASF начал проявлять интерес к муравьиной кислоте в 20-х годах прошлого века и приступил к ее крупномасштабному производству в 1935 году – после того, как этот продукт стал пользоваться спросом во многих отраслях промышленности.
Его осуществил французский химик Марселен Бертло. Концерн BASF начал проявлять интерес к муравьиной кислоте в 20-х годах прошлого века и приступил к ее крупномасштабному производству в 1935 году – после того, как этот продукт стал пользоваться спросом во многих отраслях промышленности.
В настоящее время муравьиная кислота является широко востребованным химикатом. Д-р Татьяна Леви, менеджер по инновациям в подразделении BASF Intermediates, называет ее «поистине универсальным продуктом». Муравьиная кислота в течение нескольких десятилетий находит успешное применение в самых разных областях. Так, она используется при изготовлении кормов для животных (в качестве консерванта), в кожевенном и текстильном производстве, а также в качестве компонента буровых растворов при освоении нефтяных месторождений. «Кроме того, в тесном взаимодействии с заказчиками мы постоянно находим для муравьиной кислоты новые области применения», − добавляет д-р Леви.
Соли муравьиной кислоты
Формиаты, применяемые в качестве реагентов для удаления льда и снега зимой, стоят дороже, нежели соли и вещества, препятствующие скольжению (мелкий гравий или песок). Однако разница становится не столь значительной, если учесть все последующие затраты. Так, соль (хлорида натрия) нарушает водный режим и баланс питательных веществ в почве, а также приводит к коррозии конструктивных элементов зданий, дорожных покрытий и мостов. Эффективность агентов, предотвращающих скольжение, − весьма неоднозначна, поскольку они загрязняют городскую среду и требуют больших трудозатрат при уборке. Напротив, соли муравьиной кислоты экологичны и обладают малой коррозионной активностью; они надежно защищают дороги и тротуары от снега и льда (без нежелательных побочных эффектов). При этом отпадает необходимость в дополнительных расходах, связанных с пересадкой деревьев и кустарников, а также с ремонтом зданий.
Однако разница становится не столь значительной, если учесть все последующие затраты. Так, соль (хлорида натрия) нарушает водный режим и баланс питательных веществ в почве, а также приводит к коррозии конструктивных элементов зданий, дорожных покрытий и мостов. Эффективность агентов, предотвращающих скольжение, − весьма неоднозначна, поскольку они загрязняют городскую среду и требуют больших трудозатрат при уборке. Напротив, соли муравьиной кислоты экологичны и обладают малой коррозионной активностью; они надежно защищают дороги и тротуары от снега и льда (без нежелательных побочных эффектов). При этом отпадает необходимость в дополнительных расходах, связанных с пересадкой деревьев и кустарников, а также с ремонтом зданий.
Обработка территории аэропорта с использованием формиатов
Европейские аэропорты борются с обледенением с помощью химических средств. «Соли муравьиной кислоты уже в течение десяти с лишним лет используются для удаления льда с ВПП и рулежных дорожек аэропортов», − поясняет д-р Леви. Добавка этих солей, также известных как формиаты, приводит к тому, что при понижении температуры до 0 оС вода не замерзает. В зависимости от концентрации антиобледенителя точка замерзания может быть доведена до −50оС, что значительно разнится с температурой окружающего воздуха. Соответственно, формиаты быстро удаляют тонкие наледи, эффективно препятствуют отложению снега и образованию нового льда на взлетно-посадочных полосах. При этом эти вещества не представляют опасности для окружающей среды. «Соли муравьиной кислоты вместе с талой водой могут попадать в стоки, но вред от них (по сравнению с другими антиобледенителями) может быть минимальным – из-за способности формиатов к биологическому разложению, в процессе которого расходуется очень небольшое количество кислорода», − подчеркивает Татьяна Леви.
Добавка этих солей, также известных как формиаты, приводит к тому, что при понижении температуры до 0 оС вода не замерзает. В зависимости от концентрации антиобледенителя точка замерзания может быть доведена до −50оС, что значительно разнится с температурой окружающего воздуха. Соответственно, формиаты быстро удаляют тонкие наледи, эффективно препятствуют отложению снега и образованию нового льда на взлетно-посадочных полосах. При этом эти вещества не представляют опасности для окружающей среды. «Соли муравьиной кислоты вместе с талой водой могут попадать в стоки, но вред от них (по сравнению с другими антиобледенителями) может быть минимальным – из-за способности формиатов к биологическому разложению, в процессе которого расходуется очень небольшое количество кислорода», − подчеркивает Татьяна Леви.
Служба по уборке снега в аэропорту Цюриха использует формиаты с 2005 года. «Мы возлагаем очень большие надежды на надежные антиобледенители, не наносящие ущерба окружающей среде, − объясняет Ханс-Петер Молл, ответственный за техническое обслуживание летного поля в аэропорту Цюриха. – Необходимо, чтобы эти составы быстро вступали в реакцию с наледью на ВПП и рулевых дорожках, обладали длительным сроком службы, хорошо совмещались с другими материалами и оставались безвредными. Наш опыт показывает, что соли муравьиной кислоты превосходят любые другие антиобледенители по данным критериям».
– Необходимо, чтобы эти составы быстро вступали в реакцию с наледью на ВПП и рулевых дорожках, обладали длительным сроком службы, хорошо совмещались с другими материалами и оставались безвредными. Наш опыт показывает, что соли муравьиной кислоты превосходят любые другие антиобледенители по данным критериям».
Муниципальные службы проявляют растущий интерес к формиатам
Позитивный опыт аэропортов по использованию формиатов в качестве альтернативных антиобледенителей вызвал интерес у муниципальных органов. Снегоуборочные службы в странах Скандинавии, Швейцарии и Австрии применяют эти химикаты для удаления льда с проезжей части, велосипедных дорожек и тротуаров – там, где требуется повышенная осторожность (к примеру, на бульварах древесными посадками или в районах с исторической застройкой). В Базеле уже на протяжении многих лет аналогичным образом убирают остатки снега с искусственных покрытий спортивных арен. При этом вначале очистка производится механическим способом, а затем тонкий оставшийся слой снега растапливается с помощью формиатов.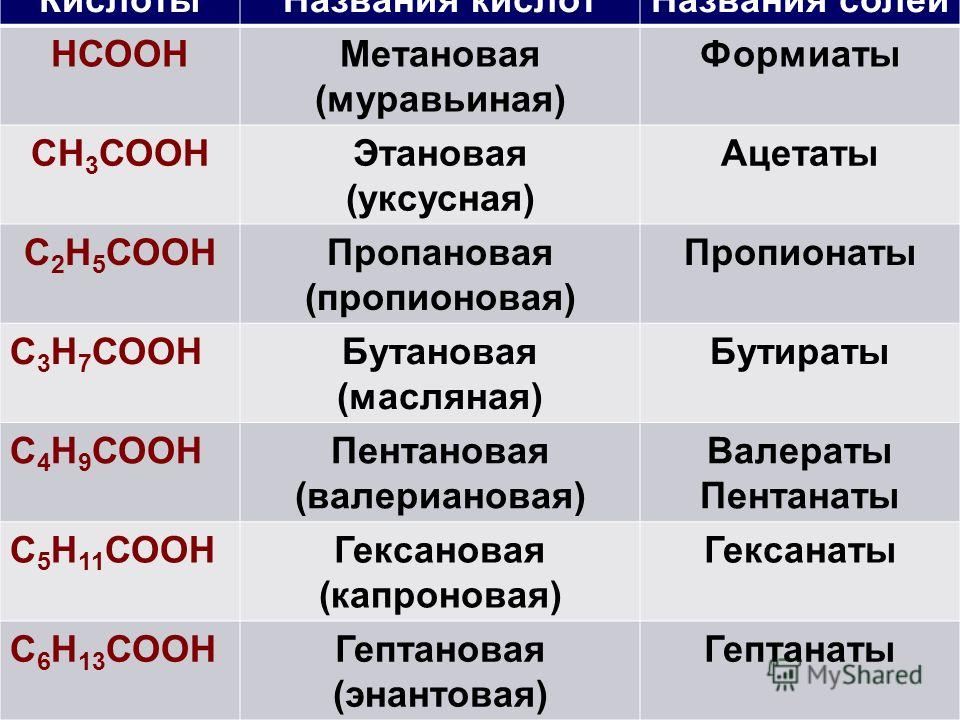 Благодаря их эффективному противообледенительному действию возможно быстро привести площадки в состояние, пригодное для спортивных состязаний. «Большое впечатление на нас произвела способность солей муравьиной кислоты к биологическому разложению при низких температурах. Таким образом, они не создают препятствий спортсменам в ходе соревнований. Кроме того, искусственные покрытия и спортивный инвентарь (мячи, ракетки, штанги, сетки) получают меньше повреждений и лучше сохраняются в течение зимнего периода в тех случаях, когда для удаления снега и льда используются формиаты», − резюмирует Эрик Хардман, ответственный за состояние спортивных объектов в Базеле.
Благодаря их эффективному противообледенительному действию возможно быстро привести площадки в состояние, пригодное для спортивных состязаний. «Большое впечатление на нас произвела способность солей муравьиной кислоты к биологическому разложению при низких температурах. Таким образом, они не создают препятствий спортсменам в ходе соревнований. Кроме того, искусственные покрытия и спортивный инвентарь (мячи, ракетки, штанги, сетки) получают меньше повреждений и лучше сохраняются в течение зимнего периода в тех случаях, когда для удаления снега и льда используются формиаты», − резюмирует Эрик Хардман, ответственный за состояние спортивных объектов в Базеле.
Стоит отметить, что абсолютным лидером в области производства муравьиной кислоты являются именно животные и растения, которые совместно продуцируют большее количество данного вещества, нежели все вместе взятые предприятия химической отрасли.
Муравьиная кислота, химические свойства, нахождение в природе
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
ФосфорФосфор
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
КриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИридийИридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Реакции муравьиной кислоты и ее солей
Реакции муравьиной кислоты и ее солей
Скачать PDF
Ваша статья скачана
Карусель с тремя слайдами одновременно. Используйте кнопки «Назад» и «Далее» для перехода по трем слайдам за раз или кнопки с точками в конце для перехода по трем слайдам за раз.
Скачать PDF
- Опубликовано:
- ПОЛ ХААС 1
Природа том 167 , страница 325 (1951)Процитировать эту статью
1371 Доступ
2 Цитаты
Сведения о показателях
Abstract
В БОЛЬШИНСТВЕ учебников по органической химии содержится утверждение, что муравьиная кислота и формиаты обязаны своим восстановительным характером присутствию в их молекуле альдегидной группы, в подтверждение этого приводится их способность восстанавливать аммиачный нитрат серебра до металла; хотя эту реакцию, безусловно, вызывают альдегиды, она не является специфической для этого класса соединений, поскольку многие другие кислоты, такие как винная или лимонная, аналогичным образом восстанавливают нитрат серебра. Восстановление хлорида ртути до хлорида ртути формиатами также не подтверждает альдегидную теорию, поскольку альдегиды в целом, включая формальдегид, не могут влиять на это изменение. На самом деле формиаты не дают ни одной из реакций, характерных для альдегидов; таким образом, они не восстанавливают окраску реактива Шиффа, не вызывают реакции с гидрохлоридом 2,4-динитрофенилгидразина и, прежде всего, не восстанавливают раствор Фелинга, который, вероятно, является наиболее специфичным из всех альдегидных реактивов.
Восстановление хлорида ртути до хлорида ртути формиатами также не подтверждает альдегидную теорию, поскольку альдегиды в целом, включая формальдегид, не могут влиять на это изменение. На самом деле формиаты не дают ни одной из реакций, характерных для альдегидов; таким образом, они не восстанавливают окраску реактива Шиффа, не вызывают реакции с гидрохлоридом 2,4-динитрофенилгидразина и, прежде всего, не восстанавливают раствор Фелинга, который, вероятно, является наиболее специфичным из всех альдегидных реактивов.
Информация о авторе
Авторы и принадлежности
Химический отдел, Королевская медицинская школа Бесплатной больницы, Лондон
Пол Хаас
Авторы
- Paul Haas
Просмотреть автора. в PubMed Google Scholar
Права и разрешения
Перепечатка и разрешения
Об этой статье
Комментарии
Отправляя комментарий, вы соглашаетесь соблюдать наши Условия и правила сообщества.
