Урок химии на тему «Соли угольной кислоты» (9 класс)
Тема. Соли угольной кислоты.
Цель:
повторить средние и кислые соли на примере карбонатов и гидрокарбонатов, познакомить учащихся с характерными свойствами солей угольной кислоты, качественной реакцией на карбонат – ион; показать взаимосвязь двух солей на примере переходов карбонатов в гидрокарбонаты и обратно, на примере этих переходов
проследить взаимосвязь и взаимообусловленность явлений природы, а также взаимосвязь свойств веществ и применение их;
формировать общенаучные умения и навыки;
развивать познавательную активность и самостоятельности учащихся;
воспитывать у учащихся любознательность, культуру труда.
Тип урока: изучение нового материала.
Ход урока:
1. Организационный момент.
О тайные природы волшебства:
Пещеры, сталактиты, сталагмиты.
И…запах дома, значит пирога.
Как связано всё это, как всегда,
Попробуем сегодня объяснить мы.
Тема нашего урока «Соли угольной кислоты».
-Как вы думаете, какова цель нашего урока?
Какие вопросы сегодня мы должны рассмотреть?
1. Состав и строение солей угольной кислоты.
2. Физические и химические свойства солей.
Качественная реакция на карбонат – ион.
3. Применение солей угольной кислоты.
Сегодня мы должны изучить свойства солей угольной кислоты. Но прежде чем отправиться в увлекательный мир карбонатов нам надо проверить свои знания по теме «Оксиды углерода»
1. Программированный опрос по теме «Оксиды углерода»
1. Молекула этого оксида состоит из одного атома углерода и одного атома кислорода.
2. Связь между атомами в молекуле ковалентная полярная.
3. Газ, практически нерастворимый в воде.
4. В молекуле этого оксида один атом углерода и два атома кислорода.
5. Запаха и цвета не имеет.
6. Газ растворимый в воде.
7.
Не сжижается даже при —
-190 (температура кипения — -191,5 гр. ц)
ц)
8. Кислотный оксид.
9. Легко сжимается, при 20 под давлением 58,5 атм становится жидким, затвердевает в «сухой лёд».
10. Не ядовит.
11. несолеобразующий
12. Горюч
13. Взаимодействует с водой.
14. Взаимодействует с основными оксидами.
15. Реагирует с оксидами металлов, восстанавливая из них свободные металлы.
16. Получают взаимодействием кислот с солями угольной кислоты.
17. Яд.
18. Взаимодействует со щелочами.
19. Источник углерода, усваиваемого растениями, в парниках и теплицах приводит к повышению урожая.
20. Используется при газировании воды и напитков.
3. Подготовка к изучению нового материала.
1.
Запишите молекулярную,
электронную и структурную формулу угольной кислоты.
2. Определите степени окисления каждого элемента.
3. Дайте характеристику угольной кислоте (Кислородсодержащая, двухосновная, слабая, неустойчивая)
4. Запишите уравнения диссоциации кислоты.
5. Какие виды солей и почему образует угольная кислота?
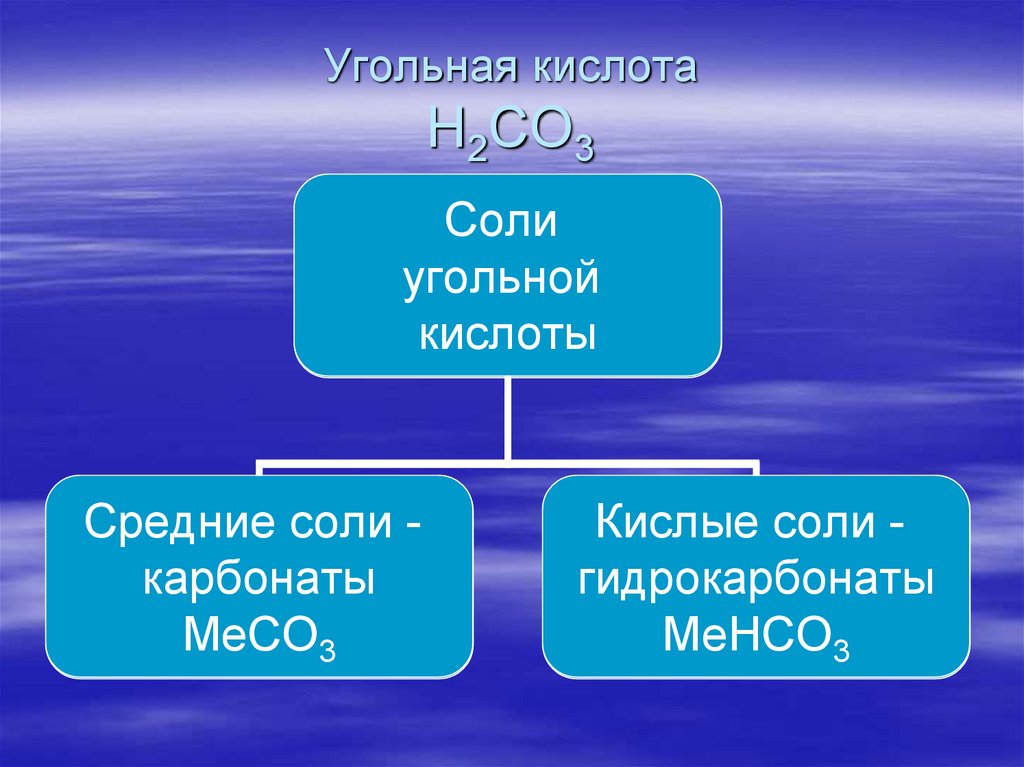
2. Изучение нового материала.
Как двухосновная, угольная кислота образует два вида солей:
1. средние – карбонаты, с кислотным остатком CO32-
2. кислые – гидрокарбонаты, с остатком HCO3—
· Какие соли называются средними?
· Какие соли называются кислыми?
· Как называются средние соли угольной кислоты?
· Как называются кислые соли угольной кислоты?
· Запишите формулы солей, образованных угольной кислотой и металлами: натрием, калием, кальцием, ионом аммония. Дайте названия солям.
(В ходе беседы заполняется схема)
Соли
Средние Кислые
CO32- HCO3—
карбонаты гидрокарбонаты
Na2CO3 NaHCO3
K2CO3 KHCO3
CaCO3 Ca(HCO3)2
(NH4)2CO3
NH
· C какими солями вы знакомы?
· Назовите их бытовые и технические названия?
Работа с таблицей.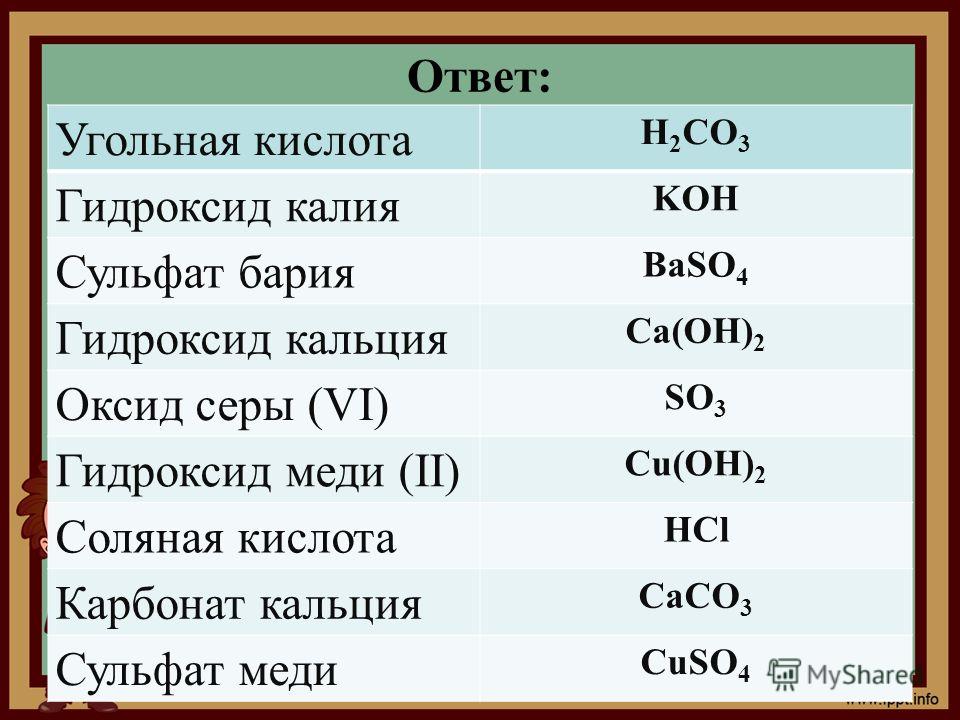
Формула | Техническое название | Области применения |
Na2CO3 | Кальцинированная или стиральная сода |
|
NaHCO3 | Пищевая или питьевая сода |
|
K2CO3 | поташ | |
CaCO3 | известняк |
|
мел |
| |
мрамор |
| |
NH4HCO3 |
|
|
Физические свойства солей
Рассмотрите образцы карбонатов, гидрокарбонатов на столе. Пользуясь
таблицей растворимости выясните их растворимость в воде.
Пользуясь
таблицей растворимости выясните их растворимость в воде.
Определите в этих солях тип связи, тип кристаллической решётки (ионная связь, ионная кристаллическая решётка).
Химические свойства.
Предположите, какими свойствами солей будут обладать карбонаты?
При каких условиях эти реакции протекают до конца?
(В ходе беседы заполняется схема)
— диссоциация
Карбонаты + кислота
+ щёлочь
+ соль
Лабораторный опыт № 11.
Качественная реакция на карбонат – ион.
Цель. Осуществить качественную реакцию на карбонат – ион.
Оборудование и реактивы:
штатив для пробирок,
пробирки (2 шт.), пробирка и пробка с газоотводной трубкой, лучинка, спички;
мел или мрамор, растворы карбоната натрия, соляной и серной кислоты,
известковая вода.
Правила техники безопасности.
Содержание и порядок выполнения опыта.
1. В пробирку прибора для получения газов положите небольшой кусочек мела или мрамора и прилейте 1-2 мл соляной кислоты. Быстро закройте пробирку пробкой с газоотводной трубкой. Газоотводную трубку поместите в известковую воду в пробирке. Что наблюдаете?__________________________________________
_________________________________________________________
Напишите молекулярное и ионные уравнения реакции мрамора (мела) с соляной кислотой.
______________________________________________________________________________________________________________________________________________________________________________
2. В пробирку налейте 1-2 мл раствора карбоната натрия и добавьте 1-2 мл серной кислоты. Что наблюдаете? ( Предложите более простой способ для обнаружения газообразного продукта реакции) ____________________________________________________________________________________________________________________
Напишите молекулярное и ионные уравнения проведённой реакции
______________________________________________________________________________________________________________________________________________________________________________
3. Впишите пропущенные слова.
Впишите пропущенные слова.
Соли угольной кислоты можно распознать, используя следующую качественную реакцию: при добавлении раствора _______________ к солям угольной кислоты образуется _________________________, который можно распознать с помощью__________________ или ________________________________________________________
Слово учителя.
Действие сильной кислоты может служить качественной реакцией на карбонаты. Геологи в полевых условиях именно так отличают карбонаты от силикатов.
Демонстрация учителя. На образец горных пород наносится капля соляной кислоты
«Вскипание» — свидетельство присутствия солей угольной кислоты.
Об удивительном свойстве некоторых минералов растворяться в кислотах
знала, очевидно, и египетская царица Клеопатра. В романе Г.Р. Халгарда
«Клеопатра» описан такой эпизод: «…она вынула из уха одну из тех огромных
жемчужин… и опустила жемчужину в уксус. Наступило молчание, потрясённые гости,
замерев, наблюдали, как несравненная жемчужина медленно растворяется в крепком
уксусе. Вот от него не осталось и следа, и тогда Клеопатра подняла кубок.
Покрутила его, взбалтывая уксус, и выпила весь до последней капли».
Вот от него не осталось и следа, и тогда Клеопатра подняла кубок.
Покрутила его, взбалтывая уксус, и выпила весь до последней капли».
А жемчуг – это минерал арагонит CaCO3
Следующий вопрос нашего урока Применение солей угольной кислоты.
Прослушайте сообщения учащихся, вам предлагается презентация. Сведения, которые вы получите, помогут вам заполнить таблицу «Применение солей угольной кислоты», а также расширить знания о специфических свойствах карбонатов.
(Сообщения учащихся с демонстрацией компьютерной презентации)
Формула | Техническое название | Области применения |
Na2CO3 | Кальцинированная или стиральная сода | Производство
стекла, бумаги, мыла. |
NaHCO3 | Пищевая или питьевая сода | Пищевая промышленность, медицина. |
K2CO3 | поташ | Производство жидкого мыла, тугоплавкого стекла, в качестве удобрения |
CaCO3 | известняк | Строительный материал, сырьё для получения цемента, гашёной и негашёной извести, стекла. |
мел | Школьные мелки, зубная паста, производство резины, бумаги, побелка | |
мрамор | Минерал скульпторов, архитекторов и облицовщиков. | |
NH4HCO3 |
| Как разрыхлитель теста |
— диссоциация
Карбонаты + кислота
+ щёлочь
+ соль
разложение
превращаются в гидрокарбонаты
Домашнее задание:
п. 29 стр.136-137, заполнить таблицу «Применение солей
угольной кислоты» (3 ст.), записать молекулярные, ионные уравнения реакций,
характеризующие свойства карбонатов.
29 стр.136-137, заполнить таблицу «Применение солей
угольной кислоты» (3 ст.), записать молекулярные, ионные уравнения реакций,
характеризующие свойства карбонатов.
Рефлексивный тест
1. Я узнал (а) много нового.
2. Мне это пригодиться в жизни.
3. На уроке было над чем подумать.
4. На все возникшие у меня вопросы я получил (а) ответы.
5. На уроке я поработал добросовестно.
Я прошу поднять руки тех учащихся, кто поставил три плюса, затем тех, у кого получилось четыре и пять плюсов.
Проверь себя.
Программированный опрос по теме «Оксиды углерода»
1 вариант
Углекислый газ 2, 4, 5, 6, 8, 9, 10, 13, 14, 16, 18, 19, 20
Угарный газ 1, 2, 3, 5, 7, 11, 12, 15, 17.
Оцени себя:
1-3 ошибки – оценка «5» (85-100%)
4-7 ошибок – оценка «4» (70-85%)
8-11 ошибок – оценка «3» (50-70%)
Проверь себя.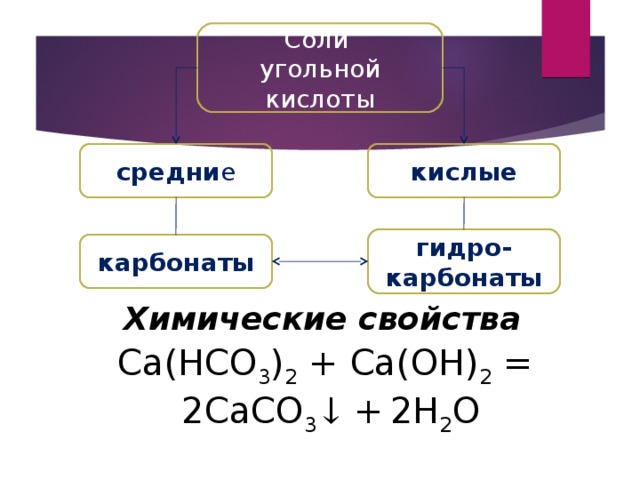
Программированный тест по теме «Оксиды углерода»
2 вариант
Углекислый газ 1, 2, 3, 6, 8, 9, 10, 11, 13, 16, 18, 19, 20
Угарный газ 2, 4, 5, 6, 7, 12, 14, 15, 17.
Оцени себя:
1-3 ошибки – оценка «5» (85-100%)
4-7 ошибок – оценка «4» (70-85%)
8-11 ошибок – оценка «3» (50-70%)
Урок соли угольной кислоты
Урок химии в 9-м классе по теме «Угольная кислота и её соли»
Тип урока: изучение и первичное закрепление новых знаний.
Цели:
Образовательная:
- закрепление знаний о средних и кислых солях на примере карбонатов и гидрокарбонатов, их взаимопревращениях. Изучение качественной реакции на карбонат – ион;
- ознакомление с практическим применением карбонатов и гидрокарбонатов.
Развивающая:
- развитие познавательной активности и самостоятельности учащихся;
- формирование исследовательских навыков.

Воспитательная:
- формирование валеологической и экологической грамотности учащихся.
Применяемые технологии: технология развития критического мышления, технология проблемного обучения, кейс-технология.
Методы обучения:
- проблемный
- исследовательский.
Организационные формы:
- фронтальная
- индивидуальная
- групповая
Оборудование:
- наборы реактивов для проведения опытов,
- компьютерная презентация,
- образцы минералов, скелеты морских звёзд, раковин, кораллов.
Ход урока
Приветствие: Я рада встрече с вами. Перед началом урока я пожелаю вам хорошего настроения и творческих успехов, надеюсь, что наша встреча пройдёт плодотворно.
- Стадия » вызов»
- ( мотивация, актуализация знаний, целеполагание ).
2 . Фронтальная работа с классом по литературно-химическому тесту.
Литературно- химический тест.
Ответьте на вопросы.
1.Уголь ценнейшее из полезных ископаемых ответил инженер, — и природа как будто решила доказать это, создав алмаз, ибо он, в сущности, не что иное, как кристаллический углерод». Ж.Верн «Таинственный остров»
Какие аллотропные модификации углерода, кроме алмаза вам известны?
Б) озон; К) графит; А) карбин; Р) фуллерен
2. Между тем Рукодельница воротится, воду процедит, в кувшины нальет, да еще какая затейница: коли вода нечиста, так свернет лист бумаги, положит в нее угольков да песку крупного насыплет, вставит ту бумагу в кувшин да нальет в нее воды, а вода-то, знай, проходит сквозь песок да сквозь уголья и капает в кувшин чистая, словно хрустальна.
Русская народная сказка «Мороз Иванович»
Какие методы очистки использует Рукодельница?
Б) фильтрование; А) дистилляция; О) адсорбция; М) кристаллизация
3. Угарный газ! вскричал Холмс. Подождите немного. Сейчас он уйдет. Заглянув в дверь, мы увидели, что комнату освещает только тусклое синее пламя, мерцающее в маленькой медной жаровне посредине
В раскрытую дверь тянуло страшным ядовитым чадом, от которого мы задыхались и кашляли.
Угарный газ! вскричал Холмс. Подождите немного. Сейчас он уйдет. Заглянув в дверь, мы увидели, что комнату освещает только тусклое синее пламя, мерцающее в маленькой медной жаровне посредине
В раскрытую дверь тянуло страшным ядовитым чадом, от которого мы задыхались и кашляли.
А.К.Дойл «Случай с переводчиком»
Найдите химические ошибки в прочитанном отрывке. Почему Холмс и его спутники не могли по описанным признакам определить присутствие угарного газа в помещении?
Н) угарный газ не имеет запаха; Г) угарный газ имеет приятный запах
А) при отравлении угарным газом человек не кашляет
4.В аравийской пустыне растет дерево Caratina silikva (каратина силиква), косточки плодов которого всегда имеют одинаковый вес в любой год и на любом дереве. Поэтому ювелиры древности и применяли для своих весов такие гирьки, называя их каратами. В наши дни существует каратная проба золота и драгоценных камней.
Чему равна масса одного карата?
И) 100 г З) 0,5 г Т) 0,2 г Р) 0,1 г
5. — Вы слышали об эффекте «собачьей пещеры « в Италии?….Есть там такая пещера-яма. Человек войдет и ходит, а собака или кролик погибают через несколько минут.
— Вы слышали об эффекте «собачьей пещеры « в Италии?….Есть там такая пещера-яма. Человек войдет и ходит, а собака или кролик погибают через несколько минут.
— Почему?
— Из вулканической трещины выделяется углекислый газ
В.Короткевич «Черный замок Ольшанский»
Почему в «собачьей пещере» человек остается живым, а собаки и другие мелкие животные гибнут?
Ы) СО2 тяжелее воздуха и скапливается внизу
А) СО2 безопасен для человека, но вреден для животных
Ж) человек входит в пещеру в противогазе.
Ответы
1кар 2.б о 3 на 4 ты
III. Переход к изучению нового материала: (3 мин)
Какое слово получилось из букв, соответствующих правильным ответам?
Что такое карбонаты? Итак, тема сегодняшнего урока «Соли угольной кислоты». (Постановка целей и задач урока)
IV. Изучение нового материала. (25 мин)
2. Стадия осмысления (получение новой информации)
Учитель: Соли угольной кислоты широко распространены в природе и находят практическое применение. Об этом нам сейчас расскажет…Ваша задача не только прослушать сообщение, но и заполнить таблицу
Об этом нам сейчас расскажет…Ваша задача не только прослушать сообщение, но и заполнить таблицу
Формула | Химическое название | Техническое название |
(CuОH)2 CO3 | Гидроксокарбонат меди(II) основной карбонат меди | Малахит |
CaCO3 | Карбонат кальция | Мел, мрамор, известняк |
FeCO3 | карбонат железа (II)
| Сидерит (железный шпат) |
MnCO3
| Карбонат марганца (II)
| Родохрозит (марганцевый шпат) |
CaCO3•MgCO3
| Карбонат кальция и магния
| доломит |
Na2CO3 •10H2O | Кристаллогидрат карбоната натрия | Кристаллическая сода |
Na2CO3 | Карбонат натрия | Кальцинированная сода |
NaHCO3 | Гидрокарбонат натрия | Питьевая или пищевая |
Учитель: как классифицируются соли ? ( слайд) Проклассифицируйте соли угольной кислоты. Соли
Соли
Средние Кислые Основные Двойные
CaCO3 NaHCO3 (CuОH)2 CO3 CaCO3•MgCO3
Дайте названия этим солям
Карбонат кальция, Гидрокарбонат кальция, Гидроксокарбонат меди(II),Карбонат кальция и магния
2. Физические свойства солей угольной кислоты.
(Работа с материалами коллекции «Карбонаты», таблицей растворимости)
Что можно сказать о растворимости карбонатов? (работа с таблицей растворимости: растворимы только соли K+, Na+, NH4+ )
А гидрокарбонаты ? ( растворимы все)
Средние соли угольной кислоты | Кислые соли угольной кислоты |
карбонаты | гидрокарбонаты |
Твердые кристаллические Большинство не растворимо в воде диссоциация идет с образованием карбонат — ионов | Твердые кристаллические Растворимы в воде диссоциация идет с образованием гидрокарбонат — ионов |
Учитель: Какие химические свойства характерны для солей угольной кислоты?
кислотами качественная реакция MeCO3 + HnKO → MeKO + CO2↑ + H2O MeHCO3 + HnKO → MeKO + CO2↑ + H2O
|
Учащиеся составляют кластер: «Химические свойства солей угольной кислоты»
Карбонаты гидрокарбонаты MeCO3 + CO2 + H2O → MeHCO3 MeHCO3→ MeCO3 + CO2 + H2O |
Соли угольной кислоты |
Разлагаются (исключение карбонаты щелочных металлов) MeCO3 → MeO + CO2 MeHCO3 → MeCO3 + CO2 + H2O
|
растворами солей MeCO3 + МеKO → MeKO2 + MeCO3 2
|
3. Общие химические свойства солей угольной кислоты.
Общие химические свойства солей угольной кислоты.
а) Все соли угольной кислоты разлагаются по схемам:
MeCO3 → MeO + CO2 (исключение карбонаты щелочных металлов)
MeHCO3 → MeCO3 + CO2 + H2O
г) Растворы солей угольной кислоты взаимодействуют с растворами других солей, если образуется нерастворимые вещества.
в) Карбонаты превращаются в гидрокарбонаты при избытке углекислого газа и воды.
б) Все соли взаимодействуют с кислотами : соли угольной кислоты реагируют с кислотами. Почему? Будучи одной из самых слабых кислот она легко вытесняется из солей более сильными кислотами : соляной, серной и др.
Как на практике моно использовать эту реакцию?
(Таким образом можно распознать соли угольной кислоты среди других солей. Это качественная реакция на карбонаты и гидрокарбонаты).
дают качественную реакцию на ионы CO32- и HCO3—
MeCO3 + HnKO → MeKO + CO2↑ + H2O
MeHCO3 + HnKO → MeKO + CO2↑ + H2O
А теперь, проведем качественную реакцию на ионы CO32- и HCO3— опыт. На ваших столах находятся необходимое оборудование и инструктивные карточки. Внимательно ознакомтись с ней , не забывайте о правилах техники безопасности работы с веществами.
На ваших столах находятся необходимое оборудование и инструктивные карточки. Внимательно ознакомтись с ней , не забывайте о правилах техники безопасности работы с веществами.
Для этого: (лабораторный опыт)
1. Налейте в пробирки по 2-3 мл растворов Na2CO3( 1 вариант) и NaHCO3 (2 вариант)
2. Добавьте по каплям HCl.
3. Что наблюдаете?
4. Составьте уравнения реакций молекулярном и ионном виде.
5.Сделайте выводы из наблюдений.
Учитель: Особенностью солей угольной кислоты является их способность превращаться друг в друга (демонстрация видеоролика «Взаимопревращения карбонатов и гидрокарбонатов») Просмотрите видеофильм этого опыта, запишите уравнения химических реакций.
Какой вывод можно сделать из наблюдаемых явлений?: (в избытке кислоты карбонаты превращаются в гидрокарбонаты, а при нагревании — наоборот) (учащиеся составляют уравнения реакций) СаCO3 + CO2 + H2O → Са(HCO3)2 Са(HCO3)2→ СаCO3 + CO2 + H2O
Учитель: химические реакции мы привыкли наблюдать в школьной лаборатории, в пробирках. Но такие же процессы происходят и в природе, вокруг нас. Об этом нам сейчас расскажет … (сообщение учащегося об образовании карстовых пещер. Приложение1)
Но такие же процессы происходят и в природе, вокруг нас. Об этом нам сейчас расскажет … (сообщение учащегося об образовании карстовых пещер. Приложение1)
Учитель. Вспомните, как мама в одной руке держит ложку с содой, а другой капает в неё раствором уксуса. Потом всё громко шипит, и мама, торопясь, опускает пузырчатую массу в тесто. Давайте разберёмся в целесообразности сего кулинарного действия, вспомнив химию. И обратимся к химическому расследованию, которое проделала дома Алина.
Учитель: А теперь я предлагаю вам объединиться в группы с тем, чтобы поработать с предложенными текстами, из которых вы узнаете о значении и применении карбонатов и гидрокарбонатов в повседневной и практической деятельности человека ( приложение3)
V. Задание на дом: §19.10 (угольная кислота и ее соли), конспект.(1 мин)
VI. Повторение и закрепление. (4 мин)
Рефлексия.
Просмотр содержимого документа
«Урок соли угольной кислоты»
Урок химии в 9-м классе по теме «Угольная кислота и её соли»
Тип урока: изучение и первичное закрепление новых знаний.
Цели:
Образовательная:
Развивающая:
Воспитательная:
Применяемые технологии: технология развития критического мышления, технология проблемного обучения, кейс-технология.
Методы обучения:
проблемный
исследовательский.
Организационные формы:
фронтальная
индивидуальная
групповая
Оборудование:
наборы реактивов для проведения опытов,
компьютерная презентация,
образцы минералов, скелеты морских звёзд, раковин, кораллов.
Ход урока
Приветствие: Я рада встрече с вами. Перед началом урока я пожелаю вам хорошего настроения и творческих успехов, надеюсь, что наша встреча пройдёт плодотворно.
Стадия » вызов»
( мотивация, актуализация знаний, целеполагание ).
2 . Фронтальная работа с классом по литературно-химическому тесту.
Литературно- химический тест.
Ответьте на вопросы.
1.Уголь ценнейшее из полезных ископаемых ответил инженер, — и природа как будто решила доказать это, создав алмаз, ибо он, в сущности, не что иное, как кристаллический углерод». Ж.Верн «Таинственный остров»
Какие аллотропные модификации углерода, кроме алмаза вам известны?
Б) озон; К) графит; А) карбин; Р) фуллерен
2. Между тем Рукодельница воротится, воду процедит, в кувшины нальет, да еще какая затейница: коли вода нечиста, так свернет лист бумаги, положит в нее угольков да песку крупного насыплет, вставит ту бумагу в кувшин да нальет в нее воды, а вода-то, знай, проходит сквозь песок да сквозь уголья и капает в кувшин чистая, словно хрустальна.
Русская народная сказка «Мороз Иванович»
Какие методы очистки использует Рукодельница?
Б) фильтрование; А) дистилляция; О) адсорбция; М) кристаллизация
3.Угарный газ! вскричал Холмс. Подождите немного. Сейчас он уйдет. Заглянув в дверь, мы увидели, что комнату освещает только тусклое синее пламя, мерцающее в маленькой медной жаровне посредине В раскрытую дверь тянуло страшным ядовитым чадом, от которого мы задыхались и кашляли.
А.К.Дойл «Случай с переводчиком»
Найдите химические ошибки в прочитанном отрывке. Почему Холмс и его спутники не могли по описанным признакам определить присутствие угарного газа в помещении?
Н) угарный газ не имеет запаха; Г) угарный газ имеет приятный запах
А) при отравлении угарным газом человек не кашляет
4.В аравийской пустыне растет дерево Caratina silikva (каратина силиква), косточки плодов которого всегда имеют одинаковый вес в любой год и на любом дереве. Поэтому ювелиры древности и применяли для своих весов такие гирьки, называя их каратами. В наши дни существует каратная проба золота и драгоценных камней.
Поэтому ювелиры древности и применяли для своих весов такие гирьки, называя их каратами. В наши дни существует каратная проба золота и драгоценных камней.
Чему равна масса одного карата?
И) 100 г З) 0,5 г Т) 0,2 г Р) 0,1 г
5. — Вы слышали об эффекте «собачьей пещеры « в Италии?….Есть там такая пещера-яма. Человек войдет и ходит, а собака или кролик погибают через несколько минут.
— Почему?
— Из вулканической трещины выделяется углекислый газ
В.Короткевич «Черный замок Ольшанский»
Почему в «собачьей пещере» человек остается живым, а собаки и другие мелкие животные гибнут?
Ы) СО2 тяжелее воздуха и скапливается внизу
А) СО2 безопасен для человека, но вреден для животных
Ж) человек входит в пещеру в противогазе.
Ответы
1кар 2. б о 3 на 4 ты
б о 3 на 4 ты
III. Переход к изучению нового материала: (3 мин)
Какое слово получилось из букв, соответствующих правильным ответам?
Что такое карбонаты? Итак, тема сегодняшнего урока «Соли угольной кислоты». (Постановка целей и задач урока)
IV. Изучение нового материала. (25 мин)
2. Стадия осмысления (получение новой информации)
Учитель: Соли угольной кислоты широко распространены в природе и находят практическое применение. Об этом нам сейчас расскажет…Ваша задача не только прослушать сообщение, но и заполнить таблицу
Формула | Химическое название | Техническое название |
(CuОH)2 CO3 | Гидроксокарбонат меди(II) основной карбонат меди | Малахит |
CaCO3 | Карбонат кальция | Мел, мрамор, известняк |
FeCO3 | карбонат железа (II) | Сидерит (железный шпат) |
MnCO3 | Карбонат марганца (II) | Родохрозит (марганцевый шпат) |
CaCO3•MgCO3 | Карбонат кальция и магния | доломит |
Na2CO3 •10H2O | Кристаллогидрат карбоната натрия | Кристаллическая сода |
Na2CO3 | Карбонат натрия | Кальцинированная сода |
NaHCO3 | Гидрокарбонат натрия | Питьевая или пищевая |
Учитель: как классифицируются соли ? ( слайд) Проклассифицируйте соли угольной кислоты. Соли
Соли
Средние Кислые Основные Двойные
CaCO3 NaHCO3 (CuОH)2 CO3 CaCO3•MgCO3
Дайте названия этим солям
Карбонат кальция, Гидрокарбонат кальция, Гидроксокарбонат меди(II),Карбонат кальция и магния
2. Физические свойства солей угольной кислоты.
(Работа с материалами коллекции «Карбонаты», таблицей растворимости)
Что можно сказать о растворимости карбонатов? (работа с таблицей растворимости: растворимы только соли K+, Na+, NH4+ )
А гидрокарбонаты ? ( растворимы все)
Средние соли угольной кислоты | Кислые соли угольной кислоты |
карбонаты | гидрокарбонаты |
Твердые кристаллические Большинство не растворимо в воде диссоциация идет с образованием карбонат — ионов | Твердые кристаллические Растворимы в воде диссоциация идет с образованием гидрокарбонат — ионов |
Учитель: Какие химические свойства характерны для солей угольной кислоты?
Учащиеся составляют кластер: «Химические свойства солей угольной кислоты»
кислотами
качественная реакция
MeCO3 + HnKO → MeKO + CO2↑ + H2O
MeHCO3 + HnKO → MeKO + CO2↑ + H2O
Карбонаты гидрокарбонаты
MeCO3 + CO2 + H2O → MeHCO3 MeHCO3→ MeCO3 + CO2 + H2O
Соли угольной кислоты
Разлагаются (исключение карбонаты щелочных металлов)
MeCO3 → MeO + CO2 MeHCO3 → MeCO3 + CO2 + H2O
растворами солей MeCO3 + МеKO → MeKO2 + MeCO3 2
3. Общие химические свойства солей угольной кислоты.
Общие химические свойства солей угольной кислоты.
а) Все соли угольной кислоты разлагаются по схемам:
MeCO3 → MeO + CO2 (исключение карбонаты щелочных металлов)
MeHCO3 → MeCO3 + CO2 + H2O
г) Растворы солей угольной кислоты взаимодействуют с растворами других солей, если образуется нерастворимые вещества.
в) Карбонаты превращаются в гидрокарбонаты при избытке углекислого газа и воды.
б) Все соли взаимодействуют с кислотами : соли угольной кислоты реагируют с кислотами. Почему? Будучи одной из самых слабых кислот она легко вытесняется из солей более сильными кислотами : соляной, серной и др.
Как на практике моно использовать эту реакцию?
(Таким образом можно распознать соли угольной кислоты среди других солей. Это качественная реакция на карбонаты и гидрокарбонаты).
дают качественную реакцию на ионы CO32- и HCO3—
MeCO3 + HnKO → MeKO + CO2↑ + H2O
MeHCO3 + HnKO → MeKO + CO2↑ + H2O
А теперь, проведем качественную реакцию на ионы CO32- и HCO3— опыт. На ваших столах находятся необходимое оборудование и инструктивные карточки. Внимательно ознакомтись с ней , не забывайте о правилах техники безопасности работы с веществами.
На ваших столах находятся необходимое оборудование и инструктивные карточки. Внимательно ознакомтись с ней , не забывайте о правилах техники безопасности работы с веществами.
Для этого: (лабораторный опыт)
1. Налейте в пробирки по 2-3 мл растворов Na2CO3( 1 вариант) и NaHCO3 (2 вариант)
2. Добавьте по каплям HCl.
3. Что наблюдаете?
4. Составьте уравнения реакций молекулярном и ионном виде.
5.Сделайте выводы из наблюдений.
Учитель: Особенностью солей угольной кислоты является их способность превращаться друг в друга (демонстрация видеоролика «Взаимопревращения карбонатов и гидрокарбонатов») Просмотрите видеофильм этого опыта, запишите уравнения химических реакций.
Какой вывод можно сделать из наблюдаемых явлений?: (в избытке кислоты карбонаты превращаются в гидрокарбонаты, а при нагревании — наоборот) (учащиеся составляют уравнения реакций) СаCO3 + CO2 + H2O → Са(HCO3)2 Са(HCO3)2→ СаCO3 + CO2 + H2O
Учитель: химические реакции мы привыкли наблюдать в школьной лаборатории, в пробирках. Но такие же процессы происходят и в природе, вокруг нас. Об этом нам сейчас расскажет … (сообщение учащегося об образовании карстовых пещер. Приложение1)
Но такие же процессы происходят и в природе, вокруг нас. Об этом нам сейчас расскажет … (сообщение учащегося об образовании карстовых пещер. Приложение1)
Учитель. Вспомните, как мама в одной руке держит ложку с содой, а другой капает в неё раствором уксуса. Потом всё громко шипит, и мама, торопясь, опускает пузырчатую массу в тесто. Давайте разберёмся в целесообразности сего кулинарного действия, вспомнив химию. И обратимся к химическому расследованию, которое проделала дома Алина.
Учитель: А теперь я предлагаю вам объединиться в группы с тем, чтобы поработать с предложенными текстами, из которых вы узнаете о значении и применении карбонатов и гидрокарбонатов в повседневной и практической деятельности человека ( приложение3)
V. Задание на дом: §19.10 (угольная кислота и ее соли), конспект.(1 мин)
VI. Повторение и закрепление. (4 мин)
Рефлексия.
carbonate — Викисловарь
См. также: Carbonate и
также: Carbonate и
- 1.1 Этимология
- 1.2 Произношение
- 1.3 Существительное
- 1.3.1 Гипонимы
- 1.3.2 Производные термины
- 1.3.3 Переводы
- 1.4 Глагол
- 1.4.1 Производные термины
- 1,5 № по каталогу
- 2.1 Этимология
- 2.2 Произношение
- 2.3 Существительное
- 2.4 Дополнительная литература
- 3.1 Существительное
Английский[править]
Этимология[править]
От французского карбонат . Эквивалент углерода + -ate («суффикс, используемый для солей кислот, оканчивающихся на -ic»).
Произношение[править]
Существительное
- (Великобритания) enPR: käʹbənət, IPA (ключ) : /ˈkɑː(ɹ).bə.
 nət/
nət/ Аудио (Великобритания) (файл) - (США) enPR: kärʹbənət, IPA (ключ) : /ˈkɑɹbənət/
Глагол
- (Великобритания) enPR: käʹbənāt, IPA (ключ) : /ˈkɑː(ɹ).bə.neɪt/
Аудио (Великобритания) (файл) - (США) enPR: kärʹbənāt, IPA (ключ) : /ˈkɑɹbəneɪt/
Существительное
- Любая соль или эфир угольной кислоты.
Гипонимы[править]
- карбонат аммония
- карбонат бария
- бикарбонат
- висмута карбонат
- карбонат кадмия
- карбонат кальция
- карбонат кальция магния
- крышка карбонат
- карбонат извести
- карбонат меди
- карбонат меди
- дикарбонат
- диэтилкарбонат
- диметилкарбонат
- фторкарбонат
- гидрокарбонат
- гидрокарбонат
- гидрокарбонат калия
- карбонат свинца
- карбонат лития
- карбонат магния
- карбонат марганца
- метакарбонат
- оксикарбонат
- перкарбонат
- карбонат калия
- карбонат калия кислый
- карбонат калия
- гидрокарбонат калия
- карбонат серебра
- карбонат натрия
- пероксигидрат карбоната натрия
- гидрокарбонат натрия
- карбонат стронция
- сульфокарбонат
- сульфокарбонат
- карбонат тория
- уран-аммиачный карбонат
- уранозоаммиачный карбонат
- уранилкарбонат
- карбонат цинка
Производные термины[править]
- карбонат-ион
- карбонат калия
- карбонат калия
- карбонат калия
- карбонатный стронцианит
- карбонатит
- ион гидрокарбоната
- протокарбонат
Переводы[править]
любая соль или эфир угольной кислоты
|
Глагол [РЕДАКТИРОВАТЬ]
Карбонат ( Single Simplour Simplular третьего лица , СРЕДНЫЙ ПРЕДОСТАВЛЕНИЕ , , , СРЕДНЫЙ СВЕДЕНИЕ , СРЕДНЫЙ. )
)
- (переходный) Для заправки (часто напитков) углекислым газом.
Производные термины[править]
- карбонизация
- газированный
- карбонизация
- carbonator
References[edit]
- carbonate on Wikipedia.Wikipedia
Etymology[edit]
From New Latin carbonatem , from Latin carbō (“charcoal, coal”).
Произношение
| Аудио (Париж) | (файл) |
Существительное
- carbonate
Further reading[edit]
- “carbonate”, in Trésor de la langue française informatisé [Digitized Treasury of the French Language] , 2012.
Italian[edit]
Noun [править]
карбонат f pl
- множественное число от carbonata
Карбонат Определение и значение — Merriam-Webster
1 из 2
карбонат · бон · ел ˈkär-bə-ˌnāt
-nət
: соль или эфир угольной кислоты
карбонат
2 из 2
карбонат · бон · ел ˈkär-bə-ˌnāt
переходный глагол
1
: превратить в карбонат
газированные напитки
карбонизация
ˌkär-bə-nā-shən
существительное
Примеры предложений
Последние примеры в Интернете
Этот ингредиент в сочетании с химическим отбеливающим агентом карбонат пероксид удаляет пятна с поверхности зубов и делает улыбку ярче после использования. — Даниэль Зёлльнер, 9 лет.0523 Verywell Health , 31 января 2023 г.
Изображены эксперименты по трансплантации, в которых карбонатных камня (здесь серые блоки) были перемещены из активных в спящие места просачивания и наоборот.
— Джеффри Марлоу, Discover Magazine , 23 декабря 2015 г.
Карбонат кальция также составляет 97% яичной скорлупы и морских раковин.
— Стивен Сэвидж, 9 лет.0523 Forbes , 28 декабря 2022 г.
Карбонат кальция лучше всего усваивается с пищей, тогда как цитрат кальция хорошо усваивается независимо от приема пищи.
— Д-р. Кит Роуч, oregonlive , 2 декабря 2022 г.
Карбонат кальция плохо усваивается людьми, принимающими ингибиторы протонной помпы, такие как омепразол (прилосек).
— Даниэль Зёлльнер, 9 лет.0523 Verywell Health , 31 января 2023 г.
Изображены эксперименты по трансплантации, в которых карбонатных камня (здесь серые блоки) были перемещены из активных в спящие места просачивания и наоборот.
— Джеффри Марлоу, Discover Magazine , 23 декабря 2015 г.
Карбонат кальция также составляет 97% яичной скорлупы и морских раковин.
— Стивен Сэвидж, 9 лет.0523 Forbes , 28 декабря 2022 г.
Карбонат кальция лучше всего усваивается с пищей, тогда как цитрат кальция хорошо усваивается независимо от приема пищи.
— Д-р. Кит Роуч, oregonlive , 2 декабря 2022 г.
Карбонат кальция плохо усваивается людьми, принимающими ингибиторы протонной помпы, такие как омепразол (прилосек). — Д-р. Кейт Роуч, 9 лет0523 oregonlive , 2 декабря 2022 г.
Для работы своего завода REEtec будет поставлять сырье, известное как карбонат редкоземельных элементов , из Северо-Западных территорий Канады.
— Мэри Хуэй, Кварц , 25 ноября 2022 г.
По данным компании Benchmark Mineral Intelligence, занимающейся оценкой цен, цены на карбонат лития в Китае, ориентир на быстрорастущем рынке, составляют около 71 000 долларов за метрическую тонну.
— Джо Уоллес, 9 лет.0523 WSJ , 21 сентября 2022 г.
Лидерами экспорта были полу- или цельномолотый рис, сигареты, динатрий карбонат и копченые листы натурального каучука.
— Рейтер, CNN , 20 августа 2022 г.
— Д-р. Кейт Роуч, 9 лет0523 oregonlive , 2 декабря 2022 г.
Для работы своего завода REEtec будет поставлять сырье, известное как карбонат редкоземельных элементов , из Северо-Западных территорий Канады.
— Мэри Хуэй, Кварц , 25 ноября 2022 г.
По данным компании Benchmark Mineral Intelligence, занимающейся оценкой цен, цены на карбонат лития в Китае, ориентир на быстрорастущем рынке, составляют около 71 000 долларов за метрическую тонну.
— Джо Уоллес, 9 лет.0523 WSJ , 21 сентября 2022 г.
Лидерами экспорта были полу- или цельномолотый рис, сигареты, динатрий карбонат и копченые листы натурального каучука.
— Рейтер, CNN , 20 августа 2022 г.
Части головоломки Чтобы определить прошлые сезонные эффекты перехода к пастбищам, Кукла и его команда изучили изотопы кислорода, оставшиеся в глине и минералах карбоната в результате дождя или снега. — Тео Никитопулос, Discover Magazine , 15 апреля 2022 г.
Аргиллиты и карбонатные отложения вокруг образцов указывают на то, что это место находилось глубоко под водой.
— Макс Г. Леви, 9 лет.0523 ПРОВОДНАЯ , 19 декабря 2022 г.
В соответствии с так называемым соглашением о поставках REEtec купит карбонат редкоземельных элементов у Vital Metals, чтобы затем доставить его на предстоящий разделительный завод REEtec для дальнейшей очистки.
— Мэри Хуэй, Кварц , 25 ноября 2022 г.
Во-первых, несмотря на явные признаки просачивания метана — моллюсков, микробных матов, зарождающихся карбонат корки пород – метан пока не подтвержден, так как геохимические исследования не проводились.
— Джеффри Марлоу, Discover Magazine , 29 июня 2016 г.
— Тео Никитопулос, Discover Magazine , 15 апреля 2022 г.
Аргиллиты и карбонатные отложения вокруг образцов указывают на то, что это место находилось глубоко под водой.
— Макс Г. Леви, 9 лет.0523 ПРОВОДНАЯ , 19 декабря 2022 г.
В соответствии с так называемым соглашением о поставках REEtec купит карбонат редкоземельных элементов у Vital Metals, чтобы затем доставить его на предстоящий разделительный завод REEtec для дальнейшей очистки.
— Мэри Хуэй, Кварц , 25 ноября 2022 г.
Во-первых, несмотря на явные признаки просачивания метана — моллюсков, микробных матов, зарождающихся карбонат корки пород – метан пока не подтвержден, так как геохимические исследования не проводились.
— Джеффри Марлоу, Discover Magazine , 29 июня 2016 г. Химические заводы также производят двуокись углерода в качестве побочного продукта, поэтому поставки двуокиси углерода, которую производители напитков используют для газированных напитков и пива, также будут ограничены, даже несмотря на то, что газ обычно перемещается по трубопроводам.
— Джош Фанк, 9 лет.0523 Чикаго Трибьюн , 22 ноября 2022 г.
Большинство любителей пива знают, что пивовары используют CO2 для карбонизации пива.
— Майк Снайдер, , США СЕГОДНЯ, , 24 сентября 2022 г.
Такие производители, как CF Fertilizers, затем продают полученный CO2 пивоварам, которые используют его для карбонизации пива и придания ему характерной шипучести.
— Тристан Бове, Fortune , 25 августа 2022 г.
Хотя азот может заменить CO2 при перекачивании пива из одного резервуара в другой, пивовары должны использовать CO2 для газированный напиток.
Химические заводы также производят двуокись углерода в качестве побочного продукта, поэтому поставки двуокиси углерода, которую производители напитков используют для газированных напитков и пива, также будут ограничены, даже несмотря на то, что газ обычно перемещается по трубопроводам.
— Джош Фанк, 9 лет.0523 Чикаго Трибьюн , 22 ноября 2022 г.
Большинство любителей пива знают, что пивовары используют CO2 для карбонизации пива.
— Майк Снайдер, , США СЕГОДНЯ, , 24 сентября 2022 г.
Такие производители, как CF Fertilizers, затем продают полученный CO2 пивоварам, которые используют его для карбонизации пива и придания ему характерной шипучести.
— Тристан Бове, Fortune , 25 августа 2022 г.
Хотя азот может заменить CO2 при перекачивании пива из одного резервуара в другой, пивовары должны использовать CO2 для газированный напиток. — Анисса Гардизи, BostonGlobe.com , 1 августа 2022 г.
Узнать больше
— Анисса Гардизи, BostonGlobe.com , 1 августа 2022 г.
Узнать больше
Эти примеры предложений автоматически выбираются из различных онлайн-источников новостей, чтобы отразить текущее использование слова «карбонат». Мнения, выраженные в примерах, не отражают точку зрения Merriam-Webster или ее редакторов. Отправьте нам отзыв.
История слов
Первое известное использование
Существительное
1788, в значении, определенном выше
Глагол
1805, в значении, определенном в смысле 1
Путешественник во времени 1
Первое известное использование карбоната было
в 1788 г.
Посмотреть другие слова того же года
Словарные статьи рядом с
карбонаткарбонизация
карбонат
карбонат-апатит
Посмотреть другие записи поблизости
Процитировать эту запись «Карбонат.»
Словарь Merriam-Webster.com , Merriam-Webster, https://www.merriam-webster.com/dictionary/carbonate. По состоянию на 18 февраля 2023 г.Copy Citation
Детское определение
карбонат
1 из 2 существительное
карбонат · бон · ел ˈkär-bə-ˌnāt
-nət
: соединение, образованное реакцией угольной кислоты с другим веществом
карбонат
2 из 2 глагол
карбонат · бон · ел ˈkär-bə-ˌnāt
1
: для превращения в карбонат
2
: для насыщения углекислым газом
a газированные напитки
карбонизация
ˌkär-bə-nā-shən
существительное
Медицинское определение
карбонат
1 из 2 существительное
карбонат · бон · ел ˈkär-bə-ˌnāt, -nət
: соль или эфир угольной кислоты
карбонат
2 из 2 переходный глагол
карбонат · бон · ел -нат
1
: для преобразования в карбонат
2
: для пропитки диоксидом углерода
карбонизация
ˌkär-bə-nā-shən
существительное
Еще от Merriam-Webster о
карбонатеАнглийский язык: перевод carbonate для говорящих на испанском языке
Britannica.



 nət/
nət/