| Карбонат | Соль угольной кислоты (сода, поташ и т. п.) 8 букв |
| Карбонат | Соль угольной кислоты (хим.) 8 букв |
| Карбонат | Соль угольной кислоты 8 букв |
| Сульфаты | Минералы, соли серной кислоты h3SO4. В их кристаллической структуре обособляются комплексные анионы SO42. Наиболее характерны сульфаты сильных двухвалентных оснований, особенно Ba2+, а также Sr2+ и Ca2+. Более слабые основания образуют основные соли, часто весьма неустойчивые, более сильные основания 8 букв |
| Мочевина | Амид угольной кислоты 8 букв |
| Мочевина | Химическое соединение, диамид угольной кислоты. Белые кристаллы, растворимые в полярных растворителях 8 букв |
| Гуанидин | Физиологически активное вещество, представляющее собой диамид имида угольной кислоты 8 букв |
| Сульфаты | Соли серной кислоты 8 букв |
| Силикаты | Минералы и синтетические химические соединения, представляющие по составу соли кремниевых кислот 8 букв |
| Сульфиды | Класс химических соединений, представляющих собой соединения металлов с серой, где она имеет степень окисления -2. Могут рассматриваться как соли сероводородной кислоты h3S 8 букв |
| Карбонат | Соль угольной кислоты (сода, поташ и т. п.) 8 букв |
| Карбонат | Соль угольной кислоты (хим.) 8 букв |
| Карбонат | Соль угольной кислоты 8 букв |
| Сульфаты | Минералы, соли серной кислоты h3SO4. В их кристаллической структуре обособляются комплексные анионы SO42. Наиболее характерны сульфаты сильных двухвалентных оснований, особенно Ba2+, а также Sr2+ и Ca2+. Более слабые основания образуют основные соли, часто весьма неустойчивые, более сильные основания 8 букв |
| Мочевина | Амид угольной кислоты 8 букв |
| Мочевина | Химическое соединение, диамид угольной кислоты. Белые кристаллы, растворимые в полярных растворителях 8 букв |
| Физиологически активное вещество, представляющее собой диамид имида угольной кислоты 8 букв | |
| Сульфаты | Соли серной кислоты 8 букв |
| Силикаты | Минералы и синтетические химические соединения, представляющие по составу соли кремниевых кислот 8 букв |
| Сульфиды | Класс химических соединений, представляющих собой соединения металлов с серой, где она имеет степень окисления -2. Могут рассматриваться как соли сероводородной кислоты h3S 8 букв |
Соль угольной кислоты 8 букв
Продолжая исследования, годом позже Дюамель вместе с немецким химиком Андреасом Сигизмундом Маргграфом пришли к выводу, что сода (карбонат натрия, Na2C03) и поташ (карбонат калия, К2С03), которые до этого относили к одной группе веществ, называемой «алкали», или щелочи, — это вещества разные.
Первым из морской воды начинает выпадать карбонат кальция или известняк, затем доломит (карбонат магния).
Так, например, карбонат кальция встречается в виде благородного мрамора, а также в широко распространенных известняках и меле.
В теплых и насыщенных солями водах морей кислый
А для того, чтобы преобразовать карбонат кальция яичной скорлупы, который не усваивается организмом, в цитрат – водорастворимый кальций, усвояемость которого достигает 90 %.
Так например, при окислении широко распространенного в породах пирита получается сернокислое железо, а при действии угольной кислоты — карбонат железа.
Для этого тушку сначала поливают спиртом, а затем поджигают.При запекании или тушении подготовленное таким образом мясо приобретет привлекательный внешний вид и приятный аромат.При приготовлении некоторых блюд из дичи или курицы, а также фруктовых ассорти и тортов требуется произвести фламбирование – уже готовое блюдо после подачи на стол сбрызнуть ароматизированным спиртом или коньяком и поджечь.АммонийАммоний ( карбонат аммония, или углекислый аммоний) представляет собой соль угольной кислоты.
| Углекислый | Относящийся к солям угольной кислоты 10 букв |
| Карбонат | Соль угольной кислоты (сода, поташ и т. п.) 8 букв |
| Карбонат | |
| Сода | Общее название натриевых солей угольной кислоты, имеющих широкое применение в технике, медицине, быту 4 буквы |
| Карбонат | Соль угольной кислоты 8 букв |
| Сода | Техническое название натриевых солей угольной кислоты 4 буквы |
| Сода | Натриевая соль угольной кислоты 4 буквы |
| Бикарбонат | Двууглекислая соль, содержащая на 1 пай основания 2 пая угольной кислоты 10 букв |
| Цианиды | Соли цианистоводородной кислоты. В номенклатуре IUPAC к цианидам относят также C-производные синильной кислоты 7 букв |
| Сульфаты | Минералы, соли серной кислоты h3SO4. В их кристаллической структуре обособляются комплексные анионы SO42. Наиболее характерны сульфаты сильных двухвалентных оснований, особенно Ba2+, а также Sr2+ и Ca2+. Более слабые основания образуют основные соли, часто весьма неустойчивые, более сильные основания 8 букв |
\ [pH = 12,77 \]
,98% -ная соль кальция угольной кислоты для кормов
Содержание карбоната кальция с содержанием корма (CaCO3):> 98%:
Легкий карбонат кальция, также известный как осаждающий карбонат кальция (PCC), и осаждает карбонат кальция. Карбонат кальция получают химическим способом. Он называется легким карбонатом кальция, поскольку его расчетный объем (2,4-2,8 мл / г) больше, чем тяжелый карбонат кальция (1,1-1,9 мл / г), получаемый механически, он не токсичен, не имеет запаха, не раздражающий, обычно белый
Тестовый объект | Результат теста% | ||
Карбонат кальция (CaCO3) | 98.5% | ||
CaO | 54% | ||
Ca | > 39% | ||
Fe2O3 | 9002 | 8 9002 | <0,01 |
SiO2 | <0,02% | ||
MgO | 0.16% | ||
Al2O3 | 0.2% | ||
досуг | 0,16% | ||
рт.ст. | |||
9,0002 F | 3,7 мг / кг | ||
кд | <0,01 мг / кг | ||
Pb | <1 мг / кг | ||
As 9 0.73 мг / кг | |||
НСl Insoible Matter | 0,2% | ||
Твердость, Моос | 3,0 | ||
Потеря зажигания 9 9002 | 4300 900% 43000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000 30000 3000000000000 9000 из-за потери зажигания отстой, г / мл 2,4 ~ 2,8 | ||
Поглощение масла, моль / 100г | 60 ~ 90 | ||
водопоглощение, моль / 100г | 0.63 | ||
PH | 9-10 | ||
белизна | 95% ~ 98% |
сертификаты SGS, ISO9001, HACCP, FCC и HALAL для пищевой марки карбонат кальция
: Заявка 90 00028 : Применение (1) В качестве консерванта пшеницы, яблок, капусты, десертов и др. И пищевой добавки: 325-5000 меш, белизна: 95%, CaCO3: 99.5% (2) Используется в производстве красителей и красителей: PCC / ультрадисперсный активный тяжелый карбонат кальция: 800-1000mesh, белизна: 95%, CaCO3: 96% (3) В качестве адгезивов и герметиков : PCC / ультрадисперсный активный тяжелый карбонат кальция (4) Используется в промышленности по производству высокопроизводительных продуктов: сверхтонкий PCC / тяжелый карбонат кальция в резиновой промышленности: 325mesh, белизна: 95%, CaCO3: 98% (5) Используется в промышленности пластмасс: PCC / тяжелый карбонат кальция: 400 меш, белизна: 95%, CaCO3: 99% (6) Используется в промышленности искусственного гранита: PCC / тяжелый карбонат кальция со сверхтонкой активностью: 325 меш, белизна: 95%, CaCO3: 98.5% (7) Используется при производстве строительных работ ( сухого строительного раствора / бетона) : тяжелый карбонат кальция: 325 меш, белизна: 95%, CaCO3: 98%. (8). Производство барьерного потолка: 600 меш, белизна: 95%, CaCO3: 98,5% Мы с хорошей деловой репутацией, высоким качеством продукции, низкими ценами, Приглашаем всех друзей дома и за рубежом к сотрудничеству. Мононатриевая соль угольной кислоты 99% Свойства: Спецификация Название компании: ХИМИЧЕСКАЯ ЗЕМЛЯ21 Тел: 82-2 -783 — 8063 Электронная почта: sales21 @ chemicalland21.ком Введение продуктов: углекислота, аммониевая медная соль Основная информация Наименование продукта: углекислота, аммониевая медная соль Синонимы: углекислота, аммониевая медная соль; карбонат меди аммония; ; Карбонат меди аммония; карбонат аммония-меди; угольная кислота / аммиак / медь (1: x: x) соль CAS: 33113-08-5 MF: C3H8Cu2N2O9 МВт: 343.19562 EINECS: 251-381-7 Категории продуктов: Мол Файл: 33113-08-5.mol 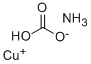
углекислота, аммониевая соль меди Химические свойства углекислота, аммонийно-медная соль Использование и синтез углекислота, соль аммония-меди Продукты и сырье для приготовления углекислота мононатриевая соль 99%
Внешний вид: белый кристаллический порошок
Запах: без запаха
Точка плавления: 270 ° C
Температура разложения:> 50 ° C
Растворимость: 9g / 100 мл в воде (при 20 ° C)
