Металлы в природе. Способы получения металлов
Урок 31. Химия 11 класс ФГОС
Данный видеоурок посвящён нахождению металлов в природе и способам получения металлов.
Конспект урока «Металлы в природе. Способы получения металлов»
С металлами в свободном состоянии человек знаком с самой глубокой древности. Изначально человеку было известно только 7 металлов, так называемы «металлы древности».
За последние 250 лет открыто и получено в свободном виде 86 новых металлов.
Использовать металлы в свободном виде человек начал в древние века. Первыми металлами из них были золото, серебро, медь. Освоение выплавки железа в больших масштабах сделало огромный переворот в промышленности.
В
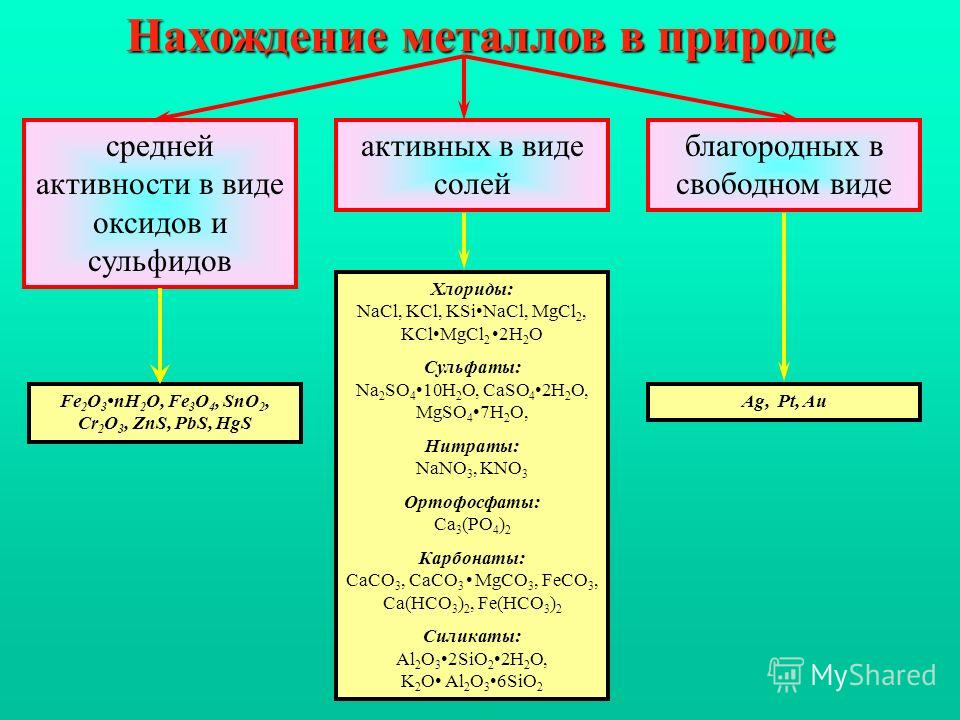
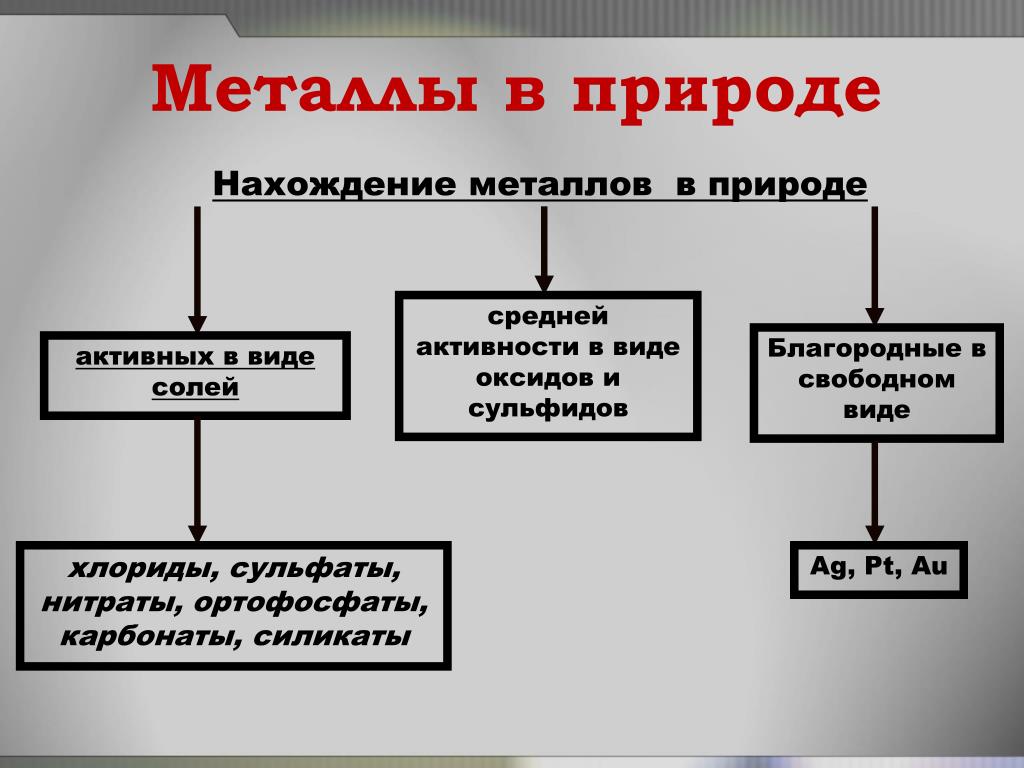
природе металлы встречаются как в виде простых веществ (в свободном виде),
а также в виде соединений. Малоактивные металлы: медь, золото, серебро,
платина, палладий и др. в природе могут находиться как в свободном виде, так и
в составе соединений. Активные металлы: натрий, калий, кальций, алюминий,
магний и др. встречаются в природе только в виде соединений: оксидов,
сульфидов, карбонатов и т.д.
в природе могут находиться как в свободном виде, так и
в составе соединений. Активные металлы: натрий, калий, кальций, алюминий,
магний и др. встречаются в природе только в виде соединений: оксидов,
сульфидов, карбонатов и т.д.
Если металл в природных условиях находится в свободном состоянии, то для получения чистого металла нужно только избавиться от соответствующих смесей. Получение металлов из соединений – это задача металлургии.
Большинство металлов находится в природных условиях в виде соединений – руд. Руда – это природное минеральное образование, в котором атомы химических элементов находятся в окисленном состоянии. Для получения металла для этого необходимо провести процесс восстановления:
Для данного процесса используют восстановители, такие как, водород, более активные металлы, углерод (в виде кокса), оксид углерода (II), постоянный электрический ток.
Технологические
процессы, лежащие в основе промышленных способов получения металлов из руд,
можно разделить на пирометаллургические, гидрометаллургические , электрометаллургические.
Пирометаллургические способы получения металлов основаны на использовании различных восстановителей для получения металлов путем восстановления из руд при высокой температуре.
В гидрометаллургических методах процесс восстановления протекает в водном растворе.
В электрометаллургических процессах восстановителем является постоянный электрический ток.
Водород как восстановитель может использоваться для получения металлов со средней и малой химической активностью: например, меди, вольфрама, молибдена. В данном случае водород восстанавливает металл из его оксида при высокой температуре.
WO3 + 3H2 = W + 3H2O↑
CuO + H2 = Cu + H2O↑
Восстановить металлы из их оксидов можно с помощью более активного металла, поэтому процесс восстановление металлами называется

Так, алюминий используется для получения кальция из его оксида, а металлический кальций используют для получения цезия.
4CaO + 2Al = Ca (AlO2)2 + 3Ca
Ca + 2СsСl = CaCl2 + 2Cs
Углерод и оксид углерода (II) являются сильными восстановителями.
CuO + CO = Cu + CO2↑
PbO + C = Pb + CO↑
Свободный углерод (в виде кокса) и оксид углерода (II) служат восстановителями при производстве железа в доменном процессе. В общем виде:
Fe2O3 + С или CO = Fe3O4 + CO2↑
Постоянный электрический ток является самым сильным восстановителем. С помощью электрического тока получают многие активные металлы: натрий, калий, кальций и др. При этом процесс идёт не в водном растворе, а в расплаве при повышенной температуре.
2NaCl = 2Na + Cl2↑
BaCl2 = Ba + Cl2↑
Алюминий
в промышленных масштабах получают путём электролиза раствора оксида алюминия в
расплавленном криолите (Na3AlF6).
Таким образом, большинство металлов в природе находятся только в виде соединений, в самородном состоянии встречаются золото, медь, палладий и др. Получение металлов из соединений – это задача металлургии. В зависимости от способа получения металлов различают следующие методы: пирометаллургия, электрометаллургия и гидрометаллургия. В пирометаллургическом методе использую восстановители: водород, углерод, оксид углерода (II), более активные металлы.
Предыдущий урок 30 Коррозия металлов
Следующий урок 32 Химия s-, р-элементов
Получите полный комплект видеоуроков, тестов и презентаций Химия 11 класс ФГОС
Чтобы добавить комментарий зарегистрируйтесь или войдите на сайт
«Металлы в природе.
 Общие способы их получения»
Общие способы их получения»Цель урока. Познакомить учащихся с природными соединениями металлов и с самородными металлами. Сформировать понятие о минералах, рудах и металлургии и ее разновидностях – пиро-, гидро- и электрометаллургии.
Образовательные задачи:
- применение обобщения знаний, умений и навыков в новых условиях – создание проблемной ситуации;
- контроль и самоконтроль знаний, умений и навыков с помощью домашней работы;
- уметь устанавливать существенные признаки, являющиеся основой различных классификаций;
- уметь устанавливать причинно-следственные связи между «составом», «химическими свойствами», «получением металла».
Развивающие задачи:
- развитие умений сравнивать, обобщать, правильно формулировать задачи и излагать мысли;
- развитие логического мышления, внимания и
умения работать в проблемной ситуации.

Воспитательные задачи:
- формирование у учащихся познавательного интереса к химии;
- воспитание таких качеств характера, как настойчивость в достижении цели;
- воспитание интереса и любви к предмету через содержание учебного материала, умение работать в коллективе, взаимопомощи, культуры общения.
Оборудование: коллекция руд железа, алюминия, мел, железо, раствор сульфата меди, таблицы «Доменный процесс», « Доменная печь», «Процессы выплавки стали в конвертере, в дуговой печи», «Электрохимическое получение алюминия», фарфоровая ступка, компас.
Оформление и наглядность: таблица размещается на доске.
План урока
1. Организационный момент.
2. Промежуточный контроль знаний.
3. Изучение новой темы.
4. Закрепление.
5. Домашнее задание.
ХОД УРОКА
I. Организационный моментПроверяется готовность к уроку, раздаются листы с тестом (Приложение 2), инструкции для выполнения лабораторной работы (Приложение 4), лотки с демонстрационным материалом – коллекция оксидных руд железа, план урока (Приложение 1), лист наблюдений (Приложение 4), объявляются этапы урока.
Вступительное слово учителя. На этом уроке мы будем рассматривать новую тему «Металлы в природе. Общие способы их получения». Для этого нам нужно вспомнить материал, который мы уже прошли в темах «Химические свойства металлов», «Сплавы». Сейчас мы выполним тест по этим темам.
II. Промежуточный контроль знаний по темам «Химические свойства металлов», «Сплавы»
Учащиеся выполняют тест – 5 минут ( После того, как учащиеся выполнят
тест, необходимо обменяться вариантами,
проверить работу соседа и поставить оценку,
затем тесты передать на проверку учителю.
Учитель просит класс поднять руки, кто написал
тест на 5 или 4 балла. На закрытой доске открывают
заранее подготовленные ответы теста для
самопроверки.
После того, как учащиеся выполнят
тест, необходимо обменяться вариантами,
проверить работу соседа и поставить оценку,
затем тесты передать на проверку учителю.
Учитель просит класс поднять руки, кто написал
тест на 5 или 4 балла. На закрытой доске открывают
заранее подготовленные ответы теста для
самопроверки.
III. Изучение новой темы
Объяснение учителя с опорой на знания учеников. Весь материал разбит на три блока, каждый включает актуализацию темы, объяснение нового материала, закрепление.
Объяснение учителя. В повседневной
жизни нас окружает множество металлических
изделий. Мы с вами познакомились с физическими,
химическими свойствами металлов, а также со
сплавами, которые образуют эти металлы, но до сих
пор нам ничего неизвестно в каком виде
встречаются металлы в природе, как их получают и
как это связано с химическими свойствами
металлов.
1. Металлы в природе
Актуализация знаний.
1.Что такое электрохимический ряд напряжений? (Это
ряд металлов, расположенных в зависимости от их
восстановительной способности.)
2. Что такое восстановительная способность
металлов? (Это способность атомов металлов
отдавать электроны в химических реакциях.)
3. Как изменяется восстановительная способность
металлов в электрохимическом ряду напряжений? (В
электрохимическом ряду напряжений слева направо
восстановительная способность атомов
металлов уменьшается).
Новый материал
Сегодня мы рассмотрим не только нахождение
металлов в природе, но и, как связаны между собой
химическая активность металлов и нахождение
металлов в природе.
Объяснение учителя, заполнение таблицы на доске,
сопровождающееся объяснением учителя с опорой
на знания учеников, и в тетрадях. Демонстрация
слайдов №1, №3-10 (тема «Получение металлов»)
Таблица № 1
Природные соединения алюминия
| Форма, в которой металлы встречаются в природе | В свободном виде | В самородном виде, и в форме соединений | В виде соединений |
| Примеры металлов | Золото Au | Серебро Ag | Литий Li |
| Платина Pt | Медь Cu | Натрий Na | |
| Ртуть Hg | Кальций Ca | ||
| Олово Sn | Алюминий Al |
*Место металла в 2-й, 3-й, или 4-й колонках
определяется учениками, после рассмотрения
образцов на слайдах коллекции.
Коллективное устное обсуждение таблицы с классом
Природные химические соединения металлов
называют минералами. минералы, содержащие в
количествах. пригодных для получения в
промышленности, называют рудами.
На основании вышесказанного можно составить
следующий логический ряд, указывая ключевые
слова. Один ученик работает у доски с помощью
учителя, класс записывает в тетради
«Формы существования металлов в природе»
Металл ––> минерал
––> руды
Природное Природное
химическое
химическое соединение, содержащее
металл в количествах,
соединение
пригодных
Составим еще одну классификацию природных соединений металлов по признаку принадлежности минералов к одному из классов неорганических соединений
Минералы, руды
| Оксиды | |
| Соли |
Таблица заполняется учениками по учебнику [2],
работа в парах. Затем проверяется – вызванный
ученик зачитывает свой вариант, и учитель
предлагает классу составить третью
классификацию природных соединений металлов по
кислотному остатку минералов, заполнить вторую
колонку таблицы № 2, работа в парах.
Затем учитель вызывает пару учеников, которые
зачитывают свой вариант, и обсуждают его с
классом. (Приложение 3)
Затем проверяется – вызванный
ученик зачитывает свой вариант, и учитель
предлагает классу составить третью
классификацию природных соединений металлов по
кислотному остатку минералов, заполнить вторую
колонку таблицы № 2, работа в парах.
Затем учитель вызывает пару учеников, которые
зачитывают свой вариант, и обсуждают его с
классом. (Приложение 3)
Закрепление темы
1. Назовите, в каком виде встречаются металлы в
природе? (Металлы встречаются в природе как
в чистом виде. так и виде соединений)
2. Как это связано с химической активностью
металлов? (Малоактивные металлы
встречаются в свободном виде: золото, платина;
более активные металлы встречаются как в
самородном виде, так и в соединениях – серебро –
олово; активные металлы – от олова до лития
встречаются только в виде соединений)
3. Какая таблица отражает эти закономерности
нахождения металлов в природе?
(Электрохимический ряд напряжения металлов. )
)
2. Металлургия – наука и отрасль промышленности, изучающая получение металлов из руд
Актуализация знаний
1. Что такое руды? (Руды – это минералы,
содержащие металл в количествах, достаточных для
получения его в промышленности.)
2. Какие руды вам известны? (Руды бывают
оксидные, сульфидные, карбонаты, сульфаты,
хлориды, нитраты.)
Новый материал
Объяснения учителя с опорой на знания учеников
– Ребята, как вы думаете, из каких руд легче
всего получить металл в чистом виде и почему?
Наиболее пригодны для получения металлов
оксидные руды, затем сульфидные, следующие
карбонатные руды и сульфаты. Например, железо
получают именно из оксидных руд, поэтому такие
руды имеют наибольшее значение. Следующими
считаются сульфидные руды железа. Среди
оксидных руд железа наиболее удобен для
переработки магнитный железняк Fe3O4, так как там
наибольший процент содержания железа по
сравнению с другими образцами.
Учащиеся рассматривают коллекцию руд железа
(работа в группах), выполняют по инструкции (Приложение 4)
исследование физических свойств руд железа,
записывают результаты в лист наблюдений,
предварительно обсудив в группе. Работа в
группах, с распределением функций участников:
руководитель, выполняющий эксперименты, ученик,
который ведет протокол, то есть пишет уравнения
реакций и наблюдения. В процессе выполнения
работы в группе коллективно выставляют каждому
оценку. Результаты обсуждаются в классе
Лабораторная работа «Исследование физических свойств оксидных руд железа»
| Наименование руды, формула рудообразующего оксида железа | Окраска и блеск | Цвет черты на фарфоре | Магнитные свойства |
1. Магнитный железняк Fe3O4 Магнитный железняк Fe3O4 |
Темно-серый металлический блеск | Черная | Магнитные свойства |
| 2. Красный железняк Fe2O3 | Красный | Красная или красно-бурая | Слабомагнитные свойства |
| 3. Бурый железняк Fe2O3*nH2O | Бурый | Бурая | Не обладает магнитными свойствами |
*Текст, выделенный темным шрифтом, заполняется учащимися
Закрепление темы
1. Какие руды наиболее пригодны для получения
металлов? (Наиболее удобны для получения
металлов оксидные руды, затем сульфидные,
карбонатные, сульфатные)
2. Какая руда железа и почему, из рассмотренных
в лабораторной работе, наиболее пригодна для
промышленной обработки? (Магнитный железняк,
так как в нем в нем самый высокий процент
содержания железа)
Какая руда железа и почему, из рассмотренных
в лабораторной работе, наиболее пригодна для
промышленной обработки? (Магнитный железняк,
так как в нем в нем самый высокий процент
содержания железа)
3. Общие способы получения металлов, сопровождающие их химические процессы
Актуализация знаний
1. Написать схему восстановления металлов из
ионов. (Me+n + ne ––> Me0)
2. Что такое чугун? (Чугун – сплав на основе
железа, содержащий от 2 – 4,5 %% углерода, а также
марганец, кремний, фосфор и серу)
3. Что такое сталь? (Сталь – сплав на основе
железа, содержащий не менее 2% углерода)
Новый материал
Объяснение учителя, демонстрация
химических реакций, параллельно запись реакций в
тетрадь, на доске учениками с помощью учителя.
В зависимости от способа извлечения металла из
руды выделяют следующие виды металлургических
процессов
Схема
1. Электрометаллургия – выделение металлов из
их солей и оксидов плд действием электрического
тока
Электрометаллургия – выделение металлов из
их солей и оксидов плд действием электрического
тока
NaCl электролиз ––> 2Na + Cl2
Демонстрация слайда №2 (тема «Получение металлов»)
2. Гидрометаллургия – методы получения металлов, основанные на химических реакциях, протекающих в растворах
CuSO4 + Fe ––> FeSO4 + Cu
Демонстрация опыта
3. Пирометаллургия – методы извлечения металлов из руд под действием высоких температур. Оксидные руды и оксиды восстанавливают углем, оксидом углерода (II), более активным металлами (алюминий, магний, натрий)
FeO + C ––> Fe + CO
Fe2O3 + 2Al ––> 2Fe + Al2O3
Демонстрация видео слайда №11 (тема «Получение металлов»)
Сульфидные руды подвергаются обжигу:
2ZnS + 3O2 ––> 2ZnO + 2SO2
Доклад «От руды к чугуну» (Приложение
5).
Доклад «От чугуна к стали» (Приложение 5).
Демонстрация слайдов № 3, 4, 5 (тема «Железо»)
Доклад или презентация заранее готовятся группой учеников, где распределены роли среди участников: руководитель, помощники, докладчик. В сданной учителю работе должны быть выставлены оценки самими исполнителями работы, а также она оценивается классом, если есть или высказываются замечания. Доклад обсуждается с классом.
Закрепление темы
1. С какими видами металлургических процессов
вы сегодня познакомились? (В зависимости от
способа получения металлов выделяют пиро-.
гидро-, электрометаллургия)
2. Какие этапы переработки железа вы знаете? (От
руды к чугуну, от чугуна к стали)
IV. Закрепление
Выполнить упражнение 6,7 из рабочей тетради, тема «Получение металлов» [3]
Затем с помощью учителя ученики делается вывод
по уроку.
Вывод по уроку. Сегодня мы рассмотрели нахождение металлов в природе и получение металлов.
1. Как вы думаете от чего зависит, в какой форме
будет находиться металл в природе?
(Форма нахождения металла в природе зависит от
химической активности металла)
2. От чего зависит способ переработки руды для
получения металла? (Способ получения металла
зависит от вида, в котором находится металл в
природе, то есть от руды.)
Таким образом, мы видим, что получение металлов зависит от химической активности металлов, то есть химических свойств, а также от количественного и качественного состава природных соединений металлов.
Формулируется проблемный вопрос, для домашнего задания, выставляются оценки за урок.
V. Домашнее задание
Проблемный вопрос. Как строение
атомов металлов влияет на способы получения
металлов?
Параграф 9 «Получение металлов», страница 71-74,
упражнение 2-5[2]
рабочая тетрадь, страница 69, упражнение
6,7 [3], кто не успел в классе
Список литературы.
1. Химия 9 класс. Металлы. Получение металлов,
Железо Мультимедийное приложение к учебнику
О.С.Габриеляна. Электронное учебное издание. ООО
«Дрофа» 2011.
2. Габриелян О.С. Химия 9 класс. Учебник , М.:
Дрофа, 2011.
3. Габриелян О.С., Яшукова А.В., Рабочая
тетрадь 9 кл. О.С.Габриелян «Химия, 9 класс». М.,
Дрофа, 2011.
4. Шпаусус З. Путешествие в мир химии,
«Просвещение», М., 1967.
Откуда берутся металлы?
НАУКА — Физические науки
Задумывались ли вы когда-нибудь…
- Как человеческий организм использует металлы?
- Откуда берутся металлы?
- Что такое металлические сплавы?
Теги:
Просмотреть все теги
- Наука,
- Физические науки,
- Металл,
- Металлический сплав,
- Сталь,
- нержавеющая сталь,
- Кобальт,
- Цинк,
- Меркурий,
- Медь,
- Кальций,
- Железо,
- никель,
- Золото,
- Олово,
- Руда,
- Минерал,
- Рок,
- Корка,
- Розовое золото,
- Чугун,
- Углерод,
- Бронза,
- Хром,
- Молибден
Сегодняшнее чудо дня было вдохновлено Кэтрин. Кэтрин Уондерс , “ Как вы делаете металл? ”Спасибо, что ДУМАЕТЕ вместе с нами, Екатерина!
Кэтрин Уондерс , “ Как вы делаете металл? ”Спасибо, что ДУМАЕТЕ вместе с нами, Екатерина!
Компьютеры. Смартфоны. Ювелирные изделия. Небоскребы. Автомобили. Оглянись! Повсюду вы увидите предметы, которые не могли бы существовать без металла. Можете ли вы представить себе жизнь без этого прочного, блестящего вещества?
Даже человеческому телу нужен металл! Он использует кобальт для производства эритроцитов. Цинк помогает иммунной системе. Высокий уровень ртути и меди может вызвать серьезные проблемы. Даже вашим костям нужна помощь одного типа металла — кальция!
Да, металлы очень важны. Они помогают людям оставаться здоровыми. Люди также используют металлы для создания объектов, которые меняют мир. Но откуда берутся все эти металлы?
Некоторые металлы находятся в земной коре. Кобальт, железо и никель распространены в природе. Так же как и золото, цинк, олово, медь и многие другие. Однако редко можно найти много металлов в больших количествах отдельно от других материалов. Чаще встречающиеся в природе металлы смешивают с горными породами и минералами.
Чаще встречающиеся в природе металлы смешивают с горными породами и минералами.
Когда металл смешивается с горными породами и минералами, это называется рудой. Прежде чем использовать металлы, люди должны удалить их из руды. Этот процесс называется плавлением. Он включает в себя нагрев металла выше его точки плавления. После расплавления металл можно фильтровать для удаления других материалов.
Металлы, встречающиеся в природе, хрупкие. Они также подвержены ржавчине и коррозии. Чтобы сделать более прочные и долговечные материалы, люди смешивают металлы вместе и с другими веществами. Результат называется металлическим сплавом.
Какие сплавы металлов вам известны? Одним из самых распространенных металлических сплавов является сталь. Он сделан путем соединения железа и углерода. Нержавеющая сталь — это сплав, который часто используется для изготовления столовых приборов. Это смесь железа, углерода, хрома и молибдена.
Вы когда-нибудь видели украшение из розового золота? Это сплав золота и меди. Как насчет чугунной сковороды? Чугун – еще один сплав. Это смесь железа и углерода. Еще одним распространенным сплавом является бронза, изготовленная из меди и олова.
Как насчет чугунной сковороды? Чугун – еще один сплав. Это смесь железа и углерода. Еще одним распространенным сплавом является бронза, изготовленная из меди и олова.
Какие предметы, которые могут содержать металлы, вы используете каждый день? А сплавы металлов? Вы едете в школу на автобусе или другом транспортном средстве? Скорее всего он из стали. Стулья в вашем классе могут быть изготовлены из железа, алюминия или нержавеющей стали. Если вы используете какую-либо цифровую технологию, она, вероятно, содержит золото, серебро, медь или платину. Как только вы начнете замечать вокруг себя весь металл, уже трудно остановиться!
Common Core, Научные стандарты следующего поколения и Национальный совет по социальным исследованиям.»> Стандарты: NGSS. PS1.A, NGSS.PS1.B, CCRA.R.4, CCRA.L.3, CCRA.L.6, CCRA.R.1, CCRA.R.2, CCRA.SL.1, CCRA .R.10, CCRA.W.2, CCRA.L.1, CCRA.L.2
PS1.A, NGSS.PS1.B, CCRA.R.4, CCRA.L.3, CCRA.L.6, CCRA.R.1, CCRA.R.2, CCRA.SL.1, CCRA .R.10, CCRA.W.2, CCRA.L.1, CCRA.L.2
Интересно, что дальше?
Завтрашнее чудо дня обязательно станет большим хитом!
Попробуйте
Готовы продолжать учиться? Попросите друга или члена семьи помочь вам с этими действиями.
- Исследуйте металлы в повседневной жизни. Сколько предметов, сделанных из металлов и других добытых материалов, вы использовали? Удивил ли вас какой-либо из этих предметов? Обсудите с другом или членом семьи.
- Могут ли быть металлические предметы на вашем заднем дворе или в местном парке? Узнайте, сделав свой собственный металлоискатель! Убедитесь, что друг или член семьи помогает вам, и просмотрите список поставок, прежде чем начать. Затем проверьте свой металлоискатель. Что вы можете найти?
- Сядьте в одной комнате дома или в школе. Оглянись. Какие предметы из металла вы видите? Сделай список.
 Затем выберите один пункт из списка. Напишите несколько предложений, чтобы подробно описать его. Как это выглядит? Как вы думаете, из какого металла он сделан? Это природный металл или металлический сплав? На что похож объект? Он крепкий или хрупкий? Будьте максимально подробны.
Затем выберите один пункт из списка. Напишите несколько предложений, чтобы подробно описать его. Как это выглядит? Как вы думаете, из какого металла он сделан? Это природный металл или металлический сплав? На что похож объект? Он крепкий или хрупкий? Будьте максимально подробны.
Wonder Sources
- https://www.livescience.com/18247-metals-human-body-health-nigms.html (по состоянию на 13 ноября 2019 г.)
- https://www.industrialmetalsupply.com/ blog/where-do-metals-come-from/ (по состоянию на 13 ноября 2019 г.)
- https://www.visualcapitalist.com/20-common-metal-alloys/ (по состоянию на 13 ноября 2019 г.)
- https: //courses.lumenlearning.com/introchem/chapter/occurrence-of-metals/ (по состоянию на 13 ноября 2019 г.)
- https://www.britannica.com/technology/smelting (по состоянию на 14 ноября 2019 г.))
Получили?
Проверьте свои знанияWonder Contributors
Благодарим:
Иммануэль, Ралин, Хэдли и Шрутик
за ответы на вопросы по сегодняшней теме Wonder!
Удивляйтесь вместе с нами!
Что вас интересует?
Wonder Words
- корка
- содержат
- хрупкий
- вещество
- материалы
- минералы
- количества
- отфильтровано
- температура плавления
Примите участие в конкурсе Wonder Word
Оцените это чудо
Поделись этим чудом
×ПОЛУЧАЙТЕ СВОЕ ЧУДО ЕЖЕДНЕВНО
Подпишитесь на Wonderopolis и получайте Чудо дня® по электронной почте или SMS
Присоединяйтесь к Buzz
Не пропустите наши специальные предложения, подарки и рекламные акции. Узнай первым!
Узнай первым!
Поделитесь со всем миром
Расскажите всем о Вандополисе и его чудесах.
Поделиться Wonderopolis
Wonderopolis Widget
Хотите делиться информацией о Wonderopolis® каждый день? Хотите добавить немного чуда на свой сайт? Помогите распространить чудо семейного обучения вместе.
Добавить виджет
Ты понял!
Продолжить
Не совсем!
Попробуйте еще раз
Металлы, сплавы и соединения металлов — Science Learning Hub
Добавить в коллекцию
От титановых имплантатов до новых сверхпроводящих сплавов и полезных соединений металлов — мы все больше зависим от металлов. Без металлов современная цивилизация буквально рухнула бы. Около 80% известных химических элементов составляют металлы.
Физические свойства металлов
Металлы обладают свойствами, подходящими для широкого спектра применений. Они характерно блестящие, и большинство из них ковкие, пластичные, плотные, очень хорошие электрические проводники и имеют высокие температуры плавления. Ковкость — это способность материала деформироваться при сжатии — золото очень пластично, и его можно растолочь в чрезвычайно тонкий лист.
Они характерно блестящие, и большинство из них ковкие, пластичные, плотные, очень хорошие электрические проводники и имеют высокие температуры плавления. Ковкость — это способность материала деформироваться при сжатии — золото очень пластично, и его можно растолочь в чрезвычайно тонкий лист.
Кристаллическая структура металлов
Когда мы смотрим на поверхность металла, часто можно увидеть кристаллы. Кристаллы отражают симметричное расположение положительных ионов металла в основной структуре, которую мы не можем видеть.
Положительные ионы в металле плотно упакованы, так что промежутки между ними сведены к минимуму. Когда атомы металла собираются вместе, образуя кристалл, они могут быть:
- гексагональными плотно упакованными
- гранецентрированными кубическими
- объемноцентрированными кубическими.
При охлаждении расплавленного металла атомы металла образуют кристаллическую решетку. При достаточном количестве времени и идеальных условиях кристаллическая решетка может вырасти до очень больших размеров с идеальной внутренней кристаллической структурой. Идеальные условия встречаются редко, и реальность такова, что почти каждый твердый металл существует в виде нагромождения кристаллов разного размера. Каждый отдельный кристалл в организме называется зерном. Эти зерна представляют собой кристаллические структуры, которые имеют множество дефектов, искажающих кристаллическую решетку.
Идеальные условия встречаются редко, и реальность такова, что почти каждый твердый металл существует в виде нагромождения кристаллов разного размера. Каждый отдельный кристалл в организме называется зерном. Эти зерна представляют собой кристаллические структуры, которые имеют множество дефектов, искажающих кристаллическую решетку.
Что такое сплавы?
Смеси металлов, называемые сплавами, используются чаще, чем чистый металл. Путем легирования можно улучшить некоторые важные свойства металлов.
- Припой, используемый в электронной промышленности, представляет собой смесь олова и свинца. Один тип припоя (63% олова и 37% свинца) имеет более низкую температуру плавления, но тверже любого из металлов. Эти свойства позволяют успешно его использовать.
- Амальгама представляет собой сплав на основе ртути. Стоматологическая амальгама представляет собой сплав ртути, серебра, олова, меди и цинка. Он износостойкий, устойчивый к коррозии и обладает высокой ударной вязкостью.

- Титановый сплав, известный как Ti6Al4V, используется в аэрокосмической промышленности. Он легкий, очень прочный и обладает высокими антикоррозионными свойствами.
Исследовательская работа профессора Делян Чжан в Университете Вайкато сосредоточена на недорогих порошках из титанового сплава.
Соединения металлов
Большинство металлов не встречаются в естественном состоянии. Они часто встречаются в виде соединений, таких как оксиды металлов, сульфиды и галогениды.
- Оксид алюминия является основным металлическим соединением, присутствующим в руде, известной как боксит.
- Железный колчедан или «золото дураков» в основном представляет собой сульфид железа.
- Соляной завод на озере Грассмир в Мальборо производит соединение металла, известное как хлорид натрия, из «соленой» морской воды.
Металлы могут быть получены (выплавлены) из их руд различными способами:
- Алюминий производится из его руды (бокситов) путем пропускания очень сильного электрического тока через расплавленную смесь руды и соединения, называемого криолитом.
 .
. - Титан в основном производится из руды (рутила) с помощью процесса Кролла, при котором руда обрабатывается газообразным хлором с последующей реакцией с металлическим магнием.
Консервная банка? Жестяная крыша? Фольга?
В настоящее время жесть редко используется в консервной промышленности, в качестве кровельного материала или фольги для приготовления пищи – ее заменили более дешевые материалы.
Олово является важным легирующим металлом. Припой, бронза и стоматологическая амальгама содержат олово, а провода, используемые в сверхпроводящих магнитах, используемых в приборах ядерного магнитного резонанса (ЯМР) и сканерах магнитно-резонансной томографии (МРТ), сделаны из сплава олова и ниобия.
Олово переходит из обычного повседневного состояния, известного как «белое олово», в мягкое порошкообразное состояние, называемое «серым оловом», при воздействии температуры ниже 0 °C в течение определенного периода времени. Эти различные формы олова известны как аллотропы.
В большинстве больших соборов есть впечатляющие музыкальные органы, трубы которых сделаны из оловянно-свинцового сплава. В зимние месяцы, если температура воздуха в соборе длительное время опускается ниже нуля, трубы могут заболеть «оловянной болезнью». Трубки покрываются порошкообразным серым веществом, и они теряют качество звука.
Одной из причин, объясняющих, почему армии Наполеона не удалось победить русскую армию зимой 1812 года, было то, что оловянные пуговицы на гимнастерках французских солдат страдали «оловянной болезнью». В конце концов пуговицы превратились в порошок, а без пуговиц солдатские гимнастерки свалились, и они замерзли насмерть!
Идея занятия
В упражнении «Изготовление модельных сплавов» учащиеся используют пластилин и песок, чтобы изучить, как добавление других элементов может изменить пластичность металла.
Полезная ссылка
Узнайте больше о разнице между черными и цветными металлами на веб-сайте ScienceDirect.

 Затем выберите один пункт из списка. Напишите несколько предложений, чтобы подробно описать его. Как это выглядит? Как вы думаете, из какого металла он сделан? Это природный металл или металлический сплав? На что похож объект? Он крепкий или хрупкий? Будьте максимально подробны.
Затем выберите один пункт из списка. Напишите несколько предложений, чтобы подробно описать его. Как это выглядит? Как вы думаете, из какого металла он сделан? Это природный металл или металлический сплав? На что похож объект? Он крепкий или хрупкий? Будьте максимально подробны.
 .
.