количество газа пропан — бутан в бытовом баллоне 50 , 27, 12 , 5 литров — mAlexa.ru — Мануфактура Алекса
В бытовом газовом баллоне объемом 50 , 24 , 12 , 5 литров, согласно действующим нормативам, должно быть не более 85% сжиженного газа от объема баллона.
то есть в полностью пустые баллоны должно быть залито заправщиком:
50 литровый баллон (22кг) — 42,5 литра = газа 23,16 кг (лето) или 21,97 кг газа (зима) = полный баллон 35,16 кг (лето) или 43,97 кг (зима).
27 литровый баллон (14,4кг) — 22,95 литра = газа 12,5 кг (лето) или 11,86 кг (зима) = полный баллон 26,9 кг (лето) или 26,26 кг (зима)
12 литровый баллон (9кг) — 10,2 литра = газа 5,56 кг (лето) или 5,27 кг (зима) = полный баллон 14,56 кг (лето) или 14,27 кг (зима)
5 литровый баллон (3кг) — 4,25 литра = газа 2,32 кг (лето) или 2,2 кг (зима) = полный баллон 5,32 кг (лето) или 5,2 кг (зима).
Важно: нормы заправки баллонов по объему могут отличаться на заправках, объем заправки газа (или вес) должен быть явно указан продавцом газа при указании стоимости заправки баллона, в этом случае вес можно аналогично пересчитать, согласно указанному объему заправки бытового газового баллона.
Примечание:
заправляемая газовая смесь летняя — 50% пропана + 50% бутана имеет теплотворную способность 6470 ккал/л или 11872 кКал/кг или 115 мДж/м3. Плотность 0,545 кг/литр. Плотность паровой фазы 2,2 кг/м куб.
заправляемая газовая смесь зимняя — 90% пропана + 10% бутана имеет теплотворную способность 6175 ккал/л или 11943 кКал/кг. Плотность 0,517 кг/л.
Сколько в 1 кг сжиженного газа Киловатт часов?
Один килограмм газа при сгорании даст выделяемую энергию около 11900 кКал/кг (без учета КПД).
1кВт/ч = 860 кКал
в 1 кг сжиженного газа 11900 кКал
соответственно в 1 кг сжиженного газа примерно 13,83 кВт/ч
Эквивалентная мощность выделяемая 1 кг сжиженного газа с учетом типового КПД тепловых приборов
При использовании систем обогрева с отводом газов КПД обычно составляет около 85%, В этом случае эффективная «эквивалентная мощность» обогрева составит 85% от 13,83 (кВт/ч)/кг, что составит примерно 11,77 (кВт/ч)/кг.
Те с учетом типового КПД 85%, 1 кг сжиженного газа даст эквивалентную мощность приблизительно равную 11,77 кВт/ч.
Можно ли по давлению определить остаток сжиженного газа в пропан-бутановом баллоне?
Ответ — увы нет, давление в баллоне определяется давлением паровой фазы над жидкостью, она неизменна при любом объеме жидкости, так что определить остаток газа по давлению в баллоне с пропаном бутаном нельзя. Для определения объема остатка газа необходимо взвесить баллон, вычесть вес баллона и пересчитать исходя из плотности (см выше)
технология замены вентиля газового баллона
Искренне Ваш, Alex.
ps
Сколько килограмм газа в 50-литровом баллоне
Сколько килограмм газа в 50-литровом баллоне
- Опубликовано: 28.
 02.2018 05:05
02.2018 05:05
День добрый дорогие друзья!!! Сегодня мы ответит на вопрос «Сколько килограмм газа в 50-литровом баллоне». Данный вопрос на самом деле не много сложнее, чем может показаться на первый взгляд – формально баллон вмещает 50л газа, осталось только узнать, сколько литров содержит 1 килограмм. Но баллон – хранилище, в котором газ находится под давлением.
Газ (пропан-бутан) в баллоне находится сразу в двух состояниях – большую часть баллона занимает газ в жидком состоянии, еще некоторая часть пропан-бутана существует внутри баллона в газообразной форме.
Количество кубов сжиженного газа в баллоне меняется вместе с изменением температуры окружающей среды. Когда температура повышается, газ расширяется в баллоне и увеличивает давление на стенки сосуда, в результате чего, при слишком высоком давлении появляются трещины на баллоне.
Газ заходит в эти трещины, провоцируя все большее их появление и работая на разрушение сосуда изнутри. Таким образом может происходить и утечка газа.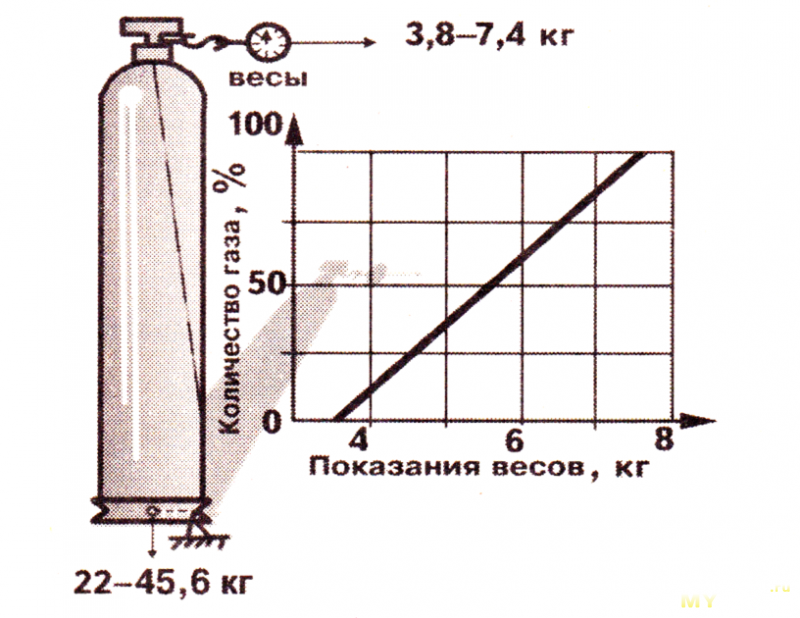
Поэтому емкости для хранении пропан-бутана наполняются не полностью, чтобы избежать аварий на случай расширения газовой смеси. Поэтому ответ на вопрос, сколько килограммов газа находится в 50-литровом баллоне, неочевиден.
Правила обращения с емкостями под давлением гласят, что уровень пропан-бутана в резервуаре не может превышать 85% от его объема. Если заправить больше, то резко возрастает угроза взрыва переполненного баллона из-за катастрофически высокого внутреннего давления пропан-бутана. Именно поэтому ни на одной заправке вам не заправят полный газовый баллон. Это опасно!
Итак, сколько килограммов газа в 50-литровом баллоне можно хранить и транспортировать, не опасаясь столкнуться с угрозой взрыва?
В бытовом газовом баллоне объемом 50 литров, согласно действующим нормативам, должно быть не более 85% сжиженного газа от объема баллона.
50 * 0,85 = 42,5 литров газа.
Итого в полностью пустой 50 литровый баллон заправщик заправляет:
42,5 литра = 23,16 кг газа (летом) или 21,97 кг газа (зимой)
На заправке вам могут обозначить количество заправляемого газа как в литрах, так и в килограммах. Если прочитав нашу статью у вас возник вопрос «стоимости 1 кг пропана» вы всегда можете обратить внимание на нашу статью. А на сегодня все друзья наша команда всегда рада ответить на ваши вопросы. Пишите нам.
Таблица бъемов технических газов в валлонах.
На данной странице мы представляем таблицу с объемами и весами газов в баллонах. С помощью нее вы сможете более точно рассчитать потребность и расход на вашей производственной площадке.
В таблице представлены технические газы продающиеся у нас на сайт 50ballon.ru их объем и вес кислорода, углекислоты, азота, аргона, пропана, ацетилена в стандартных 40 или 50 литровых баллонах.
Так-же более подробно узнать о каждом из этих продуктов, вы сможете, нажав на соответствующую ссылку в таблице объема и веса этих технических газов.
Таблица объема и веса баллонов с техническими газами.
Газ Объем баллона Объем газа Вес газа
Кислород технический 40 л 6,3 куб.м 8,3 кг
ГОСТ 6331-78
Азот технический 40 л 5,7 куб.м 7,5 кг
ГОСТ 9293-74
Аргон технический 40 л 6,3 куб.м 7,5 кг
Углекислота техническая 40 л 6,0 куб. м 20-24 кг
м 20-24 кг
ГОСТ 8050-85
Пропан газ 50 л 9,5 куб.м 21,5 кг
ГОСТ 20448-90
Ацетилен технический 40 л 5,3 куб.м 5 кг
ГОСТ 5457-7
Гелий технический 40 л 5,7 куб.м 1 кг
В Компании 50ballon.ru вы можете купить газовые баллоны, баллоны как новые так и бывшие в употреблении, заправить баллоны или обменять свои старые. Наши менеджеры оперативно примут заявку будь то заправка пропановых баллонов и вы просто хотите купить пустые пропановыее баллоны, обработают ее и по вашему желанию произведут доставку в кратчайшие сроки а нашем автотранспорте.
Благодаря многолетнему опыту работы, современному оборудованию и компетентным сотрудникам наша компания способна гарантировать своевременные поставки полных пропановых баллонов в любом требуемом количестве.
Объем газа в 50 литровом баллоне
Re: А сколько кубов газа в 50л баллоне?Я правильно > считаю, что примерно 10?
> В баллоне 42л сжиженного газа.
В бытовом баллоне 50 литров получается 10 куб газа, проверено экпериментально (стоит счетчик). При условии заправки пустого баллона 40-41 литров газа.
Здравствуйте. Сколько литров газа содержится в в 50-литровом баллоне? На сколько его хватает?
Для того, чтобы оставить свой ответ на вопрос
Необходимо авторизоваться Или пройти быструю процедуру регистрации
Зарегистрироваться!
Технические газы – это специальные вещества, получаемые из атмосферы путём разделения, а также из углеводородного сырья во время определенных химических реакций. В большинстве случаев технические газы используются в промышленных, а также бытовых целях, в том числе во время строительства и сварки.
Современная промышленность предполагает образование смесей, которые включают в себя несколько компонентов – газов.
Вне зависимости от вида технического газа или газовой смеси, предполагается её хранение и транспортировка в специальных баллонах. В частном пользовании довольно популярны баллоны на 50 литров.
Рассмотрим сколько литров газа в 50 литровом баллоне содержится по факту? Ответы на поставленный вопрос могут быть разными, так как они зависят от молекулярной массы вещества и степени сжатия газа.
- Углекислота – 24, 6 килограммов.
- Пропан – 21 килограмм или 40 литров.
- Азот и аргон – 10 – 12 килограммов.
- Гелий – 8 – 10 килограммов.
- Ацетилен – 6 килограммов.
50-литрового баллона с пропаном для отопления большого дома, в лютую зиму, хватит на сутки, в остальных случаях – максимум на неделю. Баллон с газом для приготовления еды может использоваться, как минимум, месяц.
Баллонов с газом при сварке потребуется много, ориентировочно – 10 литров – 300 минут, 40 литров – 1200 минут.
Принимая во внимание подобные значения, можно понять, что 50-литровый баллон с газом – это не слишком значительные запасы.
Сколько газа помещается в 50-литровый баллон? Ни для кого не секрет, что объем измеряется в литрах. Многие еще со школьной скамьи помнят о том, что у разных веществ, разная плотность, поэтому и их вес, несмотря на одинаковый объем, может отличаться. Часто твердые вещества, обычно тяжелее, чем жидкости. Однако самый легкий вес у газообразных веществ. Поэтому их иногда закачивают в сжиженном виде (сжижают), чтобы поместилось больше. Так как многие приобретают газ для использования в бытовых целях, в качестве топлива для авто и т. д., их интересует, сколько литров газа в 50 литровом баллоне, или в других объемах. Но, 50 литров – это стандарт, поэтому чаще всего интересуются именно тем, сколько газа в таком баллоне.
Дать точный ответ на данный вопрос достаточно сложно, если учесть, что редко используется чистый газ. Если допустить, что в баллоне чистый пропан, объем будет равен 22,44 м3, если бутан – 16,67 м3. Тем не менее, нередко используется смесь этих газов, поэтому в среднем в 50-литровый баллон помещается около 20 кубометров.
Если допустить, что в баллоне чистый пропан, объем будет равен 22,44 м3, если бутан – 16,67 м3. Тем не менее, нередко используется смесь этих газов, поэтому в среднем в 50-литровый баллон помещается около 20 кубометров.
Вопрос «Сколько литров газа в 50-литровом баллоне» вводит некоторых людей в ступор – баллон на 50 литров должен вмещать эти же 50 литров сжиженного газа. Но баллон – хранилище газа, находящееся под давлением. Газ (пропан-бутан) в баллоне находится сразу в двух состояниях – большую часть баллона занимает пропан в жидком состоянии, еще некоторая часть газа существует внутри баллона как раз в газообразной форме.
При изменении температуры газ в баллоне изменяет свой объем, при повышении температуры происходит расширение пропан-бутана и увеличение давления газа на стенки баллона изнутри. Таким образом, ответ на вопрос, сколько литров газа помещается в 50-литровом баллоне, неочевиден.
Как перевести килограммы пропан-бутана в литры?
Литр=Килограмм/Плотность
Как перевести пропан-бутан из литров в килограммы?
Килограмм= Литр*Плотность
Как узнать плотность? Плотность пропан-бутана непостоянна. Мы для вас приготовили таблицу плотности пропан-бутановой смеси в зависимости от температуры воздуха (измеряемой в о С) и процентного соотношения пары двух газов в получаемой сжиженной смеси.
Мы для вас приготовили таблицу плотности пропан-бутановой смеси в зависимости от температуры воздуха (измеряемой в о С) и процентного соотношения пары двух газов в получаемой сжиженной смеси.
В верхней строке приведена температура окружающего воздуха (в о С), в левом столбце – процентное соотношение пропан-бутан (то есть, «90/10» означает, что смесь содержит 90% пропана и 10% бутана). На пересечении значений соотношения и температуры находится плотность смеси.
Газовый наполненный баллон объемом 50 литров будет содержать (при условии пропана и бутана в соотношении 70/30 и температуре 5 о С):
Сколько газа в баллоне 50 литров с пропаном?
Газоснабжение
Пятидесятилитровые баллоны являются самой распространенной емкостью для хранения сжиженного газа. Их используют на дачах и в не газифицированных поселках, ставят в автомобили и бытовки. Причем всех пользователей подобных емкостей интересует один вопрос. И дачники, и домовладельцы, и автомобилисты желают знать: насколько хватит им такого баллона.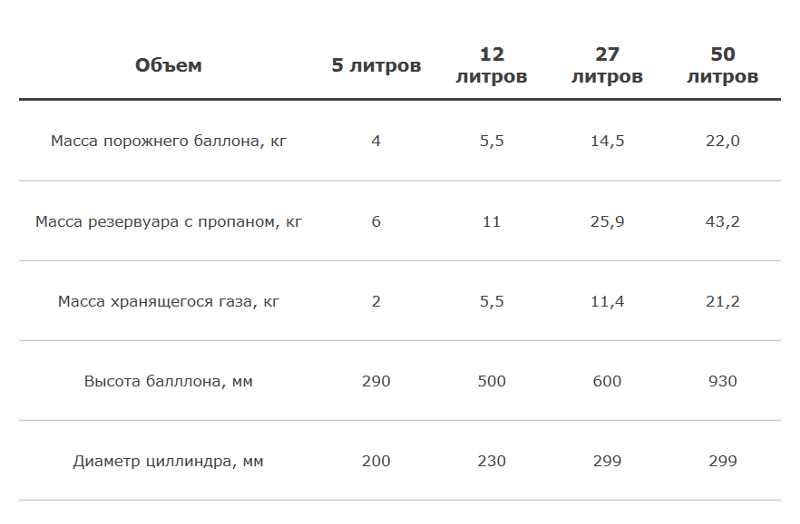 И в данной статье мы узнаем, во-первых, сколько газа влезает в 50-литровый баллон и, во-вторых, как быстро израсходуется этот объем.
И в данной статье мы узнаем, во-первых, сколько газа влезает в 50-литровый баллон и, во-вторых, как быстро израсходуется этот объем.
1
Как устроен газовый баллон – основные детали
Любой баллон собирается на основе сваренной из листового металла колбы, верх и низ которой оформлены с помощью штампованных чашеобразных крышек. Причем к нижней части приварен кольцеобразный фартук-подставка (опорный башмак), а в верхнюю часть колбы (кольцо горловины) вкручивают особый запорный узел – вентиль для газового баллона. Основной цилиндр (обечайку) и обе чаши изготавливают из стального листа толщиной не менее 2 мм. Причем чашеобразная форма дна и крышки объясняется физическими свойствами газа, который, находясь в замкнутой емкости, давит на каждый квадратный миллиметр ее внутренней площади с одинаковой силой. Поэтому сварочные швы, с помощью которых соединяют обечайку и чаши, должны соответствовать самым высоким критериям качества.
Вентиль баллона должен работать долго и выдерживать большое давление
К баллонному вентилю предъявляют особые требования. Он должен выдерживать огромное давление и работать очень долго. Поэтому нижняя сторона его корпуса оформлена, как конический резьбовой штуцер, а сверху находится маховик резьбового штока, запирающего седло. Причем запорный механизм некоторых вентилей способен выдержать давление до 190 атмосфер, сохраняя работоспособность. Боковой отвод в корпусе вентиля оптимизирован под подключение гайки армированного или сильфонного шланга. Однако в большинстве случаев на отвод накручивают редуктор, выравнивающий давление до приемлемого уровня. А в случае транспортировки отвод в газовом вентиле закрывается специальной резьбовой заглушкой.
Он должен выдерживать огромное давление и работать очень долго. Поэтому нижняя сторона его корпуса оформлена, как конический резьбовой штуцер, а сверху находится маховик резьбового штока, запирающего седло. Причем запорный механизм некоторых вентилей способен выдержать давление до 190 атмосфер, сохраняя работоспособность. Боковой отвод в корпусе вентиля оптимизирован под подключение гайки армированного или сильфонного шланга. Однако в большинстве случаев на отвод накручивают редуктор, выравнивающий давление до приемлемого уровня. А в случае транспортировки отвод в газовом вентиле закрывается специальной резьбовой заглушкой.
Кроме того, в некоторых баллонах вокруг вентиля обустраивается стальной воротник, защищающий запорный узел от механических повреждений. А в месте врезки вентиля монтируется особая шайба из мягкого металла (алюминия), на которую с помощью штамповки наносят даты последнего технического осмотра всей конструкции. В случае задержки технического осмотра заправлять баллон до предельного уровня давления категорически запрещается. Причем обнаружить факт отложенной проверки может любой пользователь. Для этого нужно прочитать символы на шайбе под кольцом горловины. Там, помимо времени последнего осмотра, есть и дата следующего. Если сегодняшнее число больше этой даты – баллон лучше не использовать.
Причем обнаружить факт отложенной проверки может любой пользователь. Для этого нужно прочитать символы на шайбе под кольцом горловины. Там, помимо времени последнего осмотра, есть и дата следующего. Если сегодняшнее число больше этой даты – баллон лучше не использовать.
2
Какую нагрузку выдержит корпус и вентиль
Стандартные емкости, изготовленные по нормам ГОСТ, могут выдержать рабочее давление в пределах от 9,8 до 19,6 МПа. Причем толщина листа, из которого готовят обечайку и чаши для баллона, выдерживающего давление до 190 атмосфер, доходит до 6 мм. Однако такой напор не выдержит ни один газопотребляющий прибор. Да и вес баллона из 6-миллиметровой стали будет очень значительным. Поэтому рабочее давление газа в баллоне емкостью 50 литров всегда равно 16 атмосферам, а точнее 1,6 МПа. Именно на такое давление рассчитаны бытовые редукторы, к которым подключают домашние котлы, колонки, плиты, духовые шкафы и конвекторы.
В баллоне на 50 литров рабочее давление равно 16-ти атмосферам
Впрочем, швы корпуса и запорный узел емкости ориентируют на более значительное давление в газовом баллоне – на 25 атмосфер (2,5 МПа). Правда, такое давление емкость испытывает только раз в пять лет – во время текущей проверки. И если швы баллона не смогут выдержать 25 атмосфер, то емкость отбраковывают и сдают в утиль. Вентиль может выдержать громадное давление – до 190 атмосфер. Именно такому напору может сопротивляться запорный узел, состоящий из штока и резьбовой пары. Хотя даже во время испытаний запор держит всего 25 атмосфер, а во время эксплуатации – не более 16 атмосфер. Именно на такое давление и нужно ориентироваться, рассчитывая, сколько газа помещается в стальном баллоне на 50 литров.
Правда, такое давление емкость испытывает только раз в пять лет – во время текущей проверки. И если швы баллона не смогут выдержать 25 атмосфер, то емкость отбраковывают и сдают в утиль. Вентиль может выдержать громадное давление – до 190 атмосфер. Именно такому напору может сопротивляться запорный узел, состоящий из штока и резьбовой пары. Хотя даже во время испытаний запор держит всего 25 атмосфер, а во время эксплуатации – не более 16 атмосфер. Именно на такое давление и нужно ориентироваться, рассчитывая, сколько газа помещается в стальном баллоне на 50 литров.
3
Сколько газа можно закачать в 50-литровую емкость
В пропановом баллоне на 50 литров помещается не более 42,5 литров сжиженного газа. Дело в том, что по нормам безопасности в емкость можно закачать не более 85 процентов от общего внутреннего объема (50х85%=42,5). Нарушать это правило нельзя ни заправщикам, ни владельцам емкостей! Кроме того, техника безопасности запрещает расходовать сжиженное топливо до конца. Поэтому остаточное давление в баллоне с пропаном не может быть менее 0,1 МПа, и фактически в распоряжении владельца емкости оказывается от 40 до 42 литров пропана. Ну а если перевести это в килограммы, то получается, что в баллон можно закачать 20-21 кг газа (1 л пропана = 0,5 кг).
Поэтому остаточное давление в баллоне с пропаном не может быть менее 0,1 МПа, и фактически в распоряжении владельца емкости оказывается от 40 до 42 литров пропана. Ну а если перевести это в килограммы, то получается, что в баллон можно закачать 20-21 кг газа (1 л пропана = 0,5 кг).
В единицах измерения энергии – ваттах – баллон пропана вмещает 966 МДж (1 кг пропана = 46 МДж) или 268 кВт*ч. Если используется пропанобутановая смесь с более высокой теплотворной способностью, то в один баллон войдет до 273 кВт*ч. Много это или мало – зависит от аппетитов потребителя. Если вы подключаете баллон к котлу, то одной емкости вам хватит на 2-3 дня (при сильных морозах и площади дома от 50 квадратов). Для стандартной газовой плитки мощностью 3 кВт такого источника энергии хватит почти на 90 часов непрерывной работы конфорок на полной мощности. Или на 60 приготовлений обедов (при условии, что на первое и второе блюдо уйдет 1,5 часа работы конфорки).
А вот для плиты и газовой колонки одного баллона будет мало. Ведь даже маломощный проточный водонагреватель потребляет не менее 15 кВт*ч, следовательно, запаса энергии в емкости хватит только на 17-18 часов непрерывной работы. А если учесть, что средняя продолжительность принятия душа равняется 15-20 минутам, то семья из четырех человек истощит 40-литровый запас пропана за месяц, при условии, что водные процедуры они будут принимать через день. И о горячей воде на кухне в этом случае можно и не мечтать.
Ведь даже маломощный проточный водонагреватель потребляет не менее 15 кВт*ч, следовательно, запаса энергии в емкости хватит только на 17-18 часов непрерывной работы. А если учесть, что средняя продолжительность принятия душа равняется 15-20 минутам, то семья из четырех человек истощит 40-литровый запас пропана за месяц, при условии, что водные процедуры они будут принимать через день. И о горячей воде на кухне в этом случае можно и не мечтать.
Автомобилисты могут подсчитать расход газа по простой формуле: 1 литр бензина = 1,2 литра сжиженного топлива.
В итоге большинство владельцев участков без центрального газопровода строят автономную систему газоснабжения на базе трех или даже четырех 50-литровых емкостей. И такой запас взрывоопасного и пожароопасного вещества требует совершенно особых условий хранения.
4
Как хранят и транспортируют газовые баллоны
При эксплуатации 50-литровых емкостей с чистым пропаном или пропанобутановой смесью принято придерживаться следующих правил:
- Баллоны стоят только в вертикальном положении, опираясь на башмак.
- Емкости со сжиженным газом стоят исключительно на улице, в железном ящике.
- Ящик для баллонов обязательно имеет перфорацию, обеспечивающую проветривание.
- Расстояние от емкости до двери и окна первого этажа не может быть менее 50 см.
- Расстояние от места хранения емкостей до колодца или выгребной ямы не должно быть менее 300 см.
- Баллоны следует поставить с северной стороны, поскольку максимальная температура эксплуатации не может быть выше 40-45 градусов по Цельсию. А на прямых солнечных лучах металл нагревается сильнее.
- Между баллоном и газопотребляющим прибором должен стоять редуктор, который выравнивает давление в газопроводе.
Причем этот свод правил касается и одного баллона, и целой группы емкостей, объединяемой с помощью газораспределительного коллектора.
|
Наши консультанты+375 17 317-90-09 (магазин)+375 29 170-6-100 (магазин) +375 17 317-90-01 (безналичный расчет) +375 17 317-90-99 (безналичный расчет) E-mail: Ltddash@tut.  by by |
Статьи > Сколько газа в бытовом баллоне? Пропан-бутановая смесь СПБТ (СУГ) Сжиженный углеводородный газ, реализуемый через розничные сети торговых предприятий и газовых АЗС, именуемый в просторечии «пропан», на самом деле является смесью пропана (не менее 40%) и бутана (все остальное). Верное наименование: «СПБТ». Компонентный состав сжиженного газа регламентируется техническими нормами ГОСТ 27578-87 «Газы углеводородные сжиженные для автомобильного транспорта. Технические условия» и ГОСТ 20448-90 «Газы углеводородные сжиженные топливные для коммунально-бытового потребления. Технические условия». Первый стандарт описывает состав сжиженного газа, используемом в автомобильном транспорте. Физико-химические свойства составляющих сжиженного газа.
Таблицы пересчета физических величин. 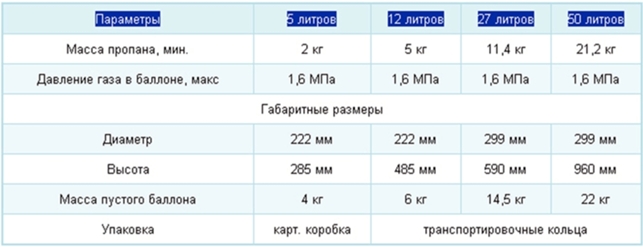 Энергия, тепло, работа Энергия, тепло, работа
СООТНОШЕНИЯ МЕЖДУ ЕДИНИЦАМИ ИЗМЕРЕНИЯ ЭНЕРГИИ:
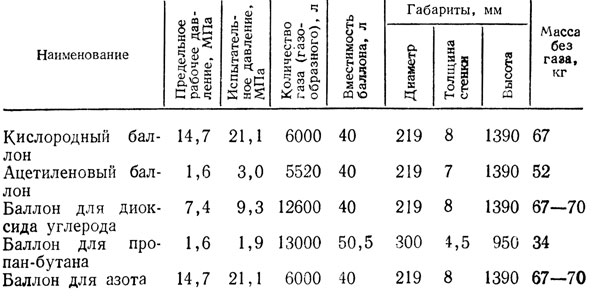
• Теплота сгорания это количеством выделившейся теплоты при полном сгорании массовой (для твердых и жидких веществ) или объёмной (для газообразных) единицы вещества.  Различают высшую (QBp) и низшую (QHp) теплоту сгорания. Низшая теплота сгорания соответствует тому количеству теплоты, которое выделяется при полном сгорании, без учёта теплоты конденсации водяного пара. Теплоту конденсации водяных паров также называют скрытой теплотой сгорания. Различают высшую (QBp) и низшую (QHp) теплоту сгорания. Низшая теплота сгорания соответствует тому количеству теплоты, которое выделяется при полном сгорании, без учёта теплоты конденсации водяного пара. Теплоту конденсации водяных паров также называют скрытой теплотой сгорания. Пропан-бутановая смесь обладает большим коэффициентом объемного расширения жидкой фазы, который для пропана составляет 0,003, а для бутана — 0,002 на 1°С повышения температуры газа. Для сравнения: коэффициент объемного расширения пропана в 15 раз, а бутана — в 10 раз, больше, чем у воды. Техническими нормативами и регламентами устанавливается, что cтепень заполнения резервуаров и баллонов зависит от марки газа и разности его температур во время заполнения и при последующем хранении. Для резервуаров, разность температур которых не превышает 40° С, степень заполнения принимается равной 85%, при большей разности температур степень заполнения должна снижаться. Баллоны заполняются по массе в соответствии с указаниями «Правил устройства и безопасной эксплуатации сосудов, работающих под давлением». 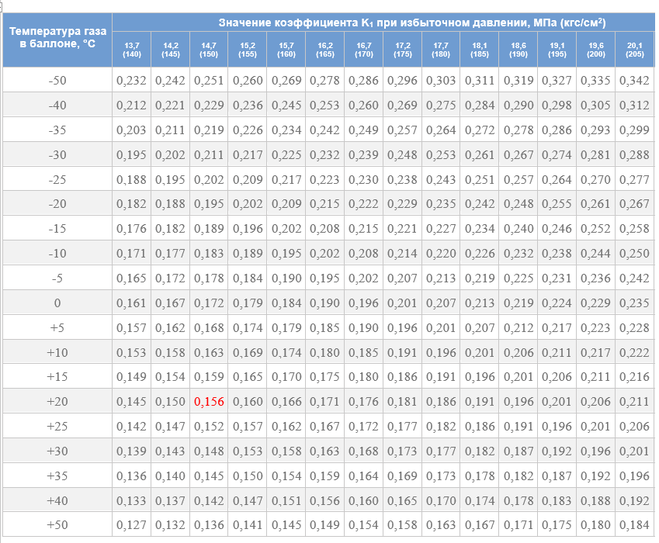 Максимальная допустимая температура нагрева баллона не должна превышать 45°С, при этом упругость паров бутана достигает 0,385 МПа, а пропана — 1,4–1,5 МПа. Баллоны должны предохраняться от нагрева солнечными лучами или другими источниками тепла. Максимальная допустимая температура нагрева баллона не должна превышать 45°С, при этом упругость паров бутана достигает 0,385 МПа, а пропана — 1,4–1,5 МПа. Баллоны должны предохраняться от нагрева солнечными лучами или другими источниками тепла.При испарении 1 л сжиженного газа образуется около 250 л газообразного. Таким образом, даже незначительная утечка СУГ может быть очень опасной, так как объем газа при испарении увеличивается в 250 раз. Плотность газовой фазы в 1,5–2,0 раза больше плотности воздуха. Этим объясняется тот факт, что при утечках газ с трудом рассеивается в воздухе, особенно в закрытом помещении. Пары его могут накапливаться в естественных и искусственных углублениях, образуя взрывоопасную смесь. Сегодня ОАО «Новогрудский завод газовой аппаратуры» производит стальные сварные бытовые газовые баллоны объемом 5, 12, 27 и 50 литров. Данные баллоны предназначены для транспортирования и хранения сжиженных углеводородных газов (пропана, бутана и их смесей). Основные параметры этих баллонов приведены ниже в таблице:
Для выполнения расчет емкости газа в бытовом баллоне можно принимать следующие значения: Баллон бытовой заполняется газом примерно на 85% его номинального объема.  Поскольку массу газа в баллоне определяет плотность закаченной смеси, ее значения находятся в очень широком диапазоне, для смеси 40% пропан, остальное бутан можно принять значение около 550 кг/куб. м.
 Поэтому для дальнейших расчетов имеет смысл использовать именно минимальную массу газа в заправленном баллоне, указанную заводом-изготовителем. Поэтому для дальнейших расчетов имеет смысл использовать именно минимальную массу газа в заправленном баллоне, указанную заводом-изготовителем.Расчет времени работы конкретного газового оборудования выполним на примере газового конвектора Betta 2, мощностью 2 кВт. Его паспортное потребление составляет 0,18 кг/час, тогда при массе газа в баллоне 2 кг мы получаем примерно 2/0,18 = 11,11 часов. Результаты расчета времени работы различного газового оборудования, выполненные первым способом, сведем в следующую таблицу:
На ��сякий случай еще раз напоминаем, что приведенные в данном материале значения и расчеты носят информативный характер и выполнены по усредненным значениям для того, что бы потребитель имел возможность изначально при покупке различных газовых приборов и оборудования сформировать примерное представление о том, сколько минимально сможет работать данное оборудование от стандартного баллона со сжиженным газом.  И в каждом конкретном случае расчетное значение может значительно отличаться от приводимого в рамках настоящей статьи, поскольку очень сильно зависит от состава смеси в баллоне, ее массы, теплоемкости, и мощности, которую мы хотим получить. Так, в таблице расчета времени, мы брали максимальное потребление газа, для указанного оборудования, однако, на максимальной мощности оно используется достаточно редко, а практические средние значения расходов должны быть меньше, указанных нами. И в каждом конкретном случае расчетное значение может значительно отличаться от приводимого в рамках настоящей статьи, поскольку очень сильно зависит от состава смеси в баллоне, ее массы, теплоемкости, и мощности, которую мы хотим получить. Так, в таблице расчета времени, мы брали максимальное потребление газа, для указанного оборудования, однако, на максимальной мощности оно используется достаточно редко, а практические средние значения расходов должны быть меньше, указанных нами. |
|||||
Расход пропанового баллона в бытовых целях
При покупке бытовых пропановых баллонов часто возникает вопрос: какой будет расход пропана?
При ответе на данный вопрос необходимо знать объем газа в баллоне.
Сколько газа в баллонах?
Баллон объемом 50 литров. В баллоне находится 21,5 кг*.
Баллон объемом 27 литров. В баллоне находится 11,4 кг*.
Баллон объемом 12 литров. В баллоне находится 5,3 кг*.
Баллон объемом 5 литров. В баллоне находится 2,3 кг*.
*Данные взяты с клейма на баллонах.
Расход газа в газовых плитах
Чтобы определить сколько газа потребляет ваша газовая плита, необходимо обратиться к технической документации плиты.
Например, у газовой плиты гефест ПГ 900 с 4 конфорками максимальный расход газа 486 г/ч (или 0,486 кг/час). Следовательно, если включены все 4 конфорки на максимум, то баллона 50 литров хватит на 44 часа (количество газа в баллоне 21,5 кг делим на расход 0,486 кг/час). Конечно, если включено меньше конфорок, то и расход газа уменьшится. Следовательно, баллона хватит на больший срок.
Аналогично рассчитывается расход газа, если в технической документации он обозначается в литрах или кубических метрах.
Расход газа в котлах для отопления дома.
Расход газа котлом рассчитывается аналогично расходу газа в газовых плитах.
Из нюансов следует отметить, что расход сильно зависит от степени утепления вашего дома, а также от температуры окружающей среды. Чем меньше утеплен дом и чем ниже температура на улице, тем больше необходимо котлу затратить энергии (сжечь газ), чтобы нагреть помещения до необходимой температуры.
Также следует учитывать, что котлы в среднем работают 10-12 часов в день. Если котел также необходим для подогрева горячей воды, то в среднем расход увеличивается на 15-20% и более.
Например, у напольного газового котла Buderus Logano G124 WS 20 максимальный расход газа — 1,69 кг/час. Рассчитаем, на сколько дней хватит баллона объемом 50 литров. Массу газа 21,5 кг делим на расход 1,69 кг/час и получаем 12,7 часов. Учитывая неполный рабочий день котла, баллона для обогрева на максимальной мощности хватит на 1 день. В среднем, баллона хватает на 2-3 дня.
Для того, чтобы не проснуться в остывающем доме, можно приобрести газовую рампу и подсоединить несколько пропановых баллонов: 2 основных и 2 резервных, например, или можно приобрести баллонную установку РП-2.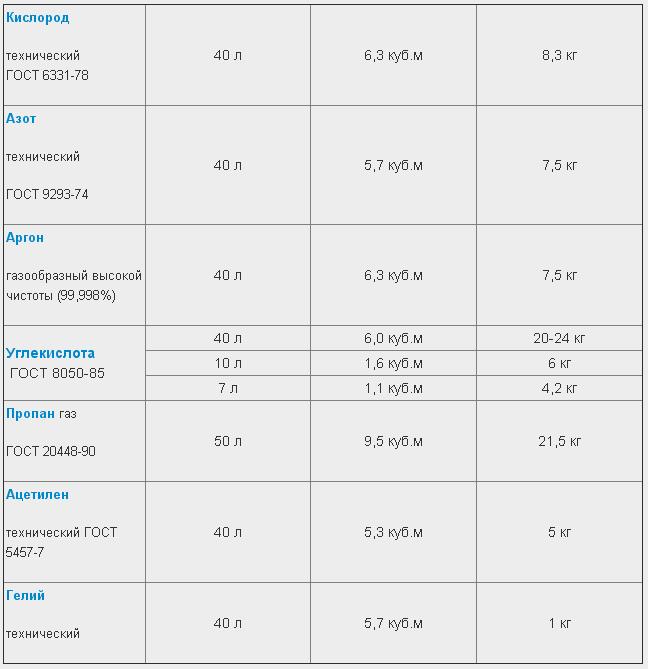
Расход газа при устройстве наплавляемой кровли.
Расход газа зависит от размера наконечника кровельной горелки. Например, расход газа горелки проп.+воздух ГВ «Донмет» 231 в среднем — 2 кг/час. Следовательно, баллона 50 литров хватит на 10,8 часов (21,5/2=10,8).
В среднем расход газа на 1 м² наплавляемой кровли равен 0,2 кг. Следовательно, баллона объемом 50 литров хватит на 100 м². Не забудьте, что зимой расход газа возрастает в 1,5-2 раза.
P.S. Чтобы получить на выходе необходимое давление газа, не забудьте купить редуктор для баллона. Для котла и газовых плит подойдет редуктор типа «Лягушка» , для горелок и резаков нужен больший расход, следовательно, подойдёт редуктор БПО-5-2.
Universal Industrial Gases, Inc. … Конверсия кислородных единиц (газ, жидкость)
Universal Industrial Gases, Inc. … Конверсия кислородных единиц (газ, жидкость)Данные преобразования единиц для кислорода
| Масса | Газ | Жидкость | ||||
| фунтов (фунты) | килограмм (кг) | кубических футов (scf) | куб. м м (Нм 3 ) | галлонов (галлон) | литров (л) | |
| 1 фунт | 1.0 | 0,4536 | 12.076 | 0,3174 | 0,105 | 0,3977 |
| 1 килограмм | 2.205 | 1.0 | 26,62 | 0,6998 | 0,2316 | 0. 8767 8767 |
| 1 ст. Газ | 0,08281 | 0,03756 | 1.0 | 0,02628 | 0,008691 | 0,0329 |
| 1 Нм 3 газ | 3,151 | 1.4291 | 38.04 | 1.0 | 0,3310 | 1,2528 |
| 1 галлон жидкость | 9,527 | 4,322 | 115,1 | 3,025 | 1. 0 0 | 3,785 |
| 1 литр жидкость | 2.517 | 1,1417 | 30,38 | 0,7983 | 0,2642 | 1.0 |
| 1 короткая тонна | 2000 | 907,2 | 24160 | 635 | 209,9 | 794.5 |
scf (стандартный кубический фут) измеренный газ
при 1 атмосфере и 70F. Нм3 (нормальный кубический метр) газа измеряется при 1 атмосфере и 0C. Жидкость измерена при 1 атмосфере и температуре кипения. |
Universal Industrial Gases, Inc.
3001 Emrick Blvd., Suite 320
Bethlehem, Пенсильвания 18020 США
Телефон (610) 559-7967 Факс (610) 515-0945
Все материалы, содержащиеся в данном документе, принадлежат UIG 2003/2016.
Ваш браузер не поддерживает скрипт| Размер цилиндра | 47AL | 30AL | 16AL | 7AL | 3AL | 1AL |
| Спецификация DOT | 3AL | 3AL | 3AL | 3AL | 3AL | 3AL |
Рабочее давление (фунт / кв. Дюйм) Дюйм) | 2216 | 2015 | 2216 | 2216 | 2015 | 2216 |
| Приблизительная вместимость (кубические футы) | 244 | 141 | 83 | 31 | 8 | 5 |
| Приблизительная емкость (литры) | 6909 | 3993 | 2350 | 878 | 227 | 142 |
| Внешний диаметр (дюймы) | 9.8 | 8 | 7,25 | 6,9 | 4,4 | 3,2 |
| Высота (дюймы) | 51,9 | 47,9 | 33 | 15,6 | 10,5 | 11,7 |
| Масса тары (фунт.) | 90 | 48 | 30 | 15 | 3,5 | 2,3 |
| Внутренний водный объем (кубические дюймы) | 2831 | 1800 | 958 | 360 | 103 | 61 |
| Внутренний объем воды (литры) | 46. 4 4 | 29,3 | 15,7 | 5,9 | 1,7 | 1 |
Технические характеристики баллона / Хранение и использование — Scott Medical Products
Алюминиевые многоразовые лекционные бутылки высокого давления
* Многоразовые баллоны являются собственностью Scott Medical Products. Клиенты не могут загружать или заправлять баллоны, поставляемые компанией Scott Medical Products, поскольку это запрещено федеральными правилами.
Возвратные цилиндры высокого давления
* Многоразовые баллоны являются собственностью Scott Medical Products. Клиенты не могут загружать или заправлять баллоны, поставляемые компанией Scott Medical Products, поскольку это запрещено федеральными правилами.
Возвратные цилиндры низкого давления
Одноразовые баллоны высокого давления
Одноразовые баллоны низкого давления
Выходы и соединения клапана цилиндра CGA
Соединение 110
5/16 ″ — 32 RH INT. с прокладкой
с прокладкой
Соединение 160
1/8 ″ — 27 NGT RH INT.
Соединение 165
0,4375 ″ — 20 UNF 2A RH EXT.
Соединение 170
5/16 ″ — 32 RH INT., С прокладкой
Соединение 180
0,625 ″ — 18 UNF 2A RH EXT. с прокладкой (можно использовать шайбу или уплотнительное кольцо)
Соединение 296
0,803 ″ — 14 RH INT.
Соединение 320
0.825 ″ — 14 ПРАВ. с прокладкой
Соединение 326
0,825 ″ — 14 ПРАВ.
Соединение 330
0,825 ″ — 14 Л / С ВНЕШН. с прокладкой
Соединение 510
0,885 ″ — 14 LH INT.
Соединение 350
0,903 ″ — 14 RH EXT.
Соединение 580
0,965 ″ — 14 RH INT.
Соединение 590
0.965 ″ — 14 LH INT.
Соединение 600
1. 000 ″ — 20 UNEF RH EXT. с прокладкой
000 ″ — 20 UNEF RH EXT. с прокладкой
Соединение 660
1.030 ″ — 14 ПРАВ. с прокладкой
Клапаны для медицинских газовых баллонов для соединений с индексированными штифтами
Соединение 870
Соединение 880
Соединение 890
Соединение 910
Соединение 930
Соединение 940
Соединение 950
Соединение 960
Соединение 965
Соединение 973
Соединение 977
Выходы и соединения клапанов цилиндра
Скотт поставляет специальные газы в цилиндры с клапанами, имеющими стандартные выходные соединения CGA, DIN и BS.В некоторых случаях могут использоваться альтернативные соединения CGA, которые по запросу клиента будут предоставлены вместо стандартов, указанных ниже.
Баллоны и инертирование азотом — конденсаторы и факелы PURGIT VOC
Работа с баллонами высокого давления и их использование должны выполняться только обученным персоналом.
Обратите внимание: баллоны могут содержать накопленную энергию в виде давления, которое может быть очень опасным при неправильном использовании. Например, удаление клапана баллона с давлением в баллоне может быть очень опасным.Любое повреждение баллона под давлением может привести к травме.
Небольшие потребности в газе лучше всего удовлетворять с помощью баллонов. Типичный баллон высотой около 5 футов может вместить около 230 кубических футов газообразного азота, если он заполнен до максимального рабочего давления, которое может находиться в диапазоне 2200 фунтов на квадратный дюйм, то есть, если он заполнен. На баллоне будет указано максимально допустимое давление сбоку рядом с клапаном. Давление — это главный индикатор, определяющий, заполнен ли баллон. Температура является фактором, но не таким важным, пока цилиндр не нагревается.Примечание. Существуют баллоны, рассчитанные на гораздо более высокое давление, но они не являются типичными.
Баллоны высокого давления бывают разных размеров, некоторые из которых достаточно малы, чтобы их можно было носить под рукой, а другие устанавливаются на 18-колесные грузовики. Внутренний объем цилиндра и давление газа (и, в некоторой степени, температура) — вот вещи, которые важны для определения количества кубических футов сжатого газа. У баллонов очень интересное качество — они будут удерживать давление и объем практически вечно, независимо от времени.Единственное сокращение — использование газа или утечка. Громкость — самое большое ограничение.
Внутренний объем цилиндра и давление газа (и, в некоторой степени, температура) — вот вещи, которые важны для определения количества кубических футов сжатого газа. У баллонов очень интересное качество — они будут удерживать давление и объем практически вечно, независимо от времени.Единственное сокращение — использование газа или утечка. Громкость — самое большое ограничение.
Для больших требований цилиндры собираются в стойки.
Цилиндр высокого давления 230 scf «Стеллажи» представляют собой стальные рамы с 6 или 12 цилиндрами, скрепленными вместе, подающимися в один коллектор. Они часто используют газовые баллоны на 230 куб. Футов. Таким образом, 12 цилиндров x 230 куб. Футов = 2760 куб. Футов или 78 м3. Сильным преимуществом баллонов является то, что азот остается в них годами.И он всегда будет готов к работе в одно мгновение (если клапаны сработают). Однако владелец баллона обычно взимает плату за простой — арендную плату за баллоны, и со временем это может быть дорого. Эту проблему можно решить, купив цилиндры. Баллоны следует проверять каждые 5 лет, и на них проставляется дата последнего испытания. Заправочные станции могут не заправляться, если период тестирования превышает номинальную дату тестирования.
Эту проблему можно решить, купив цилиндры. Баллоны следует проверять каждые 5 лет, и на них проставляется дата последнего испытания. Заправочные станции могут не заправляться, если период тестирования превышает номинальную дату тестирования.
Другой вариант для больших партий — Дьюар.Контейнеры Дьюара могут содержать жидкий азот, аргон, кислород, CO2 и т. Д. 180-литровый сосуд Дьюара может вместить 140 кубических метров при 10 бар. Недостаток жидкого азота в том, что это скоропортящийся товар. Он испарится и ускользнет из сосудов Дьюара за короткий период времени. Все это может исчезнуть через 3 недели, если дьюар окажется на палящем солнце. Портативные сосуды Дьюара бывают разных размеров — от маленького 1 литра, который дерматолог может использовать, до 265 литров. Обычно, когда сосуд Дьюара очень большой, его называют просто резервуаром с жидким азотом или резервуаром с жидким азотом, и он может вмещать тысячи галлонов или литров.
Автоцистерны с жидким азотом могут вмещать около 500 000 кубических футов (около 5 000 галлонов), и азот всегда улетучивается из-за кипения, приблизительно от 0,2% до 5% в день в зависимости от того, насколько хороша изоляция. Обычно у них есть резервуары с относительно низким давлением, нормальным является 25 фунтов на квадратный дюйм. Обычно у них есть перекачивающий насос для перекачки азота в стационарные резервуары.
Обычно у них есть резервуары с относительно низким давлением, нормальным является 25 фунтов на квадратный дюйм. Обычно у них есть перекачивающий насос для перекачки азота в стационарные резервуары.
Цистерны с жидким азотом могут быть стационарными на бетонных площадках (это большие резервуары с тысячами галлонов), и они часто имеют меньший коэффициент потерь, чем автоцистерны, но они всегда выпускают испарительный газ на уровне около.От 2% до 5% в день. Все зависит от вакуума в вакуумной рубашке. У них должен быть очень хороший вакуум, чтобы противостоять высокой температуре и свести к минимуму выкипание. В этих резервуарах давление может составлять от 30 до 225 фунтов на квадратный дюйм.
Резервуар PURGIT ISO Резервуары ISO могут иметь очень низкий уровень утечки. 0,2% нет ничего необычного. Резервуары ISO используются для специализированных перевозок азота, аргона, кислорода и других специализированных криогенных и промышленных химикатов. Емкость должна соответствовать содержимому. То есть цистерны сертифицированы для перевозки конкретных грузов.Баллон с азотом будет иметь фитинги, которые будут подключаться только к другим резервуарам с азотом.
То есть цистерны сертифицированы для перевозки конкретных грузов.Баллон с азотом будет иметь фитинги, которые будут подключаться только к другим резервуарам с азотом.
Цистерны с жидким азотом, которыми я владею, могли быть заполнены аргоном, кислородом или гелием, если они были очищены, подготовлены к новому грузу с помощью новых фитингов для шлангов и новых табличек.
Углекислый газ поставляется в резервуарах в виде жидкости, но технически СО2 не является криогенной жидкостью, потому что он недостаточно холодный.
Важное примечание: Для успешного вывода газа из баллона высокого давления необходим специальный редукционный регулятор давления.Большинство клапанов баллона предназначены для газового баллона. Кислород берет один поток, топливный газ — другой, азот — другой и так далее. Регулятор должен иметь правильную резьбу, подходящую для цилиндра. Кислородные шланги, регуляторы, клапаны никогда не должны использоваться для других газов. Может возникнуть самопроизвольный пожар, потому что почти все является топливом для кислорода.
Различные рисунки резьбы на клапанах имеют номера для идентификации. Например, соединение № 510 предназначено для топливного газа, такого как пропан или ацетилен.Его также называют POL, который когда-то, я полагаю, обозначал Perst-O-Lite, который был одним из первых производителей. Резьбовое соединение № 240 и № 660 — аммиак, № 320 — для CO2, № 580 — для азота, криптона или гелия, № 540 — кислород, и этот список можно продолжить….
Кислород опасен, потому что почти все является топливом для чистого кислорода. Если для нефтепродукта использовался шланг или труба, и при подключении чистого кислорода присутствуют даже следы углеводорода, он может самовоспламеняться, вызывая взрыв или пожар.
Когда большие производственные цеха используют резаки для резки толстой стали, в резаках используется смесь кислорода и ацетилена. Когда резка началась, иногда можно уменьшить или перекрыть поток ацетилена и использовать только кислород. Смешивание кислорода с топливным газом чрезвычайно опасно и почти наверняка приведет к взрыву или пожару из-за быстрого окисления, вызванного смесью топливо-O2. Кислородное оборудование нельзя использовать в топливном газе, а затем снова в кислороде без очистки.
Кислородное оборудование нельзя использовать в топливном газе, а затем снова в кислороде без очистки.
Альтернативой баллону или жидкому азоту является генератор азота. Они отделяют газообразный азот и кислород от воздуха. Их довольно дорого покупать, и для них требуется воздушный компрессор, но они производят азот, когда он вам нужен, и при их отключении нет никаких затрат или потерь. Они особенно полезны в отдаленных районах. Побочным продуктом производства газообразного азота является газообразный кислород, и генераторы азота можно переконфигурировать для получения газообразного кислорода для использования в больницах и для промышленного производства O2.
Инертизация бака Уловка инертизации бака заключается в правильном размещении подающего шланга по отношению к месту выхода. Газ должен подаваться с одного конца баллона, а выходить с другого. Обычно это не так просто, потому что очень немногие резервуары имеют соединения на каждом конце. Для больших резервуаров, даже с подходящими местами подключения, может потребоваться 3 или более объемов газообразного азота для снижения содержания кислорода до менее 8%.
Для больших резервуаров, даже с подходящими местами подключения, может потребоваться 3 или более объемов газообразного азота для снижения содержания кислорода до менее 8%.
CO2 намного лучше подходит для инертизации резервуаров, потому что молекула CO2 тяжелая и недорогая по сравнению с другими газами.Он может вытеснять более легкие газы, а не разбавлять их. Инертизация резервуаров азотом может быть опасна для операторов или инспекторов из-за возможности удушья. Маска с фильтром НЕ ХОРОШАЕТ, если пар имеет пониженное содержание кислорода. Если кислорода недостаточно, маска с фильтром не подходит. В случае низкого уровня кислорода вы должны надеть маску из комплекта поставки. Запрещается работать в резервуарах с содержанием кислорода менее 19,5% без подачи воздуха. Подача воздуха может происходить из баллонов для акваланга или из воздушного шланга, подводимого снаружи, но это очень опасная работа, и ее должен выполнять только обученный персонал.
Некоторые правила работы с инертными газами:
НИКОГДА не входите в баллон, если он не прошел проверку на содержание кислорода и его содержание не превышает 19,5%. Самые опасные стальные резервуары — сухие и ржавые. Ржавчина может поглощать свободный кислород, создавая атмосферу с дефицитом кислорода. Счетчики кислорода можно купить или арендовать в магазинах средств безопасности.
Самые опасные стальные резервуары — сухие и ржавые. Ржавчина может поглощать свободный кислород, создавая атмосферу с дефицитом кислорода. Счетчики кислорода можно купить или арендовать в магазинах средств безопасности.
НЕ ИСПОЛЬЗУЙТЕ баллонов с низким содержанием кислорода. Маски с угольным фильтром никуда не годятся. Убедитесь, что кислорода достаточно для дыхания.
ЕЖЕДНЕВНО проветривайте каждый резервуар большим количеством наружного воздуха, используя принудительный вентилятор перед входом. Другие химические вещества могут представлять такую же опасность, как и недостаток кислорода.
НИКОГДА не заменяйте кислородные регуляторы или шланги и т. Д. С оборудованием для топливного газа. Всегда читайте и понимайте паспорта безопасности материала для газа.
КАЖДЫЙ раз обращайтесь к опытному специалисту для работы с баллонами высокого давления.
Большинство цистерн, даже те, у которых есть люки или люки, будут «замкнутыми пространствами».Есть много правил, регулирующих вход в закрытые помещения. Если вы планируете войти в замкнутое пространство, пожалуйста, прочтите и поймите опасности и соблюдайте правила.
Если вы планируете войти в замкнутое пространство, пожалуйста, прочтите и поймите опасности и соблюдайте правила.
PURGIT — подрядчик по дегазации резервуаров, использующий конденсаторы, охлаждаемые жидким азотом. У нас есть опытные резервуары для дегазации и инертизации с азотом, углекислым газом и др.
Кислородный баллон на 10 кубических метров
AirLocus обеспечивает отличные рабочие характеристики кислородных баллонов объемом 10 кубических метров для промышленного и медицинского применения.Наши кислородные баллоны объемом 10 кубических метров спроектированы, изготовлены и проверены в соответствии с международными стандартами. Кислородные баллоны объемом 10 кубических метров изготовлены из высокопрочной стали или алюминия марки 6061 и имеют характеристики одинаковой высоты, четкой гравировки, длительного срока службы и т. Д. По любым вопросам, связанным с кислородным баллоном на 10 кубических метров, обращайтесь к нам.
50 л 200 бар кислородный баллон | |||
Тип | ISO232-50-200A | Наружный диаметр | 232 мм |
Объем воды | 50 л | Высота без клапана | 1425 мм |
Рабочее давление | 200 бар | Мин. | 5,2 мм |
Испытательное давление | 300 бар | Масса без клапана | 50,6 кг |
Производственный стандарт | ISO9809-1 | Материал | 34CrMo4 |
50 л 200 бар кислородный баллон | |||
Тип | ISO232-50-200B | Наружный диаметр | 232 мм |
Объем воды | 50 л | Высота без клапана | 1450 мм |
Рабочее давление | 200 бар | Мин.толщина стенки | 5,8 мм |
Испытательное давление | 300 бар | Масса без клапана | 56,3 кг |
Производственный стандарт | ISO9809-1 | Материал | 34CrMo4 |
50 л 200 бар кислородный баллон | |||
Тип | ISO229-50-200A | Наружный диаметр | 229 мм |
Объем воды | 50 л | Высота без клапана | 1505 мм |
Рабочее давление | 200 бар | Мин. | 6,2 мм |
Испытательное давление | 300 бар | Масса без клапана | 64.0 кг |
Производственный стандарт | ISO9809-1 | Материал | 30CrMo трубка |
50 л 200 бар кислородный баллон | |||
Тип | ISO229-50-200B | Наружный диаметр | 229 мм |
Объем воды | 50 л | Высота без клапана | 1510 мм |
Закон об идеальном газе | Физика
Цели обучения
К концу этого раздела вы сможете:
- Сформулируйте закон идеального газа, используя молекулы и моль.

- Используйте закон идеального газа для расчета изменения давления, температуры, объема или количества молекул или молей в заданном объеме.
- Используйте число Авогадро для преобразования числа молекул в число молей.
Рис. 1. Воздух внутри этого воздушного шара, летящего над Путраджайей, Малайзия, горячее, чем окружающий воздух. В результате воздушный шар испытывает подъемную силу, толкающую его вверх. (Источник: Кевин По, Flickr)
В этом разделе мы продолжаем исследовать термическое поведение газов.В частности, мы исследуем характеристики атомов и молекул, из которых состоят газы. (Большинство газов, например азот, N 2 , и кислород, O 2 , состоят из двух или более атомов. Мы в первую очередь будем использовать термин «молекула» при обсуждении газа, поскольку этот термин также может применяться к одноатомные газы, такие как гелий.)
Газы легко сжимаются. Мы можем увидеть доказательства этого в Таблице 1 в Термическом расширении твердых тел и жидкостей, где вы заметите, что газы имеют наибольших коэффициентов объемного расширения. Большие коэффициенты означают, что газы расширяются и сжимаются очень быстро при изменении температуры. Кроме того, вы заметите, что большинство газов расширяются с такой же скоростью или имеют такое же значение β . Это поднимает вопрос, почему все газы должны действовать почти одинаково, когда жидкости и твердые тела имеют сильно различающиеся скорости расширения.
Большие коэффициенты означают, что газы расширяются и сжимаются очень быстро при изменении температуры. Кроме того, вы заметите, что большинство газов расширяются с такой же скоростью или имеют такое же значение β . Это поднимает вопрос, почему все газы должны действовать почти одинаково, когда жидкости и твердые тела имеют сильно различающиеся скорости расширения.
Ответ заключается в большом разделении атомов и молекул в газах по сравнению с их размерами, как показано на рисунке 2. Поскольку атомы и молекулы имеют большие расстояния, силы между ними можно игнорировать, кроме случаев, когда они сталкиваются друг с другом во время столкновений. .Движение атомов и молекул (при температурах, значительно превышающих температуру кипения) происходит быстро, так что газ занимает весь доступный объем, и газы расширяются быстро. Напротив, в жидкостях и твердых телах атомы и молекулы расположены ближе друг к другу и весьма чувствительны к силам между ними.
Рис. 2. Как показано, атомы и молекулы в газе обычно широко разделены. Поскольку силы между ними на этих расстояниях довольно слабы, свойства газа больше зависят от числа атомов в единице объема и температуры, чем от типа атома.
2. Как показано, атомы и молекулы в газе обычно широко разделены. Поскольку силы между ними на этих расстояниях довольно слабы, свойства газа больше зависят от числа атомов в единице объема и температуры, чем от типа атома.
Чтобы получить некоторое представление о том, как давление, температура и объем газа связаны друг с другом, рассмотрим, что происходит, когда вы закачиваете воздух в изначально спущенную шину. Объем шины сначала увеличивается прямо пропорционально количеству впрыскиваемого воздуха без значительного увеличения давления в шине. Когда шина расширилась почти до своего полного размера, стенки ограничивают объемное расширение. Если продолжать закачивать в него воздух, давление возрастает. Давление будет еще больше увеличиваться, когда автомобиль движется, а шины двигаются.Большинство производителей указывают оптимальное давление в шинах для холодных шин. (См. Рисунок 3.)
Рис. 3. (a) Когда воздух нагнетается в спущенную шину, его объем сначала увеличивается без значительного увеличения давления. (b) Когда шина заполнена до определенной точки, стенки шины сопротивляются дальнейшему расширению, и давление увеличивается с увеличением количества воздуха. (c) Когда шина накачана, ее давление увеличивается с температурой.
(b) Когда шина заполнена до определенной точки, стенки шины сопротивляются дальнейшему расширению, и давление увеличивается с увеличением количества воздуха. (c) Когда шина накачана, ее давление увеличивается с температурой.
При комнатной температуре столкновениями между атомами и молекулами можно пренебречь.В этом случае газ называется идеальным газом, и в этом случае связь между давлением, объемом и температурой задается уравнением состояния, называемым законом идеального газа.
Закон об идеальном газе
Закон идеального газа гласит, что PV = NkT , где P — абсолютное давление газа, V — объем, который он занимает, N — количество атомов и молекул в газа, а T — его абсолютная температура.Константа k называется постоянной Больцмана в честь австрийского физика Людвига Больцмана (1844–1906) и имеет значение k = 1,38 × 10 −23 Дж / К.
Закон идеального газа может быть выведен из основных принципов, но первоначально он был выведен из экспериментальных измерений закона Чарльза (объем, занимаемый газом, пропорционален температуре при фиксированном давлении) и из закона Бойля (для фиксированной температуры, произведение PV является константой). В модели идеального газа объем, занимаемый его атомами и молекулами, составляет ничтожную долю от V . Закон идеального газа описывает поведение реальных газов в большинстве условий. (Обратите внимание, например, что N — это общее количество атомов и молекул, независимо от типа газа.)
В модели идеального газа объем, занимаемый его атомами и молекулами, составляет ничтожную долю от V . Закон идеального газа описывает поведение реальных газов в большинстве условий. (Обратите внимание, например, что N — это общее количество атомов и молекул, независимо от типа газа.)
Давайте посмотрим, как закон идеального газа согласуется с поведением заполнения шины, когда она накачивается медленно и температура постоянна. Сначала давление P по существу равно атмосферному давлению, а объем V увеличивается прямо пропорционально количеству атомов и молекул N , введенных в шину.Когда объем шины постоянен, уравнение PV = NkT предсказывает, что давление должно увеличиваться пропорционально числу N атомов и молекул .
Пример 1. Расчет изменений давления из-за изменений температуры: давление в шинах
Предположим, ваша велосипедная шина полностью накачана, с абсолютным давлением 7,00 × 10 5 Па (манометрическое давление чуть менее 90,0 фунтов / дюйм 2 ) при температуре 18,0 ° C. Какое давление будет после того, как его температура повысится до 35,0ºC? Предположим, что нет заметных утечек или изменений объема.
Какое давление будет после того, как его температура повысится до 35,0ºC? Предположим, что нет заметных утечек или изменений объема.
Стратегия
Давление в шине меняется только из-за изменения температуры. Сначала нам нужно определить, что мы знаем и что мы хотим знать, а затем определить уравнение, которое нужно решить для неизвестного.
Известно начальное давление P 0 = 7,00 × 10 5 Па, начальная температура T 0 = 18.0ºC, а конечная температура T f = 35,0ºC. Мы должны найти конечное давление P f . Как мы можем использовать уравнение PV = NkT ? На первый взгляд может показаться, что информации недостаточно, потому что объем V и количество атомов N не указаны. Что мы можем сделать, так это использовать уравнение дважды: P 0 V 0 = NkT 0 и P f V f = NkT f . Если мы разделим P f V f на P 0 V 0 , мы сможем получить уравнение, которое позволяет нам решить для P f .
Если мы разделим P f V f на P 0 V 0 , мы сможем получить уравнение, которое позволяет нам решить для P f .
[латекс] \ displaystyle \ frac {P _ {\ text {f}} V _ {\ text {f}}} {P_0V_0} = \ frac {N _ {\ text {f}} kT _ {\ text {f}}} {N_0kT_0} \\ [/ latex]
Поскольку громкость постоянна, V f и V 0 одинаковы, и они компенсируются. То же самое верно для N f и N 0 и k , что является константой.Следовательно,
[латекс] \ displaystyle \ frac {P _ {\ text {f}}} {P_0} = \ frac {T _ {\ text {f}}} {T_0} \\ [/ latex]
Затем мы можем изменить это, чтобы решить для P f : [latex] P _ {\ text {f}} = P_0 \ frac {T _ {\ text {f}}} {T_0} \\ [/ latex] , Где температура должна быть в единицах кельвина, потому что T 0 и T f являются абсолютными температурами.
Решение
Преобразование температуры из Цельсия в Кельвин:
T 0 = (18.5 \ text {Pa} \\ [/ latex]
Обсуждение
Конечная температура примерно на 6% выше исходной температуры, поэтому конечное давление также примерно на 6% больше. Обратите внимание, что абсолютное давление и абсолютное температура должны использоваться в законе идеального газа.
Подключение: домашний эксперимент — охлаждение воздушного шара
Надуть баллон при комнатной температуре. Оставьте надутый баллон в холодильнике на ночь.Что происходит с воздушным шаром и почему?
Пример 2. Расчет количества молекул в кубическом метре газа
Сколько молекул содержится в типичном объекте, таком как газ в шине или вода в напитке? Мы можем использовать закон идеального газа, чтобы дать нам представление о типичных размерах N .
Рассчитайте количество молекул в кубическом метре газа при стандартной температуре и давлении (STP), которые определены равными 0ºC и атмосферному давлению.
Стратегия
Поскольку давление, объем и температура все указаны, мы можем использовать закон идеального газа PV = NkT , чтобы найти N .{25} \ text {молекулы} \\ [/ latex]
Обсуждение
Это число, несомненно, велико, учитывая, что газ — это в основном пустое пространство. N огромен даже в небольших объемах. Например, 1 см 3 газа в STP содержит 2,68 × 10 19 молекул. Еще раз отметим, что N одинаков для всех типов или смесей газов.
Родинки и число Авогадро
Иногда при измерении количества вещества удобно работать с единицей, отличной от молекул. моль. (сокращенно моль) определяется как количество вещества, которое содержит столько атомов или молекул, сколько атомов имеется ровно в 12 граммах (0,012 кг) углерода-12. Фактическое количество атомов или молекул в одном моле называется числом Авогадро ( N A ) по признанию итальянского ученого Амедео Авогадро (1776–1856). Он разработал концепцию мола, основываясь на гипотезе о том, что равные объемы газа при одинаковом давлении и температуре содержат равное количество молекул.То есть количество не зависит от типа газа. Эта гипотеза подтвердилась, и значение числа Авогадро составляет N A = 6,02 × 10 23 моль -1 .
Он разработал концепцию мола, основываясь на гипотезе о том, что равные объемы газа при одинаковом давлении и температуре содержат равное количество молекул.То есть количество не зависит от типа газа. Эта гипотеза подтвердилась, и значение числа Авогадро составляет N A = 6,02 × 10 23 моль -1 .
Число Авогадро
Один моль всегда содержит 6,02 × 10 23 частиц (атомов или молекул), независимо от элемента или вещества. Моль любого вещества имеет массу в граммах, равную его молекулярной массе, которая может быть вычислена из атомных масс, указанных в периодической таблице элементов.
N A = 6,02 × 10 23 моль −1
Рис. 4. Насколько велика родинка? На макроскопическом уровне один крот мячей для настольного тенниса покроет Землю на глубину около 40 км.
Проверьте свое понимание
Активный ингредиент таблетки Тайленола — 325 мг ацетаминофена (C 8 H 9 NO 2 ). Найдите количество активных молекул ацетаминофена в одной таблетке.
Найдите количество активных молекул ацетаминофена в одной таблетке.
Решение
Сначала нам нужно рассчитать молярную массу (массу одного моля) ацетаминофена.{-3} \ text {moles} \\ [/ latex]
Затем используйте число Авогадро, чтобы вычислить количество молекул.
N = (2,15 × 10 −3 моль) (6,02 × 10 23 молекул / моль) = 1,30 × 10 21 молекул
Пример 3. Расчет молей на кубический метр и литров на моль
Рассчитайте следующее:
- Количество молей в 1,00 м 3 газа на СТП
- Количество литров газа на моль.3} = 22,5 \ text {л / моль} \\ [/ latex]
Обсуждение
Это значение очень близко к принятому значению 22,4 л / моль. Небольшая разница связана с ошибками округления, вызванными использованием трехзначного ввода. Опять же, это число одинаково для всех газов. Другими словами, он не зависит от газа.
(Средняя) молярная масса воздуха (приблизительно 80% N 2 и 20% O 2 составляет M = 28,8 г. Таким образом, масса одного кубического метра воздуха равна 1,28 кг.Если гостиная имеет размеры 5 м × 5 м × 3 м, масса воздуха внутри комнаты составляет 96 кг, что является типичной массой человека.
Проверьте свое понимание
Плотность воздуха при стандартных условиях ( P = 1 атм и T = 20ºC) составляет 1,28 кг / м. 3 . При каком давлении будет плотность 0,64 кг / м 3 , если температура и количество молекул остаются постоянными?
Решение
Лучший способ подойти к этому вопросу — подумать о том, что происходит.Если плотность упадет до половины от исходного значения и никакие молекулы не потеряны, объем должен удвоиться. Если мы посмотрим на уравнение PV = NkT , мы увидим, что когда температура постоянна, давление обратно пропорционально объему. Следовательно, если объем увеличится вдвое, давление должно упасть до половины от исходного значения, и P f = 0,50 атм.
Закон об идеальном газе, пересмотренный с использованием молей
Очень распространенное выражение закона идеального газа использует число молей, n , а не число атомов и молекул, N .Мы начнем с закона идеального газа, PV = NkT , и умножим и разделим уравнение на число Авогадро N A . Это дает [latex] PV = \ frac {N} {N _ {\ text {A}}} N _ {\ text {A}} kT \\ [/ latex].
Обратите внимание, что [латекс] n = \ frac {N} {N _ {\ text {A}}} \\ [/ latex] — это количество молей. Мы определяем универсальную газовую постоянную R = N A k и получаем закон идеального газа в молях.
Закон идеального газа (в молях)
Закон идеального газа (в молях): PV = nRT .
Числовое значение R в единицах СИ составляет R = N A k = (6,02 × 10 23 моль −1 ) (1,38 × 10 −23 Дж / К ) = 8,31 Дж / моль · К.
В других единицах,
R = 1,99 кал / моль · K
R = 0,0821 л · атм / моль · K
Вы можете использовать любое значение R , наиболее подходящее для конкретной задачи.
Пример 4. Расчет количества молей: газ в шине велосипеда
Сколько молей газа в шине велосипеда объемом 2.00 × 10 −3 м 3 (2,00 л), давление 7,00 × 10 5 Па (манометрическое давление чуть менее 90,0 фунт / дюйм 2 ) и при температуре 18,0 ° C?
Стратегия
Определите известные и неизвестные и выберите уравнение для решения неизвестного. В этом случае мы решаем закон идеального газа, PV = nRT , для числа молей n .
Решение
Определите известных:
[латекс] \ begin {array} {lll} P & = & 7.3 \ right)} {\ left (8.31 \ text {J / mol} \ cdot \ text {K} \ right) \ left (291 \ text {K} \ right)} \\\ text {} & = & 0. 579 \ text {mol} \ end {array} \\ [/ latex]
Обсуждение
Наиболее удобный выбор для R в этом случае — 8,31 Дж / моль · К, потому что известные нам величины выражены в единицах СИ. Давление и температура получены из начальных условий в примере 1, но мы получили бы тот же ответ, если бы использовали окончательные значения.
Давление и температура получены из начальных условий в примере 1, но мы получили бы тот же ответ, если бы использовали окончательные значения.
Закон идеального газа можно рассматривать как еще одно проявление закона сохранения энергии (см. Сохранение энергии).Работа, выполняемая с газом, приводит к увеличению его энергии, увеличению давления и / или температуры или уменьшению объема. Эту повышенную энергию также можно рассматривать как увеличенную внутреннюю кинетическую энергию с учетом атомов и молекул газа.
Закон идеального газа и энергия
Давайте теперь рассмотрим роль энергии в поведении газов. Когда вы накачиваете велосипедную шину вручную, вы выполняете работу, многократно прилагая силу на расстоянии. Эта энергия идет на повышение давления воздуха внутри шины и повышение температуры насоса и воздуха.
Закон идеального газа тесно связан с энергией: единицы измерения с обеих сторон — джоули. Правая часть закона идеального газа в PV = NkT равна NkT . Этот термин примерно соответствует количеству поступательной кинетической энергии N атомов или молекул при абсолютной температуре T , как мы формально увидим в «Кинетической теории: атомное и молекулярное объяснение давления и температуры». Левая часть закона идеального газа — это PV , который также имеет единицы измерения в джоулях.Из нашего исследования жидкостей мы знаем, что давление — это один из видов потенциальной энергии на единицу объема, поэтому давление, умноженное на объем, является энергией. Важным моментом является то, что в газе есть энергия, связанная как с его давлением, так и с его объемом. Энергия может изменяться, когда газ выполняет работу по мере расширения — это мы исследуем в разделе «Методы теплопередачи и теплопередачи» — аналогично тому, что происходит в бензиновых или паровых двигателях и турбинах.
Этот термин примерно соответствует количеству поступательной кинетической энергии N атомов или молекул при абсолютной температуре T , как мы формально увидим в «Кинетической теории: атомное и молекулярное объяснение давления и температуры». Левая часть закона идеального газа — это PV , который также имеет единицы измерения в джоулях.Из нашего исследования жидкостей мы знаем, что давление — это один из видов потенциальной энергии на единицу объема, поэтому давление, умноженное на объем, является энергией. Важным моментом является то, что в газе есть энергия, связанная как с его давлением, так и с его объемом. Энергия может изменяться, когда газ выполняет работу по мере расширения — это мы исследуем в разделе «Методы теплопередачи и теплопередачи» — аналогично тому, что происходит в бензиновых или паровых двигателях и турбинах.
Стратегия решения проблем: Закон об идеальном газе
Шаг 1. Изучите ситуацию, чтобы определить, что речь идет об идеальном газе. Большинство газов почти идеальны.
Большинство газов почти идеальны.
Шаг 2. Составьте список того, какие количества указаны или могут быть выведены из проблемы, как указано (определите известные количества). Преобразуйте известные значения в соответствующие единицы СИ (K для температуры, Па для давления, m 3 для объема, молекул для N и молей для n ).
Шаг 3. Определите, что именно необходимо определить в проблеме (определите неизвестные количества).Письменный список полезен.
Шаг 4. Определите, известно ли количество молекул или количество молей, чтобы решить, какую форму закона идеального газа использовать. Первая форма — PV = NkT и включает N , количество атомов или молекул. Вторая форма — PV = nRT и включает n , количество молей.
Шаг 5. Решите закон идеального газа для количества, которое необходимо определить (неизвестное количество). Вам может потребоваться соотношение конечных состояний к начальным состояниям, чтобы исключить неизвестные количества, которые остаются фиксированными.
Вам может потребоваться соотношение конечных состояний к начальным состояниям, чтобы исключить неизвестные количества, которые остаются фиксированными.
Шаг 6. Подставьте известные величины вместе с их единицами измерения в соответствующее уравнение и получите численные решения с указанием единиц. Обязательно используйте абсолютную температуру и абсолютное давление.
Шаг 7. Проверьте ответ, чтобы узнать, разумен ли он: Имеет ли смысл?
Проверьте свое понимание
Жидкости и твердые вещества имеют плотность примерно в 1000 раз больше, чем газы.Объясните, как это означает, что расстояния между атомами и молекулами в газах примерно в 10 раз больше, чем размер их атомов и молекул.
Решение
В твердых телах и жидкостях атомы и молекулы расположены близко друг к другу. В газах они разделены пустым пространством. Таким образом, газы имеют меньшую плотность, чем жидкости и твердые тела. Плотность — это масса на единицу объема, а объем связан с размером тела (например, сферы) в кубе. Таким образом, если расстояние между атомами и молекулами увеличивается в 10 раз, то занимаемый объем увеличивается в 1000 раз, а плотность уменьшается в 1000 раз.
Таким образом, если расстояние между атомами и молекулами увеличивается в 10 раз, то занимаемый объем увеличивается в 1000 раз, а плотность уменьшается в 1000 раз.
Сводка раздела
- Закон идеального газа связывает давление и объем газа с количеством молекул газа и температурой газа.
- Закон идеального газа можно записать через количество молекул газа: PV = NkT , где P — давление, V — объем, T — температура, N — число молекул, k — постоянная Больцмана k = 1,38 × 10 –23 Дж / K.
- Моль — это количество атомов в образце углерода-12 массой 12 г.
- Число молекул в кроте называется числом Авогадро NA , NA = 6,02 × 10 23 моль -1 .
- Моль любого вещества имеет массу в граммах, равную его молекулярной массе, которая может быть определена из периодической таблицы элементов.
- Закон идеального газа также может быть записан и решен в терминах числа молей газа: PV = nRT , где n — число молей, а R — универсальная газовая постоянная, R = 8 .
 31 Дж / моль ⋅ К.
31 Дж / моль ⋅ К. - Закон идеального газа обычно действует при температурах, значительно превышающих температуру кипения.
Концептуальные вопросы
Узнайте человеческое население Земли. Есть ли на Земле крот людей? Если средняя масса человека 60 кг, рассчитайте массу родинки людей. Как масса крота людей соотносится с массой Земли?
При каких обстоятельствах вы ожидаете, что газ будет вести себя значительно иначе, чем предсказывается законом идеального газа?
Газовый термометр постоянного объема содержит фиксированное количество газа.Какое свойство газа измеряется, чтобы указать его температуру?
Задачи и упражнения
- Манометрическое давление в шинах вашего автомобиля составляет 2,50 × 10 5 Н / м 2 при температуре 35,0ºC, когда вы едете на пароме на Аляску. Какое у них манометрическое давление позже, когда их температура упадет до –40,0ºC?
- Преобразование абсолютного давления 7,00 × 10 5 Н / м 2 в манометрическое давление в фунтах / дюйм 2 .
(Это значение было заявлено чуть меньше 90,0 фунтов / дюйм 2 в Примере 4. Это так?)
- Предположим, что газовая лампа накаливания изготовлена таким образом, что газ внутри лампы находится под атмосферным давлением, когда температура лампы составляет 20,0 ° C. (а) Найдите манометрическое давление внутри такой колбы, когда она горячая, при условии, что ее средняя температура составляет 60,0ºC (приблизительное значение), и пренебрегая любыми изменениями в объеме из-за теплового расширения или утечки газа. (b) Фактическое конечное давление для лампочки будет меньше, чем рассчитано в части (а), потому что стеклянная колба расширится.Каким будет фактическое конечное давление с учетом этого? Это незначительная разница?
- Большие шары, наполненные гелием, используются для подъема научного оборудования на большие высоты. (а) Каково давление внутри такого воздушного шара, если он начинается на уровне моря с температурой 10,0 ° C и поднимается на высоту, на которой его объем в двадцать раз превышает исходный объем, а его температура составляет –50,0 ° C? б) Что такое манометрическое давление? (Предположим, что атмосферное давление постоянно.
 )
) - Подтвердите, что единицы nRT являются единицами энергии для каждого значения R: (a) 8.31 Дж / моль K, (b) 1,99 кал / моль K и (c) 0,0821 л атм / моль ⋅ K.
- В тексте было показано, что N / V = 2,68 × 10 25 м −3 для газа на STP. (a) Покажите, что эта величина эквивалентна N / V = 2,68 × 10 19 см −3 , как указано. (b) Примерно сколько атомов содержится в одном мкм 3 (кубический микрометр) в STP? (c) Что ваш ответ на часть (b) подразумевает разделение атомов и молекул?
- Рассчитайте количество молей в 2.00-литровый объем воздуха в легких обычного человека. Учтите, что температура воздуха 37,0 ° C (температура тела).
- У пассажира самолета в желудке 100 см. 3 воздуха непосредственно перед вылетом из аэропорта на уровне моря. Какой объем будет в воздухе на крейсерской высоте, если давление в салоне упадет до 7,50 × 10 4 Н / м 2 ?
- (a) Каков объем (в км 3 ) числа песчинок Авогадро, если каждое зерно представляет собой куб и имеет стороны равные 1.
 0 мм в длину? (b) Сколько километров протяженностью пляжей будет покрыто этим, если ширина пляжа в среднем составляет 100 м, а глубина — 10,0 м? Пренебрегайте воздушными промежутками между зернами.
0 мм в длину? (b) Сколько километров протяженностью пляжей будет покрыто этим, если ширина пляжа в среднем составляет 100 м, а глубина — 10,0 м? Пренебрегайте воздушными промежутками между зернами. - Дорогая вакуумная система может достичь давления всего 1,00 × 10 –7 Н / м 2 при 20 ° C. Сколько атомов в кубическом сантиметре при таком давлении и температуре?
- Плотность атомов газа в определенном месте в космосе над нашей планетой составляет около 1,00 × 10 11 м −3 , а давление равно 2.75 × 10 –10 Н / м 2 в этом пространстве. Какая там температура?
- Велосипедная шина имеет давление 7,00 × 10 5 Н / м 2 при температуре 18,0 ° C и содержит 2,00 л газа. Каким будет его давление, если при атмосферном давлении выпустить воздух объемом 100 см3? Предположим, что температура и объем шины остаются постоянными.
- Газовый баллон высокого давления содержит 50,0 л токсичного газа при давлении 1,40 × 10 7 Н / м 2 и температуре 25.
 0ºC. Его клапан протекает после падения баллона. Цилиндр охлаждается до температуры сухого льда (–78,5 ° C), чтобы снизить скорость утечки и давление, чтобы его можно было безопасно отремонтировать. (а) Каково конечное давление в резервуаре, если предположить, что утечка газа при охлаждении незначительна, и что фазового перехода нет? б) Какое будет конечное давление, если одна десятая газа улетучится? (c) До какой температуры необходимо охладить резервуар, чтобы снизить давление до 1,00 атм (при условии, что газ не меняет фазу и что во время охлаждения нет утечки)? (d) Является ли охлаждение резервуара практическим решением?
0ºC. Его клапан протекает после падения баллона. Цилиндр охлаждается до температуры сухого льда (–78,5 ° C), чтобы снизить скорость утечки и давление, чтобы его можно было безопасно отремонтировать. (а) Каково конечное давление в резервуаре, если предположить, что утечка газа при охлаждении незначительна, и что фазового перехода нет? б) Какое будет конечное давление, если одна десятая газа улетучится? (c) До какой температуры необходимо охладить резервуар, чтобы снизить давление до 1,00 атм (при условии, что газ не меняет фазу и что во время охлаждения нет утечки)? (d) Является ли охлаждение резервуара практическим решением? - Найдите количество родинок в 2.00 л газа при 35,0ºC и давлении 7,41 × 10 7 Н / м 2 .
- Вычислите глубину, на которую шарики для настольного тенниса Авогадро покроют Землю. Каждый шар имеет диаметр 3,75 см. Предположим, что пространство между шарами добавляет дополнительные 25,0% к их объему, и предположим, что они не раздавлены под собственным весом.

- (a) Каково манометрическое давление в автомобильной шине при 25,0 ° C, содержащей 3,60 моль газа в объеме 30,0 л? (b) Каким будет его манометрическое давление, если добавить 1.00 л газа первоначально при атмосферном давлении и 25,0ºC? Предположим, что температура возвращается к 25,0 ° C, а объем остается постоянным.
- (a) В глубоком космосе между галактиками плотность атомов всего лишь 10 6 атомов / м 3 , а температура — холодная 2,7 К. Что такое давление? (б) Какой объем (в м 3 ) занимает 1 моль газа? (c) Если этот объем — куб, какова длина его сторон в километрах?
Глоссарий
Закон идеального газа: Физический закон, который связывает давление и объем газа с количеством молекул газа или количеством молей газа и температурой газа
постоянная Больцмана: k , физическая постоянная, которая связывает энергию с температурой; к = 1.38 × 10 –23 Дж / К
Число Авогадро: NA , количество молекул или атомов в одном моль вещества; NA = 6,02 × 10 23 частиц / моль
моль: количество вещества, масса которого (в граммах) равна его молекулярной массе
Избранные решения проблем и упражнения
1. {2} \ right) \\ & = & \ text {N} \ cdot \ text {m} = \ text {J} \ конец {массив} \\ [/ latex]
{2} \ right) \\ & = & \ text {N} \ cdot \ text {m} = \ text {J} \ конец {массив} \\ [/ latex]
7.7,86 × 10 −2 моль
9. (а) 6.02 × 10 5 км 3 ; (б) 6,02 × 10 8 км
11. -73.9ºC
13. а) 9,14 × 10 6 Н / м 2 ; б) 8,23 × 10 6 Н / м 2 ; (в) 2,16 К; (d) Нет. Необходимая конечная температура слишком низкая, чтобы ее можно было легко достичь для большого объекта.
15. 41 км
17. (а) 3,7 × 10 −17 Па; б) 6.0 × 10 17 м 3 ; (в) 8.4 × 10 2 км
Измерения и преобразования жидкого топлива
Измерения и преобразование жидкого топлива
Бензин
1 галлон = 125 000 британских тепловых единиц — HHV *
1 галлон = 131,9 мегаджоулей — HHV *
1 галлон = 115400 британских тепловых единиц — LHV *
1 галлон = 121,7 мегаджоулей — LHV *
1 галлон =
1 метрическая тонна баррель = 5 250 000 британских тепловых единиц — HHV *
1 баррель = 5 539 мегаджоулей — HHV *
1 баррель = 4 846 800 британских тепловых единиц — LHV *
1 баррель = 5 113 мегаджоулей — LHV *
1 баррель =. 1172 метрических тонны
1172 метрических тонны
1 литр = 33025 британских тепловых единиц — HHV *
1 литр = 30 489 британских тепловых единиц — LHV *
1 литр = 34,8 мегаджоулей — HHV *
1 литр = 32,2 мегаджоулей — LHV *
1 метрическая тонна = 8,5 баррелей
1 метрическая тонна = 1,351 килолитра
1 килолитр = 0,740 метрической тонны
Дизельное топливо
1 галлон = 138,700 БТЕ — HHV *
1 галлон = 146,3 мегаджоулей — HHV *
1 галлон = 128,700 британских тепловых единиц — LHV *
1 галлон = 135,8 мегаджоулей — LHV *
1 галлон = 0,003192 метрическая тонна 1 баррель = 5 825 400 БТЕ — HHV *
1 баррель = 6 146 мегаджоулей — HHV *
1 баррель = 5 405 400 британских тепловых единиц — LHV *
1 баррель = 5 703 мегаджоулей LHV *
1 баррель =.1341 метрическая тонна
1 метрическая тонна = 7,5 баррелей
1 килолитр = 0,839 метрических тонн
1 метрическая тонна = 1,192 килолитра
1 литр = 36 645 БТЕ — HHV *
1 литр = 38,7 мегаджоулей — HHV *
1 литр = 34 003 БТЕ — LHV *
1 литр = 35,9 мегаджоулей — LHV *
Этанол
1 галлон = 84600 БТЕ — HHV *
1 галлон = 89,3 мегаджоулей — HHV *
1 галлон = 75 670 Btu — LHV *
1 галлон = 79,8 мегаджоулей — LHV *
1 баррель = 3553 200 Btu — HHV42 1 баррель = 3749 мегаджоулей — HHV *
1 баррель = 3,178,140 БТЕ — LHV *
1 баррель = 3,353 мегаджоулей — LHV *
1 литр = 22,351 БТЕ — HHV *
1 литр = 23. 6 мегаджоулей — HHV *
1 литр = 19,992 Btu — LHV *
1 литр = 21,1 мегаджоулей — LHV *
Средняя плотность этанола = 0,79 грамма на миллилитр
Средняя плотность этанола = 0,79 метрических тонн на кубический метр
Биодизельное топливо
1 галлон = 126 206 БТЕ — HHV *
1 галлон = 133,1 мегаджоулей — HHV *
1 галлон = 117 093 Btu — LHV *
1 галлон = 123,5 мегаджоулей — LHV *
1 баррель = 5 300 652 HV Btu *
1 баррель = 5 592 мегаджоулей — HHV *
1 баррель = 4 917 906 БТЕ — LHV *
1 баррель = 5 188 мегаджоулей — LHV *
1 литр = 33 344 БТЕ — HHV *
1 литр = 35.2 мегаджоуля — HHV *
1 литр = 30 936 Btu — LHV *
1 литр = 32,6 мегаджоулей — LHV *
1 метрическая тонна биодизеля = 37,8 гигаджоулей
Средняя плотность биодизеля = 0,88 грамма на миллилитр
Средняя плотность биодизеля = 0,88 метрических тонн на кубический метр
Остаточное топливо
1 галлон = 149 700 Btu — HHV *
1 галлон = 157,9 мегаджоулей — HHV *
1 галлон = 138 400 Btu — LHV *
1 галлон = 146,0 мегаджоулей — LHV *
1 баррель = 6 287 HVu — HHV *
1 баррель = 6 287 HHVu
1 баррель = 6 633 мегаджоулей — HHV *
1 баррель = 5 812 800 БТЕ — LHV *
1 баррель = 6 133 мегаджоулей — LHV *
1 литр = 39 551 БТЕ — HHV *
1 литр = 41. 7 мегаджоулей — HHV *
7 мегаджоулей — HHV *
1 литр = 36 565 Btu — LHV *
1 литр = 38,6 мегаджоулей — LHV *
Сжиженный нефтяной газ (сжиженный нефтяной газ — пропан)
1 галлон = 91 300 БТЕ — HHV *
1 галлон = 96,3 мегаджоулей — HHV *
1 галлон = 83,500 Btu — LHV *
1 галлон = 88,1 мегаджоулей — LHV *
баррель = 3 834 600 БТЕ — HHV *
1 баррель = 4046 мегаджоулей — HHV *
1 баррель = 3 507 000 британских тепловых единиц — LHV *
1 баррель = 3700 мегаджоулей — LHV *
1 литр = 24 121 британских тепловых единиц — HHV *
1 литр = 25.4 мегаджоуля — HHV *
1 литр = 22061 Btu — LHV *
1 литр = 23,3 мегаджоулей — LHV *
1 баррель = 0,086 метрической тонны
1 метрическая тонна = 11,6 баррелей
1 килолитр = 0,542 метрической тонны
1 метрическая тонна = 1,844 килолитра
Метанол
1 галлон = 64 600 БТЕ — HHV *
1 галлон = 68,2 мегаджоулей — HHV *
1 галлон = 56 560 Btu –LHV *
1 галлон = 59,7 мегаджоулей — LHV *
1 баррель = 2 713 200 Btu —
HHV 1 баррель = 2 862 мегаджоулей — HHV *
1 баррель = 2 375 520 Btu — LHV *
1 баррель = 2 506 мегаджоулей — LHV *
1 литр = 17067 Btu — HHV *
1 литр = 18. 0 мегаджоулей — HHV *
0 мегаджоулей — HHV *
1 литр = 14 943 Btu — LHV *
1 литр = 15,8 мегаджоулей — LHV *
Бутан
1 галлон = 103000 БТЕ — HHV *
1 галлон = 108,7 мегаджоулей — HHV *
1 галлон = 93000 Btu — LHV *
1 галлон = 98,1 мегаджоулей — LHV *
1 баррель = 4 326 000 Btu — HHV 1 баррель = 4564 мегаджоулей — HHV *
1 баррель = 3 906 000 Btu — LHV *
1 баррель = 4,121 мегаджоулей — LHV *
1 литр = 27 213 Btu — HHV *
1 литр = 28.7 мегаджоулей — HHV *
1 литр = 24 571 Btu — LHV *
1 литр = 25,9 мегаджоулей — LHV *
Замеры и переработка баррелей нефти или сопутствующих продуктов (баррелей)
Сырая нефть (на основе среднемировой плотности)
1 баррель = 42 галлона
1 бочка = 55 галлонов
1 метрическая бочка = 52,8 галлона
1 галлон = 0,0182 бочка
1 галлон = 0,0189 метрическая бочка
1 галлон = 138 100 БТЕ — HHV *
1 галлон = 145,7 мегаджоулей — HHV *
1 галлон = 131 800 БТЕ — LHV *
1 галлон = 139. 0 мегаджоулей — LHV *
0 мегаджоулей — LHV *
1 галлон = 0,003247 метрических тонн
1 галлон = 0,0038 килолитра
1 галлон = 0,0238 баррелей
1 баррель = 5 800 200 британских тепловых единиц — HHV *
1 баррель = 6,119 мегаджоулей — HHV *
600 = 5,535 Btu — LHV *
1 баррель = 5840 мегаджоулей — LHV *
1 баррель = 0,13637 метрических тонн
1 баррель = 0,159 килолитра
1 литр = 36 486 BTU — HHV *
1 литр = 38,5 мегаджоулей — HHV *
1 литр = 34 822 БТЕ — LHV *
1 литр = 36,7 мегаджоулей — LHV *
1 килолитр =.8581 метрическая тонна
1 килолитр = 6,2898 баррелей
1 килолитр = 264,17 галлона
1 килолитр = 1 кубический метр
1 метрическая тонна = 1,165 килолитра
1 метрическая тонна = 7,33 баррелей
1 метрическая тонна = 307,86 галлона
1 баррель сырой нефти = 44,60 галлона нефтепродуктов
| галлонов | Процент | |
| Бензин автомобильный готовый | 19. | 44 |
| Мазут дистиллятный | 10,50 | 24 |
| Реактивное топливо типа Kero | 4,12 | 9 |
| Кокс нефтяной | 2,23 | 5 |
| Тихий газ | 1.81 | 4 |
| Мазут остаточный | 1,68 | 4 |
| Газ нефтепереработки сжиженный | 1,51 | 3 |
| Асфальт и дорожное масло | 1,34 | 3 |
| Прочее | 2. | 4 |
Нефтяные эквиваленты
Баррель (метрическая тонна) нефтяного эквивалента — это единица энергии, основанная на приблизительной энергии, выделяемой при сжигании одного барреля (метрической тонны) сырой нефти.
1 баррель нефтяного эквивалента (bboe) = 0,1364 метрической тонны нефтяного эквивалента
1 баррель нефтяного эквивалента = приблизительно 1,364 миллиона килокалорий
1 баррель нефтяного эквивалента = приблизительно 5,73 гигаджоулей
1 баррель нефтяного эквивалента = приблизительно.20 метрических тонн каменного угля
1 баррель нефтяного эквивалента = примерно 0,41 метрической тонны бурого угля
1 баррель нефтяного эквивалента = примерно 1,64 метаватт-часа
1 миллион баррелей нефтяного эквивалента = 0,16 миллиарда кубических метров природного газа
1 миллион баррелей нефти эквивалент = 5,61 миллиарда кубических футов природного газа
1 миллион баррелей нефтяного эквивалента = 0,12 миллиона метрических тонн сжиженного природного газа
1 миллион баррелей нефтяного эквивалента = 5,8 триллиона БТЕ
1 миллион баррелей нефтяного эквивалента =. 14 миллионов метрических тонн нефтяного эквивалента
14 миллионов метрических тонн нефтяного эквивалента
1 метрическая тонна нефтяного эквивалента (тнэ) = 7,33 баррелей нефтяного эквивалента
1 метрическая тонна нефтяного эквивалента = приблизительно 10 миллионов килокалорий
1 метрическая тонна нефтяного эквивалента = приблизительно 42 гигаджоулей
1 метрическая тонна нефтяного эквивалента = приблизительно 1,5 метрические тонны каменного угля
1 метрическая тонна нефтяного эквивалента = примерно 3 метрических тонны бурого угля
1 метрическая тонна нефтяного эквивалента = примерно 12 мегаватт-часов
1 миллион метрических тонн нефтяного эквивалента = 1.111 миллиардов кубометров природного газа
1 миллион метрических тонн нефтяного эквивалента = 39,2 миллиарда кубических футов природного газа
1 миллион метрических тонн нефтяного эквивалента = 0,805 миллиона тонн сжиженного природного газа
1 миллион метрических тонн нефтяного эквивалента = 7,33 миллиона баррелей нефтяного эквивалента
Очищенные нефтепродукты
1 метрическая тонна автомобильного бензина = 8,53 баррелей
1 метрическая тонна сжиженного нефтяного газа (сжиженный нефтяной газ) (пропан) = 11,6 баррелей
1 метрическая тонна природного газа = 10 баррелей
1 метрическая тонна NGL (природный газ жидкости) = 10. 4 ствола
4 ствола
Жидкое топливо
1 кубический метр = 6,289 баррелей
1 баррель = 159 литров
1 баррель = 42 галлона США
1 галлон США = 231 кубических дюймов
1 галлон США = 0,1337 кубических футов
1 галлон США = 3,785 литра
1 галлон США = 0,8321 британского галлона
1 галлон США = 0,0238 барреля
1 галлон США = 0,003785 кубического метра
1 литр = 61,02 кубического дюйма
1 литр = 0,03531 кубического фута
1 литр = 0,2642 галлона США
1 литр =.22 британских галлона
1 литр = 0,00629 баррелей
1 литр = 0,001 кубических метров
Расход
1 баррель в час = 137,8 кубических футов в день
1 баррель в час = 49 187 кубических футов в год
1 баррель в час = 1008 галлонов США в день
1 баррель в час = 367 920 галлонов США в год
1 баррель в час = 839,3 британских галлона в день
1 баррель в час = 306 345 британских галлонов в год
1 баррель в час = 3 815 литров в день
1 баррель в час = 1,392 475 литров в год
1 галлон в час =. 5712 баррелей в день
5712 баррелей в день
1 галлон в час = 207,92 баррелей в год
1 литр в час = 0,1510 баррелей в день
1 литр в час = 55,10 баррелей в год
Измерения расхода топлива и преобразование
1 миля на галлон = 0,264 мили на литр
1 миля на галлон = 0,425 километра на литр
1 миля на галлон = 235 литров на 100 километров
1 миля на галлон = 100 галлонов на 100 миль
1 миля на литр = 3,79 мили на галлон
1 миля на литр = 1.609 километров на литр
1 миля на литр = 62,15 литра на 100 километров
1 километр на литр = 2,35 мили на галлон
1 километр на литр = 0,6215 мили на литр
1 километр на литр = 100 литров на 100 километров
1 километр за литр = 42,5 галлона на 100 миль
* Энергосодержание выражается либо как высокая (общая) теплотворная способность (HHV), либо как нижняя (чистая) теплотворная способность (LHV). LHV в большинстве случаев ближе всего к фактическому выходу энергии. HHV (включая конденсацию продуктов сгорания) больше на 5% (в случае угля) и 10% (для природного газа), в основном в зависимости от содержания водорода в топливе. Для большинства видов сырья биомассы эта разница составляет 6-7%. Целесообразность использования LHV или HHV при сравнении топлива, вычислении теплового КПД и т. Д. Действительно зависит от области применения. Для стационарного горения, когда выхлопные газы охлаждаются перед сбросом (например, на электростанциях), более подходит HHV. В тех случаях, когда не делается попыток извлечь полезную работу из горячих выхлопных газов (например, автомобилей), более подходит LHV. На практике многие европейские публикации сообщают о LHV, в то время как в североамериканских публикациях используется HHV
Для большинства видов сырья биомассы эта разница составляет 6-7%. Целесообразность использования LHV или HHV при сравнении топлива, вычислении теплового КПД и т. Д. Действительно зависит от области применения. Для стационарного горения, когда выхлопные газы охлаждаются перед сбросом (например, на электростанциях), более подходит HHV. В тех случаях, когда не делается попыток извлечь полезную работу из горячих выхлопных газов (например, автомобилей), более подходит LHV. На практике многие европейские публикации сообщают о LHV, в то время как в североамериканских публикациях используется HHV
(Источник: Bioenergy Feedstock Network — https: // bioenergy.ornl.gov/)
Список литературы
Сеть информации о сырье для биоэнергетики: http://bioenergy.ornl.gov/
Ежегодник по энергии биомассы, Министерство энергетики США
BP Коэффициенты преобразования
ConvertIt
Управление по энергетической информации
Управление по энергетической информации — страница Energy Kids: http://tonto.


 В промышленности СПБТ используют для разогрева и резки металла, укладки битумосодержащего перекрытия и т. п.
В промышленности СПБТ используют для разогрева и резки металла, укладки битумосодержащего перекрытия и т. п.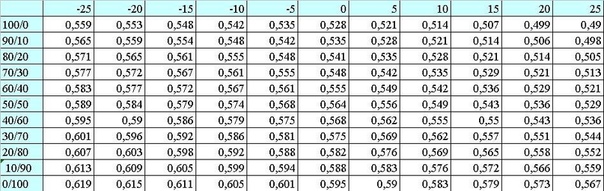 Поэтому, наверное, правильно будет принять за отправную точку минимальное значение, и ориентироваться именно на него. Конечно, выполненные нами поверхностные расчеты могут дать только приблизительные значения, однако да же на этом примере мы видим, что абсолютно однозначно установить продолжительность работы газового оборудования от одного заправленного баллона заданной емкости не зная точных параметров его смеси, массы газа внутри, его физико-химических свойств – достаточно сложно. И самым просты для потребителя способом расчета будет являться все таки первый, который мы использовали – отношение расчетной массы сжиженного газа в баллоне к паспортному расходу газового оборудования, работающего на сжиженном газе. При этом лучше пользоваться именно массовым расходом, а не объемным, поскольку объем жидкой фазы достаточно сильно зависит от плотности смеси, которая в свою очередь так же находится в очень широком диапазоне значений.
Поэтому, наверное, правильно будет принять за отправную точку минимальное значение, и ориентироваться именно на него. Конечно, выполненные нами поверхностные расчеты могут дать только приблизительные значения, однако да же на этом примере мы видим, что абсолютно однозначно установить продолжительность работы газового оборудования от одного заправленного баллона заданной емкости не зная точных параметров его смеси, массы газа внутри, его физико-химических свойств – достаточно сложно. И самым просты для потребителя способом расчета будет являться все таки первый, который мы использовали – отношение расчетной массы сжиженного газа в баллоне к паспортному расходу газового оборудования, работающего на сжиженном газе. При этом лучше пользоваться именно массовым расходом, а не объемным, поскольку объем жидкой фазы достаточно сильно зависит от плотности смеси, которая в свою очередь так же находится в очень широком диапазоне значений. )
) 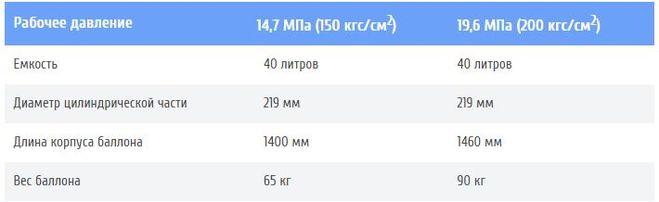 толщина стенки
толщина стенки толщина стенки
толщина стенки 40
40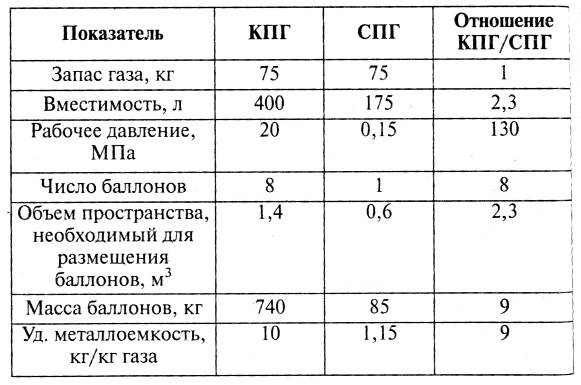 01
01