Сода. NaHCO3. Бикарбонат натрия. Натрий двууглекислый. Питьевая сода.
Здесь все собрано из институтских тетрадей и то, что я выписывала для себя из интернета.
Гидрокарбонат натрия NaHCO3, Сода или по другому: питьевая сода, пищевая сода, бикарбонат натрия, натрий двууглекислый — это соль, да не просто!, а кислая натриевая соль угольной кислоты (H2CO3 слабая двухосновная кислота).
Соль впервые описана в 1801 немецким аптекарем Б. Розе
В соответствии с основностью угольная кислота даёт два ряда солей: средние — карбонаты с анионом CO32- (водные растворы имеют !сильнощелочную реакцию) и кислые — гидрокарбонаты с анионом HCO3— — (водные растворы имеют !!слабощелочную реакцию).
Здесь нужно учитывать все параметры, и связи, и плотность, и т.п.
Стабильность гидрокарбонатов растет при переходе от Na+ к Cs+. Ионы НСО3— обычно объединяются водородными связями с образованием цепочек.
NaHCO3 — плотность 2,16—2,22 г/см3. При нагревании около 50 °С начинает отщепляться 002, а при 100—150 °С полностью разлагается, превращаясь в Na2CO3.
Мы растворяем соду в воде, опять –если вода до 50 °С, действие одно, это гидролиз соли: обратимое взаимодействие соли с водой, приводящее к образованию слабого электролита, а от 80-150 °С получается уже Na2CO3.
Вода хотя и в малой степени, но диссоциирует:
H2O H+ + OH–.
Когда концентрации ионов H+ и гидроксид-ионов OH– равны между собой, [H+] = [OH–], то среда нейтральная, если [H+] > [OH–] – среда кислая, если [Н+] < [ОН–] – среда щелочная.
Гидрокарбонат натрия реагирует с соляной кислотой, с образованием соли и угольной кислоты. Угольная кислота очень слабая, крайне неустойчивое соединение, поэтому оно тут же распадается на углекислый газ и воду:
NaHCO3 + HCl → NaCl + H2CO3
H2CO3 → H2O + CO2↑
Так происходит, если мы соду растворили в теплой воде (до 50 градусов)
А если растворяем соду в горячей воде, то уже образуется карбонат натрия, и в этом случае, водный раствор имеет уже сильнощелочную реакцию. Гидролиз.
Гидролиз.
Температура. Поскольку реакция гидролиза эндотермическая, то повышение температуры смещает равновесие в системе вправо, степень гидролиза возрастает.
Концентрация соли. равновесие в системе смещается вправо, в соответствии с принципом Ле Шателье, но степень гидролиза уменьшается. Понять это поможет константа равновесия.
Добавки посторонних веществ могут влиять на положение равновесия в том случае, когда эти вещества реагируют с одним из участников реакции.
Степень гидролиза можно увеличить, и , например, чтобы сделать щелочной моющий раствор бельевой соды более активным, мы его нагреваем – степень гидролиза карбоната натрия при этом возрастает.
Сода относится к антацидам. Взаимодействуя с соляной кислотой, сода устраивает в желудке «химлабораторию». В итоге вырабатывается уг-лекислый газ, «нападающий» на стенки желудка. Защищаясь, желудок вырабатывает новую дозу сока и соляной кислоты — на это требуется 20 минут.
Современные исследования
В организме роль соды заключается в нейтрализации кислот, повышении щелочных резервов организма в поддержании в норме кислотно-щелочного равновесия.
У человека показатель кислотности pH крови должен находиться в норме в пределах 7,35-7,47. Если pH меньше 6,8 (очень кислая кровь, сильнейший ацидоз), то наступает смерть организма.
Причинами ацидоза являются яды в пище, воде и воздухе, лекарства, пестициды. Большое самоотравление людей психическими ядами происходит от страха, беспокойства, раздражения, недовольства, зависти, злобы, ненависти, которые сейчас очень усилены благодаря нарастающим волнам Космического Огня. При потере психической энергии почки не могут удерживать в крови высокую концентрацию соды, которая при этом теряется вместе с мочой. Это другая причина ацидоза: потеря психической энергии ведет к потере щелочей (соды).
Сода, уничтожая ацидоз, повышает щелочные резервы организма, сдвигает кислотно-щелочное равновесие в щелочную сторону (pH примерно 1,45 и выше). В щелочном организме происходит активация воды, т.е. диссоциация ее на ионы Н+ и OH- за счет аминных щелочей, аминокислот, белков, ферментов, нуклеотидов РНК и ДНК. В активированной воде, насыщенной огненной энергией организма, улучшаются все биохимические процессы: ускоряется синтез белка, быстрее обезвреживаются яды, активнее работают ферменты и аминные витамины, лучше действуют аминные лекарства, имеющие огненную природу и биологически активные вещества.
В щелочном организме происходит активация воды, т.е. диссоциация ее на ионы Н+ и OH- за счет аминных щелочей, аминокислот, белков, ферментов, нуклеотидов РНК и ДНК. В активированной воде, насыщенной огненной энергией организма, улучшаются все биохимические процессы: ускоряется синтез белка, быстрее обезвреживаются яды, активнее работают ферменты и аминные витамины, лучше действуют аминные лекарства, имеющие огненную природу и биологически активные вещества.
Здоровый организм для пищеварения вырабатывает сильно щелочные пищеварительные соки. Пищеварение в двенадцатиперстной кишке происходит в щелочной среде под действием соков: панкреатический сок, желчь, сок бруттнеровой железы и сок слизистой оболочки двенадцатиперстной кишки. Все соки имеют высокую щелочность. Панкреатический сок имеет pH=7,8-9,0. Ферменты панкреатического сока действуют только в щелочной среде. Желчь в норме имеет щелочную реакцию pH=7,50-8,50. Секрет толстого кишечника имеет сильно щелочную среду pH=8,9-9,0. При сильном ацидозе желчь становится кислой pH=6,6-6,9 вместо нормы pH=7,5-8,5. Это ухудшает пищеварение, что приводит к отравлению организма продуктами плохого пищеварения, образованию камней в печени, желчном пузыре, кишечнике и почках. В кислой среде спокойно живут глисты опистархоза, острицы, аскариды, цепни и др. В щелочной среде они гибнут. В кислом организме слюна кислая pH=5,7-6,7, что приводит к медленному разрушению эмали зубов. В щелочном организме слюна щелочная: pH=7,2-7,9 и зубы не разрушаются.
Это ухудшает пищеварение, что приводит к отравлению организма продуктами плохого пищеварения, образованию камней в печени, желчном пузыре, кишечнике и почках. В кислой среде спокойно живут глисты опистархоза, острицы, аскариды, цепни и др. В щелочной среде они гибнут. В кислом организме слюна кислая pH=5,7-6,7, что приводит к медленному разрушению эмали зубов. В щелочном организме слюна щелочная: pH=7,2-7,9 и зубы не разрушаются.
Сода, нейтрализуя избыточные кислоты, повышает щелочные резервы организма, делает мочу щелочной, что облегчает работу почек (сберегает психическую энергию), сберегает глутаминовую аминокислоту, предотвращает отложение камней в почках.
Замечательным свойством соды является то, что избыток её легко выводится почками, давая щелочную реакцию мочи
В щелочной среде с активированной водой многократно возрастает биохимическая активность аминных витаминов: В1 (тиамин, кокарбоксилаза), В4 (холин), В5 или РР (никотиномид), В6 (пиридоксаль), В12 (кобимамид). Витамины, имеющие огненную природу могут полностью проявлять её только в щелочной среде.
Витамины, имеющие огненную природу могут полностью проявлять её только в щелочной среде.
Для улучшения всасывания соды из кишечника её принимают с горячим молоком. В кишечнике сода реагирует с аминокислотами молока, образуя щелочные натриевые соли аминокислот, которые легче, чем сода всасываются в кровь, повышая щелочные резервы организма.
Для борьбы с аскаридами и острицами применяют аминную щёлочь пиперазин, дополняя его клизмами соды . Сода применяется при отравлении метанолом, этиловым спиртом, формальдегидом, карбофосом, хлорофосом, белым фосфором, фосфином, фтором, йодом, ртутью и свинцом, для отвыкания от курения: полоскание рта густым раствором соды или обмазывание полости рта содой со слюной: сода кладётся на язык, растворяется в слюне и вызывает отвращение к табаку при курении. Дозы малые, чтобы не нарушать пищеварения.
В письме от 1 января 1935 г. Е.И. Рерих писала: “Вообще Владыка очень советует всем приучаться принимать соду два раза в день. Это изумительное предохранительное средство от многих тяжких заболеваний, в частности, от рака” (Письма Елены Рерих, т. 3, с. 74). 4 января 1935г.: “Я принимаю её ежедневно, иногда при сильном напряжении, до восьми раз в день по кофейной ложке. Причём я просто высыпаю её на язык и запиваю водой. Также замечательно хорошо действует при всех простудах и напряжениях центров горячее, но не прокипяченное молоко с содой” (Письма, т. 3, с 75). «Хорошо и деткам давать соду в горячем молоке» (П6, 20, 1). 18 июля 1935 г.: “Затем советую вам ежедневно принимать два раза в день двууглекислую соду. При болях в подложечке (напряжение в солнечном сплетении) приемы соды незаменимы. Да и вообще, сода – самое благодетельное средство, она предохраняет от всевозможных заболеваний, начиная от рака, но нужно приучить себя принимать её ежедневно без пропусков…Также при ломоте и горении в горле незаменимо горячее молоко, но не вскипевшее, а также с содою. Обычная пропорция кофейная ложка на стакан. Очень советуйте всем соду. Также наблюдайте, чтобы желудок не был обременен, и кишечник чист” (П, 18.
3, с. 74). 4 января 1935г.: “Я принимаю её ежедневно, иногда при сильном напряжении, до восьми раз в день по кофейной ложке. Причём я просто высыпаю её на язык и запиваю водой. Также замечательно хорошо действует при всех простудах и напряжениях центров горячее, но не прокипяченное молоко с содой” (Письма, т. 3, с 75). «Хорошо и деткам давать соду в горячем молоке» (П6, 20, 1). 18 июля 1935 г.: “Затем советую вам ежедневно принимать два раза в день двууглекислую соду. При болях в подложечке (напряжение в солнечном сплетении) приемы соды незаменимы. Да и вообще, сода – самое благодетельное средство, она предохраняет от всевозможных заболеваний, начиная от рака, но нужно приучить себя принимать её ежедневно без пропусков…Также при ломоте и горении в горле незаменимо горячее молоко, но не вскипевшее, а также с содою. Обычная пропорция кофейная ложка на стакан. Очень советуйте всем соду. Также наблюдайте, чтобы желудок не был обременен, и кишечник чист” (П, 18. 06.35).
06.35).
«Для ослабления диабета принимают соду…молоко с содою всегда хорошо…» (МО3, 536).
«Явление переполнения психической энергией вызывает многие симптомы как в конечностях, так в горле и желудке. Сода полезна, чтобы вызвать разряжение, также горячее молоко…» (С, 88).
«При раздражении и волнении Советую молоко во всех видах, как обычное противоядие. Сода укрепляет действие молока» (С, 534). «При волнении – прежде всего, недоедание и валериан, и, конечно, молоко с содою» (С, 548)
(лечение кашля) «…Мускус и горячее молоко будут хорошим предохранителем. Насколько холодное молоко не соединяется с тканями, настолько же горячее с содою проникает в центры…» (МО1, 58)
«Сода полезна и смысл ее так близок огню. Сами содовые поля назывались пеплом Великого Пожара. Так в древности люди уже знали особенности соды. Поверхность Земли покрыта содою на широкое употребление» (МО3, 595).
«Запоры лечат различными способами, упуская из вида самый простой и естественный, а именно: простую пищевую соду с горячим молоком. В данном случае действует металл натрий
В данном случае действует металл натрий
«Напряжение огненное отражается на некоторых функциях организма. Так, в этом случае для правильной работы кишечника необходима сода, принимаемая в горячем молоке… Сода тем хороша, что не вызывает раздражения кишечника» (ГАЙ11, 515).
«К обычному очищению кишечника можно добавить регулярный прием питьевой соды, которая обладает способностью нейтрализовать многие яды…» (ГАЙ12, 147.М.А.Й.)
1 июня 1936 г. Елена Рерих писала: “Но сода получила повсеместное признание, и сейчас ею увлекаются особенно в Америке, где она применяется чуть ли не против всех болезней… Нам указано принимать соду два раза в день, также как валериан, не пропуская ни одного дня. Сода предупреждает многие заболевания, включая даже рак” (Письма, т.3, с. 147).
8 июня 1936 г.: “Вообще, сода полезна почти при всех болезнях и является предохранителем от многих заболеваний, потому не опасайтесь принимать её, также как и валериан” (Письма, т.2, с. 215). «Это изумительное предохранительное средство от многих тяжких заболеваний, в частности, от рака. Я слышала о случае излечения застарелого наружного рака засыпанием его содою. Когда мы вспомним, что сода входит, как главный ингредиент, в состав нашей крови, то становится понятным ее благодетельное действие. При огненных явлениях сода незаменима» (П 3, 19, 1).
Я слышала о случае излечения застарелого наружного рака засыпанием его содою. Когда мы вспомним, что сода входит, как главный ингредиент, в состав нашей крови, то становится понятным ее благодетельное действие. При огненных явлениях сода незаменима» (П 3, 19, 1).
О дозах приёма Е.И. Рерих писала: “Доза соды для мальчика (диабетика в 11 лет) – четверть чайной ложки четыре раза в день” (Письма, т.3, с. 74). “Один английский доктор… применил простую соду от всяких воспалительных и простудных заболеваний, включая воспаление легких. Причем он давал её в довольно больших дозах чуть ли не по чайной ложке до четырех раз в день на стакан молока или воды. Конечно, английская чайная ложка меньше нашей русской. Моя семья при всех простудах, особенно при ларингите и крупозном кашле употребляет горячее молоко с содой. На чашку молока кладем чайную ложку соды” (Письма, т. 3, с. 116). “Если вы не принимали ещё соду, то начните по маленьким дозам, по пол кофейной ложечке два раза в день. Постепенно можно будет увеличить эту дозу. Лично я принимаю ежедневно две-три полные кофейные ложечки. При болях в солнечном сплетении и тягости в желудке принимаю и значительно больше. Но всегда следует начинать с малых доз” (Письма, т.3, с. 309).
Лично я принимаю ежедневно две-три полные кофейные ложечки. При болях в солнечном сплетении и тягости в желудке принимаю и значительно больше. Но всегда следует начинать с малых доз” (Письма, т.3, с. 309).
14 июня 1965 г. Б.Н. Абрамов записал от Матери Агни Йоги: “Интересно отметить, как чуткие организмы уже реагируют на огненную напряженность. И хорошо, если кто уже умеет регулировать в своем организме эти приливы огненных энергий. Сода может оказаться истинной панацеей” (Г.А.Й., т.6, с.119, п. 220).
Сода и щёлочи имеют огненную природу. “Сода полезна, и смысл её так близок Огню. Сами содовые поля назывались пеплом Великого Пожара” (М.О., ч.3, п.595).
О пользе соды для растений говорится: “Утром можно полить растения, добавляя в воду щепоть соды. При закате нужно полить с раствором валериана” (А.Й., п. 387).
В пище человека “не нужно кислоты искусственных приготовлений” (А.Й., п. 442), т.о. явно сказано о вреде искусственных кислот, но искусственные щелочи (сода и бикарбонат калия) намного полезнее хлорида и оротата калия.
!!!! Принимать соду необходимо натощак, за 20-30 мин. до еды (нельзя сразу же после еды – может быть обратный эффект). Начинать с малых доз – 1/5 чайной ложки, постепенно увеличивать дозу, доводя до 1/2 чайной ложки. Можно развести соду в одном стакане тепло-горячей кипяченой воды (горячего молока) либо принять в сухом виде, запивая (обязательно!) горячей водой или молоком (один стакан). Принимать 2-3 р. в день.
Метастазы это такие же плодовые тела «грибные» уже по всей «грибнице». Созрев, метастазы отрываются и разносятся по всему организму, ищут слабое место и растут снова. А слабое место это кислая среда в организме, различные воспаления в органах и системах. Вот и получается, чтобы вылечить рак и для его профилактики, нужно поддерживать в организме определенную среду .
РН-среда, или водородный показатель. При рождении он составляет 7,41 РН, а умирает человек с показателем 5,41-4,5. На всю жизнь ему отведено 2 единицы. Рак возникает при снижении водородного показателя до величины 5,41. Самая большая активность лимфатических клеток по уничтожению раковых заболеваний проявляется при РН 7,4. Однако обычно вокруг клеток, пораженных раком , существует более кислая среда , которая препятствует активности лимфатических клеток.
Самая большая активность лимфатических клеток по уничтожению раковых заболеваний проявляется при РН 7,4. Однако обычно вокруг клеток, пораженных раком , существует более кислая среда , которая препятствует активности лимфатических клеток.
В в кислой среде более часто возникают злокачественные новообразования слизистой оболочки пищевода. Замечено, что во многих странах возрастание потребления газированных прохладительных напитков сопровождалось параллельным увеличением распространенности рака пищевода.
Нормальное состояние внутренних жидкостей человеческого организма — слабо-щелочное. Кислая среда — благоприятная среда для буйного роста бактерий и раковых клеток.
СОДА — ПЕПЕЛ БОЖЕСТВЕННОГО ОГНЯ
«Сода полезна,и смысл ее близок огню.Сами содовые поля назывались пеплом великого Пожара. Так в древности люди уже знали особенности соды. |
Сода-универсальное средство по своей доступности в применении как в пищевом рационе, так и в медицине. Но ее изумительные предохранительные и целительные свойства еще недостаточно осознаны и не столь широко применяются. А ведь гидрокарбонат натрия (или сода) входит, как главный инградиент, в состав нашей крови. (Об этом указывала Е.И.Рерих). Сода входит в состав плазмы крови, а также лимфоплазмы, в которой находятся лимфоциты. Возможно, сода энергетически питает лимфоциты — клетки, ответственные за иммунный ответ организма.
Среди людей бытует превратное мнение,иногда поддерживаемое и медиками, что длительный и частый прием соды оказывает отрицательное воздействие на работу слизистой оболочки желудка. А прием ее людям с пониженной кислотообразующей функцией желудка или анацидном состоянием его противопоказан, что неверно. Это доказано лабораторными исследованиями на кафедре физиологии человека и животных в Гомельском госуниверситете в 1982 г. ; о влиянии соды на кислотообразование, на работу слизистой желудка (на собаках с фистулами желудка). Опытным путем подтверждено, что питьевая сода, обладая кислотонейтрализующим действием, не оказывает ни возбуждающего, ни тормозящего влияния на кислотовыделительную функцию желудка. Следовательно, прием соды может быть рекомендован при любом состоянии кислотности желудка, в т.ч. при гастрите с пониженной кислотностью.
; о влиянии соды на кислотообразование, на работу слизистой желудка (на собаках с фистулами желудка). Опытным путем подтверждено, что питьевая сода, обладая кислотонейтрализующим действием, не оказывает ни возбуждающего, ни тормозящего влияния на кислотовыделительную функцию желудка. Следовательно, прием соды может быть рекомендован при любом состоянии кислотности желудка, в т.ч. при гастрите с пониженной кислотностью.
Сода с химической точки зрения представляет собой соединение катиона натрия и аниона гидрокарбоната, которое при введении в организм активно включается в коррекцию кислото-щелочного равновесия. Оказалось, что сода способна выравнивать кислотно-щелочное равновесие в организме, восстанавливать обмен веществ в клетках, улучшать усвоение кислорода тканями, а также препятствовать потере жизненно необходимого калия. Помогает сода при изжоге, при морской болезни, при простудах, при сердечных заболеваниях и головных болях, при кожных заболеваниях. При многих тяжелых заболеваниях в клетках и тканях организма наблюдается ацидоз (или закисление организма), недостаток катионов калия и избыток натрия, что приводит к подавлению энергетических биохимических обменных процессов в клетках (тормозится цикл Кребса), снижению усвоения кислорода, уменьшению жизнеспособности как каждой клетки, так и всего организма.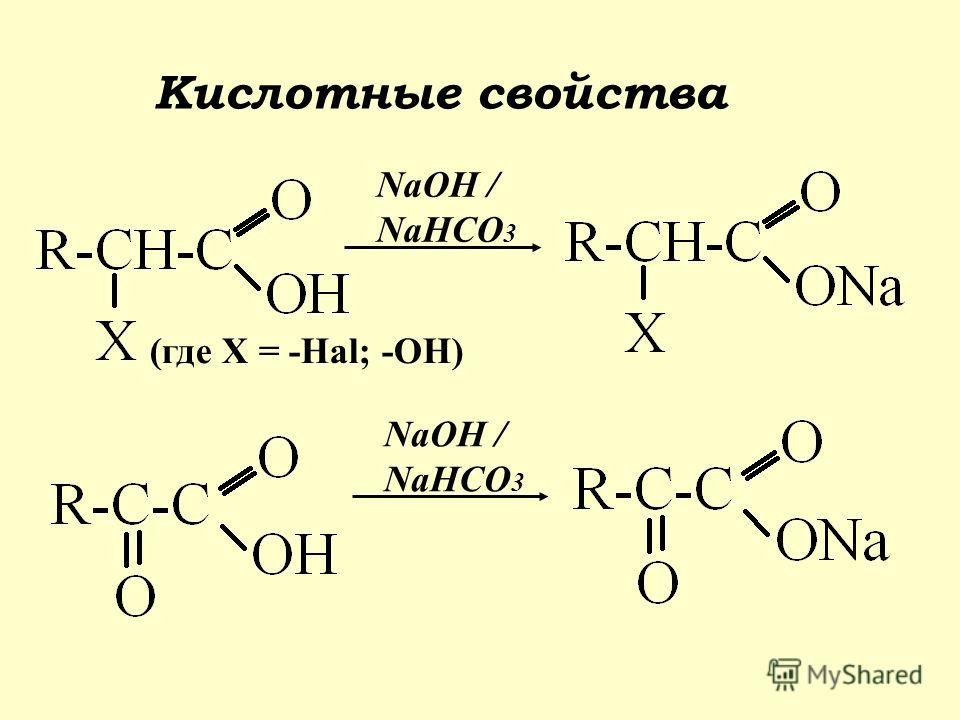 Положительное оздоравливающее действие соды уникально. Благодаря введению анионов угольной кислоты (НСО ) повышается щелочной резерв организма: анион угольной кислоты выводит через почки избыток анионов хлора и натрия, что приводит к уменьшению отеков, снижению повышенного давления, в результате чего повышается валентность тканевых буферных систем, что создает условие для вхождения катиона калия в клетки, и тем самым объясняется калийсберегающий эффект соды.
Положительное оздоравливающее действие соды уникально. Благодаря введению анионов угольной кислоты (НСО ) повышается щелочной резерв организма: анион угольной кислоты выводит через почки избыток анионов хлора и натрия, что приводит к уменьшению отеков, снижению повышенного давления, в результате чего повышается валентность тканевых буферных систем, что создает условие для вхождения катиона калия в клетки, и тем самым объясняется калийсберегающий эффект соды.
В результате в клетках восстанавливаются и повышаются биохимические и энергетические процессы,увеличивается гемодинамика и усвоение кислорода тканями, что приводит к улучшению самочувствия и трудоспособности.
К этим выводам пришли медики на кафедре терапии центрального института усовершенствования врачей в Москве (Я.П.Цаленчук,Г.П.Шульцев и др. Журнал «Терапевтический архив» N7 1976 г, N7 1978 г), которые изучали применение гидрокарбоната натрия при хроническом гломерулонефрите, пиелонефрите, хронической почечной недостаточности внутривенным и ректальным способами, что вызвало изменение в состоянии здоровья больных, увеличением кислотовыделительной функции почек, увеличением клубочковой фильтрации, снижением артериального давления, уменьшением остаточного азота в крови, уменьшением отеков.
При тяжелом шоке получены хорошие результаты лечения внутриартериальным введением раствора соды. В практике наблюдался случай быстрого и эффективного купирования отека легких с тяжелым течением инфаркта миокарда после внутривенного введения 4% р-ра соды 200,0.
Отмечено положительное действие соды при болезнях движения, или морской болезни. Гидрокарбонат натрия повышает устойчивость вестибулярного анализатора к действию угловых ускорений,угнетая вращательный и послевращательный нистагм (А.М.Сутов,И.Р.Веселов,»Космическая медицина и авиокосмическая медицина» N3 1978г).
Авторы статьи утверждают, что положительный эффект обусловлен повышением потребления кислорода тканями, нормализацией деятельности сердечно-сосудистой системы, повышением натрий- и хлоруреза. Установлено, что гидрокарбонат натрия обладает четким калийсберегающим свойством.
Проведено наблюдение за показаниями общего и биохимического анализа крови после трехмесячного приема соды с валерианом. Примечательно увеличение как общего количества лейкоцитов (белых клеток крови,имеющими непосредственную связь с тонким телом) на 1,4 10 /л, так и непосредственно лимфоцитов, отвечающим за состояние клеточного иммунитета, на 37%. Биохимический анализ показал возрастание электролитов (до приема соды показатели были несколько снижены), повышение уровня белка до верхних границ нормы (при отсутствии в пищевом рационе мясных и рыбных продуктов в течении 7 лет).
Биохимический анализ показал возрастание электролитов (до приема соды показатели были несколько снижены), повышение уровня белка до верхних границ нормы (при отсутствии в пищевом рационе мясных и рыбных продуктов в течении 7 лет).
Натрия гидрокарбонат | это… Что такое Натрия гидрокарбонат?
Гидрокарбонат натрия NaHCO3 (другие названия: питьевая сода, пищевая сода, бикарбонат натрия, натрий двууглекислый) — кристаллическая соль, однако чаще всего она встречается в виде порошка тонкого помола белого цвета.
Химическая формула
Содержание
|
Безопасность
Двууглекилый натрий не токсичен, пожаро- и взрывобезопасен.
Представляет собой мелкокристаллический порошок, который при попадании на слизистые оболочки вызывает раздражение. При постоянной работе в атмосфере, загрязненной пылью двууглекислого натрия, может возникнуть раздражение дыхательных путей.
Химические свойства
Гидрокарбонат натрия — кислая натриевая соль угольной кислоты.
Молекулярная масса (по международным атомным массам 1971 г.) — 84,00.[1]
Реакция с кислотами
Гидрокарбонат натрия реагирует с кислотами, с образованием соли и угольной кислоты, которая тут же распадается на углекислый газ и воду:
- NaHCO3 + HCl → NaCl + H2CO3
- H2CO3 → H2O + CO2↑
в кулинарии чаще встречается такая реакция с уксусной кислотой, с образованием ацетата натрия:
- NaHCO3 + CH3COOH → CH3COONa + H2O + CO2↑
Термическое разложение
При температуре 60 °C гидрокарбонат натрия распадается на карбонат натрия, углекислый газ и воду (процесс разложения наиболее эффективен при 200 °C):
- 2NaHCO3 → Na2CO3 + H2O + CO2↑
При дальнейшем нагревании до 1000 °C (например при тушении пожара порошковыми системами) полученный карбонат натрия распадается на углекислый газ и оксид натрия:
- Na2CO3 → Na2O + CO2
Применение
Гидрокарбонат натрия
Двууглекислый натрий (бикарбонат), применяется в химической, пищевой, легкой, медицинской, фармацевтической промышленности, цветной металлургии, поставляется в розничную торговлю.
Зарегистрирован в качестве пищевой добавки E500.
Применение:
- в химической промышленности — для производства красителей, пенопластов и других органических продуктов, фтористых реактивов, товаров бытовой химии, наполнителей в огнетушителях, для отделения двуокиси углерода, сероводорода из газовых смесей (газ поглощается в растворе гидрокарбоната при повышенном давлении и пониженной температуре, раствор восстанавливается при подогреве и пониженном давлении).
- в легкой промышленности — в производстве подошвенных резин и искусственных кож, кожевенном производстве (дубление и нейтрализация кож), текстильной промышленности (отделка шелковых и хлопчатобумажных тканей).
- в пищевой промышленности — хлебопечении, производстве кондитерских изделий, приготовлении напитков.
Cода пищевая, кулинарная
Кулинария
Основное применение питьевой соды — кулинария, где она применяется, преимущественно, в качестве основного или дополнительного разрыхлителя при выпечке (так как при нагревании выделяет углекислый газ), самостоятельно или в составе комплексных разрыхлителей (например, пекарского порошка, в смести с карбонатом аммония), например, в бисквитном и песочном тесте.
Медицина
Раствор питьевой соды используется в качестве слабого антисептика для полосканий, а также как традиционное кислотонейтрализующее средство от изжоги и болей в желудке (современная медицина не рекомендует применять из-за побочных эффектов, в том числе, из-за «кислотного рикошета») или для устранения ацидоза и т. п.
Пожаротушение
Гидрокарбонат натрия входит в состав порошка, применяемого в порошковых системах пожаротушения, утилизируя тепло и оттесняя кислород от очага горения выделяемым углекислым газом.
Производство
В РФ производят соду по ГОСТ 2156-76 «Натрий двууглекислый. Технические условия».[2]
Хранение
Хранить в закрытых упаковках, не допуская попадания влаги.
Гарантийный срок хранения натрия двууглекислого — 12 месяцев со дня изготовления.
Срок годности не ограничен.
См. также
- Карбонат натрия
- Пищевые добавки
Примечания
- ↑ 1
 Технические условия».[1]
Технические условия».[1]
Ссылки
- http://www.infrahim.ru/pfm/187.html
- http://www.uk-him.ru/rus/catalogue/3/43
Условие реакции NaHCO3 с образованием CO2 с органическими кислотами
спросил
Изменено 2 года, 8 месяцев назад
Просмотрено 37 тысяч раз
$\begingroup$
Мой профессор сказал нам следующее:
$\ce{NaHCO3}$ будет реагировать на эволюцию $\ce{CO2}$ всякий раз, когда кислотность реагента превышает кислая природа бензойной кислоты.
Я хочу знать, почему это так. И справедливо ли данное утверждение? Он не назвал нам причину. И в этом случае $\ce{NaHCO3}$ должен реагировать с 1,2-дигидрокси циклобутандиона для выделения углекислого газа?
- органическая химия
- кислотно-основная
$\endgroup$
$\begingroup$
$\ce{NaHCO3}$ является основной натриевой солью угольной кислоты, двухосновной кислоты, которая существует только в небольших количествах в водном растворе, так как равновесие
$$\ce{CO2 + h3O <=> h3CO3}$$
лежит в основном на стороне эдукта (по этой же причине наблюдается выделение $\ce{CO2}$).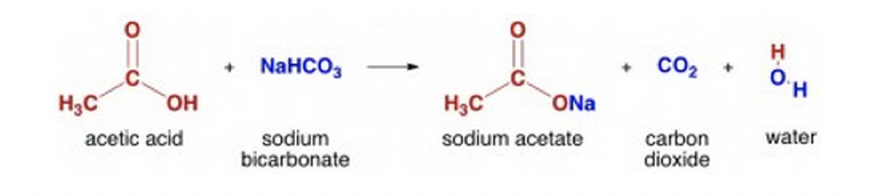 При учете этого факта для первой стадии протолиза (источник) получается значение $\ce{pK_{a}}$ 6,3 при 25 °C. Бензойная кислота имеет более низкое значение $\ce{pK_{a}}$, равное 4,19, и поэтому способна высвобождать угольную кислоту из своих солей, как и любая другая кислота, которая значительно сильнее, чем $\ce{h3CO3}$.
При учете этого факта для первой стадии протолиза (источник) получается значение $\ce{pK_{a}}$ 6,3 при 25 °C. Бензойная кислота имеет более низкое значение $\ce{pK_{a}}$, равное 4,19, и поэтому способна высвобождать угольную кислоту из своих солей, как и любая другая кислота, которая значительно сильнее, чем $\ce{h3CO3}$.
$$\ce{C6H5CO2H + NaHCO3 -> C6H5CO2Na + CO2 + h3O}$$
Если только Вы имеете в виду 3,4-Дигидроксициклобут-3-ен-1,2-дион, который также известен как скваровая кислота, то вероятна реакция с выделением $\ce{CO2}$. Квадратная кислота является довольно сильной двухосновной кислотой со значениями $\ce{pK_{a}}$ 1,5 и 3,4 соответственно. Кислотность может быть связана со стабилизацией дианиона резонансом:
Возможно ли выделение углекислого газа с 1,2-дигидроксициклобутандионом, зависит от значения $\ce{pK_{a}}$ этого соединения. Однако я ожидаю, что он будет менее кислым, чем квадратная кислота.
$\endgroup$
5
Зарегистрируйтесь или войдите в систему
Зарегистрируйтесь с помощью GoogleЗарегистрироваться через Facebook
Зарегистрируйтесь, используя электронную почту и пароль
Опубликовать как гость
Электронная почта
Требуется, но не отображается
Опубликовать как гость
Электронная почта
Требуется, но не отображается
Нажимая «Опубликовать свой ответ», вы соглашаетесь с нашими условиями обслуживания, политикой конфиденциальности и политикой использования файлов cookie
.
Что делает пищевая сода?
Пищевая сода может служить многим целям. Обладая слегка горьковатым и соленым вкусом, он в сочетании с разрыхлителем действует как разрыхлитель во многих хлебобулочных изделиях. Благодаря своему уникальному и сильнощелочному составу пищевая сода также может использоваться для очистки, дезодорации, косметических средств, средства от укусов насекомых, натурального ополаскивателя для рта, средства от сорняков и многого другого.
Каждый из нас хоть раз в жизни сталкивался с пищевой содой. Многоцелевое и многофункциональное природное химическое вещество, кажется, повсюду. В наших кладовых чистящие средства, холодильники и, конечно же, рецепты. Хотя пищевая сода широко известна и используется, многие до сих пор не знакомы с сутью того, что она делает, или в какой степени; надо в рецептах. Обычно используемую в качестве разрыхлителя в выпечке, пищевую соду часто путают с разрыхлителем, разрыхлителем. Какая разница между 9Пищевая сода 0077 против разрыхлителя ? Чтобы понять, как работает пищевая сода и почему она уникальна, мы должны понять, что такое пищевая сода на самом деле.
Какая разница между 9Пищевая сода 0077 против разрыхлителя ? Чтобы понять, как работает пищевая сода и почему она уникальна, мы должны понять, что такое пищевая сода на самом деле.
Пищевая сода, также известная как бикарбонат натрия, представляет собой встречающееся в природе кристаллическое химическое соединение, но часто встречается в виде порошка. Хотя пищевая сода встречается в природе, ее часто добывают и получают химическим путем. Большая часть пищевой соды, которая продается в Соединенных Штатах, производится из руды, добытой в Вайоминге. Руда нагревается до тех пор, пока не превратится в кальцинированную соду, а затем соединяется с углекислым газом для создания химической пищевой соды. При этом природная пищевая сода также все еще доступна и добывается в виде нахколита. Нахколит — это наиболее натуральная форма бикарбоната натрия, не содержащая химических добавок. Bob’s Red Mill с гордостью продает натуральная пищевая сода , не полученная химическим путем.
Пищевая сода очень универсальна и при использовании сама по себе или в сочетании с дополнительными соединениями может использоваться в качестве лечебного средства для различных целей. Пищевая сода, ценящаяся за свои очищающие и хлебопекарные свойства, использовалась на протяжении тысячелетий. Использование пищевой соды восходит к Древнему Египту, когда она использовалась в качестве очищающего и сушильного средства в процессе мумификации. Пищевая сода стала коммерчески доступной в середине 19 века.го века и с тех пор стал основным продуктом в большинстве домов, будь то чистящие средства, косметические товары или даже широкий спектр рецептов приготовления пищи и выпечки.
Как работает Пищевая сода ? Пищевая сода чаще всего используется в выпечке в качестве разрыхлителя, отсюда и ее название. До коммерциализации пищевой соды использовались биологические процессы разрыхления и ферментации, но они менее удобны из-за длительного периода времени, связанного с биологическим разрыхлением. Как многие уже узнали на уроках естествознания и экспериментальных мерах, когда основание встречается с кислым ингредиентом, таким как пахта, сметана или лимонный сок, происходит химическая реакция. Эта концепция одинакова для пищевой соды, поскольку она относится к выпечке. Когда пищевая сода смешивается с кислотой и жидкостью, она образует пузырьки углекислого газа, которые придают ей пушистую текстуру. При этом пищевая сода может реагировать без кислоты, если она нагревается выше 122 ° F или подвергается длительному воздействию тепла и влажности. Если пищевая сода хранится при разумных температурах (не выше 77°F и влажности 75%), она будет храниться неопределенно долго.
Как многие уже узнали на уроках естествознания и экспериментальных мерах, когда основание встречается с кислым ингредиентом, таким как пахта, сметана или лимонный сок, происходит химическая реакция. Эта концепция одинакова для пищевой соды, поскольку она относится к выпечке. Когда пищевая сода смешивается с кислотой и жидкостью, она образует пузырьки углекислого газа, которые придают ей пушистую текстуру. При этом пищевая сода может реагировать без кислоты, если она нагревается выше 122 ° F или подвергается длительному воздействию тепла и влажности. Если пищевая сода хранится при разумных температурах (не выше 77°F и влажности 75%), она будет храниться неопределенно долго.
Пищевая сода обычно используется в качестве активного ингредиента в рецептах быстрой выпечки, таких как печенье, кексы и блины. Это происходит из-за быстрой химической реакции, связанной с пищевой содой и кислотным аналогом. Когда пищевая сода смешивается с кислотой, выделяются пузырьки газа CO2, создавая «воздушный» эффект в кляре и тесте. Кроме того, как только тесто начнет выпекаться, углекислый газ начнет фильтроваться через тесто и расширять воздух, который находится внутри. Источники кислоты в сочетании с пищевой содой определят, можно ли хранить тесто в холодильнике или его нужно выпекать немедленно.
Кроме того, как только тесто начнет выпекаться, углекислый газ начнет фильтроваться через тесто и расширять воздух, который находится внутри. Источники кислоты в сочетании с пищевой содой определят, можно ли хранить тесто в холодильнике или его нужно выпекать немедленно.
Например, если источники кислоты сухие, такие как винный камень или какао-порошок, то они могут сохраняться дольше при добавлении пищевой соды. Однако, если кислоты влажные, такие как йогурт или лимонный сок, то полученное тесто нужно будет использовать незамедлительно. Пищевая сода также может придать тесту повышенный уровень pH, что создает повышенную щелочность. Из-за увеличения pH клейковина в тесте ослабевает, что создает нежную текстуру для печенья и выпечки по сравнению с чем-то более жевательным, например, хлебом. Количество является важным компонентом, учитывая влияние пищевой соды на рецепты выпечки.
Пищевая сода для домашнего использования Пищевая сода является универсальным продуктом, который сам по себе или в сочетании с другими продуктами используется во многих бытовых целях. Из-за своей грубой солевой природы пищевая сода может использоваться в качестве своего рода скраба для фруктов и овощей, грилей, столешниц и даже зубов. Пищевая сода, обычно добавляемая во многие виды зубной пасты, является натуральным чистящим средством. Пищевая сода широко используется в качестве своего рода дезодоранта для холодильника, потому что некоторые считают, что она нейтрализует стойкий запах. Химически пищевая сода реагирует аналогичным образом, когда она используется в рецептах выпечки, таких как кексы и булочки, как и с запахами. Это связано с тем, что пищевая сода является щелочной, а большинство запахов кислотными, и это обеспечивает аналогичную атмосферу для протекания нейтрализующей реакции.
Из-за своей грубой солевой природы пищевая сода может использоваться в качестве своего рода скраба для фруктов и овощей, грилей, столешниц и даже зубов. Пищевая сода, обычно добавляемая во многие виды зубной пасты, является натуральным чистящим средством. Пищевая сода широко используется в качестве своего рода дезодоранта для холодильника, потому что некоторые считают, что она нейтрализует стойкий запах. Химически пищевая сода реагирует аналогичным образом, когда она используется в рецептах выпечки, таких как кексы и булочки, как и с запахами. Это связано с тем, что пищевая сода является щелочной, а большинство запахов кислотными, и это обеспечивает аналогичную атмосферу для протекания нейтрализующей реакции.
Пищевая сода и уксус являются не только соучастниками в выпечке, но и отличными помощниками в уборке благодаря своему химическому составу. При комбинировании в рецептах выпечки пищевая сода и уксус (или кислота) гармонично работают вместе, создавая процесс разрыхления жидкого теста и теста. Точно так же при смешивании пищевой соды и уксуса для очистки создается абразивная среда, устойчивая к пятнам, грязи и забитым стокам. Как упоминалось ранее, когда пищевая сода нагревается выше 122 ° F, она создает углекислый газ. Вот что делает пищевую соду отличным огнетушителем и почему она остается одним из лучших способов потушить возгорание жира. Увеличение содержания углекислого газа отрезает источник кислорода для огня, создавая среду, которая не является устойчивой для огня.
Точно так же при смешивании пищевой соды и уксуса для очистки создается абразивная среда, устойчивая к пятнам, грязи и забитым стокам. Как упоминалось ранее, когда пищевая сода нагревается выше 122 ° F, она создает углекислый газ. Вот что делает пищевую соду отличным огнетушителем и почему она остается одним из лучших способов потушить возгорание жира. Увеличение содержания углекислого газа отрезает источник кислорода для огня, создавая среду, которая не является устойчивой для огня.
Как и пищевая сода, разрыхлитель используется в рецептах быстрой выпечки. Часто путают и ошибочно принимают друг за друга, эти два ингредиента по-разному взаимодействуют в рецептах и сильно различаются по составу. При изучении рецептов выпечки важно учитывать различия между пищевой содой и разрыхлителем. Как упоминалось ранее, пищевая сода является разрыхлителем, который при смешивании с кислотой и жидкостью активируется и образует пузырьки CO2. Точно так же разрыхлитель является разрыхлителем, который производит пузырьки CO2. Тем не менее, состав является одним из основных отличий.
Точно так же разрыхлитель является разрыхлителем, который производит пузырьки CO2. Тем не менее, состав является одним из основных отличий.
Разрыхлитель состоит из самой пищевой соды в сочетании с другой сухой кислотой, такой как винный камень. В результате разрыхлитель может быть одинарного или двойного действия. Разрыхлитель одностороннего действия действует так же, как пищевая сода, смешанная с кислотой. Он быстро высвобождает CO2 и создает процесс разрыхления, которым нужно быстро воспользоваться. Однако разрыхлитель двойного действия можно активировать дважды разными способами. Как только жидкость добавляется к разрыхлителю, он активируется и производит пузырьки CO2.
В дополнение к первой активации существует вторичная активация, которая может иметь место, когда раствор или тесто подвергается воздействию тепла (помещается в духовку). Это также создает возможность длительного периода времени, которого нет в реакции, вызванной пищевой содой и кислотой. Это означает, что поскольку разрыхлитель активируется жидкостью и уже содержит сухой кислотный компонент (винный камень), его можно дольше хранить в холодильнике. Вот почему такие продукты, как тесто для печенья, могут оставаться в холодильнике, а тесто для тортов нужно готовить быстро.
Вот почему такие продукты, как тесто для печенья, могут оставаться в холодильнике, а тесто для тортов нужно готовить быстро.


 Поверхность Земли покрыта содой на широкое употребление»
Поверхность Земли покрыта содой на широкое употребление» Технические условия».[1]
Технические условия».[1]