Разложение гипохлорита натрия
Разложение гипохлорита натрия
•Разложение гипохлорита натрия увеличивается за счет:•1. Повышения температуры (удваивается при подъеме температуры на каждые 5С)•2. Воздействие света•3. Снижения рН ниже 11•4. Наличия тяжелых металлов (железо, марганец, никель, кольбат).•При правильном складировании (внешняя температура +20С) и без растворения гипохлорита натрия концентрация активного хлора снижается:•1. При температуре +20С•2. Примерно 0,7% / неделя•3. При температуре от +5С до +10С примерно 0,3% / неделя•Разложение разбавленных растворов гипохлорита натрия происходит медленнее, при наличии в растворах гидроксида натрия с концентрацией не менее 5-10 г/л. (См. таблицу справа)•Реакции разложения:•3NaClO –2NaCl + NaClO3: содержащийся в гипохлорите натрия активный хлор переходит в хлорат.
| Температура С | Исходная концентрация активного хлора | Средняя концентрация (гр./л) после складирования на защищенном от света месте | |||||
| гр./л | 1 неделя | 2 неделя | 4 неделя | 6 месяцев | 1год | ||
| 30 | 200 | 156 | 128 | 94 | 24 | 13 | |
| 185 | 151 | 128 | 97 | 27 | 15 | ||
| 160 | 139 | 123 | 100 | 32 | 18 | ||
| 120 | 112 | 104 | 92 | 40 | 24 | ||
| 25 | 200 | 175 | 155 | 127 | 42 | 24 | |
| 185 | 166 | 151 | 127 | 47 | 27 | ||
| 160 | 149 | 139 | 123 | 54 | 33 | ||
| 120 | 116 | 131 | 106 | 64 | 44 | ||
| 20 | 200 | 187 | 175 | 155 | 69 | 42 | |
| 185 | 175 | 166 | 151 | 75 | 47 | ||
| 160 |
155 | 150 | 141 | 85 | 58 | ||
| 120 | 118 | 116 | 113 | 84 | 64 | ||
| 15 | 200 | 193 | 187 | 176 | 105 | 71 | |
| 185 | 180 | 176 | 167 | 109 | 78 | ||
| 160 | 157 | 155 | 150 | 111 | 85 | ||
| 120 | 119 | 118 | 116 | 100 | 86 | ||
| 10 | 200 | 197 | 193 | 187 | 139 | 106 | |
| 185 | 183 | 176 | 139 | 111 | |||
| 160 | 158 | 157 | 154 | 126 | 104 | ||
| 120 | 120 | 119 | 118 | 110 | 102 | ||
Разложение — гипохлорит — натрий
Cтраница 1
Разложение гипохлорита натрия приводит к загрязнению и зашламлению раствора. [1]
[1]
В процессе разложения гипохлорита натрия раствор обогащается хлоридом натрия. В табл. 4.1 представлены данные по совместной растворимости NaCIO и NaCl в водных растворах. [2]
Для улавливания абгазов на стадии разложения гипохлорита натрия установлена титановая колонна, успешно работающая более 5 лет. Используемая ранее гуммированная колонна подвергалась через 4 — 6 месяцев ремонтам. [3]
В растворах, полученных путем активации хлором, содержание активного хлора постепенно уменьшается вследствие разложения гипохлорита натрия. [4]
Среди гидроокислов марганца, кобальта и меди образованные ими бинарные системы обладают следующими каталитическими свойствами в реакции разложения гипохлорита натрия. Система Со — Мп крайне малоактивна. [5]
Хлорит натрия каталитически устойчив, он не разлагается под действием железа, меди и их соединений, которые являются катализаторами [6]
[6]
Скорость разложения гипохлорита натрия зависит от температуры. При отсутствии примесей щелочные растворы гипохлорита натрия при низких температурах достаточно стабильны и могут храниться длительное время. Растворы, получаемые электролизом нейтральных растворов хлорида натрия или морской воды, стабилизируют введением гидрокарбоната ( до 10 кг / м3) или гидроксида натрия. [7]
Смешанные катализаторы состоят из компонентов, каждый из которых обладает каталитической активностью к данной реакции. Они могут существенно отличаться по каталитической активности от компонентов в чистом состоянии. Например, реакция разложения гипохлорита натрия на хлорид и хлорат натрия в водном растворе катализируется одной из гидроокисей никеля, меди и железа. При этом скорость реакции равна ( в условных единицах) 700, 100 и 100 соответственно. При применении смешанного катализатора, содержащего 70 % гидроокиси никеля и по 15 % гидроокисей меди и железа, скорость реакции повышается до 1200 условных единиц.
Особое внимание следует обратить на материал оборудования. Оно может изготовляться из стекла, поливинилхлорида, фарфора, слоистого стеклянного волокна, глазурованной керамики, гуммированной стали или титана. Следы меди, никеля, железа, хрома, кобальта и марганца в растворе катализируют процесс разложения гипохлорита натрия, поэтому необходимо избегать материалов, содержащих эти металлы. Змеевики для хлорирования предпочтительно изготовлять из стекла, хотя для работы в течение ограниченного времени вполне приемлемы трубы из твердого поливинилхлорида. [9]
| Диаграмма активности смешанных катализаторов из гидроокисей никеля ( А, меди ( В и железа ( С. [10] |
Смешанные катализаторы могут существенно отличаться по каталитической активности от своих компонентов в чистом состоянии и, в частности, значительно превосходить каждый из них. Зависимость активности смешанного катализатора от относительного содержания компонентов может быть самой различной. На рис. 252 приведена диаграмма активности смешанных катализаторов из гидроокисей никеля, меди и железа по отношению к реакции разложения гипохлорита натрия в водном растворе.
[11]
На рис. 252 приведена диаграмма активности смешанных катализаторов из гидроокисей никеля, меди и железа по отношению к реакции разложения гипохлорита натрия в водном растворе.
[11]
Электролитическое получение раствора гипохлорита натрия осуществляют электролизом раствора поваренной соли в ваннах без диафрагмы. При этом хлор, выделяющийся на аноде, реагирует с едким натром, образующимся на катоде. Во избежание образования хлората натрия вследствие окисления на аноде ионов СЮ — по мере их накопления, электролиз ведут в условиях минимального перенапряжения при выделении хлора и низкой концентрации ионов С1О — в прианодном электролите. Для уменьшения скорости разложения гипохлорита натрия процесс ведут при 20 — 25, охлаждая циркулирующий раствор электролита. [12]
Важное значение имеет чистота исходного электролита, так как наличие примесей приводит к нарушению катодного и анодного процессов. Примеси солей кальция и магния образуют на катоде плотные осадки, что приводит к росту напряжения. Предложены 388, 389 ] добавки комплексообразующих агентов, предотвращающих осаждение щелочноземельных металлов на катоде. Наличие в электролите примесей железа, кобальта, никеля в количестве 1 — 2 мг / дм3 ускоряет процесс разложения гипохлорита натрия с выделением кислорода.
[13]
Предложены 388, 389 ] добавки комплексообразующих агентов, предотвращающих осаждение щелочноземельных металлов на катоде. Наличие в электролите примесей железа, кобальта, никеля в количестве 1 — 2 мг / дм3 ускоряет процесс разложения гипохлорита натрия с выделением кислорода.
[13]
Страницы: 1
Регистрационное досье — ECHA
В концентрированных растворах гипохлорита натрия содержание доступного хлора снижается, так как NaClO стремится к непропорциональны ионам хлора и хлора:
Реакция:
3 NaClO => 2 NaCl + NaClO3 Кэкв = 1027
Это результат двух реакций: медленной с с образованием хлорита и быстрый с образованием хлората реакция между хлоритом и гипохлоритом.
2 NaClO => NaClO2 + NaCl (медленная реакция)
NaClO + NaClO2 => NaClO3 + NaCl (быстрая реакция)
Первая реакция (производящая хлорит) контролирует
скорость реакции с образованием хлората. Скорость образования хлората, при
комнатной температуре и рН = 11, очень медленно. Процесс зависит от
время, температура, примеси, pH и концентрация натрия
раствор гипохлорита. Также свет может разлагать растворы гипохлорита.
Скорость образования хлората, при
комнатной температуре и рН = 11, очень медленно. Процесс зависит от
время, температура, примеси, pH и концентрация натрия
раствор гипохлорита. Также свет может разлагать растворы гипохлорита.
Зависимость от времени
При постоянной температуре обратный активному продукту концентрация является линейной функцией времени. Раствор с дозировкой 150 г/л доступного хлора, хранящегося вдали от солнечного света и при постоянном 15°C, теряет 1/6 своей концентрации менее чем за 3 месяца. В разбавленными растворами гипохлорита потери незначительны.
Зависимость от pH
Гипохлорит нельзя добавлять в небуферизованную среду. потому что при низком рН могут протекать следующие вторичные реакции:
В кислой среде при pH 4 гипохлорит трансформируется к газообразному хлору.
HOCl + H+ + Cl- => Cl2 + h3O
Между pH 4 и 11 присутствуют как ClO-, так и HOCl. последний гораздо более активен. Этот рН будет получен, когда все
гидроксид натрия, присутствующий в
последний гораздо более активен. Этот рН будет получен, когда все
гидроксид натрия, присутствующий в
раствор гипохлорита газирован (см. главу 1.2). Разложение HOCl происходит быстрее, чем разложение ClO-.
если pH < 6, то основная реакция: 2HClO => 2HCl + O2
если pH >6, то основная реакция: 3 NaClO => NaClO3 + 2 NaCl
Хлорноватистая кислота (HClO) очень нестабильна и внезапно разлагается с образованием кислорода:
2 HOCl => 2 НСl + O2
Зависимость от примесей
Гипохлорит натрия может разлагаться до кислорода согласно следующая реакция:
2 NaClO => 2 NaCl + O2
Реакция разложения является бимолекулярной и требует энергии активации 113,3 кДж/моль (26,6 ккал/моль). Несмотря на то что происходит медленнее, чем образование хлората
реакция катализируется следовыми количествами металлических
примеси.
Наиболее сильными катализаторами разложения до кислорода являются: Co, никель и медь; тогда как Fe и Mn являются более слабыми катализаторами. Избегать разложение технического гипохлорита
растворов, эти металлы должны быть восстановлены настолько, насколько возможный. Как правило, их удаление происходит механически путем фильтрации. так как их растворимость снижается во время
Стадия производства гипохлорита.
Соли, такие как хлорид натрия, карбонат натрия и хлорат натрия очень слабо влияет на скорость реакции в диапазон концентраций, в котором они находятся
обычно присутствует. Их влияние на скорость реакции заметны только в некоторых частных случаях (например, разбавленный раствор натрия высокого качества Гипохлорит, в котором содержание NaCl сильно снижено из-за конкретный производственный процесс).
Гидроксид натрия не влияет на скорость реакции, если
его концентрация превышает 10-3 М (0,04 г/л).
Зависимость от света
Раствор гипохлорита натрия очень чувствителен к легкий. Прямые солнечные лучи могут вызвать перегруппировку и разложение что приводит к образованию хлората и кислорода. Наличие изоциануровая кислота в растворе значительно снижает эту чувствительность.
Температурная зависимость
Влияние температуры очень велико: скорость разложения удваивается при повышении температуры на ~ 5,5°С. Если температура выше 35°С,
реакции разложения протекают очень быстро:
3NaClO => NaClO3 + 2NaCl
В любом случае температура раствора должна быть ниже 55°C, чтобы предотвратить внезапное разложение гипохлорит.
Более стабильными являются растворы с низким содержанием гипохлорита.
концентрации, с pH 11 и низким содержанием железа, меди и никеля,
хранить в темноте при низкой температуре.
Фотолиз в воде
Период полураспада водного хлора при фотолизе
до летнего полудня при ясном небе (47° с.ш.) при рН 8 составляет 12 мин, когда
измеряется на поверхности. Период полувыведения увеличивается с уменьшением рН из-за
к уменьшающемуся соотношению OCl — /HOCl до 60 мин при pH 5.
константа скорости псевдопервого порядка для фотолиза HOCl становится 2 x
10 -4 с -1 и OCl — 1,2 x 10 -3 с -1 рассчитано изменение скорости фотолиза с глубиной для воды
колонки с разным коэффициентом светопоглощения.
с учетом того, что как для HOCl, так и для OCl — наиболее эффективным
Длина волны для фотолиза на солнечном свете составляет ок. 330 нм. Эти результаты
показать, что при очистке воды фотолиз хлора должен быть сведен к минимуму
по возможности, работая при низком pH, защищая от солнца или в ночное время. добавление хлора или избегание хранения в неглубоких резервуарах. Оценка
фотолиза хлора контролирует образование радикала ОН, который действует
как вторичный высокореактивный фотооксидант.
добавление хлора или избегание хранения в неглубоких резервуарах. Оценка
фотолиза хлора контролирует образование радикала ОН, который действует
как вторичный высокореактивный фотооксидант.
При УФ-облучении (255 нм) и HOCl, и OCl- фотолизуются. со сравнимыми скоростями и достаточно медленно, чтобы не произошло истощение запасов хлора. происходят во время облучения, типичного для УФ-дезинфекции.
Фотолиз также может способствовать истощению хлора в атмосферных водах всякий раз, когда хлор образуется (медленно) озонирование хлора.
Раствор гипохлорита натрия | Caffaro Brescia S.r.l.
Применение раствора гипохлорита натрия требует хорошего знания вещества с химической и физической точек зрения. Представленная здесь информация представляет собой простой справочник по раствору гипохлорита натрия и адресована конечным пользователям для правильного использования продукта.
Реакция синтеза Химическая реакция получения раствора гипохлорита натрия следующая:
Ниже описан упрощенный процесс».
Гипохлорит является химическим источником «активного хлора» или доступного хлора, фактически, когда он диссоциирует в анионном состоянии как ClO —, он оказывает окислительное действие, переходя в восстановленное состояние в виде хлорида.
Химическая стабильность и качество продукта сильная корреляция Раствор гипохлорита натрия обладает химической стабильностью (сроком хранения), которая зависит от многих различных химических и физических факторов. Свободное остаточное содержание NaOH, возникающее в процессе производства, очень важно, так как качество сырья, такого как газообразный хлор и гидроксид натрия. Фактически, сырье высокой чистоты дает конечный продукт высокого качества. Caffaro Brescia в своем собственном промышленном процессе использует чистый газообразный хлор, который получается в результате двухэтапного химического процесса: один из кислотообразования, а второй — очистка путем отпарки, которая удаляет все примеси.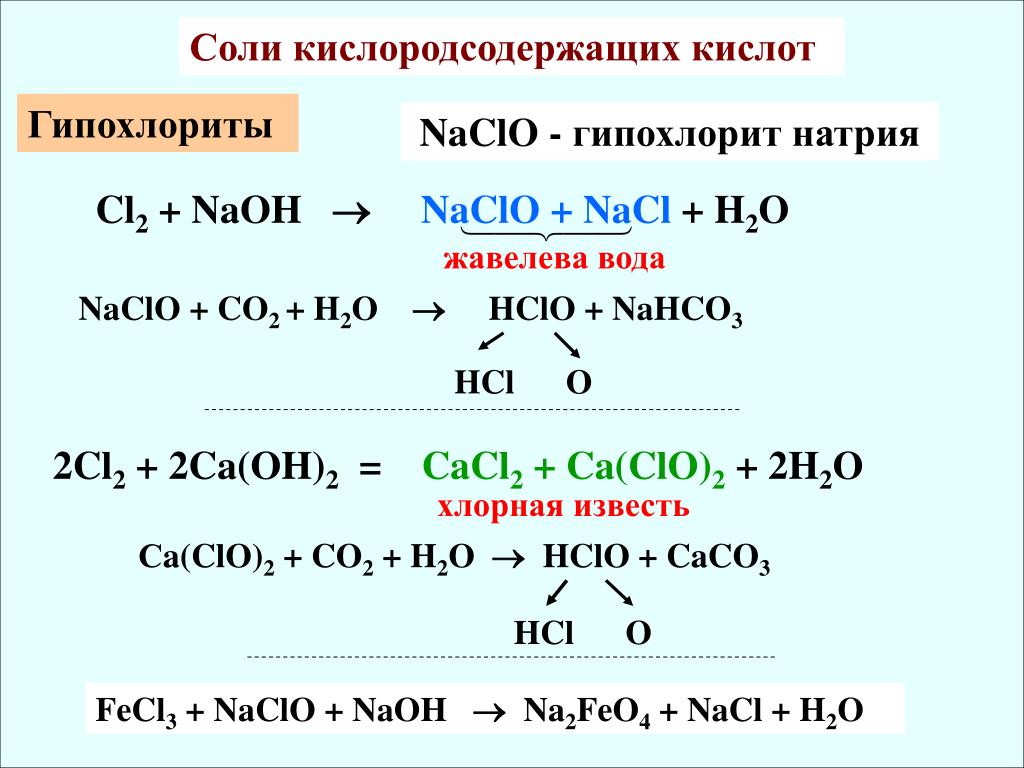 Отобранное и проверенное качество гидроксида натрия и использование воды, очищенной обратным осмосом, дополняют качество промышленного процесса производства раствора гипохлорита натрия.
Отобранное и проверенное качество гидроксида натрия и использование воды, очищенной обратным осмосом, дополняют качество промышленного процесса производства раствора гипохлорита натрия.
В любом случае раствор гипохлорита натрия может со временем разлагаться, даже при медленной кинетике реакции, в соответствии с двумя следующими реакциями:
2NaClO → 2NaCl + O
2 (реакция A)3NaClO → 2 NaCl + NaClO 3 (реакция В)
Хорошо известно, что в качественных продуктах основной реакцией разложения является реакция В, на долю которой приходится более 80% .
Причины, вызывающие эту реакцию разложения даже в высококачественном гипохлорите натрия, часто присутствуют в непростых условиях контроля. Например, прямой солнечный свет способствует этим реакциям, но наиболее важной переменной является температура, которая, как известно, увеличивает скорость химической реакции.
Принимая во внимание раствор гипохлорита натрия с активным содержанием 160 г/л (продукт, широко доступный на химическом рынке), реакция разложения активна уже при 10°C, и определена скорость около минус 0, 1 г/л (время 12 ч), может повышаться до минус 1,5 г/л (12 ч).
Следующий график дает четкое представление этого процесса разложения, подчеркивая термодинамический аспект реакции. Это означает, что более высокое начальное активное содержание соответствует более высокой скорости реакции разложения.
Registration number ( REACh ) 01-2119488154-34-0028
CAS number 7681-52-9
EINCS number 231-668-3
Classification :
Применение и использование:
- Производство
- Состав
- Промышленное использование в качестве промежуточного продукта
- Промышленное использование в текстильной промышленности
- Промышленное использование для очистки сточных вод, воды для охлаждения и отопления
- Промышленное использование в бумажной промышленности
- Промышленное использование в качестве чистящего средства
- Профессиональное использование в качестве чистящего средства
- Конечные потребители используют
Caffaro Brescia S. r.l. в сотрудничестве с Еврогруппой по регистрации гипохлорита натрия и хлора по биоцидам уведомила гипохлорит натрия (CAS № 7681-52-9; EC № 231-668-3) в качестве активного вещества в соответствии с BPD, как того требует Директива по биоцидам 98/8. /EC (теперь заменено B.P.R. – Правилами о биоцидных продуктах) для следующих PT (Тип продукта):
r.l. в сотрудничестве с Еврогруппой по регистрации гипохлорита натрия и хлора по биоцидам уведомила гипохлорит натрия (CAS № 7681-52-9; EC № 231-668-3) в качестве активного вещества в соответствии с BPD, как того требует Директива по биоцидам 98/8. /EC (теперь заменено B.P.R. – Правилами о биоцидных продуктах) для следующих PT (Тип продукта):
- PT 1: Биоцидные средства гигиены человека
- PT 2: Дезинфицирующие средства для частных и общественных помещений и другие биоцидные продукты
- PT 3: Биоцидные продукты для ветеринарной гигиены
- PT 4: Дезинфицирующие средства для пищевых продуктов и мест кормления
- PT 5: Дезинфицирующие средства для питьевой воды
- PT 11: Консерванты для систем жидкостного охлаждения и обработки
- PT 12: Слимициды
Применение
Здесь показана химическая структура гипохлорита натрия:
Химия хлора в воде, при очистке воды, учитывая требуемые диапазоны pH и дозировки, эквивалентна химии гипохлорита. На самом деле гипохлорит в виде водного раствора соли натрия предпочтительнее хлора из-за простоты и легкости использования, а также во избежание проблем с безопасностью, связанных с обращением, транспортировкой и хранением газообразного хлора. Следовательно, гипохлорит является химическим источником «активного хлора» или доступного хлора, фактически, когда он диссоциирует в анионном состоянии в виде ClO-, он оказывает окислительное действие, переходя в восстановленное состояние в виде хлорида. Поведение химической реакции для этой диссоциации состоит из двух стадий. Диспропорция хлора в воде происходит с образованием соляной и хлорноватистой кислот (1):
На самом деле гипохлорит в виде водного раствора соли натрия предпочтительнее хлора из-за простоты и легкости использования, а также во избежание проблем с безопасностью, связанных с обращением, транспортировкой и хранением газообразного хлора. Следовательно, гипохлорит является химическим источником «активного хлора» или доступного хлора, фактически, когда он диссоциирует в анионном состоянии в виде ClO-, он оказывает окислительное действие, переходя в восстановленное состояние в виде хлорида. Поведение химической реакции для этой диссоциации состоит из двух стадий. Диспропорция хлора в воде происходит с образованием соляной и хлорноватистой кислот (1):
Cl
2 + H 2 O → HClO + H + + Cl (1) В растворах с pH >3 реакция поглощения и диссоциации полностью сдвинута вправо с минимальной остаточной концентрацией молекулярный хлор.
Вместо этого хлорноватистая кислота, образующаяся в результате гидролиза хлора, представляет собой слабую кислоту, которая диссоциирует в воде в соответствии со следующей реакцией (2):
(хлорноватистая кислота) HClO ↔ H
+ + ClO- (гипохлорит-анион) (2) С константой равновесия K a равной 3,2 * 10 -8 (при 25 °C).
