Растворимость в воде алюминия — Справочник химика 21
Растворимость осадка. Растворимость оксихинолината алюминия в воде чрезвычайно мала. Произведение растворимости составляет [c.184]Безводный хлористый алюминий на воздухе дымит, выделяя небольшие количества хлористого водорода, в очень разбавленных водных растворах он в значительной степени гидролизуется. Растворимость хлористого алюминия в воде при 15 °С составляет 41,13%. Плотность растворов различной концентрации [c.516]
Растворимость хлорида алюминия в воде уменьшается при добавлении НС1. Растворимость при 25° С составляет [761] [c.15]
Гидролиз солей металлов. В большинстве случаев коагулянты представляют собой соли слабых оснований и сильных кислот. При растворении их в воде происходит гидролиз и образуются малорастворимые основания — гидроксиды алюминия или железа. При этом в результате смещения равновесия диссоциации в воде накапливаются ионы водорода и в растворе появляется кислота. Растворимость гидроксидов алюминия и железа чрезвычайно мала. Они выделяются из раствора, образуя сначала коллоидные частицы (разбавленные золи гидроксидов), которые иод влиянием электролитов, растворенных в воде, коагулируют и выпадают вместе с коллоидами, загрязняющими воду, в осадок. Этот осадок содержит связанную воду, а также несколько слоев молекул неструктурной воды, ад-сорбционно связанной с поверхностью осадка силами различной прочности [11].
Растворимость нитрата алюминия при 30° С составляет 81 г соли в 100 г воды. Сколько кристаллогидрата А1 (КОз)з ЭНгО можно растворить при указанной температуре в том же количестве воды [c.73]
Растворимость хлорида алюминия в воде [c.86]
Деформируемые алюминиевые сплавы, упрочняемые термической обработкой, легируются элементами, обладающими ограниченной растворимостью в алюминии в твердом состоянии, уменьшающейся при понижении температуры. Термическая обработка деформируемых алюминиевых сплавов заключается в закалке с последующим старением. Старение может быть естественным при комнатной температуре или искусственным при 150— 200°С. Закалка проводится нагревом до температуры, обеспечивающей полное растворение легирующего элемента и образование однородного твердого раствора с последующим охлаждением в воде. В результате закалки фиксируется при комнатной температуре пересыщенный твердый раствор, однако прочность сплава непосредственно после закалки остается низкой. В результате старения закаленного сплава при комнатной или [c.47]
Рис, 3.7. Зависимость растворимости оксида алюминия в воде от pH (по данным [65]). [c.262]
Гидратированные ионы алюминия в процессе гидролиза отдают протон от координированной молекулы воды, образуя последовательно комплексные ионы [А1 (Н2О) 5 (ОН) ] и [Л1 (Н2О)4 (ОН)2] остающиеся в растворе. Когда последний нейтральный комплекс [А1(Н20)з(0Н)з] теряет воду, образуется плохо растворимый гидроксид алюминия. Ступенчато гидролизуются и соли железа(ИI). Но, в отличие от солей алюминия, помимо гидроксидов железа могут образовываться и труднорастворимые гидроксосоли.
Изучение влияния анионного и катионного состава минеральных примесей воды на процесс растворения алюминиевого анода и выход алюминия по току показало [70], что в присутствии ионов СГ алюминиевый анод находится в активном состоянии и наряду с электрохимическим растворением алюминия идет процесс его химического растворения. Кроме того, ионы хлора, проявляя себя как специфические депассиваторы, препятствуют образованию кислородного барьера и не пассивируют анод в связи с высокой растворимостью хлорида алюминия. Сульфат- и особенно бикарбонат-ионы в некоторой степени тормозят процесс анодного растворения алюминия и уменьшают активирующее действие СГ-ионов. С целью обеспечения надежной, длительной и бесперебойной работы электролизеров рекомендуется введение в воду до 20% хлористых солей от общего количества анионов (считая в миллиграмм-эквивалентах на 1л). Катионный состав минеральных примесей воды на процесс растворения алюминиевого анода значительного влияния не оказывает. [c.155]
Сопоставление величины произведения растворимости купфероната циркония (2,35-10 ) и найденного Пятницким [239] произведения растворимости купфероната алюминия (2,3-10″ ) показывает, что легко могут быть найдены условия количественного разделения этих элементов при помощи купферона. Вычисленная по найденному значению произведения растворимости растворимость купфероната циркония в воде составляет (в моль л) [c.57]
При температуре выше комнатной метиловый спирт реагирует с алюминием, образуя растворимый метилат алюминия [12]. В технически чистом метаноле на поверхности алюминия наблюдается неглубокая точечная коррозия. Добавка воды к безводному чистому метиловому спирту резко снижает его агрессивность.
Д. Растворимые ультрафильтры. Исследуемая вода пропускается через растворимый фильтр (алюминий-альгинатное желе), концентрирующий вирусы. Далее фильтр растворяют в 3,8% растворе цитрата натрия и взвесь, содержащую вирусы, засевают в культуру ткани [22]. [c.281]
Растворимость сульфата алюминия составляет при 20° С 362 г/л. Этот коагулянт применяется для осветления и обесцвечивания воды. Плотность образующихся хлопьев гидроксида алюминия 2,4. При отсутствии щелочного резерва в воде сульфат алюминия вызывает резкое снижение pH (до 4,5) и вода становится агрессивной по отнощению к железу и бетону. [c.131]
Растворимость сернокислого алюминия в воде составляет 46 56 и 66% при температуре соответственно О, 30 и 50° С. [c.73]
Гидроокись алюминия малорастворима в воде в 1 л растворяется 7,5-10 г-мол гидроокиси алюминия (ПР = 5,1 -10 ). Однако растворимость гидроокиси алюминия в значительной степени зависит от концентрации ионов водорода. [c.109]
Сжатый пропилен конденсируется в конденсаторе 9, охлаждаемом водой. Содержащиеся в пропилене пары воды также конденсируются и, поскольку растворимость воды в жидком пропилене ниже, чем ее содержание в газообразном пропилене, часть воды отделяется и выводится из системы. Жидкий пропилен поступает в аппарат 10, заполненный активной окисью алюминия или цеолитами, где осушается до остаточной влажности 3—10 млн . Аппараты 10, их обычно бывает три, работают периодически. После насыщения адсорбента влагой аппарат переключается на десорбцию воды, которая производится продувкой горячего инертного газа (обычно азота). Температура регенерации для активной окиси алюминия 180—200 °С, для цеолитов выше. Последние имеют более высокую степень поглощения воды и потому более эффективны. [c.210]
Концентрация насыщенного раствора гидроксида алюминия в воде при 20° равна 1,855-Ю моль/л. Чему равно значение произведения растворимости гидроксида алюминия при этой температуре
Минимальную растворимость гидроокись алюминия имеет в интервале pH 6,5 — 8, при больших значениях pH гидроокись начинает растворяться, при pH Таким образом, одним из условий успешной коагуляции природной воды является оптимальная величина pH, равная 6,5 — 8 для Al(OH)j для хлорного железа и других железосодержащих коагулянтов величина pH уменьшается. При нарушении оптимальных пределов величины pH происходит ухудшение коагуляции или необходимо увеличение дозы коагулянта. [c.51]
Количество осушителя, необходимое для обезвоживания определенного объема жидкости, рассчитывают исходя из начального содержания воды в растворителе и влагопоглощающей способности твердого поглотителя. Практически рекомендуется брать осушитель с двух-, а иногда даже трехкратным избытком. Пусть, например, необходимо высушить 1 л товарного диэтилового эфира оксидом алюминия. Поскольку растворимость воды в эфире при 20 °С составляет около 1,2%, а прокаленный оксид алюминия поглощает примерно 20% воды по отношению к своей массе, расчетное количество адсорбента для осушки 1 л эфира составит 60 г. Практически следует взять 120—150 г оксида алюминия, причем разделить это количество на две равные части. С первой порцией эфир встряхивают около часа, после чего его осторожно сливают, добавляют вторую порцию и оставляют над ней на ночь. Эфир после такой обработки будет содержать не более 0,01% (масс.) воды, а если выдерл[c.166]
В разбавленной кислоте растворимость АЬ(804)3 выше, чем в чистой воде, но с дальнейшим увеличением концентрации Нг804 растворимость резко понижается, достигая 1 % в 60 %-ной серной кислоте. В более крепкой кислоте растворимость сульфата алюминия опять повышается. [c.44]
Известно несколько методов понижения адсорбционной активности. Центры адсорбции дезактивировались, например, с помощью паров воды, введенных в газ-носитель [22]. Недостатком этого метода, как общего метода понижения адсорбционной активности носителя, является введение в газ-носитель компонента, который может влиять на распределение анализируемых веществ и работу детектора. Применялась также обильная промывка кислотами и щелочами как метод удаления растворимых окисей алюминия и железа [17] и понижения адсорбционной активности. Более радикальный метод применялся Омеродом и Скоттом [25],
То обстоятельство, что алюминиЁ не реагирует с водой и с разбавленными, слабо диссоциирующими кислотами, объясняется образованием чрезвычайно трудно растворимого окисла алюминия, произведение растворимости которого в растворах с низкой концентрацией водородных ионов еще не достигается. Напротив, в щелочах окись алюминия растворима с образованием гидроксоалюминатов (см, стр. 353). [c.385]
Практически важно, что растворимость хлоридов и, в частности, 5сС1з резко понижается в воде, насыщенной НС1, особенно в присутствии эфира. Так как, однако, растворимость хлоридов алюминия и иттрия снижается в таких случаях еще резче, то этим пользуются для отделения скандия от этих элементов. [c.265]
Джефкотт и Джонстон [38] показали, что растворимость аморфного тонко изме.тьченного кремнезема в воде, которая, как они нашли, была равна 0,017% при 37°, понижалась до 0,003 и до 0,0097%, если к системе была добавлена окись алю.мпния, и меньше, чем до 0,0 001%, если присутствовал порошкообразный алюминий. Так как также было показано, что добавка кремнезема к суспензии глинозема понижает растворимость глинозема, кажется вероятным, что образование очень мало растворимого силиката алюминия на поверхности фаз кремнезема пли глинозема просто препятствует переходу этих окислов в раствор. [c.16]
При образовании алюмосиликатных катализаторов для крекинга нефти высокое содержание алюминия и общая поверхность не существенны важен объем и диаметр пор, так же как общая активная поверхность каталитически активных алюмосиликатных групп. По этой причине часто предпочитают приготовить силикагель, а затем насытить его растворимым соединением алюминия, чтобы образовать активную поверхность, либо смешать золи алюминия и кремнезема, либо дал е гели. В подобных случаях песом-иенно происходит совместное взаимодействие, так как Джефкотт и Джонстон [17] показали, что растворимость глинозема в воде уменьшалась при добавлении порошка кремнезема и, наоборот, потому что в каждом случае твердые фазы покрываются малорастворимым алюмосиликатом. Для достижения оптимальной активности процессов необходим строгий контроль концентрации, времени, температуры, рП промывной воды и условт сушки [18]. Гель катализатора должен также быть прочным против истирания и удара. Марасик [19] и его сотрудники приготовили шариковые катализаторы, пропуская капельки подкисленной смеси алюмини-
Сущность гидролиза соединений алюминия и железа сводится к отрыву протона от гидратированного иона молекулой воды и образованию гидрооксокомплексов. Обязательным условием эффективности действия коагулянтов является полнота их гидролиза с образованием труднорастворимых гидроксидов. Растворимость гидроксида алюминия при 18°С составляет 2,26-10 а гидроксида железа (1П) —2,3-10-5 мг/л. Из приведенных уравнений гидролиза следует, что для увеличения степени гидролиза необходимо связывать образующиеся ионы Н+. Это достигается за счет гидрокарбонат- карбонат- или гидроксид-ионов, присутствующих в обрабатываемой воде (щелочного резерва). [c.125]
При взаимодействии с водой и водными растворами происходит гидролиз минерала, и поэтому определяю-шим фактором, от которого зависит подвижность элемента, является его химическая природа. Максимальной подвижностью обладают щелочи, соединеиия которых наиболее растворимы, затем алюминий и кремний, способные проявлять кислотные свойства. Нет причин предполагать, что тенденция в поведении щелочей изменится в 0,2 н. натровых растворах, для которых не определяли содержания этих элементов. Основные элементы — маг-1П1Й, железо, частично кальций — менее подвижны, так как их гидроокиси труднорастворимы. [c.205]
Хорошо известна растворимость хлористого алюминия в бензоле, причем растворенное вещество в этом случае существует в виде димерной молекулы [78, 79, 115]. Однако из-за быстрого гидролиза этого соединения в водных растворах эк-стракщюнные исследования не были возможны. Большинство галогенидов металлов не растворяется в органических растворителях. Хлорид железа лишь слабо растворяется в диизопро-пиловом эфире [90], а бромид золота (III), как отмечено в работе [105], вообще не растворяется в эфире в отсутствие воды. Эти галогениды металлов могут экстрагироваться основными растворителями в виде ионных соединений, а именно в виде кислот НМХ4 (см. 6). [c.16]
Жидкий бром является плохим растворителелг. Растворимость воды в броме составляет 0,029″о. Из солей растворимы в броме только бромистый алюминий и в небольшой степени бромное железо РеВг.). Хорошо растворяются в броме галогениды и оксн-галогениды фосфора, мышьяка, сурь.мы и других металлов, а также многие органические вещества. [c.88]
Одной из неполадок, связанных с наличием в системе влаги, является замерзание нерастворенвой воды при дросселировании рабочего тела в регулирующем вентиле. Образовавшиеся частицы льда забивают проходное сечение дроссельных устройств и нарушают нормальную работу установки. Присутствие воды в рабочих телах способствует корразии металлов. Так, водоаммиачный раствор вызывает коррозию цинка, меди и ее сплавов (за исключением фосфористой бронзы) хлористый метил—коррозию цинка, магния и алюминия, хладон-12 — коррозию латуни и сплавов магния, хладон-22 — коррозию сплавов магния. По этим причинам предъявляют высокие требования к содержанию влаги в рабочем теле с ограниченной растворимостью воды, особенно для установок, работающих при низкиХ температурах. [c.126]
Разновидностью электролитической коагуляции является предложенная В. Д. Дмитриевым электрореагентная коагуляция, при которой взаимодействие примесей воды осуществляется под действием электрического поля за счет введения пониженных по сравнению с расчетными дозами химических реагентов. При этом возможно использование растворимых электродов или нерастворимых анодов (графит, ОРТА, ОКТА и других), а также растворимых катодов (алюминий и другие). [c.122]
Фторид алюминия AIF3 существенно отличается от других галогенидов этого металла. Это бесцветное кристаллическое термодинамически устойчивое соединение с преобладанием ионного характера связи. Прочность кристаллической решетки, обусловленная интенсивным электростатическим взаимодействием небольших по размерам ионов А1 + и F, а также большим зарядом катиона, является причиной малой растворимости фторида алюминия в воде. При температуре 1270 °С AIF3 возгоняется, т. е. переходит в газообразное состояние, минуя жидкое. В парах существуют плоские треугольные молекулы AIF3. [c.321]
chem21.info
Химические свойства алюминия и основные реакции
Нахождение в природе
Алюминий впервые получен химическим путем немецким химиком Ф. Велером в 1827 г., а в 1856 г. французский химик Сен-Клер Девиль выделил его электрохимическим методом.
. Алюминий является самым распространенным в природе металлом. Содержание его в земной коре составляет 7,45% (по массе). Важнейшие природные соединения алюминия — алюмосиликаты, боксит, корунд и криолит.
Алюмосиликаты составляют основную массу земной коры. Продукт их выветривания — глина и полевые шпаты (ортоклаз, альбит, анортит). Основной состав глин (каолин) соответствует формуле Аl2O3•2SiO2•2Н2O.
Боксит — горная порода, из которой получают алюминий. Состоит главным образом из гидратов оксида алюминия Аl2O3•nН2O.
Физические свойства
Физические свойства алюминия хорошо изучены. Это — серебристо-белый легкий металл, плавящийся при 660°С. Он очень пластичен, легко вытягивается в проволоку и раскатывается в листы. Из алюминия можно изготовить фольгу толщиной менее 0,01мм. Алюминий обладает очень большой тепло- и электропроводностью. Сплавы алюминия с различными металлами обладают большой прочностью и легкостью.
Химические свойства
.Алюминий очень активный металл. В ряду напряжений он стоит после щелочных и щелочноземельных металлов. Однако на воздухе он довольно устойчив, так как его поверхность покрывается очень плотной пленкой оксида, предохраняющей его от дальнейшего контакта с воздухом. Если с алюминиевой проволоки снять защитную оксидную пленку, то алюминий начнет энергично взаимодействовать с кислородом и водяными парами воздуха, превращаясь в рыхлую массу гидроксида алюминия. Эта реакция сопровождается выделением тепла. Очищенный от защитной оксидной пленки алюминий взаимодействует с водой с выделением водорода:
2Аl + 6Н2O = 2Аl(OН)3 + 3H2↑
Алюминий хорошо растворим в разбавленных серной и соляной кислотах:
2Al + 6НС1= 2AlС13 + 3H2↑
2AI + 3H2SO4 = Al2(SO4)3 + 3H2↑
Разбавленная азотная кислота на холоду пассивирует алюминий, но при нагревании алюминий растворяется в ней с выделением монооксида азота, гемиоксида азота, свободного азота или аммиака, например:
8Al + 30HNO3 = 8Al(NO3)3 + 3N2O + 15Н2O
Концентрированная азотная кислота пассивирует алюминий.
Так как оксид и гидроксид алюминия обладают амфотерными свойствами, то алюминий легко растворяется в водных растворах всех щелочей, кроме гидроксида аммония:
2AI + 6NaOH + 6Н2O = 2Na3[A1ОН)6] + 3H2↑
Порошкообразный алюминий легко взаимодействует с галогенами, кислородом и всеми неметаллами. Для начала реакций необходимо нагревание. В дальнейшем реакции протекают очень интенсивно и сопровождаются выделением большого количества тепла:
2Al + ЗВr2 — 2AlBr3 (бромид алюминия)
4Al + 3O2 = 2Al2O3 (оксид алюминия)
2Al + 3S = A12S3 (сульфид алюминия)
2Al + N2 = 2A1N (нитрид алюминия)
4Al + ЗС = Al4С3 (карбид алюминия).
Сульфид алюминия может существовать только в твердом виде. В водных растворах он подвергается полному гидролизу с образованием гидроксида алюминия и сероводорода:
A12S3 + 6H2O = 2A1(OН)3 + 3H2S.
Алюминий легко отнимает кислород и галогены у оксидов и солей других металлов. Реакция сопровождается выделением большого количества тепла:
8Al + 3Fe3O4 = 9Fe + 4Al2O3
Процесс восстановления металлов из их оксидов алюминием называется алюмотермией. Алюмотермией пользуются при получении некоторых редких металлов, которые образуют прочную связь с кислородом (ниобий, тантал, молибден, вольфрам и др.).
Смесь мелкого порошка алюминия и магнитного железняка называется термитом. После поджигания термита с помощью специального запала реакция протекает самопроизвольно и температура смеси повышается до 3500°С. Железо при такой температуре находится в расплавленном состоянии. Эту реакцию используют для сваривания рельсов.
Получение
.Впервые алюминий был получен восстановлением хлорида алюминия металлическим натрием:
AlС13 + 3Na = Al + 3NaCl
В настоящее время его получают электролизом расплавленных солей. В качестве электролита служит расплав, содержащий 85— 90% комплексной соли 3NaF • A1F3 (или Na3AlFe) — криолита и 10–15% оксида алюминия Al2O3 — глинозема. Такая смесь плавится при температуре около 1000°С. При растворении в расплавленном криолите глинозем ведет себя как соль алюминия и алюминиевой кислоты и диссоциирует на катионы алюминия и анионы кислотного остатка алюминиевой кислоты:
Al2O3 ⇔ Al3+ + АlO33−
Криолит диссоциирует:
Na3 [AlF6]⇔ 3Na+ + [A1F6]
При пропускании электрического тока катионы алюминия и натрия движутся к катоду — графитовому корпусу ванны, покрытому на дне слоем расплавленного алюминия, получаемого в процессе электролиза. Так как алюминий менее активен, чем натрий, то он восстанавливается в первую очередь. Восстановленный алюминий в расплавленном состоянии собирается на дне ванны, откуда его периодически выводят.
Анионы AlO33− и A1F63− движутся к аноду — графитовым стержням или болванкам. На аноде в первую очередь разряжается анион AlO33−:
AlO33− — 12е = 2Al2O3 + 3O2
Оксид алюминия вновь диссоциирует, и процесс повторяется. Расход глинозема все время восполняется. Количество криолита практически не меняется. Незначительные потери криолита происходят вследствие образования на аноде тетрафторида углерода CF4 . Электролитическое производство алюминия требует больших затрат электроэнергии (на получение 1 т алюминия расходуется около 20 тыс. квт • ч электроэнергии), поэтому алюминиевые заводы строят вблизи электростанций.
Применение
Алюминий находит самое широкое применение. Он используется в электротехнике, его сплавы, отличаясь большой легкостью и прочностью, применяются в самолето- и машиностроении, он все больше вытесняет стали в производстве теплообменных аппаратов, из него изготовляют фольгу, применяемую в радиотехнике и для упаковки пищевых продуктов. Алюминием покрывают стальные и чугунные изделия в целях предохранения их от коррозии: изделия нагревают до 1000° С в смеси алюминиевого порошка (49%), оксида алюминия (49%) и хлорида аммония (2%). Этот процесс называется алитированием. Алитированные изделия выдерживают нагревание°С, не подвергаясь коррозии.
Оксид алюминия Al2O3
Представляет собой белое вещество, обладающее высокой температурой плавления (2050°С). В природе оксид алюминия встречается в виде корунда и глинозема. Иногда встречаются прозрачные кристаллы корунда красивой формы и окраски. Корунд, окрашенный соединениями хрома в красный цвет, называют рубином, а окрашенный соединениями титана и железа в синий цвет — сапфиром. Рубин и сапфир являются драгоценными
камнями. В настоящее время их довольно легко получают искусственно.
Оксид алюминия обладает амфотерными свойствами, но он не растворяется в воде, кислотах и щелочах. При кипячении оксида алюминия в концентрированном растворе щелочи он частично переходит в раствор. Оксид алюминия переводят в растворимое состояние сплавлением со щелочами или с пиросульфатом калия:
Al2O3 + 2NaOH = 2NaA1O2 + Н2O
Al2O3 + 3K2S2O7 = Al2(SO4)3 + 3K2SO4.
Полученные сплавы растворяются в воде. При сплавлении оксида алюминия с поташом или содой образуются алюминаты, которые легко растворяются в воде:
Al2O3 + Na2CO3 = 2NaA1O2 + CO2,
Природный корунд — очень твердое вещество. Он применяется для изготовления наждачных кругов и шлифовальных порошков. Рубин используют для изготовления втулок часовых и других точных механизмов.
Глинозем используется как сырье для получения алюминия. Обезвоженный оксид алюминия применяется как адсорбент при очистке и разделении органических веществ методом хроматографии.
Гидроксид алюминия Al (ОН)3
Представляет собой белое вещество, которое при нагревании теряет воду, превращаясь оксид алюминия. Гидроксид алюминия обладает амфотерными свойствами. Свежеосажденный гидроксид легко растворяется в кислотах и щелочах (кроме гидроксида аммония):
Al(ОН)3 + ЗНС1 = AlС13 + ЗН2O
Al(ОН)3 + 3NaOH= Na3 [Al(OH)6].
Гидроксид алюминия является слабым основанием и еще более слабой кислотой, поэтому соли алюминия находятся в растворе только в присутствии избытка кислоты, а алюминаты — только в присутствии избытка щелочи. При разбавлении растворов водой эти соединения сильно гидролизуют.
Высушенный гидроксид алюминия теряет часть воды, не растворяется ни в кислотах, ни в щелочах и этим напоминает оксид алюминия.
Гидроксид алюминия обладает свойством поглощать различные вещества, поэтому его применяют при очистке воды.
www.metmk.com.ua
Растворимость — алюминий — Большая Энциклопедия Нефти и Газа, статья, страница 2
Растворимость — алюминий
Cтраница 2
Растворимость алюминия в azr при понижении температуры до 700 С уменьшается и составляет — 0 5 вес. [16]
Растворимость алюминия в никеле с понижением температуры падает с 9.7 % при 1300 С до 5 0 % при 500 С ( фиг. [17]
Растворимость алюминия в кислотах основана на том, что он в соответствии со своим аоложением в ряду напряжений ( см. стр. [18]
Растворимость алюминия повышается с температурой, а энергичная циркуляция электролита в промышленных ваннах обеспечивает быструю доставку растворенного металла к аноду и на поверхность электролита, где он и потребляется. [19]
Относительно растворимости алюминия в кремнии точных сведений нет, по всей вероятности она незначительна. Диаграмма указывает на наличие эвтектики кремния с твердым раствором алюминия. [20]
При снижении температуры растворимость алюминия и меди в цинке уменьшается. При 20 С в цинке растворяется всего 0 2 % алюминия и 0 6 % меди. [22]
Таким образом, растворимость алюминия зависит от рН, он нерастворим в пределах значений рН 5 — 9, что включает большинство природных вод. Растворимость алюминия осложняется образованием частично диссоциированных форм А1 ( ОН) 3 и комплексов между алюминием и органическим веществом. Понимание контроля за растворимостью алюминия важно, поскольку его токсичность может вызвать гибель рыбы в подкисленных пресных водах. [24]
От значений рН воды зависит растворимость алюминия и тяжелых металлов в ней и, следовательно, их накопление в корнеплодах, а затем и в организме человека. При изменении рН воды меняется структура почвы и снижается ее плодородие. Снижение рН питьевой воды способствует прямому поступлению в организм указанных металлов и их соединений. [25]
От значения рН воды зависит растворимость алюминия и тяжелых металлов в ней и, следовательно, их накопление в корнеплодах, а затем и в организме человека. При изменении рН воды меняется структура почвы и снижается ее плодородие. Снижение рН питьевой воды способствует поступлению в организм человека указанных выше металлов и их соединений. [26]
От значения рН воды зависит растворимость алюминия и тяжелых металлов в ней и, следовательно, их накопление в корнеплодах, а затем и в организме человека. При изменении рН воды меняется структура почвы и снижается ее плодородие. Снижение рН питьевой воды способствует прямому поступлению в организм человека указанных выше металлов и их соединений. [27]
Выше температуры 500 С — растворимость алюминия в олове и особенно в цинке резко возрастает; значительной величины достигает растворимость алюминиевых сплавов в припоях П575А, 590А, эвтектическом силумине. Особенно сильно развивается эрозия в галтельных участках швов, где скопляются большие количества жидкого припоя. В этом случае образуются более развитые и грубые галтели. [28]
От значения рН воды зависит растворимость алюминия и тяжелых металлов в ней и, следовательно, их накопление в корнеплодах, а затем и в организме человека. При изменении рН воды меняется структура почвы и снижается ее плодородие. Снижение рН питьевой воды способствует поступлению в организм человека указанных выше металлов и их соединений. [29]
Свинцовый способ основан на изменении растворимости алюминия в свинце при различной температуре и отделении кремния, железа и титана, практически не растворимых в свинце при условиях протекания процесса. [30]
Страницы: 1 2 3 4
www.ngpedia.ru
Алюминия растворимость
Растворимость гидроксидов А1 в кислых средах прямо пропорциональна третьей степени концентрации водородных ионов, а в щелочных средах обратно пропорциональна ей [4]. В изоэлектрической точке гидроксид алюминия имеет минимальную растворимость. По Кольтгофу для А1(ОН)3 эта точка лежит в пределах значений pH 6,5—7,5 [13]. Для скорости гидролиза солей алюминия также существует некоторый оптимум значений pH, который для концентраций А БО з от 400 до 100 мг/л колеблется в пределах 4,95— 5,40, а предельные значения pH. при которых гидролиз еще протекает, составляют 3 и 6,8.[ …]
Связь растворимости с химическим взаимодействием особенно четко проявляется в системах с комплексообразованием. Здесь можно напомнить широко известный факт резкого повышения растворимости молекулярного иода в воде в присутствии иодистого калия вследствие образования полииодида: Ы-К1 = К1з- Хлористый натрий, например, практически нерастворим в нитробензоле, но в присутствии хлористого алюминия растворимость его резко повышается вследствие образования комплексной соли ЫаАЮЦ, которая отлично растворяется в том растворителе.[ …]
| Растворимость сульфата алюминия при разных температурах |  |
Изотерма растворимости системы Na2S04 — A12(S04)3—Н20 при 40 °С (рис. 2.10) состоит из трех ветвей, отвечающих кристаллизации сульфата натрия, натриевых квасцов и 18-гидрата сульфата алюминия [67].[ …]
Коллоидно-растворимые формы могут быть представлены органическими и органо-минеральными веществами, золями кремнекислоты и полутораокисей железа и алюминия. По данным К. К. Гедройца, коллоидная часть составляет обычно /4—1/10 и меньше общего количества веществ в растворе. Высокое содержание коллоиднорастворимых соединений наблюдается в почвенных растворах солонцов.[ …]
| 4.2 | 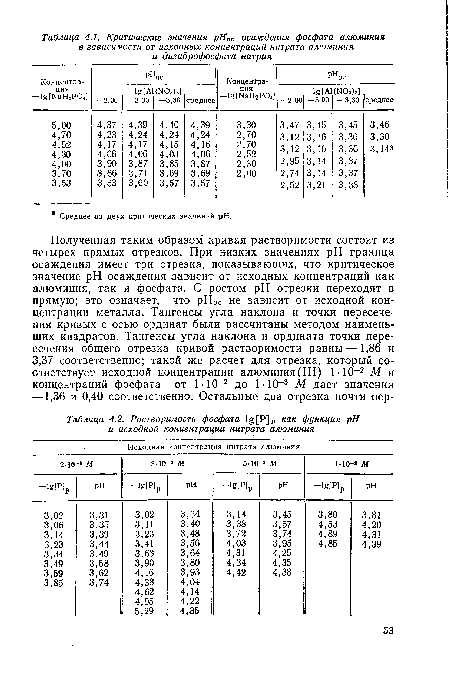 |
Минимальная растворимость гидроксида алюминия лежит в области pH = 6,5+7,5. Осаждение гидроксида алюминия начинается при pH = 3,0 и достигает максимума при pH = = 7. При дальнейшем увеличении pH осадок начинает растворяться, что становится заметным при pH = 9.[ …]
Сернокислый алюминий используют для очистки мутных и цветных вод: очищенный — при высокой мутности, неочищенный или содержащий в качестве инградиентов глины и силикатные мате-риалы — при низкой мутности воды. Этот коагулянт эффективен в диапазоне значений pH 5—7,5, причем чем выше жесткость воды и ниже ее цветность, тем выше оптимальные значения pH среды [1 (стр. 139), 2,3 (стр. 45)]. Относительно низкая стоимость, хорошая растворимость, отсутствие особых требований к обращению с сухим и растворенным продуктом сделали сульфат алюминия наиболее распространенным коагулянтом.[ …]
Произведение растворимости HgS в дистиллированной воде составляет 1,6ХЮ 52, что соответствует остаточной концентрации ионов ртути в растворе, равной 2,5X10-21 мг/л. В производственных сточных водах произведение растворимости HgS несколько больше, основная же часть сульфида ртути находится в воде в виде тонкодисперсных коллоидных частичек, выделить которые в осадок можно коагулированием сточных вод водным сульфатом алюминия Al2(S04)3-I8h3O, водным сульфатом железа FeS04-7h30, известью СаО, смесью этих коагулянтов и т. д.[ …]
Таким образом, растворимость гидроокиси алюминия в щелочной среде обратно пропорциональна концентрации водородных ионов в первой степени.[ …]
При применении растворимых электродов (обычно железных или алюминиевых) на аноде происходит анодное растворение металла, в результате чего в воду переходят катионы железа или алюминия, приводящие к образованию хлопьев гидроокисей. Одновременное образование хлопьев коагулянта и пузырьков газа в стесненных условиях межэлек-тродного пространства создает предпосылки для надежного закрепления газовых пузырьков на хлопьях и интенсивной ,.оагуляции загрязнений, что обеспечивает, эффективность флотационного процесса. Такие установки называются электрокоагуляционно-флотационными. При пропускной способности до 10—15 м3/ч установки могут быть однокамерными, а при большей пропускной способности — двухкамерными горизонтального или вертикального типа.[ …]
| Пределы растворимости фосфата алюминия как функция pH и исходных концентраций ионов фосфата для трех исходных концентраций нитрата алюминия. |
| Пределы растворимости фосфата алюминия как функция pH и исходных концентраций ионов фосфата для трех исходных концентраций нитрата алюминия. |
Некоторые трудно растворимые красители растворяют вместе с содой и обрабатывают сначала раствором сернокислого алюминия, а затем хлористого бария.[ …]
Кроме перечисленных растворимых примесей в природных водах содержатся во взвешенном состоянии нерастворимые вещества — от грубодисперсных суспензий до коллоидно растворенных соединений. Они представлены частицами песка, лесса, илистых веществ и карбонатных пород, водных окислов алюминия, железа, марганца, а также высокомолекулярных гумусовых веществ.[ …]
Гидратированные ионы алюминия в процессе гидролиза отдают протон от координированной молекулы воды, образуя последовательно комплексные ионы [А1 (Н20) 5 (ОН) ]2+ и [А1 (Н20)4 (ОН)2]+, остающиеся в растворе. Когда последний нейтральный комплекс [А1(Н20)з(ОН)з] теряет воду, образуется плохо растворимый гидроксид алюминия. Ступенчато гидролизуются и соли железа(III). Но, в отличие от солей алюминия, помимо гидроксидов железа могут образовываться и труднорастворимые гидроксосоли.[ …]
| 2 |  |
В разбавленной кислоте растворимость А12(804)з выше, чем в чистой воде, но с дальнейшим увеличением концентрации Н2Б04 растворимость резко понижается, достигая 1 % в 60 %-ной серной кислоте. В более крепкой кислоте растворимость сульфата алюминия опять повышается.[ …]
Свежеосажденные фосфаты алюминия и железа могут усваиваться растениями, но при старении осадков они кристаллизуются и становятся менее растворимыми и слабодоступными для растений. Поэтому фосфорная кислота в красноземах и дерново-подзолистых почвах закрепляется весьма прочно и значительно сильнее, чем в сероземах и черноземах.[ …]
Из изложенного видно, что растворимость гидроксида алюминия в кислой среде прямо пропорциональна третьей степени концентрации водородных ионов [Н+]3, а в щелочной — обратно пропорциональна [Н+].[ …]
В кислых растворах с избытком алюминия наиболее устойчивой твердой фазой является основной фосфат алюминия. Если значение pH больше, чем pH, соответствующее минимуму растворимости фосфата (pH = 6), то основная соль гидролизуется до гидроксида алюминия, на поверхности которого сорбируется фосфат. При большой концентрации фосфата выделяется в осадок таранакит, который переходит в среднюю соль, если pH системы возрастает.[ …]
Полиакриламид — белое аморфное, хорошо растворимое в воде вещество, содержащее ионогенные группы; при гидролизе образует акриловую кислоту и ее соли. Механизм действия ПАА основан на адсорбции его молекул на частицах примесей воды, гидроксидов алюминия или железа (III), образующихся при гидролизе солей — коагулянтов. Благодаря вытянутой форме молекулы адсорбция происходит в разных местах с несколькими частицами гидроксида, в результате чего последние связываются полимерными мостиками в тяжелые, крупные и прочные агрегаты (глобулы).[ …]
Только образцы, обладающие ограниченной растворимостью в воде (у=38), удерживаются древесной целлюлозой в количестве 60 %. Прибавление сернокислого алюминия вызывает полное удержание -КМЦ, причем оно не зависит от стехиометрического соотношения между количеством А13+, требуемого для полного удержания -КМЦ, и количеством ОСН2СОО -групп, присутствующих в КМЦ. Иначе говоря, удержание -КМЦ обусловливается не только получением нерастворимой алюминиевой соли, но и электростатической адсорбцией между положительно заряженной А1-КМЦ и отрицательно заряженными волокнами целлюлозы.[ …]
Разработана новая технология с использованием растворимых количеств хлорида алюминия в высокотемпературном процессе алкилнрования бензола пропиленом.[ …]
В данной главе рассмотрено взаимодействие между алюминием (III) и фосфатом в широкой области концентраций и pH. Для того чтобы дать характеристику реакций между растворенными частицами и растворимыми фазами, была изучена растворимость осадков фосфата алюминия. Кроме того, были идентифицированы растворимые и нерастворимые продукты реакций между алюминием (III) и фосфатом и определено распределение их концентраций в широкой области pH и концентраций Р и А1. Данные исследования проводили с использованием чистых растворов фосфатов алюминия определенного состава. Других диспергированных твердых фаз в изучаемой системе, кроме тех, что осаждались при взаимодействии между алюминием и фосфатом или в результате изменения pH, не было.[ …]
В упрощенном виде можно считать, что осаждение железом и алюминием во многом очень схоже и что определяющими факторами и в том, и в другом случае являются растворимость и соотношение концентраций добавляемого иона металла Ме и присутствующего ортофосфата. Процесс осаждения ионами кальция сильно зависит от pH, поэтому рассчитывая необходимое количество соли кальция, необходимо учитывать щелочность сточной воды.[ …]
Соли железа как коагулянты, имеют ряд преимуществ перед солями алюминия: лучшее действие при низких температурах воды; более широкая область оптимальных значений pH среды; большая прочность и гидравлическая крупность хлопьев; возможность использовать для вод с более широким диапазоном солевого состава; способность устранять вредные запахи и привкусы, обусловленные присутствием сероводорода. Однако имеются и недостатки: образование при реакции катионов железа с некоторыми органическими соединениями сильно окрашивающих растворимых комплексов; сильные кислотные свойства, усиливающие коррозию аппаратуры; менее развитая поверхность хлопьев.[ …]
При значительном содержании в почве обменнопоглощенных ионов водорода и алюминия (например, в дерново-подзолистых почвах и красноземах) многие свойства ее также ухудшаются. Ионы водорода не диспергируют почвенные коллоиды, но, вступая в поглощенное состояние, вызывают постепенное разрушение минералов, входящих в состав почвенного поглощающего комплекса. В результате почва обедняется коллоидной фракцией, ухудшается ее структура и уменьшается емкость поглощения. Кроме того, ионы алюминия и водорода из поглощенного состояния вытесняются в раствор в обмен на катионы растворимых солей. Высокая концентрация в растворе ионов водорода и алюминия оказывает вредное действие на развитие растений.[ …]
В последние годы начали применять метод получения коагулянтов в электролизерах с растворимыми электродами, называемый методом электрокоагуляции [190]. Сущность метода заключается в анодном растворении металлов, преимущественно алюминия и железа, в водных средах под воздействием электрического тока с последующим образованием гидроксидов. Этот метод позволяет производить эффективную очистку воды от взвесей минерального, органического и биологического происхождения, коллоидов и веществ в молекулярном или ионном состоянии. Электрокоагуляция обладает существенными преимуществами перед реагентными методами: компактностью установки, простотой обслуживания и возможностью полной автоматизации. Этот метод перспективен для использования на небольших автономных объектах (на судах речного флота, для малых поселков и др.).[ …]
Отрицательное действие высокой кислотности в значительной степени связано с увеличением растворимости соединений алюминия и марганца в почве. Повышенное содержание их в растворе ухудшает развитие растений даже сильнее, чем избыток ионов водорода.[ …]
Уравнение (4.17) было решено методом проб и ошибок для значения pH, соответствующего минимуму растворимости фосфата, около 6. При рН[ …]
При исследовании гидролиза в системе Ре2(504)з—А1203—Н20 при 100 °С установлено, что с увеличением количества оксида алюминия в системе выход железа в осадок основной соли повышается, достигая 98% при массовом отношении А1203/Ре2(504)3 = 0,111 и 90 % НгО. В растворе оксид алюминия в результате химического взаимодействия превращается в растворимые основные сульфаты алюминия. С увеличением содержания сульфата железа(III) в системе количество прореагировавшего оксида алюминия повышается и при массовом отношении А1203/Ре2(804)з = 3 и 40 % Н20 достигает 91 %.[ …]
Протекание процесса коагуляции в значительной степени зависит от pH среды. При добавлении к воде раствора коагулянта сернокислого алюминия цроисходит гидролиз с образованием коллоидной гидроокиси алюминия. Оптимальной величиной для сточных вод данного катализаторного цроизводства является рН=7,5-8,5. На рис.1 представлена зависимость степени очистки сточных вод с содержанием взвешенных веществ 1200 мг/л от pH.[ …]
С увеличением дозы 50 %-ной серной кислоты в пределах 80—100 % стехиометрического количества при температуре 120°С и длительности процесса 1,5 ч степень разложения гидроксида алюминия возрастает. Так, для дозы кислоты 83,3 % (мол. отношение 503/А1203 = ло = 2,5) степень разложения гидроксида алюминия составляет 92,4 %, в то время как для дозы 90 % (цо = 2,7) в указанных условиях гидроксид полностью разложился. Разложение гидроксида алюминия при неполной дозе серной кислоты можно объяснить взаимодействием гидроксида с сульфатом алюминия с образованием растворимых основных солей алюминия, что более подробно обсуждается ниже.[ …]
Электрохимический метод имеет следующие преимущества перед реа-гентным: снижение нагрузки на обессоливающие установки, поскольку при его использовании в воду не поступают растворимые соли, а дозируемый алюминий полностью удаляется из воды в процессе ее предварительной очистки [315, 316]. Метод обескремнивания воды в электролизерах с алюминиевым анодом может быть рекомендован для предварительной подготовки воды в схемах водоподготовки на ТЭЦ и других промышленных предприятиях.[ …]
Для активирования обычно используют 1,5%-ные (в пересчете на БЮг) растворы силиката натрия при степени нейтрализации щелочности 80—85%. В случае применения активного хлора степень нейтрализации растворимого стекла повышают до 100% и даже вводят некоторый избыток его. После смешения реагентов золь некоторое время «вызревает», а затем его разбавляют водой до содержания 5Ю2 менее 1%. Наиболее перспективным способом приготовления активной кремневой кислоты является обработка жидкого стекла хлором и сульфатом алюминия [44], обычно используемых в процессах очистки воды.[ …]
При взаимодействии с почвенным покровом усиливаются процессы выщелачивания биогенов. При pH [ …]
Доменные и мартеновские шлаки получаются как отходы при выплавке чугуна и стали и имеют различный состав: СаО — 30—50%; Si02—12—37; А1203-Ю-15; MgO-2-10; МпО —0,4—5,6; Р205 — 0,1—3,5; S — 0,1 — 4,5%. В большинстве случаев они требуют предварительного размола. Большая часть кальция в шлаках находится в виде менее растворимых кремнекислых соединений (CaSiO3 и Ca2Si04), поэтому тонина их размола должна быть мельче, чем известковой муки. По нейтрализующей способности основные шлаки (с содержанием CaO + MgO свыше 40%) близки к углекислой извести. Эффективность их часто выше, чем извести. Это объясняется присутствием в шлаках магния, фосфора, марганца, серы и других элементов питания растений. Кроме того, содержащаяся в них кремневая кислота может уменьшать количество подвижного алюминия в почвах и способствовать лучшему усвоению фосфора растениями. Для дерново-подзолистых почв в районах, близко расположенных от металлургических заводов, доменные шлаки, богатые известью, являются ценным удобрением.[ …]
Соединения фтора представляют собой еще одну группу специфических веществ, присутствие которых установлено в атмосферном воздухе ряда населенных мест и которые могут оказать значительное влияние на здоровье человека. В атмосферном воздухе обнаружены различные фтористые соединения — от сравнительно хорошо растворимых в жидких средах организма до совершенно нерастворимых; от крайне раздражающего и коррозирующего фтористого водорода до относительно инертных соединений. Основными промышленными процессами, которые сопровождаются выбросом в атмосферу фтористых соединений, являются производство искусственных удобрений, производство алюминия и некоторые способы производства стали.[ …]
Прибавка урожая от извести и минеральных удобрений при совместном их внесении в большинстве случаев бывает значительно выше суммы прибавок от раздельного использования этих удобрений. Особенно резко повышается при известковании эффективность физиологически кислых аммиачных и калийных удобрений . Эти удобрения при систематическом внесении на малобуферных кислых дерново-подзолистых почвах вызывают дальнейшее их подкжсление. Поэтому при систематическом внесении таких удобрений на неизвесткованной почве прибавки урожая постепенно снижаются, а в последующие годы в результате сильного подкисления почвы урожай может быть ниже, чем на контроле. Положительное влияние извести на эффективность физиологически кислых форм минеральных удобрений сильнее проявляется при внесении их под культуры, чувствительные к повышенной кислотности (свекла, кукуруза, пшеница), и меньше или вовсе не проявляется при; применении под культуры, устойчивые к кислой реакции. Действие известкования на эффективность фосфорных удобрений зависит от свойств почвы и форм этих удобрений. Эффективность растворимых фосфорных удобрений [например, суперфосфата Са(Н2Р04)2] на сильнокислых почвах со значительным содержанием подвижных соединений алюминия и железа от известкования заметно повывзается. При внесении извести в нормальной дозе подвижные соединения алюминия и железа переходят в нерастворимые формы, поэтому уменьшается химическое закрепление ими фосфора суперфосфата и повышается использование его растениями.[ …]
ru-ecology.info
Растворение — алюминий — Большая Энциклопедия Нефти и Газа, статья, страница 2
Растворение — алюминий
Cтраница 2
Скорость растворения алюминия уменьшается с увеличением содержания никеля в твердом растворе. Известно [21], что из соединения NiAl алюминий нельзя перевести в раствор даже при помощи горячего КОН. Хотя порошок сплава тонко размолот, но он спрессован и спечен с опорным скелетом из порошка карбонильного никеля, поэтому при низких температурах нельзя ожидать быстрого и полного растворения алюминия. [16]
Результаты растворения алюминия в растворе NaOH показаны на фиг. [17]
После окончательного растворения алюминия массу нагревают до 70 — 100 С, а затем охлаждают, промывают водой до нейтральной реакции, а потом спиртом. Никель, нерастворимый в щелочи, остается в виде мелкодисперсного тяжелого порошка. Полученный катализатор содержит небольшое количество алюминия, который оказывает влияние на его активность Полное удаление алюминия приводит к дезактивации катализатора Никель Ренея хранят под слоем спирта из-за его высокой пнрофорности По методу Ренея получают также скелетные кобальтовые, железные и медные катализаторы, но они применяются гораздо реже. [18]
При растворении алюминия в соляной кислоте получают ок-сихлорид алюминия высокой чистоты. [19]
При растворении алюминия и цинка в реактиве осадок не образуется. [20]
При растворении алюминия в минеральных кислотах образуются соли. К действию таких органических кислот, как разбавленные уксусная и лимонная кислоты, алюминий устойчив на холоду, но не при нагревании. В концентрированной уксусной кислоте он растворяется. Даже раствор хлорида натрия медленно действует на него; поэтому алюминий можно использовать для изготовления лишь определенной кухонной посуды. Алюминий весьма устойчив только по отношению к разбавленной и концентрированной азотной кислоте. Поэтому для хранения и транспортировки этой кислоты используются емкости и цистерны из алюминия. При нагревании до кипения азотная кислота может, однако, внезапно оказывать сильное окислительное действие. [21]
При растворении алюминия в щелочах образуется алюминат натрия и выделяется большое количество водорода. [22]
При растворении алюминия в НС1 с наложением ультразвука наблюдается уменьшение скорости растворения, и только при частоте 16 кгц и интенсивности 1 3 вт / см2 процесс несколько ускоряется. [23]
При катодном растворении алюминия анионный состав оказывает незначительное влияние на выход по току. В бикарбонат-ных и сульфатных растворах катодное растворение не ухудшается, а даже интенсифицируется. Однако ионы Са2 и Mg2 угнетают процесс катодного растворения из-за образования на поверхности катода карбонатных отложений. [24]
Затем идет растворение алюминия в воде. [25]
Нередко для растворения алюминия применяют смесь трех кислот: азотной, соляной и серной. [26]
Возможно ли растворение алюминия в щелочи. Если возможно, то составьте уравнение реакции. [27]
По мере растворения алюминия из анода вводят в анодный сплав ( через графитовую воронку) новые порции алюминия-сырца. Анодный сплав постепенно обогащается примесями железа, кремния и титана и становится трудноплавким. Поэтому время от времени его выпускают через летку и заменяют новым сплавом алюминия с медью. [29]
В результате растворения алюминия во флюсе ослабляется связь имеющихся на поверхности окислов с металлом паяемого изделия, а входящие во флюс летучие составляющие ( например, Nh5C1) и пары образовавшегося при реакции соединения А1С1, подрывают окисную пленку и тем самым очищают поверхность алюминия. [30]
Страницы: 1 2 3 4
www.ngpedia.ru
Очистка воды методом электролитического растворения алюминия
В последние годы начали применять метод получения коагулянтов в электролизерах с растворимыми электродами, называемый методом электрокоагуляции [190]. Сущность метода заключается в анодном растворении металлов, преимущественно алюминия и железа, в водных средах под воздействием электрического тока с последующим образованием гидроксидов. Этот метод позволяет производить эффективную очистку воды от взвесей минерального, органического и биологического происхождения, коллоидов и веществ в молекулярном или ионном состоянии. Электрокоагуляция обладает существенными преимуществами перед реагентными методами: компактностью установки, простотой обслуживания и возможностью полной автоматизации. Этот метод перспективен для использования на небольших автономных объектах (на судах речного флота, для малых поселков и др.).[ …]
Наличие в воде ионов-депассиваторов, интенсификация движения электролита и наложение постоянного электрического тока способствуют лучшему протеканию процесса химического растворения.[ …]
В природной воде преимущественно протекают кислородная и водородная деполяризация.[ …]
Выделение водорода на поверхности алюминиевого катода благоприятствует протеканию этой реакции, так как алюминий переходит в более активное состояние.[ …]
Обработка электродного материала перед растворением, состав электролита и электродная плотность значительно влияют на скорость растворения катода. На металлических электродах адсорбируются органические и неорганические вещества, которые могут замедлять или ускорять электрохимический процесс.[ …]
В процессе электролиза на электродах выделяются пузырьки кислорода, водорода и другие, которые транспортируют вещество из жидкости на ее поверхность. Под действием электрического тока происходит электрофорез — направленное движение взвешенных твердых частиц, пузырьков газа, коллоидных частиц и капель другой жидкости. Протекание этих процессов оказывает значительное влияние на скорбеть электрохимического растворения металла. Кроме того, на этот процесс существенно влияют солевой состав электролита и его активность, температура, чистота растворяемого металла, плотность тока, частота смены полярности, скорость движения воды в межэлектродном пространстве и др. При наличии в алюминии легирующих примесей анодное растворение его значительно ускоряется. Интенсифицирующее влияние примесей зависит от их природы, количества и условий протекания процесса.[ …]
Активность алюминиевого анода также определяется природой и концентрацией присутствующих в воде анионов. Наибольшее влияние на активность алюминиевого анода оказывает хлор-ион. С увеличением температуры воды от 2 до 80 °С выход алюминия по току повышается, и особенно резко в интервале 2—30 °С. Интенсивное растворение алюминиевого анода происходит при температуре от 2 до 60 °С и плотности тока от 1 до 4 мА/см . При более высоких значениях плотности тока с повышением температуры воды возрастает напряжение на электродах и снижается выход алюминия по току.[ …]
В кислой и особенно щелочной средах растворение алюминия повышается по сравнению с нейтральными растворами. Так, при изменении pH от 7 до 2 выход алюминия по току увеличивается на 7,39, тогда как при повышении pH от 7 до 12 он увеличивается на 25,2 %. Наиболее интенсивное хлопьеобразование происходит при pH от 3 до 10.[ …]
Рисунки к данной главе:
Вернуться к оглавлениюru-ecology.info
Растворение оболочек из алюминия
Алюминиевые оболочки растворяют в щелочи или азотной кислоте, причем в последнем случае возможно частичное или полное растворение сердечник из металлического урана.
Растворение алюминия в растворе едкого натра проходит по реакции:
Al+NaOH+ Н20 NaAlО2 + 1,5Н2, (3.1)
протекающий с выделением тепла 7000 ккал/кг растворенного алюминия. При увеличении концентрации NaOH от 2 до 5 М скорость растворения алюминия возрастает примерно в семь раз. Потери урана при использовании растворов NaOH с концентрацией до 30% очень малы, но в 50%-ном растворе скорость растворения урана становится заметной. Недостатком этого процесса является выделение взрывоопасного газа – водорода. Для подавления реакции выделения водорода в реакционную смесь вводят окислители: нитрит или нитрат натрия. В этом случае реакции растворения алюминия протекают по уравнениям:
Al + 0,5NaOH + 0,5NaNO3 + 0,5H2O = NaAlO2 + 0,5NH2↑ (3.2)
Al + 0,625NaOH + 0,375NaNO3 + 0,25H2O = NaAlO2 + 0,375NH3; (3.3)
Al + 0,85NaOH + 1,05NaNO3 = NaAlO2 + 0,9NaNO2 + 0,15NH3 + 0,2H2O (3.4)
Минимальное выделение водорода происходит при стехиометрических соотношениях последней реакции. Скорость растворения алюминия возрастает с увеличением температуры и концентрации гидроксида натрия. Например, для раствора, содержащего 10%-ный NaOH и 20%-ный NaNO3, при увеличении температуры от 60 до 100°С линейная скорость растворения алюминия возрастает примерно в 3 раза. Кристаллизация алюмината натрия зависит от концентрации этой соли в щелочи и может быть предотвращена, если молярное отношение едкого натра и алюминия в растворе равно 1,65:1.
HNO3 пассивирует поверхность алюминия, и поэтому, растворение ведут в присутствии катализатора – нитрата ртути. Возможными реакциями являются:
Al + 6HNO3 = Al(NO3)3 + 3NO2 + 3H2O; (3.5)
Al + 4HNO3 = Al(NO3)3 + NO + 2H2O; (3.6)
8Al + 30HNO3 = 8Al(NO3)3+3N2O + 15H2O4 (3.7)
2Al + 6HNO3 = 2Al(NO3)3 + 3H2 (3.8)
По мере того, как образуется при гидролизе нитрата алюминия HNO3 взаимодействует с Al, получаются растворы с недостатком кислоты:
Al(NO3)3+3H2O=Al(OH)(NO3)2+HNO3; (3.9)
HNO3+Al+H2O=Al(OH)2(NO3)3 + соединения азота. (3.10)
Для описания процесса растворения Al в 4 М HNO3 приложена реакция:
Al+3,75HNO3=Al(NO3)3+0,225NO+0,15N2O+0,1125N2+1,875h3O. (3.11)
Однако некоторые данные не подтверждают присутствия азота в продуктах реакции. Содержание водорода в отходящих газах после конденсатора составляет 2 – 8% при концентрации кислоты 1 – 2 М и быстро возрастает для растворов с недостатком кислоты, достигая максимума 23% при недостатке 2 М. Это свидетельствует о том, что по мере протекания процесса стехиометрия раствора такова, что реакция с образованием двуокиси азота постепенно затухает в пользу других реакций. Расход кислоты для растворения литых и штампованных стержней одинаков. В среднем он составляет 4 – 4,1М HNO3 на 1 М растворенного Аl. Наименьший расход кислоты 3,8М был получен при растворении штампованного стержня при 2М недостатке кислоты.
studfiles.net
