ЕГЭ по химии 2023 задание 13: номер 176
Русский язык Математика (профильная) Обществознание Физика История Биология Химия Английский язык Информатика Литература
Задания Варианты Теория
Задание 1 Задание 2 Задание 3 Задание 4 Задание 5 Задание 6 Задание 7 Задание 8 Задание 9 Задание 10 Задание 11 Задание 12 Задание 13 Задание 14 Задание 15 Задание 16 Задание 17 Задание 18 Задание 19 Задание 20 Задание 21 Задание 22 Задание 23 Задание 24 Задание 25 Задание 26 Задание 27 Задание 28 Задание 29 Задание 30 Задание 31 Задание 32 Задание 33 Задание 34
Разбор сложных заданий в тг-канале:
Посмотреть
Белки проявляют амфотерные свойства, потому что в состав их молекул входят
- аминогруппа и гидроксил
- карбоксил и аминогруппа
- углеводородный радикал и аминогруппа
- функциональная группа –SH и гидроксил
Объект авторского права ООО «Легион»
Посмотреть решение
Предыдущая задача
Следующая задача
Из предложенного перечня выберите два вещества, с каждым из которых может взаимодействовать сахароза.
- углекислый газ
- сульфат натрия
- вода
- оксид серебра (р-р $NH_3$)
- гидроксид кальция…
Из предложенного перечня выберите две реакции, которые можно использовать для получения этиламина.
- C2H6 и HNO2
- C2H5NO2 и H2
- CH3OH и N2
- [C2H5NH3]Cl и KOH
- CH3CH3 и NH3
Запишите ном…
Из предложенного перечня выберите два вещества, при взаимодействии с растворами которых проявляется амфотерность глицина.
- $CH_3OH$
- $H_2SO_4$ (разб.)
- $Ca(OH)_2$
- $CH_3–CH=CH_2$
- $Na_2SO_4$
За…
Для анилина верны следующие утверждения:
- вещество, хорошо растворимое в воде
- взаимодействует с бромной водой с образованием 2,4,6‑триброманилина
- более слабое основание, чем аммиак…
Популярные материалы
3.
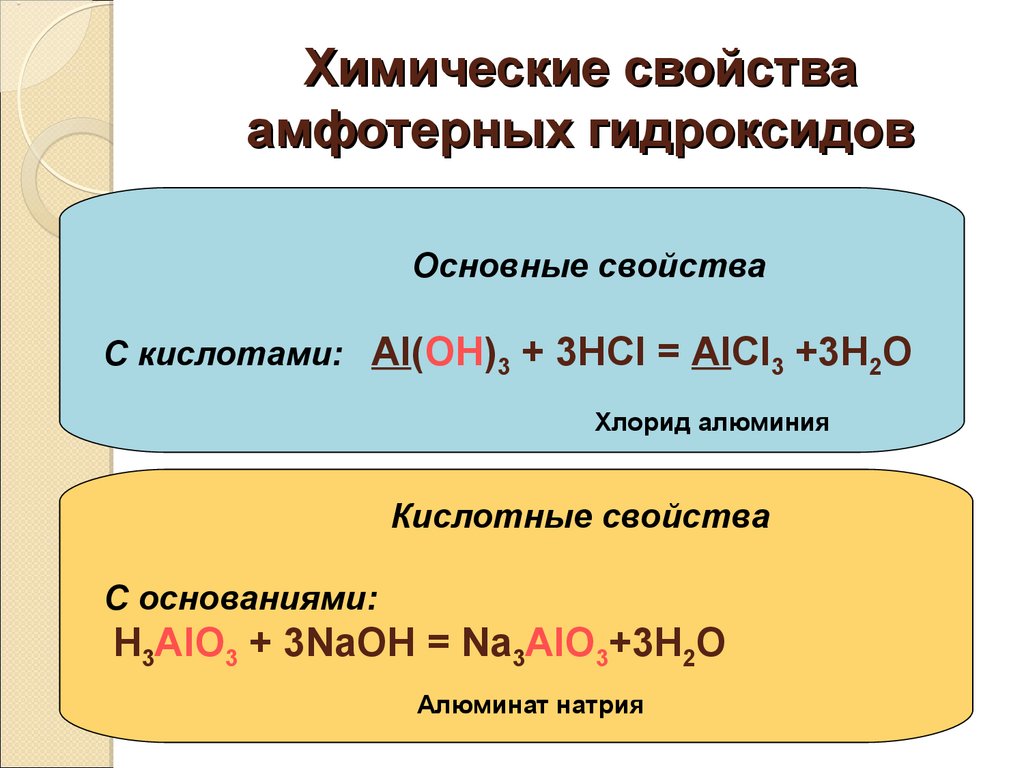 3.2 Амфотерные свойства гидроксидов некоторых элементов.
3.2 Амфотерные свойства гидроксидов некоторых элементов.Амфотерными являются следующие оксиды элементов главных подгрупп: BeO, A12O3, Ga2O3, GeO2, SnO, SnO2, PbO, Sb2O3, РоO2. Амфотерными гидроксидами являются следующие гидроксиды элементов главных подгрупп: Ве(ОН)2, А1(ОН)3, Sc(OH)3, Ga(OH)3, In(OH)3, Sn(OH)2, SnО2·nH2О, Pb(OH)2, PbО2·nH2О.
Основный характер оксидов и гидроксидов элементов одной подгруппы усиливается с возрастанием порядкового номера элемента (при сравнении оксидов и гидроксидов элементов в одной и той же степени окисления). Например, N2O3
, Р2O3, As2O3 – кислотные оксиды, Sb2O3 – амфотерный оксид, Bi2O3 – основный оксид.
Рассмотрим амфотерные свойства гидроксидов на примере соединений бериллия и алюминия.
Гидроксид алюминия проявляет амфотерные свойства, реагирует как с основаниями, так и с кислотами и образует два ряда солей:
1) в которых элемент А1 находится в форме катиона;
2А1(ОН)3 + 6НС1 = 2А1С13 + 6Н2O А1(ОН)3 + 3Н+ = А13+ + 3Н2O
В этой реакции А1(ОН)3 выполняет функцию основания, образуя соль, в которой алюминий является катионом А13+;
2) в которых элемент А1 входит в состав аниона (алюминаты).
А1(ОН)3 + NaOH = NaA1O2 + 2Н2O.
В этой реакции А1(ОН)3 выполняет функцию кислоты, образуя соль, в которой алюминий входит в состав аниона AlO2–.
Формулы
растворенных алюминатов записывают
упрощенно, имея ввиду продукт,
образующийся при обезвоживании соли.
В химической литературе можно встретить разные формулы соединений, образующихся при растворении гидроксида алюминия в щёлочи: NaA1О2 (метаалюминат натрия), Na[Al(OH)4] тетрагидроксоалюминат натрия. Эти формулы не противоречат друг другу, так как их различие связано с разной степенью гидратации этих соединений: NaA1О2·2Н2О – это иная запись Na[Al(OH)4]. При растворении А1(ОН)3 в избытке щелочи образуется тетрагидроксоалюминат натрия:
А1(ОН)3 + NaOH = Na[Al(OH)4].
При спекании реагентов – образуется метаалюминат натрия:
1000 ºС
А1(ОН)3 + NaOH ==== NaA1О2 + 2Н2О.
Таким
образом, можно говорить, что в водных
растворах присутствуют одновременно
такие ионы, как [А1(ОН)4] – или [А1(ОН)4(Н2О)2] – (для
случая, когда составляется уравнение
реакции с учетом гидратной оболочки),
а запись A1О2– является упрощенной.
Из-за способности реагировать со щелочами гидроксид алюминия, как правило, не получают действием щелочи на растворы солей алюминия, а используют раствор аммиака:
A12(SО4)3 + 6 NH3·Н2О = 2А1(ОН)3 + 3(NH4)2SО4.
Среди гидроксидов элементов второго периода амфотерные свойства проявляют гидроксид бериллия (сам бериллий проявляет диагональное сходство с алюминием).
С кислотами:
Ве(ОН)2 + 2НС1 = ВеС12 + 2Н2О.
С основаниями:
Ве(ОН)2 + 2NaOH = Na2[Be(OH)4] (тетрагидроксобериллат натрия).
В упрощенном виде (если представить Ве(ОН)2 как кислоту Н2ВеО2)
Ве(ОН)2 + 2NaOH(конц.горяч.)
= Na2BeО2 + 2H2О.
бериллат Na
Гидроксиды элементов побочных подгрупп, соответствующие высшим степеням окисления, чаще всего имеют кислотные свойства: например, Мn2О7 – НМnО4; CrО3 – H2CrО4. Для низших оксидов и гидроксидов характерно преобладание основных свойств: СrО – Сr(ОН)2; МnО – Mn(OH)2; FeO – Fe(OH)2. Промежуточные соединения, соответствующие степеням окисления +3 и +4, часто проявляют амфотерные свойства: Сr2О3 – Cr(OH)3; Fe2О3 – Fe(OH)3. Проиллюстрируем эту закономерность на примере соединений хрома (таблица 9).
Таблица 9 – Зависимость характера оксидов и соответствующих им гидроксидов от степени окисления элемента
Характерные степени окисления | Сr+2 | Сr+3 | Сr+6 |
Оксид | СrО | Сr2O3 | СrO3 |
Гидроксид | Сr(ОН)2 | Сr(ОН)3 | Н2СrO4 |
Характер | Основный | Амфотерный | Кислотный |
Взаимодействие с кислотами приводит к образованию соли, в которой элемент хром находится в форме катиона:
2Cr(OH)3 + 3H2SO 4 = Cr2(SO4)3 + 6H2O.
сульфат Cr(III)
Взаимодействие с основаниями приводит к образованию соли, в которой элемент хром входит в состав аниона:
Cr(OH)3 + 3NaOH = Na3[Cr(OH)6] + 3H2О.
гексагидроксохромат (III) Na
Оксид и гидроксид цинка ZnO, Zn(OH)2 – типично амфотерные соединения, Zn(OH)2 легко растворяется в растворах кислот и щелочей.
Взаимодействие с кислотами приводит к образованию соли, в которой элемент цинк находится в форме катиона:
Zn(OH)2 + 2HC1 = ZnCl2 + 2H2O.
Zn(OH)2 + 2NaOH = Na2[Zn(OH)4].
Или при сплавлении:
Zn(OH)2 + 2NaOH = Na2ZnO2 + 2Н2O.
Получают гидроксид цинка аналогично гидроксиду алюминия.
Какие из следующих металлических кислот проявляют амфотерную природу? ${\text{CaO}}$B. ${\text{N}}{{\text{a}}_2}{\text{O}}$C.\[{\text{BaO}}\]D. ${\text{A}}{{\text{l}}_2}{{\text{O}}_3}$
Дата последнего обновления: 06 февраля 2023 г.
•
Всего просмотров: 234,3 тыс.
•
Просмотров сегодня: 5,25 тыс.
Ответить
Подтверждено
234,3 тыс.+ просмотров
Подсказка: Чтобы ответить на этот вопрос, мы должны знать, что такое металлические, неметаллические и амфотерные оксиды. Природа оксида определяется по продукту гидролиза. Оксиды металлов ведут себя как основания. Оксиды неметаллов ведут себя как кислоты. Амфотерные оксиды ведут себя как кислоты и основания.
Полный пошаговый ответ:
Оксиды бывают трех типов: металлические, неметаллические и амфотерные. Металлические и амфотерные оксиды содержат металлы, а неметаллические оксиды — неметаллы. Оксид металла при растворении в воде образует основание, поэтому они являются основными. Оксид неметалла при растворении в воде образует кислоту, поэтому они кислые.
Некоторые оксиды металлов обычно не реагируют с водой, но реагируют с основанием, а также с кислотой, известны как амфотерные оксиды. Оксид кальция ${\text{CaO}}$ реагирует с водой с образованием основного гидроксида кальция, поэтому он является основным.
${\text{CaO}}\,{\text{ + }}\,{{\text{H}}_{\text{2}}}{\text{O}} \to \,{\ text{Ca(OH}}{{\text{)}}_2}$
Оксид натрия ${\text{N}}{{\text{a}}_2}{\text{O}}$реагирует с водой чтобы дать щелочной гидроксид натрия, поэтому он является основным.
$ {\ text {N}} {\ text {a}}_2} {\ text {O}} \, {\ text { + }} \, {{\ text {H}} _ {\ text { 2}}}{\text{O}} \to \,2\,{\text{NaOH}}$
Оксид бария ${\text{BaO}}$ реагирует с водой с образованием гидроксида бария, поэтому он базовый.
$ {\ text {BaO}} \, {\ text { + }} \, {{\ text {H}} _ {\ text {2}}} {\ text {O}} \ to \, {\ text{Ba(OH}}{{\text{)}}_2}$
Оксид алюминия${\text{A}}{{\text{l}}_2}{{\text{O}}_3}$ не реагирует с водой, поскольку нерастворим в воде.
Оксид алюминия${\text{A}}{{\text{l}}_2}{{\text{O}}_3}$ реагирует с кислотой с образованием хлорида алюминия и воды.
$ {\ text {A}} {\ text {l}} _ {\ text {2}}} {\ text {O}} _ {\ text {3}}} \, {\ text { + }} \, 6 \, {\ text {HCl}} \, \ to {\ text {2AlC}} {{\ text {l}} _ {\ text {3}}} \, {\ text { + 3 }}\,{{\text{H}}_{\text{2}}}{\text{O}}$
Оксид алюминия${\text{A}}{{\text{l}}_2} {{\text{O}}_3}$ реагирует с основанием в присутствии воды с образованием гидроксида алюминия.
${\ text {A}} {{\ text {l}} _ {\ text {2}}} {{\ text {O}} _ {\ text {3}}} \, {\ text { + }}\,2\,{\text{NaOH}}\,\, + {\text{3}}\,{{\text{H}}_{\text{2}}}{\text{O }} \to {\text{2NaAl(OH}}{{\text{)}}_4}$
Оксид алюминия ${\text{A}}{{\text{l}}_2}{{\text{ O}}_3}$ реагирует как с кислотой, так и с основанием, поэтому является амфотерным.
Итак, ${\text{A}}{{\text{l}}_2}{{\text{O}}_3}$ проявляет амфотерную природу.
Следовательно, вариант (D) ${\text{A}}{{\text{l}}_2}{{\text{O}}_3}$ верен.
Примечание. Амфотерность зависит от степени окисления металла. По мере увеличения степени окисления амфотеризм увеличивается. Из-за увеличения положительного заряда увеличивается поляризующая способность металла. Оксиды неметаллов являются кислыми. Оксиды металлов являются основными. Амфотерные оксиды бывают как кислотными, так и основными.
Недавно обновленные страницы
В Индии по случаю бракосочетания фейерверк 12 класса химии JEE_Main
Щелочноземельные металлы Ba Sr Ca и Mg могут быть устроены 12 класса химии JEE_Main
Что из следующего имеет самый высокий электродный потенциал 12 класса химии JEE_Main
Что из следующего является истинным пероксидом A rmSrmOrm2 класса 12 химии JEE_Main
Какой элемент обладает наибольшим радиусом атомов А класса 11 химии JEE_Main
Получен фосфин из следующей руды Кальций класса 12 химии JEE_Main
В Индии по случаю бракосочетания фейерверк класса 12 химии JEE_Main
Щелочноземельные металлы Ba Sr Ca и Mg могут быть организованы класс 12 химии JEE_Main
Что из следующего имеет самый высокий электродный потенциал 12 класса химии JEE_Main
Что из следующего является истинным пероксидом A rmSrmOrm2 класса 12 химии JEE_Main
Какой элемент обладает наибольшим радиусом атомов А класса 11 химии JEE_Main
Получен фосфин из следующей руды A Кальций класса 12 химия JEE_Main
Тенденции сомнения
Амфотерные поверхностно-активные вещества — Alfa Chemistry
Амфотерные поверхностно-активные вещества
Амфотерные вещества представляют собой поверхностно-активные вещества с ионным зарядом, и их свойства могут меняться между анионными свойствами, изоэлектрической нейтральной стадией и катионными свойствами в зависимости от значения pH. Амфотерные поверхностно-активные вещества обладают характеристиками устойчивости к электролитам, кислотам, щелочам и жесткой воде. Анионогенные, катионогенные и неионогенные ПАВ совместимы с амфотерными ПАВ. Основными амфотерными поверхностно-активными веществами являются N-оксид алкиламидопропиламина (АПАО), N-оксид алкилдиметиламина (АО), алкилбетаин (Bt) и алкиламидопропилбетаин (АРВ). Кокамидопропилбетаин, кокоамфоацетат и кокоамфодиацетат также являются некоторыми широко используемыми амфотерными поверхностно-активными веществами. Амфотерные вещества являются дерматологически мягкими поверхностно-активными веществами благодаря своему поведению и белковоподобной структуре. Они могут образовывать комплексы с анионными поверхностно-активными веществами, проявляют хорошие поверхностно-активные функции в широком диапазоне рН и способны снижать их раздражающие свойства, в результате чего они в основном используются в качестве мягких поверхностно-активных веществ в косметике, туалетных принадлежностях и жидкостях для мытья посуды.
Амфотерные поверхностно-активные вещества обладают характеристиками устойчивости к электролитам, кислотам, щелочам и жесткой воде. Анионогенные, катионогенные и неионогенные ПАВ совместимы с амфотерными ПАВ. Основными амфотерными поверхностно-активными веществами являются N-оксид алкиламидопропиламина (АПАО), N-оксид алкилдиметиламина (АО), алкилбетаин (Bt) и алкиламидопропилбетаин (АРВ). Кокамидопропилбетаин, кокоамфоацетат и кокоамфодиацетат также являются некоторыми широко используемыми амфотерными поверхностно-активными веществами. Амфотерные вещества являются дерматологически мягкими поверхностно-активными веществами благодаря своему поведению и белковоподобной структуре. Они могут образовывать комплексы с анионными поверхностно-активными веществами, проявляют хорошие поверхностно-активные функции в широком диапазоне рН и способны снижать их раздражающие свойства, в результате чего они в основном используются в качестве мягких поверхностно-активных веществ в косметике, туалетных принадлежностях и жидкостях для мытья посуды. Амфотерные поверхностно-активные вещества обладают многими эффектами, такими как очищение, пенообразование, эмульгирование, растворение, низкая токсичность, легкое биоразложение и так далее. Кроме того, применение амфотерных поверхностно-активных веществ тесно связано с синергетическим действием амфотерных поверхностно-активных веществ с другими поверхностно-активными веществами. Амфотерные поверхностно-активные вещества могут взаимодействовать с другими поверхностно-активными веществами, такими как неионогенные поверхностно-активные вещества, анионные поверхностно-активные вещества. Одним словом, амфотерные поверхностно-активные вещества входят в состав специальных поверхностно-активных веществ, доступных разработчикам рецептур для улучшения или разработки новых составов в соответствии с требованиями к окружающей среде, токсичности, безопасности и производительности.
Амфотерные поверхностно-активные вещества обладают многими эффектами, такими как очищение, пенообразование, эмульгирование, растворение, низкая токсичность, легкое биоразложение и так далее. Кроме того, применение амфотерных поверхностно-активных веществ тесно связано с синергетическим действием амфотерных поверхностно-активных веществ с другими поверхностно-активными веществами. Амфотерные поверхностно-активные вещества могут взаимодействовать с другими поверхностно-активными веществами, такими как неионогенные поверхностно-активные вещества, анионные поверхностно-активные вещества. Одним словом, амфотерные поверхностно-активные вещества входят в состав специальных поверхностно-активных веществ, доступных разработчикам рецептур для улучшения или разработки новых составов в соответствии с требованиями к окружающей среде, токсичности, безопасности и производительности.
Рис.1 Химическая структура гомологов AO, APAO, Bt и APB
Применение
Амфотерные поверхностно-активные вещества обладают следующими превосходными поверхностно-активными свойствами, такими как низкое раздражение кожи, глаз и слизистых оболочек, умеренная противомикробная активность, отсутствие токсичность, хорошая способность повышать мягкость, смачивающая способность, очищающая способность, пенообразующая способность, устойчивость к жесткой воде и диспергируемость известкового мыла, стабильность в условиях экстремального pH, совместимость с другими ингредиентами. Амфотерные поверхностно-активные вещества широко применяются в средствах личной гигиены, таких как увлажняющие средства для мытья тела, средства для бритья, шампуни, зубные пасты, моющие средства для контактных линз и другие косметические средства по уходу за кожей и волосами. Амфотерные поверхностно-активные вещества в значительной степени способствуют повышению вязкости косметических очищающих составов. Это, безусловно, связано с содержанием хлорида натрия, а также с синергетическим взаимодействием между анионным первичным поверхностно-активным веществом и нейтральным или положительно заряженным амфотерным соединением.
Амфотерные поверхностно-активные вещества широко применяются в средствах личной гигиены, таких как увлажняющие средства для мытья тела, средства для бритья, шампуни, зубные пасты, моющие средства для контактных линз и другие косметические средства по уходу за кожей и волосами. Амфотерные поверхностно-активные вещества в значительной степени способствуют повышению вязкости косметических очищающих составов. Это, безусловно, связано с содержанием хлорида натрия, а также с синергетическим взаимодействием между анионным первичным поверхностно-активным веществом и нейтральным или положительно заряженным амфотерным соединением.
Бытовые моющие средства
Причинами широкого использования амфотерных средств в средствах личной гигиены являются их хорошая очищающая способность и пенообразующие свойства, а также совместимость с различным pH. Имеются и другие превосходные свойства, которые приводят к применению амфотерных поверхностно-активных веществ в бытовых моющих средствах. Свойства следующие: (1) легкая биодеградация (2) сильные антиэлектролиты (3) низкая токсичность и высокая детоксикация (4) высокая эффективность при низкой концентрации (5) улучшение отмываемости. Амфотерные поверхностно-активные вещества играют роль в этих составах в качестве фосфатных структурообразователей, стабилизаторов ферментов, отбеливающих агентов и реагентов для защиты цвета. Кроме того, их можно использовать в качестве основных ПАВ в мягких моющих средствах для мытья посуды.
Свойства следующие: (1) легкая биодеградация (2) сильные антиэлектролиты (3) низкая токсичность и высокая детоксикация (4) высокая эффективность при низкой концентрации (5) улучшение отмываемости. Амфотерные поверхностно-активные вещества играют роль в этих составах в качестве фосфатных структурообразователей, стабилизаторов ферментов, отбеливающих агентов и реагентов для защиты цвета. Кроме того, их можно использовать в качестве основных ПАВ в мягких моющих средствах для мытья посуды.
Амфотерные поверхностно-активные вещества могут обеспечить совместимость каждого ингредиента жидких продуктов в сильнощелочных условиях. Амфотерные ПАВ устойчивы в сильной щелочи и обладают высокой растворимостью в щелочах, поэтому амфотерные ПАВ могут использоваться в щелочных моющих средствах на водной основе. Когда молекулы амфотерных ПАВ содержат несколько анионных групп и проявляют свойства анионов или катионов в зависимости от рН раствора, они более благоприятны для применения сильных щелочей.
