Физики раскрыли секрет того, почему вода проводит ток
https://ria.ru/20161202/1482714523.html
Физики раскрыли секрет того, почему вода проводит ток
Физики раскрыли секрет того, почему вода проводит ток — РИА Новости, 24.08.2018
Физики раскрыли секрет того, почему вода проводит ток
Ученые впервые проследили за тем, как одна молекула воды передает протоны своей «соседке», и раскрыли секрет того, почему вода пропускает ток, а другие похожие на нее вещества – не обладают таким свойством.
2016-12-02T15:39
2016-12-02T15:39
2018-08-24T12:28
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdnn21.img.ria.ru/images/152537/98/1525379896_0:313:6000:3688_1920x0_80_0_0_c8bede706fec5ea0614a0c453216b7db.jpg
сша
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og. xn--p1ai/awards/
xn--p1ai/awards/
2016
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
1920
1080
true
1920
1440
true
https://cdnn21.img.ria.ru/images/152537/98/1525379896_334:0:5667:4000_1920x0_80_0_0_bccc9455e5d59d960e66d7022cc633e4.jpg1920
1920
true
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
1
5
4. 7
7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
открытия — риа наука, сша, йельский университет, физика, вода
Открытия — РИА Наука, Наука, США, Йельский университет, Физика, Вода
МОСКВА, 2 дек – РИА Новости. Ученые впервые проследили за тем, как одна молекула воды передает протоны своей «соседке», и раскрыли секрет того, почему вода пропускает ток, а другие похожие на нее вещества – не обладают таким свойством, говорится в статье, опубликованной в журнале Science.
«Когда через воду проходит ток, атомам кислорода при этом почти не приходится двигаться. Этот процесс можно сравнить с знаменитой «колыбелью» Ньютона, набором подвешенных шариков, выстроенных в линию. Если поднять один из них и ударить им по линии, только концевые шарики будут двигаться, а остальные будут стоять на месте», — рассказывает Марк Джонсон (Mark Johnson) из Йельского университета (США).
Дистиллированная вода, как и многие другие вещества, состоящие из двух неметаллических элементов, является изолятором, почти не пропускающим электрический ток. Но если в воду добавить даже очень небольшое число ионов, ее электропроводность резко вырастает и она становится полноценным проводником. О том, почему вода проводит ток, ученые спорят уже более двух столетий.
В начале 19 века немецкий химик Теодор Гротгус предложил теорию, которая объясняла то, почему вода пропускает через себя ток и почему электричество может разлагать ее на водород и кислород. Он посчитал, что молекулы воды могут захватывать лишние протоны и передавать их друг другу, подобно палочке в эстафете, благодаря формированию новых водородных и ковалентных связей и их быстрому распаду.
Ученые раскрыли тайну происхождения воды на Земле12 ноября 2015, 22:00
Как рассказывает Джонсон, как именно протекает подобная «эстафета» и как выглядят молекулы воды, участвующие в обмене протонами, до настоящего времени никто не знал, так как проследить за этим процессом крайне сложно из-за его скоротечности и крайне малых масштабов, на которых протекает эта реакция.
Йельским химикам удалось решить эту задачу, обнаружив, что подобные реакции замедляются и становятся видными для инструментов при исполнении двух условий – охлаждения небольшого количества молекул воды почти до абсолютного нуля и использования только «тяжелой» воды – молекул, состоящих из обычного кислорода и дейтерия, тяжелого изотопа водорода.
Подсвечивая такие молекулы при помощи лучей инфракрасного лазера и наблюдая за изменениями в их спектре, ученые смогли увидеть, как свободные ионы дейтерия присоединяются к тяжелой воде, и как они «перепрыгивают» на соседнюю с ней молекулу.
Ученые нашли «соленые ручьи» из жидкой воды на Марсе28 сентября 2015, 18:10
Как показали эти наблюдения, подобные обмены идут не между отдельными молекулами воды, а между своеобразными «коллективами» их молекул, объединяющие в себе четыре молекулы h3O. Это, в целом, подтверждает то, что раньше подозревали ученые на базе компьютерных расчетов, но не могли доказать этого на практике.
Дальнейшее изучение этого процесса, как надеются химики из Йеля, поможет раскрыть другие тайны воды, в том числе ее необычно высокое поверхностное натяжение, и понять, как подобная транспортировка протонов влияет на работу нашего организма и других живых существ.
«Проводит ли дерево электричество?» — Яндекс Кью
ПопулярноеСообществаВсем привет. Случайно услышал по ТВ, что дерево вообще не проводит электричество. Так ли это? Если да, то как объяснить, что молния иногда бьет в дерево? Разве молния — это не электричество? Или я чего-то не понимаю? Не шарю в этом. В общем, объясните, пожалуйста. Заранее спасибо.
ФизикаЭлектричество+3
Алексей Иванов ·1,1 KОтветитьУточнитьИгорь СавинТоп-автор
9,0 KЭнергетик по профессии. Интересы: лингвистика, психология. · 3 сент 2022
Всё проводит электричество, только в разной степени.
Условно говоря, чтобы не сильно закапываться в теорию, если вы возьмёте батарейку и подключите её к проводнику, то в медном проводе сдвинутся 60 миллионов электронов (это не точный расчёт, просто для понимания соотношения цифр), а если эту же батарейку подключить к стальному проводу такого же размера, то там сдвинется всего 10 миллионов. А если к морской воде — то всего 3 штуки. А к стеклу нужно подключить квадриллион батареек, чтобы сдвинуть хотя бы один электрон.
А если к морской воде — то всего 3 штуки. А к стеклу нужно подключить квадриллион батареек, чтобы сдвинуть хотя бы один электрон.
Молния способна проходить сквозь воздух и дерево (и то, и другое — диэлектрики) из-за того, что обладает просто невероятно огромным зарядом, которого хватает, чтобы двигать электроны почти что где угодно.
И воздух, и дерево плохо проводят электричество по сравнению, например, с металлами, и это позволяет их использовать в быту как диэлектрики — от розетки вас через воздух ведь тоже током не бьёт. Но дерево всё-таки проводит его чуть лучше, чем воздух, поэтому мощному заряду молнии проще пройти через дерево, а не через воздух. Если рядом с деревом будет стоять металлический громоотвод — то молния, скорее, ударит в него, потому что там ещё проще.
Как-то так.
Комментировать ответ…Комментировать…Сергей Гром269Электрик, электронщик. Не чужд философии и вопросов мироустройства. · 8 сент 2022
Не проводит электричество только очень сухое дерево. Живое дерево проводит электричество, поскольку в нём присутствует вода, которая очень неплохо проводит электричество. Ведь сок любого растения в основе своей — вода. А если учесть, что в соке содержатся органические и минеральные вещества, то электропроводность его значительно увеличивается по сравнению с водой… Читать далее
Живое дерево проводит электричество, поскольку в нём присутствует вода, которая очень неплохо проводит электричество. Ведь сок любого растения в основе своей — вода. А если учесть, что в соке содержатся органические и минеральные вещества, то электропроводность его значительно увеличивается по сравнению с водой… Читать далее
🍀 Естествоиспытатель · 3 сент 2022 · shymanovsky.mooo.com
В разной степени все (или почти) материалы проводят электричество. Просто у многих — очень большое сопротивление. Поэтому считается, что они тока не проводят. Это только для простоты, чтобы никому не пришло в голову делать деревянные провода. А с деревом еще сложнее. Его сопротивление зависит еще и от влажности и от химического состава той воды, которая впиталась. Проще… Читать далее
Комментировать ответ…Комментировать…Вы знаете ответ на этот вопрос?
Поделитесь своим опытом и знаниями
Войти и ответить на вопросРжавчина никогда не спит — Лаборатория Беркли — Центр новостей лаборатории Беркли
Оксид железа (ржавчина) — плохой электрический проводник, но электроны в оксиде железа могут использовать тепловую энергию для перехода от одного атома железа к другому.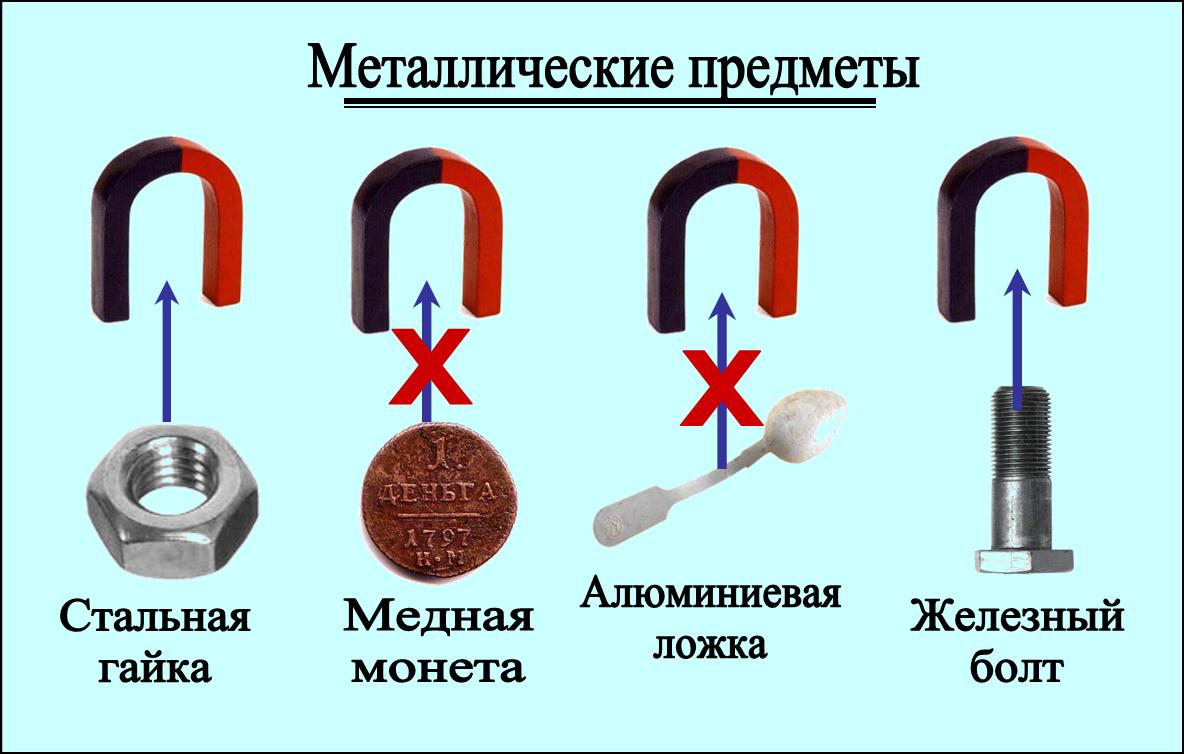 Эксперимент в лаборатории Беркли точно показал, что происходит с электронами после переноса на частицу оксида железа. (Изображение предоставлено Бенджамином Гилбертом, лаборатория Беркли)
Эксперимент в лаборатории Беркли точно показал, что происходит с электронами после переноса на частицу оксида железа. (Изображение предоставлено Бенджамином Гилбертом, лаборатория Беркли)
Ржавчина — оксид железа — плохо проводит электричество, поэтому электронное устройство с проржавевшей батареей обычно не работает. Несмотря на эту плохую проводимость, электрон, переданный частице ржавчины, будет использовать тепловую энергию, чтобы постоянно перемещаться или «прыгать» от одного атома железа к другому. Подвижность электронов в оксиде железа может иметь огромное значение для широкого спектра реакций, связанных с окружающей средой и энергией, включая реакции, связанные с ураном в подземных водах, и реакции, относящиеся к недорогим устройствам солнечной энергии. Предсказание влияния прыжков электронов на реакции оксида железа в прошлом было проблематичным, но теперь, впервые, многопрофильная группа исследователей во главе с учеными из Министерства энергетики США (DOE) Лоуренса Беркли Национальная лаборатория (Лаборатория Беркли) непосредственно наблюдала, что происходит с электронами после того, как они были перенесены на частицу оксида железа.
«Мы считаем, что эта работа является отправной точкой для новой области геохимии с временным разрешением, которая стремится понять механизмы химических реакций путем создания различных фильмов, которые в реальном времени показывают, как атомы и электроны движутся во время реакций», — говорит Бенджамин Гилберт, геохимик из отдела наук о Земле лаборатории Беркли и соучредитель Центра наногеофизических исследований Беркли, руководивший этим исследованием. «Используя сверхбыструю рентгеновскую спектроскопию с насосом-зондом, мы смогли измерить скорость, с которой электроны переносятся через спонтанные переходы от железа к железу в окислительно-восстановительных оксидах железа. Наши результаты показали, что скорости зависят от структуры оксида железа, и подтвердили правильность некоторых аспектов современной модели прыжков электронов в оксидах железа».
Гилберт является соответствующим автором статьи в журнале Science , в которой описывается эта работа. Статья называется «Маленькие электронные поляроны и их подвижность в наночастицах (оксигидроксида) оксида железа». Соавторами статьи были Джордан Кац, Сяойи Чжан, Клаус Аттенкофер, Карена Чапман, Кэтрин Франдсен, Петр Зажицки, Кевин Россо, Роджер Фальконе и Гленн Вейчунас.
Соавторами статьи были Джордан Кац, Сяойи Чжан, Клаус Аттенкофер, Карена Чапман, Кэтрин Франдсен, Петр Зажицки, Кевин Россо, Роджер Фальконе и Гленн Вейчунас.
В макромасштабе горные породы и минералы кажутся не очень реакционноспособными — подумайте о миллионах лет, которые требуются горам, чтобы вступить в реакцию с водой. Однако в наномасштабе многие распространенные минералы способны вступать в окислительно-восстановительные реакции — обмениваться одним или несколькими электронами — с другими молекулами в окружающей их среде, воздействуя на почву и воду, морскую воду, а также пресную воду. Среди наиболее важных из этих окислительно-восстановительных реакций — образование или преобразование минералов оксида железа и оксигидроксида в процессах переноса заряда, в которых железо переключается между двумя его обычными состояниями окисления — железом (III) и железом (II).
Бенджамин Гилберт, геохимик из отдела наук о Земле лаборатории Беркли, провел эксперимент, в ходе которого впервые непосредственно наблюдался термически активированный скачок электронов в частицах оксида железа.
«Поскольку железо (II) значительно более растворимо, чем железо (III), восстановительные преобразования оксида железа (III) и минералов оксигидроксида могут существенно повлиять на химический и минералогический состав почвы и поверхности», — говорит Гилберт. «В случае оксида железа (III) восстановление до железа (II) может вызвать растворение минералов в очень коротком временном масштабе, что меняет минералогию и пути потока воды. Также может происходить мобилизация железа в раствор, который может стать важным источником биодоступного железа для живых организмов».
Гилберт также отметил, что многие органические и неорганические загрязнители окружающей среды могут обмениваться электронами с фазами оксида железа. Будь то оксид железа (III) или железа (II), является важным фактором для разложения или связывания данного загрязняющего вещества. Кроме того, некоторые бактерии могут передавать электроны оксидам железа в рамках своего метаболизма, связывая окислительно-восстановительную реакцию железа с углеродным циклом.
«Подобно тому, как спортивный фотограф должен использовать камеру с очень короткой выдержкой, чтобы запечатлеть спортсмена в движении без размытия, чтобы иметь возможность наблюдать за движением электронов, нам нужно было использовать чрезвычайно короткий и очень яркий (мощный) импульс X -лучи», — говорит Джордан Кац, ведущий автор статьи Science , который сейчас работает в Университете Денисона. «Для этого исследования рентгеновские лучи были получены в усовершенствованном источнике фотонов Аргоннской национальной лаборатории».
В дополнение к коротким ярким импульсам рентгеновского излучения, Кац сказал, что ему и его соавторам также нужно было разработать экспериментальную систему, в которой они могли бы включать желаемые реакции с помощью сверхбыстрого переключателя.
Джордан Кац, в настоящее время работающий в Университете Денисона, разработал экспериментальную систему, которая синхронизировала перенос многих электронов в частицы оксида железа, чтобы можно было контролировать их совокупное поведение.
«Единственный способ сделать это в нужное время — с помощью света, в данном случае сверхбыстрого лазера», — говорит Кац. «Нам нужна была система, в которой электрон, который мы хотели изучить, мог быть немедленно введен в оксид железа в ответ на поглощение света. Это позволило нам эффективно синхронизировать перенос многих электронов в частицы оксида железа, чтобы мы могли контролировать их совокупное поведение».
С помощью своей системы спектроскопии накачки-зонда с временным разрешением в сочетании с расчетами ab initio , выполненными соавтором Кевином Россо из Тихоокеанской северо-западной национальной лаборатории, Гилберт, Кац и их коллеги определили, что скорости, с которыми электроны прыгают из одного железа переход от одного атома к другому в оксиде железа варьируется от одного прыжка в наносекунду до пяти прыжков в наносекунду, в зависимости от структуры оксида железа. Их наблюдения согласовывались с установленной моделью описания поведения электронов в таких материалах, как оксиды железа. В этой модели электроны, введенные в оксид железа, соединяются с фононами (вибрациями атомов в кристаллической решетке), искажая структуру решетки и создавая небольшие энергетические ямы или ямки, известные как поляроны.
Их наблюдения согласовывались с установленной моделью описания поведения электронов в таких материалах, как оксиды железа. В этой модели электроны, введенные в оксид железа, соединяются с фононами (вибрациями атомов в кристаллической решетке), искажая структуру решетки и создавая небольшие энергетические ямы или ямки, известные как поляроны.
«Эти небольшие поляроны электронов эффективно образуют локализованные позиции металла с более низкой валентностью, а проводимость происходит за счет термически активированных электронных прыжков с одного сайта металла на другой», — говорит Гилберт. «Измеряя скорость прыжков электронов, мы смогли экспериментально продемонстрировать, что отделение железа (II) от кристалла ограничивает скорость общей реакции растворения. Мы также смогли показать, что прыжки электронов в оксидах железа не являются узким местом для роста микробов, использующих эти минералы в качестве акцепторов электронов. Скорость переноса электронов от белка к минералу медленнее».
Кац в восторге от применения этих результатов для поиска способов использования оксида железа для сбора и преобразования солнечной энергии.
«Оксид железа — широко распространенный, стабильный и экологически чистый полупроводник, а его свойства оптимальны для поглощения солнечного света», — говорит он. «Однако, чтобы использовать оксид железа для сбора и преобразования солнечной энергии, важно понять, как электроны передаются внутри материала, который при использовании в традиционной конструкции не обладает высокой проводимостью. Подобные эксперименты помогут нам разработать новые системы с новой наноструктурной архитектурой, которые способствуют желаемым окислительно-восстановительным реакциям и подавляют вредные реакции, чтобы повысить эффективность нашего устройства».
Гилберт добавляет: «Также важна демонстрация того, что очень быстрые этапы геохимической реакции, такие как скачки электронов, могут быть измерены с помощью сверхбыстрых методов накачки-зонда».
Это исследование было поддержано Управлением науки Министерства энергетики США, которое также поддерживает усовершенствованный источник фотонов.
# # #
Национальная лаборатория Лоуренса в Беркли решает самые насущные научные проблемы мира, продвигая устойчивую энергетику, защищая здоровье человека, создавая новые материалы и раскрывая происхождение и судьбу Вселенной. Основан в 1931 марта научный опыт Berkeley Lab был отмечен 13 Нобелевскими премиями. Калифорнийский университет управляет лабораторией Беркли для Управления науки Министерства энергетики США. Для получения дополнительной информации посетите сайт www.lbl.gov.
Управление науки Министерства энергетики США является крупнейшим сторонником фундаментальных исследований в области физических наук в Соединенных Штатах и работает над решением некоторых из самых насущных проблем нашего времени. Для получения дополнительной информации посетите веб-сайт Управления науки по адресу science.
Дополнительная информация
Чтобы узнать больше об исследованиях Бенджамина Гилберта, перейдите сюда
Чтобы узнать больше об исследованиях Джордана Каца, перейдите сюда
Для получения дополнительной информации об усовершенствованном источнике фотонов перейдите сюда
Чтобы прочитать новость об этой работе из Аргоннской национальной лаборатории, перейдите сюда
Почему металлы так хорошо проводят тепло и электричество?
Структура металлов
Структуру чистых металлов легко описать, поскольку атомы, образующие эти металлы, можно представить себе как одинаковые идеальные сферы. В частности, металлическая структура состоит из «выровненных положительных ионов» (катионов) в «море» делокализованных электронов. Это означает, что электроны могут свободно перемещаться по всей структуре, что приводит к таким свойствам, как проводимость.
Какие существуют типы облигаций?
Ковалентные связи
Ковалентная связь – это связь, которая образуется, когда два атома имеют общие электроны. Примерами соединений с ковалентными связями являются вода, сахар и диоксид углерода.
Примерами соединений с ковалентными связями являются вода, сахар и диоксид углерода.
Ионные связи
Ионные связи — это полный перенос валентных электронов между металлом и неметаллом. В результате образуются два противоположно заряженных иона, которые притягиваются друг к другу. В ионных связях металл теряет электроны, становясь положительно заряженным катионом, тогда как неметалл принимает эти электроны, становясь отрицательно заряженным анионом. Примером ионной связи может быть соль (NaCl).
Металлические связи
Металлические связи являются результатом силы электростатического притяжения, возникающей между электронами проводимости (в виде электронного облака делокализованных электронов) и положительно заряженными ионами металлов. Его можно описать как совместное использование свободных электронов в решетке положительно заряженных ионов (катионов). Металлическая связь определяет многие физические свойства металлов, такие как прочность, пластичность, тепловое и электрическое сопротивление и проводимость, непрозрачность и блеск.
Делокализованные Движущиеся электроны в металлах —
Свободное движение электронов в металлах придает им проводимость.
Электропроводность
Металлы содержат свободно движущиеся делокализованные электроны. Когда прикладывается электрическое напряжение, электрическое поле внутри металла вызывает движение электронов, заставляя их перемещаться от одного конца проводника к другому. Электроны будут двигаться в положительную сторону.
Электроны текут к положительной клемме |
Теплопроводность
Металл хорошо проводит тепло. Проводимость возникает, когда вещество нагревается, частицы получают больше энергии и сильнее вибрируют. Затем эти молекулы сталкиваются с соседними частицами и передают им часть своей энергии. Затем это продолжается и передает энергию от горячего конца к более холодному концу вещества.
Почему металлы так хорошо проводят тепло?
Электроны в металле являются делокализованными электронами и являются свободно движущимися электронами, поэтому, когда они получают энергию (тепло), они вибрируют быстрее и могут перемещаться, это означает, что они могут передавать энергию быстрее.
Какие металлы лучше всего проводят ток?
Вверху: Электронные оболочки Золото (au), серебро (Ag), медь (Cu) и цинк (Zn). Логика подсказывает, что золото — лучший проводник, имеющий единственный s-орбитальный электрон в последней оболочке (см. выше)… так почему же серебро и медь на самом деле лучше (см. таблицу ниже).Электропроводность металлов | >S/м |
| Серебро | 6,30×10 7 |
| Медь | 5,96×10 7 |
| Золото | 4,10×10 7 |
| Алюминий | 3,50×10 7 |
| Цинк | 1,69×10 7 |
Серебро имеет больший атомный радиус (160 пм), чем золото (135 пм), несмотря на то, что в золоте больше электронов, чем в серебре! О причине этого см.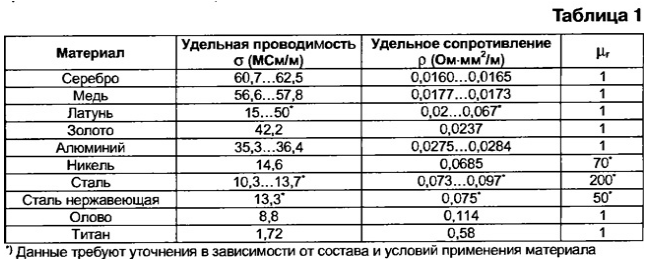 Комментарий ниже.
Комментарий ниже.
Примечание: Серебро является лучшим проводником, чем золото, но золото предпочтительнее, поскольку оно не подвержено коррозии. (Медь является наиболее распространенной, потому что она наиболее экономична) Ответ немного сложен, и мы размещаем здесь один из лучших ответов, которые мы видели для тех, кто знаком с материалом.«Серебро находится посередине среди переходных металлов, примерно на полпути между благородными газами и щелочными металлами. В столбце 11 периодической таблицы все эти элементы (медь, серебро и золото) имеют одну букву s -орбитальный электрон внешней оболочки электрона (также платина, в столбце 10).
Орбитальная структура электронов этих элементов не имеет особого сродства ни к получению электрона, ни к потере электрона по отношению к инертным газам, которые тяжелее или легче, потому что они находятся на полпути между ними.
В целом это означает, что не требуется много энергии, чтобы временно выбить электрон или временно добавить его. Удельное сродство к электрону и потенциалы ионизации варьируются, и, что касается проводимости, наличие относительно низких энергий для этих двух критериев несколько важно.
Если бы это были единственные критерии, то золото было бы лучшим проводником, чем серебро, но у золота есть дополнительные 14 f-орбитальных электронов под 10 d-орбитальными электронами и единственным s-орбитальным электроном. 14 f-электронов связаны с дополнительными атомами в ряду актинидов. С 14 дополнительными электронами, очевидно, выталкивающими электроны d и s, вы могли бы подумать, что s-электрон просто сидит там, «созревший» для проводимости (вряд ли требуется какая-либо энергия, чтобы оттолкнуть его), но НЕЕЕЕТ. Электроны f-орбиты упакованы таким образом, что атомный радиус золота на самом деле МЕНЬШЕ атомного радиуса серебра — ненамного, но он меньше.

 В целом это означает, что не требуется много энергии, чтобы временно выбить электрон или временно добавить его. Удельное сродство к электрону и потенциалы ионизации варьируются, и, что касается проводимости, наличие относительно низких энергий для этих двух критериев несколько важно.
В целом это означает, что не требуется много энергии, чтобы временно выбить электрон или временно добавить его. Удельное сродство к электрону и потенциалы ионизации варьируются, и, что касается проводимости, наличие относительно низких энергий для этих двух критериев несколько важно. 