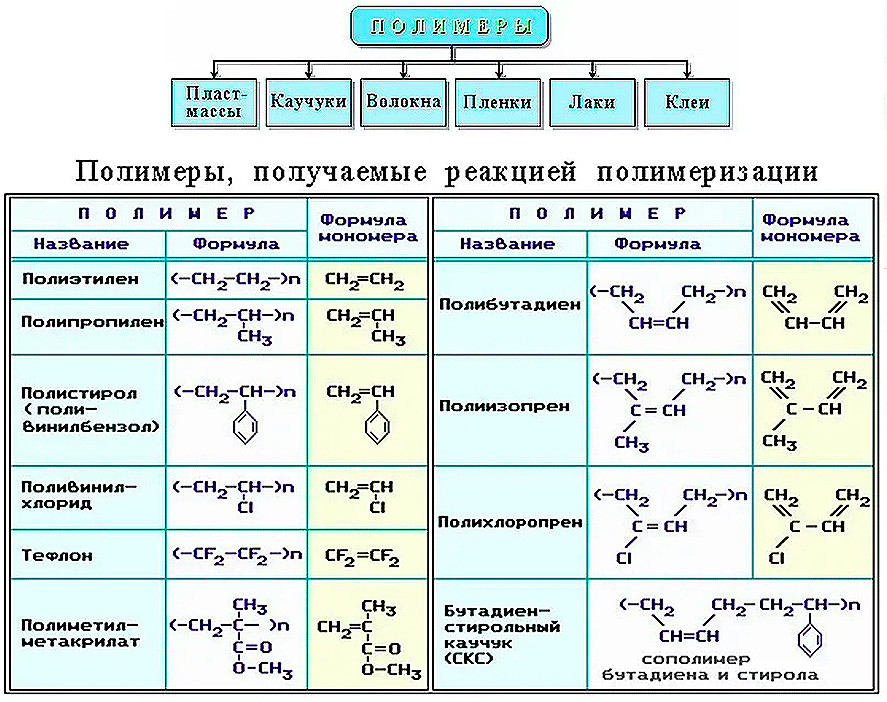
Полиэтилен, структурная формула, свойства
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
ФосфорФосфор
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
КриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИридийИридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Полиэтилен, формула: основные свойства и виды
Что собой представляет полиэтилен? Формула данного вещества относится к ряду непредельных углеводородов. Рассмотрим подробнее особенности данного соединения, выявим его основные области применения.
Особенности строения
Полиэтилен, формула которого имеет вид (С2Н4)n, представляет собой высокомолекулярное органическое вещество. В его структуре есть двойная связь между углеродными атомами, что свидетельствует о непредельном характере. Величина валентного угла – 120 градусов, тип гибридизации в данном веществе SP2.
Физические свойства
Полиэтилен, формула мономера которого относится к ряду (Cnh3)n, представляет собой белое твердое вещество, нерастворимое в воде. Отметим также стойкость данного органического продукта к действию бензина, ацетона, сильных кислот, исключая концентрированную серную кислоту.
Получение
Полиэтилен получают из вещества, формула которого имеет вид С2Н4. Именно этилен выступает в качестве мономера для процесса полимеризации. В последние годы наблюдается тенденция резкого увеличения объемов производства полиэтилена, так как возросла потребность в нем в различных промышленных производствах. Учитывая, что формула структурного звена полиэтилена имеет вид -СН2-СН2-, сам процесс можно представить в следующем виде:
Именно этилен выступает в качестве мономера для процесса полимеризации. В последние годы наблюдается тенденция резкого увеличения объемов производства полиэтилена, так как возросла потребность в нем в различных промышленных производствах. Учитывая, что формула структурного звена полиэтилена имеет вид -СН2-СН2-, сам процесс можно представить в следующем виде:
- nC2h5=(-СН2-СН2-)n.
Если дано задание: «Укажите формулу элементарного звена полиэтилена», в качестве ответа нужно представить структурное звено.
Виды полиэтилена
В настоящее время выпускается полиэтилен, формула которого не отличается от классического вида, но есть определенные отличия в свойствах продукта. Например, ПЭНП имеет низкую плотность, а ПЭВП отличается повышенной плотностью материала. В России видовую структуру ограничивают двумя видами: ПЭВП и ПЭНП.
В перерабатывающей отрасли в основном применяется упаковка и тара, элементы трубопровода, полиэтиленовые пленки, изоляция для кабелей, товары бытового предназначения. Среди основных производителей ПЭНП лидируют изготовители пленок.
Среди основных производителей ПЭНП лидируют изготовители пленок.
Особенности применения
Полиэтилен прост в механической обработке, подвергается свариванию. Благодаря отличным диэлектрическим свойствам, можно использовать данное вещество в электротехнике. Максимальной востребованностью обладает полиэтилен низкой плотности, формула которого была записана выше.
Именно полиэтилен является самым недорогим полимером, который используется в разных отраслях современной промышленности.
В кабельной промышленности, благодаря полиэтилену, получают существенную экономию меди, хлопчатобумажной ткани, свинца, иных материалов, имеющих высокую стоимость. Такой переход на провода и кабеля с полимерной изоляцией сократил трудоемкость процесса, упростил технологию применения сополимеров этилена.
Сельское хозяйство
Востребованы полиолефины также в сельском хозяйстве. Отличный экономический эффект получают путем использования полиэтилена в овощеводстве при строительстве парников, теплиц. Получаемые сооружения имеют упрощенную конструкцию, поэтому их стоимость ниже стеклянных аналогов примерно в три раза.
Получаемые сооружения имеют упрощенную конструкцию, поэтому их стоимость ниже стеклянных аналогов примерно в три раза.
Прозрачные полиолефиновые материалы отлично пропускают ультрафиолетовые лучи, в результате чего существенно сокращаются сроки созревания овощных культур. Полиэтиленовой пленкой укрывают бурты зерна и овощей при продолжительном хранении их в поле. Из данного материала изготавливают мешки, в которых хранят минеральные удобрения. Пленка нужна и для процесса силосования. Благодаря хранению в полиэтиленовых мешках силоса, нет необходимости строить дорогие башни, тратить средства и время на процедуры разгрузки и загрузки.
Полимерные пленки, изготовленные на основе полиэтилена, позволяют увеличивать урожайность плодово-ягодных культур, ограничивать испарение из почв влаги, а также тормозить рост сорных растений.
Применение полиэтилена в животноводстве
Мы уже выяснили, какова формула полиэтилена: (-СН2-СН2-)n. Проанализируем значимость данного химического соединения для молочных ферм. Именно это органическое соединение применяется для изготовления различной тары: бидонов, бочек, ведер, банок, доильных аппаратов. Полиэтиленовые трубы удобны для перекачки молока. Металлические аналоги, применяемые на протяжении длительного времени, доказали свою несостоятельность. Помимо высокой стоимости, они подвергаются химической и атмосферной коррозии, а полиэтилен устойчив к этим процессам.
Именно это органическое соединение применяется для изготовления различной тары: бидонов, бочек, ведер, банок, доильных аппаратов. Полиэтиленовые трубы удобны для перекачки молока. Металлические аналоги, применяемые на протяжении длительного времени, доказали свою несостоятельность. Помимо высокой стоимости, они подвергаются химической и атмосферной коррозии, а полиэтилен устойчив к этим процессам.
Пленка, выполненная из этого органического соединения, подходит для облицовки оросительных систем и каналов. По стоимости она будет дешевле бетонных аналогов примерно в три раза. Из полиэтилена низкого и высокого давления и его сополимеров производят гибкие шланги, применяемые в процессе полива сельскохозяйственных плантаций.
Строительная отрасль
Полиолефины востребованы в судостроении, автомобилестроении, машиностроении. Их них изготавливают трубы и разнообразные санитарно-технические изделия. На базе полиэтилена получают разнообразные композиции, вводя в полимер наполнители и определенные добавки.
К примеру, композицию ПЭВД с канальной сажей применяют при покрытии кабелей. Полученный материал выдерживает высокие давления жидкости, движущейся по трубам.
Для производства арматуры, разнообразных жестких конструкций применяют ПЭСД и ПЭНД, а также используют полипропилен. Из них производят гальванические ванны, струйные насосы, вентиляционные установки, оросительные колонны.
Заключение
Полиэтилен востребован и в отраслях, занимающихся производством предметов домашнего обихода. Из данного полимера создают разнообразные игрушки, зубные щетки, ведра, тазики, кувшины, разнообразные предметы, востребованные хозяйками.
Полиэтилен подходит для изготовления упаковочной тары для фармацевтической, парфюмерной, пищевой промышленности. Благодаря внешнему эстетичному виду, легкости, прочности, данный материал становится перспективным веществом для производства универсальных полочных систем, кресел, стульев.
В текстильном машиностроении полиэтилен востребован при создании шпулей, бобин. Данный полимер подходит для изготовления определенных узлов стиральных машин, вентиляционных систем, электрических приборов.
Данный полимер подходит для изготовления определенных узлов стиральных машин, вентиляционных систем, электрических приборов.
Полиэтиленовая пленка при нагревании подвергается усадке, плотно прилегая к предмету, материал повторяет его форму.
Если в двадцатом веке для изготовления изоляционных материалов применялась минеральная вата и пенополистирол, то в настоящее время разрабатываются абсолютно новые теплоизоляторы, базирующиеся на ППЭ (вспененном полиэтилене).
Данный материал создают из вспененного пористого гибкого полиэтилена, который предназначается для упаковки посуды и бьющихся предметов, промышленной техники, микроэлектроники. Данный продукт, получаемый из полиэтилена, востребован при изготовлении звукоизоляционных и гидроизоляционных материалов. Несмотря на то что стоимость у такой продукции будет немного выше, чем у традиционных теплоизоляционных материалов, она окупается отличными теплоизоляционными характеристиками. Такие материалы выдерживают диапазон температур от -60 до +95 градусов, имеют средний эксплуатационный срок службы порядка пятидесяти лет.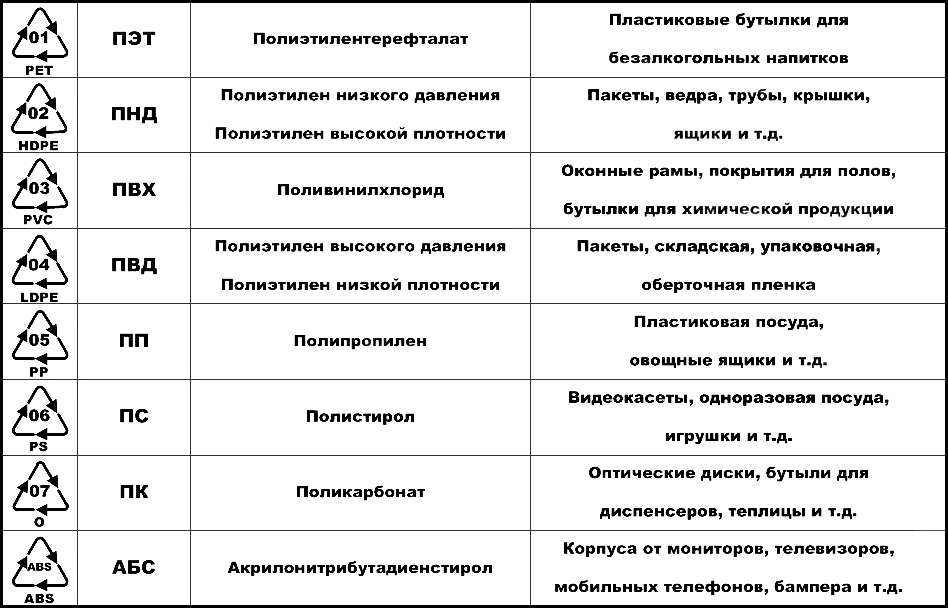 Полиэтилен по праву можно считать востребованным материалом, имеющим множество областей применения.
Полиэтилен по праву можно считать востребованным материалом, имеющим множество областей применения.
ICSC 1488 — ПОЛИЭТИЛЕН
ICSC 1488 — ПОЛИЭТИЛЕН« вернуться к списку результатов поиска
Китайский — ZHАнглийский — ENФинский — FIFФранцузский — FRНемецкий — DEИврит — HEВенгерский — HUIИтальянский — ITЯпонский — JAKКорейский — KOPперсидский — FAПольский — PLПортугальский — PTРусский — RUSиспанский — ES
| ПОЛИЭТИЛЕН | ICSC: 1488 (октябрь 2004 г.) |
| ПЭВП ПЭНП Этен, гомополимер Полимеры этилена ПЭ | |
| Номер CAS: 9002-88-4 |
| ОСТРЫЕ ОПАСНОСТИ | ПРЕДУПРЕЖДЕНИЕ | ПОЖАРОТУШЕНИЕ | |
|---|---|---|---|
| ПОЖАР И ВЗРЫВ | Горючий. При пожаре выделяет раздражающие или токсичные пары (или газы). Мелкодисперсные частицы образуют в воздухе взрывоопасные смеси. При пожаре выделяет раздражающие или токсичные пары (или газы). Мелкодисперсные частицы образуют в воздухе взрывоопасные смеси. | НЕТ открытого пламени. Замкнутая система, пылевзрывозащищенное электрооборудование и освещение. Предотвратить осаждение пыли. | Используйте распыление воды, порошка, пены, двуокиси углерода. |
| СИМПТОМЫ | ПРЕДУПРЕЖДЕНИЕ | ПЕРВАЯ ПОМОЩЬ | |
|---|---|---|---|
| Вдыхание | Кашель. | Избегайте вдыхания пыли. | Свежий воздух, отдых. |
| Кожа | Снять загрязненную одежду. Промойте, а затем вымойте кожу водой с мылом. | ||
| Глаза | Наденьте защитные очки. | Сначала промыть большим количеством воды в течение нескольких минут (снять контактные линзы, если это возможно), затем обратиться за медицинской помощью. | |
| Проглатывание | Не ешьте, не пейте и не курите во время работы. | ||
| ЛИКВИДАЦИЯ УТЕЧЕК | КЛАССИФИКАЦИЯ И МАРКИРОВКА |
|---|---|
| Смести просыпанное вещество в закрытые подходящие промаркированные контейнеры. При необходимости сначала увлажните, чтобы предотвратить запыление. Индивидуальная защита: респиратор с противоаэрозольным фильтром, адаптированный к концентрации вещества в воздухе. | В соответствии с критериями СГС ООН Транспорт |
| ХРАНЕНИЕ | |
| Отдельно от несовместимых материалов. См. Химическая опасность. | |
| УПАКОВКА | |
| ПОЛИЭТИЛЕН | КМГС: 1488 |
| ФИЗИЧЕСКАЯ И ХИМИЧЕСКАЯ ИНФОРМАЦИЯ | |
|---|---|
Физическое состояние; Внешний вид Физические опасности Химическая опасность | Формула: (C 2 H 4 )n |
| ВОЗДЕЙСТВИЕ И ВЛИЯНИЕ НА ЗДОРОВЬЕ | |
|---|---|
Пути воздействия Последствия кратковременного воздействия | Опасность при вдыхании Последствия длительного или многократного воздействия |
| ПРЕДЕЛЫ ВОЗДЕЙСТВИЯ НА РАБОЧЕМ МЕСТЕ |
|---|
| ОКРУЖАЮЩАЯ СРЕДА |
|---|
| ПРИМЕЧАНИЯ |
|---|
| LDPE означает полиэтилен низкой плотности; HDPE означает полиэтилен высокой плотности. Физико-химические свойства зависят от молекулярной массы. Термическое разложение начинается при 290°C. Изделия из полиэтилена доступны в большом количестве различных форм благодаря добавкам, используемым в производстве. Добавки могут влиять на физические и токсикологические свойства этого вещества. |
| ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ |
|---|
| Классификация ЕС |
Все права защищены. Опубликованный материал распространяется без каких-либо явных или подразумеваемых гарантий.
Ни МОТ, ни ВОЗ, ни Европейская комиссия не несут ответственности за интерпретацию и использование информации, содержащейся в этом материале. Опубликованный материал распространяется без каких-либо явных или подразумеваемых гарантий.
Ни МОТ, ни ВОЗ, ни Европейская комиссия не несут ответственности за интерпретацию и использование информации, содержащейся в этом материале. | |
горение — Какова эмпирическая формула полиэтилена?
спросил
Изменено 6 лет, 3 месяца назад
Просмотрено 5к раз
$\begingroup$
Полиэтилен представляет собой полимер только из углерода и водорода. Если 2,300 г полимера сжечь в кислороде, получится 2,955 г H3O и 7,217 г CO2. Какова эмпирическая формула полиэтилена?
Итак, мой метод решения этой проблемы таков: 1) найти массу углерода из СО2 2) найти массу Н по h30 3) Найдите массу O, вычитая 4) продолжение ответ с формулой из % состава
Следовательно:
(7,217 г x 1 моль x 1 моль углерода x 12 грамм) / 44 г CO2 = 1,96 г (2,955 г x 1 моль x 2 моль водорода x 1 г) / 18 г h3O = 0,328 г
1,96 г / 12 г = 0,163 0,328 / 16 г = 0,0205 (наименьший #)
. 163 / .0205 = 8 углерод
.0205 / .0205 = 1 Водород
163 / .0205 = 8 углерод
.0205 / .0205 = 1 Водород
Ответ Ч3 :/, но я затрудняюсь понять где я споткнулся 🙁
- горение
$\endgroup$
1
$\begingroup$
$1 \dfrac{\rm{моль(C)}}{\rm{моль(\ce{CO2})}}*\dfrac{7,217 ~\rm{г(CO2)}}}{44,01 ~\rm г (\ce{CO2})/\rm{моль(\ce{CO2})}} = 0,1640 ~\rm{моль(C)}$
$2 \dfrac{\rm{моль(H)}}{\rm{моль(h3O)}}*\dfrac{2,955 ~\rm{g(h3O)}}{18,015 ~\rm g(\ce{ h3O})/\rm{mol(\ce{h3O})}} = 0,3281~\rm{mol(H)}$
Так как меньше молей C, нормализовать по C
$\rm C = 1$
$\rm H = \dfrac{0,3281}{0,1640} = 2,000 $
Итак, эмпирическая формула $\ce{Ch3}$
$\endgroup$
$\begingroup$
Несколько комментариев. Во-первых, использование констант с таким малым числом значащих цифр является плохой практикой, поскольку константы вносят свой вклад в погрешность результатов. H имеет молярную массу 1,0079.7, C 12.011 и O 15.9994 без использования 1.008, 12.001 и 15.999 неаккуратно/лениво. Я получил массу C как 1,969686 (игнорировать значащие цифры «внутри» вычислений лучше, чем пытаться управлять ими; придайте значимость результатам после того, как вы закончите с числами. Вы получили массу 1,96. Один из нас очень ошибка 2% 1,96 против 1,97 ИЗ РАСЧЕТА действительно непростительна (если только вы не делаете это в своей голове, или вам это нужно, чтобы ваш космический корабль не разбился в следующие 2 минуты и делаете это на стене собственной кровью …). Далее, ваш «расчет»: (7,217 г x 1 моль x 1 моль углерода x 12 грамм) / 44 г CO2 — это ДРУГОЙ. Использование ненужных скобок предполагает, что вы не понимаете, когда их использовать, но это небольшая проблема Размерный анализ (работа с единицами измерения) этого расчета приводит к тому, что ваши «конечные» единицы будут (граммы² x моли x моли C ÷ граммы CO2)
Это свидетельствует о глубоком непонимании того, что вы делаете.
H имеет молярную массу 1,0079.7, C 12.011 и O 15.9994 без использования 1.008, 12.001 и 15.999 неаккуратно/лениво. Я получил массу C как 1,969686 (игнорировать значащие цифры «внутри» вычислений лучше, чем пытаться управлять ими; придайте значимость результатам после того, как вы закончите с числами. Вы получили массу 1,96. Один из нас очень ошибка 2% 1,96 против 1,97 ИЗ РАСЧЕТА действительно непростительна (если только вы не делаете это в своей голове, или вам это нужно, чтобы ваш космический корабль не разбился в следующие 2 минуты и делаете это на стене собственной кровью …). Далее, ваш «расчет»: (7,217 г x 1 моль x 1 моль углерода x 12 грамм) / 44 г CO2 — это ДРУГОЙ. Использование ненужных скобок предполагает, что вы не понимаете, когда их использовать, но это небольшая проблема Размерный анализ (работа с единицами измерения) этого расчета приводит к тому, что ваши «конечные» единицы будут (граммы² x моли x моли C ÷ граммы CO2)
Это свидетельствует о глубоком непонимании того, что вы делаете. В моле СО2 содержится 1 моль С и два моля О. Вы, наверное, это знаете. Это означает, что имеется 12,011 грамма C и 31,998 граммов O в одном моле (44,009 грамма) CO2. Вычисление равно 12,011 (грамм C)/(12,011 +31,998)(всего грамм) = 0,2729 (г C/г всего), и нет ничего плохого в том, чтобы утверждать, что это 0,2729 без каких-либо единиц (г/г «отмена») и соотношение может использоваться без необходимости продолжать управлять своими единицами, что упрощает дальнейшие вычисления. Это правда, что 7 г CO2 можно умножить на 0,2729, чтобы получить 1,97 г C. (обратите внимание, что если мы перенесем единицы отношения 0,27 гC/gTot, анализ размерностей даст нам gTot (то же, что и gCO2) x gC /gTot, который дает нам единицы gC → показывает, что мы сделали это правильно (другими словами, может быть полезно использовать единицы измерения в расчетах) Вы должны ОБРАТИТЬ ВНИМАНИЕ, что «кроты» здесь не участвуют, хотя, возможно, Вы можете утверждать, что это не 12,011 г C, а 12,011 г C на моль (или на моль C).
В моле СО2 содержится 1 моль С и два моля О. Вы, наверное, это знаете. Это означает, что имеется 12,011 грамма C и 31,998 граммов O в одном моле (44,009 грамма) CO2. Вычисление равно 12,011 (грамм C)/(12,011 +31,998)(всего грамм) = 0,2729 (г C/г всего), и нет ничего плохого в том, чтобы утверждать, что это 0,2729 без каких-либо единиц (г/г «отмена») и соотношение может использоваться без необходимости продолжать управлять своими единицами, что упрощает дальнейшие вычисления. Это правда, что 7 г CO2 можно умножить на 0,2729, чтобы получить 1,97 г C. (обратите внимание, что если мы перенесем единицы отношения 0,27 гC/gTot, анализ размерностей даст нам gTot (то же, что и gCO2) x gC /gTot, который дает нам единицы gC → показывает, что мы сделали это правильно (другими словами, может быть полезно использовать единицы измерения в расчетах) Вы должны ОБРАТИТЬ ВНИМАНИЕ, что «кроты» здесь не участвуют, хотя, возможно, Вы можете утверждать, что это не 12,011 г C, а 12,011 г C на моль (или на моль C).