Температура — водородное пламя — Большая Энциклопедия Нефти и Газа, статья, страница 2
Cтраница 2
Наиболее вероятна термоэмиссия электронов из углеродных атомов, так как в пламенно-ионизационном детекторе температура водородного пламени достигает 800 — 900 С. Такая температура недостаточна для интенсивной термоэлектронной эмиссии, однако тот низкий коэффициент ионизации ( примерно один ион на миллион атомов углерода), который характерен для пламенно-ионизационного детектора, вполне допускает, что энергия некоторых углеродных атомов при получении дополнительной энергии от водородного пламени становится достаточной для отрыва электрона. [16]
Дифференциальные детекторы основаны на измерении плотности газа ( газовые весы), теплопроводности газа, диэлектрической постоянной, на сжигании веществ и определении образовавшейся двуокиси углерода, определении температуры водородного пламени ( пламенные) и других свойств. [17]
[17]
Поэтому такую смесь называют гремучим газом.
| Схема термохимического де — [ IMAGE ] 13. Схема пламенного тектора. детектора. [19] |
К термохимическому детектору близок по принципу действия разработанный Скоттом пламенный детектор. Температура водородного пламени ( и высота факела) возрастает, если к водороду примешивают различные горючие вещества. Обычно чувствительным элементом служит термопара, находящаяся на некоторой высоте над пламенем. [20]
Измерение температур углеводородных и водородных пламен по излучению вблизи 6 67мкм ( соответствует полоса поглощения воды 6 27 мкм) производится, по-видимому, впервые. Использование этой полосы для целей пирометрии пламен обладает определенными достоинствами.
Водород в качестве горючего газа применяют очень редко. Это объясняется низкой температурой водородного пламени и отсутствием такого энергичного восстановителя, как углерод, вследствие чего диссоциация многих соединений происходит не полностью, а результаты анализа подвержены большим помехам. Водородное пламя практически невидимо. Кроме того, по сравнению с другими газами, водород обладает значительно большей способностью проникать через неплотности. Поэтому при работе с ним требуется особая осторожность. Водородное пламя удобно для определения гидридобразующих элементов, так как они перед тем, как попасть в пламя, отделяются от основы.
Пламенный детектор, предложенный Скоттом [97], основан на измерении температуры водородного пламени при сгорании элюента на выходе из эжектора малого размера. При появлении органического компонента в газе-носителе, которым является водород, пламя удлиняется и охватывает термопару, помещенную несколько выше нормального положения водородного пламени. Сигнал с термопары записывается. [23]
Горелку ПИД обычно изготовляют из нержавеющей стали, платины или кварца. Материал горелки должен обладать термической и химической стабильностью и не должен плавиться при температуре водородного пламени
. Форма пламени имеет большое значение для работы ПИД. Существует определенное соотношение между расходами водорода и газа-носителя и диаметром сопла горелки. Так, при работе с насадочными колонками и при расходе газа-носителя около 30 — 50 мл / мин диаметр сопла обычно выбирают равным 0 5 — 0 8 мм. Для капиллярных колонок применяются горелки с отверстием около 0 3 мм. Некоторые фирмы прилагают к ПИД набор горелок с различными диаметрами отверстий. Электроды детектора с целью увеличения их термической и химической стабильности обычно изготовляют из платины.
[24]
Для капиллярных колонок применяются горелки с отверстием около 0 3 мм. Некоторые фирмы прилагают к ПИД набор горелок с различными диаметрами отверстий. Электроды детектора с целью увеличения их термической и химической стабильности обычно изготовляют из платины.
[24] Горелку ПИД обычно изготовляют из нержавеющей стали, платины или кварца. Материал горелки должен обладать термической и химической стабильностью и не должен плавиться при температуре водородного пламени. Форма пламени имеет большое значение для работы ПИД. Существует определенное соотношение между расходами водорода и газа-носителя и диаметром сопла горелки. Так, при работе с насадочнымн колонками и при расходе газа-носителя около 30 — 50 мл / мин диаметр сопла обычно выбирают равным 0 5 — 0 8 мм. Для капиллярных колонок применяются горелки с отверстием около 0 3 мм. Некоторые фирмы прилагают к ПИД набор горелок с различными диаметрами отверстий. Электроды детектора с целью увеличения их термической и химической стабильности обычно изготовляют из платины.
Принцип его работы состоит в том, что введение органического вещества в водородное пламя в воздухе или в кислороде вызывает образование ионов, благодаря которым возникает ионный ток между электродами детектора, находящимися под напряжением. Действие ПИД основано на двух процессах: 1) термическом разложении органических молекул при температуре водородного пламени
и 2) окислении атома углерода. [26] В этом типе детектора поток выходящего из колонки газа смешивается с постоянным потоком водорода и образующаяся смесь входит в горелку, в отверстии которой горит маленькое пламя. Окружающее пространство поставляет необходимый для горения воздух. Температура водородного пламени при подаче в горелку лишь чистого газа-носителя дает фоновый отклик детектора. При попадании в поток газа компонента, прошедшего через хроматографическую колонку, в горелке происходит соответствующее изменение температуры пламени. Измерение температуры производится при помощи термопары.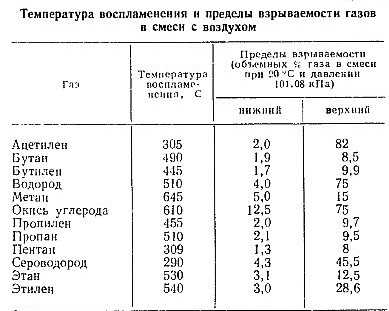 Аналитическим свойством является способность изменять температуру пламени; сигнал представляет собой тепло, образующееся при сгорании, а истинный сигнал соответствует разности в температуре пламени в присутствии и отсутствие компонентов растворенного вещества в выходящем из колонки потоке.
[27]
Аналитическим свойством является способность изменять температуру пламени; сигнал представляет собой тепло, образующееся при сгорании, а истинный сигнал соответствует разности в температуре пламени в присутствии и отсутствие компонентов растворенного вещества в выходящем из колонки потоке.
[27]
Водород плохо растворяется в воде. В воздухе и кислороде горит несветящимся пламенем с образованием воды. Температура водородного пламени довольно высокая ( до 3000 С), особенно при избытке кислорода. Поэтому во-дородно-кислородным пламенем пользуются для резки и сварки тугоплавких материалов. [28]
При поджигании смеси 2 объемов водорода с 1 объемом кислорода соединение газов происходит почти мгновенно во всей массе смеси и сопровождается сильным взрывом. Поэтому такую смесь называют гремучим газом. Таким образом, при горении водорода выделяется большое количество теплоты. Температура водородного пламени может достигать 2800 С. Водородно-кислородным пламенем пользуются для сварки и резки металлов, для плавления тугоплавких металлов.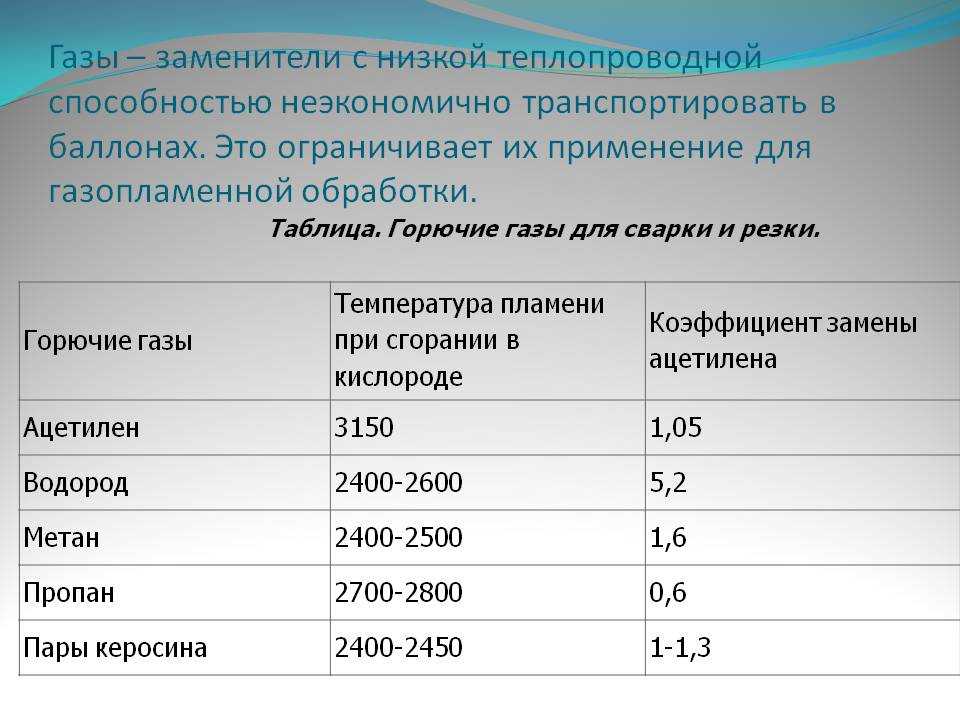 [29]
[29]
При поджигании смеси 2 объемов водорода с 1 объемом кислорода соединение газов происходит почти мгновенно по всей массе смеси и сопровождается сильным взрывом. Поэтому такую смесь называют гремучим газом. Таким образом, при горении водорода выделяется большое количество теплоты. Температура водородного пламени может достигать 2800 С. Водородно-кислородным пламенем пользуются для сварки и резки металлов, для плавления тугоплавких металлов. [30]
Страницы: 1 2 3
Море синее зажгли, или Еще о научных сенсациях Сообщение о том, что американский инженер «зажег» воду, одни назвали открытием века, другие
Занимаясь поиском лекарства от рака, Джон Канзиус решил попробовать опреснять воду. Опресняя воду, он обнаружил, что под действием радиоволн из соленой воды выделяется водород, который можно сжигать, получая температуру более 1600 градусов Цельсия. После того как Канзиус продемонстрировал миру свой аппарат, мнения разделились: одни считают, что ловкий мистификатор пытается продать вечный двигатель, другие — что наконец-то найдено альтернативное топливо.
История
В 2002 году житель острова Санибель (Sanibel), штат Флорида, Джон Канзиус (John Kanzius), бывший инженер телекоммуникационных сетей из города Эри (Erie), штат Пенсильвания, узнал, что он болен лейкемией. Пройдя несколько курсов химиотерапии, пенсионер решил найти иной способ лечения рака, чтобы в будущем избавить и других, и себя от подобных страданий.
В 2003 году Канзиусу пришла в голову мысль бороться с болезнью при помощи радиоволн. По замыслу изобретателя, в опухоль вводятся наночастицы металла (например, золота), затем пациента облучают радиоволнами, которые нагревают металл. От высокой температуры раковые клетки погибают. Канзиус подал заявку, и даже не одну, на патент. В связи с чудо-аппаратом имя Канзиуса появилось в прессе уже зимой 2007 года.
Когда изобретатель демонстрировал свой аппарат медикам в одном из исследовательских центров США, кто-то заметил на дне пробирки осадок и предложил Канзиусу попробовать использовать радиоволны для опреснения воды.
Канзиус последовал совету, и от случайной искры вода, находящаяся под воздействием радиоволн, вспыхнула. Очень скоро инженер научился достигать температуры, достаточной, чтобы расплавить пробирку. Весной 2007 года Канзиус снова появился в СМИ, уже как открыватель альтернативного горючего (обратим внимание, что знаменитого человека все считают своим: пенсильванские СМИ подчеркивают, что он «из Эри», а флоридские гордятся тем, что он «с острова Санибель»).
За лето Канзиус продемонстрировал свой аппарат СМИ, энергетическим компаниям, ученым и прочим любопытствующим. Наконец, осенью последовало авторитетное подтверждение: профессор Растум Рой (Rustum Roy), специалист по науке о материалах, сотрудник ряда университетов, воспроизвел эксперимент в университете штата Пенсильвания и заявил, что все правда: вода горит.
Аппарат Канзиуса в действии Кадр WBPF TV.
Lenta.ru
Горит, конечно, не вода, это лишь броский заголовок для привлечения внимания (в российских СМИ, благодаря Корнею Ивановичу Чуковскому, еще более популярный, чем в западных: мол, теперь каждая лисичка может взять спички, микроволновку — и туши потом моря и океаны).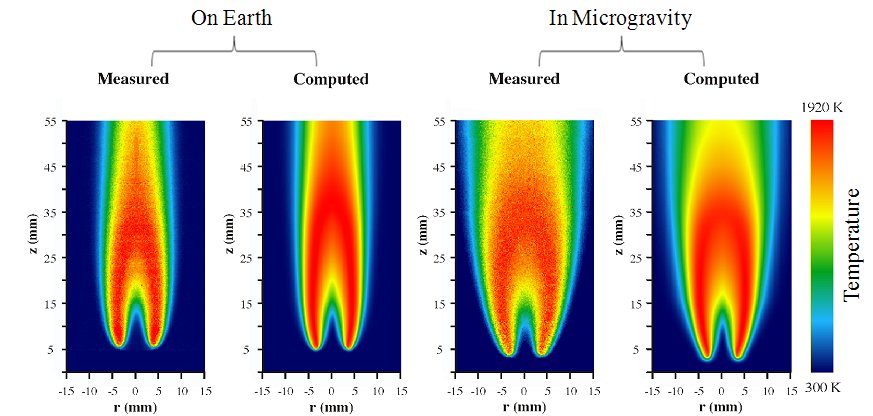 Горит водород, который выделяется из воды под действием радиоволн: в этом и состоит «соль» открытия (кстати, соль совершенно необходима: в пресной воде «эффект Канзиуса» не наблюдается).
Горит водород, который выделяется из воды под действием радиоволн: в этом и состоит «соль» открытия (кстати, соль совершенно необходима: в пресной воде «эффект Канзиуса» не наблюдается).
По словам Канзиуса и Роя, поджигая выделяющийся водород (а он выделяется все время, пока вода находится в радиополе), можно достичь температуры выше 1600 градусов Цельсия. Температура пламени и его окраска зависит от концентрации соли и других веществ, растворенных в воде.
10 сентября Рой, назвавший изобретение «самым значительным открытием в науке о воде за последние сто лет», должен был встретиться с представителями министерств обороны и энергетики США, чтобы обсудить перспективы аппарата Канзиуса.
О Канзиусе и его изобретении можно почитать в Википедии и других подобных проектах, есть фотографии и видеозаписи.
Недоверие
Канзиус поражает воображение журналиста Кадр телеканала 3.
Lenta.ru
Насколько активно расхвалили Канзиуса СМИ, настолько же яростно его и его сторонников раскритиковали завсегдатаи блогов и форумов по всему миру. Одни считают, что изобретатель — жулик, другие — что явление-то наблюдается, но объяснение совершенно неверное, третьи — что все правда, но никаких перспектив у этого изобретения нет.
Одни считают, что изобретатель — жулик, другие — что явление-то наблюдается, но объяснение совершенно неверное, третьи — что все правда, но никаких перспектив у этого изобретения нет.
Полная мистификация все же представляется маловероятной. Демонстрацию эксперимента наблюдали ученые, коммерсанты, журналисты. Трудно допустить, чтобы все эти люди оказались настолько некомпетентны и недобросовестны. Кроме того, Канзиус, судя по всему, не пытается извлечь из аппарата особую выгоду, хотя и отмечает, что не против продать его какой-нибудь крупной компании, чтобы потратить вырученные деньги на продолжение поисков средства от рака (медицинская ценность этих поисков — отдельный вопрос, который мы здесь не затрагиваем). Тем не менее, во всей истории действительно есть места, которые вызывают сомнение.
Ошибочная интерпретация более правдоподобна. Согласно популярной в Сети версии, под воздействием радиоволн между ионами Na+ и Cl— возникает дуговой разряд, который по виду напоминает пламя, хотя на самом деле является иным видом плазмы.
С другой стороны, логично считать, что Рой все же смог отличить горение водорода от дугового разряда и Канзиус говорит правду. Эта версия тоже натыкается на определенные противоречия.
Ковалентная связь между кислородом и водородом в молекуле воды очень прочна, и для того, чтобы ее разорвать, нужна немалая энергия. Классическим примером расщепления молекулы воды является электролиз, достаточно энергозатратный процесс. Канзиус, однако, подчеркивает, что в данном случае имеет место не электролиз, а совершенно иное явление. Какой именно частоты радиоволны используются в аппарате, не сообщается, однако сомнительно, чтобы их энергии было достаточно для разрушения связи. Часть молекул воды в растворе находится, конечно, в диссоциированном виде (несколько упрощая, в виде ионов H+ и OH—), но и это не помогает понять, откуда берется газообразный молекулярный водород.
Высокая температура горения достаточно правдоподобна: в чистом кислороде водород может сгорать и при 2800 градусах Цельсия. Смешиваясь с кислородом в определенной пропорции, водород дает гремучий газ, который не горит, а взрывается, однако можно предположить, что при тех концентрациях газов, которые возникают в аппарате Канзиуса, гремучего газа не образуется.
Смешиваясь с кислородом в определенной пропорции, водород дает гремучий газ, который не горит, а взрывается, однако можно предположить, что при тех концентрациях газов, которые возникают в аппарате Канзиуса, гремучего газа не образуется.
Но допустим, что все же аппарат работает: либо изобретатель не сообщает существенных деталей, либо он действительно создал что-то принципиально новое, либо где-то в скептических рассуждениях ошибка. Что же получается тогда?
Вечный двигатель
Канзиус не утверждает, что его аппарат энергетически выгоден, более того, говорит, что он пока потребляет больше энергии, чем производит. Однако Канзиус хочет проверить, может ли аппарат произвести достаточно энергии, чтобы привести в действие, например, автомобиль, а Рой говорит, что будущее аппарата зависит от его эффективности, то есть от соотношения энергии, получаемой при сгорании водорода, и энергии, затрачиваемой генератором радиоволн.
Может ли такой аппарат в принципе оказаться энергетически выгоден? Для того чтобы его запустить, необходимо разорвать связь водород-кислород, затратить энергию. Впоследствии водород сгорает, то есть вступает в реакцию с кислородом и опять же дает воду. В итоге образуется та же самая связь, при ее образовании энергия, конечно, выделяется, но она никак не может быть больше энергии, затраченной на разрыв связи.
Впоследствии водород сгорает, то есть вступает в реакцию с кислородом и опять же дает воду. В итоге образуется та же самая связь, при ее образовании энергия, конечно, выделяется, но она никак не может быть больше энергии, затраченной на разрыв связи.
А если бы все же могла, то получился бы вечный двигатель. Мы затратили энергию, разложили воду, сожгли водород, окупили затраты с лихвой, получили опять ту же воду, вернулись в начальное состояние. Можем повторять процесс до бесконечности.
Можно предположить, что на самом деле вода не является в аппарате Канзиуса возобновляемым топливом, то есть тратится необратимо (как дрова в костре, уголь в ТЭС, ядерное топливо в АЭС), а на выходе получается не вода, а что-то другое. Тогда закон сохранения энергии не нарушается, но легче не становится. Приходится допускать различные изыски: что при сгорании образуется не вода, а перекись водорода, что кислород не выделяется в виде газа (а на горение идет только кислород из воздуха), а вступает в реакцию с солью, образуя, например, хлораты ClO3—, и т. п. Все эти предположения фантастичны, а главное, все равно не объясняют, откуда берется лишняя энергия.
п. Все эти предположения фантастичны, а главное, все равно не объясняют, откуда берется лишняя энергия.
Еще одним возможным источником энергии является сама растворенная соль. Растворение хлорида натрия — эндотермический процесс, проходящий с поглощением энергии, соответственно, при обратном процессе энергия будет высвобождаться. Однако количество этой энергии ничтожно: около четырех килоджоулей на моль (примерно 50 килоджоулей на килограмм соли, что почти в тысячу раз меньше удельной теплоты сгорания бензина).
По нашим данным, никто из сторонников проекта прямо и не утверждал, что энергия на выходе может превзойти энергию на входе, речь шла (см. выше) лишь об их соотношении. Однако тогда непонятно, какую выгоду может принести такой аппарат топливной индустрии.
Может быть, у него найдутся другие применения: добыча водорода (водород используется не только как экологическое топливо) или опреснение воды. Если окажется, что аппарат позволяет удешевить эти процессы, он будет вполне востребован.
Лента.ру и альтернативное топливо
Возвращаясь к статье «Классика научных сенсаций», заметим, что в данном случае нам встретилась сенсация первого типа (долгожданный ответ на известный вопрос), инженерно-технический подтип: попытка изобрести нечто очень нужное и трудно достижимое наконец увенчалась успехом.
Заметку о Канзиусе Лента.ру не снабдила никакими комментариями, что вызвало живейший читательский отклик. Так, читатель А. любезно указал нам на то, что мы сообщаем об изобретении вечного двигателя, и убедительно аргументировал свою точку зрения, анонимный читатель посетовал, что такая заметка на Ленте — это «позор», а читатель Е. спросил, как нам не стыдно публиковать такие статьи без критических пояснений. Нам стыдно. Мы исправились.
Александр Бердичевский
ПЛАМЕНИ
Пламя включает химическую реакцию между одним химическим веществом, называемым топливом, и другим химическим веществом, которое является окислителем (или окислителем). В особых случаях горючее и окислитель могут быть объединены в одной и той же химической молекуле, как это имеет место в некоторых топливах и взрывчатых веществах. Химическая реакция между топливом и окислителем называется горением; оно сопровождается выделением тепла и обычно излучением света в видимой области спектра. В случае пламени предварительно смешанных углеводородов, горящего на воздухе, испускаемый свет обычно синего цвета, если смесь бедна топливом, и он указывает местоположение пламени и, в частности, из-за его большей интенсивности, положение фронта пламени. Однако, если смесь, поступающая в пламя, богата топливом, образуется желтое пламя с образованием сажи, которое называется светящимся пламенем.
В особых случаях горючее и окислитель могут быть объединены в одной и той же химической молекуле, как это имеет место в некоторых топливах и взрывчатых веществах. Химическая реакция между топливом и окислителем называется горением; оно сопровождается выделением тепла и обычно излучением света в видимой области спектра. В случае пламени предварительно смешанных углеводородов, горящего на воздухе, испускаемый свет обычно синего цвета, если смесь бедна топливом, и он указывает местоположение пламени и, в частности, из-за его большей интенсивности, положение фронта пламени. Однако, если смесь, поступающая в пламя, богата топливом, образуется желтое пламя с образованием сажи, которое называется светящимся пламенем.
Большинство пламен возникает в результате сильно экзотермических реакций, дающих температуры пламени около 2200К, хотя пламя может сгорать примерно до 1300К, в зависимости от соотношения топлива и воздуха. Определенное пламя может поддерживаться ниже этой температуры и называется «холодным» пламенем, но здесь происходит только частичное сгорание.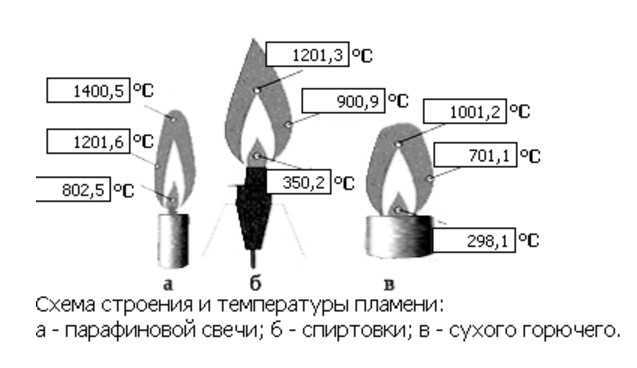 Типичное пламя возникает в результате сжигания с воздухом газообразного топлива, такого как природный газ, коммерческое и промышленное жидкое топливо, обычно называемое мазутом, которое сгорает в виде аэрозоля или пылевидных угольных частиц, взвешенных в воздухе, как в случае с энергетикой. станционный котел.
Типичное пламя возникает в результате сжигания с воздухом газообразного топлива, такого как природный газ, коммерческое и промышленное жидкое топливо, обычно называемое мазутом, которое сгорает в виде аэрозоля или пылевидных угольных частиц, взвешенных в воздухе, как в случае с энергетикой. станционный котел.
Различные типы пламени могут возникать в зависимости от того, как топливо и окислитель смешиваются в горелке, а также в зависимости от скорости их потока. Предварительно смешанное газовое пламя может возникать в результате смешивания топливного газа и воздуха перед входом в горелку, или если они смешиваются после выхода из горелки, они называются диффузионным пламенем . Скорость газового потока может быть относительно низкой, и в этом случае входящий газообразный поток топлива и воздуха является ламинарным, как и пламя. При высоких потоках газа они могут быть турбулентными. Таким образом, пламя может быть ламинарным с предварительным смешением, ламинарной диффузией, турбулентным с предварительным смешением или турбулентным диффузионным пламенем, как показано в таблице 1. Переход от ламинарного пламени к турбулентному происходит по мере увеличения скорости потока, как показано на рисунке 1 [Хоттель и Хоторн (19).49)]. Кроме того, их также можно разделить на стационарное пламя или распространяющееся (перемещающееся) пламя, первое из которых наиболее широко используется в бытовых или промышленных горелках, а последнее используется во взрывах.
Переход от ламинарного пламени к турбулентному происходит по мере увеличения скорости потока, как показано на рисунке 1 [Хоттель и Хоторн (19).49)]. Кроме того, их также можно разделить на стационарное пламя или распространяющееся (перемещающееся) пламя, первое из которых наиболее широко используется в бытовых или промышленных горелках, а последнее используется во взрывах.
Таблица 1. Различные способы смешивания топлива и окислителя
Рисунок 1. Изменение типа пламени с увеличением скорости газа [по Hottel and Hawthorne (1949)].
Наиболее изученным типом пламени является ламинарное предварительно смешанное пламя газообразного топлива и окислителя, обычно воздуха, поскольку это самое простое пламя, обладающее характеристиками, общими для многих других систем. Типичным является Пламя горелки Бунзена , тип пламени, широко используемый в газовых каминах, газовых плитах и установках центрального отопления.
Пламя горелки Бунзена показано на рисунке 2 [Gaydon and Wolfhard (1970)], но в исследовательских целях используется плоское пламя с использованием специальной горелки, которая создает равномерный поток, как показано на рисунке 3(a).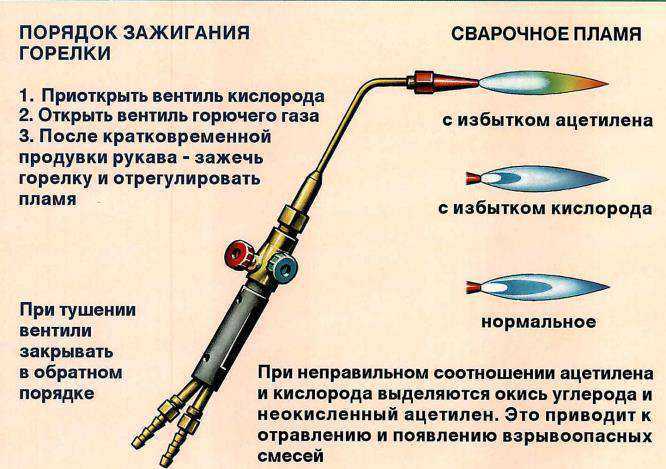 Горелка Бунзена, однако, иллюстрирует как предварительно смешанное пламя, так и принцип диффузионного пламени. Внутреннее ядро является зоной реакции предварительно перемешанного пламени, но пламя богато горючим, поэтому продукты неполного сгорания сгорают во внешнем ядре как диффузионное пламя с окружающим воздухом. Точная природа пламени определяется соотношение топливо/воздух (смесь) . Если есть избыток топлива, его можно назвать богатым, а пламя будет желтым светящимся. Если есть избыток воздуха (или кислорода), его можно назвать обедненным. Если в нем точно правильное количество топлива и воздуха, его можно назвать стехиометрическим. В целом продукты сгорания будут представлены стехиометрическим уравнением, которое в случае метана (основного компонента природного газа) выглядит следующим образом:
Горелка Бунзена, однако, иллюстрирует как предварительно смешанное пламя, так и принцип диффузионного пламени. Внутреннее ядро является зоной реакции предварительно перемешанного пламени, но пламя богато горючим, поэтому продукты неполного сгорания сгорают во внешнем ядре как диффузионное пламя с окружающим воздухом. Точная природа пламени определяется соотношение топливо/воздух (смесь) . Если есть избыток топлива, его можно назвать богатым, а пламя будет желтым светящимся. Если есть избыток воздуха (или кислорода), его можно назвать обедненным. Если в нем точно правильное количество топлива и воздуха, его можно назвать стехиометрическим. В целом продукты сгорания будут представлены стехиометрическим уравнением, которое в случае метана (основного компонента природного газа) выглядит следующим образом:
где –ΔH c – теплота, выделяющаяся при сгорании, известная как теплота сгорание или теплотворная способность (cv). Термин стехиометрический относится к ситуации, когда сгорание завершено без неиспользованного топлива или неиспользованного окислителя.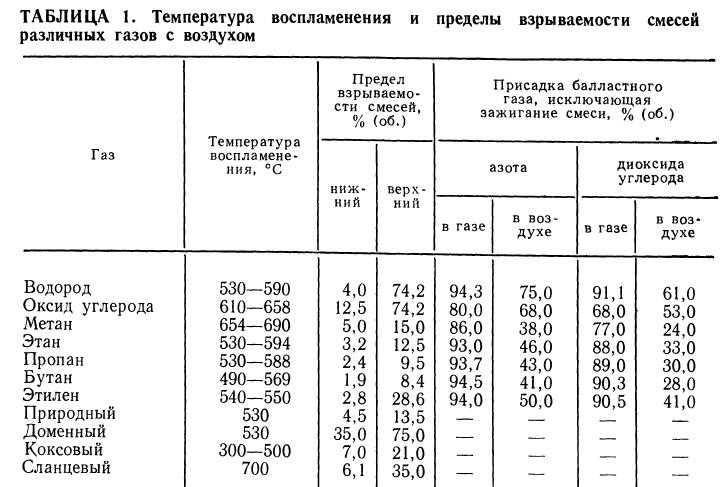 Область неполного сгорания в пламени, показанная на рис. 2, представляет собой лишь частичное сгорание топлива с образованием монооксида углерода и водорода, которые впоследствии сгорают с вторичным воздухом с образованием CO 2 и H 2 O. Это двухстадийное сгорание может представить реакциями, например для метана,
Область неполного сгорания в пламени, показанная на рис. 2, представляет собой лишь частичное сгорание топлива с образованием монооксида углерода и водорода, которые впоследствии сгорают с вторичным воздухом с образованием CO 2 и H 2 O. Это двухстадийное сгорание может представить реакциями, например для метана,
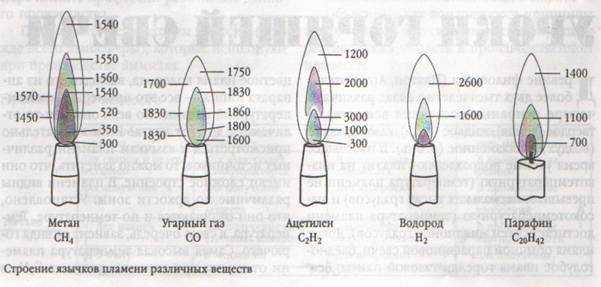
В общем, все углеводородные пламена, как богатые, так и обедненные, проходят через такую стадию с образованием CO и H 2 в первой основной реакционной зоне, а вторая стадия горения первоначально образовавшихся CO и H 2 характеризуется излучением синего света; это синее излучение является ключевой особенностью сгорания всех видов топлива, содержащих углерод (и углеводороды). Этот процесс более выражен в пламени с небольшим содержанием топлива и называется дожиганием 9.0006 .
Рис. 2. Горелка Бунзена.
Рисунок 3. (a) Горелка с плоским пламенем, показывающая определение скорости горения.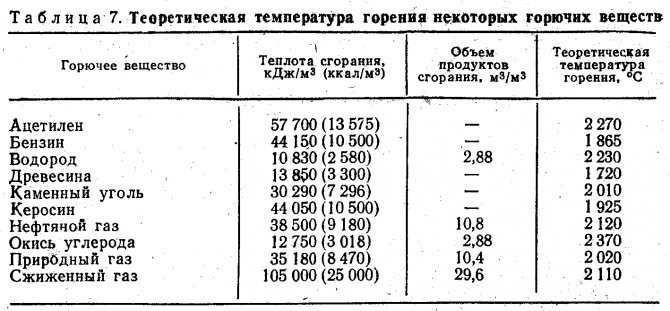 (b) Угол конуса пламени и определение скорости горения S u = v sin α.
(b) Угол конуса пламени и определение скорости горения S u = v sin α.
Предварительно перемешанное пламя конкретной топливно-воздушной смеси характеризуется тремя основными параметрами: скоростью горения , температурой пламени и пределом воспламеняемости , которые также определяются давлением, температурой и, конечно же, соотношением смеси. Предварительно смешанные топливно-воздушные смеси имеют характеристическую скорость горения, и это позволяет стабилизировать пламя на горелке, как показано на рисунках 2, 3 (а) и 3 (б), если поток газовой смеси равен ламинарной скорости горения. Скорость горения просто определена для плоского ламинарного пламени, как показано на рисунке 3(а), то есть скорость приближения дает скорость горения (относительно несгоревшего газа, S u ) и обычно указывается в м/с. Для конического пламени ламинарное пламя соответствует рисунку 3(b). В случае ламинарного диффузионного пламени топливо и окислитель встречаются только в горловине горелки (т. е. они не смешиваются предварительно) и смешиваются за счет процессов диффузии по мере горения пламени, как показано на рис. 4. В этом случае топливный газ и окислитель газовые потоки представляют собой щели, дающие плоское пламя, но аналогичные осесимметричные пламена можно получить при использовании концентрических трубок с подачей топлива обычно через внутреннюю трубку.
е. они не смешиваются предварительно) и смешиваются за счет процессов диффузии по мере горения пламени, как показано на рис. 4. В этом случае топливный газ и окислитель газовые потоки представляют собой щели, дающие плоское пламя, но аналогичные осесимметричные пламена можно получить при использовании концентрических трубок с подачей топлива обычно через внутреннюю трубку.
Рисунок 4. Типичный тип ламинарной диффузионной горелки и пламени.
Пламя будет гореть только в том случае, если оно находится в пределах предела воспламеняемости, то есть состава топливно-окислительных смесей, который поддерживает стабильное пламя. Существует два типа ограничений, связанных с распространением ламинарного пламени. Первый связан с химической способностью смеси поддерживать пламя, т. е. с пределом воспламеняемости. Второй связан с влиянием газового потока. Типичными значениями являются метан, где нижний и верхний пределы воспламеняемости составляют 5 и 14 мольных %, стехиометрическое соотношение будет равно 9. .47 мол. %. В случае н-гептана пределы составят 1 и 6 мол.% соответственно при стехиометрическом соотношении 1,87 мол.%.
.47 мол. %. В случае н-гептана пределы составят 1 и 6 мол.% соответственно при стехиометрическом соотношении 1,87 мол.%.
Сжигание жидкого топлива или пылевидного угля (или пылевидного топлива, сокращенно pf) широко используется в промышленных горелках, особенно в крупных котлах, используемых для выработки пара для производства электроэнергии. Промышленное пламя, как правило, носит турбулентный характер и по соображениям удобства и безопасности включает диффузионное пламя, в котором топливо и воздух впрыскиваются раздельно по соображениям безопасности, а развитие длины диффузионного пламени после выхода из горелки происходит с увеличением скорости потока газа. как показано на рисунке 1. С увеличением скорости газа происходит переход от ламинарного к турбулентному диффузионному горению, хотя некоторое диффузионное перемешивание имеет место, многое является результатом турбулентного взаимодействия (турбулентной диффузии).
Пламя жидкого топлива [Williams (1990)] может варьироваться от голубого, предварительно перемешанного, как пламя, до сильно светящегося пламени, похожего на угольное пламя. Чтобы жидкое топливо сгорело, оно должно полностью испариться, чтобы получить пар, который горит так же, как газообразное пламя. Это называется «гомогенным» распылением . Для более нелетучих видов топлива частично испарившееся топливо горит в виде сферического пламени, окружающего каждую каплю, как показано на рисунке 5, это называется «гетерогенным» распылением . Примером первого режима горения является сжигание авиационного керосина в газовой турбине самолета, где топливо в значительной степени испаряется после впрыска в виде аэрозоля в камеру сгорания, однако некоторые более крупные капли горят неоднородно и имеют тенденцию давать дым. Второй режим называется струйным горением, при котором горение происходит неоднородно. Это происходит в промышленных печах и котлах, а также в дизельных двигателях.
Чтобы жидкое топливо сгорело, оно должно полностью испариться, чтобы получить пар, который горит так же, как газообразное пламя. Это называется «гомогенным» распылением . Для более нелетучих видов топлива частично испарившееся топливо горит в виде сферического пламени, окружающего каждую каплю, как показано на рисунке 5, это называется «гетерогенным» распылением . Примером первого режима горения является сжигание авиационного керосина в газовой турбине самолета, где топливо в значительной степени испаряется после впрыска в виде аэрозоля в камеру сгорания, однако некоторые более крупные капли горят неоднородно и имеют тенденцию давать дым. Второй режим называется струйным горением, при котором горение происходит неоднородно. Это происходит в промышленных печах и котлах, а также в дизельных двигателях.
Рисунок 5. Схематическая модель идеализированного гетерогенного струйного горения.
При сжигании пылевидного топлива частицы угля, обычно диаметром 100 мм, проходят следующие стадии.
Частица угля попадает в горячую камеру сгорания и нагревается, в результате чего происходит пиролиз некоторых наиболее реакционноспособных компонентов (обычно 50%) угля, процесс, называемый дегазацией . Продукты дегазации сгорают в первой части факельного пламени с желтым пламенем газовой фазы. Затем образующийся углеродистый уголь горит медленнее гетерогенным образом с участием поверхностных реакций типа
оставляя остаточную минеральную золу, если горение идет до конца. Образующееся пламя представляет собой светящееся сильно излучающее облако раскаленных докрасна углей и частиц минеральной золы.
Хотя чаще всего используется пламя углеводородов (природный газ, нефть, уголь) с воздухом, следует отметить множество других комбинаций. Особый интерес представляют:
Высокотемпературное пламя, создаваемое кислородно-топливными смесями, такими как ацетилен (этин) с кислородом для сварочных и газовых горелок, а также с природный газ для быстрого плавления металлов.
 Первый дает температуру пламени (T f ) около 3300К, а второй около 2700К. Эти высокие температуры возникают из-за отсутствия разбавляющего азота, присутствующего в воздухе, и большого выделения энергии из энергетического (высокоэкзотермического) топлива.
Первый дает температуру пламени (T f ) около 3300К, а второй около 2700К. Эти высокие температуры возникают из-за отсутствия разбавляющего азота, присутствующего в воздухе, и большого выделения энергии из энергетического (высокоэкзотермического) топлива.В принципе, при сгорании водорода с фтором образуется самое горячее пламя (T f 4300K). Порошковые металлы, напр. алюминий также дают высокие температуры пламени, которые приблизительно контролируются температурой кипения образующегося оксида, которая в случае алюминия составляет 3800К. Их можно использовать для резки толстых металлических листов, таких как сейф, или бетонных стен. Также можно использовать металлические трубы, и использование стальной трубы с протекающим через нее кислородом составляет основу термического копья, также используемого для резки.
Топливо : Ракеты приводятся в движение за счет сжигания твердого или жидкого топлива, то есть топлива, которое можно хранить.
 Топливо жидкого топлива может состоять, как правило, из жидкого водорода (LH 2 ) плюс жидкий кислород (LOx) (T f = 3100K), используемого в космическом шаттле, или жидкого диоксида азота (NO 2 ) с жидкий гидразин (T f = 3000K), используемый в ракетах меньшего размера. Можно использовать твердое топливо, например, перхлорат аммония и каучуковое полимерное связующее. Перхлорат возгоняется с образованием газа (NH 3 + HClO 4 ), а сильно окисляющая хлорная кислота быстро реагирует с NH 3 и связующим, особенно при высоких давлениях. Цель во всех случаях состоит в том, чтобы создать высокотемпературное пламя, чтобы можно было максимизировать тягу, хотя могут играть роль и другие факторы.
Топливо жидкого топлива может состоять, как правило, из жидкого водорода (LH 2 ) плюс жидкий кислород (LOx) (T f = 3100K), используемого в космическом шаттле, или жидкого диоксида азота (NO 2 ) с жидкий гидразин (T f = 3000K), используемый в ракетах меньшего размера. Можно использовать твердое топливо, например, перхлорат аммония и каучуковое полимерное связующее. Перхлорат возгоняется с образованием газа (NH 3 + HClO 4 ), а сильно окисляющая хлорная кислота быстро реагирует с NH 3 и связующим, особенно при высоких давлениях. Цель во всех случаях состоит в том, чтобы создать высокотемпературное пламя, чтобы можно было максимизировать тягу, хотя могут играть роль и другие факторы.Эти пропелленты могут содержать топливо и окислитель в одной молекуле (монотопливы) или они могут смешиваться до или во время сгорания (бипропелленты).
Пламя саморазложения: некоторые виды пламени можно сжигать без добавления окислителя, поскольку топливо разлагается экзотермически, хотя в таких системах достигаются только относительно низкие температуры пламени (T f ).
 Двумя хорошо известными примерами являются ацетилен (этин) и гидразин . В первом случае реакция горения выглядит так:
Двумя хорошо известными примерами являются ацетилен (этин) и гидразин . В первом случае реакция горения выглядит так:что дает температуру пламени 1650К.
Для гидразина реакция саморазложения
дает температуру пламени 1800К.
Поскольку гидразин является жидкостью для хранения, он или его метилпроизводные (CH 3 ) 2 N 2 H 2 используются в ракетной технике.
Необычное пламя: Пламя может образовываться при сгорании воздуха или кислорода с различными необычными видами топлива, такими как аммиак (NH 3 , дающий продукты N 2 + H 2 O), сероуглерод (CS 2 , дающий CO 2 + SO 2 ). Цианоген (C 2 N 2 ) и другое необычное топливо субнитрид углерода дают одни из самых высоких температур пламени, а именно 4800K и 5260K соответственно, поскольку продукты CO и N 2 не диссоциируют.
 существенно.
существенно.
В то время как многие виды пламени горят в неограниченных условиях, например, в газовом камине или в газовой плите, большинство промышленных видов пламени и многие виды пламени, используемые в бытовых условиях, например, в котлах центрального отопления, горят в условиях частичного замкнутого пространства, а именно в камере сгорания. В некоторых исключительных обстоятельствах, обычно при неисправности, могут произойти взрывы. Таким образом, при воспламенении, если в камеру сгорания поступило слишком много топлива или если скорость, с которой топливо поступает в камеру сгорания, слишком велика, то скорость генерируемой энергии и объем образующихся продуктов сгорания слишком велики для того, чтобы они могли выйти через дымоход. В таких обстоятельствах расширяющееся пламя может привести к повышению давления и взрыву. Как правило, такие ограниченные процессы горения приводят к быстрому увеличению давления, которое может повредить камеру сгорания и даже привести к разрушению оборудования. По этой причине во многих промышленных процессах сжигания в камеру сгорания (или технологический сосуд) встроен предохранитель от взрыва (или давления) для преодоления проблем, вызванных высоким повышением давления и последующим взрывом.
По этой причине во многих промышленных процессах сжигания в камеру сгорания (или технологический сосуд) встроен предохранитель от взрыва (или давления) для преодоления проблем, вызванных высоким повышением давления и последующим взрывом.
В крайнем случае может произойти ограниченный взрыв из-за сгорания горючей смеси в полностью закрытой системе. Наиболее распространенным, но безопасным примером является обнаружение в камере сгорания автомобиля с возвратно-поступательным движением поршня во время его работы. Здесь искра поджигает смесь, пламя расширяется и переходит в замкнутый взрыв, хотя фактически в этом случае оно только частично ограничено из-за движения поршня. Примеры действительно закрытых взрывов имеют место в случае, когда произошел взрыв в результате утечки природного газа в помещении или горючих технологических смесей, таких как пары углеводородов, при взрыве на химическом заводе. Подробности этого рассматриваются в другом разделе. (См. Двигатели внутреннего сгорания; Явления взрыва. )
)
ССЫЛКИ
Gaydon, A.G. and Wolfhard, H.G. (1970) Пламя: их структура, излучение и температура , Third Edition, Chapman and Hall Ltd., London. DOI: 10.1016/0022-460X(72)90510-X
Glassman, I. (1977) Combustion , Academic Press, Нью-Йорк.
Hottel, H.C. and Hawthorne, W.R. (1949) Третий симпозиум по явлениям горения, пламени и взрыва , 254, Williams & Wilkins, Baltimore.
Уильямс, А. (1990) Горение распылителей жидкого топлива , Баттервортс, Лондон.
Горение | Определение, реакция, анализ и факты
сжигание
Посмотреть все СМИ
- Ключевые люди:
- Антуан Лавуазье Отто фон Герике Иоганн Иоахим Бехер
- Похожие темы:
- Пожар флогистон точка возгорания пламя случайное возгорание
Просмотреть весь связанный контент →
Понять химию, лежащую в основе того, что заставляет спичку загораться
Посмотреть все видео к этой статье горение , химическая реакция между веществами, обычно включающая кислород и обычно сопровождающаяся выделением тепла и света в форме пламени. Скорость или скорость соединения реагентов высока отчасти из-за природы самой химической реакции, а отчасти потому, что генерируется больше энергии, чем может уйти в окружающую среду, в результате чего температура реагентов повышается. чтобы еще больше ускорить реакцию.
Скорость или скорость соединения реагентов высока отчасти из-за природы самой химической реакции, а отчасти потому, что генерируется больше энергии, чем может уйти в окружающую среду, в результате чего температура реагентов повышается. чтобы еще больше ускорить реакцию.
Известным примером реакции горения является зажженная спичка. Когда зажигается спичка, трение нагревает голову до температуры, при которой химические вещества вступают в реакцию и выделяют больше тепла, чем может выйти в воздух, и горят пламенем. Если ветер сдувает тепло или химические вещества влажные, а трение недостаточно повышает температуру, спичка гаснет. При правильном воспламенении тепло от пламени повышает температуру близлежащего слоя спички и кислорода в воздухе, прилегающем к нему, и древесина и кислород вступают в реакцию горения. Когда достигается равновесие между полными тепловыми энергиями реагентов и полными тепловыми энергиями продуктов (включая реально излучаемое тепло и свет), горение прекращается. Пламя имеет определяемый состав и сложную структуру; о них говорят, что они многообразны и способны существовать как при достаточно низких температурах, так и при чрезвычайно высоких температурах. Испускание света в пламени обусловлено присутствием возбужденных частиц и, как правило, заряженных атомов и молекул, а также электронов.
Пламя имеет определяемый состав и сложную структуру; о них говорят, что они многообразны и способны существовать как при достаточно низких температурах, так и при чрезвычайно высоких температурах. Испускание света в пламени обусловлено присутствием возбужденных частиц и, как правило, заряженных атомов и молекул, а также электронов.
Горение охватывает большое разнообразие явлений с широким применением в промышленности, науке, профессиях и быту, и применение основано на знаниях физики, химии и механики; их взаимосвязь становится особенно очевидной при рассмотрении распространения пламени.
В общих чертах горение является одной из наиболее важных химических реакций и может считаться кульминационным этапом окисления определенных видов веществ. Хотя когда-то окисление считалось просто сочетанием кислорода с любым соединением или элементом, значение этого слова было расширено и теперь включает любую реакцию, в которой атомы теряют электроны, тем самым окисляясь. Как уже отмечалось, в любом процессе окисления окислитель забирает электроны у окисляемого вещества, тем самым сам восстанавливаясь (приобретая электроны).

 Первый дает температуру пламени (T f ) около 3300К, а второй около 2700К. Эти высокие температуры возникают из-за отсутствия разбавляющего азота, присутствующего в воздухе, и большого выделения энергии из энергетического (высокоэкзотермического) топлива.
Первый дает температуру пламени (T f ) около 3300К, а второй около 2700К. Эти высокие температуры возникают из-за отсутствия разбавляющего азота, присутствующего в воздухе, и большого выделения энергии из энергетического (высокоэкзотермического) топлива. Топливо жидкого топлива может состоять, как правило, из жидкого водорода (LH 2 ) плюс жидкий кислород (LOx) (T f = 3100K), используемого в космическом шаттле, или жидкого диоксида азота (NO 2 ) с жидкий гидразин (T f = 3000K), используемый в ракетах меньшего размера. Можно использовать твердое топливо, например, перхлорат аммония и каучуковое полимерное связующее. Перхлорат возгоняется с образованием газа (NH 3 + HClO 4 ), а сильно окисляющая хлорная кислота быстро реагирует с NH 3 и связующим, особенно при высоких давлениях. Цель во всех случаях состоит в том, чтобы создать высокотемпературное пламя, чтобы можно было максимизировать тягу, хотя могут играть роль и другие факторы.
Топливо жидкого топлива может состоять, как правило, из жидкого водорода (LH 2 ) плюс жидкий кислород (LOx) (T f = 3100K), используемого в космическом шаттле, или жидкого диоксида азота (NO 2 ) с жидкий гидразин (T f = 3000K), используемый в ракетах меньшего размера. Можно использовать твердое топливо, например, перхлорат аммония и каучуковое полимерное связующее. Перхлорат возгоняется с образованием газа (NH 3 + HClO 4 ), а сильно окисляющая хлорная кислота быстро реагирует с NH 3 и связующим, особенно при высоких давлениях. Цель во всех случаях состоит в том, чтобы создать высокотемпературное пламя, чтобы можно было максимизировать тягу, хотя могут играть роль и другие факторы.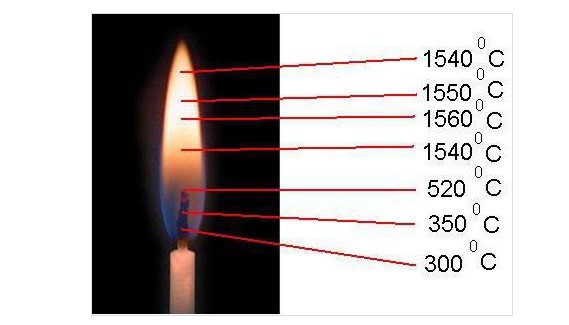 Двумя хорошо известными примерами являются ацетилен (этин) и гидразин . В первом случае реакция горения выглядит так:
Двумя хорошо известными примерами являются ацетилен (этин) и гидразин . В первом случае реакция горения выглядит так: существенно.
существенно.