Физические и химические явления. Превращение веществ. 8-й класс
Цели урока.
Образовательная: опираясь на знания учащихся из курса природоведения и компьютерную презентацию, конкретизировать знания учащихся о физических и химических явлениях, на примерах выявить их отличия; опираясь на жизненный опыт учащихся, познакомить их с признаками химических реакций и условиями их возникновения и течения.
Развивающая: способствовать развитию творческого мышления учащихся, умений устанавливать причинно-следственные связи, зависимость течения химических реакций от внешних условий, развивать общеучебные и практические навыки при наблюдении и выполнении химического эксперимента.
Воспитательные: формировать научное мировоззрение учащихся, интерес к предмету.
Тип урока: изучение новой темы.
Методы: словесно-наглядный, практический,
частично-поисковый, работа с учебником.
Формы организации познавательной деятельности: фронтальная, групповая, индивидуальная.
Учащиеся должны:
знать: определение физических и химических явлений, признаки и условия течения химических реакций, значение физических и химических явлений в жизни человека.
уметь: отличать физические и химические явления, применять знания о физических и химических явлениях на практике.
Оборудование: компьютер, мультимедийный проектор, презентация.
На столе учителя.
- Смесь порошков железа и серы, пробирка, спиртовка, штатив.
На столах учащихся.
- Штатив, колба с водой закрытая пробкой с газоотводной трубкой, химический стакан, стеклянная пластинка, спиртовка.
- Железные опилки, порошок серы, фильтровальная
бумага, магнит, цилиндр с водой.

Ход урока
I. Организационный этап
Приветствие учащихся учителем.
Проверка готовности учащихся и их рабочих мест к уроку.
II. Сообщение темы и целей урока
На уроках природоведения вы получили первоначальные знания о явлениях, происходящих в природе. Сегодня на уроке вы расширите свой знания о физических и химических явлениях, научитесь отличать их друг от друга, познакомитесь с признаками и условиями течения химических реакций и их значением в жизни человека (слайд №1).
III. Изучение новой темы
План изучения новой темы:
1. Явления, происходящие в природе. Классификация явлений.
2. Физические явления.
- Лабораторный опыт “Испарение воды и конденсация пара”.
3. Химические явления.
- Лабораторный опыт “Изучение свойств железа и
серы”.

- Демонстрационный опыт “Нагревание смеси железа и серы. Изучение свойств полученного вещества”.
4. Признаки химических реакций. Демонстрация видеофрагмента.
5. Условия возникновения и течения химических реакций (сообщение учащегося).
6. Значение физических явлений и химических реакций.
1. Явления, происходящие в природе. Классификация явлений
Учитель: Ребята, что нас окружает? (слайд № 2)
Ученик: Природа. Неживая и живая.
Учитель: В природе постоянно происходят изменения. Приведите примеры.
Ученик:
День сменяется ночью (слайд № 3)
Идёт дождь или снег, испаряется вода (слайд № 4)
Зеленеет трава, течёт ручей (слайд № 5)
Дует ветер, горит костёр (слайд № 6)
Человек готовит пищу. (слайд № 7)
Учитель: Как можно назвать эти изменения?
Ученик: Все изменения, происходящие в природе,
называются явлениями природы.
Учитель: Как классифицируют все природные явления?
Ученик: Природные явления могут быть биологическими, физическими и химическими (слайд № 8). Познакомимся с физическими и химическими явлениями.
2. Физические явления
Учитель: Какие явления называются физическими?
Ученик: Явления, при которых не происходит превращения одних веществ в другие, называются физическими. Например: плавление воска, испарение воды, таяние льда
Лабораторный опыт
“Испарение воды и конденсация пара”
Учитель: Проведём опыт “Испарение воды и конденсация пара”. Соберите прибор как показано на слайде (слайд № 10), проверьте его герметичность. Соблюдая технику безопасности при работе со спиртовкой и стеклянной посудой, зажгите спиртовку и нагревайте колбу с водой.
— Что вы наблюдаете?
Ученик: При закипании жидкая вода переходит в
газообразное состояние (водяной пар). При
попадании на стеклянную пластину водяной пар
конденсируется в капельки воды.
При
попадании на стеклянную пластину водяной пар
конденсируется в капельки воды.
Учитель: В чём же сущность физических явлений?
Ученик: При физических явлениях изменяется агрегатное состояние и форма вещества (слайд № 11).
3. Химические явления
Учитель: Совсем другое дело химические явления. Горение костра, скисание молока, ржавление железных и стальных изделий (слайд № 12).
— Что происходит при химических явлениях?
Ученик: При химических явлениях одни вещества превращаются в другие.
Лабораторный опыт
“Изучение свойств серы и железа”
Учитель: Проведём опыт “Изучение свойств
серы и железа” по плану (слайд № 13).
Определите цвет веществ.

Учитель: Изменяются ли свойства веществ в смеси?
Ученик: Нет. Вещества, входящие в состав смеси, сохраняют свои индивидуальные свойства.
Демонстрационный опыт “Нагревание
смеси железа и серы.
Изучение свойств полученного вещества”
Учитель: Нагреем полученную смесь серы и железа (слайд № 15). Возьмём смесь серы и железа и нагреем её в пробирке.
— Что наблюдаете?
Ученик: Смесь начала темнеть, затем раскалилась до красна.
Учитель: Извлечём из пробирки то, что образовалось после реакции, и изучим его свойства (цвет, отношение к воде и магниту). Для этого измельчим полученное вещество и подействуем на него магнитом.
— Что наблюдаете?
Ученик: Порошок не притягивается магнитом.
Учитель: Опустим полученное вещество в воду.
— Что наблюдаете?
Ученик: Вещество тонет, на серу и железо не
разделяется.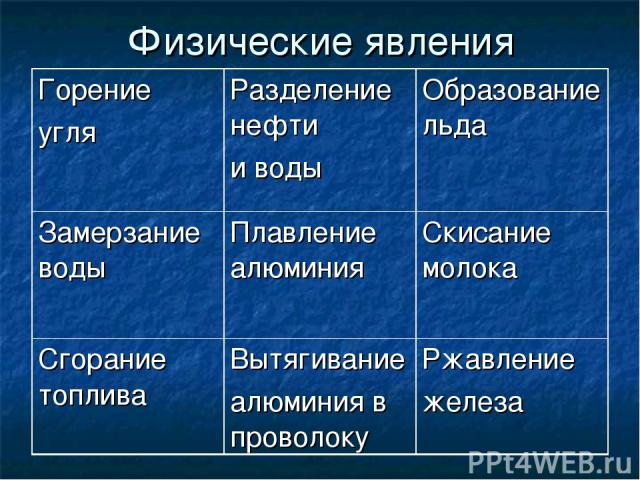
Учитель: Что произошло при нагревании смеси серы и железа?
Ученик: При нагревании смеси серы и железа образовалось новое вещество, которое по своим свойствам отличается от свойств исходных веществ (слайд № 16).
Учитель: Химические явления называются химическими реакциями.
4. Признаки химических реакций
Учитель: О том, что произошла химическая реакция можно судить по признакам. Посмотрите видеофрагмент с демонстрацией опыта (слайд №17).
— Какие признаки химических реакций вы наблюдали при демонстрации опытов?
Ученик: Мы наблюдали такие признаки химических реакций, как изменение окраски, выпадение осадка, выделение газа, выделение энергии.
Учитель: На следующем слайде (слайд № 18) показаны все признаки, которые можно наблюдать во время химических реакций.
5. Условия возникновения и течения химических реакций
Учитель: Чтобы началась химическая реакция,
необходимы определённые условия.
Условия возникновения и течения химических реакций
Сообщение учащегося (слайд № 19)
| Самое главное условие
возникновения химических реакций –
соприкосновение веществ. Например, ржавчина
образуется на поверхности железного изделия,
если оно соприкасается с влажным воздухом. Другое условие – измельчение веществ. Что лучше разгорится – полено или тонкие лучинки? Многие реакции идут в растворе, поэтому исходные вещества необходимо растворить. Третье условие – нагревание вещества до
определённой температуры. Например, медь не
взаимодействует с кислородом при обычных
условиях. Чтобы произошла реакция, медь нужно
нагреть. Также нагревают до определённой
температуры уголь и древесину, чтобы они начали
гореть. Иногда высокая температура нужна на протяжении всей реакции – иначе реакция прекратится. Например, кислород в лаборатории получают при разложении перманганата калия при постоянном нагревании последнего (слайд № 20). В этом случае температура – условие течения химической реакции. Другие условия течения химических реакций |
6. Значение физических явлений и химических реакций
Учитель: Изучите текст параграфа §3 “Значение физических явлений и химических реакций”, заполните таблицу:
Значение физических явлений и химических реакций
| Название явлений | Значение в жизни человека |
1. Физические Физические1) Плавление стекла 2)… и т.д. |
Стеклянной массе можно придать любую форму. |
| 2. Химические 1) Скисание молока 2) … и т.д. |
Приготовление продуктов на его основе: простокваша, сметана, творог. |
IV. Закрепление
Фронтальный опрос (слайд № 21)
Тест “Физические и химические
явления.
Химические явления”
1, 2. Определить физические и химические явления (слайды № 22, 23)
3. Явления, при которых изменяется форма и
агрегатное состояние вещества, называются … (слайд
№ 24)
Явления, при которых изменяется форма и
агрегатное состояние вещества, называются … (слайд
№ 24)
А – химическое
Б – физическое
В – биологическое
4. Явления, при которых происходит превращение одних веществ в другие, называются … (слайд № 25)
А – физические
Б – химические
В – биологические
5. К физическим явлениям относятся: (слайд № 26)
А – плавление стекла
Б – горение древесины
В – испарение воды
Г – скисание молока
Д – растворение соли в воде
Е – протухание яиц
6. К химическим явлениям относятся: (слайд № 27)
А – ржавление железа
Б – образование тумана
В – гниение фруктов
Г – плавление воска
Д – горение керосина
Е – испарение воды
7. Укажите признак химической реакции при
действии кислоты на соду: (слайд № 28)
Укажите признак химической реакции при
действии кислоты на соду: (слайд № 28)
А – образование осадка
Б – изменение цвета
В – выделение газа
8. Укажите признак химической реакции при ржавлении железа: (слайд № 29)
А – выделение газа
Б – образование осадка
В – изменение цвета
9. Укажите признак химической реакции при горении древесины: (слайд № 30)
А – изменение цвета
Б – выпадение осадка
В – выделение тепла
V. Подведение итогов урока, выставление оценок
VI. Домашнее задание
Литература
- Аликберова Л.Ю. Занимательная химия: Книга для
учащихся, учителей, родителей. – М.
 : Аcт-Пресс, 1999.
: Аcт-Пресс, 1999. - Рудзитес Г.Е., Фельдман Ф.Г. Химия. 8 класс.: Учебник для общеобразовательных учебных – М.: Просвящение, 2007.
- Хрипкова А.Г. и другие. Естествознание: учебник для 7 класса общеобразовательных учреждений. – М.: Просвещение, 2005.
- http://chemistry.r2.ru/
- http://www.chem.msu.su/rus/elibrary/
- CD диск “Большая энциклопедия Кирилла и Мефодия 2009”. – ООО “Кирилл и Мефодий, 2009.
- CD-диск “Химия общая и неорганическая”: Углубленный курс по общей и неорганической химии. – Лаборатория систем мультимедиа, МарГТУ, 2001.
Стекло. Получение и использование. Температура плавления стекла
Являясь одним из самых древних материалов, стекло используется человечеством на протяжении не одной тысячи лет. Универсальность этого вещества позволила ему найти применение в самых различных отраслях. По физико-химическим свойствам стекло относится к неорганическим соединениям, оно твёрдое, имеет аморфную структуру, изотропно.
Для каждого вида стекла характерно в процессе изготовления преобразование агрегатного состояния от жидкотекучего, чрезвычайно вязкого до стеклообразного вида. Технология производства предусматривает его остывание со скоростью, которая не позволяет перейти в фазу кристаллизации расплава.
Температура плавления стекла зависит от его качества и предполагаемых характеристик. Как правило, варка происходит в довольно широком диапазоне температур от 300 до 2500 °C. Зависят свойства этого вещества от компонентов, входящих в состав стеклообразующих расплавов. Их перечень довольно обширный и представлен различными оксидами, фосфатами, фторидами и прочими добавками. При этом классическая прозрачность является далеко не последней характеристикой для различных видов стёкол, встречающихся как в природе, так и синтезируемых в ходе производства.
С самыми древними стеклянными поделками, датированными семью веками до нашей эры, познакомились археологи, занимающиеся раскопками в Египте. Это были бусы и амулеты. Но прошло несколько тысячелетий, пока не появились первые промышленные предприятия, стекольные заводы восемнадцатого века. Особенностью стеклопроизводства в шихтах стало то, что температура плавления стекла достигалась использованием угля, а котлы для варки стали закрытыми.
Но прошло несколько тысячелетий, пока не появились первые промышленные предприятия, стекольные заводы восемнадцатого века. Особенностью стеклопроизводства в шихтах стало то, что температура плавления стекла достигалась использованием угля, а котлы для варки стали закрытыми.
До этого в качестве топлива использовались дрова, стекловаренные мастерские долго не находились на месте, печи рассыпались, а топливо в округе быстро расходовалось. Котлы были открытыми, дрова не выделяли веществ, влияющих на прозрачность и цвет выходного продукта. Температура плавления стекла в технологическом процессе такого типа достигала 1450 °C.
Важным событием стало изобретение в начале XX века метода производства листового стекла, названного по имени его разработчика Эмиля Фурко, предложившего машинный способ вытяжки. Просуществовав вплоть до 1959 года, он был вытеснен Флоат-методом, разработанным фирмой «Пилкингтон».
Основными составляющими обычного стекла является кварцевый песок в пропорции 69-74 %, сода (12-16 %), доломит и известняк (5-12 %). Но в технологическом процессе производства имеет важное значение не только при какой температуре плавится стекло, но и какая скорость охлаждения расплава. Теоретически при быстром охлаждении можно получить стекловидное тело и из металла, главное успеть охладить расплав до образования кристаллической решётки.
Но в технологическом процессе производства имеет важное значение не только при какой температуре плавится стекло, но и какая скорость охлаждения расплава. Теоретически при быстром охлаждении можно получить стекловидное тело и из металла, главное успеть охладить расплав до образования кристаллической решётки.
При всём многообразии привлекательных свойств обычного стекла в своё время возникла острая необходимость в более прочном и лёгком прозрачном материале. Прежде всего, это коснулась отрасли, специализирующейся на самолётостроении. Оргстекло получило своё название лишь по внешним сходствам с традиционным стеклом.
Ударопрочность его в пять раз выше, оно легче в 2,5 раза. По светопропусканию оно достигает уровня 92%, имеет высокую стойкость к старению. Намного проще и доступней оргстекло в обработке. Температура плавления оргстекла находится в пределах 90-105 градусов, что позволяет его подвергать термической обработке.
Но оба эти материала заняли каждый свою нишу в современном производстве. Традиционное неорганическое стекло прочно удерживает свои позиции и не собирается их сдавать новейшим органическим полимерам.
Традиционное неорганическое стекло прочно удерживает свои позиции и не собирается их сдавать новейшим органическим полимерам.
Использование широкого спектра различных примесей и добавок позволяет получить не только удивительные оптические характеристики стекла, но и значительно улучшить его механические свойства.
Кроме промышленного использования, нельзя не отметить роль художественного стекла. Мастера–стеклодувы, продолжая традиции древних художников, превратили создание шедевров из стекла в истинное искусство. В печах их мастерских достигается температура плавления стекла, работая практически вручную, в своём творчестве они не только проявляют незаурядную фантазию, но и затрачивают массу физических усилий.
Осторожно — вы сделаны из стекла
Исследователи выяснили, как формируются ткани и органы во время эмбриогенеза
Соня Фернандес развивающийся эмбрион рыбы
Вы когда-нибудь задумывались, как группам клеток удалось построить ваши ткани и органы, пока вы были всего лишь эмбрионом?
Используя разработанные им передовые методы, исследователь Калифорнийского университета в Санта-Барбаре Отгер Кампас и его группа раскрыли эту давнюю загадку, раскрыв поразительную внутреннюю работу физического строения эмбрионов. Мало того, что это переносит вековую гипотезу в современную эпоху, исследование и его методы дают исследователям основу для изучения других вопросов, имеющих ключевое значение для здоровья человека, таких как то, как формируются и распространяются раковые образования или как создавать органы.
Мало того, что это переносит вековую гипотезу в современную эпоху, исследование и его методы дают исследователям основу для изучения других вопросов, имеющих ключевое значение для здоровья человека, таких как то, как формируются и распространяются раковые образования или как создавать органы.
«Короче говоря, мы открыли фундаментальный физический механизм, который клетки используют для придания эмбриональным тканям их функциональных трехмерных форм», — сказал Кампас, профессор машиностроения в Инженерном колледже, заведующий кафедрой Duncan & Suzanne Mellichamp в области систем. Биология. Его группа исследует, как живые системы самоорганизуются, чтобы создавать замечательные структуры и формы, встречающиеся в природе.
Клетки координируют свои действия, обмениваясь биохимическими сигналами, но они также держатся друг за друга и толкают друг друга, создавая структуры тела, необходимые нам для жизни, такие как глаза, легкие и сердце. И, как оказалось, лепка эмбриона не так уж далека от лепки из стекла или 3D-печати. В своей новой работе «Переход заклинивания из жидкого состояния в твердое лежит в основе удлинения оси тела позвоночных», опубликованном в журнале Nature, Кампас и его коллеги показывают, что коллективы клеток переключаются из жидкого состояния в твердое контролируемым образом для построения эмбриона позвоночного. подобно тому, как мы лепим из стекла вазы или печатаем на 3D-принтере наши любимые предметы. Или, если хотите, печатаем себя в 3D, изнутри.
В своей новой работе «Переход заклинивания из жидкого состояния в твердое лежит в основе удлинения оси тела позвоночных», опубликованном в журнале Nature, Кампас и его коллеги показывают, что коллективы клеток переключаются из жидкого состояния в твердое контролируемым образом для построения эмбриона позвоночного. подобно тому, как мы лепим из стекла вазы или печатаем на 3D-принтере наши любимые предметы. Или, если хотите, печатаем себя в 3D, изнутри.
Большинство объектов изначально представляют собой жидкости. От металлических конструкций до желатиновых десертов их форма создается путем заливки расплавленных исходных материалов в формы, а затем их охлаждения для получения твердых предметов, которые мы используем. Как и в стеклянной скульптуре Чихули, созданной путем осторожного плавления кусочков стекла, чтобы медленно превратить его в жизнь, клетки в определенных областях эмбриона более активны и «плавят» ткань до жидкого состояния, которое можно реструктурировать. После этого клетки «остывают», чтобы принять форму ткани, объяснил Кампас.
«Переход от состояния жидкости к состоянию твердой ткани, который мы наблюдали, известен в физике как «заклинивание», — сказал Кампас. «Переходы заклинивания — это очень общее явление, которое происходит, когда частицы в неупорядоченных системах, таких как пены, эмульсии или стекла, сжимаются или охлаждаются».
Это открытие стало возможным благодаря методам, ранее разработанным Кампасом и его группой для измерения сил между клетками внутри эмбрионов, а также для воздействия незначительных сил на клетки, когда они строят ткани и органы. Используя эмбрионы рыбок данио, отличающиеся оптической прозрачностью, но развивающиеся так же, как их человеческие аналоги, исследователи поместили крошечные капельки специально разработанной ферромагнитной жидкости между клетками растущей ткани. Сферические капли деформируются, когда клетки вокруг них толкают и тянут, что позволяет исследователям увидеть силы, которые клетки воздействуют друг на друга. И, делая эти капельки магнитными, они также могли оказывать крошечное напряжение на окружающие клетки, чтобы увидеть, как отреагирует ткань.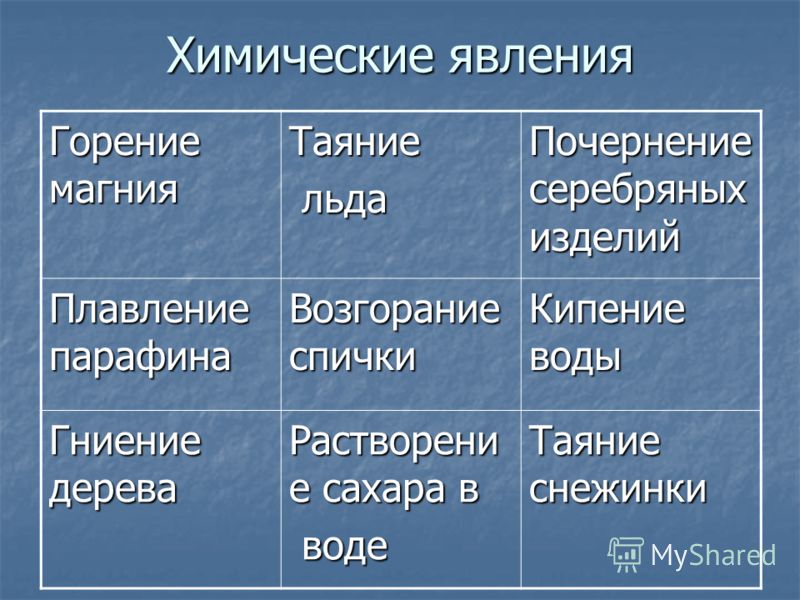
«Мы смогли измерить физические величины, которые не могли быть измерены ранее, из-за сложности введения миниатюрных зондов в крошечные развивающиеся эмбрионы», — сказал научный сотрудник Алессандро Монгера, который является ведущим автором статьи.
«Рыбы данио, как и другие позвоночные, начинаются с практически бесформенного скопления клеток, и им необходимо преобразовать тело в удлиненную форму, с головой на одном конце и хвостом на другом», — сказал Кампас. Физическая реорганизация клеток, стоящая за этим процессом, всегда была загадкой. Удивительно, но исследователи обнаружили, что клеточные коллективы, образующие ткань, физически напоминали пену (да, как пивную пену), которая застревала во время развития, чтобы «заморозить» архитектуру ткани и придать ей форму.
Эти наблюдения подтверждают замечательную интуицию, сделанную шотландским математиком викторианской эпохи Д’Арси Томпсоном 100 лет назад в его основополагающей работе «О росте и форме».
«Он был убежден, что некоторые физические механизмы, придающие форму инертным материалам, также участвуют в формировании живых организмов. Примечательно, что он сравнил группы клеток с пеной и даже формирование клеток и тканей с выдуванием стекла», — сказал Кампас. Столетие назад не было инструментов, которые могли бы напрямую проверить идеи, предложенные Томпсоном, добавил Кампас, хотя работы Томпсона продолжают цитироваться и по сей день.
Примечательно, что он сравнил группы клеток с пеной и даже формирование клеток и тканей с выдуванием стекла», — сказал Кампас. Столетие назад не было инструментов, которые могли бы напрямую проверить идеи, предложенные Томпсоном, добавил Кампас, хотя работы Томпсона продолжают цитироваться и по сей день.
Новая статья в Nature также представляет собой отправную точку, с которой исследователи группы Campàs могут приступить к изучению других процессов эмбрионального развития и смежных областей, таких как физическое проникновение опухолей в окружающие ткани и создание органов с определенными трехмерными формами.
«Одним из признаков рака является переход между двумя различными тканями. Этот переход в принципе можно объяснить как аномальный переход от твердого к жидкообразному состоянию ткани», — пояснил Монгера. «Настоящее исследование может помочь выяснить механизмы, лежащие в основе этого переключения, и выделить некоторые из потенциальных мишеней, которые можно препятствовать этому».
Исследования в рамках этого проекта также проводились исследователями UCSB Пайамом Роуганяном, Ханной Дж. Густафсон, Элайджей Шелтоном, Дэвидом А. Килхофером, Эмметом К. Карном, Фридхеймом Серване, Адамом А. Лучио и Джеймсом Джаммона.
Контактная информация:
Соня Фернандес
(805) 893-4765
Соня (точка) Фернандес (ат) ucsb (точка) edu
Отгер Кампас
кампас (ат) инжиниринг (точка) 904u 9000ed2 Темы:
- морфология тканей
- эмбриональное развитие
- эмбриогенез
- Отгер Кампас
10 примеров температуры плавления в повседневной жизни – StudiousGuy
Температура плавления – это температура, при которой данное твердое вещество переходит из твердого состояния в жидкое. Обе фазы, т. е. твердая и жидкая, находятся в равновесии при температуре плавления. Следовательно, температура плавления данного твердого вещества равна температуре замерзания жидкости. Например, вода показывает равновесие при 0°C.
Это физическое свойство вещества, которое используется для различных целей. Наиболее распространенным примером таяния в повседневной жизни является таяние кубиков льда при воздействии тепла.
Указатель статей (щелкните, чтобы перейти)
Как происходит плавление? Кристаллические твердые тела состоят из трехмерного расположения чрезвычайно мелких частиц, которые называются решетчатыми структурами. Силы решетки действуют внутри частиц решетчатых структур. Когда этот тип твердой структуры нагревается, составляющие ее частицы вибрируют быстрее, потому что они поглощают кинетическую энергию. Эта вибрация продолжается до тех пор, пока силы притяжения между ними перестают быть достаточно сильными для поддержания кристаллической структуры. Это, в свою очередь, разрушает твердую структуру, и, в конце концов, твердое тело начинает плавиться. Температура, при которой происходит этот процесс, известна как температура его плавления. В аморфных твердых телах частицы располагаются в кристаллической решетке хаотично, например, в стекле, смолах и многих синтетических пластмассах.
Это, в свою очередь, разрушает твердую структуру, и, в конце концов, твердое тело начинает плавиться. Температура, при которой происходит этот процесс, известна как температура его плавления. В аморфных твердых телах частицы располагаются в кристаллической решетке хаотично, например, в стекле, смолах и многих синтетических пластмассах.
Процесс плавления
Факторы, влияющие на температуру плавления Температура плавления вещества зависит от силы сил притяжения, действующих внутри твердой структуры. Например, хлорид натрия (NaCl) представляет собой ионное соединение, состоящее из сильных ионных связей. Так, он плавится при высоких температурах, т. е. 801°С, тогда как лед представляет собой соединение, состоящее из водородных связей, прочность которых меньше, чем у ионных связей. Следовательно, лед тает при низких температурах, т. е. при 0°С. При повышении давления твердого тела температура плавления вещества понижается. Присутствие примесей в твердой структуре также снижает ее температуру плавления, что называется «понижением температуры плавления».
Аналитические лаборатории проводят различные тесты для исследования материалов, которые проводятся в различных отраслях промышленности, таких как фармацевтика, пищевая промышленность, электроника и производство пластмасс, для проверки чистоты продуктов. Одним из аналитических методов, применяемых для характеристики чистоты продуктов (от сырья до готовой продукции), является определение температуры плавления. Важно тщательно выбрать процедуру определения точки плавления для получения удостоверяемых результатов контроля качества (КК) и обеспечения качества (ОК). Аналитические лаборатории КК/ОК обязаны регулярно калибровать свои приборы для определения точки плавления, чтобы определить, соответствуют ли их приборы конкретным требованиям, установленным их местными, национальными и международными лабораториями.
Топленое масло или масло является одним из наиболее потребляемых продуктов в Индии. Очень важно обеспечить его чистоту, так как фальсифицированное коровье топленое масло смешивают с растительными маслами и жиром животного происхождения. Прогорклое топленое масло также доступно на рынке из-за того же цвета и текстуры. Вот несколько простых трюков, которые можно выполнять дома, и они основаны на концепции плавления для обеспечения его чистоты.
Тепловой тестВозьмите чайную ложку топленого масла в сосуд и нагрейте его. Если топленое масло сразу же тает и приобретает коричневатый цвет, значит, оно чистое. Однако, если для плавления требуется некоторое время и появляется светло-желтая текстура, то это нечистый, т. Е. Смешанный с некоторыми примесями.
Тест на ладонь Возьмите чайную ложку топленого масла в ладонь, если оно тает само по себе, значит оно чистое или нет.
Гхи также фальсифицируют различными видами масел, особенно кокосовым, поэтому для проверки того, содержит ли гхи кокосовое масло, используется метод пароварки. В этом методе топленое масло растапливают в стеклянной банке с помощью пароварки, которая содержит банку, помещенную над кастрюлей с кипящей водой, а затем помещают эту банку на некоторое время в холодильник. Если топленое масло и кокосовое масло затвердевают отдельными слоями, то топленое масло не является чистым, поскольку разные слои показывают присутствие масла в топленом масле.
2. Катание на коньках Зимой многие находят лед очаровательным. Им нравится кататься на коньках в заснеженных районах, но задумывались ли вы когда-нибудь, что стоит за скользкостью льда, которая позволяет им кататься на коньках? Причиной скользкости льда является идея таяния под давлением и трения. Когда на лед оказывается давление, он тает верхний слой льда и создает тонкий слой воды, который позволяет кататься на коньках. Теория плавления под давлением основана на том факте, что температура замерзания воды ниже 0°C для определенного диапазона высокого давления.
Теория плавления под давлением основана на том факте, что температура замерзания воды ниже 0°C для определенного диапазона высокого давления.
Примером плавления является образование сплава. Большинство сплавов получают путем смешения различных металлов в расплавленном состоянии с последующим затвердеванием. Все металлы имеют разную температуру плавления. Это создает некоторые трудности при формировании сплава. Например, медь плавится при 1083°С, а цинк плавится при 419°С и кипит при 907°С. Так, при изготовлении латуни (сплава меди и цинка), если расплавить оба металла, нагрев их выше 1083°С, жидкий цинк тоже выкипит, а пары окислятся на воздухе. Чтобы этого избежать, сначала приходится плавить металл с высокой температурой, т. е. медь, а когда медь приходит в расплавленное состояние, к ней добавляют твердый цинк, и он быстро растворяется в жидкой меди до того, как большая часть цинка расплавится. выкипело. Здесь правильное знание температуры плавления металлов и процесса плавления является обязательным для изготовления различных сплавов, что, в свою очередь, предлагает множество применений в различных отраслях промышленности.
Суперсплавы состоят из различных комбинаций сплавов никеля, железа и кобальта, и эти сплавы в основном используются в реактивных двигателях. Они производятся методом электронно-лучевой плавки. Этот специализированный процесс плавки включает плавку в высоком вакууме с использованием электронного луча. Этот процесс плавления является дорогостоящим, поэтому его использование ограничено.
Плавка сталиСталь представляет собой сплав железа и углерода. Знание его температуры плавления важно для его изготовления в ценной форме. Температура плавления стали зависит от ее типа. Следы других элементов также добавляются для улучшения его свойств, и их процентное содержание в них также влияет на их температуру плавления. Из 5 основных типов стали нержавеющая сталь используется в основном для кухонных столовых приборов.
4. Лампочки
Лампы содержат нить накаливания, состоящую из металлического вольфрама. Металлический вольфрам используется, потому что он имеет самую высокую температуру плавления среди металлов. Чтобы произвести свет, металл, используемый в нитях накала лампы, должен быть нагрет до экстремальных температур. Большинство металлов обычно плавятся до достижения таких экстремальных температур. Поэтому лампочки изготавливаются с вольфрамовой нитью, потому что она имеет аномально высокую температуру плавления. Нить накаливания в лампочке закрыта герметичной бескислородной камерой, чтобы избежать возгорания. Вольфрамовая нить испаряется тем быстрее, чем выше температура нити. По мере того, как все больше и больше атомов испаряется, происходит распад нити накала, и стекло темнеет, что сокращает срок службы колбы, тогда как в современных лампочках используется газ аргон, который увеличивает срок службы вольфрамовой нити. В таких лампах, когда атомы вольфрама испаряются, они сталкиваются с атомами аргона и отскакивают обратно к нити накала, где воссоединяются с твердой структурой.
Металлический вольфрам используется, потому что он имеет самую высокую температуру плавления среди металлов. Чтобы произвести свет, металл, используемый в нитях накала лампы, должен быть нагрет до экстремальных температур. Большинство металлов обычно плавятся до достижения таких экстремальных температур. Поэтому лампочки изготавливаются с вольфрамовой нитью, потому что она имеет аномально высокую температуру плавления. Нить накаливания в лампочке закрыта герметичной бескислородной камерой, чтобы избежать возгорания. Вольфрамовая нить испаряется тем быстрее, чем выше температура нити. По мере того, как все больше и больше атомов испаряется, происходит распад нити накала, и стекло темнеет, что сокращает срок службы колбы, тогда как в современных лампочках используется газ аргон, который увеличивает срок службы вольфрамовой нити. В таких лампах, когда атомы вольфрама испаряются, они сталкиваются с атомами аргона и отскакивают обратно к нити накала, где воссоединяются с твердой структурой. Поскольку аргон — инертный газ, нет возможности объединить этот элемент в реакции горения. Хотя это по-прежнему популярный метод освещения внутри домов, в последнее время охлаждаемые источники света, такие как люминесцентные лампы и светодиоды, постепенно вытесняют старые лампочки.
Поскольку аргон — инертный газ, нет возможности объединить этот элемент в реакции горения. Хотя это по-прежнему популярный метод освещения внутри домов, в последнее время охлаждаемые источники света, такие как люминесцентные лампы и светодиоды, постепенно вытесняют старые лампочки.
Сахар представляет собой форму углеводов, которая содержит атомы углерода, водорода и кислорода. Когда человеческое тело потребляет углеводы, они превращаются в глюкозу, которая служит предпочтительным источником энергии для всех клеток человеческого тела. Существуют две основные формы сахаров: простые и сложные. Отличие заключается в их химическом строении. Простые углеводы состоят из молекул сахара, тогда как сложные углеводы состоят из двух или более молекул сахара. Четыре наиболее распространенные формы сахара в нашем рационе — это глюкоза, фруктоза (фруктовый сахар), сахароза (столовый сахар), лактоза (дневной сахар).
Плавящиеся сахара Диапазон температур разложения сахаров составляет от 184°C до 186°C. Когда мы осторожно нагреваем сахарозу, возникает явление, известное как «кажущееся плавление». Кристаллы сахара на самом деле не плавятся, а демонстрируют реакцию, называемую «инверсией», которая означает разложение двух молекулярных компонентов сахаров, то есть глюкозы и фруктозы. Этот процесс известен как карамелизация и состоит из двух фаз. На первом этапе структура сахара изменяется при повышении температуры. Это можно наблюдать, когда сахар начинает «таять». На втором этапе более сильное повышение температуры вызывает элиминацию молекул воды, что приводит к реакции, называемой «бета-элиминация». После этого вещество темнеет по цвету и по вкусу больше напоминает «карамель». При чрезмерном нагреве останется только нагар, а это говорит о том, что наша карамель подгорела. Когда происходит инверсия, мы получаем «инвертный сахар», который очень гигроскопичен (способен поглощать большое количество молекул воды), что делает его идеальным для приготовления мягких сладостей и десертов.
Когда мы осторожно нагреваем сахарозу, возникает явление, известное как «кажущееся плавление». Кристаллы сахара на самом деле не плавятся, а демонстрируют реакцию, называемую «инверсией», которая означает разложение двух молекулярных компонентов сахаров, то есть глюкозы и фруктозы. Этот процесс известен как карамелизация и состоит из двух фаз. На первом этапе структура сахара изменяется при повышении температуры. Это можно наблюдать, когда сахар начинает «таять». На втором этапе более сильное повышение температуры вызывает элиминацию молекул воды, что приводит к реакции, называемой «бета-элиминация». После этого вещество темнеет по цвету и по вкусу больше напоминает «карамель». При чрезмерном нагреве останется только нагар, а это говорит о том, что наша карамель подгорела. Когда происходит инверсия, мы получаем «инвертный сахар», который очень гигроскопичен (способен поглощать большое количество молекул воды), что делает его идеальным для приготовления мягких сладостей и десертов.
 Плавка стекла
Плавка стекла В процессе производства стекла сырье нагревается до температуры от 1500°C до 1700°C в стекловаренных печах. Он трансформируется через последовательность химических реакций. Стекловаренные печи могут быть электрическими, газовыми или жидкотопливными.
7. Плавление монет Вы когда-нибудь замечали, почему размер монет в Индии уменьшается? Логика этого заключается в плавлении монет. Правительство всегда пытается снизить металлическую стоимость монеты по сравнению с ее номинальной стоимостью, потому что, если металлическая стоимость монет больше ее номинальной стоимости, то люди будут поощряться к тому, чтобы переплавить монету и продать этот металл на открытом рынке, чтобы получить прибыль. . Это можно понять на этом примере, предположим, что у человека есть монета в 1 рупию, если он переплавит монету и продаст металл на открытом рынке за 2 рупии, то он получит прибыль в размере 1 рупии. Представьте, если бы все люди начнут этот процесс плавления, тогда все монеты исчезнут, и это создаст сложную ситуацию для правительства. Таким образом, это причина того, что правительство пытается снизить стоимость металла по сравнению с ее номинальной стоимостью, чтобы люди не поощрялись к переплавке монет.
Таким образом, это причина того, что правительство пытается снизить стоимость металла по сравнению с ее номинальной стоимостью, чтобы люди не поощрялись к переплавке монет.
Сильный снегопад в регионах с холодным климатом вызывает повсеместное промерзание почвы и большие отложения снега, что часто приводит к дорожно-транспортным происшествиям и риску для жизни водителей и пассажиров. Таким образом, таяние снега необходимо, чтобы избежать таких ситуаций. Для таяния снега используются два типа методов: химический метод, который включает применение химикатов, таких как NaCl или CaCl2, для удаления снега, и метод нагрева, который включает тепловой насос, инфракрасную лампу или нагревательные провода для таяния снега. снег.
9. Восковые расплавы Восковые расплавы представляют собой свечи без фитиля. Они доступны в различных формах и размерах. Это тип ароматизированного воска, который расплавляют в устройствах для нагревания воска (электрических устройствах), который выделяет более сильный и стойкий аромат, чем свеча.



 : Аcт-Пресс, 1999.
: Аcт-Пресс, 1999.