61. Оксид и гидроксид алюминия
Оксид алюминия – Al2O3. Физические свойства: оксид алюминия – белый аморфный порошок или очень твердые белые кристаллы. Молекулярная масса = 101,96, плотность – 3,97 г/см3, температура плавления – 2053 °C, температура кипения – 3000 °C.
Химические свойства: оксид алюминия проявляет амфотерные свойства – свойства кислотных оксидов и основных оксидов и реагирует и с кислотами, и с основаниями. Кристаллический Аl2О3 химически пассивен, аморфный – более активен. Взаимодействие с растворами кислот дает средние соли алюминия, а с растворами оснований – комплексные соли – гидроксоалюминаты металлов:
При сплавлении оксида алюминия с твердыми щелочами металлов образуются двойные соли – метаалюминаты (безводные алюминаты):
Получение: оксид алюминия получают методом восстановления алюминием металлов из их оксидов: хрома, молибдена, вольфрама, ванадия и др. – металлотермия, открытый Бекетовым:
Применение: оксид алюминия применяется для производства алюминия, в виде порошка – для огнеупорных, химически стойких и аб-разивных материалов, в виде кристаллов – для изготовления лазеров и синтетических драгоценных камней (рубины, сапфиры и др.), окрашенных примесями оксидов других металлов – Сr2О3 (красный цвет), Тi2О3 и Fe2О3 (голубой цвет).
Гидроксид алюминия – А1(ОН)3. Физические свойства: гидроксид алюминия – белый аморфный (гелеобразный) или кристаллический. Почти не растворим в воде; молекулярная масса – 78,00, плотность – 3,97 г/см3.
Химические свойства: типичный амфотерный гидроксид реагирует:
1) с кислотами, образуя средние соли: Al(ОН)3 + 3НNO3 = Al(NO3)3 + 3Н2О;
2) с растворами щелочей, образуя комплексные соли – гидроксоалюминаты: Al(ОН)3 + КОН + 2Н2О = К[Al(ОН)4(Н2О)2].
При сплавлении Al(ОН)3 с сухими щелочами образуются метаалюминаты: Al(ОН)3 + КОН = КAlO2 + 2Н2О.
Получение:
1) из солей алюминия под действием раствора щелочей: AlСl3 + 3NaOH = Al(ОН)3 + 3Н2О;
2) разложением нитрида алюминия водой: AlN + 3Н2О = Аl(ОН)3 + NН3?;
3) пропусканием СО2 через раствор гидроксокомплекса: [Аl(ОН)4]-+ СО2 = Аl(ОН)3 + НСО3-;
4) действием на соли Аl гидратом аммиака; при комнатной температуре образуется Аl(ОН)3.
62. Общая характеристика подгруппы хрома
Элементы подгруппы хрома занимают промежуточное положение в ряду переходных металлов. Имеют высокие температуры плавления и кипения, свободные места на электронных орбиталях. Элементы
Все элементы образуют оксид MVIO3, известны также оксиды с низшими степенями окисления. Все элементы данной подгруппы амфотерны – образуют комплексные соединения и кислоты.
Хром, молибден и вольфрам востребованы в металлургии и электротехнике. Все рассматриваемые металлы покрываются пассивирующей оксидной пленкой при хранении на воздухе или в среде кислоты-окислителя. Удалив пленку химическим или механическим способом, можно повысить химическую активность металлов.
Хром. Элемент получают из хромитной руды Fe(CrO2)2, восстанавливая углем: Fe(CrO2)2 + 4C = (Fe + 2Cr) + 4CO?.
Чистый хром получают восстановлением Cr2O3 с помощью алюминия или электролиза раствора, содержащего ионы хрома. Выделяя хром с помощью электролиза, можно получить хромовое покрытие, используемое в качестве декоративных и защитных пленок.
Из хрома получают феррохром, применяемый при производстве стали.
Молибден. Получают из сульфидной руды. Его соединения используют при производстве стали. Сам металл получают при восстановлении его оксида. Прокаливая оксид молибдена с железом, можно получить ферромолибден. Используют для изготовления нитей и трубок для обмотки печей и электроконтактов. Сталь с добавлением молибдена используют в автомобильном производстве.
Вольфрам. Получают из оксида, добываемого из обогащенной руды. В качестве восстановителя используют алюминий или водород. Получившийся вольфрам в идее порошка впоследствии формуют при высоком давлении и термической обработке (порошковая металлургия). В таком виде вольфрам используют для изготовления нитей накаливания, добавляют к стали.
studfiles.net
Как из оксида алюминия получить алюминий? Химические формулы
Алюминий обладает свойствами, которые применимы во многих промышленностях: военном деле, строительстве, питании, транспорте и др. Он пластичный, легкий и широко распространен в природе. Многие люди даже не подозревают того, как широко можно использовать алюминий.
Многие сайты и книги описывают этот чудесный металл и его свойства. Информация находится в свободном доступе.
В лаборатории можно производить любые соединения алюминия, но в малых количествах и по высоким ценам.
История добычи элемента
Вплоть до середины девятнадцатого века ни об алюминии, ни о восстановлении его оксида речи не шло. Первая попытка получения алюминия была предпринята химиком Х. К. Эрстедом и закончилась успешно. Чтобы восстановить металл из его оксида, он использовал амальгамированный калий. Но никто не понял, что получилось в итоге.
Прошло несколько лет, и алюминий снова был получен химиком Велером, который нагрел безводный хлорид алюминия с калием. Ученый упорно трудился 20 лет и, наконец, сумел создать гранулированный металл. По цвету он напоминал серебро, но был легче него в несколько раз. Длительное время до начала двадцатого века алюминий ценился больше золота и выставлялся в музеях как экспонат.
Где-то в начале XIX века английский химик Дэви провел электролиз оксида алюминия и получил металл, названный «алюмиум» или «алюминум», что можно переводить как «квасцы».
Алюминий очень трудно отделить от других веществ — это одна из причин его дороговизны в то время. Ученое собрание и промышленники быстро узнали о потрясающих свойствах нового металла и продолжили попытки его добычи.
В больших количествах алюминий стали получать уже в конце того же девятнадцатого века. Ученый Ч. М. Холлом предложил растворять оксид алюминия в расплаве криолита и пропускать эту смесь через электрический ток. Через какое-то время в сосуде появлялся чистый алюминий. В промышленности и сейчас производят металл этим методом, но об этом позже
Для производств нужна прочность, которой, как выяснилось чуть позднее, у алюминия не было. Тогда металл стали сплавлять с иными элементами: магнием, кремнием и т. д. Сплавы были намного прочнее обычного алюминия — именно из них стали выплавлять самолеты и военную технику. А придумали слить алюминий и другие металлы в единое целое в Германии. Там же, в Дюрене, сплав, названный дюралюминием, поставили на производство.
Как из оксида алюминия получить алюминий
В рамках школьной программы по химии проходят тему «Как из оксида металла получить чистый металл».
К этому методу мы можем отнести и наш вопрос, как из оксида алюминия получить алюминий.
Чтобы образовать металл из его оксида, нужно добавить восстановитель — водород. Пойдет реакция замещения с образованием воды и металла: МеО + Н2 = Ме + Н2О (где Ме — металл, а Н2 — водород).
Пример с алюминием: Al2О3 + 3Н2 = 2Al + 3Н2О
На практике такой прием позволяет получать чистые активные металлы, которые не восстанавливаются оксидом углерода. Метод подходит для очистки небольшого количества алюминия и довольно-таки дорого стоит.
Как получить алюминий из оксида алюминия через добавление более электроотрицательного металла
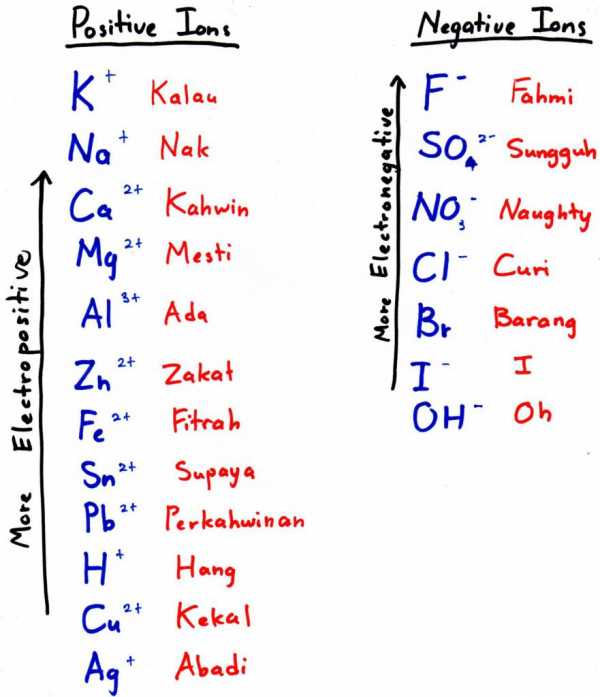
Чтобы получить алюминий этим способом, нужно подобрать более электроотрицательный металл и добавить его к оксиду — он вытеснит наш элемент из кислородного соединения. Более электроотрицательный металл — это тот, что стоит левее в электрохимическом ряду (на фото к подзаголовку — выше).
Примеры: 3Mg + Al2О3 = 2Al + 3MgO
6К + Al2О3 = 2Al + 3К2О
6Li + Al2О3 = 2Al + 3Li2О
Но как получить алюминий из оксида алюминия в условиях широкой промышленности?
Промышленный способ

Большинство производств для добычи элемента используют руды, которые называют бокситами. Сначала из них выделяют оксид, потом растворяют его в расплаве криолита, а затем получают чистый алюминий путем электрохимической реакции.
Это обходится дешевле всего и не требует дополнительных операций.
Кроме того, можно получить хлорид алюминия из оксида алюминия. Как это сделать?
Получение хлорида алюминия
Хлоридом алюминия называют среднюю (нормальную) соль из соляной кислоты и алюминия. Формула: AlCl3.
Для получения нужно добавить кислоту.
Уравнение реакции выглядит следующим образом — Al2О3 + 6HCl = 2AlCl3 + 3Н2О.
Как получить хлорид алюминия из оксида алюминия, не добавляя кислот?
Для этого надо прокалить спрессованную смесь оксида алюминия и углерода (сажа) в токе хлора при 600-800 гр. Хлорид должен отогнаться.
Эту соль применяют в качестве катализатора многих реакций. Ее главная роль — образование продуктов присоединения с разными веществами. Хлоридом алюминия протравливают шерсть, и его добавляют в антиперспиранты. Также соединение играет не последнюю роль в переработке нефти.
Получение гидроксоалюмината натрия

Как из оксида алюминия получить гидроксоалюминат натрия?
Чтобы получить это сложное вещество, можно продолжить цепочку превращений и сначала получить из оксида хлорид, а потом добавить гидроксид натрия.
Хлорид алюминия — AlCl3, гидроксид натрия — NaOH.
Al2O3 → AlCl3 → Na[Al(OH)4]
Al2О3 + 6HCl = 2AlCl3 + 3Н2О
AlCl3 + 4NaOH (концентрированный) = Na[Al(OH)4] + 3NaCl5
Но как из оксида алюминия получить тетрагидроксоалюминат натрия, избегая превращения в хлорид?
Чтобы из оксида алюминия получить алюминат натрия, нужно создать гидроксид алюминия и добавить к нему щелочь.
Следует напомнить, что щелочь — это основание, растворимое в воде. Сюда относят гидроксиды щелочных и щелочноземельных металлов (I и II группа таблицы Менделеева).
Al→ Al(ОН)3 → Na[Al(OH)4]
Из оксидов металлов средней активности, к которым относится алюминий, нельзя получать гидроксиды. Поэтому сначала мы восстановим чистый металл, например, через водород:
Al2О3 + 3Н2 = 2Al + 3Н2О.
А потом получим гидроксид.
Чтобы получить гидроксид, надо растворить алюминий в кислоте (для примера, во фтороводородной): 2Al + 6HF = 2AlF3 + 3Н2. А затем прогидролизовать полученную соль с добавлением равного количества щелочи в разбавленном растворе: AlF3 +3NaOH = Al(ОН)3 + 3NaF.
И дальше: Al(ОН)3 + NaOH = Na[Al(ОН)4]
(Al(ОН)3 — амфотерное соединение, которое может взаимодействовать и с кислотами, и с щелочами).
Тетрагидроксоалюминат натрия отлично растворяется в воде, а еще это вещество широко применяют в оформлении и добавляют в бетон, чтобы ускорить отвердевание.
Про метаалюминаты

Начинающие производители глинозема, наверное, задавались вопросом: «Как из оксида алюминия получить метаалюминат натрия?»
Алюминаты используются в широком производстве для ускорения некоторых реакций, окрашивания тканей и получения глинозема.
Лирическое отступление: глинозем — это, по сути, и есть оксид алюминия Al2О3.
Обычно оксид добывают из метаалюминатов, но здесь будет рассмотрен «обратный» способ.
Итак, чтобы получить наш алюминат, нужно просто смешать оксид натрия с оксидом алюминия при очень высокой температуре.
Случится реакция соединения — Al2О3 + Na2О = 2NaAlO2
Для нормального протекания требуется температура в 1200°C.
Можно проследить за изменением энергии Гиббса в реакции:
Na2O(к.)+ Al2O3(к.)= 2NaAlO2(к.), ΔG0298= -175 кДж.
Еще одно лирическое отступление:
Энергия Гиббса (или «свободная энергия Гиббса») — это зависимость, которая существует между энтальпией (энергией, доступной для преобразований) и энтропией (мерой «хаоса», беспорядка в системе). Абсолютное значение измерить невозможно, поэтому измеряются изменения во время протекания процесса. Формула: G (энергия Гиббса) = Н (изменение энтальпии между продуктами и исходными веществами реакции) — Т (температура) * S (изменение энтропии между продуктами и исходниками). Измеряется в Джоулях.
Как из оксида алюминия получить алюминат?
Для этого подойдет и тот способ, который был рассмотрен выше — с глиноземом и натрием.
Оксид алюминия, смешанный с оксидом другого металла при высоких температурах, и дает метаалюминат.
Но еще можно сплавить гидроксид алюминия со щелочью в присутствии оксида углерода СО:
Al(ОН)3 + NaOH = NaAlO2 + 2Н2О.
Примеры:
- Al2О3 + 2КОН = 2KAlO2 + Н2О (здесь глинозем растворяется в едкой щелочи калия) — алюминат калия;
- Al2О3 + Li2О = 2LiAlO2 — алюминат лития;
- Al2О3 + СаО = СаО × Al2О3 — сплавление оксида кальция с окисью алюминия.
Получение сульфата алюминия

Как получить сульфат алюминия из оксида алюминия?
Способ включен в школьную программу восьмых и девятых классов.
Сульфат алюминия — это соль вида Al2(SO4)3. Представлена может быть в виде пластинок или порошка.
Это вещество может разлагаться на оксиды алюминия и серы при температуре от 580 градусов. Сульфат используется для очистки воды от мельчайших частиц, очень полезен в пищевой, бумажной, тканевой и других отраслях производства. Он широко доступен благодаря своей низкой цене. Очистка воды происходит из-за некоторых особенностей сульфата.
Дело в том, что загрязняющие частицы имеют вокруг себя двойной электрический слой, а рассматриваемый реагент является коагулянтом, который, при проникновении в электрическое поле частиц, вызывает сжатие слоев и нейтрализует заряд частиц.
Теперь о самом методе. Чтобы получить сульфат, нужно смешать оксид и серную (не сернистую) кислоту.
Выходит реакция взаимодействия глинозема с кислотой:
Al2O3+3H2SO4=Al2(SO4)3+H2O
Вместо оксида можно добавить сам алюминий или его гидроксид.
В промышленности для получения сульфата используют уже известную из третьей части этой статьи руду — боксит. Ее обрабатывают серной кислотой и получают «загрязненный» сульфат алюминия. В боксите содержится гидроксид, а реакция в упрощенном виде выглядит так:
3H2SO4 + 2Al(OH)3 = Al2(SO4)3 + 6H2O
Бокситы
Боксит — это руда, состоящая сразу из нескольких минералов: железа, бемита, гиббсита и диаспора. Является главным источником добычи алюминия, образуется путем выветривания. Крупнейшие месторождения бокситов находятся в России (на Урале), США, Венесуэле (река Ориноко, штат Боливар), Австралии, Гвинее и Казахстане. Эти руды бывают моногидратными, тригидратными и смешанными.
Получение оксида алюминия
Про глинозем выше сказано много, но до сих пор не описано, как получить оксид алюминия. Формула — Al2О3.
А нужно всего-навсего сжечь алюминий в кислороде. Горение — процесс взаимодействия О2 и другого вещества.
Простейшее уравнение реакции выглядит следующим образом:
4Al + 3О2 = 2Al2О3
Оксид не растворяется в воде, но он хорошо растворим в криолите при высокой температуре.
Свои химические свойства оксид проявляет при температуре от 1000°С. Именно тогда он начинает взаимодействовать с кислотами и щелочами.
В естественных условиях корунд является единственный устойчивой вариацией вещества. Корунд очень твердый, с плотностью примерно 4000 г/м3. Твердость этого минерала по шкале Мооса — 9.

Оксид алюминия — амфотерный оксид. Легко преобразовывается в гидроксид (см. выше), а превратившись, сохраняет все свойства своей группы с преобладанием основных.
Амфотерные оксиды — это оксиды, которые могут проявлять как основные (свойства оксидов металлов), так и кислотные (оксидов неметаллов) свойства в зависимости от условий.
К амфотерным оксидам, исключая оксид алюминия, относятся: оксид цинка (ZnO), оксид бериллия (ВеО), оксид свинца (PbO), оксид олова (SnO), оксид хрома (Cr2О3), оксид железа (Fe2О3) и оксид ванадия (V2О5).
Соли: комплексные и не очень
Бывают средние (нормальные), кислые, основные и комплексные.
Средние соли состоят из самого металла и кислотного остатка и имеют вид AlCl3 (хлорид алюминия), Na2SO4 (сульфат натрия), Al(NO3)3 (нитрат алюминия) или MgPO4.
Кислые соли — это соли из металла, водорода и кислотного остатка. Их примеры: NaHSO4, CaHPO4.
Основные соли так же, как и кислые, состоят из кислотного остатка и металла, но вместо Н там ОН. Примеры: (FeOH)2SO4, Ca(OH)Cl.
И, наконец, комплексные соли — это вещества из ионов разных металлов и кислотного остатка многоосновной кислоты (соли, содержащие сложный ион): Na3[Co(NO2)6], Zn[(UO2)3(CH3COO)8].
Речь пойдет о том, как из оксида алюминия получить комплексную соль.
Условием превращения оксида в это вещество является его амфотерность. Глинозем отлично подходит для метода. Чтобы получить комплексную соль из оксида алюминия, нужно смешать этот оксид с раствором щелочи:
2NaOH + Al2O3 + H2O → Na2[Al(ОН)4]
Этот род веществ также образуется при воздействии растворов щелочей на амфотерные гидроксиды.
Раствор гидроксида калия взаимодействует с основанием цинка с получением тетрагидроксоцинката калия:
2KOH + Zn(OH)2 → K2[Zn(OH)4]
Раствор щелочи натрия реагирует, например, с гидроксидом берилия с образованием тетрагидроксобериллата натрия:
NaOH + Be(OH)2 → Na2[Be(OH)4]
Использование солей
Комплексные соли алюминия часто используют в фармацевтике, производстве витаминов и биологически активных веществ. Препараты, созданные на основе этих веществ, помогают в борьбе с похмельем, улучшают состояние желудка и общее самочувствие организма человека. Очень полезные соединения, как можно заметить.
Реактивы дешевле покупать в интернет-магазинах. Там большой выбор веществ, но сайты лучше выбирать надежные и проверенные временем. Если покупать что-то на «однодневках», то риск потерять деньги увеличивается.
При работе с химическими элементами нужно соблюдать правила безопасности: обязательно наличие перчаток, защитного стекла, специализированной посуды и приборов.
Эпилог
Химия – несомненно, сложная для понимания наука, но иногда полезно в ней разобраться. Проще всего это сделать через интересные статьи, простой слог и понятные примеры. Не лишним будет прочитать пару книг по теме и освежить в памяти курс школьной программы по химии.
Здесь было разобрано большинство тем химии, связанных с преобразованиями алюминия и его оксидов, в том числе, как из оксида алюминия получить тетрагидроксоалюминат, и еще множество интересных фактов. Оказалось, что у алюминия есть много самых необычных сфер применения в производстве и в быту, да и история получения металла весьма незаурядна. Химические формулы соединений алюминия тоже заслуживают внимания и подробного разбора, что и было освящено в этой статье.
fb.ru
Оксид алюминия — WiKi
Окси́д алюми́ния Al2O3 — бинарное соединение алюминия и кислорода. В природе распространён как основная составляющая часть глинозёма[3], нестехиометрической смеси оксидов алюминия, калия, натрия, магния и т. д.
Свойства
Бесцветные нерастворимые в воде кристаллы. Амфотерный оксид. Практически не растворим в кислотах. Растворяется в горячих растворах и расплавах щелочей. Является диэлектриком[4][5][6], но некоторые[7][8] исследователи считают его полупроводником n-типа. Диэлектрическая проницаемость 9,5—10. Электрическая прочность 10 кВ/мм.
Плотность
| Модификация | Плотность, г/см3 |
|---|---|
| α-Al2O3 | 3,99[2] |
| θ-Al2O3 | 3,61[3] |
| γ-Al2O3 | 3,68[4] |
| κ-Al2O3 | 3,77[5] |
Основные модификации оксида алюминия
В природе можно встретить только тригональную α-модификацию оксида алюминия в виде минерала корунда и его редких драгоценных разновидностей (рубин, сапфир и т. д.). Она является единственной термодинамически стабильной формой Al
Известны также следующие кристаллические модификации оксида алюминия: кубическая η-фаза, моноклинная θ-фаза, гексагональная χ-фаза, орторомбическая κ-фаза. Спорным остаётся существование δ-фазы, которая может быть тетрагональной или орторомбической[9][10].
Вещество, иногда описываемое как β-Al2O3, на самом деле представляет собой не чистый оксид алюминия, а ряд алюминатов щелочных и щёлочноземельных металлов со следующими общими формулами: MeO·6Al 2O3 и Me2O·11Al2O3, где МеО — это оксиды кальция, бария, стронция и т. д., а Ме2О — оксиды натрия, калия, лития и других щелочных металлов. При 1600—1700 °С β-модификация разлагается на α-Al2O3 и оксид соответствующего металла, который выделяется в виде пара.
Получение
Получают из бокситов, нефелинов, каолина, алунитов алюминатным или хлоридным методом. Сырьё в производстве алюминия, катализатор, адсорбент, огнеупорный и абразивный материал.
- 3Cu2O + 2Al →1000 ∘C 6Cu + Al2O3{\displaystyle {\mathsf {3Cu_{2}O\ +\ 2Al\ {\xrightarrow {1000\ ^{\circ }C}}\ 6Cu\ +\ Al_{2}O_{3}}}}
Плёнки оксида алюминия на поверхности алюминия получают электрохимическими или химическими методами. Так, например, получают диэлектрический слой в алюминиевых электролитических конденсаторах. В микроэлектронике также применяется эпитаксия оксида алюминия, которая многими учёными считается перспективной, например, в изоляции затворов полевых транзисторов.[5][6]
Применение
Оксид алюминия (Al2O3), как минерал, называется корунд. Крупные прозрачные кристаллы корунда используются как драгоценные камни. Из-за примесей корунд бывает окрашен в разные цвета: красный корунд (содержащий примеси хрома) называется рубином, синий, традиционно — сапфиром. Согласно принятым в ювелирном деле правилам, сапфиром называют кристаллический α-оксид алюминия любой окраски, кроме красной. В настоящее время кристаллы ювелирного корунда выращивают искусственно, но природные камни всё равно ценятся выше, хотя по виду не отличаются. Также корунд применяется как огнеупорный материал. Остальные кристаллические формы используются, как правило, в качестве катализаторов, адсорбентов, инертных наполнителей в физических исследованиях и химической промышленности.
Керамика на основе оксида алюминия обладает высокой твёрдостью, огнеупорностью и антифрикционными свойствами, а также является хорошим изолятором. Она используется в горелках газоразрядных ламп, подложек интегральных схем, в запорных элементах керамических трубопроводных кранов, в зубных протезах и т. д.
Так называемый β-оксид алюминия в действительности представляет собой смешанный оксид алюминия и натрия. Он и соединения с его структурой вызывают большой научный интерес в качестве металлопроводящего твёрдого электролита.
γ-Модификации оксида алюминия применяются в качестве носителя катализаторов, сырья для производства смешанных катализаторов, осушителя в различных процессах химических, нефтехимических производств (ГОСТ 8136-85).
Литература
- Pillet, S.; Souhassou, M.; Lecomte, C.; Schwarz, K. и др. Acta Crystallograica A (39, 1983-) (2001), 57, 209—303
- Husson, E.; Repelin, Y. Europen Journal of Solid State Inogranic Chemistry
- Gutierrez, M.; Taga, A.; Johansson, B. Physical Review, Serie 3. B — Condensed Matter (18, 1978-) (2001), 65, 0121011-0121014
- Smrcok, L.; Langer, V.; Halvarsson, M. Ruppi, S. Zeitschrift fuer Kristallographie (149, 1979-) (2001), 216, 409—412
См. также
Ссылки
Примечания
ru-wiki.org
Оксид алюминия(III) — это… Что такое Оксид алюминия(III)?
- Оксид алюминия(III)
Оксид алюминия Al2O3 — в природе распространён как глинозём, нестехиометрическая смесь оксидов алюминия, калия, натрия, магния и т. д.
Свойства
бесцветные нерастворимые в воде кристаллы.
- химические свойства — амфотерный оксид. Практически не растворим в кислотах. Растворяется в горячих растворах и расплавах щелочей.
- tпл 2044 °C.
- Является полупроводником n-типа.
Получение
Получают из бокситов, нефелинов, каолина, алунитов алюминатным или хлоридным методом. Сырьё в производстве алюминия, катализатор, адсорбент, огнеупорный и абразивный материал.
Чистый оксид алюминия может находиться в нескольких кристаллических формах: α-Al2O3 (корунд), γ-Al2O3, δ-Al2O3, θ-Al2O3, χ-Al2O3 и др.
Применение
Средние цены на глинозем металлургического сорта в 2007 году — $370/тонна /по материалам infogeo.ru/metalls
Оксид алюминия (α-Al2O3), как минерал, называется корунд. Крупные прозрачные кристаллы корунда используются, как драгоценные камни. Из-за примесей корунд бывает окрашен в разные цвета: красный корунд называется рубином, синий, традиционно — сапфиром. Согласно принятым в ювелирном деле правилам, сапфиром называют кристаллический α-оксид алюминия любой окраски кроме красной. В настоящее время кристаллы ювелирного корунда выращивают искусственно, но природные камни всё равно ценятся дороже, хотя по виду и не отличаются. Также корунд применяется как огнеупорный материал.
Остальные кристаллические формы используются, как правило, в качестве катализаторов, адсорбентов, инертных наполнителей в физических исследованиях и химической промышленности.Так называемый β-оксид алюминия в действительности представляет собой смешанный оксид алюминия и натрия. Он и соединения с его структурой вызывают большой научный интерес в качестве металлопроводящего твёрдого электролита.
Примечания
См. также
Ссылки
Арсенид алюминия (AlAs) • Диборид алюминия (AlB2) • Додекаборид алюминия (AlB12) • Бромид алюминия (AlBr3) • Монохлорид алюминия (AlCl) • Хлорид алюминия (AlCl3) • Монофторид алюминия (AlF) • Фторид алюминия (AlF3) • Гидрид алюминия (AlH3) • Иодид алюминия (AlI3) • Нитрид алюминия (AlN) • Нитрат алюминия (Al(NO3)3) • Монооксид алюминия (AlO) • Гидроксид алюминия (Al(OH)3) • Оксинитрид алюминия (AlON) • Фосфид алюминия (AlP) • Фосфат алюминия (AlPO4) • Антимонид алюминия (AlSb) • Молибдат алюминия (Al2(MoO4)3) • Оксид алюминия (Al2O3) • Сульфид алюминия (Al2S3) • Сульфат алюминия (Al2(SO4)3) • Селенид алюминия (Al2Se3) • Силикат алюминия (Алюмосиликаты) (Al2SiO5) • Карбид алюминия (Al4C3)
Wikimedia Foundation. 2010.
- Оксид азота (IV)
- Оксид алюминия (III)
Смотреть что такое «Оксид алюминия(III)» в других словарях:
Оксид алюминия (III) — Оксид алюминия Общие Сокращения Корунд Химическая формула Al2O3 Молярная масса 101.96 г/моль … Википедия
Хлорид алюминия (III) — AlCl3· 6h3O Хлорид алюминия (хлористый алюминий) AlCl3 соль. Свойства Бесцветные кристаллы, плотностью 2,44 г/см³. При обычном давлении возгоняется при 183 °C (под давлением плавится при 192,6 °C). В воде хорошо растворим (44,38 г в 100 г h3O… … Википедия
Хлорид алюминия(III) — AlCl3· 6h3O Хлорид алюминия (хлористый алюминий) AlCl3 соль. Свойства Бесцветные кристаллы, плотностью 2,44 г/см³. При обычном давлении возгоняется при 183 °C (под давлением плавится при 192,6 °C). В воде хорошо растворим (44,38 г в 100 г h3O… … Википедия
Оксид-сульфат титана — Общие Систематическое наименование Оксид сульфат титана Традиционные названия Основной сернокислый титан; оксосульфат титана; сульфат титанила Химическая формула TiOSO4 Физические свойства … Википедия
Оксид кобальта(II) — Общие Систематическое наименование оксид кобальта(II) Традиционные названия окись кобальта Химическая формула CoO Физические свойства Состояние ( … Википедия
Оксид — (окисел, окись) соединение химического элемента с кислородом, в котором сам кислород связан только с менее электроотрицательным элементом. Химический элемент кислород по электроотрицательности второй после фтора, поэтому к оксидам относятся… … Википедия
АЛЮМИНИЯ СЕМЕЙСТВО — ПОДГРУППА IIIA. СЕМЕЙСТВО АЛЮМИНИЯ БОР, АЛЮМИНИЙ, ГАЛЛИЙ, ИНДИЙ, ТАЛЛИЙ Внешняя электронная конфигурация у всех элементов подгруппы s2p1, но наличие внутренней электронной структуры типа электронной конфигурации благородного газа у B и Al и… … Энциклопедия Кольера
Трифторид алюминия — Трифторид алюминия … Википедия
Сульфат алюминия-калия — Общие Систематическое наименование Сульфат алюминия калия Традиционные названия Сернокислый алюминий калий Химическая формула KAl(SO4)2 Физические свойства Мо … Википедия
Спектральный метод определения никеля, алюминия, магния, марганца, кобальта, олова, меди и циркония в ниобии — 4.2. Спектральный метод определения никеля, алюминия, магния, марганца, кобальта, олова, меди и циркония в ниобии Спектральному методу предшествует перевод анализируемой пробы в пятиокись ниобия. Метод основан на измерении интенсивности линий… … Словарь-справочник терминов нормативно-технической документации
dic.academic.ru
Оксид алюминия | khimie.ru
Оксид алюминия Аl2О3 получается при горении алюминия и при прокаливании гидроксида алюминия или солей алюминия с летучими кислотами в
Оксид алюминия применяют в виде корунда и наждака (мелкокристаллическая разновидность корунда, загрязненная окисью железа и кварцем) для шлифования и полирования. Далее, корунд используют для получения чрезвычайно огнеупорных материалов, например, «плавленого глинозема», применяющегося для футеровки цементных печей. Из обезвоженного гидроксида алюминия в больших количествах получают металлический алюминий.
Оксид алюминия кристаллизуется обычно в гексагональных гемиэдричееких ромбоэдрах (α-А1203) с уд. весом 3,99. Решетку оксида алюминия можно рассматривать в качестве молекулярной, так как в ней весьма отчетливо выражены молекулы А12О3. Тем не менее, каждый атом алюминия окружен шестью атомами кислорода, причем кислородные атомы, принадлежащие соседним молекулам, расположены даже ближе, чем те, которые принадлежат самой молекуле. Это объясняется сильным отталкиванием, проявляющимся внутри молекул между одноименно заряженными атомами. Одна молекула Аl2O3 полностью показаны внутри злементарной ячейки; другие же молекулы. Верхний атом алюминия, относящийся к молекуле Аl2O3
Другая гексагональная модификация (β-А12О3) с уд. весом 3;30 образуется при медленном охлаждении расплавленного оксида, но только в присутствии некоторых посторонних веществ, например МgO. По Биверсу эти посторонние вещества в значительной степени участвуют в построении решетки β-Аl2O3, так что последнюю, собственно, следует рассматривать не как модификацию А1203, но как двойной оксид, например Na2O∙11Al2O3.
Адсорбционная способность поверхностно активного оксида алюмипия возрастает еще и вследствие того, что посторонние ионы располагаются не только на поверхности оксида, но частично поверхностно внедряются в ее решетку, вытесняя ионы алюминия в раствор. Эта способность к ионному обмену обозначается как пермутоидное свойство оксида алюминия, и та часть адсорбции, которая сводится к этому явлению, называется химической адсорбцией. Фриже показал, что способность поверхностноактивного оксида алюминия к ионному обмену не обусловлена содержанием в последнего щелочей, как это первоначально предполагалось. Действительно, при применении А12О3, содержаний щелочи (например, мерковской А12О3, полученной по Ерокману), щелочные ионы принимают участие в обмене. Однако чистый γ-А12О3, приготовленный по Фрике, обладает более чем вдвое большей (по сравнению о брокмановским А12О3) адсорбционной способностью по отношению, например, к ионам Сu2+, и часть общей адсорбции, приходящаяся на долю химической адсорбции, в обоих случаях практически оказывается одинаковой (около 40%).
Ваш отзыв
Вы должны войти, чтобы оставлять комментарии.
khimie.ru
Алюминия оксиды — Справочник химика 21
Оксид и гидроксид натрия Оксид и гидроксид магния Оксид и гидроксид алюминия Оксид и гидроксид кремния Оксид и гидроксид фосфора Оксид и гидроксид серы Оксид и гидроксид хлора [c.98]Другим перспективным методом является производство кальцинированной соды на базе комплексной переработки нефелинов путем спекания нефелина с известняком или мелом и дальнейшего выщелачивания окиси алюминия. Оксид алюминия содержит до 0,5% примесей. Сода, полученная таким способом, имеет более высокую насыпную массу, чем получаемая по способу Сольве. [c.259]
Оксид алюминия оксид магния, тальк силикагели [c.151]
Для разделения бензина и газойлевой фракции нефти Понка было испытано несколько полярных и неполярных адсорбентов — силикагель, оксид алюминия, оксид магния, активный уголь [4]. Отмечен ряд закономерностей адсорбции углеводородов на силикагеле 1) снижение сорбируемости происходит в ряду поли- и бициклические арены > арены с одним ароматическим кольцом > циклоалканы и алканы 2) адсорбируемость нормальных алканов уменьшается с увеличением в молекуле числа углеродных атомов 3) циклопентан и алкилциклонентаны сорбируются более прочно, чем циклогексан и соответствуюшие алкилциклогексаны 4] нормальные алканы адсорбируются сильнее, чем разветвленные с тем же числом углеродных атомов 5) гексан сорбируется более прочно, чем циклогексан, но нормальные алкилциклогексаны — сильнее, чем нормальные алканы с тем же числом углеродных атомов 6) полиалкилбензолы сорбируются более прочно, чем моноалкилбензолы с тем же числом углеродных атомов 7) о-дизамешенные гомологи бензола сорбируются сильнее, чем и-изомеры и, по-видимому, чем ж-изомеры. Различия в сорбируемости углеводородов, отмеченные в пунктах 2—7, сравнительно невелики, и порядок может измениться при малых концентрациях одного из компонентов. [c.60]
В трех пробирках находятся следующие сухие вещества оксид кальция, оксид алюминия, оксид фосфора. При помощи каких реагентов можно различить эти вещества Напишите уравнения реакций. Ответ использовать раствор соляной (или азотной) кислоты и раствор щелочи. [c.75]
Азота диоксид Азота оксид Азотная кислота Алюминий Алюминия оксид Алюминия сульфат Аминобензол (анилин) [c.100]
При получении натрия гидроксид натрия При получении калия гидроксид калия При получении магния хлорид магния При получении алюминия оксид алюминия [c.457]
Образование простых эфиров из спиртов может происходить в газовой фазе в присутствии оксида алюминия, оксида тория или обезвоженного КА1 (804)2. При проведении реакции необходимо строго соблюдать температурный режим, так как повышение температуры влечет за собой образование алкенов. [c.146]
Алюминия оксид (электрокорунд) с легированными сталями [c.76]
Последнее должно быть критерием выбора постоянного изготовителя. Автор катализатора должен убедиться, что изготовитель имеет большой опыт в нужной области. Некоторые фирмы зарекомендовали себя как превосходные изготовители ряда металлических катализаторов, например палладия, платины, никеля и ванадия, или таких их носителей, как оксид алюминия, оксид кремния, цеолиты или уголь. Кроме того, фирма может в значительной мере владеть специфическими методиками приготовления катализатора. [c.40]
Оксид и гидроксид алюминия. Оксид алюминия, или глинозем, AI2O3 представляет собой белый порошок. Существуют модификации этого оксида в виде бесцветных кристаллов. Оксид алюминия можно получить, сжигая металл или прокаливая гидроксид алюминия [c.226]
На установках с подвижным слоем твердого теплоносителя пиролиз мазута и гудрона осуществляют при 580—680 °С. Кратность циркуляции теплоносителя на этих установках 20—30 кг/кг. В качестве теплоносителя применяют оксид алюминия, оксид кремния, углеродистый кальций, кокс, шамот, базальт, кварцевый песок и силикагель 34, 35]. Характеристика коксового теплоносителя приведена на с. 136. Песок имеет истинную плотность 2500— 2800 кг/м и насыпную плотность 1400—1600 кг/м . В нагревателе теплоноситель подогревается при помощи дымовых газов до 900— 950 °С и затем поступает в реактор. Тепловая напряженность нагревателя достигает 10,5 млн. кДж/(м»-ч). Сырье — тяжелые нефтяные остатки — нагревают в печи до 350—500 °С и подают в реактор. К сырью добавляют 40—45% масс, водяного пара. [c.147]
Абразивы искусственные карборунд, корунд Алмазы природные и нскусственные Алюминат титана и тнтанат кальция Алюмниия оксид с примесью диоксида кремния в виде аэрозоля конденсации Алюминия оксид (электрокорунд) со сплавом никеля (до 15 %) [c.76]
KATAL O 83-ЗК Оксид Меди / Оксид Цинка / Оксид Алюминия / Оксид калия Таблетки [c.31]
В течение многих лет катализаторы риформинга совершенствовались вместе с самим процессом. Наиболее широко применяемые сегодня катализаторы риформинга представляют собой один или несколько драгоценных металлов, нанесенных на оксид алюминия. Оксид алюминия в качестве носителя, используется в одной из двух кристаллических форм т) или у. г]-Форма содержит больше кислотных центров, чем -у-форма, и служит носителем для большинства монометаллических платиновых катализаторов. Она имеет более развитую начальную поверхность. При катализе и регенерациях илощадь поверхности этого носителя снижается. Уменьшение площади поверхности ограничивает срок службы катализаторов лишь несколькими циклами. [c.148]
Несмотря на то что алюминат магния плавится при 2135 °С, т. е. выше, чем оксид алюминия, реакции со смесью восстановителей идут лучше. Это объясняется тем, что при использовании данной смеси металлов теплоты выделяется больше, чем прп использовании в качестве восстановителя алюминия. Например, алюминий оксид хрома (III) непосредственно не восстанавливает ввиду недостаточного количества выделяющейся тепло-1Ы. Смесь алюминия с магнием пли кальцием этот оксид восстанавливает. [c.21]
В 1886 году двадцатидвухлетний Чарльз Мартин Холл через год после окончания Оберлинского колледжа (шт. Огайо) разработал электролизный способ восстановления алюминия (рис. VIII. 16). Этот метод до сих пор широко используется во всем мире для производства алюминия. Оксид алюминия (боксит) растворяется в расплавленном криолите (МазА1Р ) при температуре около 1000° С в большой стальной ванне, покрытой углеродом. Это покрытие выполняет роль катода, который передает электроны ионам алюминия, восстанавлива J его до металла. Расплавленный металл собирается на дне, откуда его периодически сливают. Далее он заливается в формы и используется для производства разнообразнейших вещей — от лестниц-стремянок до деталей самолетов. [c.535]
Ализарин — 85 Алюминия оксид — 67 Амидопирин — 71 Аммиак 2 н. — 3 Аммоний нитрат — 65 Аммоний хлорид, насыщенный раствор — 64 Ангидрид уксусный — 99 Ангидрид фталевый — 76 Анилин — 90 Антипирин — 72 Антрахинон — 84 [c.168]
Оксид алюминия, оксид кальция [c.151]
Посуда, приборы и реактивы установка для восстановления оксидов металлов водородом, химический стакан, пробирки, центрифуга, никелевые контейнеры, прибор для фильтрования, фильтровальная бумага, электроплитка, вольфрамат натрия, соляная кислота, оксид алюминия, оксид титана. [c.141]
Для улучшения метрологических характеристик при определении токсичных примесей в соединениях А1 и В изучена закономерность изменения интенсивности их линий в аналитических системах оксид алюминия (оксид бора) — фафит порошковый. С целью оптимизации условий определения мышьяка и сурьмы в А1 и его соединениях гидридным методом изучено влияние концентрации матричного компонента на величину абсорбции резонансных линий. Полученные результаты использованы при разработке методик атомно-эмиссионного и атомно-абсорбционного определения токсикантов в соединениях бора (фармацевтическое назначение) и сернокислом алюминии, применяемом в процессе очистки питьевой воды с пределами обнаружения ниже уровня ПДК. [c.18]
Алюминия оксид и руды [c.158]
При восстановлении алюминием оксида железа (III) образовалось 25,5 г оксида алюминия и выделилось 213,4 кДж теплоты. Теплота образования оксида и елеза (III) равна —816,7 кДж/моль. Вычислить теплоту образования оксида алюминия. [c.199]
Гидрирование этилеиа в этан было впервые осуществлено в середине XIX в. Фарадеем, применившим в качестве катализатора платиновую чернь. Впоследствии для гидрирования олефинов использовали платину, скелетный никелевый катализатор (никель Ренея), никель на носителях, медь, смешанные оксидные катализаторы (медь-хромитный и цинк-хромитный) и многие другие гетерогенные контакты.. Наиболее типичны для промышленной практики металлический никель и никель, осажденный ыа оксиде алюминия, оксиде хрома или других носителях. В их присутствии высокая скорость реакции достигается при 100—200 °С и давлении водорода 1—2 МПа. Если исходное сырье содержит сернистые соеди-Г ения, рекомендуется применять катализаторы, стойкие к сере (сульфиды никеля, вольфрама и молибдена) при 300—320°С и 5-30 МПа. [c.496]
Алюминия оксид (электрокоруид) с хромом Алюминия сплавы (в пересчете на А1) [c.76]
Соединения алюминия. Оксид алюминия известен в виде нескольких модификаций. Наиболее устойчивой является а — А Оз. Эта модификация встречается в земной коре в виде минерала корунда, из которого готовят шлифовальные диски и наждачные порошки. Применение корунда в качестве абразивного материала основано на его высокой твердости, уступающей лишь твердости алмаза, карборунда 81С и боразона ВЫ. Сплавлением А]20з с СгаОз получают искусственные рубины. Из них изготовляют опорные камни в точных механизмах. В последнее время искусственные рубины применяют в квантовых генераторах (лазерах). Изделия из А12О3 используют как огнеупоры и диэлектрики. [c.279]
Напишите химические реакции, которые могут происходить между следующими веществами, алюминий, оксид кремния, карбоиат натрия, гидроксид натрия, серная кислота. [c.77]
Алюминий получают электролизом оксида. Температура плавления оксида (2050 °С) очень высока, и поэтому электролизу подвергают расплавленную смесь его с криолитом (гексафторалюминат натрия NaaAlFe) и фторидами кальция и алюминия. Оксид алюминия растворяется в расплаве, который и подвергают электролизу при 850 °С в результате образуются алюминий и кислород (рис. 19.2). [c.407]
Сплав марганца с хромом. При восстановлении алюминием оксида марганца (И, П1) с оксидом хрома (И ) около 20% марганца остается в шлаке, который в осноп-ном состоит из алюмината марганца Мп(А102)2- Реакция начинается при 45-процентном содержании оксида марганца (И, 1П). Но лучше содержание этого оксида увеличить, например, до 50—60%. Тогда следует взять 25 г оксида марганца (Н, П1), 25 г оксида хрома (П1) и 16,71 г алюминия. [c.249]
Оксид алюминия Оксид и гидроксид. Оксид алюминия составляет амфотерен,., основу минерала боксита. Он амфотерен с кислотами реагирует, образуя соли с ионом [А1 (Н20)б] [обычно записывают как АГ + (водн.)], а с щелочами образует соли— тетрагидроксоалюминаты — с ионом А (ОН)Г (алюминат-ион). [c.411]
Реактивы и оборудование азобензол калил дихромат бензин алюминил оксид (просеянный через сито с размером отверстий О, Ыа СО., Ка2Й04 (безвод.), [c.12]
Для у-гиббсита- С° 91,97 Дж/(моль-К), ДЯ°6 — 1293,5 кДж/моль, 3°де 68,44 ДжДмоль К), Ок. 180°С разлагается до бемита, выще 250°С-до А12О3. Промежут. продукт в произ-ве А12О3 и А1 по способу Байера. М, б. получен также при медленном пропускании СО2 через р-ры алюмината Ыа (см. Алюминия оксид) Применяют для получения соед. А1, как антипирен лакокрасочных материалов и пластмасс, компонент зубных паст, обволакивающее и адсорбирующее ср-во в медицине. [c.118]
chem21.info
Оксид алюминия — Википедия РУ
Окси́д алюми́ния Al2O3 — бинарное соединение алюминия и кислорода. В природе распространён как основная составляющая часть глинозёма[3], нестехиометрической смеси оксидов алюминия, калия, натрия, магния и т. д.
Свойства
Бесцветные нерастворимые в воде кристаллы. Амфотерный оксид. Практически не растворим в кислотах. Растворяется в горячих растворах и расплавах щелочей. Является диэлектриком[4][5][6], но некоторые[7][8] исследователи считают его полупроводником n-типа. Диэлектрическая проницаемость 9,5—10. Электрическая прочность 10 кВ/мм.
Плотность
| Модификация | Плотность, г/см3 |
|---|---|
| α-Al2O3 | 3,99[2] |
| θ-Al2O3 | 3,61[3] |
| γ-Al2O3 | 3,68[4] |
| κ-Al2O3 | 3,77[5] |
Основные модификации оксида алюминия
В природе можно встретить только тригональную α-модификацию оксида алюминия в виде минерала корунда и его редких драгоценных разновидностей (рубин, сапфир и т. д.). Она является единственной термодинамически стабильной формой Al2O3. При термообработке гидроксидов алюминия около 400 °С получают кубическую γ-форму. При 1100—1200 °С с γ-модификацией происходит необратимое превращение в α-Al2O3, однако скорость этого процесса невелика, и для завершения фазового перехода необходимо либо наличие минерализаторов, либо повышение температуры обработки до 1400—1450 °С[9].
Известны также следующие кристаллические модификации оксида алюминия: кубическая η-фаза, моноклинная θ-фаза, гексагональная χ-фаза, орторомбическая κ-фаза. Спорным остаётся существование δ-фазы, которая может быть тетрагональной или орторомбической[9][10].
Вещество, иногда описываемое как β-Al2O3, на самом деле представляет собой не чистый оксид алюминия, а ряд алюминатов щелочных и щёлочноземельных металлов со следующими общими формулами: MeO·6Al2O3 и Me2O·11Al2O3, где МеО — это оксиды кальция, бария, стронция и т. д., а Ме2О — оксиды натрия, калия, лития и других щелочных металлов. При 1600—1700 °С β-модификация разлагается на α-Al2O3 и оксид соответствующего металла, который выделяется в виде пара.
Получение
Получают из бокситов, нефелинов, каолина, алунитов алюминатным или хлоридным методом. Сырьё в производстве алюминия, катализатор, адсорбент, огнеупорный и абразивный материал.
- 3Cu2O + 2Al →1000 ∘C 6Cu + Al2O3{\displaystyle {\mathsf {3Cu_{2}O\ +\ 2Al\ {\xrightarrow {1000\ ^{\circ }C}}\ 6Cu\ +\ Al_{2}O_{3}}}}
Плёнки оксида алюминия на поверхности алюминия получают электрохимическими или химическими методами. Так, например, получают диэлектрический слой в алюминиевых электролитических конденсаторах. В микроэлектронике также применяется эпитаксия оксида алюминия, которая многими учёными считается перспективной, например, в изоляции затворов полевых транзисторов.[5][6]
Применение
Оксид алюминия (Al2O3), как минерал, называется корунд. Крупные прозрачные кристаллы корунда используются как драгоценные камни. Из-за примесей корунд бывает окрашен в разные цвета: красный корунд (содержащий примеси хрома) называется рубином, синий, традиционно — сапфиром. Согласно принятым в ювелирном деле правилам, сапфиром называют кристаллический α-оксид алюминия любой окраски, кроме красной. В настоящее время кристаллы ювелирного корунда выращивают искусственно, но природные камни всё равно ценятся выше, хотя по виду не отличаются. Также корунд применяется как огнеупорный материал. Остальные кристаллические формы используются, как правило, в качестве катализаторов, адсорбентов, инертных наполнителей в физических исследованиях и химической промышленности.
Керамика на основе оксида алюминия обладает высокой твёрдостью, огнеупорностью и антифрикционными свойствами, а также является хорошим изолятором. Она используется в горелках газоразрядных ламп, подложек интегральных схем, в запорных элементах керамических трубопроводных кранов, в зубных протезах и т. д.
Так называемый β-оксид алюминия в действительности представляет собой смешанный оксид алюминия и натрия. Он и соединения с его структурой вызывают большой научный интерес в качестве металлопроводящего твёрдого электролита.
γ-Модификации оксида алюминия применяются в качестве носителя катализаторов, сырья для производства смешанных катализаторов, осушителя в различных процессах химических, нефтехимических производств (ГОСТ 8136-85).
Литература
- Pillet, S.; Souhassou, M.; Lecomte, C.; Schwarz, K. и др. Acta Crystallograica A (39, 1983-) (2001), 57, 209—303
- Husson, E.; Repelin, Y. Europen Journal of Solid State Inogranic Chemistry
- Gutierrez, M.; Taga, A.; Johansson, B. Physical Review, Serie 3. B — Condensed Matter (18, 1978-) (2001), 65, 0121011-0121014
- Smrcok, L.; Langer, V.; Halvarsson, M. Ruppi, S. Zeitschrift fuer Kristallographie (149, 1979-) (2001), 216, 409—412
См. также
Ссылки
Примечания
http-wikipediya.ru
