ОГЭ по химии | Задание 3
Задания Варианты Теория
Задание 1 Задание 2 Задание 3 Задание 4 Задание 5 Задание 6 Задание 7 Задание 8 Задание 9 Задание 10 Задание 11 Задание 12 Задание 13 Задание 14 Задание 15 Задание 16 Задание 17 Задание 18 Задание 19 Задание 20 Задание 21 Задание 22
Разбор сложных заданий в тг-канале:
Посмотреть
Задача 1
Какой вид химической связи в молекуле аммиака?
- ковалентная неполярная
- ковалентная полярная
- металлическая
- ионная
Задача 2
Ковалентная полярная связь образуется между атомами
- натрия и брома
- серы и кислорода
- водорода
- калия и хлора
Задача 3
Какое из указанных веществ имеет ионную связь?
- H2S
- NaCl
- H2
- Cl2O
Задача 4
Длина ковалентной связи наибольшая в молекуле
- H2Te
- H2O
- H2Se
- H2S
Задача 5
Какое из указанных веществ имеет ковалентную неполярную связь?
- сахар
- вода
- фуллерен
- поваренная соль
Задача 6
Химическая связь в хлориде кальция
- ковалентная полярная
- ионная
- ковалентная неполярная
- металлическая
Задача 7
Ионная связь характерна для каждого из двух веществ:
- карбида алюминия и угольной кислоты
- хлорида лития и гидрида кальция
- угарного газа и этилового спирта
- серы и нитрата железа(III…
Задача 8
Формулы веществ только с ковалентными полярными связями приведены в ряду
- HCl, N2
- Br2, HI
- СH4, NH3
- Na2O, PH3
Задача 9
Какое из указанных веществ имеет металлическую связь?
- Fe3C
- Si
- Be
- P
Задача 10
Для какого вещества характерна ковалентная полярная связь?
- MgO
- Br
- NO
- Al
Задача 11
Для какого вещества характерна ионная связь?
- H2S
- K2S
- SO2
- S8
Задача 12
Какой вид химической связи характерен для вещества, формула которого P4?
- ковалентная неполярная
- ковалентная полярная
- металлическая
- ионная
Задача 13
Одинаковый вид химической связи имеют хлороводород и
- бром
- вода
- хлорид калия
- водород
Задача 14
В гидроксиде бария связи
- только ионные
- только ковалентные полярные
- как ионные, так и ковалентные неполярные
- как ковалентные полярные, так и ионные
Задача 15
В гидроксиде кальция связи
- только ионные
- только ковалентные полярные
- как ионные, так и ковалентные неполярные
- как ковалентные полярные, так и ионные
Задача 16
В каком ряду записаны вещества только с ионной связью?
- сероуглерод, вода, нашатырь
- хлорид натрия, бромид кальция, оксид бария
- фосфат калия, сероводород, аммиак
- угарный газ, аргон,…
Задача 17
Соединениями с ковалентной полярной и ковалентной неполярной связью являются соответственно
- хлороводород и силан
- фосфат натрия и нитрид калия
- фосфин и водород
- аммиак и сероуглерод…
Задача 18
Одинаковый вид химической связи имеют алмаз и
- карбид кальция
- хлороводород
- фосфор
- вода
Задача 19
Соединениями с ковалентной полярной и ковалентной неполярной связью являются соответственно
- I2 и H2Te
- HBr и N2
- Fe и HF
- CO и SO2
Задача 20
Веществами с ковалентной полярной и ковалентной неполярной связью являются соответственно
- кислород и углерод
- вода и хлороводород
- сероводород и водород
- аммиак и хлорид натрия
1 2
Популярные материалы
Тест А4 А6Хим св
Химическая
связь.
Упражнения.
1. Определить тип химической связи в следующих веществах:
Вещество | Медь | Хлорид фосфора | Серная кислота | Озон | Алмаз |
Тип связи | |||||
Вещество | Метан | Оксид бария | Хлор | Сера S8 | Аммиак |
Тип связи |
2.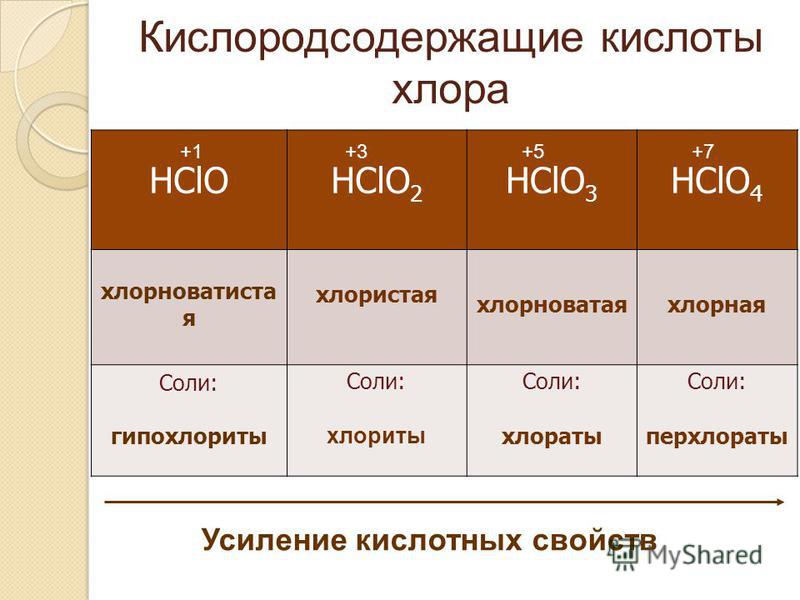 Подчеркните вещества, в которых МЕЖДУ молекулами существует водородная
связь:
Подчеркните вещества, в которых МЕЖДУ молекулами существует водородная
связь:
сернистый газ; лёд; озон; этанол; этилен; уксусная кислота; фтороводород.
3. Как влияют на длину, прочность и полярность связи
а) Чем больше радиусы атомов, образовавших связь, тем длина связи _______
б) Чем больше кратность ( одинарная, двойная или тройная) связи, тем её прочность ____________________
в) Чем больше разность электроотрицательностей между двумя атомами, тем полярность связи ____________
4. Сравните длину, прочность и полярность связей в молекулах:
а) длина связи: HCl ___HBr
б) прочность связи PH3_______NH3
в) полярность связи ССl4 ______CH4
г) прочность связи: N2 _______O2
д) длина связи между атомами углерода в этилене и в ацетилене: __________
е) полярность связей в NH3_________Н2О
Тесты. А4.Химическая
связь.
А4.Химическая
связь.
1. Валентность атома — это
1) число химических связей, образованных данным атомом в соединении
2) степень окисления атома
3) число отданных или принятых электронов
4) число электронов, недостающее для получения электронной конфигурации ближайшего инертного газа
2. Оцените правильность суждений о химической связи.
А. При образовании химической связи энергия всегда выделяется
Б. Энергия двойной связи меньше, чем энергия одинарной связи.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
3.В веществах, образованных путем соединения одинаковых атомов, химическая связь
1)ионная 2)ковалентная полярная 3)водородная 4) ковалентная неполярная
4. Соединениями с ковалентной полярной и ковалентной неполярной связью являются соответственно
1) вода и сероводород 2) бромид калия и азот
3) аммиак и водород 4) кислород и метан
5. За счет общей электронной пары химическая
связь образована в соединении
За счет общей электронной пары химическая
связь образована в соединении
1) KI 2) НВr 3) Li2O 4) NаВr
6.Выберите пару веществ, все связи в которых — ковалентные:
1) NаСl, НСl 2) СО2, ВаО 3) СН3Сl, СН3Nа 4) SO2, NO2
7.Вещество с ковалентной полярной связью имеет формулу
1)KCl 2)HBr 3)Р4 4)CaCl2
8. Соединение с ионным характером химической связи
1)хлорид фосфора 2)бромид калия 3)оксид азота (II) 4)барий
9. В аммиаке и хлориде бария химическая связь соответственно
1) ионная и ковалентная полярная 2)ковалентная неполярная и ионная 3)ковалентная полярная и ионная 4)ковалентная неполярная и металлическая
10. Веществом с ковалентной полярной связью являются
1)оксид серы (IV) 2)кислород 3)гидрид кальция 4)алмаз
11. В каком ряду перечислены вещества только
с ковалентной полярной связью:
В каком ряду перечислены вещества только
с ковалентной полярной связью:
1) СН4 Н2 Сl2 2)NH3 HBr CO2 3) PCl3 KCl CCl4 4) H2S SO2 LiF
12. В каком ряду перечислены вещества только с ионным типом связи:
1) F2O LiF SF4 2) PCl3 NaCl CO2 3) KF Li2O BaCl2 4) СаF2 CH4 CCl4
13. Соединение с ионной связью образуется
1) CH4 и O2 2)NH3 и HCl 3) C2H6 и HNO3 4) SO3 и H2O
14. В каком веществе все химические связи — ковалентные неполярные?
1) Алмаз 2) Оксид углерода (IV) 3) Золото 4) Метан
15. Связь, образующаяся между элементами с порядковыми номерами 15 и 53
1)ионная 2)металлическая
3)ковалентная неполярная 4)ковалентная полярная
16. Водородная
связь образуется между молекулами
Водородная
связь образуется между молекулами
1) этана 2) бензола 3) водорода 4) этанола
17. В каком веществе есть водородные связи?
1) Сероводород 2)Лед 3) Бромоводород 4) Бензол
18.В каком веществе есть одновременно ионные и ковалентные химические связи?
1) Хлорид натрия 2) Хлороводород 3) Сульфат натрия 4) Фосфорная кислота
19. Более выраженный ионный характер имеет химическая связь в молекуле
1)бромида лития 2)хлорида меди 3)карбида кальция 4)фторида калия
20. Тремя общими электронными парами образована ковалентная связь в молекуле 1) азота 2) сероводорода 3) метана 4) хлора
21.Сколько электронов участвует в образовании химических связей в молекуле воды? 1) 2 2) 3 3) 4 4) 18
22. Четыре
ковалентные связи содержит молекула:
1) СО2 2) С2H4 3) Р4 4) С3Н4
Четыре
ковалентные связи содержит молекула:
1) СО2 2) С2H4 3) Р4 4) С3Н4
23. Число связей в молекулах увеличивается в ряду
1) СНСl3, СH4 2) СН4, SО3 3) СО2, СН4 4) SО2, NН3
24. В каком соединении ковалентная связь между атомами образуется по донорно-акцепторному механизму? 1)КСl 2)ССl4 3) NН4Сl 4)СаСl2
25. Какая из перечисленных молекул требует наименьшей затраты энергии для разложения на атомы? 1) HI 2) Н2 3) O2 4) СО
26. Укажите молекулу, в которой энергия связи — наибольшая:
1) N≡N 2) Н-Н 3) О=О 4) Н-F
27. Укажите молекулу, в которой химическая связь — самая прочная:
1) НF 2) НСl 3) НВr 4) HI
28. Укажите ряд, характеризующийся увеличением
длины химической связи
Укажите ряд, характеризующийся увеличением
длины химической связи
1)O2, N2, F2, Cl2 2)N2, O2, F2, Cl2 3)F2, N2, O2, Cl2 4)N2, O2, Cl2, F2
29. Длина связи Э-O увеличивается в ряду
1) оксид кремния(IV), оксид углерода(IV)
2) оксид серы(IV), оксид теллура(IV)
3) оксид стронция, оксид бериллия
4) оксид серы(IV), оксид углерода(IV)
30. В ряду СН4 – SiH4 происходит увеличение
1) прочности связей 2) окислительных свойств
3) длины связей 4) полярности связей
31. В каком ряду молекулы расположены в порядке увеличения полярности связей?
1)НF,НСl,НВr 2)Н2Sе, Н2S, Н2О 3) NH3, РН3, АsН3 4) СO2, СS2, СSе2
32. Наиболее полярна ковалентная связь в
молекуле:
Наиболее полярна ковалентная связь в
молекуле:
1) СН4 2) СF4 3) CCl4 4) CBr4
33.Укажите ряд, в котором полярность возрастает:
1)AgF, F2, HF 2)Cl2, HCl, NaCl 3)CuO, CO, O2 4) KBr, NaCl, KF
А6. Зависимость свойств веществ от особенностей их кристаллической решетки
Упражнения.
1. Определить тип кристаллической решетки в веществах:
Вещество | СаО | О2 | СО2 | NaCl | SiO2 |
Тип решетки | |||||
Вещество | натрий | кремний | барий | фосфор | сера |
Тип решетки |
2. Заполнить таблицу:
Заполнить таблицу:
Вещество | Бром | Бор | Барий | Поваренная соль |
Тип решетки | ||||
Какие частицы в узлах решетки? | ||||
Какими связями связаны частицы в решетке? | ||||
Тв, ж, газ? |
Тесты.
1.
Установите соответствие между типом
кристаллической решетки и свойствами
веществ.
ТИП КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ | СВОЙСТВА ВЕЩЕСТВ |
A) ионная | 1) твердые, тугоплавкие, не растворяются в воде |
Б) металлическая | 2) хрупкие, легкоплавкие, не проводят электрический ток |
В) атомная | 3) пластичные, имеют различные температуры плавления, проводят электрический ток |
Г) молекулярная | 4) твердые, тугоплавкие, хорошо растворяются в воде |
2. Вещества, обладающие твёрдостью, тугоплавкостью, хорошей растворимостью в воде, как правило, имеют кристаллическую решетку:
1) молекулярную 2) атомную 3) ионную 4) металлическую
3. Вещества твердые, прочные, с высокой
температурой плавления, расплавы которых
проводят электрический ток, имеют
кристаллическую решетку
Вещества твердые, прочные, с высокой
температурой плавления, расплавы которых
проводят электрический ток, имеют
кристаллическую решетку
1) металлическую 2) молекулярную 3) атомную 4) ионную
4. Оцените правильность суждений о связи между строением и свойствами вещества.
А. Среди веществ молекулярного строения есть газообразные, жидкие и твёрдые при обычных условиях.
Б. Вещества с атомной кристаллической решеткой при обычных условиях твёрдые.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
5. Оцените правильность суждений о связи между строением и свойствами вещества:
А. Если между частицами в кристалле прочная химическая связь, то вещество тугоплавко.
Б. Все твёрдые вещества имеют немолекулярное строение
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
6. Какие из приведенных утверждений верны:
Какие из приведенных утверждений верны:
А. Вещества с молекулярной решеткой имеют низкие температуры плавления и низкую электропроводность.
Б. Вещества с атомной решеткой пластичны и обладают высокой электропроводностью.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
7. Вещества с атомной кристаллической решеткой
1) очень твёрдые и тугоплавкие 2)проводят электрический ток в расплавах. 3) хрупкие и легкоплавкие 4)проводят электрический ток в растворах
9. Для твердых веществ с металлической кристаллической решеткой характерна высокая…
1) растворимость в воде 2) электроотрицательность атомов
3) летучесть 4) электропроводность
10. Из разноимённо заряженных ионов состоят кристаллы
1) сахара 2) гидроксида натрия 3) алмаза 4) серебра
11.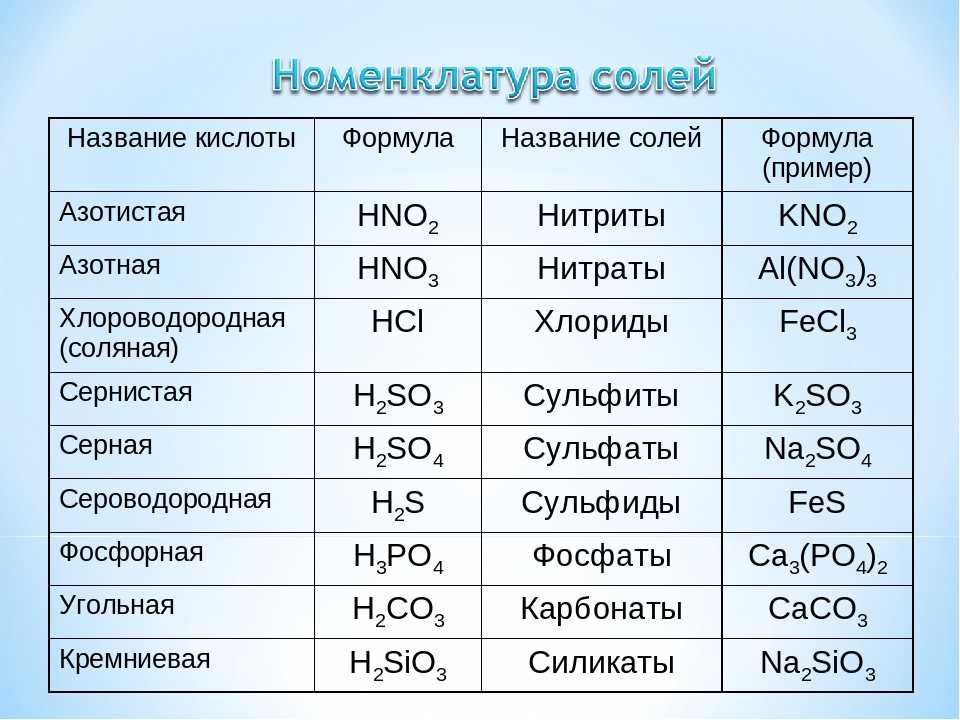 Какие частицы образуют кристалл нитрата
натрия?
Какие частицы образуют кристалл нитрата
натрия?
1) Атомы Nа, N и О 2) Ионы Nа+, NO3— 3)Ионы Nа+,N5+,О2- 4) Молекулы NаNО3
12. Утверждение о том, что структурной частицей данного вещества является молекула, справедливо только для
1)алмаза 2)поваренной соли 3) кремния 4) азота
13. Укажите вещество, которое в твердом состоянии имеет молекулярную кристаллическую решетку.
1) Графит 2) Натрий 3) Гидроксид натрия 4) Водород
14. Укажите вещество, которое в твердом состоянии имеет атомную кристаллическую решетку:
1) Хлороводород 2) Хлор 3) Оксид кремния (IV) 4) Оксид кальция
15. Кристаллическая решетка льда:
1) атомная 2) молекулярная 3) ионная 4) металлическая
16. Из молекул состоят кристаллы.1) сахара 2) соли 3) алмаза 4) серебра
17. Атомная кристаллическая решетка у
простого вещества:
Атомная кристаллическая решетка у
простого вещества:
1) алмаз 2) медь 3) фтор 4) олово
18. Ионную кристаллическую решетку имеет
1) вода 2) фторид натрия 3) серебро 4) бром
19. Кристаллическую структуру, подобную структуре алмаза, имеет:
1) кремнезем SiO2 2) оксид натрия Na2O
3) оксид углерода(II) CO 4) белый фосфор Р4
20. Немолекулярное строение имеет каждое из двух веществ:
1) S8 и O2 2) Fe и NaCl 3) CO и Mg 4) Na2CO3 и I2
21. Молекулярное строение имеет
1) ртуть 2) бром 3) гидроксид натрия 4) сульфат калия
22. Вещества атомного и молекулярного строения, соответственно
1) оксид кремния, оксид углерода (IV) 2) оксид кальция, оксид серы (IV)
3) кремний, алмаз 4) хлорид натрия, хлорид фосфора (V)
23. Молекулярную кристаллическую решетку
имеет
Молекулярную кристаллическую решетку
имеет
1) кремний 2) оксид углерода(IV) 3) диоксид кремния 4) нитрат аммония
24. Молекулярную кристаллическую решетку имеет 1)НВr 2) K2О 3)ВаО 4)КСl
25. Ионную кристаллическую решетку имеет каждое из веществ, расположенных в ряду
1) натрий, хлорид натрия, гидрид натрия
2) кальций, оксид кальция, карбонат кальция
3) бромид натрия, сульфат калия, хлорид железа (II)
4) фосфат магния, хлорид калия, оксид фосфора (V)
26. Немолекулярное строение имеют все неметаллы группы
1) углерод, бор, кремний 3) кислород, сера, азот
2) фтор, бром, йод 4) хлор, фосфор, селен
27. Молекулярную кристаллическую решетку имеет каждое из двух веществ
1) графит и алмаз 2) кремний и йод
3) хлор и оксид углерода(IV) 4) хлорид бария и оксид бария
28. Молекулярная кристаллическая решетка характерна для каждого из веществ, расположенных в ряду
1) хлорид калия, азот, метан 2) иод, диоксид углерода, озон
3) алюминий, бром, алмаз 4) водород, сульфат магния, оксид железа (III)
Видео с вопросами: Определение вещества, которое содержит как ионные, так и ковалентные связи
Стенограмма видео
Какое из следующих веществ
содержит как ковалентные, так и ионные связи? (А) ВаО, (Б) СО2, (В) ВаСО3, (Г)
h3CO3, или (Е)h3O.
Этот вопрос касается нас два типа связи: ковалентная связь и ионная связь.
Ионные связи часто образуются между атом металла и атом неметалла. В ионной связи один или несколько электроны передаются от одного элемента на связи к другому. NaCl или хлорид натрия для Например, содержит ионную связь. Ионные связи обычно не представлена визуально. Мы предполагаем его наличие между металлические и неметаллические элементы в одной структуре.
Ковалентная связь между
атом неметалла и другой атом неметалла. В ковалентной связи электроны
распределяется между атомами по обе стороны связи. Ковалентные связи, как и связи
между водородом и кислородом в воде обычно изображают линиями. В этом случае у нас есть одиночные строки
обозначающие одинарные связи. Но мы могли бы также иметь двойной или
тройные линии обозначают двойные или тройные связи.
Из элементов, которые появляются в вариантов ответа, неметаллами являются водород, углерод и кислород. Единственный присутствующий металл — барий, который можно найти в левой части периодической таблицы. Чтобы лучше понять, какой ответ варианты содержат, какие типы связи, давайте нарисуем их структуры связи.
Сначала три варианта ответа — CO2, h3CO3 и h3O — содержат только неметаллы. Поэтому они будут содержать только ковалентные связи. Поскольку они не содержат ионных облигации, они не могут быть правильным ответом на проблему. Вариант (А), оксид бария, содержит атом металла и атом неметалла с ионной связью между ними. Однако эта ионная связь является единственная связь в структуре, поэтому вариант (А) не может быть правильным ответом.
Давайте поближе познакомимся с
оставшийся вариант ответа, карбонат бария, чтобы подтвердить, что это правильный
отвечать.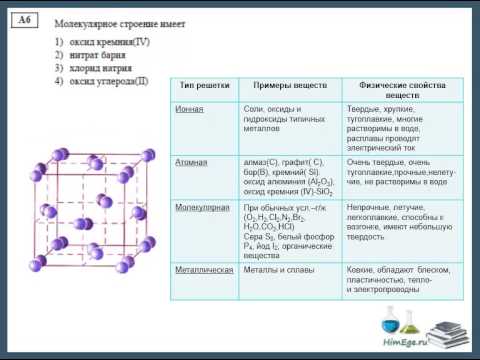 Есть много способов нарисовать это
структура, но один общий способ показывает два иона, ион бария и карбонат
ион. Многоатомный карбонат-ион
удерживаются вместе ковалентными связями между его атомом углерода и каждым из трех его атомов кислорода.
атомы. Когда мы рассматриваем то, что имеет место
вместе два иона, мы можем сделать вывод, что существует ионная связь, которая соединяет
ион бария в карбонат-ион, катион металла в многоатомный анион. Так как он содержит ионную связь и
несколько ковалентных связей, мы можем подтвердить, что карбонат бария является правильным
отвечать.
Есть много способов нарисовать это
структура, но один общий способ показывает два иона, ион бария и карбонат
ион. Многоатомный карбонат-ион
удерживаются вместе ковалентными связями между его атомом углерода и каждым из трех его атомов кислорода.
атомы. Когда мы рассматриваем то, что имеет место
вместе два иона, мы можем сделать вывод, что существует ионная связь, которая соединяет
ион бария в карбонат-ион, катион металла в многоатомный анион. Так как он содержит ионную связь и
несколько ковалентных связей, мы можем подтвердить, что карбонат бария является правильным
отвечать.
Итак, что из следующего вещества содержат как ковалентные, так и ионные связи? Это выбор (C), BaCO3.
Используйте точечные структуры Льюиса, чтобы показать ионную связь в следующих парах элементов. Покажите перенос электронов с помощью стрелок. Напишите правильную химическую формулу для образующегося ионного соединения.
 1) оксид бария (Ba и 0)
4) оксид натрия (Na и 0) 2) хлорид кальция (Ca и CI)
5) нитрид натрия (Na и N)
Формула 3) оксид алюминия (Al и 0)
фосфид магния (Mg и
Формула
Формула
Используйте точечные структуры Льюиса, чтобы показать ковалентную связь в следующих парах элементов. После того, как вы определили структуру молекулы, запишите ее структурную формулу в отведенном месте; используйте тире для обозначения общей пары электронов, а точки t0 показывают неподеленные электроны
1) трийодид азота (Nls) Показать работу здесь ПОДСКАЗКА; nrogen In Ine миддлол
2) четырехбромистый углерод (CBra)
углерод
средний
3) монооксид дигидрогена (HzO)
кислород В LFO млддлл’
1) оксид бария (Ba и 0)
4) оксид натрия (Na и 0) 2) хлорид кальция (Ca и CI)
5) нитрид натрия (Na и N)
Формула 3) оксид алюминия (Al и 0)
фосфид магния (Mg и
Формула
Формула
Используйте точечные структуры Льюиса, чтобы показать ковалентную связь в следующих парах элементов. После того, как вы определили структуру молекулы, запишите ее структурную формулу в отведенном месте; используйте тире для обозначения общей пары электронов, а точки t0 показывают неподеленные электроны
1) трийодид азота (Nls) Показать работу здесь ПОДСКАЗКА; nrogen In Ine миддлол
2) четырехбромистый углерод (CBra)
углерод
средний
3) монооксид дигидрогена (HzO)
кислород В LFO млддлл’Вопрос
Пошаговые ответы
‘PARL 2: Используйте точечные структуры Льюиса, чтобы показать ионную связь в следующих парах элементов_ Покажите перенос электронов с помощью стрелок_ Запишите правильный химический f…
‘PARL 2: Используйте структуры точек Льюиса, чтобы показать ионную связь в следующих парах элементов_ Покажите перенос электронов с помощью стрелок_ Напишите правильную химическую формулу ионного соединения, которое образуется
1) оксид бария (Ba и 0)
4) оксид натрия (Na и 0)
Формула:_
Формула:_
2) хлорид кальция (Ca и CI)
5) нитрид натрия (Na и N)
Формула
Формула:_
3) оксид алюминия (Al и 0)
фосфид магния (Mg и
Формула
Формула
PARL 3: Используйте точечные структуры Льюиса, чтобы показать ковалентную связь в следующих парах элементов. После того, как вы определили структуру молекулы, запишите ее структурную формулу в отведенном месте; используйте тире для обозначения общей пары электронов, а точки t0 показывают неподеленные электроны
1) трийодид азота (Nls)
Окончательный ответ:
Показать работу здесь ПОДСКАЗКА; nrogen In Ine миддлол
2) четырехбромистый углерод (CBra)
Показать работы здесь ПОДСКАЗКА: карбон
средний
3) монооксид дигидрогена (HzO)
Показать работы здесь_ПОДСКАЗКА: кислород в LFO mlddll’
После того, как вы определили структуру молекулы, запишите ее структурную формулу в отведенном месте; используйте тире для обозначения общей пары электронов, а точки t0 показывают неподеленные электроны
1) трийодид азота (Nls)
Окончательный ответ:
Показать работу здесь ПОДСКАЗКА; nrogen In Ine миддлол
2) четырехбромистый углерод (CBra)
Показать работы здесь ПОДСКАЗКА: карбон
средний
3) монооксид дигидрогена (HzO)
Показать работы здесь_ПОДСКАЗКА: кислород в LFO mlddll’
Рекомендуемый AI ответ:
1. Нарисуйте структуры точек Льюиса для элементов в парах.
Рекомендация видео с лучшим совпадением:
Решено проверенным экспертом
У нас нет заданного вами вопроса, но вот рекомендуемое видео, которое может помочь.
Вопрос о наилучшем совпадении:
Используйте точечные структуры Льюиса, чтобы показать ионную связь в следующих парах элементов.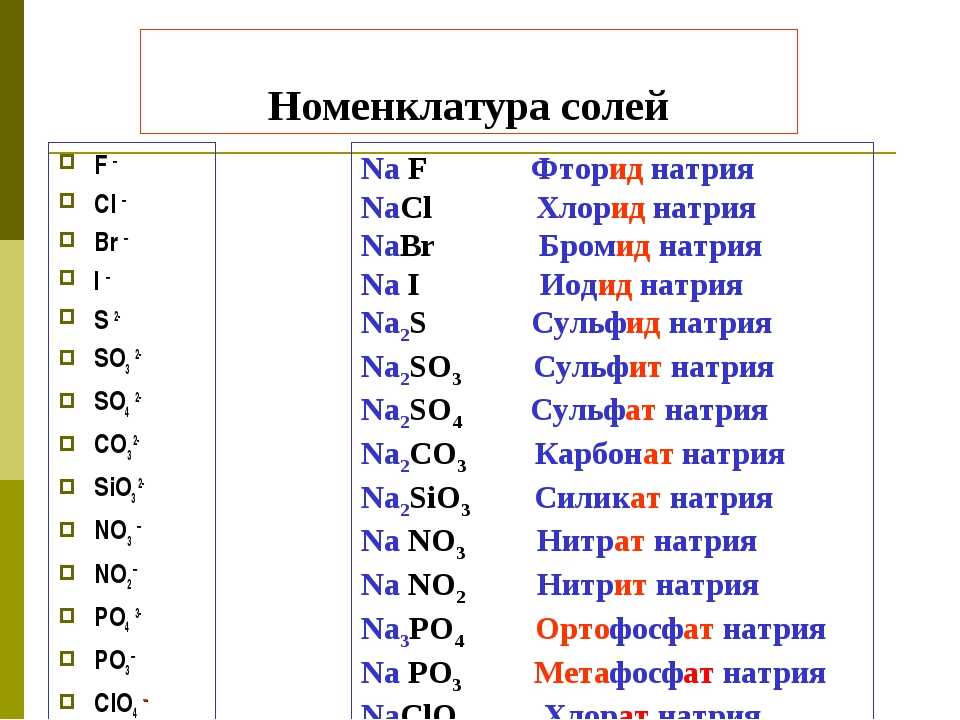 Покажите перенос электронов стрелками. Напишите правильную химическую формулу образующегося ионного соединения.
1) оксид бария (Ва и О)
2) оксид натрия (Na и O)
3) хлорид кальция (Ca и Cl)
4) нитрид натрия (Na и N)
5) оксид алюминия (Al и O)
6) фосфид магния (Mg и P)
Покажите перенос электронов стрелками. Напишите правильную химическую формулу образующегося ионного соединения.
1) оксид бария (Ва и О)
2) оксид натрия (Na и O)
3) хлорид кальция (Ca и Cl)
4) нитрид натрия (Na и N)
5) оксид алюминия (Al и O)
6) фосфид магния (Mg и P)
Рекомендуемые видеоролики
Стенограмма
С помощью структуры дамб мы должны показать средства ионной связи между упомянутой молекулой. Давайте посмотрим на это. Первая и вторая молекулы – это кальций и хлор. Название соединения – хлористый кальций. Дана формула CACL два. Название соединения — оксид видео um, и для некоторых партий это первая поддержка, вторая. Третье соединение в третьем наборе — это натрий вместе с кислородом. Часть пищи состояла из магния, а название соединения — магний-фосфор. Структура должна быть нарисована вместе с предупреждением. Вы должны сбалансировать электрон, а у хлора семь электронов. Будет дан еще один хлор. Есть ли предупреждения в этом году? Кальций плюс два заряда и одежда за вычетом газа судейской мамы будут образованы этим ночным электроном карты, идущим к этому хлору.
