NASA насыпало в полярное сияние барий и стронций
NASA
В ночь на субботу жители северной Норвегии стали свидетелями необычного эксперимента — на фоне полярного сияния возникли цепочки из ярких зеленовато-голубых пятен, которые затем исчезли. Такой эффект получился после запуска геофизических ракет в рамках проекта NASA AZURE. С помощью этих ракет на большой высоте распыляются частицы триметилалюминия, бария и стронция, что позволяет ученым исследовать поведение заряженных частиц в ионосфере, где возникают полярные сияния, сообщает SpaceWeather.
Эксперимент AZURE (Auroral Zone Upwelling Rocket Experiment), который финансируется NASA, предполагает серию из восьми пусков геофизических ракет на высоту до 250 километров для изучения поведения заряженных частиц в ионосфере, в особенности, двух ее слоев, E и F. Оба этих слоя содержат свободные электроны, «содранные» с атомов ионизирующим излучением Солнца (этот процесс называется фотоионизацией). С наступлением ночи, когда излучение Солнце уже не обеспечивает ионизацию, электроны и ионы начинают «воссоединяться». Суточный цикл ионизации и рекомбинации делает поведение слоев E и F достаточно сложным и малопредсказуемым.
Подготовка геофизических ракет к пуску
NASA’s Wallops Flight Facility Ракетное зондирование в рамках AZURE призвано в первую очередь измерить параметры вертикальных потоков воздуха в ионосфере, которые непрерывно перемешивают «суп» из заряженных частиц. Измерения с земли не позволяют увидеть эти процессы на всех высотах, кроме того, некоторые данные противоречат теоретически предсказанным. Решить эту проблему и должна проверка с помощью рассеивания облака аэрозолей прямо на месте и наблюдения за поведением частиц с земли.
Измерения с земли не позволяют увидеть эти процессы на всех высотах, кроме того, некоторые данные противоречат теоретически предсказанным. Решить эту проблему и должна проверка с помощью рассеивания облака аэрозолей прямо на месте и наблюдения за поведением частиц с земли.Вечером 5 апреля с территории космического центра Андоя в Норвегии были запущены две ракеты, которые на высотах от 100 до 250 километров выпустили вещества-маркеры: триметилалюминий и смесь бария и стронция. Триметилалюминий реагирует с кислородом и порождает химическую люминесценцию, что позволяет следить за потоками воздуха. Продуктом реакции являются оксид алюминия, углекислый газ и водяной пар. Барий быстро ионизируется и порождает пурпурно-красные облака, наблюдения за которым позволяют следить за потоками ионов в атмосфере. Неионизованный барий тоже светится голубовато-белым цветом и может послужить маркером для нейтральных частиц.
За поведением светящихся облаков, которые были видны на небе в течение получаса, наблюдали астрономы из обсерватории Аломар на севере Норвегии, их основным инструментом были серийные «зеркалки».
Сергей Кузнецов
основных, амфотерных, кислотных – HIMI4KA
У нас вышел новый курс, где всё объясняется ещё проще. Подробннее по ссылке
Определения и формулы основных, амфотерных и кислотных оксидов были приведены ранее в уроке 6.
Характерные химические свойства основных оксидов: реакции с кислотными оксидами с образованием солей и с кислотами с образованием солей и воды, например:
Некоторые основные оксиды реагируют с водой с образованием оснований. Эта реакция проходит в том случае, если продукт реакции растворим в воде:
Эта реакция проходит в том случае, если продукт реакции растворим в воде:
В аналогичных условиях, например, оксид железа (II) с водой реагировать не будет, так как гидроксид железа (II) в воде нерастворим.
Амфотерные оксиды взаимодействуют как с кислотами, так и с основаниями с образованием солей и воды или комплексных соединений:
Кроме того, амфотерные оксиды могут взаимодействовать как с кислотными, так и с основными оксидами, например:
С водой амфотерные оксиды не взаимодействуют.
Кислотные оксиды реагируют с основными оксидами с образованием солей; с основаниями, с образованием солей и воды или кислых солей, а также с водой, в том случае если образующаяся в ходе такой реакции кислота растворима в воде:
Кроме того, кислотные оксиды вступают в окислительно-восстановительные и обменные реакции:
Тренировочные задания
1. Оксид натрия взаимодействует с каждым из двух веществ:
1) серная кислота и вода
2) уксусная кислота и азот
3) оксид лития и фосфор
4) оксид бария и серная кислота
2. Оксид калия взаимодействует с
Оксид калия взаимодействует с
1) азотом и фосфором
2) водой и сульфатом натрия
3) серной кислотой и оксидом фосфора (V)
4) литием и хлоридом натрия
3. Оксид кальция взаимодействует с
1) оксидом кремния
2) оксидом углерода (II)
3) оксидом азота (II)
4) оксидом азота (I)
4. Оксид бария взаимодействует с каждым из двух веществ:
1) азотной кислотой и водой
2) уксусной кислотой и хлором
3) оксидом натрия и азотом
4) оксидом серы (IV) и кремнием
5. Оксид магния не взаимодействует с
1) соляной кислотой
2) серной кислотой
3) оксидом лития
4) оксидом кремния
6. Оксид кальция взаимодействует с каждым из двух веществ:
1) оксидом фосфора (V), водой
2) оксидом углерода (IV) и сульфидом натрия
3) оксидом магния и азот
4) кислородом и сульфатом натрия
7. Оксид кальция реагирует с
1) медью
2) фосфором
3) оксидом углерода (IV)
4) оксидом магния
8. Оксид натрия реагирует с
Оксид натрия реагирует с
1) водой
2) сульфатом калия
3) нитратом железа (II)
4) оксидом азота (II)
9. Оксид бария реагирует с каждым из двух веществ:
1) оксидом азота (II) и хлором
2) азотной кислотой и водой
3) оксидом углерода (II) и железом
4) серой и хлоридом кальция
10. Оксид магния реагирует с каждым из двух веществ:
1) оксидом кальция и оксидом железа (II)
2) оксидом алюминия и оксидом хрома (II)
3) соляной кислотой и оксидом кремния (VI)
4) оксидом фосфора (V) и цинком
11. Оксид цинка
1) растворяется в кислотах, но не реагирует с основаниями
2) растворяется в щелочах, но не реагирует с кислотами
3) реагирует с оксидом натрия, но не реагирует с водой
4) реагирует с оксидом калия и водой
12. Оксид хрома (III) реагирует с
1) оксидом калия
2) водой
3) оксидом серы (VI)
4) оксидом азота (I)
13. Оксид алюминия амфотерен, поскольку он способен взаимодействовать
Оксид алюминия амфотерен, поскольку он способен взаимодействовать
1) как с азотной, так и серной кислотой
2) с водой и кислотами
3) с водой и щелочами
4) как с кислотами, так и со щелочами
14. Оксид алюминия реагирует с
1) сульфатом калия
2) оксидом калия
3) оксидом азота (II)
4) оксидом углерода (IV)
15. Оксид серы (VI) взаимодействует с каждым из двух веществ:
1) оксидом лития и углекислым газом
2) водой и углекислым газом
3) водой и гидроксидом калия
4) кислородом и натрием
16. Оксид фосфора (V) взаимодействует с каждым из двух веществ:
1) кислородом и водородом
2) водой и углекислым газом
3) водой и гидроксидом натрия
4) водой и оксидом углерода (II)
17. Оксид серы (VI) не взаимодействует с
1) водой
2) хлоридом калия
3) гидроксидом натрия
4) оксидом бария
18. Оксид серы (IV) взаимодействует с
1) оксидом углерода (IV) и водой
2) оксидом фосфора (V) и водой
3) сульфатом калия и водой
4) оксидом кальция и гидроксидом натрия
19. Оксид серы (IV) не взаимодействует с
Оксид серы (IV) не взаимодействует с
1) водой
2) фосфатом кальция
3) раствором гидроксида натрия
4) гидроксидом кальция
20. Оксид хлора (VII) взаимодействует с каждым из двух веществ:
1) кальцием и углекислым газом
2) водой и углеродом
3) водой и оксидом калия
4) кислородом и азотом
21. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) Na2O + HCl →
Б) Na2O + CO2 →
В) Na2O + O2 →
ПРОДУКТЫ РЕАКЦИИ
1) Na2CO3
2) NaCl + H2
3) NaCl + H2O
4) NaO3
5) Na2O2
22. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) Na2O + H2SO4 (изб.) →
Б) Na2O + Al2O3 →
В) Na2O + P2O5 →
ПРОДУКТЫ РЕАКЦИИ
1) NaHSO4
2) NaHSO4 + H2O
3) NaAlO2
4) Na3PO4
5) Na2SO4 + H2O
23. Установите соответствие между реагирующими веществами и продуктами реакций.
Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) CaO + H3PO4 (изб.) →
Б) CaO + H2O →
В) CaO + CO2 →
ПРОДУКТЫ РЕАКЦИИ
1) Ca(H2PO4)2 + H2O
2) CaCO3
3) Ca(OH)2
4) CaCO2
5) Ca3(PO4)2
24. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) CaO + SiO2 →
Б) CaO + H3PO4 (разб.) →
В) CaO + HCl →
ПРОДУКТЫ РЕАКЦИИ
1) Ca(H2PO4)2 + H2O
2) Ca3(PO4)2 + H2O
3) CaCl2 + H2O
4) CaSiO3 5) Ca(OCl)2
25. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) ZnO + HCl →
Б) ZnO + NaOH ⎯⎯H2O→
В) ZnO + Na2O ⎯⎯сплавление→
ПРОДУКТЫ РЕАКЦИИ
1) ZnCl2 + H2O
2) ZnCl2
3) Na2[Zn(OH)4]
4) Na2ZnO2 + H2O
5) Na2ZnO2
26. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) ZnO + H3PO4 →
Б) ZnO + NaOH + H2O →
В) ZnO + C →
ПРОДУКТЫ РЕАКЦИИ
1) Na2[Zn(OH)4] + H2
2) Na2ZnO2
3) Zn(H2PO4)2 + H2O
4) Zn + CO
5) Zn3(PO4)2 + H2O
27. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) P2O5 + H2O →
Б) P2O5 + Ca(OH)2 ⎯⎯сплавление→
В) P2O5 + NaOH (изб. ) →
) →
ПРОДУКТЫ РЕАКЦИИ
1) Ca3(PO4)2 + H2O
2) CaHPO4
3) Na3PO4 + H2O
4) Na3PO4
5) H3PO4
28. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) P2O5 + H2O →
Б) P2O5 + Na2O →
В) P2O5 + HNO3 →
ПРОДУКТЫ РЕАКЦИИ
1) H3PO4 + HNO2
2) H3PO4
3) Na3PO4
4) H3PO3
5) HPO3 + N2O5
29. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) SO2 + Ca(OH)2 (изб.) →
Б) SO2 + Na2O →
В) SO2 + O2 →
ПРОДУКТЫ РЕАКЦИИ
1) CaSO3 + H2O
2) SO3
3) Ca(HSO3)2
4) Na2SO4
5) Na2SO3
30. Установите соответствие между реагирующими веществами и продуктами реакций.
Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) SO2 + H2S →
Б) SO2 (изб.) + NaOH →
В) SO2 + NaOH (изб.) →
ПРОДУКТЫ РЕАКЦИИ
1) Na2SO4 + H2O
2) Na2SO3 + H2O
3) NaHSO3
4) S + H2O
5) NaHSO4
31. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
32. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
33. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
Для третьего превращения составьте сокращённое ионное уравнение реакции.
34. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для первого превращения составьте сокращённое ионное уравнение реакции.
35. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
36. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
37. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
38. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
39. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
40. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
41. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
42. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для первого превращения составьте сокращённое ионное уравнение реакции.
Для первого превращения составьте сокращённое ионное уравнение реакции.
43. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
44. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
45. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
46. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
47. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для первого превращения составьте сокращённое ионное уравнение реакции.
48. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
49. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
50. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
Ответы
Хотите ещё проще? Мы создали новый курс, где максимум за 7 дней вы овладете химией с нуля. Подробннее по ссылке
Подробннее по ссылке
Как получают и как используют оксид алюминия
Как правило, в качестве сырья для получения оксида алюминия служат бокситы, алуниты, а также нефелины. При содержании в них оксида алюминия более 6−7% производство ведется основным способом — методом Байера, а при меньшем содержании вещества используют метод спекания руды с известью или содой.Метод Байера — это гидрохимический способ получения глинозема из бокситов. Он представляет собой обработку измельченной породы в шаровых мельницах, затем бокситы обрабатывают щелочными растворами при температуре 225−250°С. Полученный таким образом состав алюмината натрия разбавляют водным раствором и фильтруют.
В процессе фильтрации шлам, содержащий оксид алюминия, свойства которого соответствуют стандартным, подвергают разложению на центрифугах. Выделяется около ½ образовавшегося при этом Аl (ОН)3. Его отфильтровывают и прокаливают во вращающихся печах или в кипящем слое при температуре ~ 1200 °C. В результате получается глинозем, содержащий 15−60% α-Аl2О3. Применение данного метода позволяет сохранить маточный раствор для использования в последующих операциях по выщелачиванию бокситов.
Применение данного метода позволяет сохранить маточный раствор для использования в последующих операциях по выщелачиванию бокситов.
Метод спекания руды с известью или содой работает следующим образом: высококремнистую измельченную руду (нефелин и др.) смешивают с содой и известняком и спекают во вращающихся печах при 1250−1300 °С. Полученную массу выщелачивают водным щелочным раствором. Раствор алюмината Na отделяют от шлама, затем освобождают от SiO2, осаждая его в автоклаве при давлении около 0,6 Мпа, а затем известью при атмосферном давлении и разлагают алюминат газообразным СО2. Полученный Аl (ОН)3 отделяют от раствора и прокаливают при температуре около 1200 °C. При переработке нефелина, помимо глинозема, получают Na2CO3, K2CO3 и цемент.
При производстве глинозема из алунитов одновременно получают H2SO4 и K2SO4. Алунитовую руду обжигают при 500−580°С в восстановительной атмосфере и обрабатывают раствором NaOH по способу Байера.
Для производства высокопрочной корундовой керамики применяют порошок оксида алюминия, полученный термическим разложением некоторых солей алюминия, например, азотнокислого, алюмоаммиачных квасцов различной степени чистоты. Оксид алюминия, полученный при разложении солей, является высокодисперсным порошком γ-Al2O3 (при прокаливании до 1200°С) и обладает большой химической активностью.
Для получения ультра- и нанодисперсных порошков Аl2O3, которые используются в технологии конструкционной и инструментальной керамики, широкое распространение получил способ совместного осаждения гидроксидов (СОГ) и плазмохимического синтеза (ПХС).
Сущность метода СОГ заключается в растворении солей алюминия, например, AlCl3 в растворе аммиака и последующем выпадении образующихся гидратов в осадок. Процесс ведут при низких температурах и больших сроках выдержки. Полученные гидроксиды сушат и прокаливают, в результате образуется порошок Аl2O3 с размером частиц 10−100 нм.
В технологии ПХС водный раствор Al (NO3)3 подается в сопло плазмотрона. В каплях раствора возникают чрезвычайно высокие температурные градиенты, происходит очень быстрый процесс синтеза и кристаллизации Аl2O3. Частицы порошка имеют сферическую форму и размер 0,1−1 мкм.
Барий оксид — Справочник химика 21
Бария гидроксид Бария оксид. [c.3]Какие из перечисленных ниже оксидов пригодны в качестве осушителей оксид меди (П), оксид бария, оксид фосфора (V), смешанный оксид железа (П) и оксида железа (П1) (магнитный железняк) Напишите уравнения соответствующих реакций. [c.186]
БАРИЯ Оксид бария [c.140]
БАРИЯ ПЕРОКСИД, см. Бария оксид. [c.243]
С какими из указанных ниже веществ может взаимодействовать раствор гидроксида калня иодоводородная кислота, хлорид меди (И), хлорид бария, оксид углерода [c. 60]
60]
Древесная мука, тальк, молотый кварц, графит, барит, оксид алюминия и др.
Напишите в молекулярном и ионном виде уравнения реакций между сульфатом цинка и гидроксидом натрия серной кислотой и хлоридом бария оксидом меди и серной кислотой карбонатом бария и соляной кислотой. [c.81]
Карбонат кальция Карбонат магния Оксид магния Гидроксид бария Оксид кальция То же [c.60]
Укажите, с какими из перечисленных веществ реагирует гидроксид калия оксид бария, оксид фосфора (V), нитрат натрия. Напишите уравнения возможных реакций. [c.156]
Для повышения коэффициента трения ФПМ используют различные по свойствам и морфологии наполнители асбест, кварц, стекло, тетрагональный графит, аэросил, сульфат бария, оксиды металлов и др. Повышение теплофизических характеристик достигается применением порошка, стружки или проволоки металлов и сплавов. [c.173]
[c.173]
Барий оксид /в пересчете на барий/ 1304-28-5 ВаО 0,004 [c.895]
Диметилформамид рекомендуется предварительно высушивать с помощью безводного сульфата магния, оксида бария, оксида алюминия или безводного сульфата меди с последующей перегонкой либо под вакуумом, либо при невысоком давлении. В некоторых случаях перегонку рекомендуется проводить в токе азота. [c.143]
Для получения фрикционного материала на основе фторуглеродных каучуков, например, сополимеров ВФ и ГФП [пат. США 4051100, 1977] или смесей фторсодержащего и акрилатного каучуков с соотношением от 1 И до 11 1 (можно 1 1) [пат. США 4045402, 1977] рекомендуется вводить стеклянные или керамические несферические частицы с эффективным диаметром 0,0025— 0,125 мм. Такой фрикционный материал содержит 20—50% (масс.) каучука, 12—40% (масс.) газового технического углерода и 20—60% (масс.) стеклянных или керамических частиц, которые равномерно диспергированы во фрикционном материале и удерживаются в нем только механическими силами.
Чаще всего в качестве носителей используются силикагель, крахмал, оксид алюминия, сульфат бария, оксид кальция, ионообменные смолы в 0Н -, СОз — и Р -форме. Лучшим носителем считается оксид алюминия, но в каждом конкретном случае целесообразность использования того или иного носителя для разделения и количественного определения ионов устанавливается экспериментально. [c.102]
Основными стадиями процесса получения являются нейтрализация алкилфенола, сушка нейтрализованного продукта, фосфоросернение алкилфенолята и фильтрование присадки. В производстве используют алкилфенол, гидроксид бария, оксид цинка, сульфид фосфора(V), масло И-20 (разбавитель) и бензин (растворитель).
 [c.232]
[c.232]С какими из указанных ниже веществ может взаимодействовать раствор гидроксида калия иодоводородиая кислота, хлорид меди (II), хлорид бария, оксид углерода (IV), оксид свинца (II) Напишите уравнения решщий в молекулярной, ионной и сокращенной ионной формате. [c.73]
БАРИЯ ОКСИД ВаО, in., ок. 2020 С в воде образует Ва(ОН)2 на иоздухе реаг, с СО2 и переходит в ВаСОз, нри нагрев, до 500 °С образует BaOj. Получ. разложение [c.66]
Б. интенсивно окисляется на воздухе, образуя пленку, содержащую бария оксид ВаО и нитрид ВазЫ (т. пл. 10б0°С). При незначит. нагревании на воздухе воспламеняется. Энергично реагирует с водой, давая бария гидроксид Ba(OH)j. С разб. к-тами образует соли. Большинство солей Б. с анионами слабых к-т и к-т средней силы малораство-
БАРИЯ ОКСИД ВаО, бесцв. кристаллы с кубич. решеткой (а = 0,5542 нм, пространств, группа Fmim плоти. 5,7 г/см ) при 23 °С и 9200 МПа превртщ. в тетрагон, модификацию (а = 0,4459 им, с = 0,3606 нмХ при 14000 МПа-в тетрагональную др. типа (а = 0,4397 нм, с = 0,3196 нм, пространств, группа Р4/птп). Т. пл 2017°С при нагр. возгоняется С° 4 99 ДжДмоль-КХ ур-ние температурной зависимости С° = 48,117 -I- 11,527-10- Г — 3,896 -10 Г -н 2,083 -10 Г» (298 — 2290 К) АН озг 24,3 к Дж/моль, — 548,0 [c.243]
в тетрагон, модификацию (а = 0,4459 им, с = 0,3606 нмХ при 14000 МПа-в тетрагональную др. типа (а = 0,4397 нм, с = 0,3196 нм, пространств, группа Р4/птп). Т. пл 2017°С при нагр. возгоняется С° 4 99 ДжДмоль-КХ ур-ние температурной зависимости С° = 48,117 -I- 11,527-10- Г — 3,896 -10 Г -н 2,083 -10 Г» (298 — 2290 К) АН озг 24,3 к Дж/моль, — 548,0 [c.243]
Процессы гидрирования и жидкой фа.зе широко используют в органическом синтезе для присоединения водорода по кратным связям, полного или частичною восстановления кислородсодержащих функциональных групп и деструктивного гидрирования с разрывом связей в исходном соединении, В качестве катализаторов используют N1, Со, Си, Р1 и Рс1, скелетные, сплавные или нанесенные. В качестве носителей применяют активный уголь, сульфат бария, оксиды ЛЬОз, СггОд и др. Используют также гомогенные металлокомилексные кат ал и.» а-торы. [c.208]
Турбидиметрический метод чаще всего применяется для определения концентраций аэрозолей вредных соединений в воздухе рабочих помещений, например тумана серной кислоты в атмосфере сернокислотных цехов в диапазоне 0 1 мг/л. Метод позволяет определять и такие примеси в воздухе, как оксид (10″ мол. %) и диоксвд (и-10 мол. %) углерода, циановодород. При определении содержания диоксида углерода регистрация рассеянного излучения осуществляется в насыщенном водном растворе гидроксида бария, оксида углерода — в аммиачном растворе нитрата серебра, циановодорода — в аммиачной суспензии иодида серебра.
Метод позволяет определять и такие примеси в воздухе, как оксид (10″ мол. %) и диоксвд (и-10 мол. %) углерода, циановодород. При определении содержания диоксида углерода регистрация рассеянного излучения осуществляется в насыщенном водном растворе гидроксида бария, оксида углерода — в аммиачном растворе нитрата серебра, циановодорода — в аммиачной суспензии иодида серебра.
БАРИЯ ОКСИД ВаО, (ил ок. 2020 «С в иоде образует Ва(ОН)г иа воздухе реаг. с Oj н переходит в ВаСОз, прв нагрев, до 500 С образует ВаО . Получ, разложение [c.66]
Бария оксид. Серовато-белая пористая масса. Легко растирается в порошок. На воздухе поглощает пары воды, а также СО2, образуя ВаСОз. Применяют как осушитель для газов по осушающей способности превосходит СаО я a l2 [c.95]
Основные стадии получения присадки ВНИИ НП-360 омыление алкилфенола . сушка омыленного продукта фосфоросернение алкилфенолята фильтрование присадки. В производстве используют алкилфенол, гидроксид бария, оксид цинка, пятисернистый фосфор, масло И-20А (разбавитель) и бензин. (растворитель). [c.71]
(растворитель). [c.71]
Резольные (термореактивные] смолы образуются при поликонденсации молярного избытка формальдегида по отношению к фенолу в присутствии катализатора основного характера (едкий натр, гидроксид бария, оксид магния, аммиак). Образующиеся олигомеры представляют собой смесь линейных и разветвленных молекул, содержащих реакционноспособные метилольные группы или метиленэфирные мостики. Среднее число Фенольных ядер в молекуле олигомера составляет от 2 до 8. Некоторые смолы представляют собой мономерные гидроокси-метилфенолы (фенолоспирты). [c.3]
Запасы материалов (ие более недельной нормы) могут храниться только-в специально предназначенном помещении с выходом на участок обработки сырья и составления шихты. Содержание пыли, газов, паров вредных веществ в юздухе помещений должно соответствовать установленным санитарным нормам. Приток воздуха в помещении должен составлять 80—90% объема всей механизированной вытяжки. Вытяжная вентиляция оборудуется устройствами для очистки удаляе. мого воздуха. Наряду с производственными помещениями должны сооружаться санитарно-бытовые помещения (душевые, гардеробные, умывальные). Помещения для приготовления шихты с использованием токсичных сырьевых материалов (марганец, хром, кобальт, свинец и его соединения, соли бария, оксид мышьяка и др,) должны соответствовать требованиям санитарных правил и норм. Следует применягь увлажнение обрабатываемых материалов на всех операциях, где это не противоречит требованиям технологии, [c.247]
Химический энциклопедический словарь (1983) — [ c.66 ]
Большой энциклопедический словарь Химия изд.2 (1998) — [ c.66 ]
Справочник Химия изд.2 (2000) — [ c.300 ]
Химия справочное руководство (1975) — [ c.43 ]
Лабораторная техника химического анализа (1981) — [
c. 95
]
95
]
Вредные химические вещества Неорганические соединения элементов 1-4 групп (1988) — [ c.132 , c.134 , c.137 , c.143 , c.470 ]
Общая и неорганическая химия (1981) — [ c.314 , c.325 ]
Машинный расчет физико химических параметров неорганических веществ (1983) — [ c.232 ]
Общая и неорганическая химия (1994) — [ c.332 , c.341 ]
оксид бария — это… Что такое оксид бария?
Оксид бария — Оксид бария одно из бинарных неорганических веществ, имеющее химическую формулу BaO. Является основным оксидом. Оксид бария Общие Систематическое наименование Оксид бария Традиционные названия Окись бария Химическая формула BaO … Википедия
Является основным оксидом. Оксид бария Общие Систематическое наименование Оксид бария Традиционные названия Окись бария Химическая формула BaO … Википедия
оксид бария — (напр. используется в качестве добавки для улучшения свойств тяжёлого бетона защитной оболочки ядерного реактора с целью защиты от излучения) [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN baryta … Справочник технического переводчика
Оксид иттрия-бария-меди — (англ. Yttrium barium copper oxide), также известный как YBCO это широко применяемый высокотемпературный сверхпроводник, известный тем, что он является первым полученным сверхпроводником с критической температурой больше 77 К. Его… … Википедия
Оксид-сульфат титана — Общие Систематическое наименование Оксид сульфат титана Традиционные названия Основной сернокислый титан; оксосульфат титана; сульфат титанила Химическая формула TiOSO4 Физические свойства … Википедия
Оксид-тетрафторид ксенона — Оксид тетрафторид ксенона … Википедия
Оксид меди(I) — Оксид меди(I) … Википедия
Оксид марганца(VII) — Mn2O7 зеленовато бурая маслянистая жидкость (tпл=5,9 °C), неустойчив при комнатной температуре; сильный окислитель, при соприкосновении с горючими веществами воспламеняет их, возможно со взрывом. Получить оксид марганца(VII) Mn2O7 можно… … Википедия
Получить оксид марганца(VII) Mn2O7 можно… … Википедия
Оксид марганца(II) — Общие … Википедия
Оксид марганца(IV) — Общие … Википедия
Оксид золота(III) — Общие … Википедия
Оксид титана(IV) — Общ … Википедия
| Имена | |
|---|---|
| Другие имена Окись бария | |
| Идентификаторы | |
| ChemSpider | |
| ECHA InfoCard | 100.013.753 |
| Номер ЕС | |
| Номер RTECS | |
| UNII | |
| Номер ООН | 1884 |
| |
| Характеристики | |
| БаО | |
| Молярная масса | 153,326 г / моль |
| Внешность | белое твердое вещество |
| Плотность | 5,72 г / см3, твердый |
| Температура плавления | 1923 ° С (3493 ° F, 2196 К) |
| Точка кипения | ~ 2000 ° С (3630 ° F, 2270 К) |
| 3,48 г / 100 мл (20 ° С) 90,8 г / 100 мл (100 ° С) Реагирует на форму Ва (ОН)2 | |
| Растворимость | растворим в этиловый спирт, разбавленные минеральные кислоты и щелочи; не растворим в ацетон и жидкость аммиак |
| -29.1·10−6 см3/ моль | |
| Структура | |
| кубический, cF8 | |
| FM3м, №225 | |
| Восьмигранный | |
| Термохимия | |
| 70 Дж · моль−1· K−1[1] | |
| −582 кДж · моль−1[1] | |
| Опасности | |
| Паспорт безопасности | Видеть: страница данных |
| Пиктограммы GHS | |
| Сигнальное слово GHS | Опасность |
| h401, h402, «>h414, h415, h418, h432, h512 | |
| P210, P220, P221, P260, P261, P264, P270, «>P271, P273, P280, P283, P301 + 310, P301 + 312, P301 + 330 + 331, P302 + 352, P303 + 361 + 353, P304 + 312, «>P304 + 340, P305 + 351 + 338, P306 + 360, P310, P312, P321, P330, P332 + 313 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Негорючий |
| Родственные соединения | |
| Гидроксид бария Перекись бария | |
| Оксид кальция Оксид стронция | |
| Страница дополнительных данных | |
| Показатель преломления (п), Диэлектрическая постоянная (εр), так далее.  | |
Термодинамический | Фазовое поведение твердое тело – жидкость – газ |
| УФ, ИК, ЯМР, РС | |
| N проверять (что YN ?) | |
| Ссылки на инфобоксы | |
| Другие результаты | |
| оксид железа, сера, уран, торий, кальций, калий, капля диоксида кремния. | iron oxide, sulfur, uranium, thorium, calcium, potassium, a smidgen of silicon dioxide. |
| Мы ещё ждём доказательства изнасилования Тони, но анализ её крови обнаружил оксид азота. | We’re still waiting on the results from Tawny’s rape kit, but her blood test did come back positive for nitrous oxide. |
Комитет отметил, что три уведомления охватывают различные соединения трибутилолова; общим для всех трех уведомлений является лишь оксид трибутилолова. | The Committee noted that the three notifications covered different tributyl tin compounds, of which only tributyl tin oxide was common to all three. |
| Пары цинка-металла вступают в реакцию с кислородом в атмосфере вращающейся трубчатой печи, при этом получается оксид цинка, который отсасывается и собирается в фильтрах. | This zinc metal vapour reacts with the oxygen in the rotating tube furnace atmosphere to zinc oxide which is sucked off and collected in filters. |
| В результате этого процесса получаются три полностью используемые продукта: оксид цинка, металлизированные окатыши и гранулы свинца. | Three fully usable products zinc oxide, iron pellets and lead fraction are gained. |
| Сырье, например, известняк, кремнезем, глинозем и оксид железа, загружаются с верхнего, или холодного конца вращающейся печи. | Raw materials such as limestone, silica, alumina and iron oxides are fed into the upper or “cold” end of the rotary kiln. |
| Потому что без работы креатин или оксид азота не помогут. | ‘Cause without the work, the creatine or nitric oxide’s not gonna do it. |
| Сырье, например, известняк, кремнезем, глинозем и оксид железа, загружаются с верхнего, или холодного конца вращающейся печи. | Raw materials, such as limestone, silica, alumina and iron oxides are fed into the upper or so-called “cold” end of the rotary kiln. |
| Весь остающийся оксид урана, обогащенный до 5–20%, будет перерабатываться в топливо для Тегеранского исследовательского реактора. | All remaining uranium oxide enriched to between 5% and 20% will be fabricated into fuel for the Tehran Research Reactor (TRR). |
| Воскресенье, 3 июля, 10:40 Через Италию до Бари, потом на пароме в Грецию, оттуда в Турцию. | We’ll head south, through Italia to Bari, and take the ferry boat to — Greece, and then to Turky. |
Кремнезем, оксид натрия, с широкополосным противоотражательным покрытием. | Silica, sodium oxide, with a broadband anti-reflective coating. |
| Оксид железа за магнитной ленте прикреплен к полиуретану через связующее вещество. | Iron oxide in mag tape- it sticks to polyurethane with a binder. |
| Этот оксид беспроводной и полностью автоматизированый. | This nitrous oxide regulator is wireless and fully automated. |
| Я помчался с ней к ветеринару, но их оксид азота украли. | I rushed her to the vet emergency room, but their nitrous oxide tank had been stolen. |
| С одной стороны мы имеем оксид ртути и графит с твоих тормозных колодок. | On one side, we have mercuric oxide and graphite from your brake pads. |
| Точнее оксид кремния, соединения серы и синтетические каучуки. | Specifically silica, sulfur compounds and synthetic rubbers. |
| Потому что без работы креатин или оксид азота не помогут. | ‘Cause without the work, the creatine or nitric oxide’s not gonna do it. |
| Студия Бари поможет в строительсве комуникации для Синепса. -Это хорошо. | Barry’s studio is going to help us build the SYNAPE pipeline / Oh, good |
| Сапфир – это оксид алюминия, а ледник состоит из сложного кварца, пигментированного железом. | Sapphire’s an aluminum oxide, but the glacier is just a compound silicon with iron pigmentation. |
| Но нам нужен магний для того, чтобы оксид железа загорелся. | But we’d need magnesium to ignite some iron oxide. |
| Конт назвал 250 известных атлетов, в том числе, короля хоумранов Бари Бондса. | Conte’s files named over 250 athletes, including the home-run king himself, Barry Bonds. |
| Мой дядя живет в Бари, он хозяин Очень Шикарного Супер Бара. | My uncle is the owner of the Very Chic Super Bar in Bari. |
| Да, я бы сказал, как алюминий и оксид железа. | Yeah, like I was saying, uh, aluminum and iron oxide. |
| Вопреки тому, что люди думают как Бари Бондс, что можешь взять ампулу тестостерона, и положить её в спортивную форму Бари и он сделает 700 хоумранов | Regardless of what people think of Barry Bonds, you can’t take a bottle of testosterone, put on Barry’s baseball uniform and make him hit 700 home runs. |
| Завтра мой Бари играет здесь на выезде. | Tomorrow Bari F.C. is playing an away match here. |
| Посмотрите, там был оксид железа, который остался в остеонах, а также в канальцах. | Look, there was iron oxide caught in the osteons as well as canaliculi. |
| Кьяра, это постановления суда Бари. | Chiara, this is from the Court in Bari. |
| Бари, я хочу водички. | Barry, I need some water. |
| Похоже, это уже не впервый раз, когда вы просите меня заменить Бари Цукеркорна. | Look, this is not the first time I’ve been brought in to replace Barry Zuckerkorn. |
| Этот оксид служит диэлектриком, а также защищает конденсатор от агрессивных реакций металлического алюминия на части электролита. | This oxide serves as dielectric and also protects the capacitor from the aggressive reactions of metallic aluminum to parts of the electrolyte. |
| Гончары начали рисовать полихромные картины на белой непрозрачной поверхности с металлическими оксидами, такими как оксид кобальта, и производить люстру. | Potters began to draw polychrome paintings on the white opaque surface with metallic oxides such as cobalt oxide and to produce lustreware. |
| Эти факторы-высокий показатель преломления, низкая растворимость в глазури и размер частиц делают оксид олова отличным глушителем. | These factors – the high refractive index, the low solubility in glazes and the particle size make tin oxide an excellent opacifier. |
Оксид алюминия и оксид железа присутствуют только в виде флюса для снижения температуры спекания и вносят незначительный вклад в прочность цемента. | Aluminium oxide and iron oxide are present only as a flux to reduce the sintering temperature and contribute little to the cement strength. |
| Сульфидные руды цинка обжигают в присутствии кислорода, превращая сульфид цинка в оксид. | Zinc sulfide ores are roasted in the presence of oxygen, converting the zinc sulfide to the oxide. |
| 2 декабря 1943 года 105 Ju 88 A-4s, вооруженные бомбами и мотобомбой, кружащими торпедами, атаковали удерживаемый союзниками порт Бари, Италия. | On 2 December 1943, 105 Ju 88 A-4s, armed with bombs and motobomba circling torpedoes, attacked the Allied-held port of Bari, Italy. |
| Ранние формулы лака для ногтей были созданы с использованием основных ингредиентов, таких как лавандовое масло, Кармин, оксид олова и масло бергамота. | Early nail polish formulas were created using basic ingredients such as lavender oil, Carmine, oxide tin, and bergamot oil. |
Оксид цинка эвгенол также используется в качестве антимикробной добавки в красках. | Zinc oxide eugenol is also used as an antimicrobial additive in paint. |
| Одна трубка содержит оксид цинка и растительное или минеральное масло, другая-эвгенол и канифоль. | One tube contains zinc oxide and vegetable or mineral oil; the other contains eugenol and rosin. |
| В таких городах, как Бари и Неаполь, беспорядки можно было подавить, а Флоренцию на целый день контролировали демонстранты. | In towns like Bari and Naples rioting could be suppressed, while Florence was controlled by demonstrators for a whole day. |
| Оксид свинца-это флюс, который заставляет свинцовую и оловянную глазурь плавиться на глиняном корпусе печенья при низкой температуре печи, около 800 ° C. | Lead oxide is a flux that causes lead and tin glazes to fuse to the earthenware biscuit body at a low oven temperature, about 800°C. |
Оксид урана сушат перед вставкой в трубы, чтобы попытаться устранить влагу в керамическом топливе, которая может привести к коррозии и водородному охрупчиванию. | The uranium oxide is dried before inserting into the tubes to try to eliminate moisture in the ceramic fuel that can lead to corrosion and hydrogen embrittlement. |
| Сравнивая диэлектрические проницаемости различных оксидных материалов, видно, что пентоксид тантала имеет диэлектрическую проницаемость примерно в три раза выше, чем оксид алюминия. | Comparing the permittivities of the different oxide materials it is seen that tantalum pentoxide has a permittivity approximately three times higher than aluminum oxide. |
| Оксид индия-олова используется в качестве светофильтра в натриевых лампах низкого давления. | Indium tin oxide is used as a light filter in low-pressure sodium-vapor lamps. |
| Еще позже римляне использовали ступку без пуццолана с использованием измельченной терракоты, вводя в смесь оксид алюминия и диоксид кремния. | Even later, the Romans used a mortar without pozzolana using crushed terra cotta, introducing aluminum oxide and silicon dioxide into the mix. |
| Гораздо реже встречаются всплывающие окна, вызванные присутствием пирита, сульфида железа, который генерирует расширение, образуя оксид железа и эттрингит. | Far less common are pop-outs caused by the presence of pyrite, an iron sulfide that generates expansion by forming iron oxide and ettringite. |
| Гадолиний был открыт в 1880 году Жаном Шарлем де Мариньяком, который обнаружил его оксид с помощью спектроскопии. | Gadolinium was discovered in 1880 by Jean Charles de Marignac, who detected its oxide by using spectroscopy. |
| Было отмечено, что нерастворимый оксид этого элемента имеет коричневый оттенок. | The insoluble oxide of this element was noted to be tinged brown. |
| Оксиды растворяются в азотной кислоте, которая исключает один из основных компонентов, церий, оксид которого нерастворим в HNO3. | The oxides are dissolved in nitric acid that excludes one of the main components, cerium, whose oxide is insoluble in HNO3. |
| Например, обожженный свинец был из рода оксид и вида свинец. | For example, burned lead was of the genus oxide and species lead. |
| Атмосферный натрий под этим слоем обычно химически связан в соединениях, таких как оксид натрия, в то время как атомы натрия над слоем, как правило, ионизированы. | Atmospheric sodium below this layer is normally chemically bound in compounds such as sodium oxide, while the sodium atoms above the layer tend to be ionized. |
| Чтобы преобразовать оксид или сульфид металла в более чистый металл, руда должна быть восстановлена физически, химически или электролитически. | In order to convert a metal oxide or sulphide to a purer metal, the ore must be reduced physically, chemically, or electrolytically. |
| В порту Бари произошел непреднамеренный выброс химического оружия. | An unintended chemical weapon release occurred at the port of Bari. |
Это описание не является уникальным для SiC, но также применимо к другим бинарным тетраэдрическим материалам, таким как оксид цинка и сульфид кадмия. | This description is not unique to SiC, but also applies to other binary tetrahedral materials, such as zinc oxide and cadmium sulfide. |
| Оксид свинца также способствует растворимости других оксидов металлов и используется в цветном стекле. | Lead oxide also facilitates solubility of other metal oxides and is used in colored glass. |
| Как и оксид, фторид является высокоосновным анионом и, как известно, стабилизирует ионы металлов в высоких степенях окисления. | Like oxide, fluoride is a highly basic anion and is known to stabilize metal ions in high oxidation states. |
| Обладая высокой температурой плавления, оксид иттрия используется в некоторых керамических и стеклянных изделиях для придания им ударопрочности и низких свойств теплового расширения. | Having a high melting point, yttrium oxide is used in some ceramic and glass to impart shock resistance and low thermal expansion properties. |
Оксид цинка эвгенол образует смесь оксида цинка и эвгенола с образованием полимеризованного эвгенольного цемента. | Zinc oxide eugenol constituents a mixture of zinc oxide and eugenol to form a polymerised eugenol cement. |
| Металл-Оксид-Полупроводниковый Полевой Транзистор. | Metal-Oxide-Semiconductor Field-Effect Transistor. |
| В этой реакции оксид серебра на первой стадии действует как донор гидроксида, в то время как Ион серебра не играет никакой роли в реакции. | In this reaction, the silver oxide in the first step acts as a hydroxide donor while the silver ion plays no role in the reaction. |
| Себациновая кислота производится из касторового масла с использованием гидроксида натрия, серной кислоты с катализаторами, включая оксид цинка и фенол. | Sebacic acid is produced from castor oil by using sodium hydroxide, sulfuric acid with catalysts including zinc oxide and phenol. |
Обработанный на растворе слой оксида цинка, модифицированного гидроксидом бария, легированный алюминием для высокоэффективных инвертированных органических солнечных элементов
rsc.org/schema/rscart38″> Инвертированные органические солнечные элементы (iOSC) с воздухоустойчивыми интерфейсными материалами и верхними электродами и КПД 6,01% достигаются за счет введения слоя гидроксида бария (Ba (OH) 2 ) между оксидом цинка, легированным алюминием (AZO) слой вывода электронов и активный слой. В качестве соединений активного слоя были выбраны чередующийся сополимер дикетопирролопиррола и хинкетиофена с низкой шириной запрещенной зоны (pDPP5T-2) и метиловый эфир фенил-C61-масляной кислоты (PC 61 BM).По сравнению с устройством управления без Ba (OH) 2 , введение слоя Ba (OH) 2 толщиной в несколько нанометров приводит к усилению В OC на 10%, Дж SC 28%, FF 28% и PCE 80%. Модификация AZO раствором, обработанным дешевым слоем Ba (OH) 2 , увеличила эффективность инвертированного устройства за счет значительного снижения энергетического барьера для вывода электронов из ПК 61 BM и, следовательно, снижения заряда рекомбинация наблюдается. Резкое повышение эффективности устройства и простота изготовления путем обработки раствора предполагают, что Ba (OH) 2 является перспективным и практичным способом снижения потерь рекомбинации на поверхности раздела на катоде органических солнечных элементов.
Резкое повышение эффективности устройства и простота изготовления путем обработки раствора предполагают, что Ba (OH) 2 является перспективным и практичным способом снижения потерь рекомбинации на поверхности раздела на катоде органических солнечных элементов.
У вас есть доступ к этой статье
Подождите, пока мы загрузим ваш контент… Что-то пошло не так. Попробуй еще раз?Катализаторы | Бесплатный полнотекстовый | Pt-аморфный барий-оксид алюминия / углеродные катализаторы для усиленной реакции электроокисления метанола
2.
 1. Влияние различных температур прокаливания на MOR катализатора На рисунке 1a показана циклическая вольтамперометрия (CV) катализаторов Pt-Ba 0,5 AlO x / C с Ba 0,5 AlO x , подвергнутых различным прокаливанию. температуры. Все катализаторы имели одинаковые потенциалы прямого пика, а именно 0,66, 0,65 и 0,65 В. Однако максимальная плотность тока при прямой развертке CV для окисления CH 3 OH и электрохимически активная площадь поверхности (ECSA) являются важными свойствами для определяющие элементы при оценке активности MOR электрода в DMFC.Катализатор с большой ECSA обычно обладает высокой электрокаталитической активностью [24]. На рис. 1a, b характеристики полученного некальцинированного катализатора Ba 0,5 AlO x были выше, чем у двух других катализаторов при температурах прокаливания 200 ° C и 400 ° C. Этот результат показал, что максимальная плотность тока (3,89 мА / см 2 ) и ECSA (49,83 м 2 / г) для MOR некальцинированных катализаторов были выше, чем у катализаторов, прокаленных при 200 ° C (2.
1. Влияние различных температур прокаливания на MOR катализатора На рисунке 1a показана циклическая вольтамперометрия (CV) катализаторов Pt-Ba 0,5 AlO x / C с Ba 0,5 AlO x , подвергнутых различным прокаливанию. температуры. Все катализаторы имели одинаковые потенциалы прямого пика, а именно 0,66, 0,65 и 0,65 В. Однако максимальная плотность тока при прямой развертке CV для окисления CH 3 OH и электрохимически активная площадь поверхности (ECSA) являются важными свойствами для определяющие элементы при оценке активности MOR электрода в DMFC.Катализатор с большой ECSA обычно обладает высокой электрокаталитической активностью [24]. На рис. 1a, b характеристики полученного некальцинированного катализатора Ba 0,5 AlO x были выше, чем у двух других катализаторов при температурах прокаливания 200 ° C и 400 ° C. Этот результат показал, что максимальная плотность тока (3,89 мА / см 2 ) и ECSA (49,83 м 2 / г) для MOR некальцинированных катализаторов были выше, чем у катализаторов, прокаленных при 200 ° C (2. 89 мА / см 2 и 25,12 м 2 / г) и 400 ° C (1,08 мА / см 2 и 22,52 м 2 / г). Свойства переноса заряда различных катализаторов оценивали с использованием графиков Найквиста для измерения спектров электрохимического импеданса (EIS); диаметр первичного полукруга тесно связан с сопротивлением зарядовой реакции (R ct ), связанным с MOR [25]. Малый диаметр полукруга соответствует высокой электрокаталитической активности катализатора MOR.Как показано на рисунке 1c, диаметр первичного полукруга для данных импеданса может быть смоделирован в модели эквивалентной схемы, показанной на рисунке 1d [25,26]. В схеме использовались следующие элементы: R s — сопротивление раствора, R o — контактное сопротивление между катализатором и опорным электродом, а элемент постоянной фазы (CPE) — двухслойная емкость, которая равна связано с адсорбцией интермедиатов, образующихся при MOR [25]. На рисунке 1c, R ct из 20% Pt-Ba 0.
89 мА / см 2 и 25,12 м 2 / г) и 400 ° C (1,08 мА / см 2 и 22,52 м 2 / г). Свойства переноса заряда различных катализаторов оценивали с использованием графиков Найквиста для измерения спектров электрохимического импеданса (EIS); диаметр первичного полукруга тесно связан с сопротивлением зарядовой реакции (R ct ), связанным с MOR [25]. Малый диаметр полукруга соответствует высокой электрокаталитической активности катализатора MOR.Как показано на рисунке 1c, диаметр первичного полукруга для данных импеданса может быть смоделирован в модели эквивалентной схемы, показанной на рисунке 1d [25,26]. В схеме использовались следующие элементы: R s — сопротивление раствора, R o — контактное сопротивление между катализатором и опорным электродом, а элемент постоянной фазы (CPE) — двухслойная емкость, которая равна связано с адсорбцией интермедиатов, образующихся при MOR [25]. На рисунке 1c, R ct из 20% Pt-Ba 0. Катализаторы 5 AlO x / C, полученные с некальцинированным Ba 0,5 AlO x , были меньше, чем катализаторы, прокаленные при 200 ° C и 400 ° C. Эти результаты показали, что скорость ионного переноса MOR катализатора 20% Pt-Ba 0,5 AlO x / C, полученного некальцинированием Ba 0,5 AlO x , была выше, чем у двух других катализаторов, прокаленных при 200 ° C и 400 ° C из-за наличия проводящей углеродной подложки [12]. Таким образом, была получена наилучшая электрокаталитическая активность катализатора MOR.Аморфные структуры были получены при использовании некальцинированных катализаторов Ba 0,5 AlO x и катализаторов, прокаленных при температуре от 200 ° C до 400 ° C, как показали данные XRD и изображение ПЭМ, показанные на рис. 2a, b. Однако их гранулометрический состав различается, что позволяет предположить, что размер частиц влияет на активность катализатора. Гистограммы гранулометрического состава некальцинированных катализаторов Ba 0,5 AlO x и катализаторов, прокаленных при температуре от 200 ° C до 400 ° C, показаны на рисунке 3.
Катализаторы 5 AlO x / C, полученные с некальцинированным Ba 0,5 AlO x , были меньше, чем катализаторы, прокаленные при 200 ° C и 400 ° C. Эти результаты показали, что скорость ионного переноса MOR катализатора 20% Pt-Ba 0,5 AlO x / C, полученного некальцинированием Ba 0,5 AlO x , была выше, чем у двух других катализаторов, прокаленных при 200 ° C и 400 ° C из-за наличия проводящей углеродной подложки [12]. Таким образом, была получена наилучшая электрокаталитическая активность катализатора MOR.Аморфные структуры были получены при использовании некальцинированных катализаторов Ba 0,5 AlO x и катализаторов, прокаленных при температуре от 200 ° C до 400 ° C, как показали данные XRD и изображение ПЭМ, показанные на рис. 2a, b. Однако их гранулометрический состав различается, что позволяет предположить, что размер частиц влияет на активность катализатора. Гистограммы гранулометрического состава некальцинированных катализаторов Ba 0,5 AlO x и катализаторов, прокаленных при температуре от 200 ° C до 400 ° C, показаны на рисунке 3.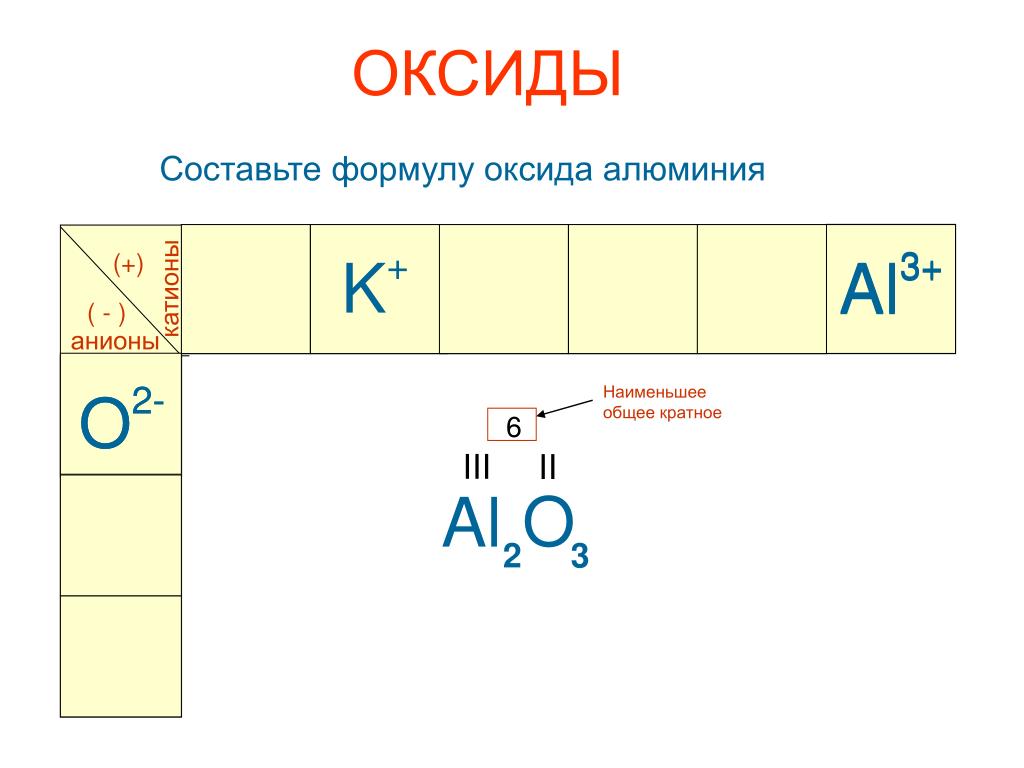 Результаты показали, что максимальный средний размер частиц составлял от 0,6 мкм до 3,0 мкм, 0,6, 2,0 и 8,0 мкм, от 5,0 мкм до 10,5 мкм, соответственно. Их удельная поверхность составляла 7,79 ± 0,01, 5,24 ± 0,01 и 3,48 ± 0,01 м 2 / г, что соответствовало малым размерам частиц катализаторов с большой удельной поверхностью. Эти результаты прояснили влияние наблюдаемого размера частиц на MOR. Bergamaski et al. [27] сообщили об увеличении прочности связи Pt-CO и Pt-OH с уменьшением размера частиц на MOR.Следовательно, влияние размера частиц Ba 0,5 AlO x , наблюдаемое на MOR, было связано с увеличением прочности связи Ba 0,5 AlO x -OH адс с уменьшением размера их частиц, приводит к более высокому СОЖ. Следовательно, активность MOR снижалась с повышением температуры прокаливания катализаторов Ba 0,5 AlO x , с возрастающим влиянием на увеличенный размер частиц и уменьшение площади поверхности.
Результаты показали, что максимальный средний размер частиц составлял от 0,6 мкм до 3,0 мкм, 0,6, 2,0 и 8,0 мкм, от 5,0 мкм до 10,5 мкм, соответственно. Их удельная поверхность составляла 7,79 ± 0,01, 5,24 ± 0,01 и 3,48 ± 0,01 м 2 / г, что соответствовало малым размерам частиц катализаторов с большой удельной поверхностью. Эти результаты прояснили влияние наблюдаемого размера частиц на MOR. Bergamaski et al. [27] сообщили об увеличении прочности связи Pt-CO и Pt-OH с уменьшением размера частиц на MOR.Следовательно, влияние размера частиц Ba 0,5 AlO x , наблюдаемое на MOR, было связано с увеличением прочности связи Ba 0,5 AlO x -OH адс с уменьшением размера их частиц, приводит к более высокому СОЖ. Следовательно, активность MOR снижалась с повышением температуры прокаливания катализаторов Ba 0,5 AlO x , с возрастающим влиянием на увеличенный размер частиц и уменьшение площади поверхности. Полученные результаты показали, что непрокаленный Ba 0.5 катализаторов AlO x обладают выдающейся активностью MOR, имеют наименьший размер частиц и наибольшую удельную поверхность. Показаны XPS O 1s, Ba 3d и Al 2p для Ba 0,5 AlO x при различных температурах прокаливания. на рисунке 4. Энергии связи O 1s и Ba 3d были аналогичными в некальцинированных катализаторах Ba 0,5 AlO x или катализаторах, прокаленных при 200 ° C и 400 ° C. Пик при энергии связи O 1 с для каждого катализатора показывает состояние гидроксида алюминия (Al (OH) 3 ) или оксигидроксида алюминия (AlO (OH)) при 532.4 эВ и оксид алюминия (Al 2 O 3 ) при 531,33 эВ [28]. Наличие -OH, возможно, заставляет Al 2 O 3 реагировать с водой с образованием Al (OH) 3 [29]. В этой реакции вода поступает из катализатора, подвергающегося воздействию атмосферы (влаги) до измерения XPS [30], и Al 2 O 3 , который реагирует с Al (OH) 3 с образованием AlO (OH) [29] .
Полученные результаты показали, что непрокаленный Ba 0.5 катализаторов AlO x обладают выдающейся активностью MOR, имеют наименьший размер частиц и наибольшую удельную поверхность. Показаны XPS O 1s, Ba 3d и Al 2p для Ba 0,5 AlO x при различных температурах прокаливания. на рисунке 4. Энергии связи O 1s и Ba 3d были аналогичными в некальцинированных катализаторах Ba 0,5 AlO x или катализаторах, прокаленных при 200 ° C и 400 ° C. Пик при энергии связи O 1 с для каждого катализатора показывает состояние гидроксида алюминия (Al (OH) 3 ) или оксигидроксида алюминия (AlO (OH)) при 532.4 эВ и оксид алюминия (Al 2 O 3 ) при 531,33 эВ [28]. Наличие -OH, возможно, заставляет Al 2 O 3 реагировать с водой с образованием Al (OH) 3 [29]. В этой реакции вода поступает из катализатора, подвергающегося воздействию атмосферы (влаги) до измерения XPS [30], и Al 2 O 3 , который реагирует с Al (OH) 3 с образованием AlO (OH) [29] . Пики при энергиях связи 780,4 и 795,5 эВ для всех катализаторов можно отнести к основным линиям Ba 3d 5/2 и 3d 3/2 Ba 2+ соответственно [31].В частности, энергии связи Al 2p XPS варьировались между катализаторами Ba 0,5 AlO x , прокаленными при различных температурах. Только один пик энергии связи при 74,1 эВ был получен для некальцинированного Ba 0,5 AlO x . Однако, когда температура прокаливания увеличилась до 200 ° C и 400 ° C, пики энергий связи Al 2p положительно сдвинулись до 75,3 и 75,8 эВ, которые были отнесены к Al (OH) 3 и AlO (OH), соответственно [31].
Пики при энергиях связи 780,4 и 795,5 эВ для всех катализаторов можно отнести к основным линиям Ba 3d 5/2 и 3d 3/2 Ba 2+ соответственно [31].В частности, энергии связи Al 2p XPS варьировались между катализаторами Ba 0,5 AlO x , прокаленными при различных температурах. Только один пик энергии связи при 74,1 эВ был получен для некальцинированного Ba 0,5 AlO x . Однако, когда температура прокаливания увеличилась до 200 ° C и 400 ° C, пики энергий связи Al 2p положительно сдвинулись до 75,3 и 75,8 эВ, которые были отнесены к Al (OH) 3 и AlO (OH), соответственно [31].2.2. Влияние различных соотношений предшественников Ba и Al на MOR
. CV MOR от -0,2 В до 0,9 В на 20% Pt с различными катализаторами BaAlO x / C, состоящими из BaAlO x , были получены с различными соотношениями Прекурсоры Ba и Al: мольные отношения 1/1, 1/2, 1/3, 2/1 и 3/1, названные Ba 0,5 Al 0,5 O x , Ba 0,5 AlO x , Ba 0,33 AlO x , BaAl 0,5 O x и BaAl 0,33 O x соответственно, как показано на рисунке 5a. Потенциалы прямого пика катализаторов BaAlO x , приготовленных с различным соотношением контактов Ba и Al на 20% Pt-различных катализаторах BaAlO x / C, наблюдаемые при примерно 0,66–0,67 В при прямом сканировании (таблица 1), были характерны для MOR путем окисления Pt- (CH 3 OH) адсорбирует на поверхности катализатора [32]. Однако прямые пики потенциалов 20% Pt-Al 2 O 3 / C и 20% Pt / C отрицательно сдвинулись до 0,64 и 0,65 В по сравнению с 20% Pt-Ba 0.5 катализаторов AlO x / C, что указывает на низкую активность их MOR. Напротив, поддерживаемые пики потенциалов различных катализаторов при около 0,46–0,48 В были аналогичны таковому для 20% Pt / C (0,47 В) при обратном сканировании и в основном связаны с удалением остаточных углеродных частиц, образовавшихся при прямом сканировании. [33]. Одновременно эти катализаторы BaAlO x могут улучшить поверхность Pt и будут покрыты метанолом, вызывая повышенную хемосорбцию H на чистой Pt, такой как PtOH и + H + + e — → Pt + H 2 O [34].
Потенциалы прямого пика катализаторов BaAlO x , приготовленных с различным соотношением контактов Ba и Al на 20% Pt-различных катализаторах BaAlO x / C, наблюдаемые при примерно 0,66–0,67 В при прямом сканировании (таблица 1), были характерны для MOR путем окисления Pt- (CH 3 OH) адсорбирует на поверхности катализатора [32]. Однако прямые пики потенциалов 20% Pt-Al 2 O 3 / C и 20% Pt / C отрицательно сдвинулись до 0,64 и 0,65 В по сравнению с 20% Pt-Ba 0.5 катализаторов AlO x / C, что указывает на низкую активность их MOR. Напротив, поддерживаемые пики потенциалов различных катализаторов при около 0,46–0,48 В были аналогичны таковому для 20% Pt / C (0,47 В) при обратном сканировании и в основном связаны с удалением остаточных углеродных частиц, образовавшихся при прямом сканировании. [33]. Одновременно эти катализаторы BaAlO x могут улучшить поверхность Pt и будут покрыты метанолом, вызывая повышенную хемосорбцию H на чистой Pt, такой как PtOH и + H + + e — → Pt + H 2 O [34]. Кроме того, таблица 1, полученная из рисунка 5a, показывает, что максимальные плотности тока при прямом и обратном пиковом потенциале для катализаторов 20% Pt-Al 2 O 3 / C составляли 0,58 и 0,27 мА / см 2 , которые были ниже, чем у катализаторов 20% Pt / C (1,47 и 0,4 мА / см 2 ). Этот результат показал, что Al 2 O 3 не был каталитически активен в MOR. Следовательно, он получил наименьшее значение ECSA и наибольшее значение EIS, как показано на рис. 5b, c соответственно.Однако максимальная плотность тока при прямом и обратном пиковом потенциале катализаторов BaAlO x , приготовленных с различными соотношениями Ba, смешанного с Al, была выше, чем у Al 2 O 3 . Эти результаты свидетельствуют о том, что присутствие Ba в катализаторах BaAlO x облегчает окисление только что хемосорбированных частиц и приводит к увеличению MOR, благодаря которому катализаторы BaAlO x обеспечивают активный кислород для эффективного удаления промежуточных продуктов, таких как CO на Pt.
Кроме того, таблица 1, полученная из рисунка 5a, показывает, что максимальные плотности тока при прямом и обратном пиковом потенциале для катализаторов 20% Pt-Al 2 O 3 / C составляли 0,58 и 0,27 мА / см 2 , которые были ниже, чем у катализаторов 20% Pt / C (1,47 и 0,4 мА / см 2 ). Этот результат показал, что Al 2 O 3 не был каталитически активен в MOR. Следовательно, он получил наименьшее значение ECSA и наибольшее значение EIS, как показано на рис. 5b, c соответственно.Однако максимальная плотность тока при прямом и обратном пиковом потенциале катализаторов BaAlO x , приготовленных с различными соотношениями Ba, смешанного с Al, была выше, чем у Al 2 O 3 . Эти результаты свидетельствуют о том, что присутствие Ba в катализаторах BaAlO x облегчает окисление только что хемосорбированных частиц и приводит к увеличению MOR, благодаря которому катализаторы BaAlO x обеспечивают активный кислород для эффективного удаления промежуточных продуктов, таких как CO на Pt. поверхность.Максимальная плотность тока (4,07 мА / см 2 ) на прямом пике катализаторов 20% Pt-Ba 0,5 AlO x / C (мольное отношение Ba / Al 1/2) была выше, чем у 20% катализаторов. % Pt / C и другие катализаторы BaAlO x , приготовленные с различными мольными соотношениями контакта Ba и Al. Эти результаты показали, что метанол легче окисляется с катализатором 20% Pt-Ba 0,5 AlO x / C, чем с другими катализаторами, включая катализатор 20% Pt / C. Кроме того, ECSA различных катализаторов показан на Рисунок 5b и Таблица 1.Результаты показали, что MOR катализаторов 20% Pt-Ba 0,5 AlO x / C зависит от самого большого ECSA (49,83 м 2 / г) среди катализаторов. На рисунке 5d, R ct катализаторов 20% Pt-Ba 0,5 AlO x / C было ниже, чем у катализаторов 20% Pt / C и других катализаторов, и этот параметр соответствовал высокой электрокаталитической активности MOR.
поверхность.Максимальная плотность тока (4,07 мА / см 2 ) на прямом пике катализаторов 20% Pt-Ba 0,5 AlO x / C (мольное отношение Ba / Al 1/2) была выше, чем у 20% катализаторов. % Pt / C и другие катализаторы BaAlO x , приготовленные с различными мольными соотношениями контакта Ba и Al. Эти результаты показали, что метанол легче окисляется с катализатором 20% Pt-Ba 0,5 AlO x / C, чем с другими катализаторами, включая катализатор 20% Pt / C. Кроме того, ECSA различных катализаторов показан на Рисунок 5b и Таблица 1.Результаты показали, что MOR катализаторов 20% Pt-Ba 0,5 AlO x / C зависит от самого большого ECSA (49,83 м 2 / г) среди катализаторов. На рисунке 5d, R ct катализаторов 20% Pt-Ba 0,5 AlO x / C было ниже, чем у катализаторов 20% Pt / C и других катализаторов, и этот параметр соответствовал высокой электрокаталитической активности MOR. На рисунке 6 показаны данные XRD для различных катализаторов BaAlO x с различным соотношением контактов Ba и Al.Аморфные структуры образовывались, когда мольное отношение контактов предшественника Al было больше или равно таковому у предшественников Ba, например Ba 0,5 Al 0,5 O x (Ba / Al = 1/1), Ba 0,5 AlO x (Ba / Al = 1/2) и Ba 0,33 AlO x (Ba / Al = 1/3). Кристаллизационное соединение, состоящее из кристаллических структур Al 2 O 3 (CCDS11-0517) и Ba 2 Al 2 O 5 (44-0474), образованных мольным соотношением предшественников Ba, было больше, чем молярное соотношение предшественников Al, таких как BaAl 0.5 O x (Ba / Al = 2/1) и BaAl 0,33 O x (Ba / Al = 3/1). К сожалению, активность MOR этих кристаллических катализаторов BaAlO x была ниже, чем у аморфных катализаторов BaAlO x , поскольку аморфные катализаторы BaAlO x , возможно, состояли из аморфного Al 2 O 3 , существующего в вакансиях нейтрального кислорода [35] .
На рисунке 6 показаны данные XRD для различных катализаторов BaAlO x с различным соотношением контактов Ba и Al.Аморфные структуры образовывались, когда мольное отношение контактов предшественника Al было больше или равно таковому у предшественников Ba, например Ba 0,5 Al 0,5 O x (Ba / Al = 1/1), Ba 0,5 AlO x (Ba / Al = 1/2) и Ba 0,33 AlO x (Ba / Al = 1/3). Кристаллизационное соединение, состоящее из кристаллических структур Al 2 O 3 (CCDS11-0517) и Ba 2 Al 2 O 5 (44-0474), образованных мольным соотношением предшественников Ba, было больше, чем молярное соотношение предшественников Al, таких как BaAl 0.5 O x (Ba / Al = 2/1) и BaAl 0,33 O x (Ba / Al = 3/1). К сожалению, активность MOR этих кристаллических катализаторов BaAlO x была ниже, чем у аморфных катализаторов BaAlO x , поскольку аморфные катализаторы BaAlO x , возможно, состояли из аморфного Al 2 O 3 , существующего в вакансиях нейтрального кислорода [35] . Обильные кислородные вакансии демонстрируют резко улучшенную электрокаталитическую активность MOR [36]. По мере того, как образуется больше кислородных вакансий, они приводят к увеличению поверхностной концентрации кислорода на металлооксидных катализаторах, обеспечивая большее количество связи оксид металла-OH адс [37], что увеличивает конверсию CO адс в CO 2 на Оксид Pt-металла / C катализатор [38].Следовательно, кислородные вакансии катализатора Ba 0,5 AlO x были больше, чем вакансии катализатора Ba 0,5 Al 0,5 O x , поскольку мольное отношение Al в Ba 0,5 AlO x было выше, чем у Ba 0,5 Al 0,5 O x из-за наличия в катализаторах более аморфного Al 2 O 3 . Аморфный Al 2 O 3 с большим количеством отрицательных зарядов также способствует осаждению и диспергированию наночастиц Pt за счет сильного электростатического взаимодействия [39].
Обильные кислородные вакансии демонстрируют резко улучшенную электрокаталитическую активность MOR [36]. По мере того, как образуется больше кислородных вакансий, они приводят к увеличению поверхностной концентрации кислорода на металлооксидных катализаторах, обеспечивая большее количество связи оксид металла-OH адс [37], что увеличивает конверсию CO адс в CO 2 на Оксид Pt-металла / C катализатор [38].Следовательно, кислородные вакансии катализатора Ba 0,5 AlO x были больше, чем вакансии катализатора Ba 0,5 Al 0,5 O x , поскольку мольное отношение Al в Ba 0,5 AlO x было выше, чем у Ba 0,5 Al 0,5 O x из-за наличия в катализаторах более аморфного Al 2 O 3 . Аморфный Al 2 O 3 с большим количеством отрицательных зарядов также способствует осаждению и диспергированию наночастиц Pt за счет сильного электростатического взаимодействия [39].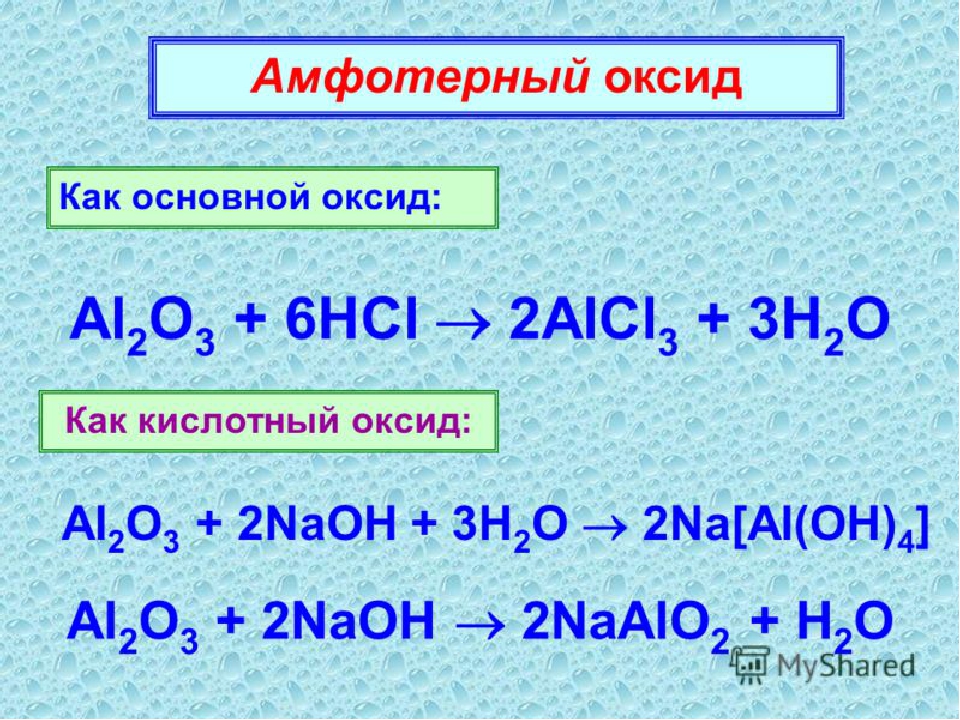 Однако мольное отношение Al увеличилось до 3. В результате активность MOR катализатора Ba 0,33 AlO x была ниже, чем у других катализаторов, возможно, потому, что избыточные контакты Al производят дефекты кислородных вакансий и вызывают длительное -дистанционное удлинение связи O – O [40]; таким образом, активность MOR снизилась. СЭМ и ПЭМ-изображения катализатора 20% Pt-Ba 0,5 AlO x / C показаны на рисунках 7 и 8a. На рисунке 8b представлены XPS-спектры Pt 4f для 20% Pt / C и 20% Pt-Ba 0.Катализаторы 5 AlO x / C были отнесены к металлическому состоянию Pt 0 и оксидным состояниям Pt 2+ и Pt 4+ . Энергия связи пиков Pt 4f для 20% Pt-Ba 0,5 AlO x / C сдвинута положительно по сравнению с пиками 20% Pt / C, и этот сдвиг можно отнести к взаимодействиям между Pt и оксидами металлов [ 14] или взаимодействия металл-носитель [41], что указывает на перенос электрона [42] между Pt и Ba 0,5 AlO x или атомно-дисперсными Pt 0 и агрегатами Pt на оксиде металла [43].
Однако мольное отношение Al увеличилось до 3. В результате активность MOR катализатора Ba 0,33 AlO x была ниже, чем у других катализаторов, возможно, потому, что избыточные контакты Al производят дефекты кислородных вакансий и вызывают длительное -дистанционное удлинение связи O – O [40]; таким образом, активность MOR снизилась. СЭМ и ПЭМ-изображения катализатора 20% Pt-Ba 0,5 AlO x / C показаны на рисунках 7 и 8a. На рисунке 8b представлены XPS-спектры Pt 4f для 20% Pt / C и 20% Pt-Ba 0.Катализаторы 5 AlO x / C были отнесены к металлическому состоянию Pt 0 и оксидным состояниям Pt 2+ и Pt 4+ . Энергия связи пиков Pt 4f для 20% Pt-Ba 0,5 AlO x / C сдвинута положительно по сравнению с пиками 20% Pt / C, и этот сдвиг можно отнести к взаимодействиям между Pt и оксидами металлов [ 14] или взаимодействия металл-носитель [41], что указывает на перенос электрона [42] между Pt и Ba 0,5 AlO x или атомно-дисперсными Pt 0 и агрегатами Pt на оксиде металла [43]. Кроме того, в катализаторах Pt 0 содержание 20% катализаторов Pt-Ba 0,5 AlO x / C увеличилось до 70% по сравнению с 52,6% катализаторов 20% Pt / C, тем самым обеспечивая более доступные активные центры Pt для адсорбция метанола [14]. Бифункциональный механизм катализаторов Pt-металл-оксид / C зависит от синергетического вклада биметаллического оксида на Pt-катализаторах в MOR [12], происходящего от ОН, адсорбированного на поверхности оксида металла, который может окислять CO присутствует на поверхности Pt [11,37,44].Таким образом, бифункциональный механизм MOR с катализаторами 20% Pt-Ba 0,5 AlO x / C можно резюмировать в (1) — (4). В (1) метанол первоначально адсорбируется на Pt, и его метанольный протон одновременно теряется с образованием основного оксидного иона. В (2) присутствие групп Ba 0,5 AlO x может побуждать частицы OH адс реагировать с CO адс на поверхности Pt.
Кроме того, в катализаторах Pt 0 содержание 20% катализаторов Pt-Ba 0,5 AlO x / C увеличилось до 70% по сравнению с 52,6% катализаторов 20% Pt / C, тем самым обеспечивая более доступные активные центры Pt для адсорбция метанола [14]. Бифункциональный механизм катализаторов Pt-металл-оксид / C зависит от синергетического вклада биметаллического оксида на Pt-катализаторах в MOR [12], происходящего от ОН, адсорбированного на поверхности оксида металла, который может окислять CO присутствует на поверхности Pt [11,37,44].Таким образом, бифункциональный механизм MOR с катализаторами 20% Pt-Ba 0,5 AlO x / C можно резюмировать в (1) — (4). В (1) метанол первоначально адсорбируется на Pt, и его метанольный протон одновременно теряется с образованием основного оксидного иона. В (2) присутствие групп Ba 0,5 AlO x может побуждать частицы OH адс реагировать с CO адс на поверхности Pt. В результате образуется CO 2 , как показано в (3). Следовательно, высвобождается больше активных центров на поверхности Pt, что способствует окислению метанола.Ожидается, что прочно связанный промежуточный продукт будет удален с поверхности электрокатализатора путем взаимодействия с Ba 0,5 AlO x . В (4) Pt, загруженная на Ba 0,5 AlO x , может реагировать с CO с образованием CO 2 .
В результате образуется CO 2 , как показано в (3). Следовательно, высвобождается больше активных центров на поверхности Pt, что способствует окислению метанола.Ожидается, что прочно связанный промежуточный продукт будет удален с поверхности электрокатализатора путем взаимодействия с Ba 0,5 AlO x . В (4) Pt, загруженная на Ba 0,5 AlO x , может реагировать с CO с образованием CO 2 .CH 3 OH ad → CO ad + 4H + + 4e —
(1)
Ba 0,5 AlO x + H 2 O → Ba 0,5 AlO x -OH ad + H + + e —
(2)
Pt-CO объявления + Ba 0.5 AlO x -OH ad → Pt + Ba 0,5 AlO x + CO 2 + H + + e —
(3)
Pt-Ba 0,5 AlO x + yCO → Pt-Ba 0,5 AlO x-y + yCO 2
(4)
Долговременную электрохимическую стабильность катализаторов 20% Pt / C и 20% Pt-Ba 0,5 AlO x / C в MOR исследовали путем выполнения 1000 циклов непрерывного потенциала в 1 M CH 3 OH + 0. 5 M H 2 SO 4 раствор (рисунок 9). Ясно, что плотность тока обоих образцов уменьшалась при увеличении количества циклов. Максимальная плотность тока катализатора 20% Pt-Ba 0,5 AlO x / C была все еще выше, чем у катализатора 20% Pt / C после 1000 циклов. Следовательно, долговременная электрохимическая стабильность катализаторов 20% Pt-Ba 0,5 AlO x / C была лучше, чем у катализаторов 20% Pt / C, что объяснялось эффективным удалением промежуточных частиц, извлеченных из синергетический эффект [19] между Pt и Ba 0.5 AlO x .
5 M H 2 SO 4 раствор (рисунок 9). Ясно, что плотность тока обоих образцов уменьшалась при увеличении количества циклов. Максимальная плотность тока катализатора 20% Pt-Ba 0,5 AlO x / C была все еще выше, чем у катализатора 20% Pt / C после 1000 циклов. Следовательно, долговременная электрохимическая стабильность катализаторов 20% Pt-Ba 0,5 AlO x / C была лучше, чем у катализаторов 20% Pt / C, что объяснялось эффективным удалением промежуточных частиц, извлеченных из синергетический эффект [19] между Pt и Ba 0.5 AlO x .Заявка на патент США для МЕТАЛЛИЧЕСКОГО ДЕКОРИРОВАННОГО ОКСИДА АЛЮМИНИЯ БАРИЯ КАЛЬЦИЯ И РОДСТВЕННЫХ МАТЕРИАЛОВ ДЛЯ КАТАЛИЗА Nh4 Заявка на патент (Заявка № 20200197911 от 25 июня 2020 г.)
ПЕРЕКРЕСТНАЯ ССЫЛКА НА СООТВЕТСТВУЮЩУЮ ЗАЯВКУ В этой заявке заявлен приоритет и льготы согласно 35 USC. § 119 (e) к предварительной заявке на патент США сер. № 62/506,463, поданной 15 мая 2017 г., и 62/590 570, поданной 25 ноября 2017 г. Каждая из этих заявок полностью включена в настоящий документ посредством ссылки.
№ 62/506,463, поданной 15 мая 2017 г., и 62/590 570, поданной 25 ноября 2017 г. Каждая из этих заявок полностью включена в настоящий документ посредством ссылки.
Данное изобретение относится к катализатору на носителе для синтеза аммиака (NH 3 ) из газообразного азота (N 2 ) и газообразного водорода (H 2 ), способу изготовления носителя и способы декорирования носителя катализатором.
ИСТОРИЯ ВОПРОСА Угроза непрерывному экономическому развитию и безопасности, создаваемая изменением климата, вызванным антропогенными выбросами диоксида углерода (CO 2 ), хорошо известна специалистам в данной области техники.Чтобы противостоять этой угрозе, источники энергии, которые практически не содержат выбросов CO 2 , пользуются большим спросом как в развитых, так и в развивающихся странах. Хотя несколько вариантов производства энергии без CO 2 (например, ветровая, солнечная, гидроэлектрическая и ядерная энергия) были широко разработаны, ни один из них в настоящее время не включает в себя практически не содержащее CO 2 топливо.
Аммиак (NH 3 ) можно сжигать в качестве топлива согласно следующему уравнению реакции (1):
4NH 3 ( г ) + 3O 2 → 2N 2 + 6H 2 O ( г ) + тепло (1)
Таким образом, в принципе, NH 3 может использоваться как топливо, не содержащее CO 2 , и / или как среда для хранения водорода при термическом преобразовании в водород. и азотные газы.Однако почти все текущие производственные процессы NH 3 используют сырье и топливо, которые производят CO 2 .
Предыдущие усилия по устойчивому производству топлива были сосредоточены на биотопливе, H 2 и «искусственном фотосинтезе». Хотя этанол и биодизель имеют более высокую удельную энергию, чем NH 3 , использование пищевых ресурсов для производства топлива приводит к повышению цен на продовольствие как за счет смещения пахотных земель с продовольствия на топливо, так и за счет повышения цен на культуры, используемые для производства топлива. Такое перераспределение может вызвать политическую нестабильность в развивающихся странах из-за более высоких цен на продовольствие.
Такое перераспределение может вызвать политическую нестабильность в развивающихся странах из-за более высоких цен на продовольствие.
Водород никогда не мог решить проблемы с плотностью хранения, хотя NH 3 можно рассматривать как решение проблемы хранения H 2 . NH 3 имеет примерно вдвое большую плотность энергии жидкого водорода при легко достигаемых давлениях и температурах (около 9 атм при около 25 ° C; около 1 атм при около -33 ° C).
Хотя «искусственный фотосинтез» может создать замкнутый топливный цикл, для этого он должен извлекать CO 2 из воздуха.Поскольку газообразного азота гораздо больше (79%), чем CO 2 (0,04%) в атмосфере, использование NH 3 является более жизнеспособным путем для процесса этого типа; синтез одного моля метана (CH 4 ) требует обработки в 3550 раз больше воздуха, чем синтез одного моля NH 3 . Коммерческие воздушные сепараторы для атмосферной экстракции N 2 уже существуют и хорошо известны специалистам в данной области.
Основным промышленным способом производства аммиака является процесс Габера-Боша, проиллюстрированный следующим уравнением реакции (2):
N 2 ( г ) + 3H 2 ( г ) → 2NH 3 ( г ) (ΔH = −92.2 кДж / моль) (2)
Процесс Хабера-Боша требует примерно 31,4 гигаджоулей энергии, и по состоянию на 2005 год производит примерно 2,1 тонны CO 2 на тонну произведенного NH 3 . Около двух третей производства CO 2 происходит за счет парового риформинга углеводородов с получением газообразного водорода, а оставшаяся треть — за счет сжигания топлива для обеспечения энергией установки синтеза. По состоянию на 2005 год около 75% заводов Haber-Bosch NH 3 использовали природный газ в качестве сырья и топлива, а остальные использовали уголь или нефть.В результате на синтез Haber-Bosch NH 3 уходит от примерно 3% до примерно 5% мировой добычи природного газа и от примерно 1% до примерно 2% мирового производства энергии. Таким образом, желательно обеспечить усовершенствования методов синтеза аммиака, которые уменьшают зависимость методов от топлива с интенсивным содержанием CO 2 .
Таким образом, желательно обеспечить усовершенствования методов синтеза аммиака, которые уменьшают зависимость методов от топлива с интенсивным содержанием CO 2 .
Реакцию Габера-Боша обычно проводят в реакторе, содержащем оксид железа или рутениевый катализатор, при температуре примерно 300 ° C.и примерно 550 ° C, и при давлении от примерно 90 бар до примерно 180 бар. Повышенная температура требуется для достижения разумной скорости реакции. Из-за экзотермической природы синтеза NH 3 повышенная температура приводит к установлению равновесия в сторону реагентов, но этому противодействует высокое давление. В промышленном производстве отходящее тепло от синтеза аммиака способствует производству водорода путем парового риформинга природного газа.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ Реакция образования аммиака, показанная в уравнении (2), протекает медленно без помощи катализатора.Металлы, которые, как известно, катализируют реакцию, включают осмий (Os), рутений (Ru) и железо (Fe). Каталитическая активность этих металлов может быть улучшена путем добавления «промоторов», таких как щелочные металлы. Промоторы, упомянутые в литературе, включают металлический калий (K), оксид калия (K 2 O), оксид цезия (Cs 2 O), гидроксид цезия (CsOH), оксид кальция (CaO), оксид магния (MgO), металлический алюминий (Al), оксид алюминия (Al 2 O 3 ) и оксид бериллия (BeO).
Каталитическая активность этих металлов может быть улучшена путем добавления «промоторов», таких как щелочные металлы. Промоторы, упомянутые в литературе, включают металлический калий (K), оксид калия (K 2 O), оксид цезия (Cs 2 O), гидроксид цезия (CsOH), оксид кальция (CaO), оксид магния (MgO), металлический алюминий (Al), оксид алюминия (Al 2 O 3 ) и оксид бериллия (BeO).
NH 3 Активность катализатора также может быть улучшена путем нанесения катализатора на поверхность определенных «материалов носителя».«Украшение поверхности материала носителя катализатором имеет по крайней мере два преимущества. Во-первых, высокодисперсное осаждение частиц катализатора на носителе, то есть осаждение частиц с размером и формой, которые заставляют многие молекулы катализатора подвергаться воздействию реагентов, позволяет более эффективно использовать катализатор. Во-вторых, в зависимости от природы носителя, носитель также может взаимодействовать с катализатором таким образом, что увеличивает активность катализатора, например, изменяя работу выхода катализатора.
Материалы носителя, которые упоминались в литературе для использования с катализаторами NH 3 , включают активированный уголь, MgO, BeO, Al 2 O 3 , CaO, амид кальция (Ca (NH 2 ) 2 ) и C12A7: e- (электрид майенита в обозначении химии цемента). Заявка на патент США сер. № 628421,482, поданной 14 ноября 2016 г. и сер. No. 15/446929, поданной 1 марта 2017 г., также описывается использование материалов из алюмината кальция, включая CA, C5A3, C3A (обозначение химического состава цемента, C = CaO, A = Al 2 O 3 ) и CaO как в их электроизоляционной, так и в электропроводящей форме.Эти заявки полностью включены в настоящий документ посредством ссылки.
Настоящее изобретение обеспечивает улучшенный материал носителя для катализаторов синтеза NH 3 .
Одним из аспектов изобретения является обеспечение материала оксида бария-кальция-алюминия для носителя Ru или других каталитических металлов с целью синтеза NH 3 .
Одним из аспектов изобретения является обеспечение материала оксида бария, кальция и бора для носителя Ru или других каталитических металлов с целью синтеза NH 3 .
Одним из аспектов изобретения является обеспечение материала оксида бария, кальция, алюминия, бора для носителя Ru или других каталитических металлов с целью синтеза NH 3 .
Аспект изобретения состоит в том, чтобы предоставить способ преобразования опоры из электроизоляционного материала в электропроводящий материал. Метод включает отжиг электроизоляционного материала в атмосфере оксида углерода (CO).
Аспектом изобретения является обеспечение способа диспергирования Ru или другого каталитического металла из раствора на поверхности носителя.
Аспектом изобретения является диспергирование украшенного металлом порошка носителя на поверхности грубого материала для создания слоя катализатора с высокой проводимостью. Грубый материал может быть относительно инертным материалом, таким как крошка оксида алюминия, или он может быть каталитически активным материалом, таким как катализатор с активированным железом NH 3 в гранулированной форме.
Аспектом изобретения является формирование порошка носителя с металлическим декором в гранулу, таблетку или другой формованный объект.
Аспектом изобретения является формование порошка носителя в виде гранул, пеллет или объекта другой формы с последующим декорированием его каталитическим металлом.
Аспектом изобретения является приклеивание порошка подложки с металлическим декором к механической подложке, такой как песок, гранула, сетка, соты или лист.
Аспектом изобретения является приклеивание порошка подложки к механической подложке, такой как экран, гранула, соты или лист, с последующим нанесением на нее каталитического металла.
Аспектом изобретения является аммиачный катализатор, содержащий материал носителя из оксида бария-кальция-алюминия, украшенный каталитическим металлом.Материал носителя катализатора может включать по меньшей мере одну легирующую добавку. Легирующая добавка может представлять собой магний, стронций, галлий, бор, индий или их комбинации. Материал носителя аммиачного катализатора может включать более примерно 0 мас. % и меньше или равно примерно 100 мас. % хотя бы одной легирующей примеси. Материал носителя катализатора может иметь, по меньшей мере, часть, по меньшей мере, одного из бариевого компонента или кальциевого компонента, материала носителя из оксида алюминия, бария, кальция и, по меньшей мере, одного из компонентов из магния или стронция.Материал носителя катализатора может иметь по меньшей мере часть алюминиевого компонента, включающего по меньшей мере один компонент из индия, галлия или бора. В некоторых вариантах реализации барий, кальций или алюминий аммиачного катализатора могут включать более примерно 0 мас. % и меньше или равно примерно 100 мас. % магния, стронция, галлия, индия или бора. Магний, стронций, галлий, индий или бор могут представлять собой оксид магния, оксид стронция, оксид галлия, оксид индия или оксид бора или их комбинации.
Каталитический металл может быть по меньшей мере одним из Ti, V, Cr, Mn, Fe, Co, Ni, Cu, Mo, Ru, Rh, Pd или Os. . В некоторых вариантах реализации каталитическим металлом может быть Ru. Дисперсия катализатора может составлять от примерно 0,1% до примерно 90%. В некоторых вариантах реализации каталитический металл может включать Ru и включать примерно 1 мас. % каталитического металла.
Носитель из оксида бария-кальция-алюминия или замещенного оксида алюминия-бария-кальция может быть в виде порошка, гранул, таблеток или таблеток.В некоторых вариантах осуществления материал носителя, украшенный катализатором, может быть диспергирован, по меньшей мере, на части вторичного материала. Вторичный материал может представлять собой гранулы, крошку, пеллету, сетку, соты или лист.
Формула катализатора может быть по меньшей мере одной из B7C2A3, оксида бария, кальция и бора, BA, B2CA или может быть замещенной формой этих формул. Подложка из оксида бария-кальция-алюминия или подложка из замещенного оксида бария-кальция-алюминия может быть электрически изолирующей или электропроводной.
Аспектом изобретения является способ получения материала носителя катализатора. Способ включает объединение по меньшей мере одного вкладчика бария, по меньшей мере одного вкладчика кальция и по меньшей мере одного вкладчика алюминия (или вкладчика бора) в соотношении от примерно 1 до примерно 10 от вкладчика бария: от примерно 1 до примерно 10 от вкладчик кальция: от примерно 1 до примерно 10 вкладчиков алюминия (или вкладчиков бора) для образования первой смеси. Первую смесь измельчают до образования измельченной смеси.Измельченная смесь смешивается с растворителем с образованием суспензии или пасты. Суспензию или пасту сушат, чтобы получить вторую смесь. Вторую смесь отжигают с образованием материала носителя катализатора.
В некоторых вариантах воплощения вкладом бария может быть по меньшей мере один из карбоната бария, гидроксида бария, гидрата гидроксида бария, нитрата бария, оксида бария или изопропоксида бария. Вкладчик кальция может быть по меньшей мере одним из карбоната кальция, гидроксида кальция, гидрата гидроксида кальция, оксида кальция или метоксида кальция.При использовании вкладчиком алюминия может быть по меньшей мере один из оксида алюминия или изопропоксида алюминия. При использовании борной добавкой может быть по меньшей мере один из оксида бора или борной кислоты. Материал носителя катализатора может быть, по меньшей мере, одним из порошка, крупки, гранул, сита, сот или листов. Площадь поверхности измельченной смеси может составлять от примерно 0,5 до примерно 25 м 2 2 г -1 . Измельчение может происходить в присутствии растворителя или может быть смешано с растворителем после измельчения.Растворителем может быть безводный растворитель, такой как метиловый спирт, пентан, толуол, гептан, ацетон, хлороформ, гексан или их комбинации. Отношение измельченной смеси к растворителю может составлять от примерно 1 до примерно 10 порошка к примерно от 1 до примерно 10 растворителя. Температура сушки может составлять от около 0 ° C до около 300 ° C. В некоторых вариантах осуществления температура сушки может составлять около 25 ° C. Давление отжига может составлять от около 300,1 бар до около 10 бар. Среда отжига может включать по меньшей мере один газ, содержащий воздух, азот, кислород, аргон или гелий.Среда отжига может включать газы азота и кислорода в некоторых вариантах осуществления, где отношение газообразного азота к газообразному кислороду может составлять от примерно 1 до примерно 10 газообразный азот: от примерно 1 до примерно 10 газообразный кислород. Температура отжига может быть больше примерно 1000 ° C и меньше примерно 1450 ° C. Скорость линейного изменения для достижения температуры отжига может составлять примерно 5 ° C / минуту. Время выдержки или время отжига может составлять от примерно 1 минуты до примерно 12 часов. Среда отжига может включать примерно 5 об.% и примерно 100% по меньшей мере одного восстановительного газа. Восстановительный газ может быть монооксидом углерода. В некоторых вариантах осуществления материал носителя катализатора можно измельчить. Материал носителя катализатора может быть смешан со вторым растворителем с образованием суспензии или пасты. Второй растворитель может быть по меньшей мере одним из следующих: метиловый спирт, пентан, толуол, гептан, ацетон, хлороформ или гексан. Отношение измельченного материала носителя к растворителю может составлять от примерно 1 до примерно 10 от измельченного материала носителя до примерно от 1 до примерно 10 от второго растворителя.Суспензию или пасту можно сушить при температуре от примерно 0 ° C до примерно 300 ° C.
В некоторых вариантах реализации в первую смесь можно включить по меньшей мере одну легирующую присадку. Легирующая добавка может представлять собой стронций, магний, индий, бор, алюминий или галлий. В некоторых вариантах реализации примерно от 0 мас. % и примерно 100 мас. % участника, вносящего алюминий (или участника, вносящего бор), может быть заменен дополнительным участником. Дополнительным вкладчиком может быть как минимум один из Ga 2 O 3 , In 2 O 3 , B 2 O 3 или оксид алюминия.В некоторых вариантах осуществления материал носителя катализатора может иметь формулу B7C2A3, оксид бария, кальция и бора, BA или B2CA или может быть замещен, как объясняется ниже.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙРИС. 1 показана картина дифракции рентгеновских лучей от номинального материала B2CA ((BaO) 2 (CaO) (Al 2 O 3 ), барий-кальций-оксид алюминия). Это показывает, что материал на самом деле представляет собой смесь B7C2A3 ((BaO) 7 (CaO) 2 (Al 2 O 3 ) 3 ) и BA ((BaO) (Al 2 O 3 ) фаз.
РИС. 2 иллюстрирует картину дифракции рентгеновских лучей материала оксида бария кальция и бора. Он показывает, что материал в основном представляет собой (BaO) 2 (CaO) (B 2 O 3 )
РИС. Фиг.3 иллюстрирует картины дифракции рентгеновских лучей электрически изолирующих и электропроводящих порошков оксида бария-кальция-алюминия.
РИС. 4 показана номинальная температура катализатора и скорость синтеза NH 3 как функция потока реагентов для катализатора, состоящего из 1 мас.% Ru на номинальном носителе B2CA.
РИС. 5 иллюстрирует возможности катализатора NH 3 для порошков оксида бария, кальция, бора и оксида бария, кальция, алюминия, каждый из которых украшен 1 мас.% Ru.
РИС. Фиг.6 иллюстрирует картину дифракции рентгеновских лучей материала оксида бария-кальция-алюминия после отжига реагентов при 1300 ° C в 1: 1 N 2 : O 2 в течение 6 часов.
РИС. 7 иллюстрирует способность к синтезу NH 3 порошка носителя из оксида бария-кальция-алюминия, украшенного 0.5 мас.% Ru.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯНастоящее изобретение направлено на керамический катализатор на носителе и материалы, используемые в нем, а также на способ использования катализатора на носителе для получения NH 3 . Также предложены способы изготовления керамического носителя и катализатора на керамическом носителе.
В данном контексте «BCA» означает материал из оксида алюминия, кальция, бария. Когда используется формула B # C # A #, используется обозначение химического состава цемента. В этом обозначении B = BaO, C = CaO, A = Al 2 O 3 , а число после каждого материала обозначает количество этих химических единиц в стехиометрическом составе материала.Таким образом, B7C2A3 обозначает (BaO) 7 (CaO) 2 (Al 2 O 3 ) 3 или Ba 7 Ca 2 Al 6 O 18 . Точно так же «BA» означает (BaO) (CaO) или BaCaO 2 .
Синтез материала носителя катализатораОксид бария, кальция и алюминия (BCA) не является широко синтезируемым материалом. Алюминаты кальция — это обычно синтезируемые материалы, используемые для изготовления цемента. Алюминаты бария также синтезируются для некоторых применений, таких как газопоглотители кислорода и огнеупорные цементы, но они менее распространены.
Настоящее изобретение направлено на масштабируемый способ получения порошка оксида бария-кальция-алюминия. Вкладчик бария, вкладчик кальция и вкладчик алюминия объединяются для получения порошка оксида бария-кальция-алюминия. Подходящие составляющие бария могут включать карбонат бария, гидроксид бария, гидрат гидроксида бария, нитрат бария, оксид бария, изопропоксид бария и их комбинации. Подходящие компоненты, вносящие кальций, могут включать карбонат кальция, гидроксид кальция, гидрат гидроксида кальция, оксид кальция, метоксид кальция и их комбинации.Подходящие компоненты алюминия могут включать оксид алюминия, изопропоксид алюминия и их комбинации. Вкладчик бария, вкладчик кальция и / или вкладчик алюминия могут быть в форме порошка, растворов или их комбинаций. Вкладчики бария, кальция и алюминия могут быть объединены в различных молярных соотношениях с образованием порошка. Молярное соотношение может составлять от примерно 1 до примерно 10 вкладчиков бария: от примерно 1 до примерно 10 вкладчиков кальция: от примерно 1 до примерно 10 вкладчиков алюминия.Только в качестве примера, молярное соотношение материалов может составлять 2,0 BaCO 3 : 1,0 CaCO 3 : 1,0 Al 2 O 3 . Другие молярные отношения с другим вкладом бария, кальция или алюминия могут быть использованы без отклонения от изобретения. Различные молярные соотношения вкладчика бария: вкладывающего кальция: реагенты, вносящие вклад в алюминий, могут использоваться для получения материалов из оксида бария, кальция и алюминия с различной стехиометрией или многофазных смесей. Многофазные смеси могут включать оксид бария-кальция-алюминия, оксид бария-алюминия, оксид кальция-алюминия, оксид бария, оксид кальция и оксид алюминия.Порошок также может включать комбинации различных смесей, например, более одного компонента кальция. Порошок также может включать случайные материалы. Соотношение и, в конечном итоге, конечный продукт можно определить на основе конечного использования носителя и катализатора. Специалист в данной области может определить наилучший конечный продукт и, следовательно, наилучшее соотношение для конкретного носителя и катализатора, измерив производительность синтеза NH 3 материала BCA, украшенного рутением, чтобы определить наивысшую скорость синтеза аммиака.В некоторых вариантах реализации материалы с высоким содержанием B7C2A3 или (BaO) 7 (CaO) 2 (Al 2 O 3 ) 3 , могут давать самые высокие скорости синтеза NH 3 .
Участвующие материалы могут быть измельчены с использованием любого подходящего метода, включая дробящие шарики, молотковые мельницы, вальцовые мельницы или их комбинации. Измельченный материал можно измельчить в присутствии растворителя или смешать с растворителем после измельчения с образованием суспензии или пасты.Растворителем может быть безводный растворитель, например метиловый спирт, пентан, толуол, гептан, ацетон, хлороформ, гексан и их комбинации. В некоторых вариантах реализации объемное отношение порошковой смеси к растворителю может составлять от примерно 1 до примерно 10 порошка к примерно от 1 до примерно 10 растворителя. Суспензия или паста могут быть смешаны с использованием подходящих средств, включая шаровую мельницу, валковую мельницу, шнековое перемешивание, лопастное перемешивание или их комбинации. Суспензию или пасту можно высушить для удаления растворителя.Сушка может происходить при комнатной температуре или может происходить при температуре от примерно 0 ° C до примерно 300 ° C, что может зависеть от давления и температуры испарения растворителя. Растворитель может иметь давление пара, достаточно низкое, чтобы работать с ним для образования суспензии или пасты, но достаточно высокое, чтобы он быстро испарялся во время этапов сушки. Смешанный высушенный порошок можно фильтровать или просеивать для удаления крупных частиц (т.е. частиц размером более 25 микрон) и любых измельчающих материалов, используемых для смешивания или измельчения порошка.
Смешанный сухой порошок можно отжигать. Когда неоксидный материал используется в качестве источника бария, кальция или алюминия, неоксидные материалы могут разлагаться до BaO, или CaO, или Al 2 O 3 при повышенных температурах. Профиль отжига можно регулировать, чтобы дать реагентам время для разложения до оксидной формы перед нагреванием до температуры твердофазной реакции для синтеза оксида бария-кальция-алюминия. Следует проявлять осторожность с гидроксидом и гидратированными реагентами, чтобы вода, выделяющаяся из реагентов, не конденсировалась в тех частях печи, где она может вызвать повреждение.Отжиг может быть непрерывным или периодическим. Давление отжига может составлять от 0,1 до 10 бар. В некоторых вариантах отжиг может происходить при атмосферном давлении. Средой отжига может быть воздух, чистый азот, чистый кислород в инертной среде (например, аргон, гелий, азот, другие газы, которые не реагируют с материалами-вкладчиками легче, чем кислород) или их комбинации. В некоторых вариантах осуществления среда может представлять собой атмосферу N 2 : O 2 , где отношение газообразного азота к газообразному кислороду составляет от примерно 1 до примерно 10 газообразный азот: от примерно 1 до примерно 10 газообразный кислород.В некоторых вариантах реализации отношение газообразного азота к газообразному кислороду может составлять примерно 1: 1. Расход газа зависит от конкретного оборудования для отжига, размера партии и используемых материалов. Соответствующий расход для конкретной установки может определить специалист в данной области. Например, скорость потока газа через трубчатую печь с внутренним диаметром 3 дюйма, содержащую от 1 до 500 г карбонатов, может составлять около 500 кубических сантиметров в минуту. Газы не участвуют в чистой реакции синтеза оксида алюминия-бария-кальция; скорее они уносят CO 2 , который выделяется при прокаливании карбонатного реагента, или другие газы, которые выделяются при разложении других материалов (например, воды, выделяющейся из гидроксидов или гидратов).
Процедура отжига может выполняться со скоростью линейного изменения от более чем примерно 0 ° С / мин до примерно 600 ° С / минуту, в некоторых вариантах реализации со скоростью линейного изменения примерно 5 ° С / мин. Максимальная скорость линейного изменения может быть определена сочетанием надежности оборудования и скорости выделения газов из материалов, участвующих в процессе. Наклонные материалы, которые слишком быстро выделяют воду, могут сломать оборудование, если они конденсируются в определенных местах на оборудовании. Специалисты в данной области техники поймут, что эти переменные необходимо учитывать при определении подходящей скорости линейного изменения.Температура может быть повышена до температуры отжига от примерно 1000 ° C до примерно 1450 ° C. Температура не должна превышать примерно 1450 ° C, поскольку эта температура приближается к температуре плавления смешанного высушенного порошка. В некоторых вариантах реализации температура отжига может составлять примерно 1200-1300 ° C. Смешанный высушенный порошок может выдерживаться при температуре отжига от примерно 1 минуты до примерно 12 часов, в некоторых вариантах реализации примерно 6 часов. В некоторых вариантах реализации время отжига может составлять от примерно 1 часа до примерно 7 часов.В некоторых вариантах осуществления отжиг может включать последовательные выдержки при промежуточных температурах до достижения конечной температуры выдержки. Время отжига также может зависеть от количества отжигаемого порошка. Например, если конечная температура составляет около 900 ° C, процесс отжига может включать выдержку при температуре около 150 ° C, затем около 300 ° C, затем около 500 ° C и так далее до конечной температуры достигается примерно 900 ° C. Носитель можно поддерживать при промежуточной температуре от более 0 минут до примерно 15 часов, и время выдержки может быть одинаковым при каждой температуре или может быть различным.В некоторых вариантах осуществления выдержка при промежуточной температуре может составлять от примерно 1 часа до примерно 6 часов. Порошок можно вернуть к комнатной температуре или температуре практической обработки так быстро, как позволяет оборудование. Быстрое охлаждение не повредит порошку, поэтому скорость охлаждения определяется возможностями оборудования и другими практическими соображениями, известными специалистам в данной области. В некоторых вариантах реализации скорость охлаждения примерно до 25 ° C может составлять примерно 5 ° C / мин. Скорость нарастания может быть ограничена скоростью естественного охлаждения печи.Можно использовать более низкие температуры отжига, если время отжига отрегулировано, чтобы гарантировать, что реакция в твердом состоянии завершится. Однако диффузия в твердом состоянии, необходимая для образования оксида бария, кальция и алюминия, является термически активируемым процессом, поэтому требуемое время отжига нелинейно увеличивается при понижении температуры. Более высокие скорости линейного изменения возможны при использовании соответствующего оборудования, хотя скорость линейного изменения может быть ограничена необходимостью в диоксиде углерода, воде или других газах, выделяемых из реагентов, для диффузии из порошков.Повышенное парциальное давление диоксида углерода над материалами, вносящими карбонат, увеличивает температуру, необходимую для обжига. Повышенное парциальное давление воды в печи может вызвать конденсацию воды в более холодных частях печи, что может вызвать повреждение оборудования.
Отожженный материал может быть электроизоляционным порошком. Отожженный материал может быть белого или сине-белого цвета. Материал, который имеет белый оттенок синего цвета, когда его вынимают из печи, становится белым примерно через час на воздухе в помещении.Не желая ограничиваться теорией, этот цвет может быть связан с небольшим количеством воды или диоксида углерода, поступающих в решетку в качестве допанта в концентрациях, слишком малых, чтобы повлиять на кристаллические свойства, но достаточных для небольшого изменения оптических свойств. Структуру отожженного порошка можно исследовать с помощью дифракции рентгеновских лучей. ИНЖИР. 1 иллюстрирует картину дифракции рентгеновских лучей отожженного порошка. Пики в измеренном образце объясняются как наложение пиков для фаз BA и B7C2A3, в которых B = BaO, C = CaO и A = Al 2 O 3 .Это обозначение распространено в химии цемента. Следует отметить, что дифрактограмма для B7C2A3 рассчитывалась только до 2Θ = 52 °. Немаркированные выступающие пики под углами более 2Θ = 52 °, вероятно, связаны с B7C2A3, но не отмечены из-за отсутствия расчетных данных в этой области. Картина B7C2A3 имеет ту же форму, что и картина дифракции рентгеновских лучей B3A (стехиометрически эквивалентна B9A3), но размещение линий смещено из-за того, что CaO заменяет 2/9 BaO.
Отожженный материал можно сделать электропроводным путем отжига в восстановительном газе, таком как монооксид углерода.Преимущественно порошок сохраняет свою кристаллическую структуру после отжига в присутствии восстановительного газа. Отжиг при примерно 5 об. % и около 100% восстановительного газа в течение от около 0,1 часа до около 30 часов, в некоторых вариантах реализации около 15 часов, при температуре отжига от около 600 ° С до около 1100 ° С, в некоторых вариантах реализации около 900 ° С. C. может привести к тому, что порошок (по меньшей мере, примерно от 95% до примерно 100%, в некоторых вариантах осуществления — 100%) будет электропроводящим порошком.Более низкая проводимость может быть вызвана отжигом при более низких температурах и / или меньшем времени. Дополнительную информацию об этом процессе отжига можно найти в публикации патента США № 2017/0253492 (заявка № 15/446929), поданной 1 марта 2017 г., которая полностью включена посредством ссылки.
Отожженный порошок можно измельчить для уменьшения размера частиц порошка и гранул и увеличения площади его поверхности. Отожженный порошок можно измельчить с использованием любого подходящего метода, включая измельчение, измельчение, дробление и их комбинации.Могут выполняться несколько этапов измельчения. В некоторых вариантах осуществления стадии измельчения могут происходить после охлаждения порошка между несколькими стадиями измельчения. Измельченный порошок, который можно агломерировать, может иметь площадь поверхности от примерно 0,5 до примерно 25 м 2 2 г -1 . Отожженный порошок можно объединить с растворителем с образованием суспензии или пасты либо во время измельчения, либо после измельчения. Количество отожженного порошка и растворителя может варьироваться, но его достаточно для приготовления суспензии или пасты.Растворителем может быть безводный растворитель, например метиловый спирт, пентан, толуол, гептан, ацетон, хлороформ, гексан и их комбинации. В некоторых вариантах реализации объемное отношение порошковой смеси к растворителю может составлять от примерно 1 до примерно 10 порошка к примерно от 1 до примерно 10 растворителя. Растворителю можно дать испариться или высохнуть. Сушка может происходить при комнатной температуре или может происходить при температуре от примерно 0 ° C до примерно 300 ° C, в зависимости от температуры испарения и давления растворителя.Например, растворитель может иметь давление пара, которое достаточно низкое, чтобы работать с ним для образования суспензии или пасты, но достаточно высокое, чтобы он быстро испарялся во время этапов сушки. Высушенный порошок (проводящий или изолирующий) можно просеять для удаления крупных частиц (т.е. частиц размером более 25 микрон) и любых измельчающих материалов, используемых для смешивания или измельчения порошка.
В порошок могут входить присадки. Подходящие легирующие добавки могут включать стронций, магний, галлий, индий, бор и их комбинации.Добавки могут быть введены в порошок в виде чистых элементов или в качестве соединений-вкладчиков, таких как оксид стронция, оксид магния, оксид галлия, оксид индия, оксид бора или борная кислота. Доля компонентов порошка (компонент бария, вклад кальция и вклад алюминия), который может быть заменен легирующей добавкой, составляет от примерно 0% до примерно 100% в расчете на атом металла. В некоторых вариантах реализации материалы с одинаковой кристаллической структурой, но с разными постоянными решетки могут быть получены путем замены частей вкладов бария и кальция легирующими добавками стронция и / или магния или заменой частей вкладов алюминия на Ga 2 O 3 , In 2 O 3 , B 2 O 3 , борная кислота или их комбинации
Синтез бариево-кальциево-борно-оксидного катализатора Материал носителяЗамещенный бариево-кальциево-алюминиевый оксидный материал является аспектом изобретения.Некоторые материалы могут быть заменены по меньшей мере частью оксида алюминия, включая оксид бора, Ga 2 O 3 , In 2 O 3 , борную кислоту или их комбинации. Хотя замещение борной кислотой обсуждается очень подробно, специалист в данной области поймет, что по меньшей мере часть оксида алюминия можно заменить другим материалом без отклонения от настоящего изобретения.
Оксид бария-кальция и бора может быть получен способом, описанным для оксида бария-кальция-алюминия, но борной кислотой можно заменить Al 2 O 3 .Картина дифракции рентгеновских лучей для полученного порошка проиллюстрирована на фиг. 2. Это указывает на то, что порошок преимущественно (BaO) 2 (CaO) (B 2 O 3 ) (расчетные пики отмечены). Пики, которые не идентифицированы как (BaO) 2 (CaO) (B 2 O 3 ), в основном могут быть отнесены к небольшим количествам CaO.
Соединение оксида бария-кальция-алюминия-бора может быть синтезировано способом, описанным для оксида алюминия-бария-кальция, путем замены борной кислоты только части Al 2 O 3 .
Вкладчик бария, вкладчик кальция и вкладчик бора объединяются для получения порошка оксида бария, кальция и бора. Подходящие составляющие бария могут включать карбонат бария, гидроксид бария, гидрат гидроксида бария, нитрат бария, оксид бария, изопропоксид бария и их комбинации. Подходящие компоненты, вносящие кальций, могут включать карбонат кальция, гидроксид кальция, гидрат гидроксида кальция, оксид кальция, метоксид кальция и их комбинации. Подходящие компоненты бора могут включать оксид бора, борную кислоту и их комбинации.Вкладчик бария, вкладчик кальция и / или вкладчик бора могут быть в форме порошка, растворов или их комбинаций. Вкладчики бария, кальция и бора могут быть объединены в различных молярных соотношениях для образования порошка. Молярное соотношение может составлять от примерно 1 до примерно 10 вкладчиков бария: от примерно 1 до примерно 10 вкладчиков кальция: от примерно 1 до примерно 10 вкладчиков бора. Только в качестве примера, молярное соотношение материалов может составлять 2.0 BaCO 3 : 1,0 CaCO 3 : 1,0 B 2 O 3 . Другие молярные отношения с другим вкладом бария, кальция или бора могут быть использованы без отклонения от изобретения. Различные молярные соотношения вкладчика бария: вкладывающего вещества кальция: реагенты, вносящие вклад в состав бора, могут использоваться для производства материалов оксида бария, бора, кальция и бора различной стехиометрии или многофазных смесей. Многофазные смеси могут включать оксид бария, кальция, бора, оксид бария, бора, оксид бора и кальция, оксид бария, оксид кальция и оксид бора.Порошок также может включать комбинации различных смесей, например, более одного компонента кальция. Порошок также может включать случайные материалы. Соотношение и, в конечном итоге, конечный продукт можно определить на основе конечного использования носителя и катализатора. Специалист в данной области может определить наилучший конечный продукт и, следовательно, наилучшее соотношение для конкретного носителя и катализатора, измерив производительность синтеза NH 3 материала оксида бария-кальция, бария, украшенного рутением, чтобы определить наивысшую скорость синтеза аммиака.В некоторых вариантах реализации материалы с высоким содержанием (BaO) 7 (CaO) 2 (B 2 O 3 ) 3 могут давать самые высокие скорости синтеза NH 3 .
Участвующие материалы могут быть измельчены с использованием любого подходящего метода, включая шлифовальные круги, молотковые мельницы, валковые мельницы или их комбинации. Измельченный материал можно измельчить в присутствии растворителя или смешать с растворителем после измельчения с образованием суспензии или пасты.Растворителем может быть безводный растворитель, например метиловый спирт, пентан, толуол, гептан, ацетон, хлороформ, гексан и их комбинации. В некоторых вариантах реализации объемное отношение порошковой смеси к растворителю может составлять от примерно 1 до примерно 10 порошка к примерно от 1 до примерно 10 растворителя. Суспензия или паста могут быть смешаны с использованием подходящих средств, включая шаровую мельницу, валковую мельницу, шнековое перемешивание, лопастное перемешивание или их комбинации. Суспензию или пасту можно высушить для удаления растворителя.Сушка может происходить при комнатной температуре или может происходить при температуре от примерно 0 ° C до примерно 300 ° C, что может зависеть от давления и температуры испарения растворителя. Растворитель может иметь давление пара, достаточно низкое, чтобы работать с ним для образования суспензии или пасты, но достаточно высокое, чтобы он быстро испарялся во время этапов сушки. Смешанный высушенный порошок можно фильтровать или просеивать для удаления крупных частиц (т.е. частиц размером более 25 микрон) и любых измельчающих материалов, используемых для смешивания или измельчения порошка.
Смешанный сухой порошок можно отжигать. Когда неоксидный материал используется в качестве источника бария, кальция или бора, неоксидные материалы могут разлагаться до BaO или CaO или B 2 O 3 при повышенных температурах. Профиль отжига можно регулировать, чтобы дать реагентам время для разложения до оксидной формы перед нагреванием до температуры твердофазной реакции для синтеза оксида бария-кальция-бора. Следует проявлять осторожность с гидроксидом и гидратированными реагентами, чтобы вода, выделяющаяся из реагентов, не конденсировалась в тех частях печи, где она может вызвать повреждение.Отжиг может быть непрерывным или периодическим. Давление отжига может составлять от 0,1 до 10 бар. В некоторых вариантах отжиг может происходить при атмосферном давлении. Средой отжига может быть воздух, чистый азот, чистый кислород в инертной среде (например, аргон, гелий, азот, другие газы, которые не реагируют с материалами-вкладчиками легче, чем кислород) или их комбинации. В некоторых вариантах осуществления среда может представлять собой атмосферу N 2 : O 2 , где отношение газообразного азота к газообразному кислороду составляет от примерно 1 до примерно 10 газообразный азот: от примерно 1 до примерно 10 газообразный кислород.В некоторых вариантах реализации отношение газообразного азота к газообразному кислороду может составлять примерно 1: 1. Расход газа зависит от конкретного оборудования для отжига, размера партии и используемых материалов. Соответствующий расход для конкретной установки может определить специалист в данной области. Например, скорость потока газа через трубчатую печь с внутренним диаметром 3 дюйма, содержащую от 1 до 500 г карбонатов, может составлять около 500 кубических сантиметров в минуту. Газы не участвуют в чистой реакции синтеза оксида алюминия-бария-кальция; скорее они уносят CO 2 , который выделяется при прокаливании карбонатного реагента, или другие газы, которые выделяются при разложении других материалов (например, воды, выделяющейся из гидроксидов или гидратов).
Процедура отжига может выполняться со скоростью линейного изменения от более чем примерно 0 ° С / мин до примерно 600 ° С / минуту, в некоторых вариантах реализации со скоростью линейного изменения примерно 5 ° С / мин. Максимальная скорость линейного изменения может быть определена сочетанием надежности оборудования и скорости выделения газов из материалов, участвующих в процессе. Наклонные материалы, которые слишком быстро выделяют воду, могут сломать оборудование, если они конденсируются в определенных местах на оборудовании. Специалисты в данной области техники поймут, что эти переменные необходимо учитывать при определении подходящей скорости линейного изменения.Температура может быть повышена до температуры отжига от примерно 251000 ° C до примерно 1450 ° C. Температура не должна превышать примерно 1450 ° C, поскольку эта температура приближается к температуре плавления смешанного высушенного порошка. В некоторых вариантах реализации температура отжига может составлять примерно 1200-1300 ° C. Смешанный высушенный порошок может выдерживаться при температуре отжига от примерно 1 минуты до примерно 12 часов, в некоторых вариантах реализации примерно 6 часов. В некоторых вариантах реализации время отжига может составлять от примерно 1 часа до примерно 7 часов.В некоторых вариантах осуществления отжиг может включать последовательные выдержки при промежуточных температурах до достижения конечной температуры выдержки. Время отжига также может зависеть от количества отжигаемого порошка. Например, если конечная температура составляет около 900 ° C, процесс отжига может включать выдержку при температуре около 150 ° C, затем около 300 ° C, затем около 500 ° C и так далее до конечной температуры достигается примерно 900 ° C. Носитель можно поддерживать при промежуточной температуре от более 0 минут до примерно 15 часов, и время выдержки может быть одинаковым при каждой температуре или может быть различным.В некоторых вариантах осуществления выдержка при промежуточной температуре может составлять от примерно 1 часа до примерно 6 часов. Порошок можно вернуть к комнатной температуре или температуре практической обработки так быстро, как позволяет оборудование. Быстрое охлаждение не повредит порошку, поэтому скорость охлаждения определяется возможностями оборудования и другими практическими соображениями, известными специалистам в данной области. В некоторых вариантах реализации скорость охлаждения примерно до 25 ° C может составлять примерно 5 ° C / мин. Скорость нарастания может быть ограничена скоростью естественного охлаждения печи.Можно использовать более низкие температуры отжига, если время отжига отрегулировано, чтобы гарантировать, что реакция в твердом состоянии завершится. Однако диффузия в твердом состоянии, необходимая для образования оксида бария, кальция и алюминия, является термически активируемым процессом, поэтому требуемое время отжига нелинейно увеличивается при понижении температуры. Более высокие скорости линейного изменения возможны при использовании соответствующего оборудования, хотя скорость линейного изменения может быть ограничена необходимостью в диоксиде углерода, воде или других газах, выделяемых из реагентов, для диффузии из порошков.Повышенное парциальное давление диоксида углерода над материалами, вносящими карбонат, увеличивает температуру, необходимую для обжига. Повышенное парциальное давление воды в печи может вызвать конденсацию воды в более холодных частях печи, что может вызвать повреждение оборудования.
Отожженный материал может быть электроизоляционным порошком. Отожженный материал может быть белого или сине-белого цвета. Материал, который имеет белый оттенок синего цвета, когда его вынимают из печи, становится белым примерно через час на воздухе в помещении.Не желая ограничиваться теорией, этот цвет может быть связан с небольшим количеством воды или диоксида углерода, поступающих в решетку в качестве допанта в концентрациях, слишком малых, чтобы повлиять на кристаллические свойства, но достаточных для небольшого изменения оптических свойств. Структуру отожженного порошка можно исследовать с помощью дифракции рентгеновских лучей.
Отожженный материал можно сделать электропроводным путем отжига в восстановительном газе, таком как монооксид углерода. Преимущественно порошок сохраняет свою кристаллическую структуру после отжига в присутствии восстановительного газа.Отжиг при примерно 5 об. % и около 100% восстановительного газа в течение от около 0,1 часа до около 30 часов, в некоторых вариантах реализации около 15 часов, при температуре отжига от около 600 ° С до около 1100 ° С, в некоторых вариантах реализации около 900 ° С. C. может привести к тому, что порошок (по меньшей мере, примерно от 95% до примерно 100%, в некоторых вариантах осуществления — 100%) будет электропроводящим порошком. Более низкая проводимость может быть вызвана отжигом при более низких температурах и / или меньшем времени. Дополнительную информацию об этом процессе отжига можно найти в U.S. Публикация патента № 2017/0253492 (заявка № 15/446 929), поданная 1 марта 2017 г., которая полностью включена посредством ссылки.
Отожженный порошок можно измельчить, чтобы уменьшить размер частиц порошка Гранулы песка и увеличить его площадь поверхности. Отожженный порошок можно измельчить с использованием любого подходящего метода, включая измельчение, измельчение, дробление и их комбинации. Могут выполняться несколько этапов измельчения. В некоторых вариантах осуществления стадии измельчения могут происходить после охлаждения порошка между несколькими стадиями измельчения.Измельченный порошок, который может быть агломерирован, может иметь площадь поверхности от примерно 100,5 до примерно 25 м 2 2 г -1 Отожженный порошок может быть объединен с растворителем с образованием суспензии или пасты либо во время измельчения, либо после него. измельчение. Количество отожженного порошка и растворителя может варьироваться, но его достаточно для приготовления суспензии или пасты. Растворителем может быть безводный растворитель, например метиловый спирт, пентан, толуол, гептан, ацетон, хлороформ, гексан и их комбинации.В некоторых вариантах реализации объемное отношение порошковой смеси к растворителю может составлять от примерно 1 до примерно 10 порошка к примерно от 1 до примерно 10 растворителя. Растворителю можно дать испариться или высохнуть. Сушка может происходить при комнатной температуре или может происходить при температуре от примерно 0 ° C до примерно 300 ° C, в зависимости от температуры испарения и давления растворителя. Например, растворитель может иметь давление пара, которое достаточно низкое, чтобы работать с ним для образования суспензии или пасты, но достаточно высокое, чтобы он быстро испарялся во время этапов сушки.Высушенный порошок (проводящий или изолирующий) можно просеять для удаления крупных частиц (т.е. частиц размером более 25 микрон) и любых измельчающих материалов, используемых для смешивания или измельчения порошка.
В порошок могут входить присадки. Подходящие легирующие добавки могут включать стронций, магний, галлий, индий, алюминий и их комбинации. Легирующие добавки могут быть введены в порошок в виде чистых элементов или в качестве соединений-вкладчиков, таких как оксид стронция, оксид магния, оксид галлия, оксид индия или оксид алюминия.Доля компонентов порошка (компонент бария, вклад кальция и вклад бора), которые могут быть заменены легирующей добавкой, составляет от примерно 0% до примерно 100% в расчете на атом металла. В некоторых вариантах реализации материалы с одинаковой кристаллической структурой, но с разными постоянными решетки могут быть получены путем замены частей вклада бария и кальция легирующими добавками стронция и / или магния или заменой частей вклада бора на Ga 2 O 3 , In 2 O 3 , Al 2 O 3 или их комбинации.
Способ украшения материалов подложки каталитическим металлом
Аспектом настоящего изобретения является способ украшения материала подложки и получаемая в результате декорированная подложка. В настоящем изобретении можно использовать метод начальной влажности, метод шаровой мельницы или метод влажной пропитки для украшения материалов носителя каталитическим металлическим материалом. Начальная влажность и способы измельчения в шаровой мельнице описаны в заявке на патент США сер. № 15 / 446,929, подана 30 марта.1, 2017, который полностью включен сюда посредством ссылки.
Поддерживающие материалы могут быть в нескольких формах. Например, материал носителя может быть рассыпчатым порошком, порошком, диспергированным на глиноземной крошке, порошком, приклеенным к механической основе, или порошком, спрессованным в гранулы с использованием пресса (например, таблеточного пресса). Подложка может представлять собой гранулу, которую можно изготавливать, сначала изготавливая гранулы, а затем измельчая и просеивая их.
Материалы подложки и способы изготовления материалов подложки по настоящему изобретению были описаны очень подробно и могут включать различные формы BCA или замещенный BCA материал.
Металлический катализатор может украшать подложку (т.е. наноситься на поверхность подложки). Катализатор может включать, без ограничения, оксид металла, нитрид металла (например, нитрид кобальта и молибдена), металл (включая промотированное железо), катализатор, промотированный щелочью, и их комбинации. В некоторых вариантах реализации катализатор может быть оксидом металла, например оксидом железа. В некоторых вариантах реализации катализатор может содержать металл, например любой металл группы VIII, такой как рутений, железо, осмий, никель, палладий, платина или их комбинации.В некоторых вариантах реализации катализатор может представлять собой катализатор на основе оксида металла, активированного щелочью, например катализатор на основе оксида железа и калия. В некоторых вариантах реализации катализатор может быть металлическим катализатором, активированным щелочью, например, металлическим Ru, активированным Cs. «Промотированный» катализатор относится к катализатору, к которому был добавлен другой материал, в результате чего катализатор имеет более высокую активность. В случае катализаторов NH 3 к катализатору часто добавляют щелочные металлы (Cs, K, Na и т.д.) в элементарной или сложной форме, например Ru или Fe, для увеличения активности Ru или Fe.Обычно щелочные металлы сами по себе не катализируют синтез NH 3 ; скорее эти металлы оптимизируют Fe и Ru.
Методика начального увлажнения
Аспектом настоящего изобретения является способ декорирования материала основы и получаемая в результате декорированная основа. Начальная влажность — это обычный метод декорирования, при котором соединение металла растворяют в растворителе с образованием раствора, порошок носителя смачивают этим раствором, растворителю дают испариться из порошка носителя, а затем оставшееся диспергированное соединение металла обрабатывают. превращены в металл при соответствующем отжиге, известном специалистам в данной области техники.Например, карбонил Ru можно превратить в Ru или оксид Ru путем отжига до примерно 250 ° C либо в инертной, либо в кислородсодержащей атмосфере. Гидрат RuCl 3 можно превратить в оксид Ru или металлический Ru аналогичным образом путем отжига при 450 ° C.
Растворитель, используемый в этом способе для украшения материала носителя, будет зависеть от материала, растворенного в растворителе. Таким образом, невозможно составить исчерпывающий список растворителей. Однако оптимально, чтобы растворяемый материал был хорошо растворим в растворителе, и растворитель быстро испарялся в условиях процесса.Кроме того, для достижения желаемых результатов можно изменять температуру и атмосферу. В некоторых вариантах осуществления процесс декорирования можно проводить при комнатной температуре, и растворитель может быть неводным растворителем (поскольку эти материалы будут гидратироваться или изменять фазу при использовании водного раствора). В общем, неводные растворители обычно могут использоваться с металлоорганическими соединениями, тогда как соли желаемого металла, которые обладают высокой растворимостью в воде, обычно могут использовать водные растворители. Однако в любом случае растворитель также должен быть совместим с материалом носителя.Все поддерживающие порошки являются цементирующими добавками и, таким образом, изменяются водой. Таким образом, неводный растворитель должен использоваться для отделки Ru на начальной стадии увлажнения. Карбонил Ru и RuCl 3 плохо растворяются в органических растворителях, что увеличивает количество растворителя, которое необходимо использовать и испарять. Количество каталитического соединения, которое будет давать желаемый вес.% Каталитического металла для количества обрабатываемого материала носителя, может быть растворено в растворителе. Количество используемого растворителя может быть по крайней мере достаточным для полного растворения каталитического соединения.Количество используемого растворителя может быть больше минимума, необходимого для растворения каталитического соединения, если это способствует более равномерному смачиванию материала носителя. Оптимальное количество растворителя и концентрация каталитического соединения в растворителе будут зависеть от конкретных свойств материала носителя (площадь поверхности на грамм, шероховатость поверхности, пористость и т. Д.) И могут определяться в каждом конкретном случае. специалистами в данной области техники.
Дисперсия катализатора — это процентное содержание атомов катализатора, находящихся на свободной поверхности и, таким образом, способных взаимодействовать с реагентами.Дисперсия катализатора может составлять от примерно 0,1% до примерно 90%, в некоторых вариантах реализации от примерно 0,1% до примерно 50%. Дисперсия катализатора, составляющая примерно 40-60% дисперсии, в некоторых вариантах реализации примерно 50% дисперсии, соответствует островкам катализатора с наибольшим диаметром от примерно 2 нм до примерно 5 нм.
Носители, украшенные катализатором, в диапазоне от примерно 0,5 мас. % до примерно 20 мас. % металлического катализатора, в некоторых вариантах осуществления можно использовать Ru. В некоторых вариантах реализации носители, украшенные катализатором, могут находиться в диапазоне от 0.05 вес. % металла до примерно 5 мас. % металла. В общем, дисперсия металла уменьшается после критического значения масс. % металла превышается, потому что металл начинает образовывать более крупные островки вместо маленьких (т.е. наибольшая длина составляет от примерно 1 нм до примерно 5 нм), что более желательно. Кроме того, количество нанесенного катализатора может зависеть от материала носителя. Изображения, полученные с помощью просвечивающей электронной микроскопии, показывают, что материалы BCA способствуют образованию небольших островков Ru, возможно, из-за взаимодействий Ru-Ba на границе раздела Ru-BCA.Кроме того, хотя загрузка катализатора обычно указывается в мас. %, это количество может ввести в заблуждение при сравнении различных материалов носителя или разных катализаторов, поскольку каждый материал имеет разную молекулярную массу. Например, железо (молекулярная масса около 55,85) намного легче рутения (молекулярная масса около 101,1), поэтому носитель с 1 мас. % Fe будет иметь намного больше атомов катализатора, чем один с 1 вес. % RU. В конце концов, оптимальная загрузка катализатора определяется эмпирически. Например, если идет от 1 вес.% Ru до 2 мас. % Ru увеличивает активность только на 25%, может быть более экономичным может быть использование 25% больше 1 мас. Опора, украшенная% Ru в реакторе.
Способ измельчения на шаровой мельнице
Аспект изобретения направлен на способ декорирования порошков носителя металлическим катализатором, таким как Ru. Рутений будет обсуждаться очень подробно, хотя понятно, что другие катализаторы или промотированные катализаторы могут быть использованы с этим способом без отклонения от изобретения. Порошки карбонила Ru или гидрата RuCl 3 добавляют к порошку носителя вместе с достаточным количеством органического растворителя, неограничивающими примерами являются ацетон или гептан, чтобы получить рыхлую пасту.Количество используемого каталитического соединения определяется желаемым масс.% Каталитического металла на готовом носителе, декорированном катализатором. Эту пасту измельчают любыми подходящими средствами. Неограничивающие примеры измельчения включают планетарную шаровую мельницу в течение от около 5 минут до около 1 часа, в некоторых вариантах реализации около 30 минут и при скорости от 100 до около 1000 об / мин, в некоторых вариантах реализации около 400 об / мин. Скорость шаровой мельницы может зависеть от модели шаровой мельницы, используемой в процессе.Этот метод разрушает соединение Ru и диспергирует его на порошке носителя, не требуя полного растворения катализатора в растворителе. Измельченная паста подложки Ru + может быть подвергнута обжигу или отжигу с использованием способов и параметров, известных специалистам в данной области техники для конкретного соединения металла, чтобы преобразовать соединение Ru в металлический Ru или оксид Ru. Гидрат RuCl 3 является предпочтительным соединением Ru, поскольку он намного дешевле, чем карбонил Ru.
Хотя с помощью этого метода можно получить высокодисперсный Ru, в некоторых вариантах реализации дисперсия от более примерно 0% до примерно 90%, он также может привести к тому, что проводящий опорный порошок станет непроводящим, вероятно, из-за повреждения поверхности порошка. частицы.Воздействие на порошки электропроводящего носителя соединения Ru и растворителя без измельчения не приводит к снижению его проводимости, а измельчение порошков проводящего носителя без соединения Ru действительно снижает его проводимость. Порошок по-прежнему сохраняет свой темный цвет и, следовательно, по-прежнему является электропроводящим сердечником, окруженным более изолирующей оболочкой, которая может быть подходящей для улучшения синтеза NH 3 .
Изолирующая оболочка может быть полезной для улучшенного электрического синтеза Haber-Bosch NH 3 , поскольку она позволяет использовать отожженный CO порошок в режиме электрического поля, поскольку изолирующий порошок не будет закорачивать пластины конденсатора.Если изоляционная оболочка по-прежнему сохраняет свойства, способствующие активации N 2 , это может быть полезно.
Способ влажной пропитки
Аспектом изобретения является влажная пропитка носителя катализатора. Украшение металлической подложки катализатора влажной пропиткой включает растворение соединения металла в растворителе с образованием раствора. Количество используемого каталитического соединения определяется желаемым вес.% Металла катализатора в конечном носителе, украшенном катализатором. Количество используемого растворителя должно быть, по крайней мере, достаточным для растворения количества каталитического соединения.Можно использовать большие объемы растворителя, чтобы гарантировать, что носитель катализатора может быть полностью покрыт раствором и что носитель катализатора может быть легко перемешан. Смесь можно периодически перемешивать, перемешивать или аналогичным образом перемешивать для циркуляции растворенного соединения металла вокруг материала носителя. Растворенное соединение металла откладывается на доступных для раствора поверхностях материала носителя. Изменение цвета раствора может указывать на то, что металл перешел из растворителя в носитель.Раствору можно дать возможность испариться или декорированный материал носителя (т.е. порошок носителя-катализатора) можно удалить из раствора. После того, как декорированный материал носителя удален из раствора, диспергированное соединение металла на его поверхностях может быть преобразовано в металл с помощью соответствующего отжига, известного специалистам в данной области техники. Например, карбонил Ru можно превратить в Ru или оксид Ru путем отжига при температуре от около 150 ° C до около 450 ° C, в некоторых вариантах реализации около 250 ° C., в инертной или кислородсодержащей атмосфере. Температуру отжига можно постепенно повышать до конечной температуры отжига и поддерживать при промежуточной температуре более примерно 0 часов и менее примерно 12 часов. В некоторых вариантах осуществления промежуточная температура поддерживается от около 30 секунд до около 2 часов. В качестве альтернативы, температура отжига может быть увеличена до конечной температуры отжига со скоростью 0-600 ° C / минуту. В некоторых вариантах реализации гидрат RuCl 3 может быть превращен в оксид Ru или металлический Ru аналогичным образом путем отжига в окислительной, инертной или восстановительной атмосферах.Конкретный профиль отжига, температуры и атмосфера будут зависеть от того, должно ли каталитическое соединение превращаться в металл, оксид или другое соединение. Например, гидрат RuCl 3 можно превратить в металлический рутений путем отжига в атмосфере водорода до температуры от примерно 200 ° C до примерно 500 ° C. Затем металлический Ru можно превратить в оксид путем изменения атмосферы отжига. от водородного к кислородному.
Растворитель, используемый в способе декорирования материала носителя, будет зависеть от материала, растворенного в растворителе.Растворитель также должен быть совместим с материалом носителя. Таким образом, невозможно составить исчерпывающий список растворителей. Однако лучше всего, чтобы растворяемый материал был хорошо растворим в растворителе и чтобы растворитель быстро испарялся в условиях процесса. Температуру раствора можно регулировать таким образом, чтобы каталитическое соединение растворялось более легко, или для увеличения растворимости каталитического соединения в растворителе, или для изменения скорости испарения растворителя. Атмосферу над раствором можно контролировать для предотвращения воспламенения растворителя, если его температура вспышки ниже желаемой температуры процесса.Замкнутая атмосфера также может использоваться для подавления испарения растворителя. В некоторых вариантах осуществления процесс декорирования можно проводить при комнатной температуре на воздухе, и растворитель может быть неводным растворителем (поскольку обсуждаемые здесь материалы будут гидратироваться или менять фазу при использовании водного раствора).
Дисперсия катализатора — это процентное содержание атомов катализатора, находящихся на свободной поверхности и, таким образом, способных взаимодействовать с реагентами. Дисперсия катализатора, составляющая примерно 40-60% дисперсии, в некоторых вариантах реализации примерно 50% дисперсии, соответствует островкам катализатора между примерно 1 нм и примерно 5 нм на самой большой длине.Измерения хемосорбции водорода отожженного порошка BCA, декорированного Ru, показали, что дисперсия Ru составляет около 20%. По данным просвечивающей электронной микроскопии, диаметр Ru составляет 5 нм или меньше.
Количество нанесенного катализатора может зависеть от материала носителя. Некоторые материалы способствуют образованию множества небольших островков (т.е. менее 50 нм, более примерно 1 нм и менее примерно 40 нм в некоторых вариантах реализации) катализатора при высокой загрузке катализатора, в то время как другие способствуют образованию более крупных островков (т.е.е. более 50 нм, в некоторых вариантах реализации от примерно 60 нм до примерно 100 мкм) по мере увеличения нагрузки. Многие небольшие островки обычно лучше используют каталитический материал, потому что они имеют более высокую дисперсию (т. Е. Большее количество атомов подвергается воздействию реагентов, а не окружено другими атомами каталитического материала внутри островка), в то время как меньшее количество более крупных островков приводит к низкой дисперсии и плохому использованию материал катализатора. Изображения, полученные с помощью просвечивающей электронной микроскопии, показывают, что материалы BCA способствуют образованию небольших островков Ru, возможно, из-за взаимодействий Ru-Ba на границе раздела Ru-BCA.Кроме того, хотя загрузка катализатора обычно указывается в мас.%, Это количество может вводить в заблуждение при сравнении различных материалов носителя или разных катализаторов, поскольку каждый материал имеет разную молекулярную массу. Например, железо (молекулярная масса около 55,85) намного легче рутения (молекулярная масса около 101,1), поэтому носитель с 1 мас.% Fe будет иметь намного больше атомов катализатора, чем носитель с 1 мас.% Ru. В конце концов, оптимальная загрузка катализатора определяется эмпирически. Например, если переход от 1 мас.% Ru к 2 мас.% Ru увеличивает активность только на 25%, может быть более экономичным использовать в реакторе 25% больше 1 мас.% Ru декорированного носителя.
Материал основыАспектом изобретения является материал основы. Материал представляет собой оксид бария-кальция-алюминия или замещенный оксид бария-кальция с добавкой или без нее. Материал может быть сформирован описанными здесь способами. В некоторых вариантах реализации по меньшей мере один компонент оксида бария-кальция-алюминия может быть заменен по меньшей мере одним вторичным материалом. Таким образом, в некоторых вариантах реализации по меньшей мере часть бария, кальция или алюминия может быть заменена вторичным материалом.Неограничивающие примеры замещенных оксидов бария-кальция-алюминия включают оксид бария-кальция-бора и оксид бария-кальция-алюминия.
В некоторых вариантах реализации оксид бария, кальция и алюминия может быть украшен каталитическим металлом. В качестве примера, порошок оксида бария-кальция-алюминия, полученный, как описано здесь, катализирует синтез NH 3 , когда он декорирован примерно 0,1 мас. % и примерно 10 мас. % каталитической загрузки металла, в некоторых вариантах реализации между примерно 0,5-1 мас.% каталитической загрузки металла.Менее 0,5 мас.% Ru приводит к снижению скорости синтеза NH 3 . Содержание Ru более 2 мас.% Не может увеличить скорости синтеза NH 3 и существенно увеличивает стоимость порошка, декорированного Ru. В некоторых вариантах реализации порошок алюмината бария-кальция может сам по себе не катализировать синтез NH 3 ; требуется некоторое количество каталитического металла, например Ru.
Барий-кальций-оксид алюминия или замещенный оксид бария-кальция-алюминия может действовать как носитель для любого катализатора NH 3 .Таким образом, хотя украшение Ru подробно обсуждалось и потенциально дает самые высокие скорости синтеза NH 3 , для украшения BCA или BCA-замещенных носителей можно использовать другие катализаторы, включая Mo, Cr, Mn, Fe, Co, Сплавы Mo-Co, Os, Ni, Cu и их комбинации. Скорость синтеза NH 3 может увеличиваться по мере того, как катализатор перемещается вправо в периодической таблице (то есть Cr
Декорированный катализатором порошок алюмината бария-кальция можно использовать в качестве катализатора синтеза NH 3 . Порошок алюмината бария-кальция может быть сформирован в виде слоя катализатора с высокой проводимостью несколькими способами. Требуемая удельная проводимость слоя катализатора будет зависеть от конструкции конкретного реактора.Как правило, слой катализатора должен иметь достаточную проводимость, чтобы перепад давления в слое для расчетного газового потока (а) не влиял отрицательно на скорость реакции и (б) не требовал затрат энергии, которые делают процесс слишком дорогостоящим для будьте практичны.
Аспектом изобретения является способ формования порошка алюмината бария-кальция или порошка замещенного алюмината бария-кальция в гранулы путем экструзии и получаемых гранул. Растворитель может быть объединен с порошком алюмината бария-кальция с образованием «теста» (т.е.е. густая податливая смесь порошка и растворителя). Подходящие растворители включают ацетон, гексан, гептан, минеральное масло, более тяжелые масла и их комбинации. В некоторых вариантах реализации в смесь также может быть включен связующий агент. Связующим агентом могут быть воски, смазки, метилцеллюлоза и их комбинации. Тесто формуют в шарики или другие формы. Растворителю и / или связующему агенту можно дать испариться или его можно высушить для удаления растворителя и / или связующего агента из гранулы, получая тем самым высушенный гранулу.Температуру сушки можно определить по давлению паров растворителя. Форма гранулы может быть любой подходящей формы, включая цилиндр, пирамиду, куб, сферу, лист, кубоид или любую другую желаемую форму.
Аспектом изобретения является способ формирования гранул алюмината бария-кальция с декорированным катализатором путем прессования порошка алюмината бария-кальция или порошка замещенного алюмината бария-кальция в таблеточном прессе или подобном устройстве. Затем гранулы можно использовать «в сжатом состоянии».Гранулы также являются аспектом изобретения.
Аспектом изобретения является способ формирования гранул алюмината бария-кальция путем прессования порошка алюмината бария-кальция или порошка замещенного алюмината бария-кальция в таблеточном прессе или аналогичном устройстве с последующим декорированием поверхности гранул Ru с помощью техники начальной влажности. и / или метод влажной пропитки. Полученные гранулы также являются аспектом изобретения.
Аспектом изобретения является способ образования гранул алюмината бария-кальция или гранул замещенного алюмината бария-кальция путем прессования порошка алюмината бария-кальция или порошка замещенного алюмината бария-кальция с или без порообразователей или агентов, улучшающих текучесть, в таблеточный пресс и полученные гранулы.Пористые агенты или агенты, улучшающие текучесть, могут представлять собой по меньшей мере одно из кукурузного крахмала, муки, целлюлозы, метилцеллюлозы или восков. Отношение порошка к порообразующему или улучшающему текучесть агенту Scan составляет от примерно 1% до примерно 50% по объему порообразователя. Полученные гранулы обжигают в печи с использованием температуры и атмосферы, которые заставляют порообразующие агенты покидать гранулы в виде газа и вызывают спекание гранул порошка алюмината бария-кальция. Это создает пористую, механически прочную гранулу.Температура может составлять от примерно 500 ° C до примерно 1400 ° C, и гранулу можно поддерживать при температуре от примерно 10 минут до примерно 10 часов. Атмосфера может содержать от около 1% до 100% кислорода для преобразования порообразователей в CO 2 при сохранении порошка BCA в его оксидном состоянии. Затем полученные гранулы украшают катализатором методом начальной влажности или методом влажной пропитки.
Аспектом изобретения является способ получения гранул алюмината бария-кальция или гранул замещенного алюмината бария-кальция путем прессования смеси реагентов носителя катализатора с или без порообразующих агентов или агентов, улучшающих текучесть, в таблеточном прессе. и полученные гранулы.Пористые агенты или агенты, улучшающие текучесть, могут представлять собой по меньшей мере одно из кукурузного крахмала, муки, целлюлозы, метилцеллюлозы или восков. Отношение порошка к порообразующему или улучшающему текучесть агенту может составлять от примерно 1% до примерно 50% по объему порообразователя. Полученные гранулы обжигают в печи с использованием температуры и атмосферы, которые заставляют порообразующие агенты выходить из гранул в виде газа, заставляют порошки реагентов реагировать с образованием алюмината бария-кальция и вызывают спекание гранул порошка алюмината бария-кальция.Это создает пористую, механически прочную гранулу. Температура может составлять от примерно 500 ° C до примерно 1400 ° C, и гранулу можно поддерживать при температуре от примерно 10 минут до примерно 10 часов. Атмосфера может содержать от около 1% до 100% кислорода для преобразования порообразователей в CO 2 при сохранении порошка BCA в его оксидном состоянии. Затем полученный шарик декорируют Ru методом начального увлажнения или методом влажной пропитки.
Аспектом изобретения является способ промывания покрытия механической несущей конструкции порошком алюмината бария-кальция или порошком замещенного алюмината бария-кальция и полученное в результате устройство.Механическая опорная конструкция может представлять собой, например, экраны, листы, соты из конструктивно прочного материала. Порошок связывают со структурой путем отжига при температуре от около 300 ° C до около 1400 ° C в течение от около 10 минут до около 10 часов в инертной, окислительной или восстановительной атмосфере. Конкретный состав атмосферы и температура отжига будут зависеть от состава материала несущей конструкции. Например, приклеивание порошка BCA с нанесенным промывочным покрытием к алюминиевой опорной конструкции может включать отжиг при 300 ° C.в восстановительной атмосфере для подавления образования оксида на поверхности алюминия до тех пор, пока частицы порошка BCA не будут связаны с металлом, а затем переход в окислительную атмосферу для пассивирования любых оставшихся свободных поверхностей алюминия. Превышение 400 ° C может привести к расплавлению многих алюминиевых сплавов. Спеченное покрытие декорируется Ru методом начального увлажнения или методом мокрой пропитки.
Аспектом изобретения является способ смывания покрытия механической несущей конструкции порошком алюмината бария-кальция или порошком замещенного алюмината бария-кальция, декорированным катализатором, и полученное в результате устройство.Механическая опорная конструкция может представлять собой, например, экраны, листы, соты из конструктивно прочного материала. Порошок связывают со структурой путем отжига при температуре от около 300 ° C до около 1400 ° C в течение от около 10 минут до около 10 часов в инертной, окислительной или восстановительной атмосфере. Конкретный состав атмосферы и температура отжига будут зависеть от состава материала несущей конструкции. Например, связывание порошка BCA, украшенного катализатором, с нанесенным промыванием, с алюминиевой опорной структурой может включать отжиг при 300 ° C.в восстановительной атмосфере для подавления образования оксида на поверхности алюминия до тех пор, пока частицы порошка BCA не будут связаны с металлом, а затем переход в окислительную атмосферу для пассивирования любых оставшихся свободных поверхностей алюминия. Превышение 400 ° C может привести к расплавлению многих алюминиевых сплавов. Температуру можно выбрать так, чтобы островки катализатора на поверхности порошка алюмината бария-кальция не диффундировали в гранулы порошка (например, между примерно 300 ° C и примерно 700 ° C). Состав атмосферы следует выбирать так, чтобы избежать реакций с катализатором, которые могут привести к образованию летучих каталитических соединений (например,г. хлор или окись углерода в случае катализатора Ru).
Аспектом изобретения является способ диспергирования украшенного катализатором порошка алюмината бария-кальция или порошка замещенного алюмината бария-кальция по поверхности более крупных материалов для получения слоя катализатора с проводимостью примерно в 5-50 раз большей, чем может быть достигнуто с помощью только порошок. Примером крупного материала является зернистость оксида алюминия от 1 до 3 мм. Идеальные материалы будут демонстрировать хорошую адгезию порошка алюмината бария-кальция и не будут ухудшать каталитические свойства порошка алюмината бария-кальция с металлической отделкой.Одним из таких материалов является глиноземная крошка, но также могут быть подходящими другие материалы, включая железную крошку, стальную вату, стеклянную крошку и муллитовую крошку.
Аспектом изобретения является способ диспергирования декорированного катализатором порошка алюмината бария-кальция или порошка замещенного алюмината бария-кальция по поверхности грубодисперсного катализатора NH 3 на основе активированного железа и полученного в результате устройства. Такие катализаторы с активированным железом коммерчески доступны, например AmoMax 10 от Clariant. Диспергирование украшенного металлом порошка алюмината бария-кальция на поверхности катализатора NH 3 с активированным железом обеспечит слой катализатора с высокой проводимостью, содержащий два каталитических материала.Катализаторы в виде порошка и гранул будут работать совместно, чтобы обеспечить более высокую каталитическую активность в более широком диапазоне условий в реакторе, чем любой материал может обеспечить по отдельности.
Аспектом изобретения является способ диспергирования украшенного катализатором порошка алюмината бария-кальция или порошка замещенного алюмината бария-кальция на механической подложке, такой как сетка, соты или лист, и полученное устройство. Порошок, украшенный катализатором, может быть прикреплен к подложке путем покрытия подложки высокотемпературным клеем (например, краской для нержавеющей стали Cotronics DURALCO 6105SP) и разбрызгивания порошка, украшенного катализатором, на краску до ее высыхания.Высохшая краска связывает украшенный катализатором порошок с механической подложкой без необходимости отжига.
Способ использования BCA или BCA-замещенного носителяДекорированный катализатором BCA или BCA-замещенный порошок можно использовать для синтеза NH 3 из смеси 1% -99% водорода в азоте, нагретой до температуры 200 ° C. С и 800 ° С при давлении от 0,1 до 300 атм. Конкретные смеси реагентов, давления, температуры и потоки газа зависят от конкретного устройства, используемого для проведения реакции и извлечения производимого NH 3 , и известны специалистам в области синтеза NH 3 .
ПРИМЕРЫ Пример 1Лабораторный реактор для дифференциальных испытаний использовали для проверки возможности синтеза NH 3 декорированного Ru оксида бария-кальция-алюминия по способу Габера-Боша. Носитель катализатора представлял собой порошок с площадью поверхности около 4 м 2 г -1 , как измерено азотным БЭТ-анализом. Его поверхность была украшена примерно 1 мас. % Ru методом начальной влажности с использованием гидрата RuCl 3 , растворенного в ацетоне.Дисперсия металлического Ru составляла около 20%, как измерено хемосорбцией водорода.
Реактор работал с примерно 1,019 г номинальной декорированной Ru смеси B7C2A3 и BA с примерно 1 мас.% При общем давлении примерно 140 фунтов на кв. Дюйм и соотношении потоков H 2 : N 2 примерно 3: 1. Номинальная температура катализатора измерялась термопарами в металлической оболочке, касающимися держателя катализатора на носителе. Реагенты и катализатор на носителе могли быть ниже этой температуры из-за плохих характеристик поглощения излучения газов-реагентов и низкой теплопроводности носителя катализатора.
Скорость синтеза NH 3 и эталонная температура были измерены для общих потоков реагентов в диапазоне от примерно 3,8 до 23,3 сЛм и показаны на фиг. 4. Скорость синтеза NH 3 увеличивается с увеличением потока реагента, достигая примерно 190 ммоль г -1 ч -1 при общем потоке реагента примерно 23 сЛм. Скорость синтеза NH 3 снижалась, когда общий поток превышал примерно 23 сЛм.
Подобные эксперименты с другими носителями из алюмината бария и кальция алюмината бария показали, что носители с большей долей B7C2A3 работают лучше, чем носители с более низким содержанием.
Сложное соединение барий-кальций-алюминий было получено сверхкритической сушкой, чтобы проверить, связана ли каталитическая способность декорированного Ru оксида бария-кальция-алюминия с NH 3 его кристаллической структурой или его составом. Изопропоксид бария, метоксид кальция и изопропоксид алюминия смешивали в метаноле с получением молярного отношения 2 Ba: 1 Ca: 1 Al. Такое же молярное соотношение реагентов можно использовать для изготовления носителя катализатора B7C2A3 + BA. Смесь нагревали примерно до 265 ° C.в реакторе Парра с образованием сверхкритической смеси.
Клапан на реакторе Парра был открыт, в результате чего растворитель быстро испарился, оставив после себя тонкий порошок, состоящий из соединений бария, кальция и алюминия. Конкретными соединениями, вероятно, являются оксиды, карбонаты, гидроксиды и гидриды, но их трудно идентифицировать точно, потому что они имеют аморфную структуру и, следовательно, не могут быть легко проанализированы с помощью дифракции рентгеновских лучей.
Полученный порошок был декорирован 1 мас.% Ru путем влажной пропитки, и его каталитическая способность NH 3 сравнивалась со способностью 1 мас.% Ru, декорированного B7C2A3 + BA.Два носителя катализатора работали почти одинаково, что позволяет предположить, что кристаллическая структура B7C2A3 + BA не является источником его каталитических свойств NH 3 . Более вероятно, что непосредственная близость соответствующих соотношений Ba, Ca и Al является релевантными факторами.
Пример 2Лабораторный дифференциальный реактор использовали для тестирования каталитической способности NH 3 порошка оксида бария-бора, декорированного Ru. Порошок оксида бария-кальция-бора был декорирован 1 мас.% Ru с использованием влажной пропитки из раствора гидрата RuCl 3 в ацетоне.ИНЖИР. 5 иллюстрирует скорость синтеза NH 3 по сравнению с аналогичным образом приготовленным катализатором на основе 1 мас.% Ru-декорированного оксида бария-кальция-алюминия. В условиях испытаний они работали практически одинаково.
Пример 3Порошок оксида бария-кальция-алюминия, полученный из стехиометрии реагента B3C3A2, как описано в Примере 5, разделяли на два образца. Один был отожжен в смеси 1: 1 N 2 : O 2 , а другой — в 100% CO. Оба отжига проводились при 5 ° C.с линейным изменением температуры до 900 ° C, выдержкой при 900 ° C в течение 15 часов и со скоростью 5 ° C / мин (или медленнее, ограничивается естественной скоростью охлаждения трубчатой печи) до комнатной температуры. Отжиг 1: 1 N 2 : O 2 не вызвал видимых изменений в порошке оксида бария-кальция-алюминия. Отжиг CO преобразовал оксид бария-кальция-алюминия из белого электроизоляционного порошка в серый электропроводящий порошок.
РИС. 3 показаны дифрактограммы рентгеновских лучей обоих порошков (т.е.е. N 2 : O 2 отожженные и CO отожженные). Оба паттерна объясняются наложением паттернов B7C2A3 и BA (см. Пример 5). Дифрактограммы показывают, что отожженный порошок N 2 : O 2 1: 1 и отожженный порошок CO имеют структурное сходство, что позволяет предположить, что изменение цвета и электропроводности связано с созданием кислородных вакансий в материале. а не изменения стехиометрии материалов или кристаллической структуры.Кислородные вакансии являются обычным механизмом электропроводности в оксидных материалах.
Пример 4Барий-кальций-оксид алюминия может быть декорирован Ru влажной пропиткой с использованием гидрата RuCl 3 , растворенного в ацетоне. В контейнер можно добавить достаточный объем ацетона, чтобы обеспечить легкое перемешивание желаемого количества порошка алюмината бария и кальция и полное растворение намеченного количества гидрата RuCl 3 . Объем ацетона может быть достаточным для того, чтобы весь порошок во время перемешивания суспендировался в растворителе.Гидрат RuCl 3 может быть растворен в ацетоне с получением примерно 1 мас.% Ru в порошке оксида бария-кальция-алюминия. Полученный раствор RuCl 3 имел темно-зелено-черный цвет. Порошок оксида бария, кальция и алюминия + раствор RuCl 3 можно периодически перемешивать. Для предотвращения испарения растворителя на емкость между перемешиванием можно накрыть крышку или другую крышку. Когда порошок оседал после каждого перемешивания, цвет раствора становился заметно светлее, а порошок в растворе темнее.Изменение цвета указывает на то, что RuCl 3 осаждается на порошке. После нескольких перемешиваний раствор стал почти прозрачным и светлым, что указывает на то, что практически весь RuCl 3 нанесен на порошок оксида бария-кальция-алюминия. В этот момент ацетону давали возможность испариться из непокрытого контейнера без дальнейшего перемешивания.
После испарения ацетона из порошка, украшенного RuCl 3 , сухой порошок помещали в трубчатую печь для отжига.Он был отожжен в 10% H 2 + 90% N 2 при атмосферном давлении. Профиль отжига был последовательным примерно 1 час выдержек при примерно 150 ° C, примерно 250 ° C, примерно 350 ° C и примерно 450 ° C. Изменение температуры составляло примерно 5 ° C / мин. После выдержки при 450 ° C температура печи увеличивалась до комнатной со скоростью примерно 5 ° C / мин (или медленнее, ограничиваясь естественной скоростью охлаждения трубчатой печи). Было показано, что этот отжиг превращает RuCl 3 в металлический Ru.
Измерения хемосорбции водорода отожженного порошка, декорированного Ru, показали, что дисперсия Ru составляет около 20%.По данным просвечивающей электронной микроскопии, диаметр Ru составляет 5 нм или меньше.
Пример 5Порошки оксида бария, оксида кальция и оксида алюминия объединяли в молярном соотношении 3: 3: 2. В частности, 24,881 г BaO, 9,102 г CaO и 11,035 г Al 2 O 3 помещали в агатовый сосуд планетарной шаровой мельницы объемом 500 мл с 101 г агатовых измельчающих шариков 5 мм и 34 г гептана, чтобы получить суспензия или паста. Эту суспензию или пасту измельчали при 200 об / мин в планетарной шаровой мельнице Retsch PM400 в течение 30 минут для смешивания порошков.После измельчения размольный сосуд перемещали в вытяжной шкаф и открывали, чтобы гептан испарился из суспензии. Сухой порошок и шарики пропускали через грубое сито для удаления шариков. Смешанный сухой порошок отжигали в трубчатой печи в атмосфере 1: 1 N 2 : O 2 . Отжиг состоял из линейного повышения температуры 5 ° C / мин до 1300 ° C, выдержки при 1300 ° C в течение 6 часов и скорости 5 ° C / мин (или меньше, что ограничивается скоростью естественного охлаждения трубчатой печи). рампа до комнатной температуры.Отожженный материал представлял собой белый электроизоляционный порошок.
Структура отожженного порошка была исследована методом дифракции рентгеновских лучей. ИНЖИР. 6 иллюстрирует картину дифракции рентгеновских лучей отожженного порошка. Картина хорошо совпадает с наложением положений пиков B7C2A3 и BA. Положения B7C2A3 не отмечены выше примерно 55 градусов, потому что они не были рассчитаны для больших углов.
Пример 6Оксид бария-кальция-алюминия из Примера 5 декорировали Ru методом начальной влажности с использованием гидрата RuCl 3 , растворенного в ацетоне.Достаточное количество гидрата RuCl 3 растворяли в ацетоне для обеспечения примерно 0,5 мас.% Ru в порошке оксида бария-кальция-алюминия. Раствор RuCl 3 наносили на порошок несколькими порциями, каждая порция обеспечивала ровно столько раствора, чтобы увлажнить порошок, не оставляя стоячих пулов раствора. Ацетону давали полностью испариться, и сухой порошок перемешивали и выравнивали перед каждым нанесением раствора RuCl 3 . После нанесения всего раствора сухой порошок помещали в трубчатую печь для отжига в 10% H 2 + 90% N 2 при атмосферном давлении.Профиль отжига состоял из последовательных 30-минутных выдержек при 100, 200, 300, 400 и 450 ° C. Изменение температуры составляло 5 ° C / мин. После выдержки при 450 ° C температура печи увеличивалась до комнатной со скоростью 5 ° C / мин (или медленнее, ограничиваясь естественной скоростью охлаждения трубчатой печи).
Пример 7Лабораторный реактор для дифференциальных испытаний использовали для проверки возможности синтеза NH 3 оксида бария-кальция-алюминия, декорированного Ru, из Примера 6 в процессе типа Габера-Боша.Носитель катализатора представлял собой порошок размером -45 меш с площадью поверхности около 3,846 м 2 г 1 , как измерено с помощью азотного БЭТ-анализа. Поверхность порошка декорировали 0,5 мас. % Ru методом начальной влажности с использованием гидрата RuCl 3 , растворенного в ацетоне.
Реактор работал с примерно 0,999 г оксида бария-кальция-алюминия, декорированного Ru, при общем давлении 140 фунтов на кв. Дюйм и соотношении потоков 2: 1 H 2 : N 2 . Температура термопар в металлической оболочке, прилегающих к держателю катализатора на носителе, по измерениям, составляет около 575 ° C.и примерно 595 ° С; по оценкам, реагенты и катализатор на носителе были на 100-150 ° C ниже температуры термопары из-за плохих характеристик поглощения излучения газов-реагентов и низкой теплопроводности носителя катализатора.
Скорость синтеза NH 3 , концентрация продуктового газа NH 3 и эталонные температуры были измерены для общих потоков реагентов в диапазоне от 5 стандартных литров в минуту до 30 стандартных литров в минуту; эти данные проиллюстрированы на фиг.7. Скорость синтеза NH 3 увеличивается с увеличением потока реагента, достигая примерно 203 ммоль г -1 ч -1 при примерно 30 стандартных литрах в минуту общего потока реагента.
В дополнение к измерениям общего давления 140 фунтов на кв. Дюйм, показанным на фиг. 7, расход NH 3 был измерен при общем давлении около 2 фунтов на кв. Дюйм (около 1 бара) и составил около 18 ммоль г -1 h -1 . Для сравнения, в промышленных реакторах NH 3 , использующих катализаторы на основе Fe, скорость синтеза NH 3 составляет около 20 ммоль · г -1 ч -1 при температурах около 450 ° C.и давления от около 2000 фунтов на квадратный дюйм до около 4000 фунтов на квадратный дюйм.
В этом документе диапазоны обсуждались и использовались в предыдущих описаниях. Специалист в данной области техники поймет, что любой поддиапазон в указанных диапазонах будет подходящим, как и любое число в широких диапазонах, без отклонения от изобретения.
Приведенные выше описания настоящего изобретения были представлены в целях иллюстрации и описания. Кроме того, описания не предназначены для ограничения изобретения формой, раскрытой в данном документе.Следовательно, вариации и модификации, соизмеримые с вышеизложенными идеями, а также навыки или знания в соответствующей области, находятся в пределах объема настоящего изобретения. Описанные выше варианты осуществления дополнительно предназначены для объяснения лучших способов, известных для практического применения изобретений, и для того, чтобы дать возможность другим специалистам в данной области техники использовать изобретения в таких или других вариантах осуществления и с различными модификациями, необходимыми для конкретных приложений или применений настоящего. изобретения. Подразумевается, что прилагаемая формула изобретения должна быть истолкована как включающая альтернативные варианты осуществления в пределах, допускаемых предшествующим уровнем техники.
Когда твердый оксид бария и алюминий нагреваются до высокая температура, продукты жидкий барий
3. Атом ИЗ Элемент A имеет массовое число 39 и 19 протонов Напишите электронное устройство атома
Q — раствор, содержащий 4,2 г хлороводорода в 250 см³. Если 16,20 см³ Q полностью нейтрализует 25 см³ R (раствор гидроксида натрия). Calcu … поздно а. концентрация щелочей в моль / дм³. б. объем Q, который нейтрализует раствор, содержащий 0.25 моль R в см³. NaOH + HCl ——— NaCl + h3O.
3 примера осмоса у животных
В таблице показан диапазон количества энергии, необходимого для разрыва связей между молекулами вещества в твердом, жидком и газообразном состоянии. … тейтс. Разрывная энергия Государственная энергия P 3 единицы Q 0,01 ед. R 0,1 шт. Что из следующего является правильным порядком относительных сил межмолекулярных сил в трех состояниях? A. P & gt; R & gt; Q (Я думаю, что это, но я не слишком уверен) Б.Q & gt; R & gt; п С. R & gt; Q & gt; п D. P & gt; Q & gt; р
Различают эмперический и молекулярная формула. Приведите пример вещество, имеющее разные эмперические свойства и молекулярная формула
Наибольший общий множитель 26 и 36?
Жидкость нагревается. Марион измерила объем жидкости в начале и в конце эксперимента Марион. Как вы думаете, было меньше, м … руда или тот же объем жидкости в конце, что и в начале? Обоснуйте свой ответ.
Фиксированная масса газа имеет объем 92 см куб и 3 градуса Цельсия. Каким будет его объем при 18 градусах Цельсия, если давление останется постоянным?
Майк собирает оборудование для лаборатории, где он будет измерять массы различных химикаты. Что из следующего является наиболее полным списком электронных … оборудование он будет нужно? электрические весы, мерный цилиндр, пробирка пробирка с градуированным цилиндром, защитные очки Стакан с градуированным цилиндром, пробирка электрические весы, очки, стакан
пожалуйста, ответьте на мой вопрос с объяснением, мой выбор — просто радом
Алюминат бария, техн.| VWR
Положения и условия
Спасибо, что посетили наш сайт. Эти условия использования применимы к веб-сайтам США, Канады и Пуэрто-Рико (далее «Веб-сайт»), которыми управляет VWR («Компания»). Если вы заходите на веб-сайт из-за пределов США, Канады или Пуэрто-Рико, пожалуйста, посетите соответствующий международный веб-сайт, доступный по адресу www.vwr.com, для ознакомления с применимыми условиями. Все пользователи веб-сайта подчиняются следующим условиям использования веб-сайта (эти «Условия использования»).Пожалуйста, внимательно прочтите эти Условия использования перед доступом или использованием любой части веб-сайта. Заходя на веб-сайт или используя его, вы соглашаетесь с тем, что прочитали, понимаете и соглашаетесь соблюдать настоящие Условия использования с поправками, которые время от времени вносятся, а также Политику конфиденциальности компании, которая настоящим включена в настоящие Условия. использования. Если вы не желаете соглашаться с настоящими Условиями использования, не открывайте и не используйте какие-либо части веб-сайта.
Компания может пересматривать и обновлять настоящие Условия использования в любое время без предварительного уведомления, разместив измененные условия на веб-сайте.Продолжение использования вами веб-сайта означает, что вы принимаете и соглашаетесь с пересмотренными Условиями использования. Если вы не согласны с Условиями использования (в которые время от времени вносятся поправки) или недовольны Веб-сайтом, ваше единственное и исключительное средство правовой защиты — прекратить использование Веб-сайта.
Использование сайта
Информация, содержащаяся на этом веб-сайте, предназначена только для информационных целей. Хотя считается, что информация верна на момент публикации, вам следует самостоятельно определить ее пригодность для вашего использования.Не все продукты или услуги, описанные на этом веб-сайте, доступны во всех юрисдикциях или для всех потенциальных клиентов, и ничто в настоящем документе не предназначено как предложение или ходатайство в какой-либо юрисдикции или какому-либо потенциальному покупателю, где такое предложение или продажа не соответствует требованиям.
Приобретение товаров и услуг
Настоящие Условия и положения распространяются только на использование веб-сайта. Обратите внимание, что условия, касающиеся обслуживания, продажи продуктов, рекламных акций и других связанных мероприятий, можно найти по адресу https: // us.vwr.com/store/content/externalContentPage.jsp?path=/en_US/about_vwr_terms_and_conditions.jsp, и эти условия регулируют любые покупки продуктов или услуг у Компании.
Интерактивные функции
Веб-сайт может содержать службы досок объявлений, области чата, группы новостей, форумы, сообщества, личные веб-страницы, календари и / или другие средства сообщения или связи, предназначенные для того, чтобы вы могли общаться с общественностью в целом или с группой ( вместе «Функция сообщества»).Вы соглашаетесь использовать функцию сообщества только для публикации, отправки и получения сообщений и материалов, которые являются надлежащими и относятся к конкретной функции сообщества. Вы соглашаетесь использовать веб-сайт только в законных целях.
A. В частности, вы соглашаетесь не делать ничего из следующего при использовании функции сообщества:
1. Оскорблять, оскорблять, преследовать, преследовать, угрожать или иным образом нарушать законные права (например, право на неприкосновенность частной жизни и гласность) других.
2. Публиковать, размещать, загружать, распространять или распространять любую неуместную, непристойную, дискредитирующую, нарушающую авторские права, непристойную, непристойную или незаконную тему, название, материал или информацию.
3. Загружайте файлы, содержащие программное обеспечение или другие материалы, защищенные законами об интеллектуальной собственности (или правами на неприкосновенность частной жизни), если вы не владеете или не контролируете права на них или не получили все необходимое согласие.
4. Загрузите файлы, содержащие вирусы, поврежденные файлы или любое другое подобное программное обеспечение или программы, которые могут повредить работу чужого компьютера.
5. Перехватить или попытаться перехватить электронную почту, не предназначенную для вас.
6. Рекламировать или предлагать продавать или покупать какие-либо товары или услуги для любых деловых целей, если такая функция сообщества специально не разрешает такие сообщения.
7. Проводите или рассылайте опросы, конкурсы, финансовые пирамиды или письма счастья.
8. Загрузите любой файл, опубликованный другим пользователем функции сообщества, который, как вы знаете или разумно должен знать, не может распространяться на законных основаниях таким образом или что у вас есть договорное обязательство сохранять конфиденциальность (несмотря на его доступность на веб-сайте).
9. Подделывать или удалять любые ссылки на авторов, юридические или другие надлежащие уведомления, обозначения собственности или ярлыки происхождения или источника программного обеспечения или других материалов, содержащихся в загружаемом файле.
10. Предоставление ложной информации о принадлежности к какому-либо лицу или организации.
11. Участвовать в любых других действиях, которые ограничивают или препятствуют использованию веб-сайта кем-либо или которые, по мнению Компании, могут нанести вред Компании или пользователям веб-сайта или подвергнуть их ответственности.
12. Нарушать любые применимые законы или постановления или нарушать любой кодекс поведения или другие правила, которые могут быть применимы к какой-либо конкретной функции Сообщества.
13. Собирать или иным образом собирать информацию о других, включая адреса электронной почты, без их согласия.
B. Вы понимаете и признаете, что несете ответственность за любой контент, который вы отправляете, вы, а не Компания, несете полную ответственность за такой контент, включая его законность, надежность и уместность. Если вы публикуете сообщения от имени или от имени вашего работодателя или другой организации, вы заявляете и гарантируете, что у вас есть на это право. Загружая или иным образом передавая материалы в любую часть веб-сайта, вы гарантируете, что эти материалы являются вашими собственными или находятся в общественном достоянии или иным образом свободны от проприетарных или иных ограничений, и что вы имеете право размещать их на веб-сайте.Кроме того, загружая или иным образом передавая материалы в любую область веб-сайта, вы предоставляете Компании безотзывное, бесплатное право во всем мире на публикацию, воспроизведение, использование, адаптацию, редактирование и / или изменение таких материалов любым способом, в любые и все средства массовой информации, известные в настоящее время или обнаруженные в будущем по всему миру, в том числе в Интернете и World Wide Web, для рекламных, коммерческих, торговых и рекламных целей, без дополнительных ограничений или компенсации, если это не запрещено законом, и без уведомления, проверки или одобрения.
C. Компания оставляет за собой право, но не принимает на себя никакой ответственности (1) удалить любые материалы, размещенные на веб-сайте, которые Компания по своему собственному усмотрению сочтет несовместимыми с вышеуказанными обязательствами или иным образом неприемлемыми по любой причине. ; и (2) прекратить доступ любого пользователя ко всему или части веб-сайта. Однако Компания не может ни просмотреть все материалы до того, как они будут размещены на веб-сайте, ни обеспечить быстрое удаление нежелательных материалов после их размещения.Соответственно, Компания не несет ответственности за какие-либо действия или бездействие в отношении передач, сообщений или контента, предоставленных третьими сторонами. Компания оставляет за собой право предпринимать любые действия, которые она сочтет необходимыми для защиты личной безопасности пользователей этого веб-сайта и общественности; тем не менее, Компания не несет ответственности перед кем-либо за выполнение или невыполнение действий, описанных в этом параграфе.
D. Несоблюдение вами положений пунктов (A) или (B) выше может привести к прекращению вашего доступа к веб-сайту и может повлечь за собой гражданскую и / или уголовную ответственность.
Особое примечание о содержании функций сообщества
Любой контент и / или мнения, загруженные, выраженные или отправленные с помощью любой функции сообщества или любого другого общедоступного раздела веб-сайта (включая области, защищенные паролем), а также все статьи и ответы на вопросы, кроме контента, явно разрешенного Компания, являются исключительно мнениями и ответственностью лица, представляющего их, и не обязательно отражают мнение Компании.Например, любое рекомендованное или предлагаемое использование продуктов или услуг, доступных от Компании, которое публикуется через функцию сообщества, не является признаком одобрения или рекомендации со стороны Компании. Если вы решите следовать какой-либо такой рекомендации, вы делаете это на свой страх и риск.
Ссылки на сторонние сайты
Веб-сайт может содержать ссылки на другие веб-сайты в Интернете. Компания не несет ответственности за контент, продукты, услуги или методы любых сторонних веб-сайтов, включая, помимо прочего, сайты, связанные с Веб-сайтом или с него, сайты, созданные на Веб-сайте, или стороннюю рекламу, и не делает заявлений относительно их качество, содержание или точность.Наличие ссылок с веб-сайта на любой сторонний веб-сайт не означает, что мы одобряем, поддерживаем или рекомендуем этот веб-сайт. Мы отказываемся от всех гарантий, явных или подразумеваемых, в отношении точности, законности, надежности или действительности любого контента на любых сторонних веб-сайтах. Вы используете сторонние веб-сайты на свой страх и риск и в соответствии с условиями использования таких веб-сайтов.
Права собственности на контент
Вы признаете и соглашаетесь с тем, что все содержимое веб-сайта (включая всю информацию, данные, программное обеспечение, графику, текст, изображения, логотипы и / или другие материалы) и его дизайн, выбор, сбор, расположение и сборка являются являются собственностью Компании и защищены законами США и международными законами об интеллектуальной собственности.Вы имеете право использовать содержимое веб-сайта только в личных или законных деловых целях. Вы не можете копировать, изменять, создавать производные работы, публично демонстрировать или исполнять, переиздавать, хранить, передавать, распространять, удалять, удалять, дополнять, добавлять, участвовать в передаче, лицензировать или продавать какие-либо материалы в Интернете. Сайт без предварительного письменного согласия Компании, за исключением: (а) временного хранения копий таких материалов в ОЗУ, (б) хранения файлов, которые автоматически кэшируются вашим веб-браузером в целях улучшения отображения, и (в) печати разумного количество страниц веб-сайта; в каждом случае при условии, что вы не изменяете и не удаляете какие-либо уведомления об авторских правах или других правах собственности, включенные в такие материалы.Ни название, ни какие-либо права интеллектуальной собственности на любую информацию или материалы на веб-сайте не передаются вам, а остаются за Компанией или соответствующим владельцем такого контента.
Товарные знаки
Название и логотип компании, а также все связанные названия, логотипы, названия продуктов и услуг, появляющиеся на веб-сайте, являются товарными знаками компании и / или соответствующих сторонних поставщиков. Их нельзя использовать или повторно отображать без предварительного письменного согласия Компании.
Отказ от ответственности
Компания не несет никакой ответственности за материалы, информацию и мнения, предоставленные или доступные через Веб-сайт («Контент сайта»). Вы полагаетесь на Контент сайта исключительно на свой страх и риск. Компания не несет никакой ответственности за травмы или убытки, возникшие в результате использования любого Контента Сайта.
ВЕБ-САЙТ, СОДЕРЖАНИЕ САЙТА И ПРОДУКТЫ И УСЛУГИ, ПРЕДОСТАВЛЯЕМЫЕ ИЛИ ДОСТУПНЫЕ ЧЕРЕЗ САЙТ, ПРЕДОСТАВЛЯЮТСЯ НА УСЛОВИЯХ «КАК ЕСТЬ» И «ПО ДОСТУПНОСТИ», СО ВСЕМИ ОШИБКАМИ.КОМПАНИЯ И НИ ЛИБО, СВЯЗАННОЕ С КОМПАНИЕЙ, НЕ ДАЕТ НИКАКИХ ГАРАНТИЙ ИЛИ ЗАЯВЛЕНИЙ В ОТНОШЕНИИ КАЧЕСТВА, ТОЧНОСТИ ИЛИ ДОСТУПНОСТИ ВЕБ-САЙТА. В частности, НО БЕЗ ОГРАНИЧЕНИЯ ВЫШЕИЗЛОЖЕННОГО, НИ КОМПАНИЯ И НИ ЛИБО, СВЯЗАННОЕ С КОМПАНИЕЙ, НЕ ГАРАНТИРУЕТ ИЛИ ЗАЯВЛЯЕТ, ЧТО ВЕБ-САЙТ, СОДЕРЖАНИЕ САЙТА ИЛИ УСЛУГИ, ПРЕДОСТАВЛЯЕМЫЕ НА САЙТЕ ИЛИ ЧЕРЕЗ САЙТ, БУДУТ ТОЧНЫМИ, НАДЕЖНЫМИ ИЛИ БЕСПЛАТНЫМИ ИЛИ БЕСПЛАТНЫМИ ЧТО ДЕФЕКТЫ БУДУТ ИСПРАВЛЕНЫ; ЧТО ВЕБ-САЙТ ИЛИ СЕРВЕР, ДЕЛАЮЩИЙ ЕГО ДОСТУПНЫМ, НЕ СОДЕРЖИТ ВИРУСОВ ИЛИ ДРУГИХ ВРЕДНЫХ КОМПОНЕНТОВ; ИЛИ ЧТО ВЕБ-САЙТ ИНАЧЕ ОТВЕЧАЕТ ВАШИМ ПОТРЕБНОСТЯМ ИЛИ ОЖИДАНИЯМ.КОМПАНИЯ ОТКАЗЫВАЕТСЯ ОТ ВСЕХ ГАРАНТИЙ, ЯВНЫХ ИЛИ ПОДРАЗУМЕВАЕМЫХ, ВКЛЮЧАЯ ЛЮБЫЕ ГАРАНТИИ КОММЕРЧЕСКОЙ ЦЕННОСТИ, ПРИГОДНОСТИ ДЛЯ ОПРЕДЕЛЕННОЙ ЦЕЛИ И НЕ НАРУШЕНИЯ.
НИ ПРИ КАКИХ ОБСТОЯТЕЛЬСТВАХ КОМПАНИЯ ИЛИ ЕЕ ЛИЦЕНЗИАРЫ ИЛИ ПОДРЯДЧИКИ НЕ НЕСЕТ ОТВЕТСТВЕННОСТИ ЗА ЛЮБОЙ ВИД ЛЮБОГО ВИДА УБЫТКОВ, ПРИ КАКИХ-ЛИБО ЮРИДИЧЕСКИХ ТЕОРИЯХ, ВЫЗВАННЫХ ИЛИ В СВЯЗИ С ИСПОЛЬЗОВАНИЕМ ВАМИ ИЛИ НЕВОЗМОЖНОСТЬЮ ИСПОЛЬЗОВАТЬ ВЕБ-САЙТ, СОДЕРЖИМОЕ САЙТА, ЛЮБЫЕ УСЛУГИ, ПРЕДОСТАВЛЯЕМЫЕ НА ВЕБ-САЙТЕ ИЛИ ЧЕРЕЗ ВЕБ-САЙТ ИЛИ ЛЮБОЙ САЙТ, ВКЛЮЧАЮЩИЙ ПРЯМЫЕ, КОСВЕННЫЕ, СЛУЧАЙНЫЕ, СПЕЦИАЛЬНЫЕ, КОСВЕННЫЕ ИЛИ КАРАТНЫЕ УБЫТКИ, ВКЛЮЧАЯ, НО НЕ ОГРАНИЧИВАЯСЯ, ЛИЧНЫЕ ТРАВМЫ, ПОТЕРЯ ПРИБЫЛИ ИЛИ УБЫТКОВ , ВИРУСЫ, УДАЛЕНИЕ ФАЙЛОВ ИЛИ ЭЛЕКТРОННЫХ СООБЩЕНИЙ, ИЛИ ОШИБКИ, УПУЩЕНИЯ ИЛИ ДРУГИЕ НЕТОЧНОСТИ НА ВЕБ-САЙТЕ ИЛИ СОДЕРЖАНИИ САЙТА ИЛИ УСЛУГ, ИЛИ ИЛИ НЕ ИСПОЛЬЗУЕТСЯ КОМПАНИЯ, И ПРЕДОСТАВЛЯЛА ЛИ КОМПАНИЯ ВОЗМОЖНОСТЬ ЛЮБЫЕ ТАКИЕ УБЫТКИ, ЕСЛИ НЕ ЗАПРЕЩЕНЫ ПРИМЕНИМЫМ ЗАКОНОДАТЕЛЬСТВОМ.
Компенсация
Вы соглашаетесь возместить и обезопасить Компанию и ее должностных лиц, директоров, агентов, сотрудников и других лиц, участвующих в работе Веб-сайта, от любых обязательств, расходов, убытков и издержек, включая разумные гонорары адвокатам, возникающих в результате любое нарушение вами настоящих Условий использования, использование вами Веб-сайта или любых продуктов, услуг или информации, полученных с Веб-сайта или через него, ваше подключение к Веб-сайту, любой контент, который вы отправляете на Веб-сайт через любые Функция сообщества или нарушение вами каких-либо прав другого лица.
Применимое право; Международное использование
Настоящие условия регулируются и толкуются в соответствии с законами штата Пенсильвания без учета каких-либо принципов коллизионного права. Вы соглашаетесь с тем, что любые судебные иски или иски, вытекающие из настоящих Условий использования или связанные с ними, будут подаваться исключительно в суды штата или федеральные суды, расположенные в Пенсильвании, и вы тем самым соглашаетесь и подчиняетесь личной юрисдикции таких судов для цели судебного разбирательства любого такого действия.
Настоящие Условия использования применимы к пользователям в США, Канаде и Пуэрто-Рико. Если вы заходите на веб-сайт из-за пределов США, Канады или Пуэрто-Рико, пожалуйста, посетите соответствующий международный веб-сайт, доступный по адресу www.vwr.com, для ознакомления с применимыми условиями. Если вы решите получить доступ к этому веб-сайту из-за пределов указанных юрисдикций, а не использовать доступные международные сайты, вы соглашаетесь с настоящими Условиями использования и тем, что такие условия будут регулироваться и толковаться в соответствии с законами США и штата. Пенсильвании и что мы не делаем никаких заявлений о том, что материалы или услуги на этом веб-сайте подходят или доступны для использования в этих других юрисдикциях.В любом случае все пользователи несут ответственность за соблюдение местных законов.
Общие условия
Настоящие Условия использования, в которые время от времени могут вноситься поправки, представляют собой полное соглашение и понимание между вами и нами, регулирующее использование вами Веб-сайта. Наша неспособность реализовать или обеспечить соблюдение какого-либо права или положения Условий использования не означает отказ от такого права или положения. Если какое-либо положение Условий использования будет признано судом компетентной юрисдикции недействительным, вы, тем не менее, соглашаетесь с тем, что суд должен попытаться реализовать намерения сторон, отраженные в этом положении и других положениях Условия использования остаются в силе.Ни ваши деловые отношения, ни поведение между вами и Компанией, ни какая-либо торговая практика не может считаться изменением настоящих Условий использования. Вы соглашаетесь с тем, что независимо от какого-либо закона или закона об обратном, любые претензии или основания для иска, вытекающие из или связанные с использованием Сайта или Условий использования, должны быть поданы в течение одного (1) года после такой претензии или причины. иска возникла или будет навсегда запрещена. Любые права, прямо не предоставленные в настоящем документе, сохраняются за Компанией.Мы можем прекратить ваш доступ или приостановить доступ любого пользователя ко всему сайту или его части без предварительного уведомления за любое поведение, которое мы, по нашему собственному усмотрению, считаем нарушением любого применимого законодательства или наносящим ущерб интересам другого пользователя. , стороннего поставщика, поставщика услуг или нас. Любые вопросы, касающиеся настоящих Условий использования, следует направлять по адресу [email protected].
Жалобы на нарушение авторских прав
Мы уважаем чужую интеллектуальную собственность и просим наших пользователей поступать так же.Если вы считаете, что ваша работа была скопирована и доступна на Сайте способом, который представляет собой нарушение авторских прав, вы можете уведомить нас, предоставив нашему агенту по авторским правам следующую информацию:
электронная или физическая подпись лица, уполномоченного действовать от имени правообладателя;
описание работы, защищенной авторским правом, в отношении которой были нарушены ваши претензии;
идентификация URL-адреса или другого конкретного места на Сайте, где находится материал, который, по вашему мнению, нарушает авторские права;
ваш адрес, номер телефона и адрес электронной почты;
ваше заявление о том, что вы добросовестно полагаете, что спорное использование не разрешено владельцем авторских прав, его агентом или законом; и
ваше заявление, сделанное под страхом наказания за лжесвидетельство, о том, что приведенная выше информация в вашем уведомлении является точной и что вы являетесь владельцем авторских прав или уполномочены действовать от имени владельца авторских прав.
С нашим агентом для уведомления о жалобах на нарушение авторских прав на Сайте можно связаться по адресу: [email protected].
| 3.4.2 Оксидная керамика 3.4.2.1 Оксид алюминия Оксид алюминия (Al 2 O 3 ) является важнейшим техническим оксидным керамическим материалом и имеет широчайший спектр применения.Плотно спеченный алюминий оксид характеризуется
Эти синтетические материалы
с содержанием оксида алюминия от 80% до более
99% проверено на практике. Выбор этого материала
определяется по технико-экономическим критериям. Материал
с более высоким содержанием оксида алюминия не обязательно соответствует
потребности приложения лучше всего. Рисунок 6: Поверхность оксид алюминия «после обжига» Рисунок 7: Микроструктура алюминия
оксидная керамика (99.7%) Материалы из оксида алюминия удовлетворяют всем требованиям требования к изоляционным материалам для применения в электротехнике инженерное дело. Выдающиеся значения прочности на изгиб и устойчивость материала к износу и высоким температурам к механическим приложениям. Микроструктура, а значит и другие свойства керамики из оксида алюминия могут заметно отличаться (см. рисунки 8 и 9).
Поверхности с максимально возможной опорой площадь не всегда либо необходима, либо желательна. Нить направляющие, используемые, например, в текстильной промышленности, должны иметь небольшую площадь контакта с резьбой и не иметь любые острые края, в то время как уплотнительные пластины требуют материала пропорция прибл.80%. Рисунок 10: «В момент срабатывания» поверхность экструдированного оксида алюминия Благодаря хорошему соотношению цена / качество и в целом полезные свойства, применяется керамика оксид алюминия
|
Рост наноостровов наночастиц оксида алюминия бария на поверхности композита Al2O3-MgO: получение и оценка их каталитической активности
Название: Рост наноостровов наночастиц оксида алюминия бария на поверхности композита Al 2 O 3 -MgO: получение и оценка их каталитических свойств. Деятельность
ОБЪЕМ: 11 ВЫПУСК: 1
Автор (ы): Маджид Гашанг, Саид Джаббарзаре, Хамед Таваколи, Хамид Банисадеги, Амир Хосейн Соханвар, Махмод Лотфи и Акбар Чами
Место работы: Отделение химии, факультет наук, Наджафабадское отделение, Исламский университет Азад, Наджафабад, П.О. Ящик: 517, Исфахан, Иран.
Ключевые слова: Al 2 O 3 -MgO композит, BaAl 2 O 4 , оксид бария, 1,4-дигидропиридины, оксид магния.
Abstract: На поверхности Al 2 O 3 -MgO были выращены островки, подобные оксиду бария и алюминия BaAl 2 O 4 наносфер. композит, полученный методом микроэмульсии масло в воде (М / В).Гексан, 2-аминоэтанол и этанол использовали в качестве масляной фазы, неанионное поверхностно-активное вещество и вспомогательное поверхностно-активное вещество соответственно. Синтезированные наносферы Ba Al 2 O 4 были выращены на поверхности композита Al 2 O 3 -MgO и были охарактеризованы с помощью дифракции рентгеновских лучей (XRD), автоэмиссионного сканирующего электронного микроскопия (FE-SEM) и энергодисперсионная рентгеновская спектроскопия (EDAX). Наносферы BaAl 2 O 4 , выращенные на поверхности Композит Al 2 O 3 -MgO проявил высокую каталитическую активность в превращении коричного альдегида, метил / этил ацетоацетат и ароматические амины в качестве исходных материалов для производных 1,4-дигидропиридина.

 O / rBaO / c1-2
O / rBaO / c1-2