Окисление изопропилового спирта — Справочник химика 21
Частичное окисление изопропилового спирта в ацетон при одновременном образовании перекиси водорода можно осуществить в жидкой п в газовой фазе. [c.196]
Уже в настоящее время работают устаповки, в которых полностью отсутствуют отходы (например, установка для получения перекиси водорода). Процесс получения перекиси водорода основан на реакции окисления изопропилового спирта кислородсодержащим газом в жидкой фазе в четыре стадии. Установка отличается простотой аппаратурного оформления, удобством обслуживания. Основное оборудование установки может быть расположено на открытой площадке, что ведет к уменьшению средств на строительство (см. 7.1). [c.206]
В современном производстве перокси водорода применяют реакции с участием органических веществ, в частнокаталитическое окисление изопропилового спирта [c.435]
Окисление в газовой фазе. Об окислении изопропилового спирта в газовой фазе впервые было сообщено в 1949 г. [103]. Реакция проводится при 460 °С н отношении воздух изопропиловый спирт = 10 7 в присутствии 3 я. водяного пара или при 400 и отношении воздух изопропиловый спирт =1 1 [104]. Достигается конверсия кислорода порядка 6Q—80%, причем время пребывания изопропилового спирта в реакторе составляет от 0,5 до 1 с. Реактор должен быть облицован кислотоупорной эмалью. Очень важно быстрое охлаждение реакционной смеси до температуры ниже 100 С. Лучше всего это достигается впрыскиванием воды в смесь. Выход перекиси водорода при окислении в газовой фазе достигает около 70%, выход ацетона — 90%. Прн оптимальных условиях (420 °С, время контакта 50—80 с) получаются следующие результаты
В отдельных производствах окисление изопропилового спирта осуществляют воздухом, обогащенным кислородом, при температуре около 120 °С и избыточном давлении выше 1 МПа (10 кгс/см ). При таких условиях содержание кислорода в отходящих газах может составлять 11—12,5% (об.) содержание в реакционной массе перекиси водорода может достигать 9%, ацетона 20% и изопропилового спирта 57%. Незначительное превышение указанных выше параметров может привести к взрыву в окислителе. [c.125]
В патентной литературе чаще всего упоминаются два катализатора, применяемые для дегидрирования изопропилового спирта металлическая медь и окись цинка. Медь страдает тем недостатком, что ее активность уменьшается в процессе работы, а окись цинка вызывает в некоторой степени дегидратацию изопропилового спирта в пропилен. В промышленности сейчас, по-видимому, предпочитают производить ацетон дегидрированием, используя в качестве катализатора окись цинка, чистую или промотирован-ную. Одним из преимуществ этого метода по сравнению с методом окисления изопропилового спирта, о котором сообщается ниже, является то, что при дегидрировании в качестве побочного продукта получается чистый водород. В Германии производство ацетона осуществлялось дегидрированием изопропилового спирта, полученного из Сд—С4-олефинов, образующихся в процессе каталитического гидрирования окиси углерода при атмосферном давлении в жидкое топливо (гл. 3, стр. 62 и гл. 8, стр. 149).
Окисление изопропилового спирта воздухом проводят в присутствии металлических катализаторов. Реакция [c.315]
Одним пз новых методов производства перекиси водорода является жидкофазное окисление изопропилового спирта кислородом при температурах 90—140° С. В качестве побочного продукта получается ацетон [284]. [c.582]
В последнее время все чаще получают ацетон путем окисления изопропилового спирта воздухом при этом образуется также перекись водорода [c.142]
Франк-Каменецким [2] на аналогичном примере окисления изопропилового спирта на медном катализаторе. В отличие от реакции окисления метанола и аммиака, в этом процессе угасание реакции протекает легко, если нарушаются условия устойчивости. [c.165]
Окисление изопропилового спирта может быть проведено над серебряным катализатором при 450—500° С [c.138]
В патентной литературе имеется также описание некаталитического (термического) окисления низших газообразных парафинов, которое проводили при недостатке кислорода в реакторе из металла, устойчивого к действию высоких температур и продуктов реакции [7]. Температура процесса равнялась 400—500°, причем температуру поверхности реактора поддерживали на уровне ниже 200°. Полученные гидроперекиси имели такое же строение, что и гидроперекиси, обнаруженные в только что описанном опыте, однако незначительные изменения в условиях реакции приводили к образованию водного раствора перекиси водорода как основного продукта из числа веществ, содержавших активный кислород. Так, например, при работе со смесью из 90% пропана и 10% кислорода с продолжительностью реакции 5 сек. (температура в реакторе 470°, температура стенки 150°) основным кислородсодержащим продуктом была перекись водорода, полученная в виде 3—4%-ного водного раствора [8]. Этот способ получения перекиси водорода, по-видимому, уступает место прямому окислению изопропилового спирта, в результате которого тоже образуется перекись водорода (см. гл. 8, стр. 150).Ацетон получают в больших кол1 чествах различными методами при сухой перегонке дерева, разложением ацетата кальция, кумольным способом ( 17.4), окислением изопропилового спирта, гидратацией ацетилена водяным паром. В последнем способе реакция протекает при 400—460°С над катализатором, содержащим оксиды железа и марганца [c.324]
Основные правила безопасной работы. В процессе окисления изопропилового спирта кислородом воздуха возможно образование в незначительных количествах органических гидроперекисей, которые в неблагоприятных условиях и при случайном скоплении в застойных зонах могут быть опасны. [c.125]
Следует также отметить, что при окислении изопропилового спирта в жидкой фазе одновременно образуется перекись водорода, которую можно выделить [c.209]
В случае окисления изопропилового спирта воздухом, обогащенным кислородом, предусматривают соответствующую систему блокировок, исключающую превышение концентрации кислорода в смеси газов сверх допустимой. Сжатый и очищенный воздух смешивают с кислородом перед подачей в окислитель. При увеличении концентрации кислорода в обогащенном воздухе выше установленной нормы по сигналу газоанализатора, измеряющего содержание кислорода в смеси газов, срабатывает отсечной клапан на линии подачи кислорода в смеситель. В окислителях кислород воздуха, в том числе и обогащенного, исчерпывается не полностью. Часть его уходит с парогазовой фазой. При работе с воздухом, обогащенным кислородом, допустимая концентрация кислорода в отходящих газах из окислителя составляет 9—11% (об.). Поэтому для обеспечения безопасной концентрации кислорода (не выше 10,3%) отходящую парогазовую фазу разбавляют азотом в верхней части окислителя.
Смесь изопропилового спирта с другими растворителями применяется на предприятиях лесохимической промышленности для экстракции смол из древесины. При жидкофазном окислении изопропилового спирта получается перекись водорода и ацетон. [c.225]
Пример. Непрерывный процесс жидкофазного окисления изопропилового спирта воздухом в аппаратах барботажного типа с получением пероксида водорода и ацетона при 110— 135°С. Регламентированная концентрация кислорода в отходящих газах 5%, взрывоопасная концентрация 10%, соотношение регламентированного параметра и критического 50%- [c.259]
Для тушения пожара установки окисления изопропилового спирта оснащают дренчерными системами и лафетными стволами. Дрен-черные системы включаются в действие со щита управления. Эти технологические установки могут быть оснащены также системами пенотушения. [c.129]
Выше уже отмечалось, что расчет не всегда обеспечивает выбор параметров, приводящих к единственному стационарному состоянию. Условия могут быть настолько экстремальны, что их можно полностью исключить нз рассмотрения, как это было сделано для изотермического проточного реактора с перемешиванием, применяемого в процессе окисления изопропилового спирта. Кроме того, расчет, основанный на единственности стационарного состояния, часто приводит к неэкономичным результатам. Когда предварительные вычисления показывают, что можно получить интересующие нас результаты, цель расчета меняется. В то время как условия единственности могут использоваться при расчете предельных случаев, для создания реакторов, имеющих несколько стационарных состояний, необходимы другие основания. [c.46]
Пероксид водорода Н2О2 получают рядом методов, например электрохимическим окислением серной кислоты (см. 16.2), каталитическим окислением изопропилового спирта [c.249]
Основным способом получения ацетона из сырья нефтяного происхождения является окисление изопропилового спирта (гл. 8, стр. 150). Точно такими же способами, какими первичные спирты могут быть превращены в альдегиды, а именно дегидрированием или окислением воздухом (гл. 16), вторичные спирты можно перевести в кетоны. [c.314]
ОКИСЛЕНИЕ ИЗОПРОПИЛОВОГО СПИРТА [c.315]
Кетоны получают окислением вторичных спиртов. Например, ацетон получают в больших количествах при окислении изопропилового спирта [c.431]
Значительное количество ацетона производится каталитическим окислением изопропилового спирта. В этом процессе изопропанол смешивается с воздухом и направляется в peaiK-тор, в котором при температуре 500°С и давлении 4-10 Па на медном или серебряном катализаторах проводится реакция [c.277]
Ацетон получают в качестве второго продукта с помощью двух нефтехимических процессов процесса производства фенола окислением изопропилбензола (гл. 14, стр. 264) и процесса производства перекиси водорода окислением изопропилового спирта (гл. 8, стр. 151). При производстве фенола окислением изопропилбензола на каждую тонну фенола получается [c.316]
Опыт М 4. Окисление изопропилового спирта [c.55]
Пероксид водорода можно получать окислением изопропилового спирта, барботируя через него воздух при 110°С, Определите, какой теплоотвод от аппарата необходимо преду смотреть для изотермического ведения процесса, если он протекает по уравнению реакции [c.64]
Ацетон можно также получать окислением изопропилового спирта иа меди, серебре, никеле, платине по реакции [c.321]
Изопропиловый спирт, используемый для восстановления акролеина, получают из пропилена (стр. 106), а перекись водорода — при окислении изопропилового спирта (стр. 138). В качестве побочного продукта в этом процессе получается ацетон.
Для получения Н2О2 применяют также различные реакции с участием органических веществ, в частности, каталитическое окисление изопропилового спирта [c.441]
Пример 1-1. В работе Мацууры и Като (1967 г.), основанной на более ранних исследованиях Кунуги. Мацууры и Широ (1965 г.). предполагается, что окисление изопропилового спирта в жидкой фазе протекает по цепному механизму со следующими стадиями [c.22]
Отходяш,ие газы конденсируются и промываются водой для отделения ацетона и спирта от водородного потока, затем ацетон извлекается перегонкой. Одним из преимущ,еств этого метода по сравнению с методом окисления изопропилового спирта, который описывается ниже, является получение водорода в качестве побочного продукта. [c.67]
Окисление изопропилового спирта [c.67]
Впервые экспериментальный процесс с реверсом подачи газовой смеси описан в монофафии Д. А. Франк-Каменецкого. Этому описанию посвящен единственный абзац. Для окисления изопропилового спирта на медном катализаторе стационарное автотермическое проведение процесса оказалось вообще невозможным . Процесс удалось вести без внешнего подофева, только используя своеобразное явление мифации зоны реакции. Толщина слоя катализатора делалась весьма большой, и зона реакции не держалась стационарно в одном месте, но перемещалась по слою катализатора попеременно то в том, то в другом направлении. После того как зона реакции доходила до конца слоя катализатора, производилось переключение направления подачи спирто-воздушной смеси, и таким образом менялось направление мифации. При таком способе ведения про- [c.306]
Реакция окисления изопропилового спирта высоко экзотер-мична и с трудом поддается контролю. Поэтому рекомендуется в одной реакции объединять и окисление, и дегидрирование, с тем чтобы суммарный тепловой эффект приближался к нулю. [c.68]
По-видимому, впервые экспериментальный процесс с реверсом подачи газовой смеси описан в монографии Д. А. Франк-Каменецкого [2]. Этому описанию посвящен единственный абзац. Для окисления изопропилового спирта на медном катализаторе стационарное автотер-мическое проведение процесса оказалось вообще невозможным. Процесс удалось вести без внешнего нодогре- [c.97]
Для более надежной и безаварийной работы агрегаты окисления изопропилового спирта или другие аппараты для ведения подобных процессов должны быть оснащены устройствами блокирования взрыва отсечными устройствами. Блокирование взрыва может осуществляться отсечным клапаном на линии подачи окислителя в аппарат. Отсекатели можно устанавливать на вводных и выводных коммуникациях. Они срабатывают от детонатора по сигналу индикатора взрыва или датчика автоматического газоанализатора парогазовой фазы окислителя. Подобная взрывозащита реактора изображена на рис. VI1-3. Высокоскоростные отсе-кателн предотвращают распространение пламени из реактора в коммуникации. Кроме того, реактор может быть оснащен автоматической системой подавления взрыва. [c.128]
Изопропиловый метод получения пероксида водорода заключается в окислении изопропилового спирта кислородом. Достоинством этого метода является то, что одновременно с Н2О2 получают и другой ценный продукт — ацетон [c.170]
Один из способов окисления изопропилового спирта в ацетон, применяемый в промышленности, совершенгю аналогичен окислению метилового спирта в формальдегид (кислород воздуха, серебряный катализатор). Пропилен можно и прямо окислить в ацетон. [c.182]
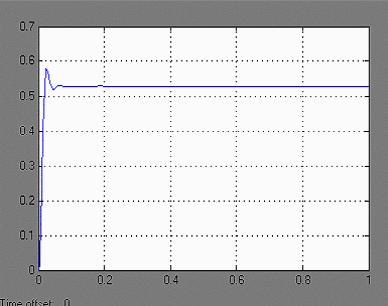
Результаты экспериментов на глубокое окисление изопропилового спирта (ИПС) в вихревом реакторе представлены графиками на рис. 2.26 и 2.27. Зависимость степени окисления X от температуры Т имеет характерную 8-образную форму, что подтверждает переход реакции при Т а 250°С из кинетической во внешнедиффузионную область. Как видно из рис. 2.27, на кривых изменения температуры катализаторного покрытия по длине вихревой трубы по ходу ПВС тметен резкий рост температуры на начальном участке, причем максимум температуры на кривой тем выше, чем больше скорость ввода ПВС при этом вершины кривых смешаются в сторону ввода газа. Затем температура плавно снижается. Более плавное изменение температуры вдоль трубы наблюдается в вихревом реакторе без ВЗУ, т. е. при прямоточном потоке (кривая 4). [c.130]
Пример И-7. Используйте метод И для случая окисления изопропилового спирта в жидкой фазе, применив модель прстэчного реактора с перемешиванием, предложенную Мацуурой и Като, при kjk, = 10 . Если = 100 мин» вычислите врел я пребывания в реакторе, которое приводит к множественным стационарным [c.49]
chem21.info
Каталитическое окисление изопропилового спирта — Справочник химика 21
Каталитическое окисление изопропилового спирта [c.424]В современном производстве перокси применяют реакции с участием органических веществ, в частно[c.435]
Эти соображения, базирующиеся на развитой выше общей теории, принесли практическую пользу при разработке технологического процесса каталитического окисления изопропилового спирта в ацетон [9]. [c.425]
Пероксид водорода Н2О2 получают рядом методов, например электрохимическим окислением серной кислоты (см. 16.2), каталитическим окислением изопропилового спирта [c.249]
Значительное количество ацетона производится каталитическим окислением изопропилового спирта. В этом процессе изопропанол смешивается с воздухом и направляется в peaiK-тор, в котором при температуре 500°С и давлении 4-10 Па на медном или серебряном катализаторах проводится реакция [c.277]
Изопропиловый спирт применяется как растворитель (заменитель этилового спирта) и сырье для органического синтеза. При каталитическом окислении изопропилового спирта воздухом получают ацетон. Производство изопропилового спирта менее сложное, чем этилового, ресурсов для его получения больше, а химизм процесса не отличается от описанного выше синтеза этилового спирта. [c.256]
Подобные же диаграммы могут быть построены и в обычной системе координат. На рис. 74, б, 74, в приведены кривые Франк-Каменецкого и Фридмана для определения состава водной смеси ацетона и изопропилового спирта, получающейся при каталитическом окислении изопропилового спирта в ацетон. По этим кривым смеси, имеющей л = 1,375 и с = 0,86, отвечает содержание ацетона в 30%, определяемое по рис. 74,6, изопропилового спирта в 43%, определяемое по рис. 71, в остаток — 27% воды. [c.111]
Применение теории к важному техническому процессу каталитического окисления изопропилового спирта в ацетон позволило наметить пути усовершенствования этого процесса [91. [c.392]
Примером применения методики моделирования может служить сопоставление медного и серебряного катализаторов при каталитическом окислении изопропилового спирта в ацетон, сделанное в недавно опубликованной работе Франк-Каменецкого, Кренцеля и Зверева . Активность медного катализатора ниже, чем серебряного. В результате, для медного катализатора потухание поверхности происходит при более высокой температуре. [c.373]
В последнее время стал приобретать практическое значение также и процесс каталитического окисления изопропилового спирта в ацетон. Все эти процессы проводятся обычно на металлических катализаторах, которыми служат при окислении аммиака платина, а при окислении спиртов — медь или серебро. [c.425]
Изопропиловый спирт С3Н7ОН наряду с этиловым находит большое применение в народном хозяйстве в качестве растворителя — заменителя этилового спирта, а также как полупродукт в органическом синтезе. В промышленности изопропиловый спирт применяют главным образом для получения ацетопа, который сравнительно легко образуется при каталитическом окислении изопропилового спирта воздухом. Кроме того, на основе изопропилового спирта получают пенный растворитель для лаковых покрытий — изопропилапетат. Изопропиловый спирт используют также в качестве растворителя в некоторых отраслях народного хозяйства и при получении косметических препаратов. [c.78]
При производстве глицерина из акролеина, получаемого неполным окислением пропилена над медными катализаторами при 300—400 °С и 1—10 кгс/см2 (0,1—1 МН/м ) [43], процесс состоиг из восстановления акролеина в аллиловый спирт донорами водорода— первичными или вторичными алифатическими спиртами (процесс ведут в газовой фазе над магний-цинковыми катализаторами при 350—450 °С и нормальном давлении или в жидкой фазе с использованием изопропилата алюминия) гидроксилирования аллилового спирта перекисью водорода в присутствии сульфокислот или вольфрамовой кислоты при 50—100 °С получения перекиси водорода каталитическим окислением изопропилового-спирта (получаемого гидратацией пропилена см. стр. 36) возду-. хом при 100—140 °С [c.85]
chem21.info
Окисление — изопропилового спирт — Большая Энциклопедия Нефти и Газа, статья, страница 1
Окисление — изопропилового спирт
Cтраница 1
Окисление изопропилового спирта с одновременным получением ацетона и перекиси водорода осуществляют в жидкой фазе некаталитически или с использованием инициаторов и катализаторов. [1]
Окисление изопропилового спирта при облучении УФ-светом в присутствии антрахинона сопровождается образованием антрагидро-хинонового радикала ( обнаружен методом ЭПР) [69], что подтверждает радикальный механизм фотосенсибилизированного окисления. Ряд особенностей фотоокисления спиртов связан с превращениями фотосенсибилизаторов, в качестве которых чаще всего используются антрахинон, его производные и бен-зофенон. Бекстрем обнаружил [67], что скорость фотоокисления изопропилового спирта ( сенсибилизатор — бензофенон) обратно пропорциональна парциальному давлению кислорода. [2]
Окисление изопропилового спирта в паровой фазе так же, как при окислении в жидкой фазе, протекает без катализатора, но с применением в качестве инициатора перекиси водорода. [3]
Окисление изопропилового спирта наиболее целесообразно проводить в контактном аппарате ( рис. 129, стр. Для быстрого охлаждения продуктов реакции аппарат снабжают холодильником. Неконденсирующиеся в холодильнике газы ( главным образом азот воздуха) промывают в скруббере водой для отделения увлеченных ими паров ацетона и изопропилового спирта и затем выводят в атмосферу. Конденсат вместе с промывной водой обрабатывают известью или содой для нейтрализации небольших примесей уксусной кислоты и подвергают дистилляции. Вначале отгоняется легкая фракция ( технический ацетон), затем-85 % — ный изопропиловый спирт, который возвращают на окисление. Остаток ( вода, содержащая небольшое количество уксуснокислого кальция или натрия) сливается в канализацию. [4]
Окисление изопропилового спирта воздухом проводят в присутствии металлических катализаторов. [5]
Реакция окисления изопропилового спирта в большой мере зависит от температуры. Энергия активации развившейся реакции составляет — 17 1 ккал / моль. [7]
Механизм окисления изопропилового спирта до ацетона при действии хромовой кислоты был исследован весьма тщательно; он очень интересен в том отношении, что показывает, каким образом изменения уровня окисления могут происходить с участием типичных неорганических и типичных органических соединений. [8]
Реакция окисления изопропилового спирта высоко экзотер-мична и с трудом поддается контролю. Поэтому рекомендуется в одной реакции объединять и окисление, и дегидрирование, с тем чтобы суммарный тепловой эффект приближался к нулю. [9]
Механизм окисления изопропилового спирта до ацетона при действии хромовой кислоты был исследован весьма тщательно; он очень интересен в том отношении, что показывает, каким образом изменения уровня окисления могут происходить с участием типичных неорганических и типичных органических соединений. [10]
Реакция окисления изопропилового спирта в большой мере зависит от температуры. Энергия активации развившейся реакции составляет — 17 1 ккал / моль. [12]
Аналогично окислению изопропилового спирта протекает реакция окисления вторичного бутилового спирта в метил-этилкетон, являющийся ценным растворителем для ряда производств химической и нефтяной отраслей промышленности. Технологическая схема получения метплэтилкетона не отличается от производства ацетона. [13]
При окислении изопропилового спирта наблюдается постепенное развитие процесса со значительным периодом индукции, что связано с медленным накоплением и распадом промежуточного продукта на радикалы, дающие начало новым цепям реакции окисления. Для сокращения периода индукции и интенсификации процесса получения перекиси водорода представляло интерес изыскать наиболее эффективные с точки зрения промышленного использования методы инициирования реакции окисления изопропилового спирта. [14]
При окислении изопропилового спирта наряду с пероксидом водорода образуется также ацетон. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
Окисление — изопропилового спирт — Большая Энциклопедия Нефти и Газа, статья, страница 3
Окисление — изопропилового спирт
Cтраница 3
Изучены основные закономерности окисления изопропилового спирта в жидкой фазе молекулярным кислородом. Установлены автокаталитический характер этой реакции и наличие ряда параллельно и последовательно протекающих макроскопических стадий. Отмечено наличие периода индукции и зависимость его от величины и состояния внутренней поверхности реактора, добавок инги-бирующих и инициирующих веществ и от других факторов. [31]
Перечисленные работы по окислению изопропилового спирта, а также исследования по окислению других вторичных спиртов [10-12] дают возможность понять многие вопросы, связанные с механизмом жидкофазного окисления изопропилового спирта. Однако пока еще не создано цельного представления о механизме всех элементарных процессов, протекающих при взаимодействии кислорода со спиртом в жидкой фазе, и ряд вопросов требует дополнительного изучения. [32]
Получают главным образом окислением изопропилового спирта. Выпускают в виде двух сортов. [33]
Метод основан на окислении изопропилового спирта персульфатом калия до ацетона. Последний образует с салициловым альдегидом в щелочной среде соединение, окрашенное в цвет от желто-зеленого до ярко-оранжевого. [34]
Как показывает вышеизложенное, окисление изопропилового спирта представляет собой сложный комплекс параллельно и последовательно протекающих процессов. Поскольку в данной работе процесс окисления изопропилового спирта изучался как путь получения перекиси водорода, особый интерес с этой точки зрения представляет стадия накопления перекисных соединений и условия, способствующие сохранению максимального их количества. [35]
Метод основан на реакции окисления изопропилового спирта до ацетона, который в щелочной среде дает окрашенное соединение с салициловым альдегидом. Оптическую плотность окрашенного раствора измеряют на фотоэлектроколориметре. [36]
Для исследования механизма реакции окисления изопропилового спирта в качестве ингибитора нами был применен р-нафтол, различные количества которого добавляли в реакционную смесь по ходу процесса окисления. [37]
Предложена схема механизма процесса окисления изопропилового спирта. [38]
Повышение давления в процессе окисления изопропилового спирта оказывает существенное положительное влияние на скорость процесса и на максимально достигаемую концентрацию пере-кисных соединений. Так, при повышении давления с 5 до 50 атм процесс ускоряется в несколько раз, а достигаемая концентрация перекисей увеличивается примерно в два раза. [39]
Предложена схема механизма процесса окисления изопропилового спирта. [40]
Для успешного осуществления реакции окисления изопропилового спирта большое значение имеет чистота исходного спирта, который не должен содержать примесей сернистых соединений, полимеров и изопропилового эфира. [41]
Для тушения пожара установки окисления изопропилового спирта эснащают дренчерными системами и лафетными стволами. Дрен-верные системы включаются в действие со щита управления. Эти технологические установки могут быть оснащены также системами ленотушения. [42]
Для тушения пожара установки окисления изопропилового спирта оснащают дренчерными системами и лафетными стволами. Дрен-черные системы включаются в действие со щита управления. Эти технологические установки могут быть оснащены также системами пенотушения. [43]
Для исследования механизма реакции окисления изопропилового спирта в качестве ингибитора нами был применен р-нафтол, различные количества которого добавляли в реакционную смесь по ходу процесса окисления. [44]
Предложена схема механизма процесса окисления изопропилового спирта. [45]
Страницы: 1 2 3 4
www.ngpedia.ru
Жидкофазное окисление — изопропилового спирт
Жидкофазное окисление — изопропилового спирт
Cтраница 1
Жидкофазное окисление изопропилового спирта техническим кислородом проводят в барботажной колонне при 90 — 140 С и давлении 14 — 21 ат, небходимом для поддержания реакционной массы в жидком состоянии. [2]
В результате жидкофазного окисления изопропилового спирта молекулярным кислородом образуются реакционные смеси, которые имеют следующий примерный состав, вес. [3]
По аналогичной схеме производится жидкофазное окисление изопропилового спирта воздухом в аппаратах барботажного типа с получением пероксида водорода и ацетона при НО-135 С и давлении 1 0 — 1 1 МПа. [4]
По аналогичной схеме производится жидкофазное окисление изопропилового спирта воздухом в аппаратах барботажного типа с получением пероксида водорода и ацетона при НО-135 С и давлении 1 0 — 1 1 МПа. Изопропиловый спирт подается в реактор насосами типа ХГ. [5]
Получается электрохимическим и органическим ( жидкофазным окислением изопропилового спирта) методами. [6]
Одним из новых методов производства перекиси водорода является жидкофазное окисление изопропилового спирта кислородом при температурах 90 — 140 С. [7]
В статье рассмотрены итоги шестилетней эксплуатации производства пергидроля, работающего по новому методу через жидкофазное окисление изопропилового спирта. [8]
Перечисленные работы по окислению изопропилового спирта, а также исследования по окислению других вторичных спиртов [10-12] дают возможность понять многие вопросы, связанные с механизмом жидкофазного окисления изопропилового спирта. Однако пока еще не создано цельного представления о механизме всех элементарных процессов, протекающих при взаимодействии кислорода со спиртом в жидкой фазе, и ряд вопросов требует дополнительного изучения. [9]
Смесь изопропилового спирта с другими растворителями применяется на предприятиях лесохимической промышленности для экстракции смол из древесины. При жидкофазном окислении изопропилового спирта получается перекись водорода и ацетон. [10]
В литературе приведены данные130 о разработанном процессе жидкофазного окисления изопропилового спирта с целью получения перекиси водорода и ацетона. Несмотря на то, что гидроперекись в этом процессе не была выделена, ее промежуточное образование, по-видимому, не вызывает сомнений. [11]
В литературе приведены данные130 о разработанном процессе жидкофазного окисления изопропилового спирта с целью получения перекиси водорода и ацетона. Несмотря на то, что гидроперекись в этом процессе не была выделена, ее промежуточное образование, по-видимому, не вызывает сомнений. [12]
Страницы: 1
www.ngpedia.ru
Изопропиловый спирт дегидрирование и окисление
Одним из важных продуктов нефтехимии является изопропиловый спирт, используемый в больших количествах в качестве растворителя, как сырье для дегидрирования или окисления в ацетон, для получения сложных эфиров и для других целей. Основные количества изопропилового спирта получаются в процессе гидратации пропилена, который во многом аналогичен гидратации этилена. Пропилен так же, как и этилен, может быть превращен в спирт по сернокислотному методу гидратации н прямой гидратацией на твердых катализаторах. Оптимальные условия гидратации пропилена по обоим этим методам несколько мягче, чем при получении спирта из этилена. Сернокислотная гидратация пропилена в промышленности была осуществлена еще в 20-х годах, задолго до организации производства синтети- [c.137]В патентной литературе чаще всего упоминаются два катализатора, применяемые для дегидрирования изопропилового спирта металлическая медь и окись цинка. Медь страдает тем недостатком, что ее активность уменьшается в процессе работы, а окись цинка вызывает в некоторой степени дегидратацию изопропилового спирта в пропилен. В промышленности сейчас, по-видимому, предпочитают производить ацетон дегидрированием, используя в качестве катализатора окись цинка, чистую или промотирован-ную. Одним из преимуществ этого метода по сравнению с методом окисления изопропилового спирта, о котором сообщается ниже, является то, что при дегидрировании в качестве побочного продукта получается чистый водород. В Германии производство ацетона осуществлялось дегидрированием изопропилового спирта, полученного из Сд—С4-олефинов, образующихся в процессе каталитического гидрирования окиси углерода при атмосферном давлении в жидкое топливо (гл. 3, стр. 62 и гл. 8, стр. 149). [c.315]
Спирты. Один из классических методов получения альдегидов и кетонов — дегидрирование соответствующих спиртов. В промышленности каталитическое дегидрирование проводят обычно над серебром или медью при температурах около 300°. Формальдегид, простейший член ряда, получают главным образом пропусканием метанола над раскаленной серебряной сеткой необходимое для осуществления этой реакции тепло получают за счет окисления водорода небольшими объемами воздуха [24]. Дегидрирование этанола является одним из важнейших способов получения ацетальдегида [25]. Большое значение имеет промышленный метод получения ацетона дегидрированием изопропилового спирта. Циклогексанон готовят дегидрированием циклогексанола, причем в качестве катализатора обычно применяют медь. н-Масляный альдегид, изомасляный альдегид и метилэтилке-тон — примеры многочисленных соединений, получаемых каталитическими методами. [c.570]
Некоторое количество ацетона получается окислением или дегидрированием изопропилового спирта. [c.138]
Вторичные спирты, получаемые гидратацией С4—Сд-олефинов нормального строения (гл. 8), превращают в соответствующие им кетоны точно так же, как получают ацетон, а именно парофазным дегидрированием или каталитическим окислением воздухом. Дегидрирование втор-бутилового спирта в метилэтилкетон протекает при 350°, т. е. при несколько более низкой температуре, чем дегидрирование изопропилового спирта (380°). Этот метод считается лучшим, чем каталитическое окисление воздухом. [c.329]
Ацетон получают при сухой перегонке дерева, окислением изопропилбензола до гидроперекиси с последующим гидролизом последней, дегидрированием изопропилового спирта и гидратацией ацети- [c.209]
Закономерности подбора катализаторов для реакций окислительно-восстановительного типа можно вывести на основании более надежных данных, чем для реакций кислотно-оснОвного типа. Однако и для первых наибольшее число данных относится к сравнительно небольшой группе реакций к реакциям окисления СО и углеводородов, разложения N30, этилового и изопропилового спиртов, дегидрирования циклогексана. Но и в этом случае по каждой из указанных реакций имеется лишь 10—15 работ. [c.99]
Дегидратация этилового и изопропилового спиртов Дегидрирование н-гептана с параллельной циклизацией Дегидрирование спиртов Сг -Си Окисление водорода Окисление окиси углерода Превращение циклогексана, н-бутана [c.383]
Ацетон — исключительно важный для нефтехимии продукт. В промышленности он получается несколькими способами окислительным, дегидрированием изопропилового спирта, окислением кумола, окислением пропилена, окислением углеводородных газов — пропана и бутана, брожением. Так, например, в 1960 г. в США 347 тыс. т ацетона было получено из изопропилового спирта, 42 тыс. т — через гидроперекись кумола. 16 тыс. т — окислением сжиженных углеводородных газов и 20 тыс. т — брожением в 1963 г. производство ацетона составляло 377 тыс. г. [c.34]
Основным способом получения ацетона из сырья нефтяного происхождения является окисление изопропилового спирта (гл. 8, стр. 150). Точно такими же способами, какими первичные спирты могут быть превращены в альдегиды, а именно дегидрированием или окислением воздухом (гл. 16), вторичные спирты можно перевести в кетоны. [c.314]
Нередко поверхностные соединения сами являются катализаторами. Так, реакции окисления водорода, окиси углерода, метанола, изопропилового спирта на серебре с энергией активации 16—19 ккал протекают при соударении окисляемых молекул с поверхностными кислородными соединениями серебра. Было экспериментально установлено, что прогрев серебра при 700— 800° в атмосфере кислорода прекращает на этом катализаторе реакции окисления изопропилового спирта в ацетон молекулярным кислородом. Вместо окисления начинает идти реакция дегидрирования спирта с выделением водорода, которая не идет на металлическом серебре. [c.191]
Основным промышленным способом получения ацетона из сырья нефтяного происхождения является дегидрирование или окисление воздухом изопропилового спирта. [c.66]
Реакция окисления изопропилового спирта высоко экзотер-мична и с трудом поддается контролю. Поэтому рекомендуется в одной реакции объединять и окисление, и дегидрирование, с тем чтобы суммарный тепловой эффект приближался к нулю. [c.68]
Наиболее важным в промышленном отношении является первый представитель класса кетонов — ацетон. Сейчас его получают в основном дегидрированием изопропилового спирта или при окислении кумола (см. стр. 105). Ацетон — жидкость, кипя-ш,ая при 56°С, со своеобразным запахом, смешивающаяся с водой во всех отношениях. Используется он в качестве растворителя и как исходный материал в ряде органических производств. Следует иметь в виду легкую воспламеняемость ацетона и взрывчатость его паров в смеси с воздухом. [c.123]
Получение ацетона. Ацетон может быть получен дегидрированием или неполным окислением изопропилового спирта [c.214]
Ацетон, или диметилкетон, СНз—СО—СНз является простейшим представителем класса кетонов. Он получается в довольно значительных количествах при сухой перегонке дерева. В небольшом количестве ацетон образуется также и при сухой перегонке каменного угля. Синтетически ацетон может быть получен нагреванием уксуснокислого кальция или из уксусной кислоты по реакции кетонизации (см. стр. 238), а также окислением или каталитическим дегидрированием изопропилового-спирта в паровой фазе над металлической медью [c.265]
Приведите примеры одноатомных, двух- и трехатомных спиртов первичного, вторичного и третичного спиртов и назовите их. Напишите уравнения реакций получения изопропилового спирта из пропилена образования и разложения этилата натрия взаимодействия вторичного пропилового спирта с металлическим натрием окисления метилового, первичного и вторичного пропило-вых спиртов дегидрирования метилового спирта дегидратации этилового спирта образования сложного эфира при взаимодействии этилового спирта и уксусной кис- [c.17]
Изопропиловый спирт окислением (над серебряным катализатором при 450—500°) или дегидрированием переводят в ацетон. [c.119]
В иром-сти А. получают исходя из пропилена, гидратацией которого производят изопропиловый спирт. Последний перерабатывают в ацетон окислением или дегидрированием. Окисление изопропилового спирта [c.177]
Изопропиловый спирт в этом процессе превращается в ацетон другие высшие спирты также окисляются в присутствии серебряных катализаторов, но обычно для получения продуктов их окисления используют каталитическое дегидрирование (разд. VI. гл.6). [c.312]
Из изопропилового спирта путем его каталитического дегидрирования или неполного окисления получают ацетон. [c.189]
Получение ацетона окислением изопропилового спирта Окисление изопропилового спирта производится в паро-газовой фазе. Паро-газовую смесь, полученную пропусканием воздуха через нагретый спирт, подают в контактный аппарат, где при 650° происходит одновременное окисление и дегидрирование спирта [c.191]
Более поздние работы [309, 310] по изучению каталитической активности таких катализаторов показали, что их удельные поверхности изменяются неаддитивно по мере возрастания содержания одного окисла металла в другом. Скорость реакции дегидрирования изопропилового спирта уменьшается при увеличении содержания окиси хрома в смеси с окисью цинка [310]. Падение скорости дегидратации изопропилового спирта наблюдал Рубинштейн с сотрудниками [311] при уменьшении АЬОз в смеси с закисью никеля. Чаплин, Чаиман и Грифите [312] изучали смешанные катализаторы, содержащие окись хрома и окись алюминия, и ноказали (рис. 83), что в зависимости от состава изменяются удельная поверхность катализатора и количество адсорбированного гептана (100°) на единицу поверхности. В качестве катализаторов окисления углеводородов [c.221]
Вторичные спирты, полученные при гидратации С4—Св-олефинов с прямой цепью (см. гл. VII), превращаются в соответствующие им кетоны точно так же, как получается ацетон, при парофазном дегидрировании или каталитическом окислении воздухом изопропилового спирта. Дегидрирование втор-бутилового спирта в метилэтилкетон протекает при 350°, т. е. при более низкой температуре, чем дегидрирование изопропилового спирта (380° С) [2]. Технические нормальные пентаноны и гексаноны представляют собой смеси, состав которых соответствует составу исходных технических спиртов. Эти спирты дегидрируют в соответствующие кетоны при 455—485°С над катализатором (латунь) [38]. [c.313]
Прп повышенных давлениях возможно ирпменение более слабой (75%-но11) кислоты. Прп гидролизе алкилсульфата некоторое количество изопропилового эфира образуется в качестве побочного продукта. Из изопропилового спирта легко получается ацетон либо путем каталитического окисления, либо путем дегидрирования над металлическим (обычно медным) катализатором. [c.578]
Изопропиловый спирт обладает всеми химическими свойствами одноатомных спиртов жирного ряда образует алкого-ляты под действием галоидных соединений фосфора образует галоидные алкилы при действии кислот образует простые и сложные эфиры при дегидрировании или окислении образует ацетон (см. стр. 67) конденсируется с ароматическими соединениями с образованием изопропил бензола (см. стр. 69), изо-пропилтолуола и т. д. [c.56]
Этот способ экономически выгоден. Относительная себестоимость ацетона, полученного дегидрированием изопропилового спирта 100%, кумолпероксидным способом 50—60%, прямым окислением пропилена — 35 %. [c.70]
Этил-3,5-диметил-пиридин Изопропиловый спирт Р е а к 1 3-Метилпентан, 2,3-диметилпентан, 3,4-диметилгексан 2-Винил-3,5-диме- тилпиридин Дегидрирование кисло Продукты дегидрогенизации и дегидратации Ацетон 1ИИ с участием м Окисление уг. Уксусная (I), муравьиная (II), пропионовая (III) кислоты Смешанные фосфаты никеля и кальция или никеля и алюминия. Превращение 22%, селективность 95% [3370] оодсодержащих соединений Феррит никеля — окись никеля [3369] NijB, активированный хромом жидкая фаза [3371J олекулярного кислорода неродного скелета Соли никеля жидкая фаза, 42 бар, 160° С. Выход 1 — 55%, 11 — 13%, III — 3,2 %[1459] [c.193]
В некоторых случаях, например при дегидрировании спиртов (см. таблицу), корреляция к. а. с параметром решетки наблюдается в других (дегидратация изопропилового спирта, Нд — Вд-обмеп, окисление СО, разложение КзО )— она не имеет места. Рассмотрение соответствующих кинетических данных показывает, что в тех случаях, когда корреляция к. а. с величиной I наблюдается, предэкспонепт/со в уравнении Аррениуса имеет понжкенные значения. Это может быть объяснено образованием двух-и многоточечных комплексов при адсорбции. [c.82]
В работах [1111—1113, 1178] изучалась кинетика реакций дегидрирования изопропилового спирта, гидрирования и окисления этилена, синтеза аммиака и синтеза метанола, см. также [1252, 1265]. В работе [1114] отмечается, что сочетание проведения реакции в дифференциальном реакторе с псевдоожнженным слоем катализатора позволяет свести неточности эксперимента к минимуму. Эта точка зрения, разумеется, может быть справедливой в некоторых случаях, но обычно применение безградиентных методов (одним из которых может быть проведение реакции в псевдоожиженном слое) достаточно для получения точных и надежных кинетических данных. [c.540]
Процесс прямого окисления олефинов с получением кетонов является экономически выгодным. По технико-экономическим расчетам относительная себестоимость ацетона, полученного различными методами, следующая (в %) дегидрированием изопропилового спирта — 100, из кумола — 50—60, прямым окислением пропилена — 35. Объем производства кетонов весьма значителен. Так, в США в 1963 г. было ползгчено 365 тыс. т ацетона и 110 тыс. т метилэтилкетона. [c.315]
Дегидрирование и деГидроцикли-зация углеводородов Превращение этилового спирта, изопропилового спирта Кетонизация н-бутилового спирта Окисление метанола Окисление метана в СО2 и НаО [c.382]
Окисление проводят при значительном избытке изо-пропилового снирта в аппарате с тонким слоем серебряного ката,лизатора известны и другие катализаторы этого процесса, напр. Сп, N1, РЬ однако они менее эффективны. Продукты реакции быстро охлаждают в холоди.] ьнике. Конденсат после нейтрализации небольших примесей СН3СООН дистиллируют выделенный технический ацетон ректифицируют, а не-прореагировавшш изопропиловый спирт возвращают на окислении. Дегидрирование изопрониловох о спирта [c.177]
Ацетон Gh4 O h4. Этот простейший кетон, еще недавно получавшийся вместе с метиловым и древесным спиртом из нодсмольной воды при сухой перегонке дерева, ныне почти исключительно получают каталитическим дегидрированием (окислением) синтетического изопропилового спирта, по реакции [c.763]
chem21.info
Реакция — окисление — изопропилового спирт
Реакция — окисление — изопропилового спирт
Cтраница 3
Хотя из трех испытанных перскисных соединений перекись третичного бутила оказывает наиболее сильное инициирующее действие на реакцию окисления изопропилового спирта, однако в качестве инициатора для данной реакции была выбрана перекись водорода. Выбор этот основан, главным образом, па том, что введение в реакционную смесь нового компонента, каким является перекись третичного бутила, не целесообразно, поскольку это затруднит дальнейшее выделение и очистку перекиси водорода. [31]
Анализ данных, полученных при исследовании различных методов инициирования, показывает, что из испытанных инициаторов наилучшее инициирующее действие в реакции окисления изопропилового спирта оказывают перекиспые соединения, добавка которых позволяет не только значительно сокращать период индукции и достигать более высоких скоростей процесса по сравнению с другими инициаторами, но и получать перекись водорода с высоким выходом. [32]
В работах Пневой с Борисовой [6] и Пневой с Селютиной [7], осуществлявших окисление изопропилового спирта при повышенных температурах ( 115) и давлении 2 5 атм, методом инициирующих добавок были получены данные, доказывающие цепной, вы-рождепно-разветвленный механизм реакции окисления изопропилового спирта с квадратичным обрывом цепей. Об этом свидетельствовала полученная авторами пропорциональность скорости реакции корню квадратному из скорости инициирования. [33]
В работах Пневой с Борисовой [6] и Пневой с Селютиной [7], осуществлявших окисление изопропилового спирта при повышенных температурах ( 115) и давлении 2 5 атм, методом инициирующих добавок были получены данные, доказывающие цепной, вы-рожденно-разветвленный механизм реакции окисления изопропилового спирта с квадратичным обрывом цепей. Об этом свидетельствовала полученная авторами пропорциональность скорости реакции корню квадратному из скорости инициирования. [34]
Изыскание более эффективных методов инициирования реакции окисления изопропилового спирта, Отч. [35]
Данных о возможности инициирования действием бромистого водорода реакций окисления спиртов в литературе не имеется, поэтому реакция окисления изопропилового спирта, инициированная бромистым водородом, интересна как с точки зрения теоретической, так и для практических целей — интенсификации процесса. [36]
При окислении изопропилового спирта наблюдается постепенное развитие процесса со значительным периодом индукции, что связано с медленным накоплением и распадом промежуточного продукта на радикалы, дающие начало новым цепям реакции окисления. Для сокращения периода индукции и интенсификации процесса получения перекиси водорода представляло интерес изыскать наиболее эффективные с точки зрения промышленного использования методы инициирования реакции окисления изопропилового спирта. [37]
Нередко поверхностные соединения сами являются катализаторами. Так, реакции окисления водорода, окиси углерода, метанола, изопропилового спирта на серебре с энергией активации 16 — 19 ккал протекают при соударении окисляемых молекул с поверхностными кислородными соединениями серебра. Было экспериментально установлено, что прогрев серебра при 700 — 800 в атмосфере кислорода прекращает на этом катализаторе реакции окисления изопропилового спирта в ацетон молекулярным кислородом. Вместо окисления начинает идти реакция дегидрирования спирта с выделением водорода, которая не идет на металлическом серебре. [38]
Страницы: 1 2 3
www.ngpedia.ru