физические свойства, получение, применение, история :: ТОЧМЕХ
Физические свойства алюминия
Алюминий — мягкий, легкий, серебристо-белый металл с высокой тепло- и электропроводностью. Температура плавления 660°C.
По распространенности в земной коре алюминий занимает 3-е место после кислорода и кремния среди всех атомов и 1-е место — среди металлов.
К достоинствам алюминия и его сплавов следует отнести его малую плотность (2,7 г/см3), сравнительно высокие прочностные характеристики, хорошую тепло- и электропроводность, технологичность, высокую коррозионную стойкость. Совокупность этих свойств позволяет отнести алюминий к числу важнейших технических материалов.
Алюминий и его сплавы делятся по способу получения на деформируемые, подвергаемые обработке давлением и литейные, используемые в виде фасонного литья; по применению термической обработки — на термически не упрочняемые и термически упрочняемые, а также по системам легирования.
Получение
Впервые алюминий был получен Гансом Эрстедом в 1825 году.
Применение
Алюминий широко применяется как конструкционный материал. Основные достоинства алюминия в этом качестве — легкость, податливость штамповке, коррозионная стойкость (на воздухе алюминий мгновенно покрывается прочной пленкой Al2O3, которая препятствует его дальнейшему окислению), высокая теплопроводность, неядовитость его соединений. В частности, эти свойства сделали алюминий чрезвычайно популярным при производстве кухонной посуды, алюминиевой фольги в пищевой промышленности и для упаковки.
Основной недостаток алюминия как конструкционного материала — малая прочность, поэтому его обычно сплавляют с небольшим количеством меди и магния (сплав называется дюралюминий).
Электропроводность алюминия сравнима с медью, при этом алюминий дешевле. Поэтому он широко применяется в электротехнике для изготовления проводов, их экранирования и даже в микроэлектронике при изготовлении проводников в чипах. Правда, у алюминия как электротехнического материала есть неприятное свойство — из-за прочной оксидной пленки его тяжело паять.
Благодаря комплексу свойств широко распространен в тепловом оборудовании.
Внедрение алюминиевых сплавов в строительстве уменьшает металлоемкость, повышает долговечность и надежность конструкций при эксплуатации их в экстремальных условиях (низкая температура, землетрясение и т.п.).
Алюминий находит широкое применение в различных видах транспорта. На современном этапе развития авиации алюминиевые сплавы являются основными конструкционными материалами в самолетостроении. Алюминий и сплавы на его основе находят все более широкое применение в судостроении. Из алюминиевых сплавов изготовляют корпусы судов, палубные надстройки, коммуникацию и различного рода судовое оборудование.
Идут исследования по разработке пенистого алюминия как особо прочного и легкого материала.
Драгоценный алюминий
В настоящее время алюминий является одним из самых популярных и нашедших широкое применение металлов. С самого момента открытия в середине XIX века его считали одним из ценнейших благодаря удивительным качествам: белый как серебро, легкий по весу и не подверженный воздействию окружающей среды. Стоимость его была выше цен на золото. Не удивительно, что в первую очередь алюминий нашел свое применение в создании ювелирных изделий и дорогих декоративных элементов.
В 1855 г. на Универсальной выставке в Париже алюминий был самой главной достопримечательностью. Изделия из алюминия располагались в витрине, соседствующей с бриллиантами французской короны. Постепенно зародилась определенная мода на алюминий. Его считали благородным малоизученным металлом, используемым исключительно для создания произведений искусства.
Наиболее часто алюминий использовали ювелиры. При помощи особой обработки поверхности ювелиры добивались наиболее светлого цвета металла, из-за чего его часто приравнивали к серебру. Но в сравнении с серебром, алюминий обладал более мягким блеском, чем обуславливалась еще большая любовь к нему ювелиров.
При помощи особой обработки поверхности ювелиры добивались наиболее светлого цвета металла, из-за чего его часто приравнивали к серебру. Но в сравнении с серебром, алюминий обладал более мягким блеском, чем обуславливалась еще большая любовь к нему ювелиров.
Так как химические и физические свойства алюминия сначала были слабо изучены, ювелиры сами изобретали новые техники его обработки. Алюминий технически легко обрабатывать, этот мягкий металл позволяет создавать отпечатки любых узоров, наносить рисунки и создавать желаемой формы изделия. Алюминий покрывался золотом, полировался и доводился до матовых оттенков.
Но со временем алюминий стал падать цене. Если в 1854-1856 годах стоимость одного килограмма алюминия составляла 3 тысячи старых франков, то в середине 1860-х годов за килограмм этого металла давали уже около ста старых франков. Впоследствии из-за низкой стоимости алюминий вышел из моды.
В настоящее время самые первые алюминиевые изделия представляют большую редкость. Большинство из них не пережило обесценивания металла и было заменено серебром, золотом и другими драгоценными металлами и сплавами. В последнее время вновь наблюдается повышенный интерес к алюминию у специалистов. Этот металл стал темой отдельной выставки , организованной в 2000 году Музеем Карнеги в Питсбурге. Во Франции расположен Институт истории алюминия, который в частности занимается исследованием первых ювелирных изделий из этого металла.
Большинство из них не пережило обесценивания металла и было заменено серебром, золотом и другими драгоценными металлами и сплавами. В последнее время вновь наблюдается повышенный интерес к алюминию у специалистов. Этот металл стал темой отдельной выставки , организованной в 2000 году Музеем Карнеги в Питсбурге. Во Франции расположен Институт истории алюминия, который в частности занимается исследованием первых ювелирных изделий из этого металла.
В Советском союзе из алюминия делали общепитовские приборы, чайники и т.д. И не только. Первый советский спутник был выполнен из алюминиевого сплава. Другой потребитель алюминия — электротехническая промышленность: из него делаются провода высоковольтных линий передач, обмотки моторов и трансформаторов, кабели, цоколи ламп, конденсаторы и многие другие изделия. Кроме того, порошок алюминия применяют во взрывчатых веществах и твердом топливе для ракет, используя его свойство быстро воспламеняться: если бы алюминий не покрывался тончайшей оксидной пленкой, то мог бы вспыхивать на воздухе.
Последнее изобретение — пеноалюминий, т.н. «металлический поролон», которому предсказывают большое будущее.
общая характеристика, строение; свойства и получение — урок. Химия, 8–9 класс.
Алюминий как атом и химический элемент
Алюминий находится в \(IIIA\) группе Периодической системы химических элементов Д. И. Менделеева.
Строение электронной оболочки атома алюминия — 1s22s22p63s23p1.
На внешнем электронном уровне атом содержит \(3\) электрона.
Поэтому в своих соединениях алюминий всегда проявляет только одну степень окисления, равную \(+3\).
Обрати внимание!
По распространённости в земной коре алюминий находится на третьем месте после кислорода и кремния, а среди металлов — на первом.
В земной коре алюминий встречается только в составе соединений.
Основные природные минералы алюминия:
- боксит, состав которого можно примерно выразить формулой Al2O3 \(•\) xh3O,
- нефелин (Na,K)O2 \(•\) Al2O3 \(•\) 2h3O,
- каолинит Al2O3 \(•\) SiO2 \(•\) 2h3O.

Каолинит — образец многочисленных алюмосиликатов, включающих преимущественно атомы кремния и кислорода, которые очень широко распространены в природе.
Физические свойства
В свободном состоянии алюминий — светлый блестящий металл, лёгкий, относительно мягкий, легкоплавкий, имеет высокую тепло- и электропроводность.
Алюминий является химически активным металлом, однако при обычных условиях он устойчив на воздухе и сохраняет свой металлический блеск длительное время. Это объясняется тем, что поверхность алюминия покрыта тонкой, невидимой глазу, прозрачной, но плотной плёнкой оксида алюминия, которая препятствует взаимодействию алюминия с компонентами атмосферы (парами воды и кислородом).
Свойства алюминия обусловили его широкое применение и необходимость получения алюминия в свободном виде.
В лабораторных условиях небольшое количество алюминия можно получить путём восстановления хлорида алюминия калием при высокой температуре:
AlCl3+3K=t3KCl+Al.
Так был впервые получен алюминий.
В промышленных условиях алюминий получают из бокситов. При нагревании бокситов образуется оксид алюминия. Восстановить алюминий из оксида с помощью традиционных восстановителей практически невозможно, поэтому его получают методом электролиза.
При этом на катоде восстанавливается алюминий, а на аноде — окисляется кислород.
Суммарная реакция электролиза выражается уравнением:
2Al2O3=4Al+3O2↑.
Контрольная работа по химии для 9 класса «Металлы»
Контрольная работа №2
Вариант 1
- Охарактеризуйте алюминий по его положению в периодической системе.
А) группа, подгруппа, период, строение атома, степень окисления
Б) Характер простого вещества (металл, неметалл)
В) Сравнение металлических свойств с магнием и галлием
Г) Состав высшего оксида, его характер
Д) Состав высшего гидроксида, его характер
- Осуществите превращения:
Al →Al2O3 →Al2(SO4)3 →Al(OH)3 →Al2O3
- Сколько литров водорода выделится при действии избытка соляной кислоты на 2,7г алюминия, если выход водорода составляет 90% от теоретического?
Контрольная работа №2
«Металлы»
Вариант 2
- Охарактеризуйте магний по его положению в периодической системе.

А) группа, подгруппа, период, строение атома, степень окисления
Б) Характер простого вещества(металл, неметалл)
В) Сравнение металлических свойств с натрием и кальцием
Г) Состав высшего оксида, его характер
Д) Состав высшего гидроксида, его характер
- Осуществите превращения:
- 3→MgCl2→Mg(OH)2→MgO →MgCl2
- Сколько грамм оксида магния можно получить разложением карбоната магния массой 10г, если выход реакции составляет 90% от теоретического.
Просмотр содержимого документа
«Контрольная работа по химии для 9 класса «Металлы» »
Контрольная работа №2
«Металлы»
Вариант 1
Охарактеризуйте алюминий по его положению в периодической системе.

А) группа, подгруппа, период, строение атома, степень окисления
Б) Характер простого вещества (металл, неметалл)
В) Сравнение металлических свойств с магнием и галлием
Г) Состав высшего оксида, его характер
Д) Состав высшего гидроксида, его характер
Осуществите превращения:
Al →Al2O3 →Al2(SO4)3 →Al(OH)3 →Al2O3
Сколько литров водорода выделится при действии избытка соляной кислоты на 2,7г алюминия, если выход водорода составляет 90% от теоретического?
Контрольная работа №2
«Металлы»
Вариант 2
Охарактеризуйте магний по его положению в периодической системе.
А) группа, подгруппа, период, строение атома, степень окисления
Б) Характер простого вещества(металл, неметалл)
В) Сравнение металлических свойств с натрием и кальцием
Г) Состав высшего оксида, его характер
Д) Состав высшего гидроксида, его характер
Осуществите превращения:
MgCO3→MgCl2→Mg(OH)2→MgO →MgCl2
Сколько грамм оксида магния можно получить разложением карбоната магния массой 10г, если выход реакции составляет 90% от теоретического.

Природные ресурсы мировой экономики
№2(29), 2014
Материалы из будущего учебника по мировой экономике и международным экономическим отношениям
В.Горбанев, д.геогр.н, профессор
И.Митрофанова, к.геогр.н., доцент
Природные ресурсы — это компоненты природной среды, используемые в процессе производства для удовлетворения материальных и культурных потребностей общества.[1]
Природные ресурсы по своей сути имеют физическое происхождение, однако в процессе их использования они становятся экономическим ресурсом.
Природные ресурсы делятся на неисчерпаемые (агроклиматические, геотермальные, гидроэнергетические) и исчерпаемые. В свою очередь, исчерпаемые ресурсы делятся на невозобновляемые (минеральные) и возобновляемые (земельные, водные, биологические, рекреационные). Базируясь на этой классификации и развивая ее, данный учебник выделяет следующие виды природных ресурсов: минеральные (полезные ископаемые), энергетические, водные, биологические, земельные, агроклиматические, рекреационные.
При рассмотрении природных ресурсов важно оценивать ресурсообеспеченность, т.е. соотношение между разведанными запасами ресурсов и объемами их использования. Ресурсообеспеченность исчерпаемых невозобновляемых ресурсов оценивается количеством лет, на которые хватит этих ресурсов при современном уровне добычи. Для возобновляемых ресурсов определяют величину этих ресурсов, приходящуюся на душу населения.
Ресурсы минерального сырья в мире
Минеральное сырье по своему геологическому происхождению и назначению можно разделить на топливное, рудное, химическое, строительное и техническое.
По степени изученности запасы минеральных ресурсов подразделяются на четыре категории — разведанные (промышленные) — А, В и С1 и предварительно оцененные С2.
К категории, А (достоверные запасы) относят детально разведанные и изученные запасы с точным определением границ тел полезных ископаемых, на запасах этой категории уже ведется промышленная разработка, а допустимая погрешность в оценке запасов составляет до 10% от их объема. К категории В относят запасы, которые разведаны и изучены с детальностью, обеспечивающей выяснение основных особенностей условий залегания, но без точного отражения пространственного положения каждого типа, и при этом запасы этой категории либо еще не разрабатываются, либо находятся в начальной стадии разработки, а допустимая погрешность в оценке не превышает 15%. Категория С1 включает в себя запасы, которые либо находятся в стадии разведки, либо по которым была осуществлена разведка и проведена их частичная оценка, а допустимая погрешность в оценке этих запасов не должна превышать 25%. Запасы категории С2 (потенциальные) относятся к предварительно оцененным, когда границы месторождений не определены, проведение разведочных работ только планируется, а погрешность в оценках объема запасов может достигать 50%.
К категории В относят запасы, которые разведаны и изучены с детальностью, обеспечивающей выяснение основных особенностей условий залегания, но без точного отражения пространственного положения каждого типа, и при этом запасы этой категории либо еще не разрабатываются, либо находятся в начальной стадии разработки, а допустимая погрешность в оценке не превышает 15%. Категория С1 включает в себя запасы, которые либо находятся в стадии разведки, либо по которым была осуществлена разведка и проведена их частичная оценка, а допустимая погрешность в оценке этих запасов не должна превышать 25%. Запасы категории С2 (потенциальные) относятся к предварительно оцененным, когда границы месторождений не определены, проведение разведочных работ только планируется, а погрешность в оценках объема запасов может достигать 50%.
Топливные минеральные ресурсы
Топливное минеральное сырье имеет осадочное происхождение, поэтому размещено неравномерно и приурочено к осадочным чехлам платформенных структур. К топливным ресурсам прежде всего относится «большая тройка» — нефть, природный газ и уголь, продуцирующие более 80% производимой в мире энергии (см. табл.11.5). Мировые геологические запасы минерального топлива оцениваются примерно в 13 трлн.т., т.е. обеспеченность человечества минеральным топливом составляет порядка 1000 лет. Причем на уголь приходится 60% запасов (по теплотворной способности), а на углеводородное топливо — 27%. В то же время структура мирового потребления первичных источников энергии складывается иная: в 2012 г. на уголь приходится около 30%, нефть — примерно 33%, газ — около 24%. Первое место в мире по разведанным запасам угля занимают США, по запасам нефти — Венесуэла и по запасам природного газа — Иран, который недавно несколько обошел Россию.
К топливным ресурсам прежде всего относится «большая тройка» — нефть, природный газ и уголь, продуцирующие более 80% производимой в мире энергии (см. табл.11.5). Мировые геологические запасы минерального топлива оцениваются примерно в 13 трлн.т., т.е. обеспеченность человечества минеральным топливом составляет порядка 1000 лет. Причем на уголь приходится 60% запасов (по теплотворной способности), а на углеводородное топливо — 27%. В то же время структура мирового потребления первичных источников энергии складывается иная: в 2012 г. на уголь приходится около 30%, нефть — примерно 33%, газ — около 24%. Первое место в мире по разведанным запасам угля занимают США, по запасам нефти — Венесуэла и по запасам природного газа — Иран, который недавно несколько обошел Россию.
Таблица 1
Первые восемь стран по разведанным запасам топливных ресурсов в 2012 г.
Страна |
Уголь |
Страна |
Нефть |
Страна |
Природный |
|
США |
237 |
Венесуэла |
298 |
Иран |
34 |
|
Россия |
157 |
Саудовская Аравия |
268 |
Россия |
33 |
|
Китай |
115 |
Канада |
173 |
Катар |
21 |
|
Австралия |
76 |
Иран |
155 |
Туркмения |
17 |
|
Индия |
61 |
Ирак |
141 |
США |
9 |
|
Германия |
40 |
Кувейт |
104 |
Саудовская Аравия |
8 |
|
Украина |
34 |
ОАЭ |
98 |
Венесуэла |
5 |
|
Казахстан |
34 |
Россия |
80 |
Нигерия |
5 |
Источник: US Energy International Administration. International Energy Outlook, 2013.
International Energy Outlook, 2013.
Достоверные запасы угля сегодня оцениваются в 860 млрд.т, причем более половины из них приходится на каменный уголь и остальное — на менее калорийный бурый, а обеспеченность планеты углем составляет 400 лет. Наиболее богатыми углем оказываются США (на них приходится 28% достоверных мировых запасов), Австралия (9%), Германия (5%), а из менее развитых стран — Россия (более 18%), Китай (13%) и Индия (7%). Таким образом, на США, Россию, Китай и Австралию приходится около 70% мировых достоверных запасов угля. Если же оценивать запасы качественных коксующихся углей (они нужны для выплавки металлов), то на первые места выходят Австралия, Германия, Китай и США.
Сегодня уголь добывается примерно в 80 странах. Каменного угля добывается около 3,5 млрд. т, бурого — 1,2 млрд. т. Во многих развитых странах, начиная со второй половины ХХ века, угледобывающую промышленность поразил структурный кризис, вызванный с одной стороны острейшей конкуренцией со стороны нефтегазовой промышленности, а с другой — неблагоприятными физико-географическими и экологическими условиями добычи. В частности, сократилась добыча угля, отличающегося повышенной сернистостью. В результате многие развитые страны стали в большей степени ориентироваться на импортный уголь, к тому же еще и более дешевый. Так, практически прекратилась добыча угля во Франции и Бельгии, а старейшие каменноугольные районы — Рурский и Саарский в Германии, Аппалачский в США испытывают кризис. Несколько более стабильная ситуация сложилась с буроугольными и теми каменноугольными бассейнами, где добыча ведется более дешевым открытым способом.
В частности, сократилась добыча угля, отличающегося повышенной сернистостью. В результате многие развитые страны стали в большей степени ориентироваться на импортный уголь, к тому же еще и более дешевый. Так, практически прекратилась добыча угля во Франции и Бельгии, а старейшие каменноугольные районы — Рурский и Саарский в Германии, Аппалачский в США испытывают кризис. Несколько более стабильная ситуация сложилась с буроугольными и теми каменноугольными бассейнами, где добыча ведется более дешевым открытым способом.
Структурный кризис не коснулся менее развитых стран, где бурно развивается промышленность и энергетика и в то же время низка стоимость рабочей силы: здесь угольная промышленность, наоборот, испытывает бурный подъем. В настоящее время на 1-е место по добыче угля вышел Китай. Еще совсем недавно в стране добывали 1 млрд. т угля, а в 2012 г. уже было добыто 3,5 млрд.т. Крупнейшими разработчиками угля остаются также США (993 млн. т, хотя объемы добычи падают), Индия (590 млн. т.), Австралия, Индонезия, Россия (354 млн. т.), Германия, ЮАР, Колумбия. Особенно быстро растет добыча угля в Индонезии и Колумбии. Крупнейшими мировыми экспортерами угля в последние годы стали Австралия, Индонезия (2-е место в мире), Россия (экспортирует 19% добываемого угля.), США, Колумбия, ЮАР.
т.), Австралия, Индонезия, Россия (354 млн. т.), Германия, ЮАР, Колумбия. Особенно быстро растет добыча угля в Индонезии и Колумбии. Крупнейшими мировыми экспортерами угля в последние годы стали Австралия, Индонезия (2-е место в мире), Россия (экспортирует 19% добываемого угля.), США, Колумбия, ЮАР.
Таблица 2
Ведущие страны по производству, экспорту и потреблению топливных ресурсов
(в скобках указано место страны)
Нефть (млн. барр./день) |
Газ (млрд. м3/год) |
Уголь (млн. т/год) |
|||||||||
|
Страна |
Добыча, |
Экспорт, |
Потребление, |
Страна |
Добы |
Экспорт, |
Потребление, |
Страна |
Добыча, |
Экспорт, |
Потребление, |
|
Россия |
10,6(2) |
7,2 (2) |
2,2 (8) |
США |
681 (1) |
32,2 (8) |
722 (1) |
Китай |
3520 (1) |
22,2 (10) |
4053 (1) |
|
Саудовская Аравия |
11,5(1) |
8,9 (1) |
2,6 (5) |
Россия |
592(2) |
185,8 (1) |
416 (2) |
США |
992,2 (2) |
114,0 (4) |
1003 (2) |
|
США |
8,9 (3) |
1,5 |
19,0 (1) |
Канада |
156(5) |
92,4 (4) |
101 (7) |
Индия |
588,5 (3) |
— |
788 (3) |
|
Иран |
3. |
1,9 (7) |
1,9 |
Катар |
157 (4) |
94,8 (3) |
26 |
Австра- лия |
415,5 (4) |
328,1 (1) |
— |
|
Китай |
4,1 (4) |
0,5 |
9,5 (2) |
Иран |
160 (3) |
7,9 |
156 (3) |
Россия |
353,5 (5) |
122,1 (3) |
262 (4) |
|
Канада |
3,7 (5) |
1,6 (9) |
2,2 (7) |
Норвегия |
115(6) |
99,7 (2) |
4 |
Индонезия |
324,9 (6) |
316,2 (2) |
— |
|
Ирак |
3,1 (9) |
2,2 (6) |
0,7 |
Китай |
107 (7) |
3,8 |
144 (4) |
ЮАР |
255,1 (7) |
76,7 (5) |
210 (6) |
|
ОАЭ |
3,4 (7) |
2,6(3) |
0,5 |
Саудовская Аравия |
103 (8) |
— |
103 (6) |
Германия |
188,6 (8) |
— |
256 (5) |
|
Венесуэла |
2,7 |
1,7(9) |
0,7 |
Индонезия |
71 (10) |
42,3 (7) |
37 |
Польша |
139,2 (9) |
18,1 |
162 (8) |
|
Мексика |
2,9 (10) |
1,5 |
2,1 (10) |
Нидерланды |
64 |
57,7 (5) |
36 |
Казах-стан |
115,9 (10) |
36,3 (8) |
— |
|
Кувейт |
3,1(8) |
2,4 (4) |
0,3 |
Алжир |
81(9) |
55,3 (6) |
31 |
Колумбия |
85,8 |
76,4 (6) |
— |
|
Нигерия |
2,4 |
2,2 (5) |
0,3 |
Малайзия |
65 |
30,8 (9) |
33 |
Канада |
68,2 |
36,9 (7) |
— |
|
Норвегия |
1,9 |
1. |
0,3 |
Велик-я |
41 |
15,6 |
78 (9) |
Вьетнам |
44,5 |
24,7 (9) |
— |
|
Индия |
0,9 |
0,8 |
3,2 (4) |
Австра-я |
49 |
24,7 (10) |
25 |
Япония |
— |
— |
202 (7) |
|
Германия |
0,2 |
0,5 |
2,5 (6) |
Германия |
9 |
16,2 |
75 (10) |
||||
|
Япония |
0,1 |
— |
4,5 (3) |
Италия |
8 |
0,1 |
69 |
||||
|
Республика Корея |
0,05 |
1,1 |
2,2 (9) |
Япония |
3 |
— |
117 (5) |
||||
|
Ангола |
1,8 |
1,7(8) |
0,1 |
Мексика |
58 |
64 |
84 (8) |
||||
Источник: BP Statistical Review of World Energy, 2013
Достоверные запасы нефти в мире оцениваются в 236 млрд.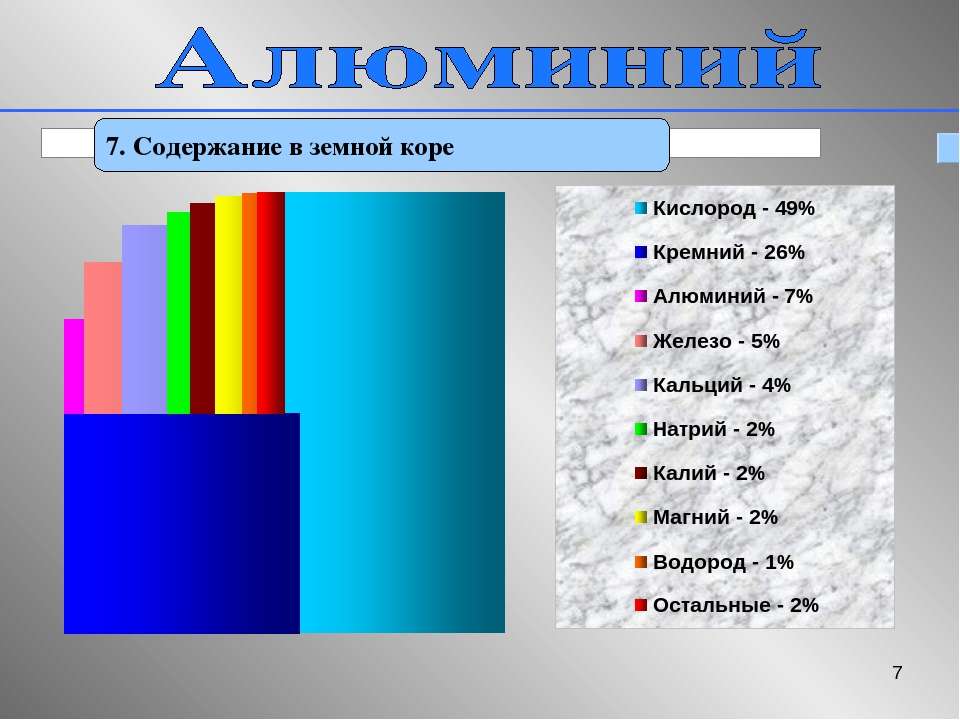 т, а ресурсообеспеченность нефтью оценивается в 55 лет. При с начала 1990-х гг обеспеченность нефтью и газом возросла на 60–65%, а объем добычи возрос всего на 25%, что говорит об опережающем развитии геологоразведочных работ. Однако геологоразведка, как и добыча, все больше перемещаются в районы с тяжелыми природными условиями с их более высокими издержками добычи. Так, более 30% запасов нефти находится в шельфовых зонах морей и океанов, поэтому в ряде стран, например, Великобритании, Норвегии, Габоне добыча нефти идет исключительно со дна моря. По прогнозам, огромные запасы углеводородного сырья сосредоточены на шельфовых морях Арктики и Дальнего Востока.
т, а ресурсообеспеченность нефтью оценивается в 55 лет. При с начала 1990-х гг обеспеченность нефтью и газом возросла на 60–65%, а объем добычи возрос всего на 25%, что говорит об опережающем развитии геологоразведочных работ. Однако геологоразведка, как и добыча, все больше перемещаются в районы с тяжелыми природными условиями с их более высокими издержками добычи. Так, более 30% запасов нефти находится в шельфовых зонах морей и океанов, поэтому в ряде стран, например, Великобритании, Норвегии, Габоне добыча нефти идет исключительно со дна моря. По прогнозам, огромные запасы углеводородного сырья сосредоточены на шельфовых морях Арктики и Дальнего Востока.
Подавляющая часть достоверных запасов нефти находится, а Азии, только в одном бассейне Персидского залива сосредоточено более 48% мировых запасов нефти. Долгое время лидером по запасам нефти была Саудовская Аравия (16% мировых запасов), но недавно ее обошла Венесуэла (18%). Далее идут Канада Иран и Ирак (по 9–10%), Кувейт, ОАЭ, Россия (5%). Канада раньше не отличалась большими запасами нефти, но после нахождения в провинции Альберта уникальных «нефтяных песков» Канада вышла в число ведущих стран по этому показателю (10%).
Канада раньше не отличалась большими запасами нефти, но после нахождения в провинции Альберта уникальных «нефтяных песков» Канада вышла в число ведущих стран по этому показателю (10%).
До начала 1970-х гг. мировая добыча нефти росла быстрыми темпами, однако после тогдашнего энергетического кризиса цена нефти резко поднялась, изменилась и география нефтедобычи — она стала перемещаться в труднодоступные места. Соответственно уровень мировой добычи нефти стал расти медленнее и сейчас составляет более 3,6 млрд. т в год. Однако если в странах ОЭСР происходит падение или очень медленный рост потребления нефти, то в остальных странах имеет место рост потребления нефти на 3,0–3,5%, что поддерживает рост ее добычи по миру в целом в районе 1%.
В 2012 г. Россия была на 2-м месте по добыче нефти (10.600 млн. барр. в день) после Саудовской Аравии (11.500 млн барр. в день). На 3-м месте стоят США (8.900 млн. барр. в день). В 2013 г., по российским данным, Россия добывала 10.800 млн барр. в сутки. Однако США (8, 4 млн. барр. в день) они имеют все шансы уже в обозримой перспективе стать мировым лидером в добыче нефти, оставив позади и Саудовскую Аравию и Россию: добыча нефти здесь растет максимальными за последние 150 лет темпами. Такое резкое увеличение объемов добычи в США становится возможным благодаря активной добыче сланцевой нефти в отдельных штатах. Крупнейшими разработчиками нефти являются также Норвегия, Иран, КНР, Канада, Ирак, ОАЭ, Мексика, Кувейт и ряд других стран. Особо следует отметить роль стран-членов ОПЕК, которые сосредотачивают 73% достоверных запасов нефти, хотя их доля в добыче в 2012 г. снизилась до 43%. Тем не менее они остаются основными мировыми экспортерами нефти и в первую очередь это Саудовская Аравия, Иран, ОАЭ.
в сутки. Однако США (8, 4 млн. барр. в день) они имеют все шансы уже в обозримой перспективе стать мировым лидером в добыче нефти, оставив позади и Саудовскую Аравию и Россию: добыча нефти здесь растет максимальными за последние 150 лет темпами. Такое резкое увеличение объемов добычи в США становится возможным благодаря активной добыче сланцевой нефти в отдельных штатах. Крупнейшими разработчиками нефти являются также Норвегия, Иран, КНР, Канада, Ирак, ОАЭ, Мексика, Кувейт и ряд других стран. Особо следует отметить роль стран-членов ОПЕК, которые сосредотачивают 73% достоверных запасов нефти, хотя их доля в добыче в 2012 г. снизилась до 43%. Тем не менее они остаются основными мировыми экспортерами нефти и в первую очередь это Саудовская Аравия, Иран, ОАЭ.
Достоверные запасы природного газа в мире растут большими темпами и сегодня они оцениваются в 187 трлн. м3, причем все больше благодаря месторождениям на труднодоступных территориях. В результате добыча газа, также как и нефтедобыча, активно перемещается на шельфовые зоны морей и океанов, где сейчас добывается 28% всего газа. Ресурсообеспеченность газом оценивается в 70 лет.
Ресурсообеспеченность газом оценивается в 70 лет.
В отличии от нефтедобычи динамика добычи газа в последние десятилетия отличается быстрым ростом и сейчас достигла 3,6 трлн. м3 в год, увеличиваясь в последние годы на 2–3%. Первое место в мире занимают США, которые в 2012 г. добыли 680 млрд. м3, все больше наращивая добычу сланцевого газа. Чуть меньше добывает газа Россия, которая в 2012 г. чуть снизила добычу до 653 млрд. м3 из-за медленного роста спроса на газ в ЕС. Далее с большим отрывом идут Канада, Катар, Иран Норвегия, Нидерланды, КНР и другие страны. Основными мировыми экспортерами природного газа являются Россия, Норвегия, Катар, Канада, Нидерланды, а в ближайшие годы — и США.
Рудные и другие минеральные ресурсы
Рудное минеральное сырье в отличие от осадочного топливного имеет за редким исключением магматическое или метаморфическое происхождение, поэтому приурочено к складчатым тектоническим структурам, к щитам, к разломам земной коры.
Урановые руды часто относят к топливным минеральным ресурсам, поскольку главное назначение урана — топливо для ядерных ректоров, устанавливаемых на АЭС. Оценки геологических запасов урановых руд сильно разнятся, хотя достоверные запасы, по данным МАГАТЭ, определены достаточно точно — 3,6 млн. т и сосредоточены в 44 государствах мира (2005 г.). Первое место безраздельно принадлежит Австралии — около 30% мировых запасов, далее идут Казахстан — 17%, Канада — около 12%, ЮАР — 10%, затем Намибия, Бразилия, Россия и др. Однако по новым российским данным Россия вышла на 2-е место в мире, обойдя Казахстан — 18% мировых запасов.
В то же время добыча руд и производство концентрата из него характеризуется несколько иной географией. Добыча урановых руд ведется в 25 странах мира: в Казахстане (33% мировой добычи), Канаде (18%), Австралии (11%), а также Намибии и Нигере (по 8%), России (7%), Узбекистане, США, ЮАР, Габоне. При этом объемы добычи урановой руды отличаются сильными колебаниями: максимальные объемы были достигнуты в конце 1970-х гг. во время энергетического кризиса, затем шло падение объемов производства, особенно после чернобыльской аварии, а с 2005 г. до 2009 г.г объемы добычи урана выросли более чем в 1,5 раза, прежде всего за счет Казахстана.
во время энергетического кризиса, затем шло падение объемов производства, особенно после чернобыльской аварии, а с 2005 г. до 2009 г.г объемы добычи урана выросли более чем в 1,5 раза, прежде всего за счет Казахстана.
Железные руды имеют широкое распространение в земной коре и их разведанные запасы оцениваются в 160 млрд. т. Содержание железа в них колеблется в широких пределах — от 20% до 68%. По разведанным запасам железных руд господствует Украина (45% мировых запасов), далее идут Австралия (20%), Бразилия (17%), Россия (15%), Китай, Индия, США. Однако содержание железа в рудах не соответствует указанному ранжиру — самыми богатыми рудами обеспечены Либерия, Индия, Австралия, Бразилия, Венесуэла — руды в этих странах содержат более 60% полезного компонента.
Крупнейшими разработчиками железной руды в 2012 г. были Китай (43% мировой добычи), Австралия (20%), Бразилия (17%), Индия, Россия, Украина — всего железные руды добываются в 43 странах, в том числе на экспорт. Ряд стран, ранее ориентировавшихся на собственную железную руду, переходят на ее импорт и в первую очередь это относится к ЕС.
Самый распространенный в земной коре металл — это алюминий, причем концентрируется он в осадочных горных породах. Разведанные запасы бокситов в мире оцениваются в 30 млрд.т. Руды легких цветных металлов, в том числе бокситы, отличаются большим содержание полезного компонента — в бокситах его содержание составляет 30–60%. Наибольшими запасами бокситов обладают Гвинея (27% мировых разведанных запасов), Австралия (25%), Бразилия, Ямайка, КНР, Индия, Вьетнам, хотя последний, благодаря новым разведенным запасам, может занять первую строчку в рейтинге. Крупнейшими разработчиками бокситов являются Австралия (33% мировой добычи), КНР (19%), Бразилия (15%), Индия, Гвинея, Ямайка — всего порядка 30 стран. Некоторые развитые страны, такие как США, Франция, Греция, Венгрия или вообще прекратили добычу бокситов, или значительно ее сократили. Россия также ориентируется на импорт бокситов.
Руды тяжелых цветных металлов содержат значительно меньше полезного компонента. Так, содержание меди в рудах обычно составляет менее 5%. Крупнейшие страны-разработчики медных руд — это Чили (36% мировой добычи), США, Перу, КНР, Австралия, Россия, Индонезия (всего около 50 стран).
Крупнейшие страны-разработчики медных руд — это Чили (36% мировой добычи), США, Перу, КНР, Австралия, Россия, Индонезия (всего около 50 стран).
По запасам и добыче остальных минеральных ресурсов ведущие позиции занимает небольшой спектр стран. Так, более 70% мировой добычи марганца сосредоточено в Китае, ЮАР, Австралии, Габоне, Казахстане и Индии; хрома — в ЮАР, Казахстане, Индии, Зимбабве, Финляндии; свинца — в Австралии, Китае, США, Перу, Канаде; цинка — в КНР, Австралии, Перу, Канаде, США, Мексике; олова — в КНР, Перу, Индонезии, Бразилии, Боливии, Австралии, Малайзии, России; никеля — в России (25% мировой добычи), Канаде, Австралии, Индонезии, Франции (Новой Каледонии), Колумбии; кобальта — в ДРК (53% мировой добычи), Канаде, Китае, России, Замбии; вольфрама — в Китае (85% мировой добычи), России, Канаде, Австрии.
Среди нерудного сырья следует выделить химическое сырье: фосфориты, апатиты, соли, серу. Фосфориты добываются почти в 30 странах мира, среди которых лидируют США, Китай, Марокко, Тунис. По добыче натриевой соли выделяются США, Китай, Германия, Индия, Канада; калийной соли — Канада, Беларусь, Германия, Россия, Израиль.
По добыче натриевой соли выделяются США, Китай, Германия, Индия, Канада; калийной соли — Канада, Беларусь, Германия, Россия, Израиль.
12.2. Земельные, водные, лесные и рекреационные ресурсы мира
За период только после 1960 г. производство продовольствия в мире увеличилось в 2,5 раза, потребление воды — в 2 раза, вырубка лесов — в 3 раза. Все это обострило внимание к обеспеченности мира земельными, водными, лесными ресурсами.
Таблица 3
Обеспеченность ряда стран пахотными землями, лесными и водными ресурсами, в расчете на жителя
Страна |
Пашня, га |
Страна |
Леса, га |
Страна |
Пресная вода, |
|
Австралия |
2,4 |
Габон |
36,0 |
Демократическая Республика Конго |
230 |
|
Казахстан |
1,9 |
Канада |
15,8 |
Норвегия |
80 |
|
Канада |
1,5 |
Россия |
5,5 |
Канада |
87 |
|
Россия |
0,9 |
Финляндия |
5,0 |
Венесуэла |
44 |
|
Аргентина |
0,9 |
Бразилия |
2,5 |
Бразилия |
42 |
|
США |
0,6 |
США |
0,9 |
Россия |
32 |
|
Индия |
0,17 |
Китай |
0,1 |
Австралия |
83 |
|
Германия |
0,1 |
Индия |
0,08 |
Китай |
2 |
|
Китай |
0,07 |
Германия |
0,06 |
Германия |
2 |
Земельные ресурсы
Земельные ресурсы — это площадь суши. Часть ее не имеет почвенного покрова (например, ледники) и поэтому не может быть базой для производства сельскохозяйственного сырья и продовольствия. Общий земельный фонд мира (площадь суши за вычетом ледников Арктики и Антарктики) равен 13,4 млрд. га., или более 26% всей площади нашей планеты.
Часть ее не имеет почвенного покрова (например, ледники) и поэтому не может быть базой для производства сельскохозяйственного сырья и продовольствия. Общий земельный фонд мира (площадь суши за вычетом ледников Арктики и Антарктики) равен 13,4 млрд. га., или более 26% всей площади нашей планеты.
Структура земельного фонда с точки зрения развития сельского хозяйства выглядит не самым лучшим образом. Так, на обрабатываемые земли (пашня, сады, плантации) приходится 11%, на луга и пастбища — еще 26%, а остальное занимают леса и кустарники — 32%, земли под населенными пунктами, объектами промышленности и транспорта — 3%, малопродуктивные и непродуктивные земли (болота, пустыни и территории с экстремальными климатическими изотермами) — 28%.
Таким образом, сельскохозяйственные угодья (пашня, сады, плантации, луга и пастбища) составляют лишь 36% земельного фонда (4,8 млрд. га) и их увеличение в последние годы хоть и продолжаться, но медленно. По величине сельскохозяйственных угодий среди стран мира выделяются Китай, Австралия, США, Канада, Россия. В структуре сельскохозяйственных угодий площадь пашни составляет 28% (1,3 млрд. га), пастбищ — 70% (3,3 млрд. га), многолетних насаждений — 2%.
В структуре сельскохозяйственных угодий площадь пашни составляет 28% (1,3 млрд. га), пастбищ — 70% (3,3 млрд. га), многолетних насаждений — 2%.
По мере роста населения обеспеченность сельскохозяйственными землями снижается: если в 1980 г. на душу населения мира приходилось 0,3 га пашни, то в 2011 г. — 0,24 га. В Северной Америке на душу населения приходится 0,65 га пахотной земли, Западной Европе — 0,28 га, Зарубежной Азии — 0,15 га, Южной Америке — 0,49 га, Африке — 0,30 га. Велики контрасты и между странами (см. табл. 12.3).
Уменьшение земельных ресурсов как общемировая тенденция происходит за счет отторжения продуктивных земель под предприятия, города и другие населенные пункты, развития транспортной сети. Огромные площади возделываемых земель утрачиваются в результате эрозии, засоления, заболачивания, опустынивания, физической и химической деградации. По данным ФАО общая площадь потенциально пригодных земель для земледелия в мире составляет около 3,2 млрд. га. Однако для включения в сельскохозяйственное производство этого резерва требуется колоссальное вложение труда и средств.
В развитых странах преобладает частное землевладение. Большая часть земельного фонда находится в руках крупных землевладельцев (фермеров и компаний) и сдается в аренду. Для развивающихся стран характерно разнообразие форм земельных отношений. Это и крупное помещичье землевладение, частное, иностранное, общинные земли, арендованные, имеются малоземельные и безземельные крестьянские хозяйства. В целом в мире доминирует частная форма землевладения, однако значительная доля крестьянских хозяйств (28%) не имеет собственной земли и вынуждена ее арендовать.
Водные ресурсы
Вода является необходимым условием существования всех живых организмов. С использованием водных ресурсов связана не только жизнь, но и хозяйственная деятельность человека.
Из общего количества воды на земле столь нужная для человечества пресная вода составляет 2,5% общего объема гидросферы (водной оболочки земли, представляющей собой совокупность морей, океанов, поверхностных вод суши, подземных вод, льдов, снегов Антарктиды и Арктики, атмосферных вод), или примерно 35 млн. м3, что превышает нынешние потребности человечества более чем в 10 тыс. раз, а остальные 97,5% объема гидросферы составляют воды мирового океана и соленые воды поверхностных и подземных озер.
м3, что превышает нынешние потребности человечества более чем в 10 тыс. раз, а остальные 97,5% объема гидросферы составляют воды мирового океана и соленые воды поверхностных и подземных озер.
Подавляющая часть пресных вод (70%) находится в полярных и горных льдах и вечной мерзлоте, которые практически не используются. Всего лишь 0,12% общего объема гидросферы составляют поверхностные воды рек, пресноводных озер, болот. Запасы пресных вод, пригодных для всех видов использования, называются водными ресурсами. Главным источником удовлетворения потребностей человечества в пресной воде являются речные воды. Их единовременный объем крайне мал — 1,3 тыс. км3, но поскольку этот объем возобновляется 23 раза в течение года, то фактический объем доступных пресных вод составляет 42 тыс. км3 (это, примерно, два Байкала). Это наш «водный паек», хотя реально можно использовать только половину этого количества.
Распределение пресной воды по земному шару крайне неравномерно. В Европе и Азии, где проживает 70% населения мира, сосредоточено лишь 39% речных вод. Многие страны находятся на грани кризиса по степени обеспеченности водными ресурсами — например, страны Персидского залива, малые островные государства. Одновременно выделяются страны с высокой степенью обеспеченности, в числе которых и Россия (см. табл. 12.3).
В Европе и Азии, где проживает 70% населения мира, сосредоточено лишь 39% речных вод. Многие страны находятся на грани кризиса по степени обеспеченности водными ресурсами — например, страны Персидского залива, малые островные государства. Одновременно выделяются страны с высокой степенью обеспеченности, в числе которых и Россия (см. табл. 12.3).
По ресурсам поверхностных вод ведущее место в мире занимает Россия. Средний суммарный сток рек составляет 4270 км3 в год в основном за счет таких рек, как Енисей, Ангара, Обь, Печора, Северная Двина и др. Эксплуатационные ресурсы подземных вод составляют 230 км3 в год. В целом в России на одного жителя приходится 31,9 тыс. м3 пресной воды в год. Тем не менее и в России ряд регионов испытывает нехватку пресной воды (Поволжье, Центрально-Черноземный район, Северный Кавказ, Уральский, Центральный районы), так как ее запасы сосредоточено на Европейском Севере, в Сибири и на Дальнем Востоке.
Объем мирового потребления воды составляет 25% водных ресурсов планеты и, по оценкам ООН, составляет 3973 м3. Можно констатировать, что человечеству в целом не угрожает недостаток чистой питьевой воды. Тем не менее если «водный паек» человечества остается неизменным, то мировое потребление воды с 1960 г. по 2000 г. возрастало на 20% каждые десять лет, хотя за прошедшее десятилетие — лишь на 10%. К тому же, по данным ООН на конец 2000-х гг., более 1,2 млрд. человек на Земле лишено качественной питьевой воды, так как они или проживают в странах с нехваткой пресной воды или около источников воды, загрязненных бытовыми и промышленными отходами.
Можно констатировать, что человечеству в целом не угрожает недостаток чистой питьевой воды. Тем не менее если «водный паек» человечества остается неизменным, то мировое потребление воды с 1960 г. по 2000 г. возрастало на 20% каждые десять лет, хотя за прошедшее десятилетие — лишь на 10%. К тому же, по данным ООН на конец 2000-х гг., более 1,2 млрд. человек на Земле лишено качественной питьевой воды, так как они или проживают в странах с нехваткой пресной воды или около источников воды, загрязненных бытовыми и промышленными отходами.
Главным потребителем воды в мире остается сельское хозяйство (82%), затем промышленность (8%), в быту потребляется всего 10%. В России структура водопотребления иная. Расход воды на промышленные нужды составляет 40%, на сельское хозяйство — 24%, бытовые расходы — 17%. Подобная структура потребления сложилась вследствие высокой доли водоемных отраслей промышленности и расточительного потребления воды в быту. Слабая обеспеченность водными ресурсами южных районов России, являющимися главными сельскохозяйственными районами страны, увеличивает уровень использования воды в сельском хозяйстве. Тем не менее суммарный расход воды в России составляет всего лишь 3% среднемноголетнего стока рек страны.
Тем не менее суммарный расход воды в России составляет всего лишь 3% среднемноголетнего стока рек страны.
Водные ресурсы играют важную роль в развитии мирового энергетического хозяйства. Мировой гидроэнергетический потенциал оценивается в 10 трлн. квт. ч. возможной выработки электроэнергии. Около ½ этого потенциала приходится на 6 стран мира: Россию, Китай, США, ДРК, Канаду, Бразилию.
Лесные ресурсы
Одним из наиболее важных видов биологических ресурсов являются лесные. Как и все остальные биологические ресурсы, они относятся к исчерпаемым, но возобновимым природным ресурсам. Лесные ресурсы оцениваются по размерам лесной площади, запасам древесины на корню, лесистости.
Среднемировая обеспеченность лесными ресурсами составляет 0,6 га на душу населения, и эта цифра также постоянно сокращается, главным образом за счет антропогенного обезлесения. Самая высокая обеспеченность лесными ресурсами (как и водными) — в экваториальных странах и северных странах умеренного пояса: в Суринаме — 36 га на душу населения, в Венесуэле — 11 га, в Бразилии — 2,5 га, в Австралии — 7 га, в России — 5,5 га, в Финляндии — 5 га, в Канаде — 16 га на душу населения. И наоборот в тропических странах и южных странах умеренного пояса обеспеченность лесом намного ниже и составляет менее 0,1 га на человека (см. табл. 12.3).
И наоборот в тропических странах и южных странах умеренного пояса обеспеченность лесом намного ниже и составляет менее 0,1 га на человека (см. табл. 12.3).
Общая лесная площадь составляет в мире 4,1 млрд. га, т.е. около 30% земной суши. Однако только за последние 200 лет лесные площади уменьшились вдвое и продолжают сокращаться со скоростью 25 млн. га, или на 0,6% в год, причем наиболее интенсивно сокращаются тропические леса южного лесного пояса. Так, Латинская Америка и Азия уже потеряли 40% вечнозеленых тропических лесов, а Африка — 5%. Вместе с тем, несмотря на интенсивную эксплуатацию лесов северного пояса в США, Канаде, скандинавских странах благодаря работам по лесовосстановлению и лесоразведению общая площадь лесов в них за последние десятилетия не уменьшилась.
Запасы древесины на корню в мире составляют примерно 350 млрд. м3. Россия занимает первое место по запасам древесины в мире — 25% мировых, или 83 млрд. м3, в т. ч. она обладает почти половиной мировых запасов древесных хвойных пород. Ежегодный прирост древесины, определяющий эксплуатацию лесов без подрыва их воспроизводства, составляет, по оценке, 5,5 млрд. м3. В начале нашего десятилетия объем заготовок древесины составил 5,5 млрд.м3 в год (включая нелегальную вырубку), т.е. объем заготовок был равен годовому приросту древесины. В России естественным путем восстанавливается около трети ежегодно вырубаемых лесов, остальные требуют специальных мер по их возобновлению.
Ежегодный прирост древесины, определяющий эксплуатацию лесов без подрыва их воспроизводства, составляет, по оценке, 5,5 млрд. м3. В начале нашего десятилетия объем заготовок древесины составил 5,5 млрд.м3 в год (включая нелегальную вырубку), т.е. объем заготовок был равен годовому приросту древесины. В России естественным путем восстанавливается около трети ежегодно вырубаемых лесов, остальные требуют специальных мер по их возобновлению.
Показатель лесистости территории — это отношение площади лесов к общей территории страны. Россия по этому показателю лишь занимает 21-е место в мире из-за большой площади тундры и степей.
Рекреационные ресурсы
Под рекреационными ресурсами понимают природные компоненты и антропогенные объекты, обладающие уникальностью, исторической, художественной и эстетической ценностью, целебно-оздоровительной значимостью, предназначенные для организации различных видов отдыха, туризма и лечения. Они подразделяются на природные и антропогенные рекреационные ресурсы. Среди природных рекреационных ресурсов выделяются геологические и геоморфологические, гидрологические, климатические, энергетические, биологические, ландшафтные ресурсы.
Среди природных рекреационных ресурсов выделяются геологические и геоморфологические, гидрологические, климатические, энергетические, биологические, ландшафтные ресурсы.
К первым можно отнести Восточно-Африканский рифт, вулкан Везувий, горы Гималаи, плоскогорье Тибет, Большой барьерный риф у северо-восточного побережья Австралии, красные монолиты Улуру-Ката Тьюта в центре Австралии, фиорды Норвегии, Гранд-Каньон в США, заповедник «Столбы» в Красноярском крае.
К гидрологическим рекреационным ресурсам относят все типы поверхностных и подземных вод, обладающим рекреационными свойствами: озеро Байкал, водопады Анхель в Венесуэле, Игуасу в Аргентине и Бразилии, Ниагарский в США и Канаде, Мертвое море в Израиле и Иордании, каскад горячих горных озер Памук-Кале в Турции, ледник Федченко и Медвежий на Памире, долины гейзеров на Камчатке, в Чили, в Исландии, временно текущие реки на Памире.
К климатическим рекреационным ресурсам относят все курорты мира (приморские, горные, степные, лесные, пустынные, пещерные) и даже некоторые места с экстремальными свойствами климата и погоды (самое холодное место на Земле, самое ветреное, самое влажное, самое жаркое).
Биологические и ландшафтные рекреационные ресурсы объединяют элементы живой и неживой природы: почвенные, флористические и фаунистические ресурсы, представляющие научную, познавательную, медико-биологическую и эстетическую ценность. Среди уникальных биологических ресурсов и ландшафтов мира выделяются: остров Мадагаскар с его экосистемой, насчитывающей 10 тыс. видов эндемичных растений и животных, бассейн Амазонки, кальдера Нгоро-Нгоро и национальный парк Серенгети в Танзании, Горный Алтай, вулканы Камчатки, девственные леса Коми, черноземы и можжевеловые рощи Краснодарского края, кедровая и пихтовая тайга в России, регуры Деканского плоскогорья и старейший национальный парк Корбетт в Индии, Йосемитский и Йеллоустонский национальные парки в США, белые медведи Арктики и пингвины Антарктиды, кенгуру, коала, собака динго, австралийский дьявол в австралийских национальных парках «Голубые горы», «Какаду» и многих других, морские котики Командорских островов, Беловежская Пуща, Галапагосские острова (Эквадор), заповедники в Южной и Экваториальной Африке.
Рекреационные ресурсы антропогенного происхождения можно подразделить на материальные (воплощенные в памятниках архитектуры, музеях, дворцово-парковых ансамблях и т. д.) и духовные, нашедшие отражение в науке, образовании, литературе, народном быте и т. д. Это многочисленные музеи мирового значения, памятники истории и культуры России, европейских стран, Китая, Индии, Японии, Ирана, Мексики, Перу, Египта.
Особо следует отметить объекты всемирного наследия человечества. В 1972 г. ЮНЕСКО приняла Конвенцию о всемирном природном и культурном наследии и стала составлять список объектов Всемирного наследия. В настоящее время в составленном на ее основе списке 911 объектов наследия, в том числе 704 объекта культурного наследия, 180 — природного наследия и 27 — смешанного наследия.
Рекреационные ресурсы являются основой для туризма. В последние десятилетия в мире идет «туристический бум». По данным Всемирной туристской организации, в 2012 г. число только международных туристов в мире достигло 1 млрд. человек, а поступления от международного туризма превысили 1 трлн. долл. Лидерами мирового туризма в 2012 г. были Франция, США, Китай, а по доходам от туризма — США, Испания, Франция (см. табл.11.10).
Природные ресурсы России
Минеральные ресурсы нашей страны крайне разнообразны. На европейской территории и в Западной Сибири, покрытых мощным осадочным чехлом, имеются богатые месторождения осадочных, прежде всего топливных полезных ископаемых. 95% топливных ресурсов страны сосредоточены в её азиатской части. На щитах и в древних складчатых зонах, — в Кольско-Карельском районе, на Алтае и Урале, Восточной Сибири и на Дальнем Востоке, где происходили многочисленные выходы магматических интрузий, имеются богатые залежи рудных полезных ископаемых, золота, алмазов, химического и строительного сырья.
В результате Россия занимает ведущее положение в мире по доказанным (разведанным) запасам многих полезных ископаемых. Так, на нее приходится 18% газовых ресурсов мира и более 5% мировых запасов нефти. Подавляющая часть запасов газа находится в Западно-Сибирском бассейне, а также в Баренцево-Печорском, Оренбургском, Астраханском, Северокавказском, Ленско-Вилюйском и Охотоморском бассейнах России. Большая часть нефтяных запасов также находится в Западно-Сибирском бассейне и, кроме того, запасы нефти имеются в Волжско-Уральском, в Баренцево-Печорском, Северокавказском, Прикаспийском и Охотоморском бассейнах. Велики потенциальные запасы углеводородов на шельфах арктических и тихоокеанских морей, однако добыча здесь пока минимальна.
Россия занимают ведущее место и по запасам угля (18% мировых достоверных запасов мира), где бесспорным лидером являются бессейны-гиганты — Тунгусский и Ленский, однако их разведанные запасы невелики, добыча здесь почти не ведется. Из разрабатываемых бассейнов следует выделить огромный Канско-Ачинский буроугольный бассейн, Кузнецкий каменноугольный и другие бассейны угля, расположенные на территории России — Печорский, Донецкий, Иркутский, Южно-Якутский, Приморский, Сахалинский, Подмосковный.
Россия располагает 18% мировых запасов урановых руд. Основные российские месторождения находятся в Восточной Сибири и Дальнем Востоке — Читинской области, Бурятии и в Республике Саха. Урановые руды России беднее зарубежных. В эксплуатируемых подземным способом российских месторождениях руды содержат всего 0,18% урана, в то время как на канадских подземных рудниках отрабатываются руды с содержанием урана до 1%. По добыче урановых руд Россия располагается на 6-м месте (6,6% мировой добычи).
Важнейшей составной частью минерально-сырьевой базы являются руды черных и цветных металлов. Крупные месторождения железных руд в России — это, прежде всего, Курская магнитная аномалия, а также уральские, кольско-карельские и приангарские месторождения. По достоверным запасам железной руды Россия является одним из мировых лидеров — 15% мировых запасов. А по добыче железной руды Россия стоит на 5-м месте — более 100 млн т. Однако обеспеченность России необходимыми для металлургии марганцевыми и хромовыми рудами невелика.
Алюминиевые руды имеются на Европейском Севере (в том числе крупнейшее месторождение нефелинов на Кольском полуострове), в Северо-Западном районе России, на Урале и в Сибири. Однако в целом запасы алюминиевых руд в России невелики.
Россия располагает большими запасами никелевых руд, которые часто добываются совместно с медными. По добыче никелевых руд Россия занимает ведущее место в мире — более 20% мировой добычи.
Медные, кобальтовые, никелевые, платиновые руды добываются в России в районе Норильска, а также на Урале, на Кольском полуострове. Руды часто носят комплексный характер и содержат одновременно медь, никель, кобальт и другие компоненты. Вольфрамо-молибденовые руды имеются на Северном Кавказе и в Забайкалье. Комплексные, главным образом, свинцово-цинковые полиметаллические месторождения встречаются в Забайкалье, в Приморье, Северном Кавказе, Алтайском регионе. Богатые месторождения оловянных руд имеются на Дальнем Востоке. Россыпные и коренные месторождения золота имеются на Дальнем Востоке, в Забайкалье, горном Алтае.
После распада СССР России приходится приступать к освоению месторождений марганца, титано-циркониевых, хромовых руд, концентраты которых ранее полностью завозились из союзных республик.
Из нерудных месторождений следует выделить месторождения солей. Россия имеет крупные месторождения солей на Урале, в нижнем Поволжье, на юге Западной и Восточной Сибири. Уникальные месторождения апатитов имеются в Хибинах на Кольском полуострове. Фосфориты добываются в Центральной России. Месторождения серы известны в Поволжье. Богатые месторождения алмазов имеются в Республике Саха, обнаружены месторождения и на Европейском Севере недалеко от Архангельска.
Вместе с тем большинство месторождений полезных ископаемых России низкого качества, содержание полезных компонентов в них на 35–50% ниже среднемировых, кроме того, в ряде случаев они труднодоступны, находятся в районах с экстремальными природными условиями. В результате, несмотря на наличие значительных разведанных запасов, степень их промышленного освоения достаточно низкая: для бокситов — 33%, нефелиновых руд — 55%, меди — 49%, цинка — 17%, олова — 42%, молибдена — 31%, свинца — 9%, титана — 1%.
Земельные ресурсы в России достаточно велики, однако сельскохозяйственный угодья, как и во всем мире, имеют тенденцию к сокращению. За последние четверть века их площадь сократилась примерно на 15%. Хотя в структуре земельного фонда России пашня составляет лишь 7% и к тому же ее площадь сокращается, обеспеченность пашней в России одна из самых высоких в мире — около 0,9га на человека, причем Россия обладают огромными запасами наиболее плодородных — черноземных почв.
Анализ данных государственного мониторинга земель за состоянием окружающей природной среды показывает, что состояние качества земель фактически во всех субъектах Российской Федерации интенсивно ухудшается. Почвенный покров, особенно пашни и других сельскохозяйственных угодий, продолжает подвергаться деградации, загрязнению, захламлению и уничтожению, катастрофически теряет устойчивость к разрушению, способность к восстановлению свойств, воспроизводству плодородия вследствие истощительного и потребительского использования земель. К тому же примерно половина (северная) территории России находится в условиях избыточного увлажнения, а южная часть европейской территории России и южная Сибирь находятся в зоне недостаточного увлажнения. Переувлажненные и заболоченные земли занимают 12%, а засоленные, солонцеватые земли и земли с солонцовыми комплексами занимают 20% площади сельскохозяйственных угодий страны.
Лесные ресурсы в России крайне богаты. Обеспеченность лесными ресурсами в России одна из самых высоких в мире — 5 га на человека, поэтому 26% мировых запасов древесины приходится на Россию. При этом Россия располагает более зрелыми и продуктивными лесами, чем другие страны, т.к. в ее лесах преобладают хвойные породы. Поэтому в нашей стране сосредоточена почти половина запасов древесных хвойных пород мира.
На протяжении последних 30 лет состояние лесов непрерывно ухудшалось. Вырубки превышают лесовосстановление. Естественным путем восстанавливается около трети ежегодно вырубаемых лесов, остальные требуют специальных мер по их возобновлению. Особенно быстро деградируют леса европейской территории. Огромный урон лесам наносят также пожары, промышленные выбросы и строительные работы. Запасы древесины за последние годы снизились на 1,2 млрд м3, что говорит о том, что леса России «молодеют», т.е. вырубаются наиболее ценные — спелые и продуктивные леса, а восстановление идет за счет малоценных мелколиственных молодняков.
Водные ресурсы весьма велики — Россия по объёму водных ресурсов занимает 2-е место в мире после Бразилии, на одного жителя приходится 32 тыс. м3 пресной воды в год. Однако распределены они очень неравномерно. Так, на бассейны Северного Ледовитого и Тихого океанов приходится 80% стока. В результате ряд регионов испытывающих нехватку пресной воды (Поволжье, Центрально-Черноземный район, Северный Кавказ, Уральский, Центральный районы), так как ее запасы главным образом сосредоточены на Европейском Севере, в Сибири и на Дальнем Востоке.
Чрезвычайно быстрыми темпами растет забор пресной воды: если в 1950 г. он составлял 80 км3, то сейчас — 400 км3 в год. Это объясняется тем, что в России сложилась иная, чем в других странах структура водопотребления воды. Расход воды на промышленные нужды самый большой и составляет 57%, на сельское хозяйство идет 16% воды, на бытовые нужды — 23% и 4% водных ресурсов сосредоточено в водохранилищах. Подобная структура потребления (много промышленного и бытового потребления) сложилась вследствие высокой доли водоемких отраслей промышленности и расточительного потребления воды в коммунальном хозяйстве. Засушливость южных районов России, являющихся главными сельскохозяйственными районами страны, увеличивает уровень использования воды в сельском хозяйстве. Тем не менее суммарный расход воды в России составляет всего лишь 3% среднемноголетнего стока рек страны.
Серьезная проблема водных ресурсов — их загрязнение. Практически все крупные реки являются «загрязненными» или «сильно загрязненными». Около 57% водоемов, с которых производится забор питьевой воды, не соответствует санитарным стандартам по химическим и микробиологическим показателям. Примерно половина населения используют воду для питья, не соответствующую гигиеническим требованиям.
Гидроэнергетические ресурсы в России достаточно велики. Гидроэнергопотенциал России оценивается в 2,5 трлн. квт. ч. (12% мирового гидроэнергопотенциала), из них технически возможно использовать 1,7 трлн. квт. ч. электроэнергии. По обеспеченности гидроэнергоресурсами Россия занимает второе место в мире после Китая. Наиболее крупным суммарным гидропотенциалом обладают Дальний Восток и Восточная Сибирь.
Рекреационные ресурсыв России очень богаты, но, к сожалению, слабо и неэффективно используются. Средняя полоса России с мягким умеренным климатом, красивыми реками, возвышенностями и смешанными лесами весьма благоприятна для отдыха и лечения. Горные районы Кавказа, Урала, Алтая, Камчатки — прекрасные места для горного отдыха, туризма и горнолыжного спорта. Минеральные целебные источники на Кавказе, Алтае, Камчатке и других районах представляют большую ценность для лечения опорно-двигательного аппарата, желудочных и других заболеваний. Черноморское побережье по своей красоте превосходит морские побережья многих стран.
Россия богата также памятниками культуры. 24 ее объекта включены в Список всемирного наследия, в том числе Московский Кремль и Красная площадь; исторические центры Санкт-Петербурга и Новгорода; архитектурный ансамбль Троице-Сергиевой лавры; памятники Владимиро-Суздальской земли; историко-культурный комплекс Соловецких островов; погост Кижи.
[1] Максаковский В.П. Общая экономическая и социальная география. Курс лекций.М.: Инфра-М, 2010. С….
Типы и причины коррозии, способы ее предотвращения Блоги по решениям для ходовых и управляющих систем
Предотвращение коррозии — важнейшая задача во многих отраслях промышленности. В отсутствие защитных мер коррозия может оказать пагубное влияние на инфраструктуру, а также безопасность и эффективность бизнеса. Риску подвержен и бюджет компаний: по результатам исследования, проведенного организацией NACE International, ежегодные затраты на борьбу с коррозией составляют 2,5 триллиона долл. США.
С другой стороны, современным инженерам-конструкторам доступно значительно больше инструментов, чем прежде. Более глубокое понимание типов и причин коррозии, усовершенствованные материалы и передовые подходы — все это помогает техническим специалистам предотвращать разрушение металлов и снижать его интенсивность.
В этой публикации представлено краткое содержание новой брошюры Parker о борьбе с коррозией.
Определение коррозии
Коррозия — это процесс, при котором инфраструктура, продукция и детали разрушаются вследствие химической либо электрохимической реакции с окружающей средой.
Основные типы коррозии
Сегодня в разных отраслях промышленности распространены шесть типов коррозии.
• Электрохимическая коррозия, возникающая при контакте двух материалов с разными электрохимическими свойствами (например, сталь и латунь) в агрессивной среде и приводящая к разрушению менее устойчивого материала.
• Точечная коррозия, при которой в металле быстро возникают глубокие и узкие отверстия, в то время как остальная поверхность остается неповрежденной. Обычно это происходит с самопассивирующимися материалами, такими как нержавеющая сталь или сплавы алюминия.
• Равномерная коррозия, которая развивается постепенно на открытой для воздействия поверхности металла, оставляя равномерный слой отложений.
• Щелевая коррозия, охватывающая те участки, где в небольших углублениях (выемках или углах) скапливается жидкость.
• Межкристаллитная коррозия, которая возникает внутри зернистой структуры сплава или рядом с ней и вызывает локальные повреждения.
• Коррозионное растрескивание под напряжением, когда материал подвергается непрерывной или меняющейся нагрузке в агрессивной среде, что приводит к появлению трещин.
Что вызывает коррозию?
Коррозия — результат воздействия ряда различных факторов, характерных для каждой конкретной отрасли. Ниже перечислены распространенные примеры для отдельных отраслей.
• В сфере строительства коррозия часто возникает в ситуациях, когда металлы подвергаются воздействию природных факторов и экстремальных температур.
• Подземные разработки обычно проводят в средах с кислой водой (нередко содержащей хлориды и сульфаты) в сочетании с высокой влажностью и температурой.
• В лесной промышленности коррозия обычно появляется при работе на удаленных участках, когда оборудование паркуют прямо на траве или земле. За ночь там накапливается большое количество воды, которая может вызывать коррозию встроенных механических систем и компонентов.
Условия окружающей среды также влияют на скорость развития и распространение коррозии. При повышенной влажности металлы реагируют друг с другом и разрушаются гораздо быстрее, чем в сухих условиях.
В агрессивных средах обычно присутствуют следующие факторы (отдельно или в различных сочетаниях):
• влажность;
• экстремальные температуры;
• сырые поверхности;
• взвешенные в воздухе частицы;
• соль;
• промышленные смазочные материалы.
Предотвращение коррозии и защита
Инженерам доступен целый ряд методов, которые помогают снизить интенсивность коррозии или предотвратить ее возникновение. Ниже перечислены методы, более подробно описанные в брошюре о борьбе с коррозией.
• Выбор материалов. Ключевую роль играет выбор подходящих материалов с учетом задачи и условий ее выполнения. В агрессивной среде разрушению подвержены все металлы, однако сплавы могут резко отличаться друг от друга по своим показателям. Решающее значение в этом случае имеет баланс между пределом прочности на разрыв и стойкостью к нагреву, воздействию химических веществ и коррозии.
• Совместимость материалов. При разработке продуктов инженеры должны учитывать вероятность соприкосновения потенциально несовместимых материалов. Так, сочетания меди и нержавеющей стали или бронзы и стали могут стать причиной электрохимической коррозии. Для решения этой проблемы следует выбирать совместимые материалы и сплавы либо применять изоляцию, которая позволяет предотвратить образование электрической цепи.
• Защитные покрытия. На некоторые металлы, такие как сталь, железо и алюминий, можно нанести защитное покрытие, устойчивое к коррозии. Чтобы выбрать оптимальную комбинацию металла и покрытия, требуется тщательно проанализировать требования к прочности, надежности, трению, моменту затяжки и коррозионной стойкости.
• Коррозионные испытания. В ходе контролируемых испытаний можно смоделировать различные агрессивные атмосферы, включая распыленную соленую воду, солевой туман, сухость и влажность. Такие испытания обычно проводят с соблюдением очень точных параметров, например моделируют сезонные циклы, чтобы воссоздать реальные погодные условия.
• Системы защиты от коррозии. Эффективная система защиты помогает предприятиям успешно справляться с коррозией. Мониторинг состояния и анализ журналов для учета инцидентов улучшают понимание практических аспектов, связанных с коррозией, а обмен информацией между подразделениями позволяет выявить потенциальную зависимость между капиталовложениями, методами обслуживания и сроком службы активов.
Борьба с коррозией: брошюра
Скачать брошюру
Автор статьи — доктор Филипп Вагенер (Philipp Wagener)
Связанные статьи:
Пыль гораздо вреднее, чем кажется
Влияние химических элементов на свойства стали.
Условные обозначения химических элементов:
| хром ( Cr ) — Х никель ( Ni ) — Н молибден ( Mo ) — М титан ( Ti ) — Т медь ( Cu ) — Д ванадий ( V ) — Ф вольфрам ( W ) — В | азот ( N ) — А алюминий ( Аl ) — Ю бериллий ( Be ) — Л бор ( B ) — Р висмут ( Вi ) — Ви галлий ( Ga ) — Гл | иридий ( Ir ) — И кадмий ( Cd ) — Кд кобальт ( Co ) — К кремний ( Si ) — C магний ( Mg ) — Ш марганец ( Mn ) — Г | свинец ( Pb ) — АС ниобий ( Nb) — Б селен ( Se ) — Е углерод ( C ) — У фосфор ( P ) — П цирконий ( Zr ) — Ц |
ВЛИЯНИЕ ПРИМЕСЕЙ НА СТАЛЬ И ЕЕ СВОЙСТВА
Углерод — находится в стали обычно в виде химического соединения Fe3C, называемого цементитом. С увеличением содержания углерода до 1,2% твердость, прочность и упругость стали увеличиваются, но пластичность и сопротивление удару понижаются, а обрабатываемость ухудшается, ухудшается и свариваемость.
Кремний — если он содержится в стали в небольшом количестве, особого влияния на ее свойства не оказывает.(Полезная примесь; вводят в качестве активного раскислителя и остается в стали в кол-ве 0,4%)
Марганец — как и кремний, содержится в обыкновенной углеродистой стали в небольшом количестве и особого влияния на ее свойства также не оказывает. (Полезная примесь; вводят в сталь для раскисления и остается в ней в кол-ве 0,3-0,8%. Марганец уменьшает вредное влияние кислорода и серы.
Сера — является вредной примесью. Она находится в стали главным образом в виде FeS. Это соединение сообщает стали хрупкость при высоких температурах, например при ковке, — свойство, которое называется красноломкостью. Сера увеличивает истираемость стали, понижает сопротивление усталости и уменьшает коррозионную стойкость. В углеродистой стали допускается серы не более 0,06-0,07%. ( От красноломкости сталь предохраняет марганец, который связывает серу в сульфиды MnS).
Фосфор — также является вредной примесью. Снижает вязкость при пониженных температурах, то есть вызывает хладноломкость. Обрабатываемость стали фосфор несколько улучшает, так как способствует отделению стружки.
ЛЕГИРУЮЩИЕ ЭЛЕМЕНТЫ И ИХ ВЛИЯНИЕ НА СВОЙСТВА СТАЛИ
Хром (Х) — наиболее дешевый и распространенный элемент. Он повышает твердость и прочность, незначительно уменьшая пластичность, увеличивает коррозионную стойкость; содержание больших количеств хрома делает сталь нержавеющей и обеспечивает устойчивость магнитных сил.
Никель (Н) — сообщает стали коррозионную стойкость, высокую прочность и пластичность, увеличивает прокаливаемость, оказывает влияние на изменение коэффициента теплового расширения. Никель – дорогой металл, его стараются заменить более дешевым.
Вольфрам (В) — образует в стали очень твердые химические соединения – карбиды, резко увеличивающие твердость и красностойкость. Вольфрам препятствует росту зерен при нагреве, способствует устранению хрупкости при отпуске. Это дорогой и дефицитный металл.
Ванадий (Ф) — повышает твердость и прочность, измельчает зерно. Увеличивает плотность стали, так как является хорошим раскислителем, он дорог и дефицитен.
Кремний (С)- в количестве свыше 1% оказывает особое влияние на свойства стали: содержание 1-1,5% Si увеличивает прочность, при этом вязкость сохраняется. При большем содержании кремния увеличивается электросопротивление и магнитопроницаемость. Кремний увеличивает также упругость, кислостойкость, окалиностойкость.
Марганец (Г) — при содержании свыше 1% увеличивает твердость, износоустойчивость, стойкость против ударных нагрузок, не уменьшая пластичности.
Кобальт (К) — повышает жаропрочность, магнитные свойства, увеличивает сопротивление удару.
Молибден (М) — увеличивает красностойкость, упругость, предел прочности на растяжение, антикоррозионные свойства и сопротивление окислению при высоких температурах.
Титан (Т) — повышает прочность и плотность стали, способствует измельчению зерна, является хорошим раскислителем, улучшает обрабатываемость и сопротивление коррозии.
Ниобий (Б) — улучшает кислостойкость и способствует уменьшению коррозии в сварных конструкциях.
Алюминий (Ю) — повышает жаростойкость и окалиностойкость.
Медь (Д) — увеличивает антикоррозионные свойства, она вводится главным образом в строительную сталь.
Церий — повышает прочность и особенно пластичность.
Цирконий (Ц) — оказывает особое влияние на величину и рост зерна в стали, измельчает зерно и позволяет получать сталь с заранее заданной зернистостью.
Лантан, цезий, неодим — уменьшают пористость, способствуют уменьшению содержания серы в стали, улучшают качество поверхности, измельчают зерно.
Государственный контроль (надзор)
Одной из важнейших составляющих административной реформы и, в том числе реформы технического регулирования, является создание новой системы государственного контроля (надзора) за соблюдением обязательных требований в отношении продукции, процессов производства, эксплуатации, хранения, перевозки, реализации и утилизации, обязательных требований в области обеспечения единства измерений.
В организационную структуру системы контрольно-надзорных органов Федерального агентства входят семь межрегиональных территориальных управлений (МТУ)
Основными задачами в области государственного контроля (надзора) Федерального агентства, определенными в положении об Агентстве, являются:
- осуществление контроля (надзора) за соблюдением обязательных требований государственных стандартов и технических регламентов до принятия Правительством Российской Федерации решения о передаче этих функций другим федеральным органам исполнительной власти;
- осуществление государственного метрологического надзора;
- сбор и обработка информации о случаях причинения вреда вследствие нарушения требований технических регламентов, а также информирования приобретателей, изготовителей и продавцов по вопросам соблюдения требований технических регламентов.
В целях повышения эффективности и совершенствования организации и проведения контрольно-надзорных мероприятий, направленных на защиту потребительского рынка от опасной продукции и обеспечение единства измерений, Федеральным агентством ежегодно формируется план надзорной деятельности.
Контрольно-надзорные мероприятия обеспечиваются путем проведения плановых и внеплановых проверок, основанием для которых служит анализ состояния дел с безопасностью продукции на потребительском рынке и обеспечением потребности граждан, общества и государства в получении объективных, достоверных результатов измерений.
Государственный надзор проводится не чаще, чем один раз в три года в отношении одного юридического лица или индивидуального предпринимателя.
Государственный надзор за соблюдением обязательных требований стандартов и технических регламентов осуществляется с применением инструментальных методов контроля, т.е. проведением испытаний отобранных образцов продукции в аккредитованных испытательных лабораториях (центрах).
В случае выявления нарушений установленных обязательных требований должностными лицами органов государственного надзора Федерального агентства к проверяемому субъекту хозяйственной деятельности и (или) должностному лицу применяются правовые меры, предусмотренные законодательством об административных правонарушениях.
На основе результатов государственного надзора Федеральное агентство проводит мониторинг состояния дел, связанных с безопасностью продукции и обеспечением единства измерений, готовит и представляет обобщенные материалы в установленной сфере деятельности в Минпромторг России, федеральным органам исполнительной власти, представителям Президента Российской Федерации в федеральных округах и администрации субъектов Российской Федерации.
Руководителям МТУ по суррогатам ДУУ (pdf , 0.50 Мб)
Приложение к 698 (pdf , 0.86 Мб)
Приказ № 689 (pdf , 0.06 Мб)
Как читать паспорт качества топлива (pdf , 1.03 Мб)
Инфографика: «Государственный контроль и надзор за соблюдением требований Технических регламентов» (pdf , 0.12 Мб)
Обзор правоприменительной практики контрольно-надзорной деятельности (docx , 0.00 Мб)
Перечень юридических лиц и индивидуальных предпринимателей, деятельности которых присвоены категории риска. (xlsx , 2.15 Мб)
Изменения в перечне юридических лиц и индивидуальных предпринимателей, деятельности которых присвоены категории риска. (xlsx , 0.57 Мб)
Обзор правоприменительной практики контрольно-надзорной деятельности за 2018 год. (docx , 0.04 Мб)
Обзор правоприменительной практики контрольно-надзорной деятельности за 2019 год (docx , 0.04 Мб)
Обзор правоприменительной практики контрольно-надзорной деятельности за 2020 год (docx , 0.03 Мб)
Взаимодействие с отраслевыми объединениями и ассоциациями
В рамках консолидации совместных усилий, направленных на борьбу с выпуском в обращение и обращением на рынке не соответствующей установленным требованиям продукции, а также построения взаимного сотрудничества и партнерства Росстандартом выстраивается взаимодействие с отраслевыми объединениями, ассоциациями, союзами. В настоящее время заключены соглашения с:
- Ассоциация «Электрокабель»;
- Союз производителей цемента «Союзцемент»;
- Алюминиевая Ассоциация;
В рамках заключенных соглашений стороны будут осуществлять обмен информацией о выпуске в обращение и обращении на рынке несоответствующей обязательным требованиям продукции, проведение совместных совещаний, конференций, круглых столов и других мероприятий.
Определение характеристик наноматериалов алюминия, оксида алюминия и диоксида титана с использованием комбинации методов анализа поверхности и размера частиц
* Соответствующие авторы
а Немецкий федеральный институт оценки рисков (BfR), Департамент химической безопасности и безопасности продукции, Max-Dohrn-Straße 8-10, 10589 Берлин, Германия
Электронная почта: Вениамин-Кристоф[email protected]
б Институт медицинской физики и биофизики, Лейпцигский университет, Härtelstrasse 16-18, 04275 Лейпциг, Германия
с Немецкий федеральный институт оценки рисков (BfR), Департамент безопасности пищевых продуктов, Max-Dohrn-Straße 8-10, 10589 Берлин, Германия
д Федеральный институт исследования и испытаний материалов (BAM), Unter den Eichen 87, 12205 Berlin, Германия
e MRIC TEM BIOSIT, Université de Rennes 1, 2 av pro Leon Bernard, Франция
f , F-35000 Rennes, France
г ANSES, Французское агентство по вопросам пищевых продуктов, окружающей среды, гигиены труда и техники безопасности, лаборатория Fougères, 10B rue Claude Bourgelat, Fougères Cedex, Франция
ч Феликс Блох Институт физики твердого тела, факультет физики и наук о Земле, отделение ядерной физики твердого тела, Лейпцигский университет, Linnéstraße 5, 04103 Лейпциг, Германия
и Федеральный институт исследования и испытаний материалов (BAM), Richard-Willstätter-Straße 11, 12489 Berlin, Германия
Синтез и характеристика наночастиц алюминия, полученных в уксусе с использованием метода импульсной лазерной абляции
Длина волны второй гармоники лазера на иттрий-алюминиевом гранате (Nd-YAG), легированного неодимом (нм), использовалась в методе импульсной лазерной абляции ( PLAL) для синтеза наночастиц алюминия, взвешенных в белом уксусе из алюминиевой мишени.Наночастицы были охарактеризованы методами HRTEM и УФ-видимой спектрофотометрии. Было обнаружено, что они имеют размер от 2 до 50 нм в диаметре при среднем диаметре нм. Наночастицы имели максимум поглощения при 237 нм и, как было обнаружено, демонстрировали структуру ядро-оболочка с алюминиевым ядром, покрытым тонким слоем аморфного материала, который можно отнести к аморфному углероду. Результаты ПЭМВР показали, что маленькие наночастицы (<20 нм) имели ГЦК-фазу кристаллической структуры алюминия, где более крупные частицы представляли наночастицы оксида алюминия ( γ -Al 2 O 3 ).Такое наблюдение предполагает, что использование белого уксуса в качестве абляционной среды может облегчить синтез наночастиц алюминия с минимальными доказательствами существования наночастиц оксида алюминия в полученной суспензии.
1. Введение
Наночастицы алюминия (НЧ Al) в настоящее время вызывают большой интерес из-за их значительного и разнообразного применения. Было обнаружено, что они являются идеальными катализаторами для реакций с ракетным топливом [1], а также имеют много других многообещающих применений в биомедицинской [2] и антимикробной [3] областях.Тем не менее, синтез наночастиц Al высокой чистоты представляет собой серьезную проблему из-за их способности к окислению с образованием наночастиц Al 2 O 3 [4]. В последние годы импульсная лазерная абляция в жидкости (PLAL) стала перспективным методом получения чистых наночастиц активных металлов [5]. PLAL — это простой одностадийный метод, при котором металлическая мишень в объеме или порошке помещается в водный раствор и облучается лазерными импульсами с коротким периодом времени, обычно около нескольких наносекунд.PLAL считается простой и недорогой технологией, не требующей вакуумного оборудования [6]. Он может обеспечивать наночастицы контролируемого размера без какого-либо химического загрязнения [7].
Однако наноматериалы, полученные этим методом, сильно зависят от используемой жидкой среды [8, 9], длины волны лазера [10], энергии лазера [11–13] и времени облучения [8], а также других параметров. Применяя длину волны первой гармоники Nd: YAG-лазера (нм), облученные алюминиевые мишени, погруженные в этанол, ацетон или этиленгликоль, приводили к получению наночастиц Al с различным диаметром в диапазоне от 30 до 100 нм [8, 9].Было замечено, что более мелкие частицы (средний диаметр 30 нм) были получены в ацетоне [8] или этаноле [9], когда применяется более длительная абляция [8]. Аналогичным образом, облученные алюминиевые мишени в сухом тетрагидрофуране (с добавлением олеиновой кислоты или без нее) приводили к наночастицам Al со средним размером 21 нм [14]. Одна из причин использования олеиновой кислоты в этой реакции состоит в том, что она служит поверхностно-активным веществом, уменьшающим агрегацию. Сообщалось, что pH жидкой среды в PLAL влияет на размеры и поверхностный заряд синтезированных наночастиц [6].С другой стороны, когда необходимы наночастицы чистого Al, требуется предотвращение образования оксидов. Одним из способов достижения этого является введение углеводородов, таких как олеиновая кислота, которые уменьшают соотношение Al / O и минимизируют окисление наночастиц [14].
В этой работе мы демонстрируем возможность изготовления наночастиц Al в кислой среде с использованием технологии PLAL. В качестве источника лазера использовалась длина волны второй гармоники (532 нм) Nd: YAG-лазера, а в качестве жидкой среды использовался белый уксус.Насколько нам известно, ни в одной из предыдущих работ уксус не использовался для получения наночастиц алюминия с использованием PLAL.
2. Эксперимент
Гранулы алюминия с содержанием металлических примесей 99,99% (Sigma-Aldrich) с размерами 3–12 мм использовались в качестве мишеней, а в качестве среды использовали сильнокислый белый уксус с pH 2. Используемый в этой работе белый уксус представляет собой органическое вещество, имеющееся на местном рынке, с кислотностью не менее 5%. В типичном эксперименте таблетку полировали наждачной бумагой для удаления коррозии на ее поверхности непосредственно перед абляцией, а затем промывали ацетоном.Затем гранулы помещали в стеклянный стакан и покрывали белым уксусом (уровень ~ 2 мм над мишенью). Затем химический стакан помещали на предметный столик XY, чтобы обеспечить движение мишени под лазерным лучом. Эта процедура была необходима, чтобы избежать образования глубокого кратера на поверхности мишени.
Использовалась длина волны второй гармоники Nd: YAG-лазера (нм, Quanta Ray, Spectra Physics) с частотой следования лазера 10 Гц и длительностью импульса 6 нс. Мощность лазера была установлена на 2 Вт.Лазерный луч фокусировался на поверхность мишени с помощью линзы 50 мм, и мишень облучалась в течение 15 мин. Эксперимент проводился в условиях окружающей среды. На рис. 1 представлена принципиальная схема экспериментальной установки. После облучения гранулы удаляли и раствор анализировали с помощью спектрофотометрии в УФ-видимом диапазоне (Thermo, Genesys 10S). Структурные и морфологические свойства наночастиц исследовали с помощью ПЭМВР (микроскоп Tecnai G2 F20 Super Twin TEM). Поддон взвешивали до и после процесса абляции, чтобы определить массу взвешенных частиц в растворе.
3. Результаты и обсуждение
Сферические наночастицы алюминия, суспендированные в белом уксусе, полученные в результате абляции 532 нм лазером Nd: YAG погруженной алюминиевой мишени после 15 минут воздействия. Рассчитанная масса суспендированного алюминия составляла 3,8 мг, что указывает на образование значительного количества наноматериалов.
Спектр поглощения суспензии раствора наночастиц показан на рисунке 2 (а). В спектре виден единственный пик ниже видимого диапазона с максимумом поглощения при 237 нм.Наличие такого пика (ниже 250 нм) свидетельствует об образовании наночастиц алюминия в суспензии [8]. В предыдущих исследованиях [8, 13, 15] сообщалось, что пик около 200 нм соответствует наночастицам в диапазоне диаметров 10 нм, а красное смещение связано с более крупными частицами [13]. Кроме того, на рис. 2 (а) показано широкое плечо поглощения в области 300–400 нм, которое приписывают наночастицам со структурой ядро-оболочка [13, 15]. ПЭМ-изображения суспензии, как показано на рисунках 2 (b) и 2 (c), указывают на существование наносфер, размер которых варьируется от 2 нм до 50 нм.Измерения наночастиц проводились непосредственно с изображений ПЭМ с помощью программного обеспечения ImageJ. Затем было построено распределение этих наночастиц по размерам и проиллюстрировано на рисунке 2 (d), где средний диаметр оказался равным нм.
При исследовании наночастиц разных размеров было замечено, что более мелкие наночастицы (<20 нм) имеют другую структуру, чем более крупные. Увеличивая более мелкие наночастицы с помощью анализа HRTEM (рисунки 3 (a) и 3 (b)), можно увидеть, что прямолинейное расстояние в кристаллической структуре частиц равно 0.2 нм и 0,23 нм, что соответствует плоскостям (200) и (111) ГЦК алюминия соответственно. Это дополнительно подтверждается анализом дифракции электронов на выбранной площади (SAED), показанным на рисунке 3 (c), где его график показывает наличие Al (111), (200), (311), (222) и (400) с начало γ -Al 2 O 3 (440) на основе Совместного комитета по стандарту порошковой дифракции и Международного центра дифракционных данных (JCPDS-ICDD) № карт. 85-1327 для чистого алюминия и 29-0063 для γ -Al 2 O 3 .Кроме того, частицы имеют структуру ядро-оболочка с алюминием в ядре и покрыты тонким слоем. Природа тонкого слоя с покрытием может потребовать дальнейшего исследования. Предполагается, что тонкий слой может быть оксидом алюминия (Al 2 O 3 ) или аморфным углеродом, который возникает в результате разложения уксусной среды во время лазерной абляции [8].
Для более крупных наночастиц (> 50 нм), показанных на рисунке 4 (a), структура HRTEM показывает ориентацию зерен (220) и шаг решетки 0.28 нм, что соответствует γ -Al 2 O 3 наночастиц. Это дополнительно подтверждается изображением решетки с преобразованием Фурье на рисунке 4 (b), которое указывает на наличие ориентаций (220) и (311) γ -Al 2 O 3 . Следует отметить, что интенсивность фазы (311) γ -Al 2 O 3 очень мала; следовательно, он не появлялся в шаблоне SAED на Рисунке 3 (c).
Согласно изображениям ПЭМ, распределению наночастиц по размерам и картине SAED (рисунки 2 и 3) можно сделать вывод, что количество наночастиц Al в приготовленном растворе превышает количество наночастиц Al 2 O 3 .В частности, было обнаружено, что отношение Al / Al 2 O 3 составляет около 9,5. Это может быть связано с обилием ионов H + в кислой среде, из-за чего ионы O 2–, полученные в результате фотолиза и термолиза, предпочитают сочетаться с ионами H + . Следовательно, большинство ионов Al 3+ упускают шанс рекомбинировать с ионами O 2– и существуют в форме металлического Al [14, 16].
С точки зрения кристаллической структуры оксид алюминия (оксид алюминия; Al 2 O 3 ) имеет множество форм [17, 18].Эти различные формы называются «переходным оксидом алюминия» и обозначаются префиксами γ , δ , θ , κ , χ , η и ρ . Оксид алюминия переходит из одной формы в другую из-за повышения температуры. Конечным продуктом этого переходного оксида алюминия является α -Al 2 O 3 , который считается наиболее стабильной формой. В наших экспериментальных условиях конечным продуктом превращения оксида алюминия был γ -Al 2 O 3 , то есть температура была недостаточно высокой для достижения α -Al 2 O 3 фаза.
4. Заключение
В заключение, наночастицы алюминия и оксида алюминия ( γ -Al 2 O 3 ), суспендированные в белом уксусе, были синтезированы с использованием технологии PLAL. Наночастицы алюминия были более многочисленными и варьировались по размеру от 2 до 50 нм при среднем диаметре нм. Однако было обнаружено очень ограниченное количество наночастиц оксида алюминия размером более 50 нм в диаметре. Наночастицы оксида алюминия могут быть вызваны реакцией гранул алюминия с кислородом в результате разложения белого уксуса под действием лазерных импульсов.Белый уксус, который, насколько нам известно, был использован здесь впервые в качестве абляционной среды, действовал как ингибитор окисления, способствуя синтезу наночастиц алюминия с минимальным количеством наночастиц оксида алюминия.
Доступность данных
Изображения HRTEM и файлы Excel, используемые для подтверждения результатов этого исследования, можно получить у соответствующего автора по запросу.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Благодарности
Авторы благодарны отделу научных исследований и инноваций факультета естественных наук и Фонду КАУ (WAQF) Университета короля Абдулазиза, Джидда, Саудовская Аравия, за поддержку этой работы (номер гранта: Scigriu38 / 10).
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно.Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки вашего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом.Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно.Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки вашего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом.Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Структурная характеристика белка, адсорбированного на адъюванте гидроксида алюминия в составе вакцины.
Гленни А. Т., Поуп К. Г., Уоддингтон Х. и Уоллес У. Иммунологические примечания. XVII − XXIV. J. Pathol. Бактериол. 29 , 31–40 (1926).
CAS Статья Google Scholar
Del Giudice, G., Rappuoli, R. & Didierlaurent, A. M. Корреляты адъювантности: обзор адъювантов в лицензированных вакцинах. Семин. Иммунол. 39 , 14–21 (2018).
Артикул Google Scholar
О’Хаган, Д. Т., Фридланд, Л. Р., Ханон, Э. и Дидьерлаурент, А. М. К подходу, основанному на фактических данных, для разработки адъювантных вакцин. Curr. Opin. Иммунол. 47 , 93–102 (2017).
Артикул Google Scholar
HogenEsch, H., O’Hagan, D. T. и Fox, C. B. Оптимизация использования алюминиевых адъювантов в вакцинах: вы можете просто получить то, что хотите. NPJ Vaccin. 3 , 51 (2018).
Артикул Google Scholar
Sokolovska, A., Hem, S. L. & HogenEsch, H. Активация дендритных клеток и индукция дифференцировки CD4 (+) Т-клеток с помощью алюминийсодержащих адъювантов. Vaccine 25 , 4575–4585 (2007).
CAS Статья Google Scholar
Jones, L. S. et al. Влияние адсорбции на адъюванты на основе солей алюминия на структуру и стабильность модельных белковых антигенов. J. Biol. Chem. 280 , 13406–13414 (2005).
CAS Статья Google Scholar
Jully, V., Mathot, F., Moniotte, N., Préat, V. & Lemoine, D. Механизмы адсорбции антигена на адъюванте из гидроксида алюминия, оцененные с помощью высокопроизводительного скрининга. J. Pharm. Sci. 105 , 1829–1836 (2016).
CAS Статья Google Scholar
Régnier, M. et al. Структурные нарушения анатоксина дифтерии при адсорбции на адъюванте гидроксида алюминия. Vaccine 30 , 6783–6788 (2012).
Артикул Google Scholar
Донг А., Джонс, Л. С., Кервин, Б. А., Кришнан, С. и Карпентер, Дж. Ф. Вторичные структуры белков, адсорбированных на гидроксид алюминия: инфракрасный спектроскопический анализ белков при низких концентрациях раствора. Анал. Biochem. 351 , 282–289 (2006).
CAS Статья Google Scholar
Киркитадзе, М., Синха, А., Ху, Дж., Уильямс, В. и Кейтс, Г. Компоненты вакцины с адъювантом: анализ структуры и стабильности. Procedureia Vaccinol. 1 , 135–139 (2009).
CAS Статья Google Scholar
Соляков, А., Харрис, Дж. Р., Уоткинсон, А. и Лейки, Дж. Х. Структура полимера Yersinia pestis Caf1 в свободном и связанном с адъювантом состояниях. Vaccine 28 , 5746–5754 (2010).
CAS Статья Google Scholar
Андреас, Л. Б. и др. Структура полностью протонированных белков с помощью детектируемого протонами ЯМР с вращением под магическим углом. Proc. Natl. Акад. Sci. США 113 , 9187–9192 (2016).
CAS Статья Google Scholar
Quinn, C.M. et al. Динамическое регулирование взаимодействия капсида ВИЧ-1 с фактором рестрикции TRIM5α, идентифицированным с помощью ЯМР с вращением под магическим углом и моделирования молекулярной динамики. Proc. Natl. Акад. Sci. США 115 , 11519–11524 (2018).
CAS Статья Google Scholar
Пейдж, Р. К., Ли, С., Мур, Дж. Д., Опелла, С. Дж. И Кросс, Т. А. Структура скелета небольшого спирального интегрального мембранного белка: уникальная структурная характеристика. Protein Sci. 18 , 134–146 (2009).
CAS PubMed Google Scholar
Soong, R. et al. Проведенные протонной эволюцией твердотельные ЯМР-исследования цитохрома b5, встроенного в бицеллы, в локальном поле, раскрывают как структурную, так и динамическую информацию. J. Am. Chem. Soc. 132 , 5779–5788 (2010).
CAS Статья Google Scholar
Park, S.H. et al. Структура хемокинового рецептора CXCR1 в фосфолипидных бислоях. Природа 491 , 779–783 (2012).
CAS Статья Google Scholar
Retel, J. S. et al. Структура белка G внешней мембраны липидных бислоев. Nat. Commun. 8 , 2073 (2017).
Артикул Google Scholar
Fusco, G. et al. Прямое наблюдение за тремя областями α-синуклеина, которые определяют его поведение, связанное с мембраной. Nat. Commun. 5 , 3827 (2014).
CAS Статья Google Scholar
Сергеев, И. В., Итин, Б., Рогавски, Р., Дэй, Л. А. и МакДермотт, А. Е. Эффективное отнесение и анализ ЯМР интактного вируса с использованием последовательных корреляций боковых цепей и сенсибилизации DNP. Proc.Natl. Акад. Sci. США 114 , 5171–5176 (2017).
CAS Статья Google Scholar
Habenstein, B. et al. Гибридная структура пилуса 1 типа уропатогенной Escherichia coli . Angew. Chem. Int. Эд. 54 , 11691–11695 (2015).
CAS Статья Google Scholar
Öster, C. et al.Характеристика границ раздела белок-белок в больших комплексах с помощью усилений парамагнитной релаксации в твердотельном ЯМР-растворителе. J. Am. Chem. Soc. 139 , 12165–12174 (2017).
Артикул Google Scholar
Tuttle, M. D. et al. Твердотельная структура ЯМР патогенной фибриллы полноразмерного α-синуклеина человека. Nat. Struct. Мол. Биол. 23 , 409–415 (2016).
CAS Статья Google Scholar
Wiegand, T. et al. Конформационные изменения, связанные с гидролизом и транслокацией АТФ в бактериальной геликазе DnaB. Nat. Commun. 10 , 31 (2019).
Артикул Google Scholar
Берш, Б., Дёрр, Дж. М., Хессель, А., Киллиан, Дж. А. и Шанда, П. Твердотельная ЯМР-спектроскопия с обнаружением протонов белка-катализатора диффузии цинка в нативных нанодисках. Angew. Chem. Int. Эд. Англ. 56 , 2508–2512 (2017).
CAS Статья Google Scholar
Joedicke, L. et al. Молекулярные основы подтипной селективности рецепторов, связанных с кинином G-белком человека. Nat. Chem. Биол. 14 , 284–290 (2018).
CAS Статья Google Scholar
Ravera, E. et al. Твердотельный ЯМР ПЭГилированных белков. Angew. Chem. Int. Эд. Англ. 55 , 2446–2449 (2016).
CAS Статья Google Scholar
Fragai, M. et al. SSNMR ферментов, захваченных биокремнеземом, позволяет легко оценить сохранение нативной конформации в атомных деталях. Chem. Commun. 50 , 421–423 (2014).
CAS Статья Google Scholar
Ravera, E. et al. Ферменты, захваченные биокремом, изучены с помощью высокопольной ЯМР-спектроскопии с динамической ядерной поляризацией. Chemphyschem 16 , 2751–2754 (2015).
CAS Статья Google Scholar
Giuntini, S. et al. Характеристика характера конъюгирования в больших конъюгатах полисахарид-белок с помощью ЯМР-спектроскопии. Angew. Chem. Int. Эд. 56 , 14997–15001 (2017).
CAS Статья Google Scholar
Джунтини, С., Церофолини, Л., Равера, Э., Фрагай, М. и Лучинат, С. Детали атомной структуры белка, привитого на наночастицы золота. Sci. Отчетность 7 , 17934 (2017).
Артикул Google Scholar
Jantschke, A. et al. Понимание супрамолекулярной архитектуры интактной биокремнезема диатомовых водорослей с помощью твердотельной ЯМР-спектроскопии с использованием ДНФ. Angew. Chem. Int. Эд. Англ. 54 , 15069–15073 (2015).
CAS Статья Google Scholar
Martelli, T. et al. Оценка качества ферментов, инкапсулированных в биоинспирированный диоксид кремния, на атомном уровне. Химия 22 , 425–432 (2015).
Артикул Google Scholar
Balayssac, S. et al. Твердотельный ЯМР матричной металлопротеиназы 12: подход, дополняющий ЯМР в растворе. Chembiochem 8 , 486–489 (2007).
CAS Статья Google Scholar
Cerofolini, L. et al. Характеристика ПЭГилированной аспарагиназы: новые возможности ЯМР-анализа больших ПЭГилированных терапевтических средств. Химия 25 , 1984–1991 (2019).
CAS Статья Google Scholar
Ван С.и другие. Определение структуры твердотельного ЯМР-спектрометра липид-встроенного белка гепталической мембраны. Nat. Методы 10 , 1007–1012 (2013).
Артикул Google Scholar
Suiter, C. L. et al. MAS ЯМР ансамблей белка ВИЧ-1. J. Magn. Резон. 253 , 10–22 (2015).
CAS Статья Google Scholar
Марчанка А., Саймон Б., Альтхофф-Оспельт Г. и Карломагно Т. Определение структуры РНК с помощью твердотельной ЯМР-спектроскопии. Nat. Commun. 6 , 7024 (2015).
CAS Статья Google Scholar
Гарсон, Н. и Фриде, М. 6 — Эволюция адъювантов на протяжении веков. В вакцине Плоткина ( Седьмое издание ) (ред.Плоткин, С.A. et al.) 61−74.e4 (Elsevier, Амстердам, 2018).
Scarselli, M. et al. Рациональный дизайн менингококкового антигена, вызывающего широкий защитный иммунитет. Sci. Пер. Med. 3 , 91ra62 (2011).
CAS Статья Google Scholar
Коцци, Р., Скарселли, М. и Ферленги, И. Структурная вакцинология: трехмерный взгляд на разработку вакцины. Curr. Вершина. Med.Chem. 13 , 2629–2637 (2013).
Артикул Google Scholar
Cerofolini, L. et al. Твердотельный ЯМР высокого разрешения, характеризующий связывание лиганда с белком, иммобилизованным в матрице диоксида кремния. J. Phys. Chem. B 121 , 8094–8101 (2017).
CAS Статья Google Scholar
Graham, M. L. Pegaspargase: обзор клинических исследований. Adv. Препарат Делив. Ред. 55 , 1293–1302 (2003).
CAS Статья Google Scholar
Kumru, O. S. et al. Нестабильность вакцины в холодовой цепи: механизмы, анализ и стратегии разработки. Биологические препараты 42 , 237–259 (2014).
CAS Статья Google Scholar
Braun, L.J. et al. Характеристика термостабильной вакцины против гепатита В. Vaccine 27 , 4609–4614 (2009).
Артикул Google Scholar
Састри, М., Бьюли, С. А. и Квонг, П. Д. Экспрессия в млекопитающих изотопно меченных белков для ЯМР-спектроскопии. Adv. Exp. Med. Биол. 992 , 197–211 (2012).
CAS Статья Google Scholar
Вернер, К., Рихтер, К., Klein-Seetharaman, J. & Schwalbe, H. Изотопное мечение GPCR млекопитающих в клетках HEK293 и характеристика С-конца бычьего родопсина с помощью жидкостной ЯМР-спектроскопии высокого разрешения. J. Biomol. ЯМР 40 , 49–53 (2008).
CAS Статья Google Scholar
Vajpai, N. et al. Конформации раствора и динамика комплексов ABL-киназа-ингибитор, определенные с помощью ЯМР, подтверждают различные способы связывания иматиниба / нилотиниба и дазатиниба. J. Biol. Chem. 283 , 18292–18302 (2008 г.).
CAS Статья Google Scholar
Strauss, A. et al. Эффективное единообразное изотопное мечение киназы Abl, экспрессируемой в инфицированных бакуловирусом клетках насекомых. J. Biomol. ЯМР 31 , 343–349 (2005).
CAS Статья Google Scholar
Морган, В. Д., Крагт, А.И Фини, Дж. Экспрессия меченного изотопом дейтерия белка в дрожжах pichia pastoris для ЯМР-исследований. J. Biomol. ЯМР 17 , 337–347 (2000).
CAS Статья Google Scholar
Takahashi, H. & Shimada, I. Производство меченных изотопами гетерологичных белков в не-E. coli прокариотические и эукариотические клетки. J. Biomol. ЯМР 46 , 3–10 (2010).
CAS Статья Google Scholar
Schuetz, A. et al. Протоколы последовательного твердотельного ЯМР-спектроскопического определения однородно меченого белка 25 кДа: HET-s (1-227). ChemBioChem 11 , 1543–1551 (2010).
CAS Статья Google Scholar
Keller, R. Учебное пособие по компьютерному назначению резонанса (CARA) (CANTINA Verlag, Goldau, 2004).
Grzesiek, S. et al. Структура раствора Nef ВИЧ-1 обнаруживает неожиданную складку и позволяет очертить поверхность связывания для домена Sh4 тирозинкиназы Hck. Nat. Struct. Биол. 3 , 340–345 (1996).
CAS Статья Google Scholar
(PDF) Синтез и характеристика пористых наночастиц оксида алюминия Синтез и характеристика пористых наночастиц оксида алюминия
NeuroQuantology | Январь 2020 | Том 18 | Выпуск 1 | Страница 109-116 | DOI: 10.14704 / nq.2020.18.1.NQ20115
Анвар Х. Али Аль-Фуади, Синтез и характеристика пористых наночастиц оксида алюминия
Заключение
Заказанный мезопористый оксид алюминия с каменистой твердой структурой Rocky-
был синтезирован гель
метод.Поливиниловый спирт, используемый в качестве поверхностно-активного агента
для организации оксида алюминия в мезопористую структуру
при испарении этанола: вода
.
Ссылки
Ибрагим А.Р., Чжу Л., Сюй Дж., Хонг И, Су И, Ван Х, Ли Дж. Синтез
мезопористого оксида алюминия с расширенной карбонизацией CO2 и
его каталитическим окислением циклогексанона. Журнал
сверхкритических флюидов, 2014; 92: 190-196.
Лю Цюй, Ван А, Ван Х, Гао П, Ван Х, Чжан Т.Синтез,
характеризация и каталитическое применение мезопористого
γ-оксида алюминия из золя бемита. Микропористые и
мезопористые материалы, 2008 г .; 111 (1-3): 323-333.
Ecsedi Z, Lazău I., Păcurariu C. Синтез мезопористого оксида алюминия
с использованием темплата из поливинилового спирта в качестве добавки для контроля пористости
. Процесс. Прил. Керамика, 2007; 1 (1–2): 5.
Чжоу Дж., Танг С., Ченг Б., Ю Дж., Яронец М. Углерод погремушек —
Сферы ядро-оболочка из оксида алюминия: синтез и применение для
адсорбции органических красителей.Прикладные материалы ACS и интерфейсы
, 2012 г .; 4 (4): 2174-2179.
Латиеф Ф.Х., Чафидз А., Джунаеди Х., Альфозан А., Хан Р. Влияние содержания глинозема
на физико-механические свойства композитов на основе полиэфира, армированного глиноземом
(). Достижения
Polymer Technology, 2019. 2019.
Xiong Y, Shen, Q, Chen, F, Luo, G, Yu, K, Zhang, L. Высокая прочность
Силикон / оксид алюминия
удержание и стабильность размеровкомпозитная панель под огнем.Огонь и материалы, 2012.
36 (4): с. 254-263.
Ruan HD, Frost RL, Kloprogge JT, Duong L. Дальний инфракрасный диапазон
Спектроскопия фаз оксида алюминия. Spectrochimica Acta Part
A: Молекулярная и биомолекулярная спектроскопия, 2002. 58 (2):
p. 265-272.
Zahir MH, Nagano T, Rahman MM, Alhooshani K, Chowdhury S,
Aziz, MA. Микроструктурные исследования трубчатых мембран из γ-Al2O3 на подложке из α-
Al2O3 и их гидротермальное улучшение
.Журнал Европейского общества керамики
, 2017. 37 (7): p. 2637-2647.
Munhoz Jr AH, De Paiva H, Figueiredo de Miranda L, De Oliveira
EC, Andrades RC, Ribeiro RR. Исследование синтеза гамма-оксида алюминия
– анализ удельной поверхности. в достижениях
в области науки и техники. Trans Tech Publ. 2014; 87: 54-
60.
Lamouri S, Hamidouche M, Bouaouadja N, Belhouchet H,
Garnier V, Fantozzi G, Trelkat JF.Контроль фазового превращения γ-оксида алюминия
в α-оксид алюминия для оптимального уплотнения оксида алюминия
. Boletín de la sociedad española de
cerámica y vidrio, 2017; 56 (2): 47-54.
Boumaza A, Favaro L, Lédion J, Sattonnay G, Brubach JB,
Berthet P, Tétot R. Переходные фазы оксида алюминия, вызванные термообработкой бемита
: исследование дифракции рентгеновских лучей и инфракрасной спектроскопии
. Журнал химии твердого тела
, 2009; 182 (5): 1171-1176.
Segal FM, Correa MF, Bacani R, Castanheira B, Politi MJ,
Brochsztain S, Triboni ER. Новый путь синтеза
мезопористого γ-оксида алюминия из полиоксогидроксида алюминия.
Materials Research, 2018. 21 (1).
Минаей С. Микро / мезопористые квазинульмерные наночастицы AlOOH
и Al2O3. Неорганические и нанометаллические
Химия, 2019: 1-8.
Чен X, Чжан В., Лин И, Цай Й, Цю М., Фан Я. Приготовление мембран для нанофильтрации на основе
с высокой плотностью потока γ-оксида алюминия с использованием модифицированного золь-гель метода
.Микропористые и мезопористые материалы
, 2015; 214: 195-203.
Заки Т., Кабель К.И., Хассан Х. Получение высокочистых наночастиц α-Al2O3
при низких температурах с использованием метода Печини.
Керамикс Интернэшнл, 2012 г .; 38 (3): 2021-2026.
Канго С., Калиа С., Челли А., Нджугуна Дж., Хабиби Ю., Кумар Р. Поверхность
модификация неорганических наночастиц для разработки
органо-неорганических нанокомпозитов — обзор. Прогресс
Полимероведение, 2013; 38 (8): 1232-1261.
Критикаки А., Цецекоу А. Изготовление пористой глиноземной керамики
из порошковых смесей с золь-гелевым производным оксида алюминия
нанометров: влияние метода смешивания. Журнал
Европейского керамического общества, 2009 г .; 29 (9): 1603-1611.
Ван Дж, Гэ Л, Ли З, Ли Л, Гуо Q, Ли Дж. Легкий контролируемый размер
синтез хорошо диспергированных сферических аморфных наночастиц оксида алюминия
путем гомогенного осаждения. Керамика
International, 2016; 42 (7): 8545-8551.
Saengkwamsawang P, Pimanpaeng S, Amornkitbamrung V,
Maensiri S. Синтез и определение характеристик нанопорошков Al2O3
с помощью простого раствора хитозан-полимерного комплекса
. Ceramics International, 2014; 40 (4): 5137-
5143.
Roque-Ruiz JH, Medellín-Castillo NA, Reyes-López SY.
Производство волокон из α-оксида алюминия методами золь-гель и
электроформование растворов предшественников нитрата алюминия.
Результаты по физике, 2019; 12: 193-204.
Назари С., Карими Г., Гадери Э., Морадиан К.М., Багерпор З.
Синтез и характеристика пористых наночастиц γ-оксида алюминия
из раствора алюмината натрия с двумя
различными поверхностно-активными веществами. Международный журнал нанонауки
и нанотехнологии, 2016 г .; 12 (4): 207-214.
Даббаг Х.А., Табан К., Замани М. Влияние вакуума и температуры прокаливания
на структуру, текстуру, реакционную способность
и селективность оксида алюминия: экспериментальные исследования и исследования
методом DFT.Журнал молекулярного катализа A: Chemical,
2010; 326 (1-2): 55-68.
Кур С., Шарма Р.К., Ясротия Р., Сингх В.П. Краткий обзор
синтеза маггемита (γ-Fe2O3) для медицинской диагностики
и приложений солнечной энергии. в AIP Conference
Proceedings. Издательство AIP. 2019; 2142 (1): 0
.
Поко Дж., Сэтчер Дж., Хрубеш Л. Синтез высокопористых,
монолитных аэрогелей оксида алюминия. Журнал некристаллических твердых тел
, 2001; 285 (1-3): 57-63.
Харазми А., Фараджи Н., Хусин Р.М., Сайон Э., Юнус WMM, Бехзад
К. Структурные, оптические, опто-термические и термические свойства
наножидкостей ZnS – PVA, синтезированных радиолитическим методом
. Журнал нанотехнологий Beilstein, 2015; 6 (1):
529-536.
Sing KS. Адсорбционные методы исследования пористых материалов
. Достижения в науке о коллоидах и интерфейсах, 1998;
76: 3-11.
Ван Ф, Цзяо Л., Лю З., Тан Х, Ван Ц., Гао Дж.Фрактальный анализ поровых структур
в песчаниках с низкой проницаемостью с использованием порометрии внедрения
ртути. Журнал Porous Media,
2018: 21 (11).
eISSN 1303-5150 www.neuroquantology.com
Алюминий | Введение в химию
Цель обучения
- Опишите свойства алюминия.
Ключевые моменты
- Алюминий — мягкий, легкий и ковкий серебристый металл, не растворимый в воде.
- В подавляющем большинстве соединений алюминий имеет степень окисления 3+, но известны соединения со степенью окисления +1 и +2.
- Алюминий содержит много известных изотопов, массовые числа которых находятся в диапазоне от 21 до 42.
- Алюминий является наиболее широко используемым цветным металлом и в основном легированным, что улучшает его механические свойства.
Условия
- алюминий Металлический химический элемент (обозначение Al) с атомным номером 13.
- пассивирование: относится к материалу, который становится «пассивным», то есть меньше подвержен влиянию факторов окружающей среды, таких как воздух или вода.
Физические свойства алюминия
Алюминий это:
- относительно мягкий
- прочный
- легкий
- пластичный
- податливый
- Внешний вид варьируется от серебристого до тускло-серого
- не растворяется в воде при нормальных условиях
- немагнитный
- плохо воспламеняется
- , способный быть сверхпроводником
Химические свойства
Алюминий устойчив к коррозии из-за явления пассивации.Когда металл подвергается воздействию воздуха, образуется тонкий поверхностный слой оксида алюминия. Этот оксидный слой защищает находящийся под поверхностью алюминий от дальнейшего окисления. Как и многие другие металлы, алюминий также может окисляться водой с образованием водорода и тепла:
[латекс] 2Al \ quad + \ quad 3 {H} _ {2} O \ quad \ longrightarrow \ quad {Al} _ {2} {O} _ {3} +3 {H} _ {2} [/ латекс]
Хотя алюминий очень легко окисляется, можно удалить оксидный слой с образца без его немедленного риформинга.Самый простой и безопасный способ — подключить батарею к образцу и провести электролиз либо в инертной атмосфере (например, газообразный аргон), либо в условиях вакуума.
Подавляющее большинство соединений алюминия имеют металл в степени окисления 3+. Координационное число алюминия может варьироваться, но обычно Al 3+ является тетра- или гексакоординированным. Это означает, что у него будет 4 или 6 лигандов.
Галогениды алюминия: использование в качестве кислот Льюиса
Алюминий — очень реактивный металл, который легко вступает в реакцию с трехвалентными соединениями продукта.Его галогениды (AlF 3 , AlCl 3 , AlBr 3 и AlI 3 ) являются общими примерами. Трехвалентный алюминий является электронодефицитным и поэтому исключительно полезен в качестве кислоты Льюиса, особенно в органическом синтезе.
Гидриды алюминия и алюминийорганические соединения
Существует множество соединений эмпирической формулы AlR 3 и AlR 1,5 Cl 1,5 . Эти разновидности обычно имеют тетраэдрические центры Al. С большими органическими группами триорганоалюминий существует в виде трехкоординированных мономеров, таких как триизобутилалюминий.
Важным гидридом алюминия является алюмогидрид лития (LiAlH 4 ), который используется в качестве восстановителя в органической химии. Его можно производить из гидрида лития и трихлорида алюминия:
[латекс] 4LiH \ quad + \ quad Al {Cl} _ {3} \ quad \ longrightarrow \ quad LiAl {H} _ {4} \ quad + \ quad 3LiCl [/ латекс]
Алюминий общего назначения
Алюминий — наиболее широко используемый цветной металл. Алюминий почти всегда легирован, что заметно улучшает его механические свойства, особенно при отпуске.Например, обычная алюминиевая фольга и банки для напитков представляют собой сплавы с содержанием алюминия от 92% до 99%. Некоторые из многих применений металлического алюминия находятся в:
- Транспортировка листов, труб, отливок и т. Д.
- Упаковка (жестяная банка, фольга и др.)
- Конструкция (окна, двери, сайдинг, строительная проволока и т. Д.)
- Широкий ассортимент предметов домашнего обихода, от кухонной утвари до бейсбольных бит и часов
- Столбы уличного освещения, мачты парусных судов, прогулочные шесты и т. Д.
- Наружные оболочки бытовой электроники, а также корпуса для оборудования (например, фотоаппаратуры)
- Линии электропередачи для распределения электроэнергии
- Алюминий особой чистоты, используемый в электронике и компакт-дисках
- Радиаторы для электронных устройств, таких как транзисторы и процессоры
- Материал подложки из ламината с металлическим сердечником, плакированного медью, используемого в светодиодном освещении высокой яркости
- Алюминий порошковый, используемый в красках и пиротехнике
- Множество стран, включая Францию, Италию, Польшу, Финляндию, Румынию, Израиль и бывшую Югославию, выпустили монеты, отчеканенные из алюминия или алюминиево-медных сплавов

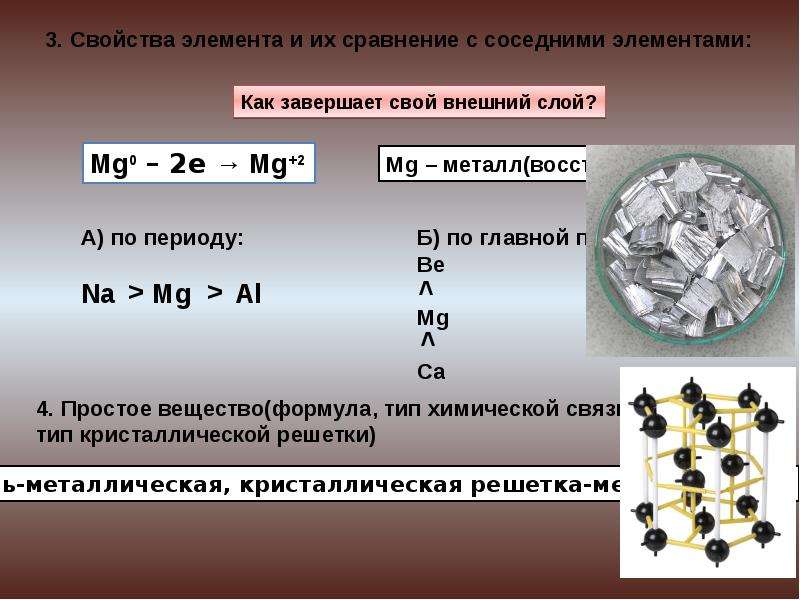 т)
т)
 7 (6)
7 (6) 7 (10)
7 (10)