Глоссарий – Приложения – Годовой отчет ПАО «ГМК «Норильский никель» за 2019 г.
Анод. Черновой металл (никель или медь), полученный в процессе анодной плавки и направляемый на электролитическое рафинирование (электролиз), где он растворяется.
Аффинаж. Процесс получения благородных металлов высокой чистоты путем их разделения и отделения загрязняющих примесей.
Богатые руды. Руды, представленные сульфидами более чем на 70%. Содержание полезных компонентов: никель — 2–5%; медь — 2–25%; металлы платиновой группы — 5–100 г/т.
Вероятные запасы руды. Часть обозначенных или в некоторых случаях разведанных запасов полезных ископаемых, добыча которых экономически оправдана.
Вкрапленные руды. Руды, содержащие 5–30% сульфидов. Содержание полезных компонентов: никель — 0,2–1,5%; медь — 0,3–2,0%; металлы платиновой группы — 2–10 г/т.
Выщелачивание. Избирательное растворение одного или нескольких компонентов обрабатываемого твердого материала в органических растворителях или водных растворах неорганических веществ.
Доказанные запасы руды. Часть разведанных запасов полезных ископаемых, добыча которых экономически оправдана.
Извлечение металла. Отношение количества извлеченного компонента из исходного сырья к его количеству в исходном материале (в процентах или долях единиц).
Катод. Чистый металл (никель или медь), полученный в результате электролитического рафинирования анодов.
Кек. Твердый остаток от фильтрации пульпы, получаемый в процессах выщелачивания руд, концентратов или промежуточных продуктов металлургического производства, а также в процессах очистки технологических растворов.
Конвертирование. Окислительный процесс переработки штейнов с выводом углерода, серы, железа и прочих примесей в шлак и получением файнштейна (при плавке медно-никелевых концентратов) или черновой меди (при плавке медных концентратов).
Концентрат. Продукт обогащения руды с повышенным содержанием извлекаемого минерала. Концентрат называют по преобладающему в нем металлу (медный, никелевый и т. д.).
Продукт обогащения руды с повышенным содержанием извлекаемого минерала. Концентрат называют по преобладающему в нем металлу (медный, никелевый и т. д.).
Медистые руды. Руды, представленные сульфидами от 20 до 70%. Содержание полезных компонентов: никель — 0,2–2,5%; медь — 1,0–15,0%; металлы платиновой группы — 5–50 г/т.
Обжиг. Высокотемпературный нагрев руды с целью химических изменений, необходимых для последующих металлургических процессов по извлечению из нее металлов.
Обогащение. Искусственное повышение содержания минералов в сырье для металлургического производства путем удаления большей части пустой породы.
Оксид. Соединение химического элемента с кислородом.
Отвальные хвосты. Отходы процессов обогащения, состоящие преимущественно из пустой породы с небольшим количеством ценных минералов.
Печь Ванюкова. Автогенная плавильная печь для переработки концентратов. Плавка происходит в шлако-штейновой ванне, в которой сырье интенсивно перемешивается с кислородно-воздушной смесью. При этом активно используется тепло, которое образуется при окислительных реакциях.
Плавка происходит в шлако-штейновой ванне, в которой сырье интенсивно перемешивается с кислородно-воздушной смесью. При этом активно используется тепло, которое образуется при окислительных реакциях.
Печь взвешенной плавки. Автогенная плавильная печь для переработки сухих концентратов. Плавка происходит при движении потока смеси измельченного сырья и газообразного окислителя (воздуха, кислорода), который удерживает частицы расплавленного металла во взвешенном состоянии. При этом активно используется тепло, которое образуется при окислительных реакциях.
Печь кипящего слоя.
Печь, в которой сыпучий (порошкообразный, зернистый, гранулированный) материал взаимодействует с проходящим через него нагретым газовым потоком (воздуха, кислорода, дымовых газов), интенсивно перемещающим твердые частицы в так называемом кипящем слое.Пирротиновый концентрат. Побочный продукт обогащения медно-никелевых руд.
Плавка. Пирометаллургический процесс, проводимый при температурах, обеспечивающих полное расплавление перерабатываемого материала.
Пирометаллургический процесс, проводимый при температурах, обеспечивающих полное расплавление перерабатываемого материала.
Подэтажное обрушение. Система подземной разработки рудных месторождений, при которой блоки отрабатываются сверху вниз подэтажами; руда в подэтажах извлекается принудительным обрушением или самообрушением с заполнением выработанного пространства обрушенными породами.
Пульпа.
Руда. Природное минеральное сырье, содержащее металлы или их соединения в количестве и виде, допускающих их промышленное использование.
Рудник. Горнопромышленное предприятие по добыче руд.
Сгущение. Процесс отделения жидкой фазы (воды) от твердой в дисперсных системах (пульпе, суспензии, коллоиде), основанный на естественном осаждении твердых частиц под действием силы тяжести в отстойниках, сгустителях или под действием центробежной силы в гидроциклонах.
Содержание металла. Отношение массы металла в сухом материале к полной сухой массе материала, выраженное в процентах или граммах на тонну.
Сульфиды. Соединения металлов с серой.
Сушка. Удаление влаги из концентрата, осуществляемое в специальных сушильных печах (до влажности менее 9%).
Толлинг. Переработка иностранного сырья с последующим вывозом готовой продукции. При этом особый таможенный режим позволяет ввозить сырье и вывозить готовую продукцию беспошлинно.
Файнштейн. Полупродукт металлургического производства, получаемый при конвертировании штейнов. По химическому составу различают медный, никелевый и медно-никелевый файнштейн.
Фильтрация. Процесс снижения влажности пульпы при ее движении сквозь пористую среду.
Флотация. Способ обогащения, основанный на избирательном прилипании минеральных частиц, взвешенных в пульпе, к пузырькам воздуха. Плохо смачиваемые водой частицы минералов прилипают к пузырькам воздуха и поднимаются с ними на поверхность пульпы, образуя пену. Хорошо смачиваемые минералы не прилипают к пузырькам и остаются в пульпе. Таким образом достигается разделение минералов.
Плохо смачиваемые водой частицы минералов прилипают к пузырькам воздуха и поднимаются с ними на поверхность пульпы, образуя пену. Хорошо смачиваемые минералы не прилипают к пузырькам и остаются в пульпе. Таким образом достигается разделение минералов.
Хвостохранилище. Комплекс гидротехнических сооружений для приема и хранения отходов обогащения полезных ископаемых — отвальных хвостов.
Шихта. Смесь материалов в определенной пропорции для получения требуемого химического состава конечного продукта.
Шлак. Расплавленное или твердое вещество переменного состава, покрывающее поверхность жидкого продукта при металлургических процессах (плавке шихты, отработке расплавленных промежуточных продуктов и рафинировании металлов). Образуется из пустой породы, флюсов, золы топлива, сульфидов и оксидов металлов, продуктов взаимодействия обрабатываемых материалов и футеровки плавильных агрегатов.
Шлам. Порошкообразный продукт, содержащий благородные металлы, выпадающие в осадок при электролизе меди и других металлов.
Штейн. Промежуточный продукт, представляющий собой сплав сульфидов железа и цветных металлов переменного химического состава. Основной продукт, в котором аккумулируются имеющиеся в сырье благородные и сопутствующие металлы.
Электролиз. Совокупность процессов электрохимических окислений-восстановлений, происходящих на погруженных в электролит электродах при прохождении электрического тока от внешнего источника.
Электроэкстракция. Электролитический способ выделения металла из раствора. Руда или концентрат подвергается выщелачиванию с помощью определенных растворителей, которые растворяют минералы, содержащие металл, или весь продукт целиком. Металл выделяется на катоде, а отработанный электролит, как правило, вновь направляют на выщелачивание. Катодный металл представляет собой конечный продукт высокой чистоты.
Пирометаллургия и примеры пирометаллургических процессов
Главная » Полезное
Полезное
Просмотров 94 Опубликовано Обновлено
Содержание
- 1 Обжиг
- 2 Температура
Во время пирометаллической переработки руда после обогащения (концентрирования путем дробления, измельчения, плавления и сушки) спекается или обжигается (прокаливается) с другими материалами, такими как пыль и флюс.
- Далее концентрат плавят или расплавляют в доменной печи, чтобы сплавить нужные металлы в нечистый расплавленный слиток.
- Затем этот слиток подвергается третьему пирометаллическому процессу для очистки металла до желаемого уровня чистоты.
Каждый раз, когда руда или слитки нагреваются, образуются отходы. Пыль из вентиляции и технологических газов может улавливаться в рукавной камере и либо удаляться, либо возвращаться в технологический процесс, в зависимости от содержания остаточного металла. Сера в газе также улавливается, и при концентрации выше 4% ее можно превратить в серную кислоту. В зависимости от происхождения руды и содержания в ней остаточных металлов в качестве побочных продуктов также могут быть получены различные металлы, такие как золото и серебро.
В зависимости от происхождения руды и содержания в ней остаточных металлов в качестве побочных продуктов также могут быть получены различные металлы, такие как золото и серебро.
Обжиг
Это является важным пирометаллургическим процессом. Сульфатирующий обжиг используется при производстве кобальта и цинка. Его цель — отделить металлы таким образом, чтобы их можно было перевести в водорастворимую форму для дальнейшей гидрометаллургической переработки.
При плавке сульфидных руд образуется частично окисленный металлический концентрат (штейн). При плавке бесполезный материал, обычно железо, образует шлак с флюсовым материалом и превращается в оксид. Ценные металлы приобретают металлическую форму на стадии конверсии, которая происходит в конвертерных печах. Этот метод используется в производстве меди и никеля. Железо, феррохром, свинец, магний и соединения железа получают восстановлением руды древесным углем и флюсом (известняком), процесс плавки обычно происходит в электрической печи.
Электролиз расплавленной соли, используемый в производстве алюминия, является еще одним примером пирометаллургического процесса.
Температура
Высокая температура, необходимая для пирометаллургической обработки металлов, достигается сжиганием ископаемого топлива или использованием экзотермической реакции самой руды (например, в процессе плавки во вспышке).
Процесс мгновенной плавки является примером энергосберегающего пирометаллургического процесса, в котором окисляются железо и сера из рудного концентрата. Экзотермическая реакция в сочетании с системой рекуперации тепла экономит много энергии при плавке.
Высокая степень извлечения серы в процессе также благоприятна для защиты окружающей среды. Большинство недавно построенных медеплавильных и никелевых заводов используют этот процесс.
Пирометаллургия
пирометаллургия
пирометаллургия – отрасль добывающей металлургии. Он состоит из термической обработки минералов и металлургических руд и концентратов для осуществления физических и химических преобразований в материалах, позволяющих извлекать ценные металлы. В результате пирометаллургической обработки могут быть получены товарные продукты, такие как чистые металлы или промежуточные соединения или сплавы, подходящие в качестве сырья для дальнейшей обработки.
В результате пирометаллургической обработки могут быть получены товарные продукты, такие как чистые металлы или промежуточные соединения или сплавы, подходящие в качестве сырья для дальнейшей обработки.
Пирометаллургические процессы обычно относят к одной или нескольким из следующих категорий:
- Сушка
- Прокаливание
- Жарка
- Плавка
- Переработка
Большинство пирометаллургических процессов требуют затрат энергии для поддержания температуры, при которой происходит процесс. Энергия обычно обеспечивается в виде сжигания ископаемого топлива, экзотермической реакции материала или электрического тепла. Когда в исходном материале присутствует достаточное количество материала для поддержания температуры процесса исключительно за счет экзотермической реакции (т. е. без добавления топлива или электрического тепла), процесс называется «автогенным».
Дополнительные рекомендуемые знания
Содержимое
|
Сушка
Сушка – термическое удаление жидкой влаги (не связанной химически) с материала. Сушка обычно осуществляется путем контакта влажных твердых веществ с горячими дымовыми газами, образующимися при сжигании ископаемого топлива. В некоторых случаях тепло для сушки может обеспечиваться горячим воздухом или инертным газом, нагретым косвенно. Количество тепла, необходимое для данной операции сушки, соответствует количеству тепла, необходимому для испарения жидкой влаги, количеству тепла, необходимому для повышения температуры продуктов (сухих веществ и водяного пара) до конечной температуры сушки, и количеству тепла, необходимому для компенсации лучистого излучения. потери тепла.
Обычно температура сушки устанавливается на номинальное значение выше температуры кипения воды, часто около 120°C. В особых случаях, например при сушке некоторых водорастворимых солей, требуются более высокие температуры сушки. При сушке соли влага сырья насыщается растворенными солями, что изменяет температуру кипения и требует более высоких температур сушки.
Сушка влажных твердых частиц осуществляется в нескольких типах промышленных сушилок, включая роторные сушилки, сушилки с псевдоожиженным слоем и мгновенные сушилки.
Другой тип сушки, называемый распылительной сушкой, осуществляется, когда высушиваемый материал полностью растворяется в водном растворе. Раствор распыляется (обычно через специально сконструированное сопло) в нагретую камеру, и по мере испарения воды твердые вещества кристаллизуются. Водяной пар выпускается из сушилки, а сухие вещества собираются, как правило, в конической части сушилки. Твердый материал, полученный с помощью распылительной сушилки, часто имеет особые характеристики размера и формы частиц, которые можно регулировать концентрацией растворенного материала в растворе и конструкцией распылительной форсунки.
Прокаливание
Основная статья: Прокаливание
Прокаливание – это термическое разложение материала. Примеры включают разложение гидратов, таких как гидроксид железа, до оксида железа и водяного пара или разложение карбоната кальция до оксида кальция и двуокиси углерода и/или карбоната железа до оксида железа. Процессы прокаливания осуществляют в различных печах, включая шахтные печи, вращающиеся печи и реакторы с псевдоожиженным слоем.
Процессы прокаливания осуществляют в различных печах, включая шахтные печи, вращающиеся печи и реакторы с псевдоожиженным слоем.
Жарка
Основная статья: Обжиг (металлургия)
Обжиг состоит из термических реакций газ-твердое вещество, которые могут включать окисление, восстановление, хлорирование, сульфатирование и пирогидролиз.
Наиболее распространенным примером обжига является окисление сульфидных руд металлов. Сульфид металла нагревают в присутствии воздуха до температуры, которая позволяет кислороду воздуха реагировать с сульфидом с образованием газообразного диоксида серы и твердого оксида металла. Твердый продукт обжига часто называют «кальцином». При сульфидном обжиге, если температура и газовые условия таковы, что сульфидное сырье полностью окисляется, этот процесс известен как «мертвый обжиг». Иногда, как в случае предварительной обработки шихты отражательной или электроплавильной печи, процесс обжига проводят с меньшим количеством кислорода, чем требуется для полного окисления шихты.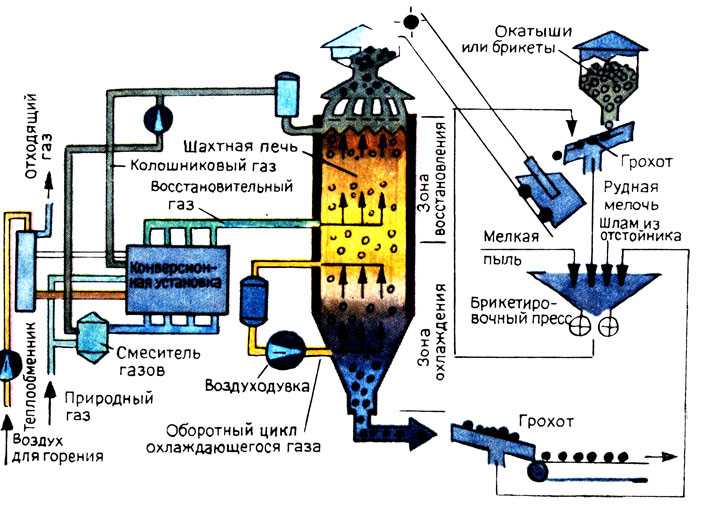 В этом случае процесс называется «частичным обжигом», поскольку сера удаляется лишь частично. Наконец, если температура и газовые условия регулируются таким образом, что сульфиды в сырье реагируют с образованием сульфатов металлов вместо оксидов металлов, этот процесс известен как «сульфатирующий обжиг». Иногда температуру и газовые условия можно поддерживать таким образом, чтобы смешанное сульфидное сырье (например, сырье, содержащее как сульфид меди, так и сульфид железа) реагировало таким образом, что один металл образовывал сульфат, а другой — оксид. Этот процесс известен как «селективный обжиг» или «селективное сульфатирование».
В этом случае процесс называется «частичным обжигом», поскольку сера удаляется лишь частично. Наконец, если температура и газовые условия регулируются таким образом, что сульфиды в сырье реагируют с образованием сульфатов металлов вместо оксидов металлов, этот процесс известен как «сульфатирующий обжиг». Иногда температуру и газовые условия можно поддерживать таким образом, чтобы смешанное сульфидное сырье (например, сырье, содержащее как сульфид меди, так и сульфид железа) реагировало таким образом, что один металл образовывал сульфат, а другой — оксид. Этот процесс известен как «селективный обжиг» или «селективное сульфатирование».
Плавка
Основная статья: Плавка
Плавка включает термические реакции, в которых по крайней мере один продукт представляет собой расплавленную фазу.
Оксиды металлов затем можно плавить путем нагревания с коксом или древесным углем (формами углерода), восстановителем, который высвобождает кислород в виде двуокиси углерода, выходящей из очищенного минерала. Беспокойство по поводу производства двуокиси углерода возникло совсем недавно, после выявления усиленного парникового эффекта.
Беспокойство по поводу производства двуокиси углерода возникло совсем недавно, после выявления усиленного парникового эффекта.
Карбонатные руды также выплавляются с древесным углем, но иногда их необходимо сначала прокалить.
Может потребоваться добавление других материалов в качестве флюса, способствующего плавлению оксидных руд и образованию шлака, поскольку флюс вступает в реакцию с примесями, такими как соединения кремния.
Плавка обычно происходит при температуре выше точки плавления металла, но процессы значительно различаются в зависимости от используемой руды и других факторов.
Переработка
Основная статья: Переработка (металлургия)
Рафинирование – это удаление примесей из материалов с помощью термического процесса. Это охватывает широкий спектр процессов, включающих различные виды печей или других установок.
Термин «рафинирование» может также относиться к некоторым электролитическим процессам. Соответственно, некоторые виды пирометаллургического рафинирования называются «огневым рафинированием».
Соответственно, некоторые виды пирометаллургического рафинирования называются «огневым рафинированием».
Экологические аспекты
Газы, образующиеся в пирометаллургических процессах, часто вызывают проблемы с загрязнением воздуха. В начале 20 века газообразные загрязнения в результате пирометаллургических процессов практически не контролировались. Например, выхлопные газы от обжига возле Квинстауна, Тасмания, на протяжении многих лет убивали всю растительность, что затем привело к эрозии всего верхнего слоя почвы. Результатом стало резкое и неестественное изменение окружающего ландшафта. Пыль или «дым» от пирометаллургических процессов представляют серьезную опасность для здоровья и безопасности рабочих и жителей вблизи пирометаллургических заводов. Эти металлургические пыли часто содержали мышьяк, кадмий, ртуть, свинец, цинк и другие тяжелые металлы. В то же время потери пыли на металлургических предприятиях также представляли собой потерю потенциально ценного продукта. Были разработаны технологии улавливания пыли, такие как рукавные фильтры и электрофильтры. Были также разработаны методы очистки газа, такие как мокрая очистка газа. Кроме того, как и в случае диоксида серы, были разработаны технологии производства серной кислоты из отходящих газов.
Были разработаны технологии улавливания пыли, такие как рукавные фильтры и электрофильтры. Были также разработаны методы очистки газа, такие как мокрая очистка газа. Кроме того, как и в случае диоксида серы, были разработаны технологии производства серной кислоты из отходящих газов.
См. также
- отражательная печь
- Доменная печь
Жареная в металлургии
Металлургическое содержание
- Химия окисляющего обжарения
- Железные пириты, FES2
- Roausting Pyrites
- Galena, PBS — Roausting
- Roastear -Arsenical Arsenical.
- Обжиг, ZnS, обжиг
- Карбонат извести, CaCO3
- Tellurides Roaust
- Metallic Gold, Silver Roausting
- Жарел для устранения мышьяка и сурьмы
- Использование соли в жарке
- Потеря золота в жарке
- Охлаждая Roasted Ore
в металлу обжиг, предшествующий хлорированию, имеет своей целью удаление серы, мышьяка, сурьмы и других летучих веществ, содержащихся в руде, и окисление оставшихся металлов с тем, чтобы не осталось ничего (кроме металлического золота), может соединяться с хлором при последующей обработке руды им в водном растворе. Для этого руду нагревают в печи, через которую пропускают ток воздуха с добавлением соли, если есть окись меди, известь, магнезия. Руды, содержащие большое количество пирита, могут быть освобождены от большей части серы путем обжига в штабеле, а затем подвергнуты тонкому дроблению и глубокому обжигу в отражательной печи, но дополнительные затраты на обработку, вероятно, превысят экономию из-за меньшего потребления топлива. Эта система не была опробована на заводах по хлорированию в больших масштабах. Обычная отражательная печь, работающая вручную, все еще используется, особенно там, где в день нужно перерабатывать всего несколько тонн или меньше концентратов. Различные механические печи, способные перерабатывать большие количества руды, были изобретены для замены устаревших устройств, и некоторые из них будут описаны в дальнейшем.
Для этого руду нагревают в печи, через которую пропускают ток воздуха с добавлением соли, если есть окись меди, известь, магнезия. Руды, содержащие большое количество пирита, могут быть освобождены от большей части серы путем обжига в штабеле, а затем подвергнуты тонкому дроблению и глубокому обжигу в отражательной печи, но дополнительные затраты на обработку, вероятно, превысят экономию из-за меньшего потребления топлива. Эта система не была опробована на заводах по хлорированию в больших масштабах. Обычная отражательная печь, работающая вручную, все еще используется, особенно там, где в день нужно перерабатывать всего несколько тонн или меньше концентратов. Различные механические печи, способные перерабатывать большие количества руды, были изобретены для замены устаревших устройств, и некоторые из них будут описаны в дальнейшем.
Sir Wm. Робертс-Остен следующим образом обсуждает обжиг «смеси, состоящей из сульфидов, в основном железа и меди, с некоторым количеством сульфида свинца, небольших количеств мышьяка и сурьмы в виде арсенидов, антимонидов и сульфосолей, обычно с медью в качестве основания. Температуру печи, в которой предстоит производить операцию, постепенно повышают, причем атмосфера является окислительной. Первым эффектом повышения температуры является отгонка серы, снижение сульфидов до более низкой стадии сульфирования. Эта сера сгорает в атмосфере печи до сернистого ангидрида (SO2), а при контакте с окисляемым материалом превращается в серный ангидрид (SO3). Следует отметить, что материал кирпичной кладки не вмешивается в реакции, кроме своего присутствия в виде горячей пористой массы, но тем не менее его влияние значительно. Обжиг этих сульфидов представляет собой хороший случай для изучения химического равновесия. Как только сернистый ангидрид достигает определенного напряжения, окисление сульфида приостанавливается, даже при наличии избытка кислорода, и окисление не возобновляется до тех пор, пока действие тяги не изменяет условия атмосферы печи. когда оставшиеся низшие сульфиды медленно окисляются, сульфид меди превращается в сульфат меди, в основном за счет вмешательства серного ангидрида, образующегося, как указано.
Температуру печи, в которой предстоит производить операцию, постепенно повышают, причем атмосфера является окислительной. Первым эффектом повышения температуры является отгонка серы, снижение сульфидов до более низкой стадии сульфирования. Эта сера сгорает в атмосфере печи до сернистого ангидрида (SO2), а при контакте с окисляемым материалом превращается в серный ангидрид (SO3). Следует отметить, что материал кирпичной кладки не вмешивается в реакции, кроме своего присутствия в виде горячей пористой массы, но тем не менее его влияние значительно. Обжиг этих сульфидов представляет собой хороший случай для изучения химического равновесия. Как только сернистый ангидрид достигает определенного напряжения, окисление сульфида приостанавливается, даже при наличии избытка кислорода, и окисление не возобновляется до тех пор, пока действие тяги не изменяет условия атмосферы печи. когда оставшиеся низшие сульфиды медленно окисляются, сульфид меди превращается в сульфат меди, в основном за счет вмешательства серного ангидрида, образующегося, как указано. Вероятно, гораздо большая часть сульфида железа становится сульфатом только на очень короткий период, разлагаясь на оксиды железа, главным образом оксид железа, с выделением серы. Любой присутствующий сульфид серебра с самого начала превратился бы в металлическое серебро, если бы не одновременное присутствие других сульфидов, особенно сульфидов меди и железа, которые позволяют сульфиду серебра превращаться в сульфат. Сульфид свинца также превращается в сульфат при этой низкой температуре (около 500°). Теперь нагревают еще больше, чтобы расщепить сульфат меди, при разложении которого остается оксид меди. Если, как в этом случае, основания слабые, серный ангидрид улетучивается в основном как таковой; но при разложении сульфатов более сильных оснований серный ангидрид в значительной степени разлагается на смесь сернистого ангидрида и кислорода. Серный ангидрид, образующийся при разложении этого сульфата меди, превращает серебро в сульфат и поддерживает его в таком виде, как, в свою очередь, при более низкой температуре сама медь поддерживалась в виде сульфата под действием серной кислоты.
Вероятно, гораздо большая часть сульфида железа становится сульфатом только на очень короткий период, разлагаясь на оксиды железа, главным образом оксид железа, с выделением серы. Любой присутствующий сульфид серебра с самого начала превратился бы в металлическое серебро, если бы не одновременное присутствие других сульфидов, особенно сульфидов меди и железа, которые позволяют сульфиду серебра превращаться в сульфат. Сульфид свинца также превращается в сульфат при этой низкой температуре (около 500°). Теперь нагревают еще больше, чтобы расщепить сульфат меди, при разложении которого остается оксид меди. Если, как в этом случае, основания слабые, серный ангидрид улетучивается в основном как таковой; но при разложении сульфатов более сильных оснований серный ангидрид в значительной степени разлагается на смесь сернистого ангидрида и кислорода. Серный ангидрид, образующийся при разложении этого сульфата меди, превращает серебро в сульфат и поддерживает его в таком виде, как, в свою очередь, при более низкой температуре сама медь поддерживалась в виде сульфата под действием серной кислоты. ангидрид отщепляется от сульфида железа. Когда неразложившимся остается лишь небольшое количество сульфата меди, сульфат серебра начинает расщепляться (примерно при 700°) частично под прямым действием одного тепла, а частично в результате реакций, подобных тем, которые показаны в следующих уравнениях:
ангидрид отщепляется от сульфида железа. Когда неразложившимся остается лишь небольшое количество сульфата меди, сульфат серебра начинает расщепляться (примерно при 700°) частично под прямым действием одного тепла, а частично в результате реакций, подобных тем, которые показаны в следующих уравнениях:
Ag2SO4 + 4Fe3O4 = 2Ag + 6Fe2O3 + SO2
Ag2SO4 + Cu2O = 2Ag + CuSO4 + CuO
Шихта по-прежнему содержит сульфат свинца, который не может быть полностью разложен ни при какой температуре, достижимой в обжиговой печи, кроме как в присутствии кремнезема. Удаление мышьяка и сурьмы порождает очень интересные проблемы и снова ставит перед плавильным заводом случай химического равновесия. Ради краткости в настоящее время будет хорошо ограничиться удалением сурьмы, которая, как можно предположить, присутствует в виде сульфида. Некоторое количество сульфида сурьмы отгоняется, но это не единственный способ его побега. Попытка удалить сурьму быстрым окислением сопряжена с опасностью превращения ее в нерастворимые соединения сурьмы металлов, содержащихся в шихте. Поэтому на ранних стадиях обжига необходимо использовать очень низкую температуру, а присутствие пара оказалось полезным в качестве источника водорода, который удаляет серу в виде сероводорода, при этом газ свободно выделяется. Реакция
Поэтому на ранних стадиях обжига необходимо использовать очень низкую температуру, а присутствие пара оказалось полезным в качестве источника водорода, который удаляет серу в виде сероводорода, при этом газ свободно выделяется. Реакция
Sb2S3 + 3h3 = 3h3S + 2Sb
между водородом и сульфидом сурьмы является, однако, эндотермическим и поэтому не может происходить без помощи, оказываемой внешним теплом. Факты, по-видимому, таковы: сульфид сурьмы при нагревании диссоциирует, и напряжение паров серы привело бы к состоянию равновесия, если бы высвобождающаяся таким образом сера не была захвачена водородом и удалена из системы. Таким образом, равновесие нарушается, и свежий сульфид диссоциирует. Общий результат состоит в том, что равновесие постоянно восстанавливается и разрушается до тех пор, пока не разложится сульфид. Сурьма соединяется с кислородом и улетучивается в виде летучей окиси, как и мышьяк, часть которого улетучивается в виде сульфида.
«Основной целью рассмотренного процесса является образование растворимого сульфата серебра». Реакции, однако, точно такие же, как и при обычном окислительном обжиге.
Реакции, однако, точно такие же, как и при обычном окислительном обжиге.
Следующие замечания о разложении различных минералов, присутствующих в полиметаллических рудах, могут помочь учащимся понять реакции, протекающие в обжиговой печи:
Пирит железа, FeS2
При нагревании этого соединения сера улетучивается , реакции, вероятно, выражались так:
3FeS2 = Fe3S4 + S2
7FeS2 = Fe7S8 + 3S2
Сера сгорает до SO2, который частично превращается нагретым кварцем и т. д. в SO3, соединяясь с присутствующим свободным кислородом. Сульфат железа, образованный этой серной кислотой, расщепляется при нагревании, и оксид железа (FeO) превращается в оксид железа (Fe2O3), который придает руде красный цвет в холодном состоянии. Некоторые основные сульфаты всегда остаются неразложившимися. Если температура части шихты рядом с огневым мостиком была слишком высокой или если шихта слишком долго выдерживалась в печи, особенно при отсутствии свободного доступа воздуха, то образуется некоторое количество магнитного оксида, таким образом:
3Fe2O3 = 2Fe3O4 + O
Присутствие магнитного оксида делает руду более темной по цвету. Это нежелательное изменение, так как магнитный оксид гораздо легче воздействует на хлор, чем на полуторный оксид.
Это нежелательное изменение, так как магнитный оксид гораздо легче воздействует на хлор, чем на полуторный оксид.
Дональд Кларк утверждает, что магнитный пирит Fe3S4, полученный на ранней стадии, окисляется непосредственно до Fe3O4 при умеренно высокой температуре и достаточном количестве воздуха. Когда его вносят в более горячую часть печи, магнитный оксид медленно превращается в полуторный оксид железа Fe2O3. Он не приводит никаких доказательств в поддержку этих заявлений, которые могут быть верны только в отношении небольшой части обвинения, если таковые имеются.
WE Greenawalt утверждает, что темный магнитный оксид может быть преобразован в красный полуторный оксид при более низкой температуре и обильной подаче воздуха. По этой причине он выступает за доводку при более низкой температуре, чем та, которая используется для предыдущих стадий обжарки. В четырех последовательных испытаниях на 100-тонных партиях он обнаружил, что более высокий процент экстракции хлорированием был получен при обжиге при высокой начальной температуре и низкой конечной температуре, чем при обжиге при более низкой начальной температуре и более высокой конечной температуре, хотя в в последнем случае удаление серы было более полным.
Обжиг медного пирита
При разложении сульфата меди, образующегося в печи, остается смесь оксидов меди и меди, растворимых в хлоре.
Галенит, PbS – Обжиг
Присутствие этого минерала в любых количествах, кроме небольших, очень вредно, так как и сульфат свинца, и силикат свинца (образующиеся при его разложении в присутствии кремнезема) очень легкоплавки, и при температуре требуется для дробления медного купороса, чтобы руда стала пастообразной и образовала комки. Обжаривание должно выполняться очень медленно и осторожно, чтобы избежать этого эффекта.
Обжиг мышьяковых пиритов, FeAsS
Арсениаты железа, меди, свинца при образовании не разлагаются легко, так как выдерживают высокую температуру, и лишь медленно превращаются в сульфаты серной кислотой при красном калении. Поэтому желательно избегать их образования, и с этой целью принимаются меры предосторожности, о которых уже упоминалось выше.
Сульфид сурьмы Обжиг
Сульфиды сурьмы С сульфидами еще труднее иметь дело, так как образующиеся соединения сурьмы разлагаются труднее, чем арсениаты. Их образования избегают уже описанным способом.
Их образования избегают уже описанным способом.
Обжиг, ZnS Обжиг
Обжиг, ZnS, образует оксид и сульфат цинка, из которых последний может быть расщеплен только при очень высокой температуре. При ярко-красном калении образуется основной сульфат, который при белом калении превращается в оксид. Если обманку обжаривать при высокой температуре и с обильной подачей воздуха, сульфат цинка в значительной степени не образуется.
Карбонат извести, CaCO3
Карбонат извести, CaCO3, разлагается при красном калении, выделяется CO2, а едкая известь, CaO, остается в шихте. Изменение происходит медленно при 600° (слабый красный калик) и быстро при 800° (полный красный калик). Подобным образом разлагается карбонат магния.
Теллуриды Обжиг
Теллуриды, содержащие золото, плавятся при температурах ниже красного каления, и могут происходить большие потери золота из-за поглощения подом печи. Расплавленные теллуриды золота могут оставаться в руде, и в этом случае при красном калении теллур частью улетучивается, частью окисляется до оксида ТеО2, который также возгоняется. Сферические шарики золота остаются, и их трудно растворить. Аналогично ведут себя селениды.
Сферические шарики золота остаются, и их трудно растворить. Аналогично ведут себя селениды.
Золото металлик, обжиг серебра
Металлическое золото, серебро сплавляются при высоких температурах, образуя сферические шарики, которые трудно растворить. По этой причине нельзя допускать, чтобы температура руды превышала 1000°.
Обжиг для удаления мышьяка и сурьмы
Х. М. Хоу, объясняя, как это происходит, выделяет в руде три горизонтальные зоны:
- верхняя поверхность, где серная и серная кислоты и продукты их окисления лишь слегка затрудняют окисление. сгорания топлива;
- средние слои, где окисление протекает в очень ограниченной степени;
- самые нижние пласты, где «окатыши руды просто подвергаются действию других окатышей, с которыми они соприкасаются, улетучившейся серы, а также сернистого и серного ангидридов, образующихся при воздействии серы на ранее образовавшиеся оксиды металлов. ”
Он продолжает: «Выбросу мышьяка и сурьмы в виде сульфидов в средней и нижней зонах способствует присутствие летучей серы, смешанной с серной кислотой, и очень ограниченное поступление свободного кислорода и серной кислоты. В верхней части среднего слоя, куда проникает небольшое количество свободного кислорода, мы имеем слабоокислительные условия, благоприятные для образования мышьяковистой кислоты и триоксида сурьмы. В верхней зоне более сильные окислительные условия скорее благоприятствуют образованию связанных мышьяковистой кислоты и сурьмы, хотя и здесь часть мышьяка и сурьмы может улетучиваться и улетучиваться при прохождении их промежуточного летучего состояния мышьяковистой кислоты и триоксида сурьмы». При перемешивании массы эти арсениты и сурьмянистые соли, подвергаясь восстановительному действию улетучившейся серы и неразложившихся сульфидов в нижних зонах, могут снова превратиться в летучие оксиды. Закись железа, перекись меди и сернистая кислота также эффективно восстанавливают мышьяковую кислоту, высшие оксиды железа и меди и образующуюся серную кислоту. Таким образом, каждый отдельный атом мышьяка может много раз путешествовать вперед и назад через летучее состояние, окисляясь на поверхности и восстанавливаясь под поверхностью, и каждый раз, когда он достигает этого летучего состояния, ему предоставляется возможность испариться и улетучиться.
В верхней части среднего слоя, куда проникает небольшое количество свободного кислорода, мы имеем слабоокислительные условия, благоприятные для образования мышьяковистой кислоты и триоксида сурьмы. В верхней зоне более сильные окислительные условия скорее благоприятствуют образованию связанных мышьяковистой кислоты и сурьмы, хотя и здесь часть мышьяка и сурьмы может улетучиваться и улетучиваться при прохождении их промежуточного летучего состояния мышьяковистой кислоты и триоксида сурьмы». При перемешивании массы эти арсениты и сурьмянистые соли, подвергаясь восстановительному действию улетучившейся серы и неразложившихся сульфидов в нижних зонах, могут снова превратиться в летучие оксиды. Закись железа, перекись меди и сернистая кислота также эффективно восстанавливают мышьяковую кислоту, высшие оксиды железа и меди и образующуюся серную кислоту. Таким образом, каждый отдельный атом мышьяка может много раз путешествовать вперед и назад через летучее состояние, окисляясь на поверхности и восстанавливаясь под поверхностью, и каждый раз, когда он достигает этого летучего состояния, ему предоставляется возможность испариться и улетучиться. ” Если к руде примешать небольшое количество угольной или коксовой пыли, то после ее полного окисления и исключения воздуха арсениаты и сурьмы снова восстанавливаются до низших оксидов, и, если они «переходят в летучее состояние ”, т. е. восстановленные до металлов, они могут быть снова пропущены через него окислительной атмосферой. «Конечно, вытеснению мышьяка и сурьмы способствует присутствие большого количества пирита, поскольку сера, перегоняемая из пирита, имеет тенденцию уносить их в виде сульфидов, а также потому, что присутствие пирита продлевает обжиг и, таким образом, увеличивает количество раз, когда мышьяк и сурьма проходят туда и обратно за пределы своих летучих состояний; следовательно, иногда желательно смешивать пирит с нечистыми рудами, чтобы способствовать вытеснению их примесей».
” Если к руде примешать небольшое количество угольной или коксовой пыли, то после ее полного окисления и исключения воздуха арсениаты и сурьмы снова восстанавливаются до низших оксидов, и, если они «переходят в летучее состояние ”, т. е. восстановленные до металлов, они могут быть снова пропущены через него окислительной атмосферой. «Конечно, вытеснению мышьяка и сурьмы способствует присутствие большого количества пирита, поскольку сера, перегоняемая из пирита, имеет тенденцию уносить их в виде сульфидов, а также потому, что присутствие пирита продлевает обжиг и, таким образом, увеличивает количество раз, когда мышьяк и сурьма проходят туда и обратно за пределы своих летучих состояний; следовательно, иногда желательно смешивать пирит с нечистыми рудами, чтобы способствовать вытеснению их примесей».
Некоторые руды требуют добавления соли при обжиге, чтобы хлорировать материал, который в противном случае поглощал бы хлор, когда руда подвергалась «газированию», и, таким образом, вызывала бы дополнительные расходы, а также неудобства . Если из руды необходимо извлечь как серебро, так и золото, необходимо добавить соль, чтобы в печи образовался хлорид серебра, поскольку металлическое серебро не подвергается воздействию хлора при самой высокой температуре, когда-либо использовавшейся в выщелачивающем чане. Затем хлорид серебра растворяют гипосульфитом соды или каким-либо другим растворителем либо до, либо после извлечения золота.
Если из руды необходимо извлечь как серебро, так и золото, необходимо добавить соль, чтобы в печи образовался хлорид серебра, поскольку металлическое серебро не подвергается воздействию хлора при самой высокой температуре, когда-либо использовавшейся в выщелачивающем чане. Затем хлорид серебра растворяют гипосульфитом соды или каким-либо другим растворителем либо до, либо после извлечения золота.
Даже если серебра нет, руда должна быть обожжена с солью, если она содержит много меди (в виде сульфида или окисленной соли), извести, магнезии или другого вещества, которое после окислительного обжига становится быстро подвергается воздействию хлора при обычных температурах. Соль обычно добавляют ближе к концу операции, когда не осталось сульфидов и лишь небольшой процент сульфатов остался неразложившимся; однако иногда руду и соль смешивают перед загрузкой. К некоторым сульфидам добавляется всего 5 фунтов соли на тонну руды, но для других требуется целых 90 фунтов за тонну. Вес добавляемой соли должен быть как минимум в шесть-восемь раз больше веса серебра, присутствующего в руде. Если используется большое количество соли, желательно выщелачивать обожженную руду водой перед ее обработкой газообразным хлором, чтобы удалить покрытие из растворимых сульфатов и хлоридов, оставшееся на поверхности гранул руды.
Если используется большое количество соли, желательно выщелачивать обожженную руду водой перед ее обработкой газообразным хлором, чтобы удалить покрытие из растворимых сульфатов и хлоридов, оставшееся на поверхности гранул руды.
Химическое действие соли обусловлено двойным разложением между ней и сульфатами тяжелых металлов, при котором образуются сульфат соды и хлориды тяжелых металлов. Следующее общее уравнение приблизительно представляет реакцию:—
2NaCl + RSO4 = RCl2 + Na2SO4
Хлор также высвобождается при действии серного ангидрида на соль, а присутствие паров воды вызывает образование большого количества соляной кислоты. Эти газы воздействуют непосредственно на несколько компонентов руды, образуя хлориды и оксихлориды. Образовавшиеся хлориды и оксихлориды металлов во многих случаях являются летучими (например, соединения меди, железа, свинца, мышьяка, сурьмы и т. д.), и, выделяясь, летучие соединения уносят с собой различные доли золота и серебра. , которые, как правило, не подлежат восстановлению в пылекамерах. Хлорид меди особенно активно вызывает эти потери.
Хлорид меди особенно активно вызывает эти потери.
Другие реакции, которые, вероятно, имеют место, следующие:
- Сульфат железа, действующий на соль при красном калении в присутствии воздуха, дает соляную кислоту и хлор, которые действуют на золото и серебро, тогда как полуторный оксид железа и натрий образуются сульфаты. Одновременно производится
- Хлорное железо Fe2Cl6. Он летуч и хлоридирует серебро с большой энергией при красном калении, образуя полуторную окись железа.
- Хлорид меди CuCl2 легко разлагается на хлорид меди Cu2Cl2 и свободный хлор или на оксихлорид Cu2O. Cl2 и свободный хлор. Пары CuCl2, таким образом, дают дополнительные запасы образующегося хлора, доступного для хлорирования серебра.
- Мышьяк и сурьма образуют летучие хлориды, которые разлагаются с помощью кислорода и водяного пара с образованием мышьяковистой и сурьмяной кислот и выделяющегося хлора или соляной кислоты.
Таким образом, очевидно, что присутствие неблагородных минералов выгодно, поскольку они могут вызывать выделение образующегося хлора в присутствии серебра во всех частях печи. С другой стороны, потеря золота увеличивается при всяком увеличении количества либо серебра, либо неблагородных металлов, так как в первом случае продлевается время обжига. Наилучший эффект хлорирования достигается в сильно окисляющей атмосфере, так что в руде требуется очень мало серы, а если ее много, то практика удаления большей части перед добавлением соли вряд ли приведет к ее уменьшению. в процентах образовавшегося хлорида серебра. Кроме того, водяной пар в топочных газах способствует образованию соляной кислоты. Когда при обжиге используется соль, руде часто дают медленно остыть в кучах после извлечения из печи. При такой обработке обнаруживается, что более высокий процент серебра и т. д. оказывается хлорированным, чем если бы руду сразу увлажняли или даже рассыпали для охлаждения тонким слоем. С другой стороны, потери золота от испарения увеличиваются при медленном охлаждении. Хлор продолжает выделяться еще долгое время после того, как произошло изъятие шихты, кучи сильно пахнут газом.
С другой стороны, потеря золота увеличивается при всяком увеличении количества либо серебра, либо неблагородных металлов, так как в первом случае продлевается время обжига. Наилучший эффект хлорирования достигается в сильно окисляющей атмосфере, так что в руде требуется очень мало серы, а если ее много, то практика удаления большей части перед добавлением соли вряд ли приведет к ее уменьшению. в процентах образовавшегося хлорида серебра. Кроме того, водяной пар в топочных газах способствует образованию соляной кислоты. Когда при обжиге используется соль, руде часто дают медленно остыть в кучах после извлечения из печи. При такой обработке обнаруживается, что более высокий процент серебра и т. д. оказывается хлорированным, чем если бы руду сразу увлажняли или даже рассыпали для охлаждения тонким слоем. С другой стороны, потери золота от испарения увеличиваются при медленном охлаждении. Хлор продолжает выделяться еще долгое время после того, как произошло изъятие шихты, кучи сильно пахнут газом.
Платтнер доказал в 1856 г., что при окислительном обжиге обычного золотосодержащего пирита потеря золота может иметь место только тогда, когда операция выполняется настолько быстро, что мелкие частицы механически уносятся проект. Этот вывод в отношении сульфидов и арсенидов был подтвержден Кустелем и проф. С. Б. Кристи, но последний добавляет, что чрезвычайно трудно предотвратить все механические потери от пыли, вызываемой даже умеренным сквозняком. . Кустель отмечает потерю 20% золота, присутствующего при окислительном обжиге некоторых теллуридов золота и серебра, и утверждает, что это не механическая потеря, а следствие улетучивания. Кажется, это ошибка, см. 7.
Потери золота при добавлении соли в шихту могут быть очень большими. Кустель обнаружил, что теллуридная руда при обжиге с 4%. соли, потерял 8 процентов. золота до того, как руда раскалится докрасна. Аарон обнаружил, что некоторые руды, состоящие из простого пирита, сильно теряют золото при обжиге с добавлением соли в начале операции; лишь небольшая часть этого золота сконденсировалась в дымоходе, в котором был обнаружен желтоватый рыхлый осадок, состоящий в основном из хлоридов меди и железа и содержащий около 30 унций. золота на тонну. Он обнаружил, что потери значительно уменьшились за счет уменьшения количества соли и сохранения ее до тех пор, пока не было почти завершено обжаривание мертвых продуктов.
золота на тонну. Он обнаружил, что потери значительно уменьшились за счет уменьшения количества соли и сохранения ее до тех пор, пока не было почти завершено обжаривание мертвых продуктов.
При хлорирующем обжиге мексиканской руды, состоящей в основном из магнетита и пирита с содержанием халькопирита от 3,5 до 7 процентов, К. А. Штетефельдт обнаружил потери золота от 42,8 до 93 процентов. всего содержащегося золота. Он утверждает, что «нет сомнения, что улетучивание золота происходит вместе с улетучиванием хлоридов меди. Потери увеличивались с увеличением количества этих образовавшихся и улетучившихся хлоридов». Далее он показывает, однако, что присутствие хлорида меди — не единственная возможная причина потерь, поскольку руда, состоящая из твердого белого кварца, тщательно смешанного примерно с 7 процентами кальцита и небольшим количеством пирита, теряет 70—80 процентов. процентов серебра и от 68 до 85 процентов. золота при обжиге с 5% соли. При окислительном обжиге потери золота не произошло. Причина необычного поведения этой руды не была обнаружена.
Причина необычного поведения этой руды не была обнаружена.
Профессор Кристи обнаружил, что в рудах, с которыми он экспериментировал в небольшом количестве в муфельной печи, потери были больше при добавлении соли ближе к концу операции обжига, чем при смешивании той же массы соли с муфельной печью. руда в начале. Он объяснил, что это связано с тем, что количество испаряемого золота зависит от количества хлора, который вступает с ним в контакт. Когда соль добавляется вначале, хлор сначала удаляется серой по мере его образования, испаряясь в виде хлорида серы, и таким образом золото предохраняется от воздействия. Когда соль добавляется после длительного окислительного обжига, быстро образуется хлор (руда раскалена докрасна и содержит большое количество сульфатов), и золото больше не защищено от воздействия серы. Потери золота также во всех случаях увеличиваются при работе при более высокой температуре из-за образования большого количества хлора и увеличения летучести золота. Из результатов, приведенных на с. 23, температура, используемая при хлоридирующем обжиге, должна очень тщательно регулироваться, так как потери золота гораздо больше увеличиваются при высокой температуре, чем при удлинении времени в печи. Кроме того, соль должна быть уменьшена до минимально возможного количества. Следует, однако, помнить, что максимальная летучесть хлорида золота приходится примерно на 250°, или намного ниже красного каления.
23, температура, используемая при хлоридирующем обжиге, должна очень тщательно регулироваться, так как потери золота гораздо больше увеличиваются при высокой температуре, чем при удлинении времени в печи. Кроме того, соль должна быть уменьшена до минимально возможного количества. Следует, однако, помнить, что максимальная летучесть хлорида золота приходится примерно на 250°, или намного ниже красного каления.
Практическое преимущество добавления соли ближе к концу операции связано с тем, что при непрерывном обжиге руды в печах с длинным подом газы, выходящие из чистового пода, проходят через большое длина сравнительно холодной, несоленой и неокисленной руды до попадания в газоход. Количество хлорида золота, смешанного с хлором, который выделяется из раскаленной руды, как только добавляется соль, несомненно велико, но SO2 из более холодной руды и пар из топлива «предлагают превосходные средства для восстановление хлорида золота прямо в печи, в то время как наиболее эффективным средством, вероятно, являются сами пириты», которые, как было доказано, легко способны конденсировать золото на своей поверхности. Если вся соль добавляется в начале, хлорид золота продолжает улетучиваться по всей печи и менее благоприятная возможность для его конденсации. Таким образом, объясняется различие результатов в муфеле и в отражательной печи.
Если вся соль добавляется в начале, хлорид золота продолжает улетучиваться по всей печи и менее благоприятная возможность для его конденсации. Таким образом, объясняется различие результатов в муфеле и в отражательной печи.
В Невада-Сити, на шахте Меррифилд и на других предприятиях по соседству в 1888 году все еще использовалась старомодная длинная печь с одним уступом, отделяющим чистовой под от остальной части печи. Эти печи от 55 до 65 футов в длину, вмещающие от 6 до 9 тонн и производящие около 3 тонн обожженной руды в день, так что руда остается в печи от двух до трех дней. Там был обычай подвергать руду длительному окислительному обжигу при слабом красном калении, заканчивающемся слабым вишнево-красным калением, а затем, когда руда доходила до отделочного этажа, температуру немного понижали и добавляли соль. Соль тщательно вмешивалась в руду, и как только она «растворялась» в прокаленной руде, т. е. примерно через полчаса, шихта стягивалась в охлаждающую яму. Это понижение температуры, очевидно, имеет большое значение для уменьшения потерь, в то время как продолжительность обжига считается менее существенной, пока не присутствует соль. Эти заводы работали по индивидуальному заказу, взимая от 15 до 17 долларов за тонну руды для обработки и гарантируя выход 90 процентов золота и 60 процентов серебра. Их метод обжарки, по-видимому, считается в Калифорнии наиболее подходящим для концентратов, содержащих высокий процент серы, но их потери при обжиге не установлены. Однако наилучший метод обжига какой-либо конкретной руды не может быть определен каким-либо общим правилом, и в каждом случае должны быть проведены исчерпывающие эксперименты, прежде чем будет окончательно принят определенный порядок действий.
Эти заводы работали по индивидуальному заказу, взимая от 15 до 17 долларов за тонну руды для обработки и гарантируя выход 90 процентов золота и 60 процентов серебра. Их метод обжарки, по-видимому, считается в Калифорнии наиболее подходящим для концентратов, содержащих высокий процент серы, но их потери при обжиге не установлены. Однако наилучший метод обжига какой-либо конкретной руды не может быть определен каким-либо общим правилом, и в каждом случае должны быть проведены исчерпывающие эксперименты, прежде чем будет окончательно принят определенный порядок действий.
На одном из калифорнийских хлораторных заводов в 1882 г. экспериментально было установлено, что почти 50% золота и 28% серебра теряются при испарении. В этом случае пирит обжигали на двух очагах в течение тридцати шести часов, добавляя 1% соли за четыре часа до подачи шихты. Профессор Кристи считал, что причиной больших потерь была высокая температура обжига, особенно на этаже загрузки.
Варьирование убыли в различных рудах, которые обрабатываются совершенно одинаково, несомненно, частично связано с присутствием или отсутствием металлов, образующих летучие хлориды, которые уносят золото, а частично с физическим состоянием последнего, причем улетучивание выше, если он находится в состоянии мельчайшего подразделения.

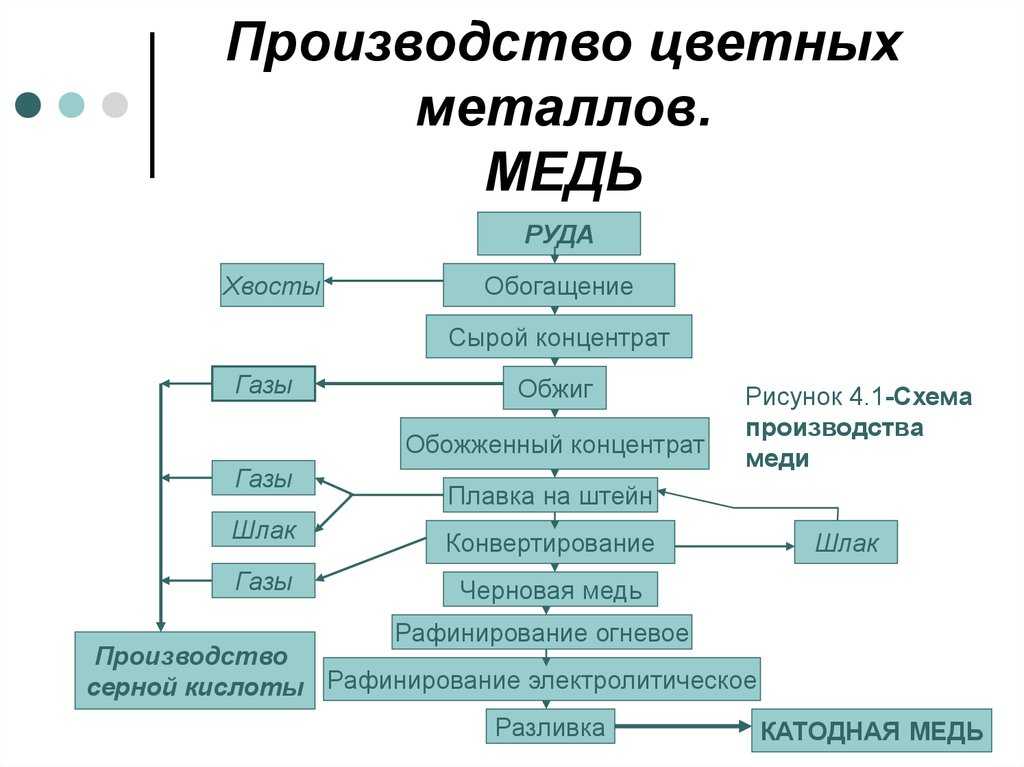 Электролиз расплавленной соли, используемый в производстве алюминия, является еще одним примером пирометаллургического процесса.
Электролиз расплавленной соли, используемый в производстве алюминия, является еще одним примером пирометаллургического процесса. также
также