Химическая связь: какие силы удерживают атомы между собой?
Всем известно, что химия – это наука, изучающая различные вещества, их свойства и взаимодействие. Сами же вещества состоят из атомов и молекул, связанных друг с другом. Характер этой химической связи определяет важнейшие свойства вещества, он может иметь разную природу, поэтому в этом посте мы разберёмся (или вспомним) в том, какими бывают химические связи. В общем случае, образование химической связи подчиняется двум законам: закону Кулона и правилу октетов. Согласно первому, если мы имеем две частицы с зарядами q1 и q2 , которые находятся на расстоянии r друг от друга, то сила их взаимодействия будет равна . Причём одноименно заряженные частицы будут отталкиваться, а
разноимённые – притягиваться друг к другу. Из этого закона следует, что
величина силы электростатического притяжения (или отталкивания) зависит от
величин зарядов и, в значительной степени, от расстояния между ними. Согласно модели Бора, атом представляет собой положительно
заряженное ядро, окружённое электронами, каждый из которых движется по своим
траекториям – орбиталям — и имеет
определённый уровень энергии. Число электронов соответствует заряду ядра, т.е.
суммарно весь атом элемента не имеет заряда, т.е. электронейтрален. Чтобы «оторвать» или «прилепить» электрон к
атому, нужно преодолеть энергию, соответствующую тому или иному электрону, и
чем глубже по подуровням он находится, тем сложнее это сделать. Поскольку
«верхние» электроны дальше всех остальных находятся от ядра, то притягиваются
им слабее, чем остальные, и имеют наименьшую энергию. Такие электроны
называются валентными, а верхний уровень, на котором они находятся – валентным.
Валентные электроны – самые подвижные, именно они и участвуют в образовании
химической связи. При попытках объяснить образование химической связи, Гилберт
Льюис предложил Правило октетов. Оно заключается в том, что все атомы стремятся
иметь замкнутую 8-ми электронную внешнюю оболочку, как у атомов благородных
газов. Это правило имеет несколько исключений, но здесь их рассмотрение не так
важно. Таким образом, глядя на Периодическую систему элементов, мы можем
поделить все элементы на те, у которых на внешнем уровне мало электронов и им
проще их отдать, чтобы замкнуть оболочку – металлы, и те, которым выгоднее
присоединить к себе несколько электронов – неметаллы. С ростом периода увеличивается радиус атомов,
и появляются более объёмные d-
и
f-орбитали,
соответственно, валентные электроны удерживаются слабее, чем в атомах той же
группы с меньшим радиусом. Поэтому такие элементы, даже если их валентный
уровень заполнен больше, чем наполовину, будут металлами. Например, в 6 группе
побочной подгруппе находится хром. Несмотря на 6 электронов на валентном
уровне, ему выгоднее не присоединять ещё два электрона, как соседу по группе
кислороду, а отдавать, поэтому хром – металл и обладает всеми свойствами
металлов. Теперь, основываясь на этих законах, можем (наконец-то) перейти и к типам химической связи. Если связь образована двумя элементами-металлами, то связь между ними будет металлическая, также будет называться и кристаллическая решётка металлов и их сплавов. Поскольку металлы склонны отдавать электроны, делают они это и в своих кристаллах, получается, что атомы металлов отдают свои валентные электроны во внешнее пространство, а сами ионизируются – превращаются в положительно заряженные частицы – катионы. Катионы находятся в узлах такой решётки, а их электроны свободно движутся по всему кристаллу, образуя электронное облако. Оно «не улетает» из-за электростатического взаимодействия с катионами, поэтому металлическая связь и не разваливается. Благодаря такой связи и металлической решётке металлы и их сплавы блестящие, твёрдые, ковкие материалы. Иначе образуется связь между двумя атомами-неметаллами.
Обоим нужны электроны для завершения валентного уровня, поэтому эти элементы,
чтобы не остаться в проигрыше, образуют общие на двоих электронные пары.  Проще всего образуется связь между металлом и неметаллом: металл отдаёт свои «лишние» электроны атому-неметаллу, который с радостью достраивает ими свою валентную оболочку до восьмиэлектронной. При этом металл становится катионом – положительно заряженной частицей, а неметалл – анионом, отрицательно заряженной частицей. Причём, если в диполе более э.о. элемент просто стягивает на себя электронную плотность, они всё равно принадлежат всей молекуле, то здесь неметалл забирает эти электроны себе «насовсем». Ионы связаны между собой электростатически, а такая кристаллическая решётка называется ионной. Ионная связь присуща в первую очередь солям, которые образованы ионом металла и кислотным остатком. Таким образом, мы можем выделить четыре типа связи,
образующихся между атомами элементов: металлическую, ковалентную полярную и
неполярную, ионную. Каждому из них соответствует свой тип кристаллической
решётки, который обуславливает свойства соответствующих им веществ. Но не
только атомы взаимодействуют между собой: химическая связь может образовываться
и между целыми молекулами и их фрагментами. |
Как ядерные частицы удерживаются вместе?
В то время, когда построение атома было уже завершено, работа над созданием модели ядра была еще в самом разгаре. Возможно, если бы ядро представляло собой один заряд Z с массой А, никаких дополнительных проблем и не возникло бы. Однако в этом случае пришлось бы ввести множество различных и не связанных между собой понятий. Поэтому в целях экономии и на основании опытных данных (превращение одного ядра в другое, излучение ядрами протонов, нейтронов, α-частиц, электронов и γ-лучей) следовало признать, что ядра состоят из более простых объектов, которые каким-то образом удерживаются вместе и могут после соответствующей перегруппировки образовать другое ядро.
Несложный расчет показывает, что для того, чтобы ядра могли считаться состоящими из нейтронов и протонов, удерживающихся вместе под действием приложенных между ними сил, следует ввести новый вид сил. С помощью классических сил — гравитационной или электромагнитной — невозможно разумным образом объяснить устойчивость ядерного вещества. Кулоновская сила расталкивания, действующая между положительно заряженными протонами, равна:
С помощью классических сил — гравитационной или электромагнитной — невозможно разумным образом объяснить устойчивость ядерного вещества. Кулоновская сила расталкивания, действующая между положительно заряженными протонами, равна:
а гравитационная сила притяжения дается формулой:
где Мр — масса протона, так что их отношение составляет
Малость этой величины (зависящей для ядерных частиц от их массы и заряда) является причиной того, что гравитационные силы считаются в ядрах несущественными по сравнению с электрическими. На этом основании приходится допустить, что между ядерными частицами (протонами и нейтронами) действует какая-то иная притягивающая сила, превышающая расталкивающее влияние электромагнитных сил, причем эта сила должна быть настолько большой, чтобы устойчивые ядра могли существовать вопреки электромагнитному расталкиванию между положительными зарядами; об устойчивости ядер говорит хотя бы то, что только к концу девятнадцатого века удалось наблюдать превращение одного ядра в другое.
Величину характерной энергии взаимодействия нуклонов легко оценить, используя тот факт, что ядерные силы притяжения должны превышать электромагнитные силы расталкивания, действующие между положительными зарядами. Так, в ядро, содержащее 50 положительных зарядов, удается ввести еще один протон (в результате получится ядро с Z=51), если на преодоление электрических сил затрачивается энергия порядка 10 МэВ. Действительно, электрическая энергия протона, находящегося внутри такого ядра, близка к 10 МэВ (фиг. 199):
Из этих оценок видно, что характерная энергия ядерных частиц и ядерных процессов исчисляется миллионами электронвольт, а не десятками электронвольт, как это было в случае атомных процессов. (Электроны в атоме находятся примерно на расстоянии 10-8 см от ядра, протоны же в ядре находятся на расстоянии порядка 10-13 см друг от друга. В результате соответствующие кулоновские силы различаются между собой множителем 108. )
)
Эти оценки совпадают с наблюдаемыми значениями энергии, получающимися при простых ядерных экспериментах. Энергия атомных переходов имеет порядок электронвольт. Энергия же продуктов ядерных превращений — α-, β- и γ-лучей — обычно порядка миллиона электронвольт. Характерная энергия ядерных процессов настолько велика по обычным масштабам, что с ее помощью можно измерить соответствующий дефект массы:
В 1905 г. Эйнштейн, говоря о своем соотношении между энергией и массой, предлагал:
«Не исключена возможность того, что теорию удастся проверить для веществ, энергия которых меняется в большой степени (например, для солей радия)».
Сравнение масс и кинетических энергий исходных и конечных ядер, участвующих в ядерных процессах, дает, вероятно, наиболее точное и убедительное подтверждение справедливости формулы Эйнштейна.
Измеренные массы протонов и нейтронов можно сравнить с массой ядра, содержащего эти частицы. Получающуюся разность масс (дефект массы) можно сопоставить с измеренными значениями энергии, высвобождающейся при слиянии протонов и нейтронов или затраченной при расщеплении ядра. В качестве примера рассмотрим дейтрон — ядро изотопа водорода, содержащее один протон и один нейтрон. Проведем расчет, напоминающий бухгалтерский баланс:
В качестве примера рассмотрим дейтрон — ядро изотопа водорода, содержащее один протон и один нейтрон. Проведем расчет, напоминающий бухгалтерский баланс:
Величина 2,225 МэВ есть энергия, которая выделяется при слиянии протона и нейтрона с образованием дейтрона или требуется для разделения дейтрона на протон и нейтрон. Этот вывод можно проверить, измеряя энергию фотона, расщепляющего дейтрон (фиг. 200).
В общем случае энергия связи ядра (энергия основного состояния ядерной системы при условии, что энергия нуклонов, на которые оно расщеплено, полагается равной нулю) определяется либо по измеренному значению энергии, необходимой для расщепления ядра на составляющие его частицы (протоны и нейтроны), либо по разности масс ядерной системы и отдельных протонов и нейтронов, из которых состоит эта система. Энергия и разность масс (дефект массы) связаны между собой с помощью соотношения Эйнштейна (как было в случае дейтрона).
Метки: атомгравитационные силыдейтрондефект массыизлучение энергиикинетическая энергияклассические силыкулоновские силымасса протонамодель ядранейтронсостояние Эйнштейнаэлектровольтэлектромагнитные силыэлектроныядерные процессы
Строение газообразных, жидких и твердых тел — Гипермаркет знаний.
 Строение газообразных жидких и твёрдых тел Газы Строение газообразных жидких и твердых тел физика
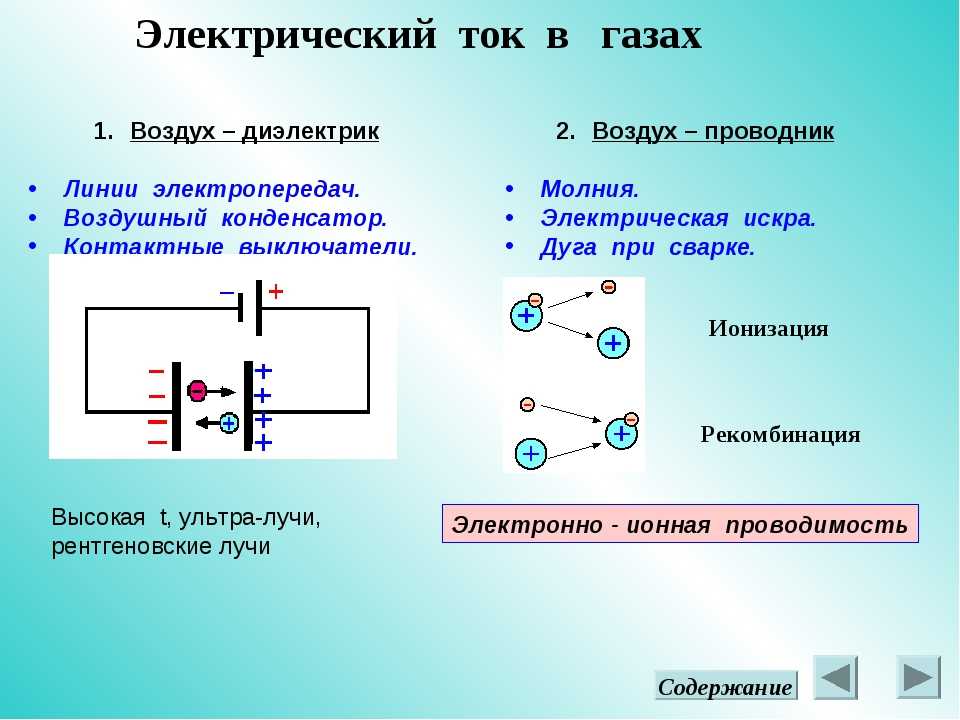
Строение газообразных жидких и твёрдых тел Газы Строение газообразных жидких и твердых тел физикаИзучив свойства и строение твёрдых, жидких и аморфных тел, для которых характерны дальний или ближний порядок в расположении частиц, перейдём к рассмотрению свойств и строения газообразных тел. Для газов характерно полное отсутствие порядка в расположении и движении частиц. Как говорят физики, во всех газах их частицы расположены и движутся хаотически (греч. «хаос» – беспорядок).
Вы знаете много газов: водород, кислород, углекислый газ, водяной пар, пары ртути, азот, озон, хлор, воздух (как смесь газов). Все они очень разные. Водород лёгкий, а углекислый газ тяжёлый; азот не пахнет, а озон «щиплет» нос; водяные пары безвредны, а пары ртути ядовиты; воздух бесцветный, а хлор имеет жёлто-зелёный цвет. Эти свойства у газов разные, но есть и общие.
Во-первых, все газы очень хорошо поддаются сжатию. Их можно сжать в 100 и более раз. Во-вторых, все газы подчиняются закону Паскаля, передавая оказанное на них давление в другие части сосуда. В-третьих, в отличие от жидкостей, газы всегда оказывают давление, даже в невесомости. Как же можно объяснить эти общие свойства всех газов? На этот вопрос отвечает молекулярно-кинетическая теория.
В-третьих, в отличие от жидкостей, газы всегда оказывают давление, даже в невесомости. Как же можно объяснить эти общие свойства всех газов? На этот вопрос отвечает молекулярно-кинетическая теория.
Строение газообразных тел. При обычных условиях расстояния между частицами газа во много раз больше размеров самих частиц, а кинетическая энергия их движения гораздо больше (по модулю) потенциальной энергии их притяжения друг к другу и/или к Земле. Поэтому частицы газа практически свободно летают, сталкиваясь друг с другом и «бомбардируя» стенки сосуда, в котором находятся.
Таково объяснение давления газов . Оно будет справедливым и в условиях невесомости, где давление газов сохраняется в отличие от давления твёрдых и жидких тел.
Заметим, что давление жидкости имеет совсем иное происхождение: вышележащие слои жидкости своим весом придавливают нижележащие слои (поэтому по мере опускания ко дну сосуда давление возрастает). В каждом слое из-за частых соударений частиц давление передаётся во все стороны, в том числе и на стенки сосуда. Поэтому в условиях невесомости (где жидкость и её отдельные слои не имеют веса) давление жидкости на дно и стенки сосуда будет равно нулю.
Поэтому в условиях невесомости (где жидкость и её отдельные слои не имеют веса) давление жидкости на дно и стенки сосуда будет равно нулю.
Это важное отличие происхождения давления газа от давления жидкости подтверждает опыт. На рисунке изображены два сосуда: левый – с жидкостью, а правый – с газом. Сосуды снабжены манометрами: вблизи дна, в средней части и вблизи горловины. Взгляните: у сосуда с газом манометры показывают одинаковые давления, а у сосуда с жидкостью – возрастающие значения по мере опускания. Причина этого – различный «механизм» происхождения давления в жидкостях и газах.
Объясним теперь свойство газов легко поддаваться сжатию и подчиняться закону Паскаля. Обратимся к рисунку. Вдвинув поршень, мы уплотним расположение частиц вблизи него. Однако вскоре эти частицы разлетятся по всему объёму сосуда, и в результате газ станет более плотным, а «бомбардировка» его частицами стенок сосуда – более интенсивной. То есть газ передаст оказанное на него давление поршня во все стороны.
Вспомним, что при увеличении температуры газа его давление возрастает (см. § 4-г). МКТ легко объясняет этот факт. Повышение температуры приводит к увеличению скорости движения частиц газа, поэтому «бомбардировка» частицами стенок сосуда усиливается, что и означает возрастание давления газа.
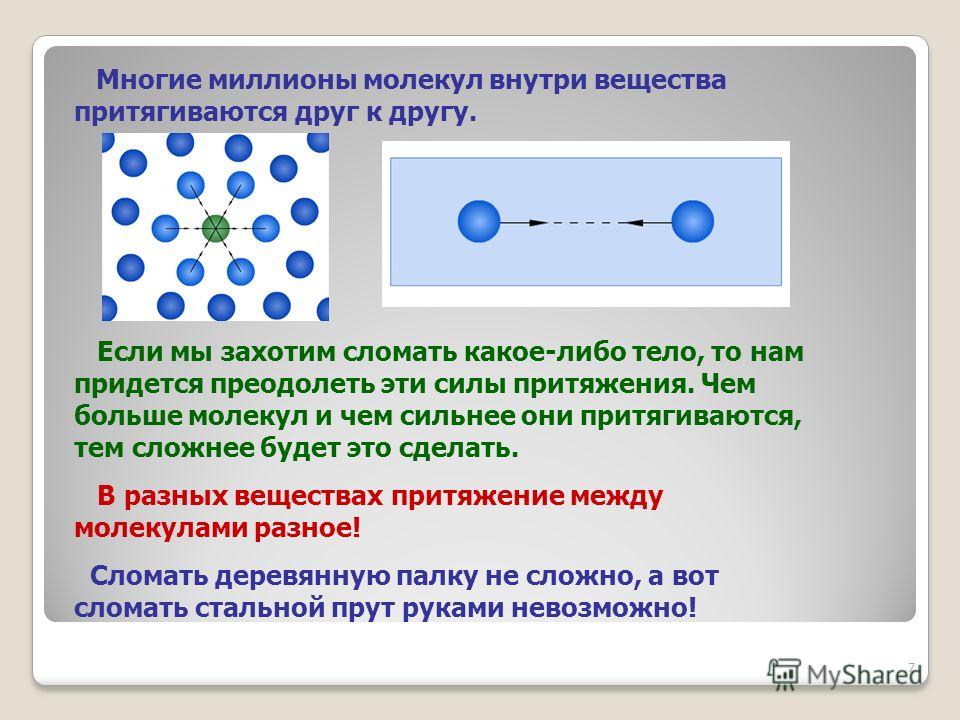
Вся неживая материя состоит из частиц, поведение которых может отличаться. Строение газообразных, жидких и твердых тел имеет свои особенности. Частицы в твердых телах удерживаются вместе, так как расположены очень тесно друг к другу, это делает их очень прочными. Кроме того, они могут держать определенную форму, так как их мельчайшие частицы практически не двигаются, а только вибрируют. Молекулы в жидкостях находятся довольно близко друг к другу, однако они могут свободно передвигаться, поэтому собственной формы они не имеют. Частицы в газах движутся очень быстро, вокруг них, как правило, много пространства, что предполагает их легкое сжатие.
Свойства и строение твердых тел
Какова структура и особенности строения твердых тел? Они состоят из частиц, которые расположены очень близко друг к другу. Они не могут перемещаться, и поэтому их форма остается фиксированной. Каковы свойства твердого тела? Оно не сжимается, но если его нагреть, то его объем будет увеличиваться с ростом температуры. Это происходит потому, что частицы начинают вибрировать и двигаться, что приводит к уменьшению плотности.
Они не могут перемещаться, и поэтому их форма остается фиксированной. Каковы свойства твердого тела? Оно не сжимается, но если его нагреть, то его объем будет увеличиваться с ростом температуры. Это происходит потому, что частицы начинают вибрировать и двигаться, что приводит к уменьшению плотности.
Одной из особенностей твердых тел является то, что они имеют неизменную форму. Когда твердое тело нагревается, средняя скорость движения частиц увеличивается. Быстрее движущиеся частицы сталкиваются более яростно, заставляя каждую частицу толкать своих соседей. Следовательно, повышение температуры обычно приводит к повышению прочности тела.
Кристаллическое строение твердых тел
Межмолекулярные силы взаимодействия между соседними молекулами твердого тела достаточно сильны, чтобы держать их в фиксированном положении. Если эти мельчайшие частицы находятся в высокоупорядоченной комплектации, то такие структуры принято называть кристаллическими. Вопросами внутренней упорядоченности частиц (атомов, ионов, молекул) элемента или соединения занимается специальная наука — кристаллография.
Химическое строение твердого тела также вызывает особый интерес. Изучая поведение частиц, того, как они устроены, химики могут объяснить и предсказать, как определенные виды материалов будут себя вести при определенных условиях. Мельчайшие частицы твердого тела расположены в виде решетки. Это так называемое регулярное расположение частиц, где немаловажное значение играют различные химические связи между ними.
Зонная теория строения твердого тела рассматривает твердое вещество как совокупность атомов, каждый их которых, в свою очередь, состоит из ядра и электронов. В кристаллическом строении ядра атомов находятся в узелках кристаллической решетки, для которой характерна определенная пространственная периодичность.
Что такое структура жидкости?
Строение твердых тел и жидкостей схоже тем, что частицы, из которых они состоят, находятся на близком расстоянии. Различие состоит в том, что молекулы жидкого вещества свободно перемещаются, так как сила притяжения между ними гораздо слабее, нежели в твердом теле.
Какими же свойствами обладает жидкость? Во-первых, это текучесть, во-вторых, жидкость будет принимать форму контейнера, в который ее помещают. Если ее нагреть, объем будет увеличиваться. Из-за близкого расположения частиц друг к другу жидкость не может быть сжата.
Какова структура и строение газообразных тел?
Частицы газа располагаются случайным образом, они находятся так далеко друг от друга, что между ними не может возникнуть сила притяжения. Какими свойствами обладает газ и каково строение газообразных тел? Как правило, газ равномерно заполняет все пространство, в которое он был помещен. Он легко сжимается. Скорость частиц газообразного тела увеличивается вместе с ростом температуры. При этом происходит также повышение давления.
Строение газообразных, жидких и твердых тел характеризуется разными расстояниями между мельчайшими частицами этих веществ. Частицы газа находятся гораздо дальше друг от друга, чем в твердом или жидком состоянии. В воздухе, например, среднее расстояние между частицами примерно в десять раз превышает диаметр каждой частицы. Таким образом, объем молекул занимает всего около 0,1 % от общего объема. Остальные 99,9 % составляет пустое пространство. В противоположность этому частицы жидкости заполняют около 70 % общего объема жидкости.
Таким образом, объем молекул занимает всего около 0,1 % от общего объема. Остальные 99,9 % составляет пустое пространство. В противоположность этому частицы жидкости заполняют около 70 % общего объема жидкости.
Каждая частица газа движется свободно по прямолинейному пути, пока она не столкнется с другой частицей (газа, жидкости или твердого тела). Частицы обычно движутся достаточно быстро, а после того как две из них сталкиваются, они отскакивают друг от друга и продолжают свой путь в одиночку. Эти столкновения меняют направление и скорость. Эти свойства газовых частиц позволяют газам расширяться, чтобы заполнить любую форму или объем.
Изменение состояния
Строение газообразных, жидких и твердых тел может меняться, если на них оказывается определенное внешнее воздействие. Они могут даже переходить в состояния друг друга при определенных условиях, например в процессе нагревания или охлаждения.
Поведение тел в разных физических состояниях
Строение газов, жидкостей, твердых тел главным образом обусловлено тем, что все эти вещества состоят из атомов, молекул или ионов, однако поведение этих частиц может быть совершенно разным. Частицы газа хаотичным образом удалены друг от друга, молекулы жидкости находятся близко друг к другу, но они не так жестко структурированы, как в твердом теле. Частицы газа вибрируют и передвигаются на высоких скоростях. Атомы и молекулы жидкости вибрируют, перемещаются и скользят мимо друг друга. Частицы твердого тела также могут вибрировать, но движение как таковое для них не свойственно.
Частицы газа хаотичным образом удалены друг от друга, молекулы жидкости находятся близко друг к другу, но они не так жестко структурированы, как в твердом теле. Частицы газа вибрируют и передвигаются на высоких скоростях. Атомы и молекулы жидкости вибрируют, перемещаются и скользят мимо друг друга. Частицы твердого тела также могут вибрировать, но движение как таковое для них не свойственно.
Особенности внутренней структуры
Для того чтобы понять поведение материи, нужно сначала изучить особенности ее внутренней структуры. Каковы внутренние различия между гранитом, оливковым маслом и гелием в воздушном шарике? Простая модель структуры материи поможет найти ответ на этот вопрос.
Модель является упрощенным вариантом реального предмета или вещества. Например, до того как начинается непосредственное строительство, архитекторы сначала конструируют модель строительного проекта. Такая упрощенная модель не обязательно предполагает точное описание, но в то же время она может дать приблизительное представление того, что будет собой представлять та или иная структура.
Упрощенные модели
В науке, однако, моделями не всегда выступают физические тела. За последнее столетие наблюдался значительный рост человеческого понимания о физическом мире. Однако большая часть накопленных знаний и опыта основана на чрезвычайно сложных представлениях, например в виде математических, химических и физических формул. Для того чтобы разобраться во всем этом, нужно быть достаточно хорошо подкованным в этих точных и сложнейших науках. Ученые разработали упрощенные модели для визуализации, объяснения и предсказания физических явлений. Все это значительным образом упрощает понимание того, почему некоторые тела имеют постоянную форму и объем при определенной температуре, а другие могут их менять и так далее.
Вся материя состоит из мельчайших частиц. Эти частицы находятся в постоянном движении. Объем движения связан с температурой. Повышенная температура свидетельствует об увеличении скорости движения. Строение газообразных, жидких и твердых тел отличается свободой передвижения их частиц, а также тем, насколько сильно частицы притягиваются друг к другу. Физические свойства вещества зависят от его физического состояния. Водяной пар, жидкая вода и лед имеют одинаковые химические свойства, но их физические свойства значительно отличаются.
Физические свойства вещества зависят от его физического состояния. Водяной пар, жидкая вода и лед имеют одинаковые химические свойства, но их физические свойства значительно отличаются.
Молекулярно-кинетическая теория дает возможность понять, почему вещество может находиться
в газообразном, жидком и твердом состояниях.
Если в самых общих чертах попробовать представить себе строение газов, жидкостей и твердых тел, то можно нарисовать следующую картину.
Газы
В газах расстояние между атомами или молекулами в среднем во много раз превышает размеры самих молекул (рис. 2.17). При атмосферном давлении объем сосуда в десятки тысяч раз превышает объем находящихся в сосуде молекул газа.
Газы легко сжимаются, так как при сжатии газа уменьшается лишь среднее расстояние между молекулами, но молекулы не «сдавливают» друг друга (рис. 2.18). Молекулы (или атомы) стремительно, как бегуны-спринтеры, но значительно быстрее проносятся в пространстве. Сталкиваясь друг с другом, они непрерывно изменяют направление своего движения и разлетаются в разные стороны.
Слабые силы притяжения молекул газа не способны удержать их около друг друга. Поэтому газы не сохраняют ни формы, ни объема. Как бы мы ни увеличивали размеры сосуда, содержащего газ, последний заполнит его целиком без каких-либо усилий с нашей стороны.
Можно получить более глубокое представление о состоянии вещества, называемого реальным газом, если проследить за характером зависимости потенциальной энергии одной из молекул от расстояния до ее ближайших соседей (рис. 2.19). При перемещении молекулы ее потенциальная энергия на большей части пути почти точно равна нулю, так как расстояние между молекулами в газе в среднем гораздо больше их размеров. В точках 1 и 2 расположены ближайшие соседи рассматриваемой молекулы. Данная молекула проходит на довольно значительном расстоянии от соседа 1 и на более близком от соседа 2.
щ
Ё Oh
Рис. 2.19
Средняя по времени потенциальная энергия молекулы от-рицательна и очень мала. По модулю она численно равна пло-щади фигуры, ограниченной потенциальной кривой между точками 1 и 2 и осью г, деленной на длину отрезка 1-2 (среднее значение потенциальной энергии на отрезке 1 -2). Полная средняя энергия обязательно больше нуля (прямая на рис. 2.19), так как при Е 0 возможно лишь при условии, что средняя кинетическая энергия молекулы газа больше среднего значения ее потенциальной энергии
Полная средняя энергия обязательно больше нуля (прямая на рис. 2.19), так как при Е 0 возможно лишь при условии, что средняя кинетическая энергия молекулы газа больше среднего значения ее потенциальной энергии
Ёк > \Ёр\, (2.6.1) так как Е = Ек + Ер, а Ер Жидкости
Молекулы жидкости расположены почти вплотную друг к другу (рис. 2.20), поэтому каждая молекула ведет себя иначе, чем молекула газа. Зажатая, как в клетке, другими молекула- ми, она совершает «бег на месте» (колеблется около положения равновесия, сталкиваясь с соседними молекулами). Лишь время от времени она совершает «прыжок», прорываясь сквозь «прутья клетки», но тут же попадает в новую «клетку», образованную новыми соседями. Время оседлой жизни молекулы воды, т. е. время колебаний около одного определенного положения равновесия, при комнатной температуре, как показывают расчеты, выполненные с применением законов статистической механики, равно в среднем Ю-11 с. Время же, за которое совершается одно колебание, значительно меньше (10~12-10~13с). С повышением температуры время оседлой жизни молекул уменьшается. Характер молекулярного движения в жидкостях, впервые установленный советским физиком Я. И. Френкелем, позволяет понять основные свойства жидкостей.
С повышением температуры время оседлой жизни молекул уменьшается. Характер молекулярного движения в жидкостях, впервые установленный советским физиком Я. И. Френкелем, позволяет понять основные свойства жидкостей.
Молекулы жидкости находятся непосредственно друг возле друга. Поэтому при попытке изменить объем жидкости даже на малую величину начинается деформация самих молекул (рис. 2.21). Для этого нужны очень большие силы. Этим и объясняется малая сжимаемость жидкостей. Понять причину малой сжимаемости жидкости ничуть не сложнее, чем понять, почему так трудно втиснуться в переполненный автобус.
Жидкости, как известно, текучи, т. е. не сохраняют своей формы. Объяснить это можно так. Если жидкость неподвижна, то перескоки молекул из одного «оседлого» положения в другое происходят с одинаковой частотой по всем направлени-
1
>1
Френкель Яков Ильич (1894-1952) — выдающийся советский физик-теоретик, внесший значительный вклад в самые различные области физики. Я. И. Френкель — автор современной теории жидкого состояния вещества. Им заложены основы теории ферромагнетизма. Широко известны работы Я. И. Френкеля по атмосферному электричеству и происхождению магнитного поля Земли. Первая количественная теория деления ядер урана создана Я. И. Френкелем. Рис. 2.21
Им заложены основы теории ферромагнетизма. Широко известны работы Я. И. Френкеля по атмосферному электричеству и происхождению магнитного поля Земли. Первая количественная теория деления ядер урана создана Я. И. Френкелем. Рис. 2.21
Рис. 2.22
Рис. 2.20 ям (см. рис. 2.20). Наличие внешней силы заметно не изменяет числа перескоков молекул в секунду, но перескоки молекул из одного «оседлого» положения в другое при этом происходят преимущественно в направлении действия внешней силы (рис. 2.22). Вот почему жидкость течет и принимает форму сосуда.
Для течения жидкости необходимо только, чтобы время действия силы было во много раз больше времени «оседлой жизни» молекулы, иначе кратковременная сила вызовет лишь упругую деформацию жидкости, и обычная капля воды поведет себя, как стальной шарик.
Теперь рассмотрим, как связаны средняя кинетическая и средняя потенциальная энергии молекулы жидкости. Каждая молекула жидкости взаимодействует сразу с несколькими соседями. Ограничимся учетом взаимодействия данной молекулы с двумя ближайшими соседями, находящимися примерно на расстоянии 2г0 друг от друга.
Искомую потенциальную кривую можно получить наложением кривой, изображенной на рисунке 2.15, а (парное взаи-модействие), на такую же кривую, смещенную относительно первой на расстояние, чуть большее 2г0. Потенциальные энергии складываются, поэтому глубина потенциальной ямы уве-личивается почти вдвое, а максимумы энергии уменьшаются (рис. 2.23). Ход потенциальной кривой с учетом взаимодействия с другими молекулами показан на рисунке 2.24.
Для того чтобы молекула не могла покинуть жидкость, ее средняя энергия должна быть отрицательна (Е в этом случае молекула останется внутри потенциальной ямы, образованной ее соседями. Если Е > 0, то молекула не удер-жится внутри жидкости и покинет ее.
Так как Е = Ец + Ер, и Ер Ёк Поэтому |.Е| |-Еро| — максимального (по модулю) значения потенциальной энергии. На рисунке 2.24 график средней энергии молекулы изображен отрезком прямой.
Колебания молекулы в потенциальной яме не продолжаются долго. Из-за хаотичности движения молекул их энергия не-прерывно меняется и становится то больше, то меньше средней энергии Е. Как только энергия молекулы превысит высоту потенциальной кривой (высоту потенциального барьера), отделяющей одну яму от другой, молекула перескочит из одного положения равновесия в другое.
Как только энергия молекулы превысит высоту потенциальной кривой (высоту потенциального барьера), отделяющей одну яму от другой, молекула перескочит из одного положения равновесия в другое.
Твердые тела
Атомы или молекулы твердых тел в отличие от жидкостей не могут разорвать свои связи с ближайшими соседями и колеблются около определенных положений равновесия. Правда, иногда молекулы изменяют положение равновесия, но происходит это крайне редко. Вот почему твердые тела сохраняют не только объем, но и форму.
Есть еще одно различие между жидкими и твердыми тела-ми. Жидкость можно сравнить с толпой, в которой люди бес-покойно толкутся на месте, а твердое тело, как правило, подобно стройной когорте, где люди хотя и не стоят по стойке «смирно», но выдерживают между собой в среднем определенные интервалы. Если соединить центры положений равновесия атомов или молекул твердого тела, то получится правильная пространственная решетка, называемая кристаллической. На рисунках 2.25 и 2. 26 показаны кристаллические решетки по-варенной соли и алмаза.
26 показаны кристаллические решетки по-варенной соли и алмаза.
Рис. 2.25
Рис. 2.26
Если кристаллу не мешают расти, то внутренний порядок в расположении атомов приводит к геометрически правильным внешним формам.
Кривая потенциальной энергии взаимодействия молекулы твердого тела со своими ближайшими соседями (рис. 2.27) похожа на кривую потенциальной энергии взаимодействия молекул жидкости (см. рис. 2.24). Только глубина потенциальной ямы должна быть несколько больше, так как молекулы
Рис. 2.27
расположены ближе друг к другу. Условие |l?| выпол-няемое для жидких тел, выполняется и для твердых. Но кине-тическая энергия молекул твердого тела значительно меньше, чем молекул жидкости. Ведь твердые тела образуются при ох- лаждении. Соответственно в твердых телах средняя кинетическая энергия молекул значительно меньше абсолютного значения средней потенциальной энергии:
Ek « \ЁР\. (2.6.3)
На рисунке 2.27 средняя энергия молекулы внутри ямы изображена отрезком прямой. Частица совершает колебания у дна потенциальной ямы. Высоты потенциальных барьеров между соседними ямами велики, и молекулы почти не перемещаются из одного положения равновесия в другое. Для перемещения молекула должна получить энергию, значительно превышающую среднюю. Это событие маловероятно. Вот почему твердые тела в отличие от жидкостей сохраняют свою форму.
Частица совершает колебания у дна потенциальной ямы. Высоты потенциальных барьеров между соседними ямами велики, и молекулы почти не перемещаются из одного положения равновесия в другое. Для перемещения молекула должна получить энергию, значительно превышающую среднюю. Это событие маловероятно. Вот почему твердые тела в отличие от жидкостей сохраняют свою форму.
У газов средняя кинетическая энергия молекул больше средней потенциальной энергии. У жидкостей средняя кинетическая энергия немного меньше средней потенциальной, у твердых тел средняя кинети-ческая энергия много меньше средней потенциальной.
Урок по МКТ для учащихся 10 класса по теме «Строение газообразных, жидких и твердых тел».
На уроке рассматриваются особенности строения и свойства газообразных, жидких и твёрдых тел с точки зрения молекулярно – кинетической теории.
Скачать:
Предварительный просмотр:
Чтобы пользоваться предварительным просмотром презентаций создайте себе аккаунт (учетную запись) Google и войдите в него: https://accounts. google.com
google.com
Подписи к слайдам:
1 В одном мгновенье видеть вечность Огромный мир – в зерне песка, В едином миге – бесконечность И небо – в чашечке цветка. У. Блейк.
Тема урока: Строение газообразных, жидких и твердых тел. 2
Различают четыре агрегатных состояния вещества: 3 Жидкое Твёрдое Газообразное Плазменное
Фазовый переход – переход системы из одного агрегатного состояния в другое. При фазовом переходе скачкообразно изменяется какая-либо физическая величина (плотность, внутренняя энергия) 4
Газы Легко сжимаются. Могут неограниченно расширяться. Не сохраняют ни форму ни объём. Многочисленные удары молекул о стенки сосуда создают давление газа. 5) Силы взаимодействия очень малы. 6) Молекулы движутся хаотически. 10
Мало сжимаются. Сохраняют свой объём. Текучи, легко меняют форму. Принимают форму сосуда. Силы взаимодействия большие. Молекулы движутся беспорядочно, перескоками. Жидкости 14
Твёрдые тела Сохраняют объём и форму Молекулы или атомы колеблются около определённых положений равновесия Силы взаимодействия очень большие 4) Большинство твёрдых тел имеет кристаллическую решётку 18
Газы Жидкости Твердые тела 200 100 100 200 200 100 300 300 300 19
20 Газы 100 Почему газы способны неограниченно расширяться? Слабые силы притяжения молекул газа не способны удержать их друг возле друга
21 Газы 200 Почему газы легко сжимаются? Расстояние между атомами или молекулами в газах во много раз больше размеров самих молекул.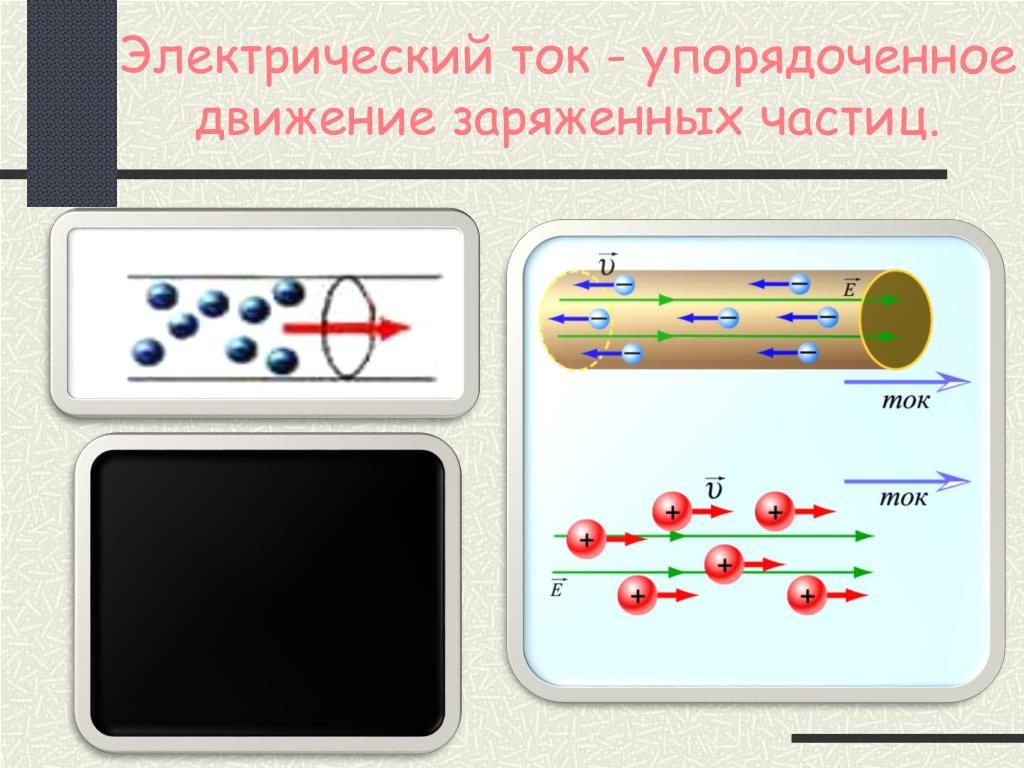
22 Газы 300 За счёт чего создаётся давление газа на дно и стенки сосуда? Многочисленные удары молекул о стенки сосуда создают давление газа.
23 Жидкости 100 Почему сжать жидкость почти так же трудно, как и твёрдое тело? Молекулы жидкости находятся непосредственно друг возле друга. При попытке сжать жидкость начинается деформация самих молекул
24 Жидкости 200 В каких агрегатных состояниях может находиться яблочный сок? Во всех трёх: жидком, твёрдом, газообразном.
25 Жидкости 300 Как называется процесс перехода вещества из жидкого состояния в твёрдое? Кристаллизация
26 Твердые тела 100 Как называется процесс перехода вещества из твёрдого состояния в газообразное? Сублимация
27 Твердые тела 200 Велики или малы силы притяжения между молекулами в твёрдых телах? Очень велики
28 Твердые тела 300 Как движутся молекулы в твёрдых телах? Колеблются около определённых положений равновесия.
I вариант I – 3 II — 2 , 5 III — 1 IV — 1 V — 4 II вариант I — 1 II — 1, 4, 5 III — 3 IV — 3 V — 4 III вариант I — 2 II — 1, 3, 5 III — 1 IV — 4 V — 4 IV вариант I — 3 II — 1, 4 III — 3 IV — 2 V — 4 Ответы к тесту 29
Домашнее задание § 61, 62 Ответить на вопросы к § 62 Заполнить таблицу Агрегатное состояние вещества Расстояние между частицами Взаимодействие частиц Характер движения частиц Сохранение формы и объема 30
Конец урока 31
Предварительный просмотр:
Строение газообразных, жидких и твердых тел. § 61, 62
§ 61, 62
Цель урока: Рассмотреть особенности строения и свойства газообразных, жидких и твёрдых тел с точки зрения молекулярно – кинетической теории.
Задачи урока:
- Образовательные
- Способствовать овладению знаниями по теме “Строение газообразных, жидких и твёрдых тел”;
- Установить характер зависимости сил притяжения и отталкивания от расстояния между молекулами;
- Учиться решать качественные задачи.
- Развивающие
Развивать:
- наблюдательность, самостоятельность;
- логическое мышление
- умение применять знания теории на практике;
- содействовать развитию речи, мышления
- Воспитательные:
- Формирование представлений о единстве и взаимосвязи явлений природы.
- Формировать положительное отношение к предмету
Тип урока:
Форма урока: комбинированный
Комплексно-методическое обеспечение:
Компьютер, экран, мультимедийный проектор,
презентация
, образцы кристаллов, тестовые задания.
Межпредметные связи:
- химия
- информатика
Этапы урока.
- Организационный этап.
- Этап объяснения нового материала.
- Этап закрепления пройденного материала.
- Заключительный этап.
- Домашнее задание.
Ход урока
1. Организационный этап
Учитель: Здравствуйте. Ещё Наполеон I говорил: “Воображение правит миром”. А Демокрит утверждал, что “Ничего не существует кроме атомов”.
- Этап постановки целей и задач урока.
Согласитесь! Мир удивителен и многообразен. Человек издавна пытался объяснить необъяснимое, увидеть невидимое, услышать неслышимое. Оглядываясь вокруг себя, он размышлял о природе и пытался решить загадки, которые она перед ним ставила.
Русский поэт Фёдор Иванович Тютчев писал.
Не то, что мните вы, природа:
Не слепок, не бездушный лик –
В ней есть любовь, в ней есть язык.
Но со временем человек стал понимать, что именно закон стоит во главе всего, что нас окружает.
Вы, конечно же, ежедневно сталкиваетесь с различными физическими явлениями, которыми управляет закон, и в большинстве случаев можете предсказать, как они закончатся. Например, предскажите, чем закончатся следующие события:
- Если открыть флакон с духами, то …;
- Если нагреть лед, то …;
- Если сильно сжать два кусочка пластилина, то …;
- Если капнуть каплю масла на воду, то …;
- Если опустить термометр в горячую воду, то …
Учитель: Итак, давая свои ответы, вы руководствовались определенными знаниями, полученными ранее. Мы с вами каждый день наблюдаем целый ряд окружающих нас предметов: столы, стулья, книги, ручки, тетради, автомобили и т.д. Скажите, они нам только кажутся сплошными или они на самом деле являются таковыми?
Ученик: Только кажутся.
Учитель: Тогда скажите, из чего состоят все вещества?
Ученик: Из молекул или атомов
Учитель:
А, как вы думаете, молекулы различных веществ одинаковы или нет? Докажите.
Ученик: Нет. Они имеют разные химические соединения.
Учитель: Лед, вода и водяной пар состоят из одних и тех же молекул или нет?
Ученик: Да.
Учитель: Почему?
Ученик: Потому что это одно и то же вещество, но в разном виде
Учитель: Вот, ребята, мы и подошли к теме нашего урока. Откройте рабочие тетради, запишите дату и тему нашего урока: “Строение газообразных, жидких и твёрдых тел”.
В мире нет двух совершенно одинаковых предметов. Невозможно найти две одинаковые песчинки в горе песка или два одинаковых листика на дереве, а вот молекулы одного и того же вещества совершенно одинаковы. Например, воду мы привыкли видеть в жидком состоянии. Химическая формула воды H 2 O. В газообразном состоянии – это пары воды. (Какова химическая формула ?). В твёрдом состоянии, это лёд или снег. Всё та же химическая формула — H 2 O.
Тогда возникает вопрос: если молекулы одного и того же вещества совершенно одинаковы, то почему это вещество может находиться в разных агрегатных состояниях?
Вот на этот вопрос нам с вами и предстоит ответить сегодня на уроке.
Различают четыре агрегатных состояния вещества:
- Твёрдое
- Жидкое
- Газообразное
- Плазменное
Сегодня мы поговорим о трёх из них. Прежде познакомимся с понятием – фазовый переход. (Слайд 4)
Фазовый переход – переход системы из одного агрегатного состояния в другое. При фазовом переходе скачкообразно изменяется какая-либо физическая величина (плотность, внутренняя энергия)
Реализация агрегатного состояния вещества зависит от соотношения кинетической и потенциальной энергии молекул, входящих в его состав.
- Этап объяснения нового материала
Что символизирует каждый рисунок? (Разные агрегатные состояния)
Облачко – газообразное состояние вещества, бутылка – жидкое, кубик – твёрдое состояние. Поэтапно разберём строение газообразных, жидких и твёрдых тел. Выводы запишем в тетрадях.
- ГАЗЫ (Слайды 6 — 10)
Расстояние между атомами или молекулами в газах в среднем во много раз больше размеров самих молекул. Газы легко сжимаются, при этом уменьшается среднее расстояние между молекулами, но молекулы не сдавливают друг друга. Молекулы движутся с огромными скоростями — сотни метров в секунду. Сталкиваясь, они отскакивают друг от друга в разные стороны. Слабые силы притяжения молекул газа не способны удержать их друг возле друга. Поэтому газы могут неограниченно расширяться. Они не сохраняют ни формы, ни объема.
Газы легко сжимаются, при этом уменьшается среднее расстояние между молекулами, но молекулы не сдавливают друг друга. Молекулы движутся с огромными скоростями — сотни метров в секунду. Сталкиваясь, они отскакивают друг от друга в разные стороны. Слабые силы притяжения молекул газа не способны удержать их друг возле друга. Поэтому газы могут неограниченно расширяться. Они не сохраняют ни формы, ни объема.
- ЖИДКОСТИ (Слайды 11 — 14)
Молекулы жидкости расположены почти вплотную друг к другу, поэтому молекула жидкости ведет себя иначе, чем молекула газа. Зажатая, как в “клетке”, другими молекулами, она совершает “бег на месте” (колеблется около положения равновесия, сталкиваясь с соседними молекулами). Лишь время от времени она совершает “ прыжок”, прорываясь сквозь “прутья клетки”, но тут же попадает в новую клетку, образованную новыми соседями. Время оседлой жизни молекулы воды, т. е. время колебаний около одного определенного положения равновесия при комнатной температуре, равно в среднем 10
-11
с. Время же одного колебания значительно меньше (10
-12
-10
-13
с). С повышением температуры время оседлой жизни молекул уменьшается.
Время же одного колебания значительно меньше (10
-12
-10
-13
с). С повышением температуры время оседлой жизни молекул уменьшается.
Молекулы жидкости находятся непосредственно друг возле друга. При попытке изменить объем жидкости (даже на малую величину) начинается деформация самих молекул, для этого нужны очень большие силы. Этим и объясняется малая сжимаемость жидкостей.
Как известно, жидкости текучи, т. е. не сохраняют своей формы, они принимают форму сосуда.
Характер молекулярного движения в жидкостях, впервые установленный советским физиком Я. И. Френкелем, позволяет понять основные свойства жидкостей. (Слайд 15)
- ТВЁРДЫЕ ТЕЛА. (Слайды 16 – 18)
Атомы или молекулы твердых тел в отличие от атомов и молекул жидкостей колеблются около определенных положений равновесия. Правда, иногда молекулы меняют положение равновесия, но происходит это редко. Вот почему твердые тела сохраняют не только объем, но и форму.
Есть еще одно важное различие между жидкостями и твердыми телами.
Жидкость можно сравнить с толпой людей, где отдельные индивидуумы беспокойно толкутся на месте, а твердое тело подобно стройной когорте тех же индивидуумов, которые хотя и не стоят по стойке смирно, но выдерживают между собой в среднем определенные интервалы. Если соединить центры положений равновесия атомов или ионов твердого тела, то получится правильная пространственная решетка, называемая кристаллической.
На рисунках изображены кристаллические решетки поваренной соли и алмаза. Внутренний порядок в расположении атомов кристаллов приводит к правильным внешним геометрическим формам.
Итак, пришло время ответить на поставленный в начале урока вопрос: от чего зависит, что одно и то же вещество может находиться в разных агрегатных состояниях?
Ответы учащихся:
4. Этап закрепления пройденного материала. Игра “Что за состояние?”
(слайды 19 – 28)
100 Почему газы способны неограниченно расширяться?
Слабые силы притяжения молекул газа не способны удержать их друг возле друга
200 Почему газы легко сжимаются?
Расстояние между атомами или молекулами в газах во много раз больше размеров самих молекул.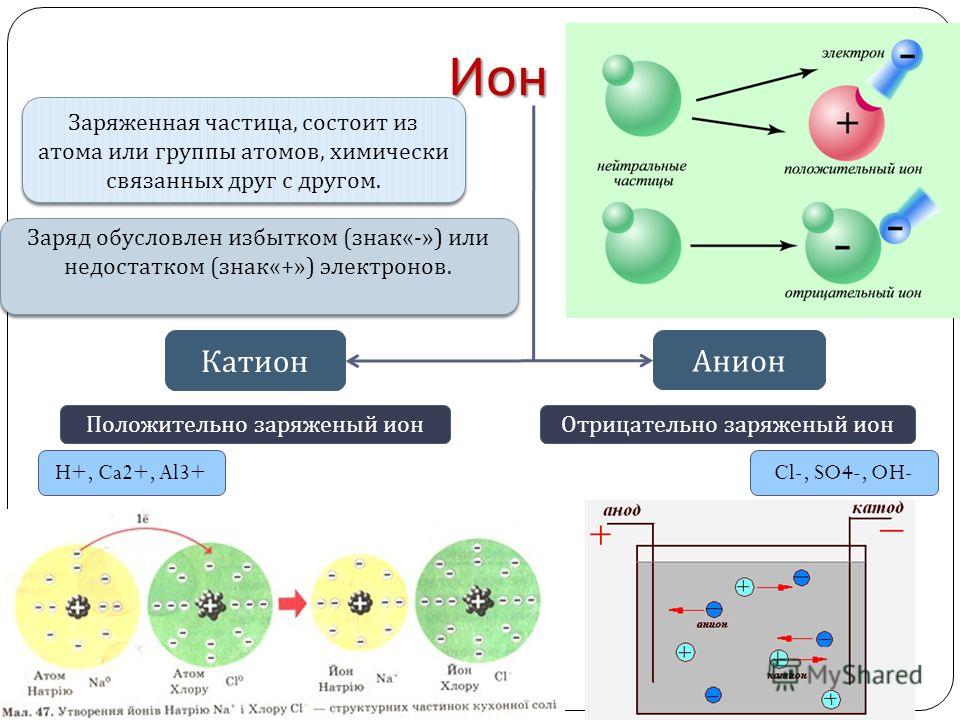
300 За счёт чего создаётся давление газа на дно и стенки сосуда?
Многочисленные удары молекул о стенки сосуда создают давление газа.
100 Почему сжать жидкость почти так же трудно, как и твёрдое тело?
Молекулы жидкости находятся непосредственно друг возле друга. При попытке сжать жидкость начинается деформация самих молекул
200 В каких агрегатных состояниях может находиться яблочный сок?
Во всех трёх: жидком, твёрдом, газообразном.
300 Как называется процесс перехода вещества из жидкого состояния в твёрдое?
Кристаллизация
100 Как называется процесс перехода вещества из твёрдого состояния в газообразное?
Сублимация
200 Велики или малы силы притяжения между молекулами в твёрдых телах?
Очень велики
300 Как движутся молекулы в твёрдых телах?
Колеблются около определённых положений равновесия
- Этап проверки полученных на уроке знаний. Тест.
Ответы к тестам
I вариант | II вариант | III вариант | IV вариант |
- Заключительный этап.
А теперь давайте подведем итоги нашей работы на сегодняшнем уроке. Что нового узнали на уроке? Какие оценки получили.
- Домашнее задание: § 61,62, ответить на вопросы после параграфа, заполнить таблицу. (Слайд 30)
Решать загадки можно вечно.
Вселенная ведь бесконечна.
Спасибо всем нам за урок,
А главное, чтоб был он впрок!
Тема: Три состояния вещества
I вариант
- Имеют определённый объём
- Занимают объём всего сосуда
- Принимают форму сосуда
- Мало сжимаются
- Легко поддаются сжатию
- Увеличится в 2 раза
- Уменьшится в 2 раза
- Не изменится
- Твёрдое тело
- Жидкость
- Такого тела нет
- Только в твёрдом состоянии
- Только в жидком состоянии
- Только в газообразном
- Во всех трёх состояниях
Тема: Три состояния вещества
II вариант
- Трудно сжимаются
- Легко сжимаются
- Не имеют собственной формы
- 3
3
.
 Изменится ли объём воды?
Изменится ли объём воды?
- Увеличится
- Уменьшится
- Не изменится
- Жидкость
- Твёрдое тело
- Таких тел нет
- Только в жидком состоянии
- Только в твёрдом состоянии
- Во всех трёх состояниях
Тема: Три состояния вещества
III вариант
- Трудно изменить форму
- Сохраняют постоянную форму
- Легко меняют форму
- Трудно сжимаются
- Увеличится в 2 раза
- Уменьшится в 2 раза
- Не изменится
- Жидкость
- Твёрдое тело
- Только в жидком
- Только в твёрдом
- Только в газообразном
- Во всех трёх состояниях
Тема: Три состояния вещества
IV вариант
- Имеют определённый объём
- Занимают объём всего сосуда
- Принимают форму сосуда
- Мало сжимаются
- Легко сжимаются
- Увеличится
- Уменьшится
- Не изменится
- Жидкость
- Твёрдое тело
- В каком состоянии может находиться спирт?
- Только в твёрдом состоянии
- Только в жидком состоянии
- Во всех трёх состояниях
Предварительный просмотр:
Тема: Три состояния вещества
I вариант
- Как расположены молекулы в твёрдых телах и как они движутся?
- Молекулы расположены на расстояниях меньших размеров самих молекул и перемещаются свободно относительно друг друга.

- Молекулы расположены на больших расстояниях друг от друга (по сравнению с размерами молекул) и движутся беспорядочно.
- Молекулы расположены в строгом порядке и колеблются около определённых положений равновесия.
- Какие из приведённых ниже свойств принадлежат газам?
- Имеют определённый объём
- Занимают объём всего сосуда
- Принимают форму сосуда
- Мало сжимаются
- Легко поддаются сжатию
- Изменится ли объём газа, если его перекачать из сосуда вместимостью 1 литр в сосуд вместимостью 2 литра?
- Увеличится в 2 раза
- Уменьшится в 2 раза
- Не изменится
- Молекулы расположены на больших расстояниях друг от друга (по отношению с размерами молекул), слабо взаимодействуют между собой, движутся хаотически. Какое это тело?
- Твёрдое тело
- Жидкость
- Такого тела нет
- В каком состоянии может находиться сталь?
- Только в твёрдом состоянии
- Только в жидком состоянии
- Только в газообразном
- Во всех трёх состояниях
Тема: Три состояния вещества
II вариант
- Как расположены молекулы жидкостей и как они движутся?
- Молекулы расположены на расстояниях, соизмеримых с размерами самих молекул, и перемещаются свободно относительно друг друга.

- Молекулы расположены на больших расстояниях (по сравнению с размерами молекул) друг от друга и движутся беспорядочно.
- Молекулы расположены в строгом порядке и колеблются около определённых положений равновесия.
- Какие из приведённых свойств принадлежат газам?
- Занимают весь предоставленный им объём
- Трудно сжимаются
- Имеют кристаллическое строение
- Легко сжимаются
- Не имеют собственной формы
- В мензурке находится вода объёмом 100 см 3 . Её переливают в стакан вместимостью 200 см 3 . Изменится ли объём воды?
- Увеличится
- Уменьшится
- Не изменится
- Молекулы плотно упакованы, сильно притягиваются друг к другу, каждая молекула колеблется около определённого положения. Какое это тело?
- Жидкость
- Твёрдое тело
- Таких тел нет
- В каком состоянии может находиться вода?
- Только в жидком состоянии
- Только в газообразном состоянии
- Только в твёрдом состоянии
- Во всех трёх состояниях
Тема: Три состояния вещества
III вариант
- Как расположены молекулы газов и как они движутся?
- Молекулы расположены на расстояниях, меньших размеров самих молекул, и перемещаются свободно относительно друг друга.
- Молекулы расположены на расстояниях, во много раз больше размеров самих молекул, и движутся беспорядочно.
- Молекулы расположены в строгом порядке и колеблются около определённых положений.
- Какие из приведённых свойств принадлежат твёрдым телам?
- Трудно изменить форму
- Занимают весь предоставленный им объём
- Сохраняют постоянную форму
- Легко меняют форму
- Трудно сжимаются
- Изменится ли объём газа, если его перекачать из баллона вместимостью 20 литров в баллон вместимость.40 литров?
- Увеличится в 2 раза
- Уменьшится в 2 раза
- Не изменится
- Есть ли такое вещество, у которого молекулы расположены на больших расстояниях, сильно притягиваются друг к другу и колеблются около определённых положений?
- Жидкость
- Твёрдое тело
- Такого вещества не существует
- В каком состоянии может находиться ртуть?
- Только в жидком
- Только в твёрдом
- Только в газообразном
- Во всех трёх состояниях
Тема: Три состояния вещества
IV вариант
- Ниже указано поведение молекул в твёрдых, жидких и газообразных телах.
 Что является общим для жидкостей и газов?
Что является общим для жидкостей и газов?
- То, что молекулы расположены на расстояниях меньших размеров самих молекул и движутся свободно относительно друг друга
- То, что молекулы расположены на больших расстояниях друг от друга и движутся беспорядочно
- То, что молекулы движутся беспорядочно друг относительно друга
- То, что молекулы расположены в строгом порядке и колеблются около определённых положений
- Какие из указанных свойств принадлежат твёрдым телам?
- Имеют определённый объём
- Занимают объём всего сосуда
- Принимают форму сосуда
- Мало сжимаются
- Легко сжимаются
- В бутылке находится вода объёмом 0,5 литра. Её переливают в колбу вместимостью 1 литр. Изменится ли объём воды?
- Увеличится
- Уменьшится
- Не изменится
- Молекулы расположены так, что расстояние между ними меньше размеров самих молекул. Они сильно притягиваются друг к другу и перемещаются с места на место.
 Какое это тело?
Какое это тело?II вариант
III вариант
IV вариант
Газообразное состояние — самое распространённое состояние вещества Вселенной (межзвёздное вещество, туманности, звёзды, атмосферы планет и т. д.). По химическим свойствам газы и их смеси весьма разнообразны — от малоактивных инертных газов до взрывчатых газовых смесей. К газам иногда] относят не только системы из атомов и молекул, но и системы из других частиц — фотонов, электронов, броуновских частиц, а также плазму
Газы могут неограниченно расширяться. Они не сохраняют не формы ни объёма Многочисленные удары молекул о стенки сосуда создают давление газа.
Жидкое состояние обычно считают промежуточным между твёрдым телом и газом: газ не сохраняет ни объём, ни форму, а твёрдое тело сохраняет и то, и другое. Форма жидких тел может полностью или отчасти определяться тем, что их поверхность ведёт себя как упругая мембрана.
 Так, вода может собираться в капли. Но жидкость способна течь даже под своей неподвижной поверхностью, и это тоже означает несохраненные формы (внутренних частей жидкого тела). Молекулы жидкости не имеют определённого положения, но в то же время им недоступна полная свобода перемещений. Между ними существует притяжение, достаточно сильное, чтобы удержать их на близком расстоянии. Вещество в жидком состоянии существует в определённом интервале температур, ниже которого переходит в твердое состояние (происходит кристаллизация либо превращение в твердотельное аморфное состояние — стекло), выше — в газообразное (происходит испарение). Границы этого интервала зависят от давления. Как правило, вещество в жидком состоянии имеет только одну модификацию. (Наиболее важные исключения — это квантовые жидкости и жидкие кристаллы.) Поэтому в большинстве случаев жидкость является не только агрегатным состоянием, но и термодинамической фазой (жидкая фаза). Все жидкости принято делить на чистые жидкости и смеси.
Так, вода может собираться в капли. Но жидкость способна течь даже под своей неподвижной поверхностью, и это тоже означает несохраненные формы (внутренних частей жидкого тела). Молекулы жидкости не имеют определённого положения, но в то же время им недоступна полная свобода перемещений. Между ними существует притяжение, достаточно сильное, чтобы удержать их на близком расстоянии. Вещество в жидком состоянии существует в определённом интервале температур, ниже которого переходит в твердое состояние (происходит кристаллизация либо превращение в твердотельное аморфное состояние — стекло), выше — в газообразное (происходит испарение). Границы этого интервала зависят от давления. Как правило, вещество в жидком состоянии имеет только одну модификацию. (Наиболее важные исключения — это квантовые жидкости и жидкие кристаллы.) Поэтому в большинстве случаев жидкость является не только агрегатным состоянием, но и термодинамической фазой (жидкая фаза). Все жидкости принято делить на чистые жидкости и смеси. Некоторые смеси жидкостей имеют большое значение для жизни: кровь, морская вода и др. Жидкости могут выполнять функцию растворителей.
Некоторые смеси жидкостей имеют большое значение для жизни: кровь, морская вода и др. Жидкости могут выполнять функцию растворителей.Образование свободной поверхности и поверхностное натяжение Из-за сохранения объёма жидкость способна образовывать свободную поверхность. Такая поверхность является поверхностью раздела фаз данного вещества: по одну сторону находится жидкая фаза, по другую — газообразная (пар), и, возможно, другие газы, например, воздух. Если жидкая и газообразная фазы одного и того же вещества соприкасаются, возникают силы, которые стремятся уменьшить площадь поверхности раздела — силы поверхностного натяжения. Поверхность раздела ведёт себя как упругая мембрана, которая стремится стянуться. Поверхностное натяжение может быть объяснено притяжением между молекулами жидкости. Каждая молекула притягивает другие молекулы, стремится «окружить» себя ими, а значит, уйти с поверхности. Соответственно, поверхность стремится уменьшиться. Поэтому мыльные пузыри и пузыри при кипении стремятся принять сферическую форму: при данном объёме минимальной поверхностью обладает шар.
 Если на жидкость действуют только силы поверхностного натяжения, она обязательно примет сферическую форму — например, капли воды в невесомости. Маленькие объекты с плотностью, большей плотности жидкости, способны «плавать» на поверхности жидкости, так как сила тяготения меньше силы, препятствующей увеличению площади поверхности.
Если на жидкость действуют только силы поверхностного натяжения, она обязательно примет сферическую форму — например, капли воды в невесомости. Маленькие объекты с плотностью, большей плотности жидкости, способны «плавать» на поверхности жидкости, так как сила тяготения меньше силы, препятствующей увеличению площади поверхности.Испарение — постепенный переход вещества из жидкости в газообразную фазу (пар). При тепловом движении некоторые молекулы покидают жидкость через её поверхность и переходят в пар. Вместе с тем, часть молекул переходит обратно из пара в жидкость. Если из жидкости уходит больше молекул , чем приходит, то имеет место испарение. Конденсация — обратный процесс, переход вещества из газообразного состояния в жидкое. При этом в жидкость переходит из пара больше молекул, чем в пар из жидкости. Кипение- процесс парообразования внутри жидкости. При достаточно высокой температуре давление пара становится выше давления внутри жидкости, и там начинают образовываться пузырьки пара, которые (в условиях земного притяжения) всплывают наверх.
 Смачивание — поверхностное явление, возникающее при контакте жидкости с твёрдой поверхностью в присутствии пара, то есть на границах раздела трёх фаз. Смешиваемость- способность жидкостей растворяться друг в друге. Пример смешиваемых жидкостей: вода и этиловый спирт, пример несмешиваемых: вода и жидкое масло. Переход жидкостей из одного состояния в другое
Смачивание — поверхностное явление, возникающее при контакте жидкости с твёрдой поверхностью в присутствии пара, то есть на границах раздела трёх фаз. Смешиваемость- способность жидкостей растворяться друг в друге. Пример смешиваемых жидкостей: вода и этиловый спирт, пример несмешиваемых: вода и жидкое масло. Переход жидкостей из одного состояния в другоеТвёрдые тела Твёрдое тело — это одно из четырёх агрегатных состояний вещества, отличающееся от других агрегатных состояний (жидкости, газов, плазмы) стабильностью формы и характером теплового движения атомов, совершающих малые колебания около положений равновесия.
МБОУ «Мужевская СОШ им. Н.В.Архангельского»
Конспект открытого урока
по теме:
Работу выполнил учитель физики
Лощаков Вячеслав Викторович
2014-2015 уч.год
Урок «Строение газообразных, жидких и твёрдых тел»
Цель урока: на основе МКТ объяснить особенности строения тел в различных состояниях, расширить кругозор учащихся по данному вопросу, показать неразрывную связь изучаемого материала с химией, математикой, способствовать развитию интереса к предмету, выработать внимание, трудолюбие, стремление к познанию окружающего мира.

Задачи урока:
Образовательные:
Способствовать овладению знаниями по теме “Строение газообразных, жидких и твёрдых тел”;
Установить характер зависимости сил притяжения и отталкивания от расстояния между молекулами;
Учиться решать качественные задачи.
Развивающие:
Развивать:
наблюдательность, самостоятельность;
логическое мышление
умение применять знания теории на практике;
содействовать развитию речи, мышления
Воспитательные:
Формирование представлений о единстве и взаимосвязи явлений природы.
Формировать положительное отношение к предмету
Тип урока: Урок изучения нового материала.
Форма урока: комбинированный
Оборудование и материалы: , компьютер, экран, мультимедийный проектор, демонстрационный материал: кусок льда, колбы различной формы с водой, эл.чайник с горячей водой, пластиковая бутылка с водой, колбы, различной формы, шприц, модели кристаллических решеток, различные материалы (сталь, чугун, медь, алюминий, пластмассы, смолы, подсолнечное масло и т.
 д.), воздушные шары, насос.
д.), воздушные шары, насос.Ход урока
Организационная часть .
Учитель: Здравствуйте. В 1836 году русский поэт Фёдор Иванович Тютчев написал такие проникновенные строки (Слайд 1)
Не то, что мните вы, природа:
Не слепок, не бездушный лик –
В ней есть душа, в ней есть свобода,
В ней есть любовь, в ней есть язык.2) Постановка целей и задач урока.
Атомы и молекулы могут располагаться в пространстве в самом причудливом порядке, составить различные вещества, которые под действием внешних условий (температуры, давления) могут находиться в различных агрегатных состояниях. (Слайд2)
Учитель: Кто назовет эти состояния?
Ответ: твердое, жидкое, газообразное.
Учитель: правильно, и есть еще одно, четвертое состояние вещества — плазма, но об этом мы поговорим на других уроках.
А сегодня мы рассмотрим строение газообразных, жидких и твердых тел. Откройте тетради и запишите тему урока:
“Строение газообразных, жидких и твёрдых тел”.
 (Слайд 3)
(Слайд 3) На партах у вас образец таблицы, перечертите её себе в тетрадь, мы заполним её в процессе урока. (Слайд 4)
состояние
вещества
расстояние
частицами
движение
взаимодействие
свойства
газообразное
В качестве примера, рассмотрим самое распространённое вещество на Земле – воду. (Слайд 5)
Какой формулой в химии обозначается вода?
Ученик: Н 2 О.
Учитель: правильно, Н 2 О – одного атома кислорода и двух атомов водорода.
Мы знаем, что вода бывает разная: твердая- лёд (демонстрирует кусок льда), жидкая- вода в стакане, газообразная – пар (наливает горячую воду из чайника).
(Слайд 5)
Отличаются ли молекулы льда и пара от молекулы воды?
Ученик: Нет.
Молекулы пара и льда также состоят из одного атома кислорода и двух атомов водорода.(Слайд 6)
Учитель: Зададимся вопросом: почему в одном случае вещество газообразное, в другом жидкое, а в третьем – твердое?
3) Этап объяснения нового материала
Найти ответ на этот вопрос позволяет молекулярно-кинетическая теория.

Вспомним основные положения МКТ, которые были впервые сформулированы великим русским ученым М.В.Ломоносовым.
Ученик :
все вещества состоят из частиц;
эти частицы беспорядочно движутся;
частицы взаимодействуют друг с другом.
Учитель:
Так как состав воды, льда и пара одинаков, то, очевидно, состояние вещества зависит от того, как частицы движутся и как взаимодействуют друг с другом..
Если в самых общих чертах представить себе строение газов, жидкостей и твердых тел, то можно нарисовать такую картину (демонстрирует таблицу с изображением молекул пара, воды, льда).
Учитель: Что можно сказать о взаимном расположении частиц в этих трех состояниях?
Ученик : *В газах частицы расположены далеко друг от друга, беспорядочно. *В жидкостях частицы расположены почти вплотную, порядка в расположении нет.
*В твердых телах молекулы расположены вплотную и в определенном порядке.
Учитель: Правильно.
 В газах расстояние между частицами в среднем во много раз превышает размеры самих частиц. Сжатие воздуха доказывает наличие больших расстояний между молекулами.
В газах расстояние между частицами в среднем во много раз превышает размеры самих частиц. Сжатие воздуха доказывает наличие больших расстояний между молекулами.Быстрое распространение запахов доказывает, что молекулы газов движутся с большими скоростями, беспорядочно. Частицы газа подобно бегунам — спринтерам, стремительно проносятся в пространстве
Частицы сталкиваются друг с другом и разлетаются в разные стороны подобно бильярдным шарам. Слабые силы притяжения в газах не способны удержать частицы друг около друга. Поэтому газы могут неограниченно расширяться.
Напоминаю, что движущееся тело обладает кинетической энергией «Е к ». Энергию взаимодействия называют потенциальной «Е п ».
Вывод: вещество находится в газообразном состоянии, если энергия движения во много раз больше энергии взаимодействия.
Учитель: заполнили в таблице, в 1 строку
Состояние
вещества
Строение
Движение
Взаимодействие
Свойства
газообразное
l>>r 0 .
беспорядочное
хаотическое,
Упругое столкновение,
F взаимодействия малы
Легко сжимаются.
Неограниченно расширяются.
Не сохраняют ни форму, ни объем
l ≈ r 0 .
Ближний порядок
Колебательное с перескоками,
Притяжение и отталкивание на расстоянии,
F взаимодействия достаточно велики
Плохо сжимаются Сохраняют объём
Текучи, легко меняют форму
l ≈ r 0
дальний порядок (кристаллическая решетка)
Колебательное около ОПР
Притяжение и отталкивание
F взаимодействия велики
Сохраняют объём и форму
Плохо сжимаются
Плохо растягиваются
Учитель: Записываем в тетрадь (СЛАЙД 7)
Легко сжимаются.
Могут неограниченно расширяться.
Не сохраняют ни форму, ни объём.
(Учащиеся выполняют запись в тетради.)
Учитель: переходим к жидкостям.

Ученик : *В жидкостях частицы расположены почти вплотную, порядка в расположении нет.
Учитель: Совершенно верно.
Молекулы жидкости находятся непосредственно друг возле друга . l ≈ r 0 . Этим и объясняется малая сжимаемость жидкостей. При попытке изменить объем жидкости (даже на малую величину) силы отталкивания становятся очень велики.
Зажатые, другими молекулами, они совершают как бы “бег на месте” (колеблются около положения равновесия, сталкиваясь с соседними молекулами). Лишь время от времени какая-нибудь молекула совершает “ прыжок”, но тут же попадает в новую «клетку», образованную новыми соседями. Нет свободного движения частиц- всегда есть взаимодействие сразу с несколькими ближайшими частицами. Потенциальная энергия взаимодействия больше кинетической энергии движения.
Характер молекулярного движения в жидкостях, впервые установленный советским физиком Яковым Ильичем Френкелем (портрет ученого на стр 158 учебника), позволяет понять основные свойства жидкостей.

Учитель: Записываем основные выводы по жидкостям (Слайд 9)
Сохраняют свой объём
Текучи, легко меняют форму
Принимают форму сосуда
Плохо сжимаются
Учитель: Твердые тела.
Ученик : *В твердых телах молекулы расположены вплотную и в определенном порядке.
Учитель: Да. l ≈ r 0 . Атомы или молекулы твердых тел в отличие от атомов или молекул жидкостей колеблются всегда около определенных положений равновесия. Это объясняется взаимодействием частиц. На каждую частицу действует большее число частиц, чем в случае с жидкостью, её положение более устойчиво, так как возникает дальний порядок. Если соединить эти положения, то получится пространственная решетка, её называют кристаллическая.
На стр. 159 учебника, рис. 8.9 и 8.10 изображены кристаллические решетки поваренной соли и алмаза. (Слайд 10)
Внутренний порядок в расположении атомов кристаллов приводит к правильным внешним геометрическим формам.
 Твердые тела сохраняют не только объем, но и форму.
Твердые тела сохраняют не только объем, но и форму.Существует притяжение и отталкивание частиц, потенциальная энергия взаимодействия частиц значительно больше их кинетической энергии (больше, чем у жидкостей).
Алмаз и графит — это атомы одного и того же элемента углерода, но расположенные в разном порядке и имеющие разные кристаллические решетки.
Алмаз — самый твердый среди минералов, это царь всех камней. Он крепче всех веществ на свете, это свет солнца, сгустившийся в земле и охлажденный временем. Он играет всеми цветами, но сам остаётся прозрачным, точно капля воды. Благодаря своей исключительной твердости алмаз играет громадную роль в технике. Алмазными пилами распиливают камни, алмазные буры используют при разведке недр. Через волочильные алмазы протягивают нити парашютной ткани, с помощью алмаза изготавливают тонкую проволоку твердых металлов.
Природный алмаз встречается редко, поэтому его получают искусственным путем.
Графит совершенно не похож на алмаз.
 Твердость графита
столь незначительна, что он легко оставляет след на бумаге. Из
него изготавливают стержни для карандашей.
Твердость графита
столь незначительна, что он легко оставляет след на бумаге. Из
него изготавливают стержни для карандашей.Разрабатывая проблему синтеза алмаза из графита исследователи обратили внимание на материал, очень схожий по структуре с графитом -нитрит бора,- и получили алмазоподобный материал борнитрит (боразон). Он оказался даже тверже алмаза и термически более стойким (алмаз сгорает при температуре 627°С, а боразон — при 2000 °С). Боразон нашел широкое применение в технике. Так наука привела к созданию нового материала.
Записываем в тетрадь:
(Слайд 11)
Учитель: пришло время ответить на поставленный в начале урока вопрос: от чего зависит, что одно и то же вещество может находиться в разных агрегатных состояниях?
Ответы учащихся: От расстояния между частицами, от сил взаимодействия, т.е от того, как расположены молекулы, как они движутся и как взаимодействуют друг с другом. (Слайд14)
4) Этап закрепления пройденного материала.
 Игра “Что за состояние?”
(СЛАЙДЫ 12-30)
Игра “Что за состояние?”
(СЛАЙДЫ 12-30)Оценку “5” получает учащийся, набравший наибольшее количество баллов.
Учитель выставляет оценки в журнал.
5) Домашнее задание: § 60, ответить на вопросы после параграфа (Слайд 32)
6) Заключение
Учитель : Решать загадки можно вечно.
Вселенная ведь бесконечна.
Спасибо всем нам за урок,
А главное, чтоб был он впрок!7) Подведение итогов урока.
Что нового узнали на уроке?
Ученик : Знание строения вещества необходимо для того, чтобы понимать все физические явления в природе.
Презентация на тему: Строение газообразных, жидких и твердых тел
№ слайда 1
Описание слайда:
№ слайда 2
Описание слайда:
№ слайда 3
Описание слайда:
Газы Газ (газообразное состояние) (от нидерл.
 gas) — агрегатное состояние вещества, характеризующееся очень слабыми связями между составляющими его частицами (молекулами, атомами или ионами), а также их большой подвижностью. Частицы газа почти свободно и хаотически движутся в промежутках между столкновениями, во время которых происходит резкое изменение характера их движения. Газообразное состояние вещества в условиях, когда возможно существование устойчивой жидкой или твёрдой фазы этого же вещества, обычно называется паром. Подобно жидкостям, газы обладают текучестью и сопротивляются деформации. В отличие от жидкостей, газы не имеют фиксированного объёма[и не образуют свободной поверхности, а стремятся заполнить весь доступный объём (например, сосуда).
gas) — агрегатное состояние вещества, характеризующееся очень слабыми связями между составляющими его частицами (молекулами, атомами или ионами), а также их большой подвижностью. Частицы газа почти свободно и хаотически движутся в промежутках между столкновениями, во время которых происходит резкое изменение характера их движения. Газообразное состояние вещества в условиях, когда возможно существование устойчивой жидкой или твёрдой фазы этого же вещества, обычно называется паром. Подобно жидкостям, газы обладают текучестью и сопротивляются деформации. В отличие от жидкостей, газы не имеют фиксированного объёма[и не образуют свободной поверхности, а стремятся заполнить весь доступный объём (например, сосуда).№ слайда 4
Описание слайда:
Газообразное состояние — самое распространённое состояние вещества Вселенной (межзвёздное вещество, туманности, звёзды, атмосферы планет и т. д.). По химическим свойствам газы и их смеси весьма разнообразны — от малоактивных инертных газов до взрывчатых газовых смесей.
 К газам иногда] относят не только системы из атомов и молекул, но и системы из других частиц — фотонов, электронов, броуновских частиц, а также плазму
К газам иногда] относят не только системы из атомов и молекул, но и системы из других частиц — фотонов, электронов, броуновских частиц, а также плазму№ слайда 5
Описание слайда:
№ слайда 6
Описание слайда:
Жидкость Жидкость — одно из агрегатных состояний вещества. Основным свойством жидкости, отличающим её от других агрегатных состояний, является способность неограниченно менять форму под действием касательных механических напряжений, даже сколь угодно малых, практически сохраняя при этом объём.
№ слайда 7
Описание слайда:
Жидкость – это физическое тело, обладающее двумя свойствами: Обладает текучестью, благодаря которой она не имеет формы и принимает форму того сосуда, в котором она находится. Она мало изменяет форму и объем при изменении давления и температуры, в чем она сходна с твердым телом.
№ слайда 8
Описание слайда:
Жидкое состояние обычно считают промежуточным между твёрдым телом и газом: газ не сохраняет ни объём, ни форму, а твёрдое тело сохраняет и то, и другое.
 Форма жидких тел может полностью или отчасти определяться тем, что их поверхность ведёт себя как упругая мембрана. Так, вода может собираться в капли. Но жидкость способна течь даже под своей неподвижной поверхностью, и это тоже означает несохраненные формы (внутренних частей жидкого тела). Молекулы жидкости не имеют определённого положения, но в то же время им недоступна полная свобода перемещений. Между ними существует притяжение, достаточно сильное, чтобы удержать их на близком расстоянии. Вещество в жидком состоянии существует в определённом интервале температур, ниже которого переходит в твердое состояние (происходит кристаллизация либо превращение в твердотельное аморфное состояние — стекло), выше — в газообразное (происходит испарение). Границы этого интервала зависят от давления. Как правило, вещество в жидком состоянии имеет только одну модификацию. (Наиболее важные исключения — это квантовые жидкости и жидкие кристаллы.) Поэтому в большинстве случаев жидкость является не только агрегатным состоянием, но и термодинамической фазой (жидкая фаза).
Форма жидких тел может полностью или отчасти определяться тем, что их поверхность ведёт себя как упругая мембрана. Так, вода может собираться в капли. Но жидкость способна течь даже под своей неподвижной поверхностью, и это тоже означает несохраненные формы (внутренних частей жидкого тела). Молекулы жидкости не имеют определённого положения, но в то же время им недоступна полная свобода перемещений. Между ними существует притяжение, достаточно сильное, чтобы удержать их на близком расстоянии. Вещество в жидком состоянии существует в определённом интервале температур, ниже которого переходит в твердое состояние (происходит кристаллизация либо превращение в твердотельное аморфное состояние — стекло), выше — в газообразное (происходит испарение). Границы этого интервала зависят от давления. Как правило, вещество в жидком состоянии имеет только одну модификацию. (Наиболее важные исключения — это квантовые жидкости и жидкие кристаллы.) Поэтому в большинстве случаев жидкость является не только агрегатным состоянием, но и термодинамической фазой (жидкая фаза). Все жидкости принято делить на чистые жидкости и смеси. Некоторые смеси жидкостей имеют большое значение для жизни: кровь, морская вода и др. Жидкости могут выполнять функцию растворителей.
Все жидкости принято делить на чистые жидкости и смеси. Некоторые смеси жидкостей имеют большое значение для жизни: кровь, морская вода и др. Жидкости могут выполнять функцию растворителей.№ слайда 9
Описание слайда:
Образование свободной поверхности и поверхностное натяжение Из-за сохранения объёма жидкость способна образовывать свободную поверхность. Такая поверхность является поверхностью раздела фаз данного вещества: по одну сторону находится жидкая фаза, по другую — газообразная (пар), и, возможно, другие газы, например, воздух. Если жидкая и газообразная фазы одного и того же вещества соприкасаются, возникают силы, которые стремятся уменьшить площадь поверхности раздела — силы поверхностного натяжения. Поверхность раздела ведёт себя как упругая мембрана, которая стремится стянуться. Поверхностное натяжение может быть объяснено притяжением между молекулами жидкости. Каждая молекула притягивает другие молекулы, стремится «окружить» себя ими, а значит, уйти с поверхности.
 Соответственно, поверхность стремится уменьшиться. Поэтому мыльные пузыри и пузыри при кипении стремятся принять сферическую форму: при данном объёме минимальной поверхностью обладает шар. Если на жидкость действуют только силы поверхностного натяжения, она обязательно примет сферическую форму — например, капли воды в невесомости. Маленькие объекты с плотностью, большей плотности жидкости, способны «плавать» на поверхности жидкости, так как сила тяготения меньше силы, препятствующей увеличению площади поверхности.
Соответственно, поверхность стремится уменьшиться. Поэтому мыльные пузыри и пузыри при кипении стремятся принять сферическую форму: при данном объёме минимальной поверхностью обладает шар. Если на жидкость действуют только силы поверхностного натяжения, она обязательно примет сферическую форму — например, капли воды в невесомости. Маленькие объекты с плотностью, большей плотности жидкости, способны «плавать» на поверхности жидкости, так как сила тяготения меньше силы, препятствующей увеличению площади поверхности.№ слайда 10
Описание слайда:
Переход жидкостей из одного состояния в другое Испарение — постепенный переход вещества из жидкости в газообразную фазу (пар). При тепловом движении некоторые молекулы покидают жидкость через её поверхность и переходят в пар. Вместе с тем, часть молекул переходит обратно из пара в жидкость. Если из жидкости уходит больше молекул, чем приходит, то имеет место испарение. Конденсация — обратный процесс, переход вещества из газообразного состояния в жидкое.
 При этом в жидкость переходит из пара больше молекул, чем в пар из жидкости. Кипение- процесс парообразования внутри жидкости. При достаточно высокой температуре давление пара становится выше давления внутри жидкости, и там начинают образовываться пузырьки пара, которые (в условиях земного притяжения) всплывают наверх. Смачивание — поверхностное явление, возникающее при контакте жидкости с твёрдой поверхностью в присутствии пара, то есть на границах раздела трёх фаз. Смешиваемость- способность жидкостей растворяться друг в друге. Пример смешиваемых жидкостей: вода и этиловый спирт, пример несмешиваемых: вода и жидкое масло.
При этом в жидкость переходит из пара больше молекул, чем в пар из жидкости. Кипение- процесс парообразования внутри жидкости. При достаточно высокой температуре давление пара становится выше давления внутри жидкости, и там начинают образовываться пузырьки пара, которые (в условиях земного притяжения) всплывают наверх. Смачивание — поверхностное явление, возникающее при контакте жидкости с твёрдой поверхностью в присутствии пара, то есть на границах раздела трёх фаз. Смешиваемость- способность жидкостей растворяться друг в друге. Пример смешиваемых жидкостей: вода и этиловый спирт, пример несмешиваемых: вода и жидкое масло.Молекулярно-кинетическая теория дает возможность понять, почему вещество может находитьсяв газообразном, жидком и твердом состояниях.Если в самых общих чертах попробовать представить себе строение…
Строение газов, жидкостей и твердых тел.
Основные положения молекулярно-кинетической теории :
все вещества состоят из молекул, а молекулы из атомов,
атомы и молекулы находятся в постоянном движении,
между молекулами существуют силы
притяжения и отталкивания.
В газах молекулы двигаются хаотически, расстояния между молекулами большие, молекулярные силы малы, газ занимает весь предоставленный ему объем.
В жидкостях молекулы располагаются упорядочно только на малых расстояниях, а на больших расстояниях порядок (симметрия) расположения нарушается – “ближний порядок”. Силы молекулярного притяжения удерживают молекулы на близком расстоянии. Движение молекул – “перескоки ” из одного устойчивого положения в другое (как правило, в пределах одного слоя. Таким движением объясняется текучесть жидкости. Жидкость не имеет форму, но имеет объем.
Твердые тела – вещества, которые
сохраняют форму, делятся на кристаллические
и аморфные. Кристаллические твердые тела имеют кристаллическую решетку, в
узлах которой могут находиться ионы,
молекулы или атомы Они совершают
колебания относительно устойчивых
положений равновесия.. Кристаллические
решетки имеют правильную структуру по
всему объему – “дальний порядок”
расположения.
Аморфные тела сохраняют форму, но не имеют кристаллической решетки и, как следствие, не имеют ярко выраженной температуры плавления. Их называют застывшими жидкостями, так как они, как жидкости имеют “ближний ” порядок расположения молекул.
Силы взаимодействия молекул
Все
молекулы вещества взаимодействуют
между собой силами притяжения и
отталкивания.
Доказательство
взаимодействия молекул: явление
смачивания, сопротивление сжатию и
растяжению, малая сжимаемость твердых
тел и газов и др.
Причина взаимодействия
молекул — это электромагнитные
взаимодействия заряженных частиц в
веществе.
Как
это объяснить?
Атом состоит из
положительно заряженного ядра и
отрицательно заряженной электронной
оболочки. Заряд ядра равен суммарному
заряду всех электронов, поэтому в целом
атом электрически нейтрален.
Молекула,
состоящая из одного или нескольких
атомов, тоже электрически
нейтральна.
Рассмотрим взаимодействие
между молекулами на примере двух
неподвижных молекул.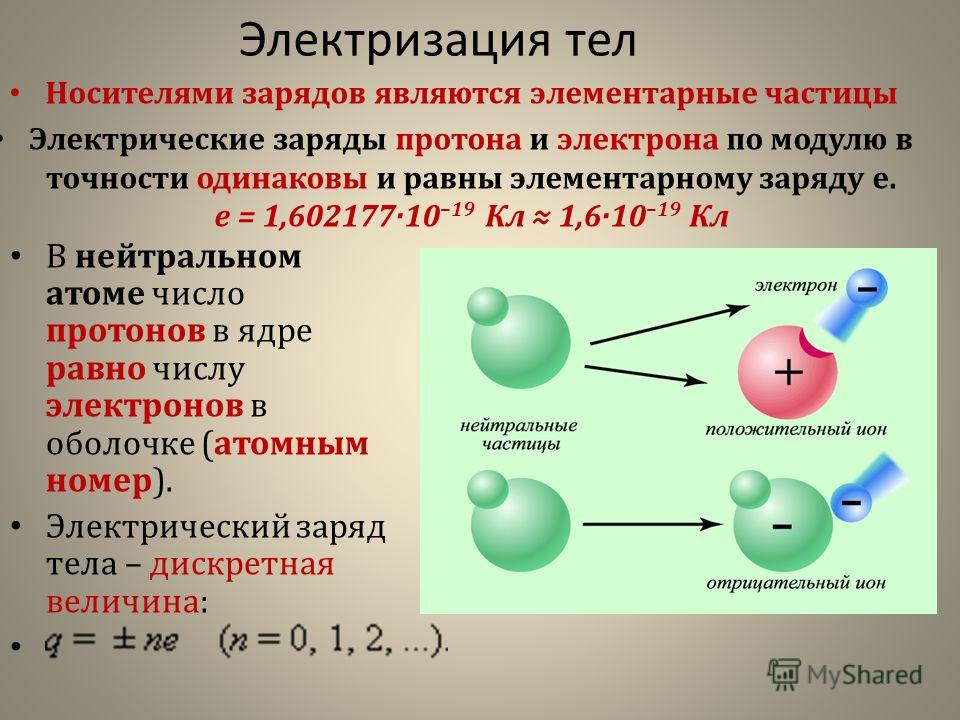 Между телами
в природе могут существовать гравитационные
и электромагнитные силы.
Так как массы
молекул крайне малы, ничтожно малые
силы гравитационного взаимодействия
между молекулами можно не рассматривать.
На
очень больших расстояниях электромагнитного
взаимодействия между молекулами тоже
нет.
Но, при уменьшении расстояния
между молекулами молекулы начинают
ориентироваться так, что их обращенные
друг к другу стороны будут иметь разные
по знаку заряды (в целом молекулы остаются
нейтральными), и между молекулами
возникают силы притяжения.
При еще
большем уменьшении расстояния между
молекулами возникают силы отталкивания,
как результат взаимодействия отрицательно
заряженных электронных оболочек атомов
молекул.
В итоге на молекулу действует
сумма сил притяжения и отталкивания.
На больших расстояниях преобладает
сила притяжения (на расстоянии 2-3
диаметров молекулы притяжение
максимально), на малых расстояниях сила
отталкивания.
Существует
такое расстояние между молекулами, на
котором силы притяжения становятся
равными силам отталкивания.
Между телами
в природе могут существовать гравитационные
и электромагнитные силы.
Так как массы
молекул крайне малы, ничтожно малые
силы гравитационного взаимодействия
между молекулами можно не рассматривать.
На
очень больших расстояниях электромагнитного
взаимодействия между молекулами тоже
нет.
Но, при уменьшении расстояния
между молекулами молекулы начинают
ориентироваться так, что их обращенные
друг к другу стороны будут иметь разные
по знаку заряды (в целом молекулы остаются
нейтральными), и между молекулами
возникают силы притяжения.
При еще
большем уменьшении расстояния между
молекулами возникают силы отталкивания,
как результат взаимодействия отрицательно
заряженных электронных оболочек атомов
молекул.
В итоге на молекулу действует
сумма сил притяжения и отталкивания.
На больших расстояниях преобладает
сила притяжения (на расстоянии 2-3
диаметров молекулы притяжение
максимально), на малых расстояниях сила
отталкивания.
Существует
такое расстояние между молекулами, на
котором силы притяжения становятся
равными силам отталкивания. Такое
положение молекул называется положением
устойчивого равновесия.
Находящиеся
на расстоянии друг от друга и связанные
электромагнитными силами молекулы
обладают потенциальной энергией. В
положении устойчивого равновесия
потенциальная энергия молекул
минимальна.
В веществе каждая
молекула взаимодействует одновременно
со многими соседними молекулами, что
также влияет на величину минимальной
потенциальной энергии молекул.
Кроме
того, все молекулы вещества находятся
в непрерывном движении, т.е. обладают
кинетической энергией.
Таким образом,
структура вещества и его свойства
(твердых, жидких и газообразных тел)
определяются соотношением между
минимальной потенциальной энергией
взаимодействия молекул и запасом
кинетической энергии теплового движения
молекул.
Такое
положение молекул называется положением
устойчивого равновесия.
Находящиеся
на расстоянии друг от друга и связанные
электромагнитными силами молекулы
обладают потенциальной энергией. В
положении устойчивого равновесия
потенциальная энергия молекул
минимальна.
В веществе каждая
молекула взаимодействует одновременно
со многими соседними молекулами, что
также влияет на величину минимальной
потенциальной энергии молекул.
Кроме
того, все молекулы вещества находятся
в непрерывном движении, т.е. обладают
кинетической энергией.
Таким образом,
структура вещества и его свойства
(твердых, жидких и газообразных тел)
определяются соотношением между
минимальной потенциальной энергией
взаимодействия молекул и запасом
кинетической энергии теплового движения
молекул.
Строение и свойства твердых, жидких и газообразных тел
Строение тел объясняется взаимодействием частиц тела и характером их теплового движения.
Твердое тело
Твердые
тела имеют постоянную форму и объем,
практически несжимаемы.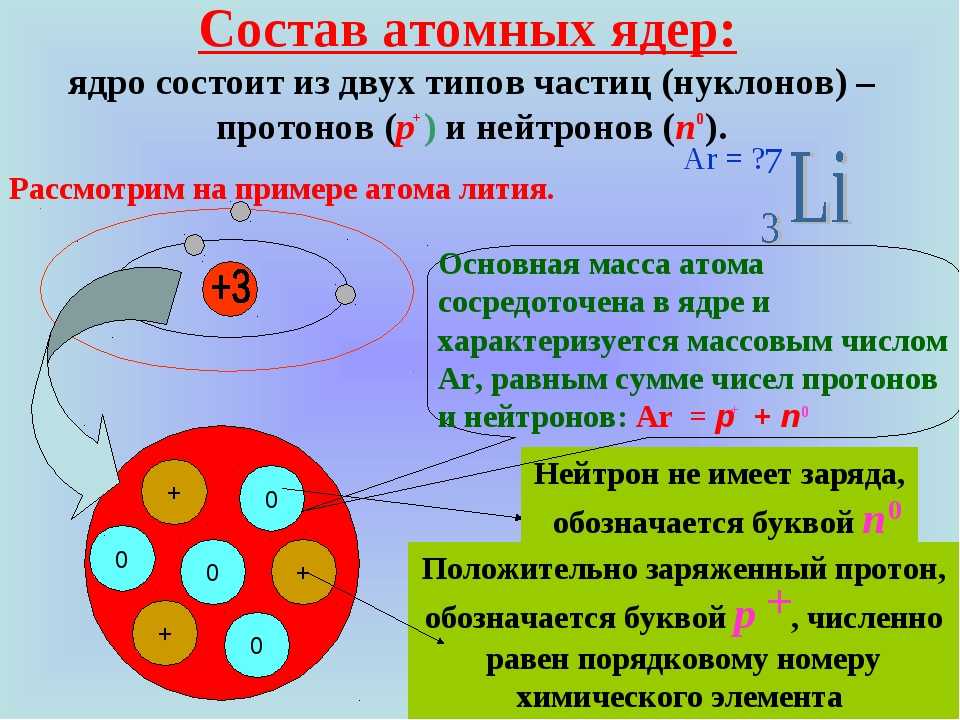 Минимальная
потенциальная энергия взаимодействия
молекул больше кинетической энергии
молекул.
Сильное взаимодействие
частиц.
Тепловое
движение молекул в твердом теле выражается
только лишь колебаниями частиц (атомов,
молекул) около положения устойчивого
равновесия.
Минимальная
потенциальная энергия взаимодействия
молекул больше кинетической энергии
молекул.
Сильное взаимодействие
частиц.
Тепловое
движение молекул в твердом теле выражается
только лишь колебаниями частиц (атомов,
молекул) около положения устойчивого
равновесия.
Из-за больших сил притяжения молекулы практически не могут менять свое положение в веществе, этим и объясняется неизменность объема и формы твердых тел. Большинство твердых тел имеет упорядоченное в пространстве расположение частиц, которые образуют правильную кристаллическую решетку. Частицы вещества (атомы, молекулы, ионы) расположены в вершинах — узлах кристаллической решетки. Узлы кристаллической решетки совпадают с положением устойчивого равновесия частиц. Такие твердые тела называются кристаллическими.
Жидкость
Жидкости
имеют определенный объем, но не имеют
своей формы, они принимают форму сосуда,
в которой находятся.
Минимальная
потенциальная энергия взаимодействия
молекул сравнима с кинетической энергией
молекул.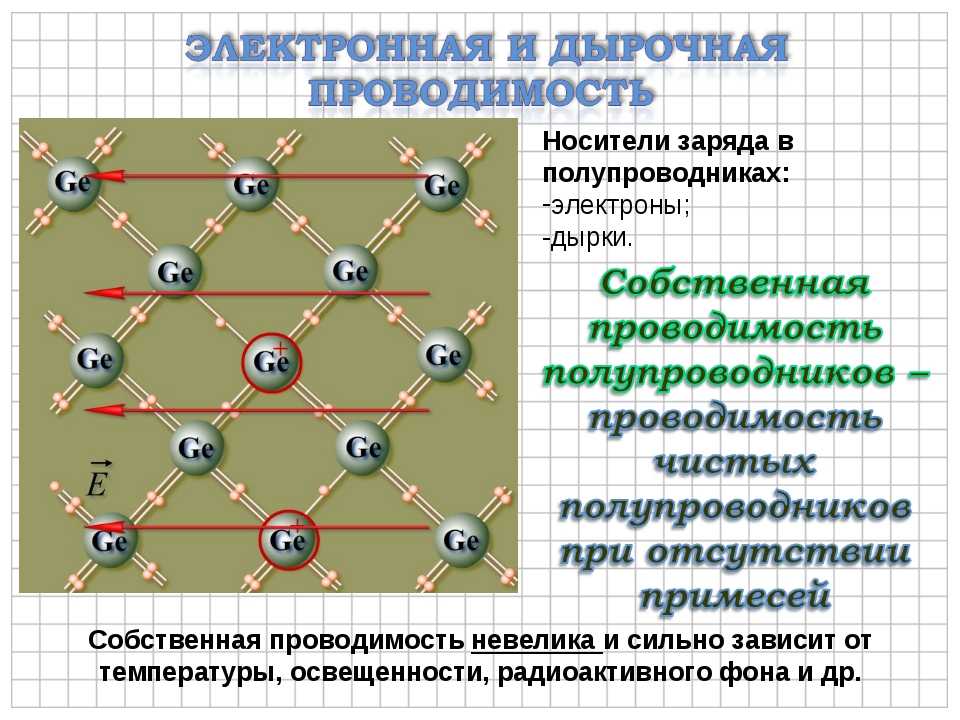 Слабое взаимодействие
частиц.
Тепловое
движение молекул в жидкости выражено
колебаниями около положения устойчивого
равновесия внутри объема, предоставленного
молекуле ее соседями.
Молекулы
не могут свободно перемещаться по всему
объему вещества, но возможны переходы
молекул на соседние места. Этим объясняется
текучесть жидкости, способность менять
свою форму.
Слабое взаимодействие
частиц.
Тепловое
движение молекул в жидкости выражено
колебаниями около положения устойчивого
равновесия внутри объема, предоставленного
молекуле ее соседями.
Молекулы
не могут свободно перемещаться по всему
объему вещества, но возможны переходы
молекул на соседние места. Этим объясняется
текучесть жидкости, способность менять
свою форму.
В
жидкостях молекулы достаточно прочно
связаны друг с другом силами притяжения,
что объясняет неизменность объема
жидкости.
В жидкости расстояние
между молекулами равно приблизительно
диаметру молекулы. При уменьшении
расстояния между молекулами (сжимании
жидкости) резко увеличиваются силы
отталкивания, поэтому жидкости
несжимаемы.
По
своему строению и характеру теплового
движения жидкости занимают промежуточное
положение между твердыми телами и
газами.
Хотя разница между жидкостью
и газом значительно больше, чем между
жидкостью и твердым телом. Например,
при плавлении или кристаллизации объем
тела изменяется во много раз меньше,
чем при испарении или конденсации.
Газы не имеют постоянного объема и занимают весь объем сосуда, в котором они находятся. Минимальная потенциальная энергия взаимодействия молекул меньше кинетической энергии молекул. Частицы вещества практически не взаимодействуют. Газы характеризуются полной беспорядочностью расположения и движения молекул.
Расстояние между молекулами газа во много раз больше размеров молекул. Малые силы притяжения не могут удержать молекулы друг около друга, поэтому газы могут неограниченно расширяться. Газы легко сжимаются под действием внешнего давления, т.к. расстояния между молекулами велики, а силы взаимодействия пренебрежимо малы. Давление газа на стенки сосуда создается ударами движущихся молекул газа.
Цель урока: Рассмотреть особенности строения и свойства газообразных, жидких и твёрдых тел с точки зрения молекулярно – кинетической теории.
Задачи урока:
- Образовательные
- Способствовать овладению знаниями по теме “Строение газообразных, жидких и твёрдых тел”;
- Установить характер зависимости сил притяжения и отталкивания от расстояния между молекулами;
- Учиться решать качественные задачи.
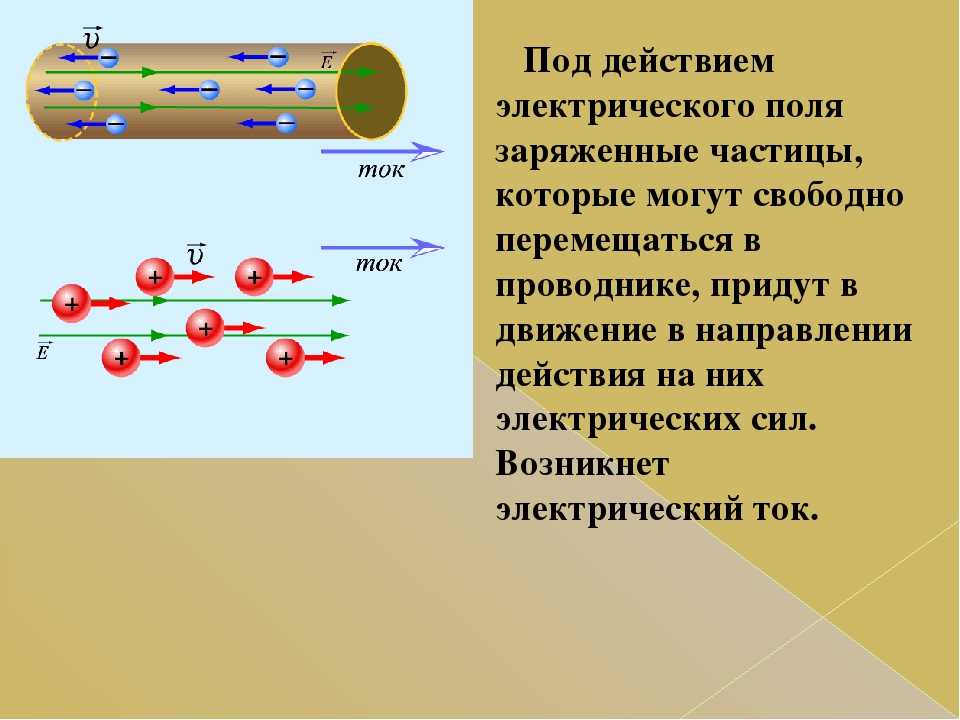
- Развивающие
Развивать:
- наблюдательность, самостоятельность;
- логическое мышление
- умение применять знания теории на практике;
- содействовать развитию речи, мышления
- Воспитательные:
- Формирование представлений о единстве и взаимосвязи явлений природы.
- Формировать положительное отношение к предмету
Тип урока: Урок изучения нового материала.
Форма урока: комбинированный
Комплексно-методическое обеспечение: Компьютер, экран, мультимедийный проектор, авторская презентация , образцы кристаллов, тестовые задания.
Межпредметные связи:
- химия
- информатика
- Организационный этап
Учитель: Здравствуйте. Ещё Наполеон I
говорил: “Воображение правит миром”. А Демокрит
утверждал, что “Ничего не существует кроме
атомов”.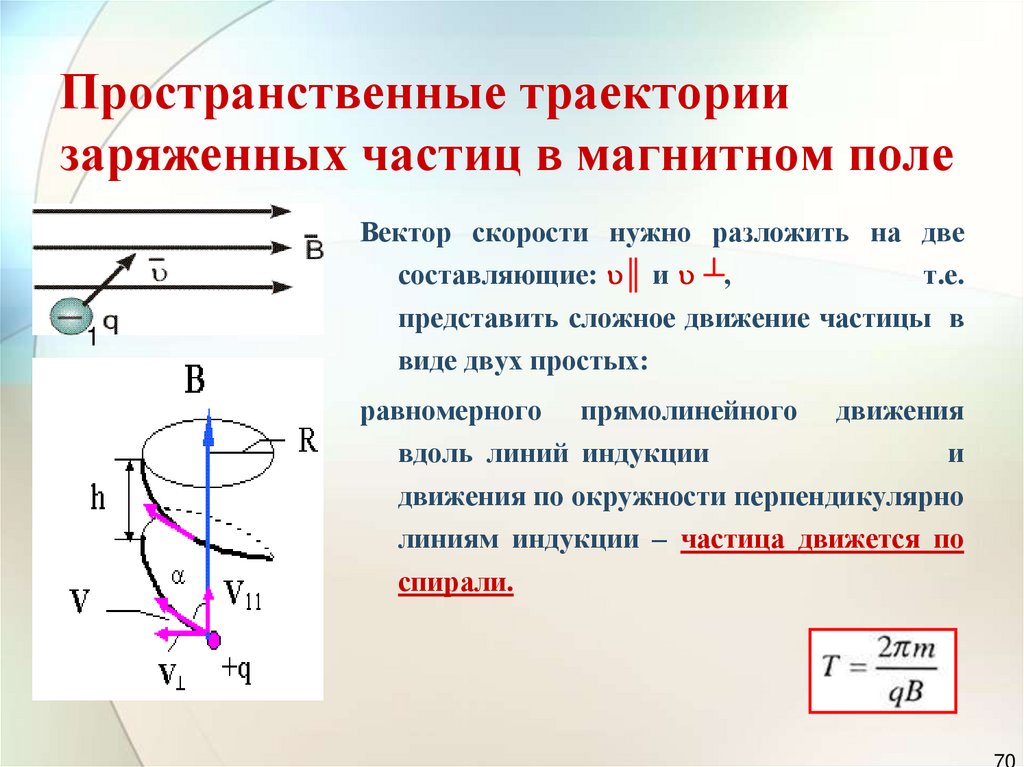
- Этап постановки целей и задач урока.
Согласитесь! Мир удивителен и многообразен. Человек издавна пытался объяснить необъяснимое, увидеть невидимое, услышать неслышимое. Оглядываясь вокруг себя, он размышлял о природе и пытался решить загадки, которые она перед ним ставила.
Русский поэт Фёдор Иванович Тютчев писал.
Не то, что мните вы, природа:
Не слепок, не бездушный лик –
В ней есть душа, в ней есть свобода,
В ней есть любовь, в ней есть язык.
Но со временем человек стал понимать, что именно закон стоит во главе всего, что нас окружает.
Вы, конечно же, ежедневно сталкиваетесь с различными физическими явлениями, которыми управляет закон, и в большинстве случаев можете предсказать, как они закончатся. Например, предскажите, чем закончатся следующие события:
- Если открыть флакон с духами, то …;
- Если нагреть лед, то …;
- Если сильно сжать два кусочка пластилина, то …;
- Если капнуть каплю масла на воду, то …;
- Если опустить термометр в горячую воду, то …
Учитель: Итак, давая свои ответы, вы
руководствовались определенными знаниями,
полученными ранее. Мы с вами каждый день
наблюдаем целый ряд окружающих нас предметов:
столы, стулья, книги, ручки, тетради, автомобили и
т.д. Скажите, они нам только кажутся сплошными или
они на самом деле являются таковыми?
Мы с вами каждый день
наблюдаем целый ряд окружающих нас предметов:
столы, стулья, книги, ручки, тетради, автомобили и
т.д. Скажите, они нам только кажутся сплошными или
они на самом деле являются таковыми?
Ученик: Только кажутся.
Учитель: Тогда скажите, из чего состоят все вещества?
Ученик: Из молекул или атомов
Учитель: А, как вы думаете, молекулы различных веществ одинаковы или нет? Докажите.
Ученик: Нет. Они имеют разные химические соединения.
Учитель: Лед, вода и водяной пар состоят из одних и тех же молекул или нет?
Ученик: Да.
Учитель: Почему?
Ученик: Потому что это одно и то же вещество, но в разном виде
Учитель: Вот, ребята, мы и подошли к теме нашего урока. Откройте рабочие тетради, запишите дату и тему нашего урока: “Строение газообразных, жидких и твёрдых тел”.
(Слайд 2).
В мире нет двух совершенно одинаковых
предметов. Невозможно найти две одинаковые
песчинки в горе песка или два одинаковых листика
на дереве, а вот молекулы одного и того же
вещества совершенно одинаковы. Например, воду мы
привыкли видеть в жидком состоянии. Химическая
формула воды H 2 O. В газообразном состоянии –
это пары воды. (Какова химическая формула?). В
твёрдом состоянии, это лёд или снег. Всё та же
химическая формула — H 2 O.
Невозможно найти две одинаковые
песчинки в горе песка или два одинаковых листика
на дереве, а вот молекулы одного и того же
вещества совершенно одинаковы. Например, воду мы
привыкли видеть в жидком состоянии. Химическая
формула воды H 2 O. В газообразном состоянии –
это пары воды. (Какова химическая формула?). В
твёрдом состоянии, это лёд или снег. Всё та же
химическая формула — H 2 O.
Тогда возникает вопрос: если молекулы одного и того же вещества совершенно одинаковы, то почему это вещество может находиться в разных агрегатных состояниях?
Вот на этот вопрос нам с вами и предстоит ответить сегодня на уроке. (Слайд 3)
Различают четыре агрегатных состояния вещества:
- Твёрдое
- Жидкое
- Газообразное
- Плазменное
Сегодня мы поговорим о трёх из них. Прежде познакомимся с понятием – фазовый переход. (Слайд 4)
Фазовый переход – переход системы из одного агрегатного состояния в другое. При фазовом переходе скачкообразно изменяется какая-либо физическая величина (плотность, внутренняя энергия)
Реализация агрегатного состояния вещества
зависит от соотношения кинетической и
потенциальной энергии молекул, входящих в его
состав.
- Этап объяснения нового материала
Перед вами на столах лежат опорные конспекты. (Приложение 3) . Что символизирует каждый рисунок? (Разные агрегатные состояния)
Облачко – газообразное состояние вещества, бутылка – жидкое, кубик – твёрдое состояние. Поэтапно разберём строение газообразных, жидких и твёрдых тел. Выводы запишем в тетрадях.
- ГАЗЫ (Слайд 6, 10)
Расстояние между атомами или молекулами в газах в среднем во много раз больше размеров самих молекул. Газы легко сжимаются, при этом уменьшается среднее расстояние между молекулами, но молекулы не сдавливают друг друга. Молекулы движутся с огромными скоростями — сотни метров в секунду. Сталкиваясь, они отскакивают друг от друга в разные стороны. Слабые силы притяжения молекул газа не способны удержать их друг возле друга. Поэтому газы могут неограниченно расширяться. Они не сохраняют ни формы, ни объема.
Многочисленные удары молекул о стенки сосуда
создают давление газа.
- ЖИДКОСТИ (Слайд 11, 14)
Молекулы жидкости расположены почти вплотную друг к другу, поэтому молекула жидкости ведет себя иначе, чем молекула газа. Зажатая, как в “клетке”, другими молекулами, она совершает “бег на месте” (колеблется около положения равновесия, сталкиваясь с соседними молекулами). Лишь время от времени она совершает “ прыжок”, прорываясь сквозь “прутья клетки”, но тут же попадает в новую клетку, образованную новыми соседями. Время оседлой жизни молекулы воды, т. е. время колебаний около одного определенного положения равновесия при комнатной температуре, равно в среднем 10 -11 с. Время же одного колебания значительно меньше (10 -12 -10 -13 с). С повышением температуры время оседлой жизни молекул уменьшается.
Молекулы жидкости находятся непосредственно
друг возле друга. При попытке изменить объем
жидкости (даже на малую величину) начинается
деформация самих молекул, для этого нужны очень
большие силы. Этим и объясняется малая
сжимаемость жидкостей.
Как известно, жидкости текучи, т. е. не сохраняют своей формы, они принимают форму сосуда.
Характер молекулярного движения в жидкостях, впервые установленный советским физиком Я. И. Френкелем, позволяет понять основные свойства жидкостей. (Приложение 5)
- ТВЁРДЫЕ ТЕЛА. (Слайд 15)
Атомы или молекулы твердых тел в отличие от атомов и молекул жидкостей колеблются около определенных положений равновесия. Правда, иногда молекулы меняют положение равновесия, но происходит это редко. Вот почему твердые тела сохраняют не только объем, но и форму.
Есть еще одно важное различие между жидкостями и твердыми телами.
Жидкость можно сравнить с толпой людей, где
отдельные индивидуумы беспокойно толкутся на
месте, а твердое тело подобно стройной когорте
тех же индивидуумов, которые хотя и не стоят по
стойке смирно, но выдерживают между собой в
среднем определенные интервалы. Если соединить
центры положений равновесия атомов или ионов
твердого тела, то получится правильная
пространственная решетка, называемая
кристаллической.
На рисунках изображены кристаллические решетки поваренной соли и алмаза. Внутренний порядок в расположении атомов кристаллов приводит к правильным внешним геометрическим формам.
Итак, пришло время ответить на поставленный в начале урока вопрос: от чего зависит, что одно и то же вещество может находиться в разных агрегатных состояниях?
Ответы учащихся: От расстояния между частицами, от сил взаимодействия, т.е от того, как расположены молекулы, как они движутся и как взаимодействуют друг с другом.
- Этап закрепления пройденного материала. Игра “Что за состояние?”
Оценку “5” получает учащийся, набравший наибольшее количество баллов.
- Этап проверки полученных на уроке знаний. Тест. (Приложение 4)
- Заключительный этап.
А теперь давайте подведем итоги нашей работы на сегодняшнем уроке. Что нового узнали на уроке? Какие оценки получили.
- Домашнее задание: § 62, ответить на
вопросы после параграфа, заполнить таблицу.
 (Слайд
38)
(Слайд
38)
Учитель:
Решать загадки можно вечно.
Вселенная ведь бесконечна.
Спасибо всем нам за урок,
А главное, чтоб был он впрок!
Литература:
- Г.В. Маркина, издательство Учитель” г. Волгоград, 97
- В.А. Волков, Москва “Вако” , 2006 В помощь школьному учителю
- Интернет-ресурсы
- Г.Я. Мякишев, физика, Москва -2007.
- CD “ Электронные уроки и тесты”
Почему извергается вулкан?
igor100 03.02.2007 20:40 Ответить
А ЕСЛИ В ЖЕРЛЕ ВУЛКАНА БУРИТЬ СКВАЖИНУ И ДАТЬ ВОЗМОЖНОСТЬ ГАЗУ ВЫХОДИТЬ ПОСТЕПЕННО, ТО «ПРОБКУ НЕ ВЫРВЕТ»! ХОТЯ ВОЗМОЖНО «ОСЕДАНИЕ» ВСЕЙ ЗОНЫ ВУЛКАНА.
Ответить
barjer 03.02.2007 21:25 Ответить
Позволю себе высказать несколько отличную версию событий при вулканических извержениях.
 Конечно, то что твердая кора литосферы лежит на жидкой магме, абсолютно верно. Но вот причина извержения скорее всего состоит в ином. Известно, что температура магмы порядка 1000 град С. Температура поверхности Земли не превышает 50 град С. Налицо температурный градиент, что приводит к тепловому потоку от горячей магмы к холодной поверхности. А это неизбежно вызывает охлаждение верхних слоев магмы и ее оседание: известно, что ВСЕ ТЕЛА ПРИ ОХЛАЖДЕНИИ СЖИМАЮТСЯ! При этом магма, на которой «лежит» кора, уходит из-под коры. В центре литосферных плит это не приводит к сколь-нибудь серьезным последствиям. Кора просто оседает вся целиком. А вот в рифтовых зонах, т.е. в местах соприкосновения литосферных плит сплошность коры нарушена. Более того, в этих зонах в коре наблюдаются разрывы и полости. Не исключено, что отдельные огромные фрагменты коры зависают над оседающей в результате охлаждения магмой. Когда прочность этого фрагмента становится недостаточной для его удержания, он оседает, оказывая давление на магму, и выдавливая ее на поверхность через наименее прочные участки коры, как правило, через жерла вулканов.
Конечно, то что твердая кора литосферы лежит на жидкой магме, абсолютно верно. Но вот причина извержения скорее всего состоит в ином. Известно, что температура магмы порядка 1000 град С. Температура поверхности Земли не превышает 50 град С. Налицо температурный градиент, что приводит к тепловому потоку от горячей магмы к холодной поверхности. А это неизбежно вызывает охлаждение верхних слоев магмы и ее оседание: известно, что ВСЕ ТЕЛА ПРИ ОХЛАЖДЕНИИ СЖИМАЮТСЯ! При этом магма, на которой «лежит» кора, уходит из-под коры. В центре литосферных плит это не приводит к сколь-нибудь серьезным последствиям. Кора просто оседает вся целиком. А вот в рифтовых зонах, т.е. в местах соприкосновения литосферных плит сплошность коры нарушена. Более того, в этих зонах в коре наблюдаются разрывы и полости. Не исключено, что отдельные огромные фрагменты коры зависают над оседающей в результате охлаждения магмой. Когда прочность этого фрагмента становится недостаточной для его удержания, он оседает, оказывая давление на магму, и выдавливая ее на поверхность через наименее прочные участки коры, как правило, через жерла вулканов.
Кстати, если фрагмент коры достаточно долго «висит» над магмой, но все же в конце концов, происходит его обрушение в магму, что прождает волны в магме. При этом земная кора «качается» на этих волнах. Так происходят землетрясения. Спасибо за внимание. barjerОтветить
mihan41 barjer 01.10.2007 22:15 Ответить
Уважаемый Barjer. Ваш сценарий развития вулкана вполне реалистичен. Тем не менее приведу для рассмотрения и другой причинно-следственный ряд возможных событий.
Согласно космогеодинамической теории Исаева С. М. движение твердо-коровой составляющей литосферы происходит преривисто, в то время как пластичная составляющая непрерывно движется по близ меридианальным направлениям в экваториальную область с обоих полушарий.В то же время эта движущаяся пластичная астеносфера является в подобие резиновой прокладки и не пропускает через себя жидкую магму к проницаемой из-за хрупкости твердой коре. Учитывая неоднородность Земной коры, пульсационный режим тангенциальных и приливных сил, расширение и сужение оледенений мы можем предпологать наличие участков нарушения сплошности астеносферного слоя и наличие так называемой «аномальной мантии» которая проникает сквозь твердую кору в наружу в виде вулкано-магматического проявления. Замете, автор при этом указывает в качестве движущей силы новую открытую им теоретически тангенциальную силу гравитационной природы. Автор также указывает на наличие под астеносферой потока легких веществ сепараторно возгоняемых в полюсовые области Земли. И благодаря последнему мы часто имеем магматизм аномально кислого состава в геосинклинальных областях, сравнительно быстрое востановление постледниковых малых депресий в сравнении с общей реологической их релаксацией.
Учитывая неоднородность Земной коры, пульсационный режим тангенциальных и приливных сил, расширение и сужение оледенений мы можем предпологать наличие участков нарушения сплошности астеносферного слоя и наличие так называемой «аномальной мантии» которая проникает сквозь твердую кору в наружу в виде вулкано-магматического проявления. Замете, автор при этом указывает в качестве движущей силы новую открытую им теоретически тангенциальную силу гравитационной природы. Автор также указывает на наличие под астеносферой потока легких веществ сепараторно возгоняемых в полюсовые области Земли. И благодаря последнему мы часто имеем магматизм аномально кислого состава в геосинклинальных областях, сравнительно быстрое востановление постледниковых малых депресий в сравнении с общей реологической их релаксацией.Ответить
PavelS 23.02.2007 23:17 Ответить
Всё здорово, но я не понимаю откуда берётся магма Гавайских островов. Там всюду океан и никаких разломов.
Там всюду океан и никаких разломов.
Ответить
barjer 07.03.2007 19:02 Ответить
Уважаемый PavelS! Неужели Вы думаете, что под океанской корой нет магмы? Кстати, кора под океаном значительно тоньше, нежели под материками: 7-6 км против 40-80. Подводные извержения вулканов хорошо известны. Иногда они же сопровождаются обрушением фрагментов коры, что порождает цунами — одиночные или двойные, тройные волны, обрушивающиеся на материки То, что подводные извержения более редкие, говорит лишь о том, что под слоем воды, являющейся хорошим изолятором, охлаждение магмы происходит медленнее. Поэтому и ее осаждение более редкое событие. Впрочем, подводные извержения, как таковые, далеко не редкость. Реже подводные землетрясения, по-видимому, потому что кора менее прочная и чаще происходт именно ее оседание, а не обрушение.
С уважением barjer
Ответить
Etwas
18. 03.2007 00:20
Ответить
03.2007 00:20
Ответить
У Земли твёрдое ядро? На мой взгляд это либо очень странное заявление, либо я знаю гораздо меньше, чем мне до сих пор казалось.
Если ядро твёрдое, то каким образом Земля обладает магнитным полем?
Ответить
barjer Etwas 19.03.2007 18:54 Ответить
Etwas Вы правы. Ядро у Земли не твердое, хотя точно сказать не берусь. Дело в том, что внутри Земли огромное давление. По гидростатической теории давление в слое вещества пропорционально плотности и глубине. Если средняя плотность Земли где-то 5,5 т в м куб, а радиус 6350 км, давление в центре Земли должно быть порядка 3,5 миллионов атмосфер. Каким выглядит вещество при таком давлении, сказать трудно. В лабораторных условиях получают такие давления, но кратковременно, взрывом.
А магнитное поле Земли по современным представлениям возникает из-за вращения слоев мантии под действием кориолисовой силы, которая неизбежно возникает при сложении вращательного и поступательного движений или двух вращательных.

Ответить
Etwas barjer 23.03.2007 18:29 Ответить
Этого — о связи мантии с магнитным полем Земли — я не знал…
Ответить
Сергей Заикин barjer 12.04.2007 19:47 Ответить
Расскажите, пожалуйста, о природе (возникновении) магнитного поля Земли поподробнее.
Ответить
mihan40 barjer 30.09.2007 22:29 Ответить
Barjer Вы не совсем правы. В центре Земли гравитационный потенциал равна нулю и Ваша гидростатическая теория давления здесь абсолютно не пригодна. Это означает, что туда должны всплывать продукты дегазации в ходе процесса гравитационной дифференциации. Такая же дегазация идет из Земли в атмосферу и где гелий и водород не удерживаются в отличии от того же центра Земли.
 Очень вероятно, что ядро Земли состоит из гелия и водорода. При этом надо еще учесть. что Земля не примитивный шар, а является фигурой вращения. Только тогда мы поймем, что легкими газами центр Земли механически накачивается и давление ядра на внешние сферы имеет природу парциального давления и вполне возможно, чо величина его достаточная чтобы гелий и водород становились жидкими.
Очень вероятно, что ядро Земли состоит из гелия и водорода. При этом надо еще учесть. что Земля не примитивный шар, а является фигурой вращения. Только тогда мы поймем, что легкими газами центр Земли механически накачивается и давление ядра на внешние сферы имеет природу парциального давления и вполне возможно, чо величина его достаточная чтобы гелий и водород становились жидкими.Ответить
Сергей Заикин mihan40 03.10.2007 09:16 Ответить
«В центре Земли гравитационный потенциал равна нулю»
+++
Уважаемый mihan40! Вы сами-то хоть поняли, что сказали?
В центре земли не потенциал, а напряженность гравитационного поля равна нулю. Напряженность это градиент потенциала. Потенциал исчисляется интегрированием, вседствие чего неизбежно возникает константа интегрирования. Конечно ее можно принять за ноль, но обычно за ноль берут бесконечно удаленную точку, в которой оцениваемый потенциал пренебрежимо мал. Тогда потенциал в центре источника поля оказывается максимальным.
Тогда потенциал в центре источника поля оказывается максимальным.
Так что Ваша версия непригодности гидростатической теории давления сама не пригодна. Соответственно остальные Ваши умозаключения также не имеют оснований.Ответить
mihan41 Сергей Заикин 03.10.2007 21:51 Ответить
Уважаемый Сергей. Рад тому, что тем кто как-то среагировал были Вы. Впечатление было таким, что Ваша дискусия сошла на нет, то есть умерла. Может я не очень правильно и выразился насчет гравитационного потенциала, так как все это делаю на улице, «с колена». В абстракциях я к тому же и не очен силен, но зато могу свою мысль Вам разьяснить другими более натуралистичными и понятными словами.
Центр Земли не является центром источника гравитационного поля, если и даже исходить из Ньютоновской версии гравитации. У такой ротационной космической фигуры Земли центром источника гравитационного поля является результирующий фокусный круг центрированных внутриземных эллипсоидаов. И поясняя скажу, что в центре Земли такие же гравитационные условия что и на поверхности, точнее в том смысле давление там более равно нулю, чем на поверхности Земли, так как в идеале нет даже атмосферного давления. В реальности вопрос сложный и требует изучения хотя бы потому, что в эту нулевую область накачиваются легкие элементы и они наверняка создают там парциальное (не гравитационное) давление. Что касается гравитационного ускорения они тоже наверняка разные, то есть в центре Земли он большой и направлен в противоположную сторону (направлен к фокусному кругу с противоположной стороны).
И поясняя скажу, что в центре Земли такие же гравитационные условия что и на поверхности, точнее в том смысле давление там более равно нулю, чем на поверхности Земли, так как в идеале нет даже атмосферного давления. В реальности вопрос сложный и требует изучения хотя бы потому, что в эту нулевую область накачиваются легкие элементы и они наверняка создают там парциальное (не гравитационное) давление. Что касается гравитационного ускорения они тоже наверняка разные, то есть в центре Земли он большой и направлен в противоположную сторону (направлен к фокусному кругу с противоположной стороны).
Если хотите анологий, то геометрический Центр Земли является вывернутым аналогом бесконечно удаленной точки с нулевым гравитационным потенциалом. Для того чтобы появилось ускорение должно быть нарушено равновессие из этой потенциальной ямы.
Сергей. Вам действительно трудно меня понять, так как новое не всегда является очевидным и поэтому прощаю Вам излишнюю резкость Вашего обращения.
Далее. При рассмотрении этой ситуации с эфиродинамической точки Зрения в рамках теории Исаева, мы получаем еще более не привычные представления о нашей умозрительной экскурсии в центр Земли и Вы убедились бы как далеко ушли своей континуальной математикой от реальной натуры.
При рассмотрении этой ситуации с эфиродинамической точки Зрения в рамках теории Исаева, мы получаем еще более не привычные представления о нашей умозрительной экскурсии в центр Земли и Вы убедились бы как далеко ушли своей континуальной математикой от реальной натуры.Ответить
rod1gin mihan41 13.01.2009 16:55 Ответить
В центре Земли действительно невесомость, но с чего Вы взяли, что там нет давления? Вся мантия Земли давит своей тяжестью на ядро, так же, как стенки воздушного шарика сдавливают воздух внутри шарика. Что, по вашему, препятствует проваливанию мантии в ядро если не давление?
Правильная картина такая: давление с глубиной растёт, но чем глубже, тем медленнее. Вблизи от центра рост давления практически прекращается. В центре давление максимально.
То, что область возле центра Земли содержит пузыри газа — возможно, потому что нет гравитационного градиента и ничто их оттуда не выдавливает.
 Только сомневаюсь, что какое-либо вещество может быть газообразным при таком давлении и такой (сравнительно небольшой) температуре.
Только сомневаюсь, что какое-либо вещество может быть газообразным при таком давлении и такой (сравнительно небольшой) температуре.Что касается гравитационного поля: если тело состоит из концентрических сфер разной массы, то на поверхности очередной сферы сила тяжести такая, как если бы эта сфера, вместе со всеми в неё вложенными, висела бы в пустом пространстве, а вышележащих сфер вообще бы не было. По-моему, ещё Ньютон эту задачу решил.
Т.е. на границе ядра и мантии сила тяжести такая, как если бы это ядро висело бы в космосе одно, без остальной Земли.
Ответить
jovany rod1gin 13.01.2012 17:31 Ответить
В центре Земли определенно газ или даже плазма.
Потому, что газ имеет большую плотность чем что-либо в жидкой или твердой фазе. Его можно сжимать сколько угодно, увеличивая плотность из за чего тот перестает всплывать. Этот эффект известен на подводных лодках, у которых есть глубины с которых она никогда не сможет всплыть т. к. газ уже не может расшириться.
к. газ уже не может расшириться.
Во-вторых: если при таких давлениях что-то испарится, то уже не сконденсируется никогда. Потому-что давление и температура выше критического. Пусть, например, газ возникший в центре начнет свой нелегкий путь к поверхности, но с уменьшением давления уменьшится и температура и он сконденсируется и перестанет быть газом. Это так же как в атмосфере: у поверхности +20С на высоте 10 000 -50С. Но воздушные массы не падают вниз понижая температуру у поверхности. Секрет в давлении. При его повышении — повышается температура.
В-третьих: как указали выше, газ выходит на поверхность из-за градиента давления, а к центру он уменьшается. Однажды образовавшись он никуда оттуда не денется.
ЗЫ. Не удивлюсь если лет через -дцать найдут, что при таких давлении и температуре тамуже не газ, а плазма в которой возможен не бурный холодный синтез и он тихо проходит в глубине нашей планеты.Ответить
rod1gin jovany 16.
 01.2012 18:08
Ответить
01.2012 18:08
Ответить> Потому, что газ имеет большую плотность
> чем что-либо в жидкой или твердой фазе.
> Его можно сжимать сколько угодноНет. Закон Клапейрона-Менделеева, как и любой известный нам физический закон, не абсолютно точный, и имеет границы применимости. При небольшом давлении он работает хорошо, но чем больше давление, тем более «неохотно» сжимается газ.
Когда плотность газа приближается к плотности жидкости, он становится столь же плохо сжимаемым, как и жидкость.
При очень больших температуре и давлении фазовый переход между жидкостью и газом становится всё менее чётким (в частности, уменьшается количество теплоты, выделяющееся/поглощающееся при этом переходе). При достижении некоторых критических значений температуры и давления разница между жидкостью и газом пропадает вообще. См. в Википедии статью «флюид» (физика). Ещё откройте там статью «тройная точка» и внимательно рассмотрите рисунок.

Ещё советую почитать про внутреннее строение больших планет (Юпитера и Сатурна) — они из этого самого сверхплотного газа состоят практически полностью. Если любите математику, можете попробовать самостоятельно рассчитать модель Юпитера согласно Клапейрону-Менделееву и сравнить с тем, что наблюдается фактически (задача вполне по силам школьнику-старшекласснику, надо только хорошо понимать, что такое интеграл).
> Этот эффект известен на подводных
> лодках, у которых есть глубины с
> которых она никогда не сможет
> всплыть т.к. газ уже не может
> расшириться.Мне лень выяснять, отчего там на самом деле тонет подводная лодка, но я предполагаю, что, тупо, давление воды за бортом становится больше, чем давление сжатого воздуха, запасённого в баллонах. Поэтому воздух не вытесняет воду из поплавка наружу, а наоборот, вода снаружи затекает в поплавок и «заталкивает» воздух обратно в баллоны.
> Не удивлюсь если лет через -дцать
> найдут, что при таких давлении и
> температуре тамуже не газ, а плазма
> в которой возможен не бурный холодный
> синтез и он тихо проходит в глубине
> нашей планеты.
Плазма это всего-лишь газ, обладающий интересными ЭЛЕКТРИЧЕСКИМИ свойствами. Механические свойства у плазмы ровно такие же, как и у обычного газа. Чёткой границы между плазмой и обычным газом, насколько я понимаю, нет, в частности, пламя костра (с температурой всего-лишь градусов 500…1000) это тоже до некоторой степени плазма. В последние годы плазму зачем-то распиарили как «четвёртое агрегатное состояние вещества».
Словосочетание «холодный синтез» рекомендую вообще не употреблять, пока не научитесь самостоятельно отличать науку от журналистских ляпов.
Ответить
mihan41 Etwas 02.10.2007 09:37 Ответить
Уважаемый Etwas. Вы правы в своих сомнениях о твердости ядра. Что касается магнитного поля Земли, то оно приобретенное. Земля не является генератором своего магнитного поля. Она им наматывается от генерируемой Солнцем м. поля. Если хотите больше знать, то прочтите книгу С.М. Исаева «Начала теории физики эфира и ее следствия» (Издательство «Ком. книга». Каталог в интернете:http://URSS.ru). Можете также заказать его новую книгу через Московское издательство учебной и научной литературы УРСС «Эврэ, электрон, эфир и постулат Исаикан»
Она им наматывается от генерируемой Солнцем м. поля. Если хотите больше знать, то прочтите книгу С.М. Исаева «Начала теории физики эфира и ее следствия» (Издательство «Ком. книга». Каталог в интернете:http://URSS.ru). Можете также заказать его новую книгу через Московское издательство учебной и научной литературы УРСС «Эврэ, электрон, эфир и постулат Исаикан»
Ответить
Сергей Заикин 08.04.2007 09:33 Ответить
Версия авторов статьи, что причиной извержений вулканов являются процессы дегазации магмы и подвижки тектонических плит, сомнительна. Даже просто из здравого смысла и необходимости огромных энергий версия спонтанного перемещения масс вещества мантии представляется неубедительной. Источники энергии для перемещений тектонических плит носят исключительно гипотетический характер.
В то же время существует принципиально иная теория глобальной тектоники земли, основанная на расширении Земли изнутри. На эту тему имеется достаточно обширная научная литература, где на сотнях фактов обосновывается гипотеза расширения Земли. В этой связи можно указать книгу австралийского ученого У. Кэри ‘В поисках закономерностей развития Земли и Вселенной’ /М. Мир, 1991. 447 с./, работы Чудинова Ю.В. (Геология активных океанических ораин и глобальная тектоника. М. Недра, 1985. 248с.) (Чудинов Ю.В. Ключ к проблемам глобальной тектоники//Наука в России 1999, N 5, стр. 54-60). (В.Нейман. Газета ‘Социалистическая индустрия’, 2 октября 1980 г.) (В.Б.нейман Расширяющаяся Земля. М. Географгиз, 1963. 185 с.)
На эту тему имеется достаточно обширная научная литература, где на сотнях фактов обосновывается гипотеза расширения Земли. В этой связи можно указать книгу австралийского ученого У. Кэри ‘В поисках закономерностей развития Земли и Вселенной’ /М. Мир, 1991. 447 с./, работы Чудинова Ю.В. (Геология активных океанических ораин и глобальная тектоника. М. Недра, 1985. 248с.) (Чудинов Ю.В. Ключ к проблемам глобальной тектоники//Наука в России 1999, N 5, стр. 54-60). (В.Нейман. Газета ‘Социалистическая индустрия’, 2 октября 1980 г.) (В.Б.нейман Расширяющаяся Земля. М. Географгиз, 1963. 185 с.)
В этих работах обосновывается сам факт расширения Земли изнутри, но, увы, это расширение не находит теоретического объяснения. Однако, как отмечает Ю.В. Чудинов ‘Отсутствие в настоящее время физического объяснения расширения нашей планеты не является доводом против него’.
Согласно концепции расширяющейся Земли происходит не субдукция (наползание одной плиты на другую), а абдукция, то есть выползание одной плиты из-под другой. Земля распирается изнутри и трещит ‘по швам’ в виде землетрясений, магма выдавливается в слабых местах в виде вулканических извержений.
Земля распирается изнутри и трещит ‘по швам’ в виде землетрясений, магма выдавливается в слабых местах в виде вулканических извержений.
Ответить
barjer Сергей Заикин 09.04.2007 20:28 Ответить
Уважаемый Сергей (простите, не знаю отчества)! Я знаком не со всеми перечисленными Вами работами. Знаком с работой Чудинова, «Геология активных океанических…» и далее и рядом других, в которых высказываются похожие идеи. Ни в одной из них нет не только теоретического обоснования этой идеи, но не приводится ни одной разумной причины такого расширения. Разумной я считаю такую причину, которую можно было бы хоть как-то привязать к известным физическим законам или феноменам.
Скажите, с какой стати охлаждающееся тело — а то что Земля охлаждается сомнений быть не должно хотя бы по причине наличия температурного градиента между недрами и окружающим пространством — станет расширяться? Напомню, что температура магмы, извергающейся из близлежаших к поверхности недр, равна примерно 1000 град С, а температура стратосферы — где-то около минус 100 град С.
Далее. Ссылки авторов на абдукцию опровергаются многократными измерениями сдвиговых деформаций в литосфере. Так вот. В так называемых рифтовых зонах, т.е. в зонах контакта литосферных плит, где и можно наблюдать субдукцию или абдукцию, на лицо напряжения сжатия, в то время как в центральных частях литосферных плит наоборот — деформации растяжения. Это означает, что литосферные плиты в местах их контакта не только «наползают», но с приличными силами ДАВЯТ друг на друга. А вот в центральных областях плит наблюдается другая картина. Там толщина коры существенно больше, чем на краях. В среднем разница составляет десятки километров. Следовательно охлаждение, а значит и температурное сжатие подкорковой магмы происходит медленнее, чем на периферии. И поскольку кромки плиты оседают быстрее, в центре плита как бы подпирается магмой, которая как «через коленку» ломает ее, вызывая напряжения растяжения и растрескивание. Одним из доводов в пользу расширения Земли изнутри являются эти самые напряжения растяжения, наблюдаемые во многих районах материковой части коры.
 А вот наблюдений, говорящих о таких напряжениях в рифтовых зонах нет.
А вот наблюдений, говорящих о таких напряжениях в рифтовых зонах нет.Наконец, Вы верно говорите о «выдавливании» магмы. Но, простите, не кажется ли Вам, что «выдавливание» проще объясняется оседанием краев плит, происходящее в результате сжатия охлаждающейся магмы, на которую они опираются? Кстати, в этом случае находится простое объяснение землятрясениям. Они происходят, когда большие фрагменты коры, постепенно теряя под собой опору из-за охлаждения магмы, не оседают, а срываются в магму, вызывая в ней волны, которые и раскачивают кору, заставляя ее трескаться, ломаться, тороситься. Если это происходит под водой, рождаются цунами, вызванные резким опусканием или наоборот вздыбливанием дна.
Ответить
Сергей Заикин barjer 10.04.2007 12:05 Ответить
Уважаемый barjer , (простите, не знаю Вашего имени-отчества)!
Согласен с Вами, что версия расширения Земли изнутри, выглядит неправдоподобной. Тем не менее, существует множество явлений, указывающих на эту версию. Меня очень впечатлила книга У. Кэри, указанная в предыдущем сообщении. В ней не только приводится большое количество эмпирического материала, но выстроена достаточно стройная система, интерпретирующая имеющиеся данные. Многочисленные данные приобретают согласованность именно в случае расширения Земли изнутри. Единственно, чего нет в этой и других публикациях, так объяснения природы расширения Земли изнутри.
Тем не менее, существует множество явлений, указывающих на эту версию. Меня очень впечатлила книга У. Кэри, указанная в предыдущем сообщении. В ней не только приводится большое количество эмпирического материала, но выстроена достаточно стройная система, интерпретирующая имеющиеся данные. Многочисленные данные приобретают согласованность именно в случае расширения Земли изнутри. Единственно, чего нет в этой и других публикациях, так объяснения природы расширения Земли изнутри.
Приведенные Вами данные о характере напряжения на краях и в середине литосферных плит, скорее не опровергают, а подтверждают версию расширения изнутри. Ведь при расширении сферы изменяется (должна изменяться) кривизна поверхности, но окаменевшая плита не изменяет своей кривизны и начинает не вписываться в изменившуюся сферу, тем самым, давит краями в магму. Отсюда напряжение сжатия большее, чем в середине. Отсюда могут возникать горизонтальные сдвиговые деформации в верхних слоях литосферы в рифтовых зонах, создающие впечатление, что плиты наползают друг на друга. А на самом деле всего лишь изменяется угол между плитами, происходит сдавливание поверхностного слоя плиты и расхождение внутреннего. В образовавшуюся расщелину устремляется магма, которая иногда вырывается наружу в виде извержения вулкана.
А на самом деле всего лишь изменяется угол между плитами, происходит сдавливание поверхностного слоя плиты и расхождение внутреннего. В образовавшуюся расщелину устремляется магма, которая иногда вырывается наружу в виде извержения вулкана.
Как видите, интерпретация одних и тех же данных может быть различной.
В статье Ю.В. Чудинова (Наука в России 1999, N 5, стр. 56) показывается, что возраст океанического фундамента с приближением к зоне предполагаемой субдукции уменьшается, а не возрастает. Из этого он сделал вывод, что плиты выдвигаются одна из-под другой, и назвал процесс эдукцией. (В предыдущем сообщении у меня ошибка в наименовании). Глубоководное бурение на активных окраинах против желобов не выявило ни одного участка, где возраст основания осадочного чехла становился бы древнее с приближением к желобу, наоборот, он становился моложе.
В зоне погружения (предполагаемого из соображений субдукции) должно быть снижение теплового потока над опускающейся в мантию холодной плиты, однако наблюдается, наоборот, его повышение в несколько раз в сравнении со среднеземным тепловым потоком.
Вместо увеличения толщины осадков в осевых частях желобов, их сгруживания и интенсивного смятия, многочисленные сейсмические изображения показывают расположение там ненарушенных горизонтально залегающих осадков малой мощности (от 200 — 100 м до полного их отсутствия), хотя обычно в океане мощность осадков 600 — 1000 м.
В областях предполагаемой субдукции широко проявлены свидетельства выноса к поверхности огромных масс глубинного материала.
Из всего этого следует, что, увы, ничего не ясно, и надо продолжать искать теоретически правильный ответ.
Мне понятно Ваше неприятие расширения Земли изнутри. Действительно, это не имеет теоретического объяснения. Но версия все же есть. В книге Кэри. Сейчас у меня ее нет под рукой, и я не могу воспроизвести дословно. У Кэри имеется ссылка на русского ученого конца 19 века, который лет за 20 до Эйнштейна предложил теорию гравитации, в основе которой лежит эфир и его всасывание внутрь планет. Всасываясь, он сносит все, что находится на его пути, порождая притяжение. Это не противоречит ни Ньютону, ни Эйнштейну. Предложенный подход всего лишь вносит физический смысл в известные законы и дает иную им интерпретацию, не изменяя математических соотношений. Так вот Кэри использовал идею (сейчас не помню фамилии) нашего соотечественника и высказал, что всасываемый эфир идет на увеличение массы и размеров Земли.
Это не противоречит ни Ньютону, ни Эйнштейну. Предложенный подход всего лишь вносит физический смысл в известные законы и дает иную им интерпретацию, не изменяя математических соотношений. Так вот Кэри использовал идею (сейчас не помню фамилии) нашего соотечественника и высказал, что всасываемый эфир идет на увеличение массы и размеров Земли.
Сами понимаете, что идея очень дерзкая. Но рассмотрение ее показывает, что не все так уж безнадежно. Посмотрите материалы дискуссии http://elementy.ru/lib/430444?context=369867&discuss=430444
При хорошем раскладе можно решить сразу целый ряд нерешенных пока проблем.
Сергей Иванович.
Дополнено 13.04.07
Пришлось сходить в библиотеку и сделать уточнения.
Австралийский геолог Семюел Уоррен Кэри ссылается на работу /Ярковский И.О. Всемирное тяготение как следствие образования вещества внутри небесных тел. Москва 1899 г. (второе издание — СПб 1912 г.)/.
И.О. Ярковский выдвинул гипотезу, что существует переход от невесомого вещества (эфира) к реальной материи и что он ведет к появлению планет и звезд. Кэри указывает далее, что через несколько десятилетий это представление было развито в СССР с геологических позиций. Небольшая группа авторов выпустила об этом несколько статей и книг. Среди них выделяются И.Б. Кириллов, В.Б. Нейман и А.И. Летавин из Москвы и В.Ф Блинов из Киева.
Кэри указывает далее, что через несколько десятилетий это представление было развито в СССР с геологических позиций. Небольшая группа авторов выпустила об этом несколько статей и книг. Среди них выделяются И.Б. Кириллов, В.Б. Нейман и А.И. Летавин из Москвы и В.Ф Блинов из Киева.
Сам Кэри до середины семидесятых годов о причинах расширения Земли говорил — не знаю. В начале восьмидесятых годов в Москве прошла конференция и издан сборник статей /Проблемы расширения и пульсации Земли. Материалы конференции. — М. Наука. 1984./
В качестве возможных причин расширения Земли рассматриваются несколько вариантов:
1. Циклические пульсации вследствие изменения плотности.
2. Аккреция. (присоединение к Земле).
3. Расширение сверхплотного ядра Земли.
4. Изменение со временем гравитационной постоянной.
5. Увеличение массы.
Кэри делает вывод, что причину должны искать физики. ‘Чем скорее физики усвоят урок, вытекающий из таких примеров (свидетельствующих о расширении Земли — С. З.), тем скорее они найдут новые законы, необходимые для объяснения этих фактов. Здесь лежит ключ к важнейшему новому открытию’. /с. 358/
З.), тем скорее они найдут новые законы, необходимые для объяснения этих фактов. Здесь лежит ключ к важнейшему новому открытию’. /с. 358/
Так что господа физики — ищите.Ответить
mihan40 barjer 30.09.2007 23:01 Ответить
Уважаемый Barjer. Вы правы, что рифтовые долины Срединно-океанических хребтов очень пассивные образования и такие же пассивные как и атлантические окраины Африканского или Американского континентов. Но Вам следует обратить внимание при этом какими динамически активными являются перпендикулярные к ним трансформные разломы. Если осмыслить эту ситуацию, то мы можем говорить о самостоятельном дрейфе океанической коры и никак не влияющей на побережье Пацифики. В регионе Атлантики она дрейфует из Северного и Южного полюсов к экватору в то время как обрамляющие данный океан материки остановили свое схожее меридиональное движение столкнувшись лбами.
 Другими словами я призываю Вас уточнить свои представления о глобальной плитной тектонике через космогеодинамическую теорию Исаева Сергея Михайловича. Издательство УРСС на днях собирается выпустить его новую книгу «Эврэ, электрон, эфир и постулат Исаикан»
Другими словами я призываю Вас уточнить свои представления о глобальной плитной тектонике через космогеодинамическую теорию Исаева Сергея Михайловича. Издательство УРСС на днях собирается выпустить его новую книгу «Эврэ, электрон, эфир и постулат Исаикан»Ответить
mihan41 Сергей Заикин 02.10.2007 09:56 Ответить
Уважаемый Сергей. Вы правы лишь отчасти в том, что механизм движения континентов носит гипотетичный характер. Такая ситуация была лишь до 1987-го года, до постановки доклада «Космогеодинамическая эволюция Земли» Исаевым С.М. в Ленинградском университете на секции планетологии в Совете Космических иследований АН СССР. К сожалению, революционная новизна и неприкрытая критика Энштейновского релятивизма и грядущие социальные перемены не позволили идеям показать всему научному сообществу. Сообщество до сих пор пребывает в состоянии «слышал звон, да не знаю где он». Исаевым наряду найдена и доказана новая тангенциальная сила гравитационной природы, действующая на твердо-коровые образования Земли, которая направлена от эклиптического полюса к эклиптическому экватору Земли.
Исаевым наряду найдена и доказана новая тангенциальная сила гравитационной природы, действующая на твердо-коровые образования Земли, которая направлена от эклиптического полюса к эклиптическому экватору Земли.
Ответить
Сергей Заикин 13.04.2007 07:59 Ответить
Сопоставление и отождествление процессов, происходящих внутри Земли и чайника, имеет определенные ограничения. Чайник имеет подогрев, вследствие которого, собственно, и происходят все теплообменные процессы. Интенсивность подогрева в чайнике существенно превосходит естественные возможности теплообмена внутри жидкости путем теплопроводности, в результате чего возникают конвекционные потоки. В случае с Землей источник подогрева либо отсутствует, либо нужно хорошо постараться, чтобы теоретически обосновать его наличие. В случае отсутствия подогрева вещества Земли изнутри, остается рассматривать теплообменные процессы, как процесс остывания планеты снаружи. В этом случае конвекционные потоки могли бы возникнуть из-за неравномерности остывания поверхности Земли. Но теплопередача зависит от градиента температур, и остывание идет быстрее там, где градиент больше. То есть возникший (непонятно каким образом) локальный более больший градиент температур в естественных условиях должен непременно снижаться. Система, согласно законам термодинамики, должна стремиться к термодинамическому равновесию. Таким образом, для возникновения и расхождения градиентов нужны надежные источники энергии. Значит, их нужно искать. И не только для конвекционных потоков. Они нужны и для горизонтального движения литосферных плит, фактически для движения континентов. Где источники энергии для этих движений? Вразумительного ответа нет.
В этом случае конвекционные потоки могли бы возникнуть из-за неравномерности остывания поверхности Земли. Но теплопередача зависит от градиента температур, и остывание идет быстрее там, где градиент больше. То есть возникший (непонятно каким образом) локальный более больший градиент температур в естественных условиях должен непременно снижаться. Система, согласно законам термодинамики, должна стремиться к термодинамическому равновесию. Таким образом, для возникновения и расхождения градиентов нужны надежные источники энергии. Значит, их нужно искать. И не только для конвекционных потоков. Они нужны и для горизонтального движения литосферных плит, фактически для движения континентов. Где источники энергии для этих движений? Вразумительного ответа нет.
Ответить
barjer Сергей Заикин 26.04.2007 20:54 Ответить
Уважаемый Сергей Иванович! Ваше представление о возможности напряжений сжатия в рифтовых зонах, когда происходит расширение Земли, не выдерживает критики.
 Очевидно, расширяясь, внутренние слои мантии ли, ядра ли, неважно, просто обязаны растаскивать кору во всех зонах, в том числе и в рифтовых, т.е. напряжения везде должны быть растягивающими. Однако не практике дело обстоит именно так, как я говорил выше: в рифтовых зонах наблюдаются именно напряжения сжатия. К той литературе, о которой я говорил выше, добавлю новую библиографию. смотрите, например, статью Л.М. Расцветаева «Альпинотипные орогены: контракционно-сдвиговая модель» в сборнике «Фундаментальные проблемы геотектоники» Мат-лы XL Тектонического совещания, М. ГЕНС, 2007 г. с. 129. И там же: Г.Ф.Уфимцев. «Феномены новейшего материкового тектогенеза»,с. 253.
Очевидно, расширяясь, внутренние слои мантии ли, ядра ли, неважно, просто обязаны растаскивать кору во всех зонах, в том числе и в рифтовых, т.е. напряжения везде должны быть растягивающими. Однако не практике дело обстоит именно так, как я говорил выше: в рифтовых зонах наблюдаются именно напряжения сжатия. К той литературе, о которой я говорил выше, добавлю новую библиографию. смотрите, например, статью Л.М. Расцветаева «Альпинотипные орогены: контракционно-сдвиговая модель» в сборнике «Фундаментальные проблемы геотектоники» Мат-лы XL Тектонического совещания, М. ГЕНС, 2007 г. с. 129. И там же: Г.Ф.Уфимцев. «Феномены новейшего материкового тектогенеза»,с. 253.
Несколько слов об «эфирном расширении». Во-первых, эфир, как такового, так и не обнаружили в опытах. То, о чем говорит, например, Ацюковский, вовсе не какой-то спец эфир, а обычные прозрачные вещественные среды, если речь идет о среде распространения света (об этом подробно в моей книге «Физические очерки», которая есть в ленинке и магазине «Физмат книга», тал 409 93 28). К тому же очень трудно, как вы справедливо говорите, представить себе какого это рожна этот «эфир» станет вдруг продираться внутрь Земли, или кто или что его будет туда загонять.
К тому же очень трудно, как вы справедливо говорите, представить себе какого это рожна этот «эфир» станет вдруг продираться внутрь Земли, или кто или что его будет туда загонять.
Что касается конвекционных потоков в слое магматической мантии Земли, то конечно, они могут иметь место, но вряд ли они имеют отношение к тем или иным напряжениям в толще коры. Источником же энергии, приводящем к возникновению температурного градиента, вызывающего охлаждеие Земли, служит именно сама расплавленая магма, температура которой не меньше чем на 1000 град С превышает наружную температуру коры. А вот конвекционные потоки в магматической мантии могут возникнуть только при условии нарушения динамического равновесия в ее слоях, например, при извержении магмы наружу.
Теперь к горизонтальным движениям плит. Все-таки представление о «дрейфе континентов», которое связывают с миллиметровыми встречными перемещениями краев литосферных плит, скорее всего связано с тем самым оседанием этих краев, вызванное охлаждением и сжатием магматической мантии.
Ответить
Сергей Заикин barjer 27.04.2007 09:23 Ответить
Уважаемый barjer!
Благодарю Вас за ответ. Мне интересна ситуация, сложившаяся в исследовании земных явлений — землетрясений, извержений вулканов, грозового электричества, земного электричества, земного магнетизма. Во всех этих вопросах просматривается какая-то недоисследованность. В данном случае рассматриваются проблемы извержений вулканов и землетрясений. Согласитесь, что неясностей предостаточно. Имеется множество версий объяснения, и ни одна из них не обладает полноценностью.
В этой ситуации настораживает линия поведения сторонников различных версий. Каждая из сторон опирается на ‘свои’ факты, на свой эмпирический материал и игнорирует факты, не вписывающиеся в их концепцию. В частности вызывает недоумение замалчивание сторонниками субдукции фактов, не вписывающихся в теорию наползания одной плиты на другую. Вот и в Вашем ответе факты, приведенные Ю.В. Чудиновым, оставлены без внимания. Почему в зоне субдукции возраст плиты возрастает при удалении от впадины, почему нет сгруживания осадков, почему толщина осадков вблизи впадины меньше, чем в океане, почему тепловой поток в зоне субдукции превышает средний. Или все это выдумки Чудинова?
Вот и в Вашем ответе факты, приведенные Ю.В. Чудиновым, оставлены без внимания. Почему в зоне субдукции возраст плиты возрастает при удалении от впадины, почему нет сгруживания осадков, почему толщина осадков вблизи впадины меньше, чем в океане, почему тепловой поток в зоне субдукции превышает средний. Или все это выдумки Чудинова?
Какова вообще стратегия исследователей Земли — найти истину или защитить свою концепцию?
У меня, чем больше я погружаюсь в проблемы геотектоники, тем больше возникает непонимания. Посмотрел в энциклопедию, ‘рифт это линейно вытянутая щелевидная или ровообразная структура растяжения земной поверхности’. Так какое напряжение в рифтах: сжатия или растяжения?
Возникает еще один вопрос. Плита, пододвигаясь, порождает повышенное напряжение сжатия, или наоборот, повышенное напряжение сжатия двигает плиту?Ответить
mihan41 Сергей Заикин 02.10.2007 21:51 Ответить
Уважаемый Сергей. Источник энергии находится внутри Земли. Представте модель Земли не в виде примитивного гравитирующего шара, а в виде реальной фигуры вращения, т. е. — эллипсоида вращения. Тогда Вы увидите в геометрическом центре Земли нулевый гравитационный птенциал и центром масс уже является не точка , а фокусный круг эллипсоида вращения. Вы увидите, что между геометрическим центром и фокусным кругом существует радиальная область ускорения и при интерполяции на объемную фигуру эта область ускорения выдвигается к полюсам по оси вращения. По теории упомянутого выше Исаева в центральной области Земли есть естественный термоядерный реактор в виде указанного гравитационного ускорителя.
Источник энергии находится внутри Земли. Представте модель Земли не в виде примитивного гравитирующего шара, а в виде реальной фигуры вращения, т. е. — эллипсоида вращения. Тогда Вы увидите в геометрическом центре Земли нулевый гравитационный птенциал и центром масс уже является не точка , а фокусный круг эллипсоида вращения. Вы увидите, что между геометрическим центром и фокусным кругом существует радиальная область ускорения и при интерполяции на объемную фигуру эта область ускорения выдвигается к полюсам по оси вращения. По теории упомянутого выше Исаева в центральной области Земли есть естественный термоядерный реактор в виде указанного гравитационного ускорителя.
Ответить
Antri 15.04.2007 00:10 Ответить
Уважаемый bajer! Напрасно не сомневаетесь в том, что Земля остывает. Наличие существующего у Земли температурного градиента ничего не доказывает. У включенной конфорки тоже градиент туда же, при этом она разогревается.
У включенной конфорки тоже градиент туда же, при этом она разогревается.
Ответить
barjer Antri 26.04.2007 21:02 Ответить
Уважаемый Антри! Не стоит путать Землю с конфоркой. Очевидно, конфорка разогревается благодаря притоку тепла от сжигаемого газа. И градиент тут ни причем. А вот наличие градиента между внутренними слоями земли и ее поверхностью неизбежно вызовет поток тепла от более нагретых слоев к менее нагретым, что, в свою очередь, неизбежно приведет к сжатию охлаждающихся внутренних слоев. Все очень физично, не правда ли?
Ответить
liberman01 26.04.2007 22:49 Ответить
На моём сайте http://www.lphysics.ru опубликована моя статья «Эффект Джоуля-Томсона — одна из причин разогрева вулканических газов». Предлагаю ознакомиться.
Предлагаю ознакомиться.
Ответить
barjer liberman01 02.05.2007 20:11 Ответить
Уважаемый Либерман! Простите, не смог войти в Ваш сайт. Может быть ломлюсь в открытую дверь, но не проще ли объяснить высокую температуру внутри планет большим давлением? А оно действительно велико. Принято считать (сведения из института физики Земли), что давление внутри планет изменяется по гидростатическому закону: Р = п г, где Р — давление, п — плотность, г — глубина. В центре Земли согласно этому закону давление где-то около 3,5 млн атм. И температура должна быть соответствующей. По мере подъема к поверхности температура, конечно, падает, но остается достаточно большой, порядка 1000 К.
Ответить
liberman01 barjer 02.05.2007 23:49 Ответить
Уважаемый Barjer! Попробуйте зайти непосредственно в http://www.
 lphysics.ru/index.htm
lphysics.ru/index.htm
Если Вам удастся ознакомиться со статьёй, то некоторые вопросы отпадут сами собой. Скажите, а в чём заключались трудности вхождения в сайт?Ответить
rod1gin barjer 13.01.2009 17:16 Ответить
Почему-это раз давление высокое, то и температура должна быть высокая? Что за логика?
Давление и температура — параметры, НИКАК не связанные между собой. На границе между атмосферой и мантией Урана или Нептуна давление побольше, чем в центре Земли, а температура почти комнатная. Или, скажем, на дне Марианской впадины давление тоже не слабое, а температура всего +4 по Цельсию.
Ответить
greve 02.05.2007 20:40 Ответить
Что Вы, господа учёные, такие невнимательные и рассеяные. Ведёте такие вумные дискуссии, читаешь и думаешь, вот же есть образованые люди /здесь я не очень сильно иронизирую/. А потом, рраз, и вылазит какая-нибудь фигня… И что нам, двоечникам, после этого думать? Шариться лишний раз в «Гугле» тоже не очень то охота…
Ведёте такие вумные дискуссии, читаешь и думаешь, вот же есть образованые люди /здесь я не очень сильно иронизирую/. А потом, рраз, и вылазит какая-нибудь фигня… И что нам, двоечникам, после этого думать? Шариться лишний раз в «Гугле» тоже не очень то охота…
Поначалу температура магмы в верхних горизонтах была 1000 град С. А потом вдруг «цельсий» превратился в «кельвина». Это же далеко не одно и то-же. Так кто же там «прячется» на самом деле под цифрой 1000?
Ответить
barjer greve 04.05.2007 12:58 Ответить
Вкралась опечатка: градус действительно Цельсия. Впрочем, существенно на результат это не повлияет. Главное то, что температурный перепад существует. От того, больше он или меньше, зависит лишь скорость остывания магмы и быстрота ее оседания.
Ответить
AD
10. 05.2007 14:34
Ответить
05.2007 14:34
Ответить
Почитал споры, удивился.
Ответьте мне, господа физики, на простые вопросы:
1. Звезды и планеты разогреваются за счет сжатия. А
так же за счет трения при опускании тяжелых фракций вглубь.
Я ошибаюсь?
2. Движение плит вызывается процессами в мантии? Движение
в мантии есть конвекционные потоки. Так?
3. Как может плита образовываться в мантии! под другой плитой!?
Или я что-то не понял?
Ответить
barjer AD 12.05.2007 21:43 Ответить
Уважаемый АД!
1. Трение, возможно, и играет какую-то роль в разогреве звед и планет, но основное — это высокие давления внутри тел.
2. Движения плит, как такового, не происходит, поскольку им некуда двигаться: на их пути соседние плиты. Кроме того, чтобы плита двигалась, надо чтобы с другой стороны она отрывалась от другой соседней. За движение плит принимается их оседание по краям по мере оседания остывающей магмы. Это оседание — причина, как я уже говорил, и другого явления: извержения вулканов. Оседая, плита выдавливает магму наружу. Конвективные потоки магмы, по-видимому, имеют место быть. И на краях плит они более интенсивные, поскольку она ближе к поверхности. Это ускоряет охлаждение магмы, а, следовательно, ее оседание, которое, в свою очередь, вызывает оседание краев плит.
За движение плит принимается их оседание по краям по мере оседания остывающей магмы. Это оседание — причина, как я уже говорил, и другого явления: извержения вулканов. Оседая, плита выдавливает магму наружу. Конвективные потоки магмы, по-видимому, имеют место быть. И на краях плит они более интенсивные, поскольку она ближе к поверхности. Это ускоряет охлаждение магмы, а, следовательно, ее оседание, которое, в свою очередь, вызывает оседание краев плит.
3. Плиты уже образовались. Теперь происходит их утолщение по мере кристаллизации остывающей магмы.Ответить
AD barjer 14.05.2007 14:47 Ответить
1. Скажем проще, при перемещении более тяжелых фракций вглубь огромная потенциальная энергия переходит в тепловую. Само по себе давление создать приток энергии не может. Да, планета разогревается при сжатии, но до определенной степени, далее сжатие останавливается.

2. Давно известно, что континенты перемещаются, при этом это движение было измерено как непосредственно, так и геологическими методами.
Почему магма должна оседать при остывании? Если это было бы так, континенты давно погрузились бы в магму. Из Ваших слов возникает, ощущение, что Земля сжимается, а это совсем не так. Многие тела при охлаждении расширяются! Например, лёд.
3. Просто тут была теория расширяющейся Земли …
Кстати, насчет утолщения я не уверен.Ответить
barjer AD 20.05.2007 20:59 Ответить
1. Внутри Земли плотность вещества выше за счет большего давления. А давление в недрах планет, как я уже говорил, возрастает по гидростатическому закону, т.е. пропорционально плотности и глубине. Поэтому более легкие верхние слои вряд ли будут оседать внутрь.
2. Давление, конечно не создает «притока энергии».
 Важнее не приток, а поток энергии. Его создает градиент температуры, который очевидно имеет место между горячей магмой и холодной поверхностью планеты.
Важнее не приток, а поток энергии. Его создает градиент температуры, который очевидно имеет место между горячей магмой и холодной поверхностью планеты.3. Рост давления очевидно прекращается в центре планеты. Там оно маскимально.
4. Перемещаться континенты могли бы, если бы между ними были свободные пространства, например, если бы они плавали в магме. Но ведь в этом случае дожны быть места, где магма находится на поверхности. чего не наблюдается. То, что принимается за перемещение, на самом деле оседание краев плит, происходящее по мере охлаждения и оседания магмы. Именно эти движения плит «были измерены».
5. Магма — обычное физическое тело. Очевидно, она не лед. Поэтому, как любое физическое тело обязано при охлаждении сжиматься. Кстати, кроме льда, мне не известно ни одного вещества, расширяющегося при охлаждении.
6. «Теория» о расширении Земли, возможно и была, но обосновывалась она проблематичным поглощением гипотетического «эфира». Почему-то при этом стыдливо забывалось, что «эфир» введен, как невесомый и всепроникающий. С чего бы это ему задерживаться в Земле?
С чего бы это ему задерживаться в Земле?7. По поводу утолщения плит. Интересно, а куда должна деваться застывающая магма? Самое естественное предположить, что происходит ее кристаллизация на «затравках» уже застывшей коры.
Ответить
barjer AD 20.05.2007 21:00 Ответить
1. Внутри Земли плотность вещества выше за счет большего давления. А давление в недрах планет, как я уже говорил, возрастает по гидростатическому закону, т.е. пропорционально плотности и глубине. Поэтому более легкие верхние слои вряд ли будут оседать внутрь.
2. Давление, конечно не создает «притока энергии». Важнее не приток, а поток энергии. Его создает градиент температуры, который очевидно имеет место между горячей магмой и холодной поверхностью планеты.
3. Рост давления очевидно прекращается в центре планеты. Там оно маскимально.

4. Перемещаться континенты могли бы, если бы между ними были свободные пространства, например, если бы они плавали в магме. Но ведь в этом случае дожны быть места, где магма находится на поверхности. чего не наблюдается. То, что принимается за перемещение, на самом деле оседание краев плит, происходящее по мере охлаждения и оседания магмы. Именно эти движения плит «были измерены».
5. Магма — обычное физическое тело. Очевидно, она не лед. Поэтому, как любое физическое тело обязано при охлаждении сжиматься. Кстати, кроме льда, мне не известно ни одного вещества, расширяющегося при охлаждении.
6. «Теория» о расширении Земли, возможно и была, но обосновывалась она проблематичным поглощением гипотетического «эфира». Почему-то при этом стыдливо забывалось, что «эфир» введен, как невесомый и всепроникающий. С чего бы это ему задерживаться в Земле?7. По поводу утолщения плит. Интересно, а куда должна деваться застывающая магма? Самое естественное предположить, что происходит ее кристаллизация на «затравках» уже застывшей коры.

Ответить
liberman01 barjer 21.05.2007 13:24 Ответить
О веществах, плотность которых уменьшается при переходе из жидкого состояния в твёрдое, читайте в моей статье: А. Либерман. «Аномальные элементы». «Квант» N3 2002.
Ответить
AD barjer 23.05.2007 16:37 Ответить
1. Представим, что мы взболтали в воде железные опилки. Через некоторое время опилки осядут на дно. В воде это произойдет быстро, а в вязкой жидкости медленно.
2. Не спорю, но нужно учитывать и п.1
3. Рост давления давно прекратился. Само давление в центре максимально,
не спорю.
4. Назвать процесс можно как угодно, но Гималаи образовались на стыке плит. Кроме того если бы происходило опускание границ плит, это происходило бы равномерно и «движения» континентов бы не было.
5. А лед — не обычное физическое тело ? ))
Серьезно? Таких веществ очень много. При переходе из жидкого в твердое состояние, например, это происходит почти со всеми веществами.
7. Поддерживается баланс между мантией и корой. Пока не прекратится
приток энергии, он сильно не изменится. Точно так же не изменяется
размер и температура Солнца, пока идет термоядерная реакция.Ответить
liberman01 AD 24.05.2007 10:34 Ответить
У «почти всех веществ» плотность при переходе из жидкого состояния в твёрдое увеличивается. Уменьшение плотности наблюдается у воды и пяти приведённых мною химических элементов: галлия — Ga, германия — Ge, висмута — Bi, ксенона — Xe и радона — Rn.
Ответить
Сергей Заикин barjer 25.05.2007 10:55 Ответить
Уважаемый barjer!
Гипотетический эфир в современной терминологии это физический вакуум, который обладает внутренней энергией-импульсом. При определенных условиях энергия вакуума преобразуется в форму массы, со всеми вытекающими последствиями, в том числе и для расширения Земли.
При определенных условиях энергия вакуума преобразуется в форму массы, со всеми вытекающими последствиями, в том числе и для расширения Земли.
Но это отдельный вопрос.
У меня возникает непонимание причин, по которым Вы игнорируете факты, не вписывающиеся в концепцию тектоники (субдукции) плит. Ваша попытка дистанцироваться от субдукции путем версии «опускания» плит или их краев, делает совсем непонятным факт, что возраст основания океанического дна в районе срединных хребтов, приближается к нулю либо имее оценки в районе 10-20 млн. лет. Что было в данном месте земной сферы 30 и более млн. лет? Субдукция хоть как-то это объясняла (и продолжает объяснять). По версии этой концепции в районе срединных океанических хребтов происходит раздвижение литосферных плит, а с их противоположной стороны происходит субдукция, то есть их погружение под другие плиты. Хотя эта теория несостоятельна, но указанный факт она объясняла. В Вашей версии объяснения, подвисает и этот факт.
Правда, версия субдукции имеет некоторые элементы правдоподобия лишь для тихоокеанского региона, где кроме срединного океанического разлома существует окраинный разлом по периметру Тихого океана. Для других океанов вообще не просматривается зон субдукции. Но зона расширения вдоль Атлантического и Индийского океанов есть.
Для других океанов вообще не просматривается зон субдукции. Но зона расширения вдоль Атлантического и Индийского океанов есть.
Для концепции субдукции вообще необъяснимо, что возраст океанического дна везде существенно моложе геологического возраста суши. Для материков возраст оценивается в 600 — 700 миллионов лет, а основания океанического дна в подавляющей части от 0 до 100 — 180, местами до 200, 300 млн. лет. А что находилось на месте дна 400 — 600 млн. лет, — неизвестно.
Необходимо отметить в этой связи, что моделирование изменения радиуса Земли приводит к интересным результатам. Все материки и острова сходятся в единый материк, идеально сопрягаясь по изгибам их современных контуров. Вопрос, что было на месте поверхности Земли, возраст которой оценивается малыми величинами, просто отпадает: этой поверхности просто не существовало, площадь поверхности Земли была значительно меньше.
Уважаемый barjer, объясните наконец факты, отсутствия проявления субдукции, сформулированные Ю. Чудиновым (см. выше), а также объясните природу различия геологического возраста различных мест земной поверхности.
Чудиновым (см. выше), а также объясните природу различия геологического возраста различных мест земной поверхности.Ответить
barjer Сергей Заикин 26.05.2007 18:49 Ответить
Здравствуйте, Сергей! Начну с объяснения малого по сравнению с материковой возраста пород океанического дна. Вода, как известно, обладает малой теплопроводностью, которая меньше, чем у твердых пород. Поэтому охлаждение магматических масс под океанами происходит медленнее, чем в районах рифтовых зон, где толщина твердых пород коры к тому же наименьшая. Оседание краев плит в рифтовых зонах происходит существенно быстрее, чем в серединных зонах тектонических плит. Дело в том, что более горячая магма под середиными областями плит как бы подпирает эти области плит. В результате в этих районах происходит «разламывние» плиты. Именно в этих районах фиксируются напряжения растяжения.
 Кстати, эти процессы наблюдаются не только в серединных областях океанических плит. Те же процессы приводят к появления растягивающих напряжений в середине евроазиатской плиты в районе Байкала. Эти данные есть в уже цитированных мной литературных источниках.
Кстати, эти процессы наблюдаются не только в серединных областях океанических плит. Те же процессы приводят к появления растягивающих напряжений в середине евроазиатской плиты в районе Байкала. Эти данные есть в уже цитированных мной литературных источниках.В серединных областях материковых плит кристаллизация застывающей магмы происходит и сейчас на больших глубинах — порядка 40 — 100 км и больше. Возраст же поверхностных пород существенно больше, поскольку они кристаллизовались раньше. В океанических же областях, где толщина плит существенно меньше — порядка 7-10 км, ее кристаллизация происходит, хотя и медленно, но ближе к поверхности. Поэтому и возраст этих пород меньше, чем у осадочных материковых. Кстати, скорости субдукции и роста океанических пород примерно одинаковы, что говорит о достаточной синхронности тех и других процессов. Утверждение о том, что «поверхность Земли была существенно(!) меньше», не подтверждается расчетами скорости субдукции и, как кажется, «раздвижения», а на самом деле растрескивания плит.
 Не следует также забывать, что водные пространства на Земле могли появиться только после образования сплошной твердой поверхности. Более того,после того, как произошли основные процессы формирования земного рельефа. В противном случае вода просто испарялась бы, соприкасаясь с расплавленной массой магмы. Эти процессы, кстати, наблюдаются и сейчас там, где толщина твердых пород мала, например, в районе Исландских островов и в некоторых районах Тихого океана, где не редки подводные извержения. Правда, в существенно меньших масштабах.
Не следует также забывать, что водные пространства на Земле могли появиться только после образования сплошной твердой поверхности. Более того,после того, как произошли основные процессы формирования земного рельефа. В противном случае вода просто испарялась бы, соприкасаясь с расплавленной массой магмы. Эти процессы, кстати, наблюдаются и сейчас там, где толщина твердых пород мала, например, в районе Исландских островов и в некоторых районах Тихого океана, где не редки подводные извержения. Правда, в существенно меньших масштабах.Теория первобытного субматерика Гондваны на самом деле не подтверждается расчетами скорости субдукции и роста океанической коры. Зато расчеты сжатия литосферы, учитывающие теплопроводность пород литосферы и океана, с учетом притока тепла от Солнца, достаточно точно соответсвуют скорости субдукции.
По поводу эфира, который, как Вы говорите, есть «физический вакуум, который обладает внутренней энергией-импульсом». Назовите хотя бы один эксперимент, в котором был обнаружен это «физический вакуум»? А ведь если бы он обладал импульсом, не составило бы труда его обнаружить.
 Тем более, если он каким-то образом «преобразуется в форму массы». Так что привлекать этот феномен в качестве элемента теории, по крайней мере не корректно, разве что в гипотезах. Но ведь и в них хорошо бы оперировать не фантастическими, а не слишком противоречащими здравому смыслу физическими свойствами этого «вакуума».
Тем более, если он каким-то образом «преобразуется в форму массы». Так что привлекать этот феномен в качестве элемента теории, по крайней мере не корректно, разве что в гипотезах. Но ведь и в них хорошо бы оперировать не фантастическими, а не слишком противоречащими здравому смыслу физическими свойствами этого «вакуума».Ответить
Сергей Заикин barjer 29.05.2007 13:01 Ответить
В Вашем ответе факты, приведенные Ю.В. Чудиновым, вновь оставлены без внимания. Напомню их: Почему в зоне предполагаемой субдукции возраст плиты возрастает при удалении от впадины в сторону океана, почему нет сгруживания осадков при субдукции, почему толщина осадков вблизи впадины меньше, чем в среднем в океане, почему тепловой поток в зоне субдукции превышает средний. Или все это выдумки Чудинова?
И еще один вопрос: что было на месте океанического дна, возраст которого оценивается в 0 — 180 млн лет, в эпоху, скажем, 400 млн лет назад?
То, что версия объяснения расширения Земли с помощью эфира является всего лишь гипотезой, не является доказательством истинности других гипотез.
Ответить
mihan41 Сергей Заикин 02.10.2007 22:26 Ответить
Уважаемый Сергей. В свою очередь тоже отвечу на акцентированным Вами вопросы Ю. В. Чудинова.
Во-первых оговорюсь, что плитную тектонику я воспринимаю лишь в принципе, то есть земная кора имеет мощное конвеерное горизонтальное движение и конечно же имеют место в меньших масштабах и вертикальные движения. Основная сила которая движет Земную кору является тангенциальной составляющей гравитационной силы и направлена она от эклиптического полюса на эклиптический экватор.
Земные вещества имеют эклиптическое вращение. Земная Кора начала оствать с полюсов. Материки образовались там же и в последующем покрылись материковым оледенением… Как видите сценарий длинный и совсем другой и на все Ваши вопросы Вы найдете ответ в космогеодинамической теории Исаева С. М.Ответить
Сергей Заикин mihan41 04.
 10.2007 09:18
Ответить
10.2007 09:18
ОтветитьВ науке установлено, что новая теория побеждает тогда, когда оказывается способной объяснить те явления, которые старые теории объяснить не способны.
У меня нет ничего против того, чтобы Вы разделяли теорию Исаева. Однако Ваша реклама теории Исаева мне неинтересна.
Продемонстрируйте работоспособность и действенность рекламируемых идей на практике и объясните:
1. Почему нет сгруживания осадочных пород в желобах на месте предполагаемой субдукции?
2. Что было 150 миллионов лет назад на том месте земной поверхности, возраст основания дна которого сейчас оцениватся в 100 миллионов лет?Ответить
mihan41 Сергей Заикин 04.10.2007 12:43 Ответить
уважаемый Сергей. Глубоководные океанические желоба как правило не являются зонами субдукции в смысле понимания традиционных мобилистов.
 К примеру, Марианская впадина возникла в эпоху Ларамийской складчатости и причиной явилось катастрофическое материковое столкновение 2-ух Америк. После чего центр инерциальных масс континентов переместился из-за появления точки опоры. Континенты провернулись к динамическому равновессию и появились такие глобальные структуры как Марианская вп. Другие глубоководные желоба происходили также из-за главной причины, как реализация действия тангенциальных сил Земли, в частности касательной силы имеющей гравитационную природу. К примеру, океанические желоба обрамляющие Карибский бассейн с востока и запада образовались за счет движения вторичных структур, так называемых клиновидных мегаблоков.Эти мегаблоки вытеснялись в сторону пассивных зон широтного растяжений. Кстати, знаменитый разлом Сан-Андреас как раз является диагональной разломной границей одного из мегаблоков отсеченной из головной части североамериканского материка. ** продолжу в сл. сообщении.
К примеру, Марианская впадина возникла в эпоху Ларамийской складчатости и причиной явилось катастрофическое материковое столкновение 2-ух Америк. После чего центр инерциальных масс континентов переместился из-за появления точки опоры. Континенты провернулись к динамическому равновессию и появились такие глобальные структуры как Марианская вп. Другие глубоководные желоба происходили также из-за главной причины, как реализация действия тангенциальных сил Земли, в частности касательной силы имеющей гравитационную природу. К примеру, океанические желоба обрамляющие Карибский бассейн с востока и запада образовались за счет движения вторичных структур, так называемых клиновидных мегаблоков.Эти мегаблоки вытеснялись в сторону пассивных зон широтного растяжений. Кстати, знаменитый разлом Сан-Андреас как раз является диагональной разломной границей одного из мегаблоков отсеченной из головной части североамериканского материка. ** продолжу в сл. сообщении.Ответить
mihan41 Сергей Заикин 04.
 10.2007 13:05
Ответить
10.2007 13:05
ОтветитьИмеет ли основание быть в реальности механизм субдукции.Судя по присутствию зеленокаменных офиолитовых поясов в геол. разрезах Земли, да, но значительно в меньших планетарных масштабах. Они связаны скорее всего не движениями консолидированных континентов, а дрейфом самой океанической коры. Океан кора, судя по результатам уникальных по масштабу комплексных геолого-геофиз. исследований силами 2-ух НПО,»Севморгео» и «Южморгео», в начале 80-х годов в экваториальной Атлантике, не ведет себя как жесткая консолидированная Земная кора, а подвержена тафрагенезу. Нам удалось гравиметрическими методами обнаружить образующуюся аномальную мантию имеющее большое широтное простирание. Простыми словами, океаническая кора все время изчезает и подновляется, по широтным зонам изливается ан. мантия погребая собой накопившийся тонкий слой пелагических осадков и в последующем их растапливая. В результате происходит порция дрейфа всей океанической коры и размягчившаяся трансформная зона сужаясь закрывается.

Как видите, мы опираемся на более продвинутые представления и такой проблемы как неминуемое накопление отвала из задранных осадков для нас не существует. *** продолжение следует.Ответить
mihan41 Сергей Заикин 04.10.2007 13:59 Ответить
До конца палеозойской эры на Земле царила весьма своеобразная эпоха вращения, т.е. не был годовой климатический цикл. В это время материки достаточно прочно консолидировались на полюсах и покрылись даже материковым оледенением. В начале мезозоя южный материк раскололся и начал перемещаться расколовшимися частями к экл.экватору, что привело к выходу из равновессия кинематики вращения внешней сферы Земли (литосферы). По хронологии эк.эп. З. простирается от самого образования Земли до 230 млн. лет. Представляю себе во времена 150 млн. лет назад вторую катастрофу — кат.раскола северного материка на фоне продолжающихся последствий от 1-ой катастрофы, в том числе продолжение процесса постоянного омоложения океанической коры.

Ответить
Сергей Заикин mihan41 04.10.2007 16:02 Ответить
Исследования показывают, что в районе срединных океанических хребтов возраст основания дна имеет минимальное значение и при удалении от хребта возраст дна возрастает так, что одновозрастные участки располагаются симметрично по обе стороны от него. Эти факты позволили сделать выводы, что срединные океанические хребты являются местом расхождения литосерных плит.
Ваше утверждение о постоянном омолаживании океанической коры вообще непонятно. Невозможно сделать из коры с возрастом 10 миллионов лет кору с возрастом 5 миллионов лет.
Расходящиеся в срединных хребтах плиты при постоянном размере Земли с неизбежностью должны наползать друг на друга с другой стороны плит, либо превращаться в гарможку где-то посредине.
Если же наползания (субдукции) и гарможки нет, то значит размеры Земли увеличиваются.
Ответить
mihan41 Сергей Заикин 04.10.2007 21:07 Ответить
Уважаемый Сергей. Данные палеомагнитных исследований океана я тоже считаю корректными. Вся проблема в том, что теория Вегенера в части интерпретации ситуации в районе Атлантического океана была не правильной. Интуитивно прав был прешедственник Вегегера американский геолог Тейлор, предположив, что материки двигаются в сторону экватора. К сожалению, аргументы Вегенера были более в свое время убедительными и научное сообщество пошло в этом направлении и в результате мы имеем тот круг проблем, которые Вы и сами знаете мобилисты решить не могут.
Ответить
mihan41 Сергей Заикин 04.10.2007 21:33 Ответить
Уважаемый Сергей. Представте себе на минуту, что Тейлор прав и Исаев тоже в части того, что материки образуются на полюсах и достаточная тангенциальная сила движет их по меридиану к экватору.
 Материк, который покрывает лишь макушку Земли не может растекаться в расширяющиеся широты шарообразной Земли не лопнув на части. И эти части пассивно расходятся друг от друга по мере движения в более низкие широкие широты. Таким образом, мы приходим к гениальному и простому выводу, что широтнй Атлантический хребет планетарного масштаба являет собой лишь пасивное образование. Мобилисты должны отказываться от своих конструкций как от элементарно ошибочных. Это не сложно делать, мало ли, пробы должны быть. Эти ошибки закономерны, так как им неизвестна была та сила, которая открылась Исаеву.
Материк, который покрывает лишь макушку Земли не может растекаться в расширяющиеся широты шарообразной Земли не лопнув на части. И эти части пассивно расходятся друг от друга по мере движения в более низкие широкие широты. Таким образом, мы приходим к гениальному и простому выводу, что широтнй Атлантический хребет планетарного масштаба являет собой лишь пасивное образование. Мобилисты должны отказываться от своих конструкций как от элементарно ошибочных. Это не сложно делать, мало ли, пробы должны быть. Эти ошибки закономерны, так как им неизвестна была та сила, которая открылась Исаеву.
Сергей согласитесь, если мобилисты ошиблись в своих конструкциях, это вовсе не значит, что размеры Земли должны увеличиваться.
Что касается теории Ярковского-Блинова, считаю ее не перспективной. Не уверен, что баланс между эфирными частями материи консервирующимися Землей и покидающими ее нарушен. Не там надо искать.Ответить
mihan41 Сергей Заикин 05.
 10.2007 21:22
Ответить
10.2007 21:22
ОтветитьМожно ли делать из коры возрасьом 10 млн. лет кору с возрастом 5 млн. лет? Представте себе, как получают из многокилометровой глубины ориентированные в пространстве образцы для палеомагнитных исследований. Один раз получили искомый возраст и этому рады. Близ срединно-Атлантического хребта удача улыбается чаше, а что делать в районе Ангольского талассакратона(Англьская глубоководная котловина)? Вы не найдете там скважину, которая добурилась бы до коренных пород. И еще. Речь все таки идет о постепенной утрате океаном старой коры по постоянно возникающим трансформным зонам. Прошло каких то 100 млн. лет (цифра взята из Вашего вопроса) и нам не удалось найти ничего старше указанного Вами возраста. За это время океаническая кора полностью обновилась. Образование новой коры по рифтовым зонам срединных хребтов происходит в ходе пассивного их раскрытия, также новая кора должна возникать и в высоких широтах. К сожалению, там проведены недостаточно подобных исследований в силу самых различных причин.

Ответить
Сергей Заикин barjer 18.06.2007 09:26 Ответить
Здравствуйте, barjer!
В Вашей фразе «скорости субдукции и роста океанических пород примерно одинаковы» непонятно, что такое «рост океанических пород».
Видимо в тексте пропущен растущий параметр. Без указания этого параметра значимость утверждения о скорости субдукции ничтожна. Кроме того, такие характеристики, как геологический возраст основания океанического дна, а также толщина осадочных пород, имеют обратную (для субдукции) динамику изменения при удалении от предполагаемого места субдукции в сторону океана, что говорит, скорее, о наличии эдукции (раздвижения) плит, чем субдукции. Может быть скорость и соответствует, только знак противоположный.
Кстати, конкретных фактов, подтверждающих само явление субдукции, в рамках настоящей дискуссии почему-то не приведено. Указывается лишь, что таких свидетельств множество. Но где хотя бы одно из них?
Указывается лишь, что таких свидетельств множество. Но где хотя бы одно из них?
+++++
Поэтому и возраст этих пород меньше, чем у осадочных материковых.
+++++
Вопрос-то ставится совсем другой. Не почему возраст одних пород больше или меньше других, а что было на месте земной поверхности «до того», например, если нынешние оценки возраста основания дна составляют 120 млн лет, что было в этом месте Земли 130 млн лет?Ответить
century Сергей Заикин 04.06.2007 05:27 Ответить
С точки зрения современных открытий, во вселенной доминирует вакуум, который отвечает за антигравитацию. Из наблюдений обнаружено, что на больших расстояниях все галактики удаляются друг от друга (1929г Хаббл). Недавние наблюдения показали, что это удаление происходит с ускорением(1998г A.G.Riess S.Perlmutter ).
В следствии чего в уравнения Эйнштейна вернулась так называемая космологическая постоянная, которая отвечает за антигравитацию. 6 м)
6 м)
также можно получить ежегодное расширение земли (порядка 0,46 мм в год.)
Как не странно такие данные были указаны в книгах у У.Керри и у P.Jordan «the expanding earth»
правда наблюдательных данных по расширению Земли найти пока не удалось. Видимо пока еще нет такой точности современных приборов. Если кто-нибудь встречал, то буду премного благодарен.Ответить
Alexis 27.05.2007 16:28 Ответить
Смены объяснений причин извержений вулканов служит наглядными примерами перехода простых чувственно-эмоциональных восприятий видимого мира вулканизма в голове человека во все более сложные и вымышленные (нелепые). Красота и совершенство реального мира механизма вулканической деятельности людьми, к сожалению, пока не востребована.
Видимый мир, или вымысел: вулканизм вызван подъемом нагретого глубинного вещества
Наблюдая излияние из вулканов лавы, человек делает однозначный вывод: раз лава поднимается из недр литосферы, они раскалены. По-другому, и быть не может. Но вот несколько примеров, показывающих, что так в естествознании думать ненаучно. Солнце закрылось темным облаком, и пошел град. Что, облако состоит из градинок? Нет, из капелек воды! Из трубы котельни выходит дым. Что, в котле ее дым? Нет, там каменный уголь, мазут, дрова, а дым образуется при неполном их сгорании. Из попы человека выходят какашки. Что, человек сложен какашками? Нет, они формируются в желудке и кишках при переваривании пищи. Может быть, и лава возникает при преобразовании горных пород?
По-другому, и быть не может. Но вот несколько примеров, показывающих, что так в естествознании думать ненаучно. Солнце закрылось темным облаком, и пошел град. Что, облако состоит из градинок? Нет, из капелек воды! Из трубы котельни выходит дым. Что, в котле ее дым? Нет, там каменный уголь, мазут, дрова, а дым образуется при неполном их сгорании. Из попы человека выходят какашки. Что, человек сложен какашками? Нет, они формируются в желудке и кишках при переваривании пищи. Может быть, и лава возникает при преобразовании горных пород?
Убежденность, без всяких на то оснований, в наличии глубинной энергии позволило создать следующее общепринятое представление о причинах и механизме вулканизма.
Ни малейшей доли научности в вышеприведенном представлении причин и механизма вулканической деятельности нет. Сплошные нелепицы, или вымышленный мир.
Отсутствие глубинной энергии
Нет ни одного доказательства наличия глубинной энергии, а отсутствия ее — многочисленные.
1. При проходке с XVI в. шахт было установлено, что с погружением в недра Земли температура постепенно растет. Появилось понятие геотермического градиента — роста температуры при опускании на 100 м. В среднем по планете он принимается 30 С. Естественно, считалось, что увеличение температуры с глубиной вызвано поступлением глубинного тепла. Поэтому, чем глубже погружаться, тем больше будут значения геотермического градиента. Реальность же оказалась противоположной.
шахт было установлено, что с погружением в недра Земли температура постепенно растет. Появилось понятие геотермического градиента — роста температуры при опускании на 100 м. В среднем по планете он принимается 30 С. Естественно, считалось, что увеличение температуры с глубиной вызвано поступлением глубинного тепла. Поэтому, чем глубже погружаться, тем больше будут значения геотермического градиента. Реальность же оказалась противоположной.
Температура горных пород с глубиной действительно возрастает, но не прогрессивно, а регрессивно, замедляясь. Чем глубже погружаться, тем прирост температуры меньше. С позиции здравого смысла такого быть не может. Но наука оперирует реально существующими фактами, а не представлениями.
2. Прямые замеры температур в глубоких скважинах свидетельствуют сначала о росте температур, а затем устойчивом понижении. Аналогичные данные получены и при бурении Кольской сверхглубокой скважины, углубленной более чем на 12 км. Значения теплового потока в ней сначала увеличивались, а с глубины 5 км резко снизились с последующим стабильным уменьшением.
3. Фактическое распространение горных пород в наблюдаемой части литосферы со сменой аморфных с глубиной все более крупнокристаллическими запрещает предполагать наличие глубинной энергии. При кристаллизации и перекристаллизации с увеличением размера кристаллов тепло из вещества выделяется, или энергонасыщенность уменьшается.
4. Наличие атмосферы, гидросферы, биосферы и находящейся под ними литосферы свидетельствует о том, что энергия на Землю поступает из Космоса, а не поднимается из ее недр.
Трещина не может понизить давление на глубине, потому что массу не уменьшает
Отсутствие глубинной энергии делает ненужным дальнейший анализ общепринятого механизма вулканизма. Чтобы показать абсурдность его в целом, предположим (хотя этого и нет), что глубинное вещество высоко нагрето, но твердое. Как перевести его в расплавленное состояние? Ответ один: нужно уменьшить давление. Предлагается это делать с помощью трещины от землетрясения.
1. Наличие районов, где происходят землетрясения, но нет действующих вулканов (материк Австралия, Китай, Сахалин и др. ), тем более районов активного вулканизма, но асейсмичных (материк Антарктиды, острова Канарские, Сейшельские, Гавайские и др.) свидетельствуют о том, что трещины для извержений вулканов не нужны.
), тем более районов активного вулканизма, но асейсмичных (материк Антарктиды, острова Канарские, Сейшельские, Гавайские и др.) свидетельствуют о том, что трещины для извержений вулканов не нужны.
2. Давление на глубинное вещество вызвано массой вышележащих горных пород. Трещина, разбив виртуальной массив (на самом деле каменная оболочка едина) на две глыбы, массу вещества уменьшить не может. Чтобы сократилась масса и уменьшилось давление на глубине, надо убрать с поверхности литосферы покрышку из горных пород толщиной несколько километров. Ничего подобного на Земле не происходит.
3. Зияющая трещина на глубине десятков километров образоваться и существовать не может.
Так что, если бы на глубине и были твердые высоконагретые породы, перевести их локально в расплавленное состояние было бы невозможно. Магма образоваться не может.
Магма при подъеме остынет
Но предположим вообще невероятное, что при отсутствии глубинной энергии трещина уменьшила давление, и возникла изолированная порция магмы. Поднимаясь вверх и контактируя с менее нагретыми окружающими породами, согласно второму началу термодинамики, магма обязана нагревать эти породы, охлаждаясь, сама. Начнется ее кристаллизация. Вязкость возрастет, подъем прекратится. Как Вы отнесетесь к человеку, утверждающему, что в комнате с температурой 20 град. С он поставил ведро горячей 90 град. С воды. Температура воды в ведре не изменится через час. Но ведь то же самое происходит и с магмой.
Поднимаясь вверх и контактируя с менее нагретыми окружающими породами, согласно второму началу термодинамики, магма обязана нагревать эти породы, охлаждаясь, сама. Начнется ее кристаллизация. Вязкость возрастет, подъем прекратится. Как Вы отнесетесь к человеку, утверждающему, что в комнате с температурой 20 град. С он поставил ведро горячей 90 град. С воды. Температура воды в ведре не изменится через час. Но ведь то же самое происходит и с магмой.
При дегазации магма остынет и не сможет стать лавой
Из вулканов изливается лава, а не магма. Лава — это магма, лишенная летучих веществ: паров воды и газов. Даже если бы магма и была, дегазация ее, или уменьшение в ней содержания наиболее энергонасыщенной газовой доли привела бы к охлаждению расплавленной массы. Из магмы с температурой близкой к началу ее кристаллизации лава теоретически образоваться не может. Это очередной вымысел!
Объяснение вулканизма с помощью магмы — пример вечного двигателя второго (теплового) типа
Но лава все же поднимается, без охлаждения, к поверхности литосферы и там вызывает извержение вулкана. Температура лавы в изливающемся потоке по прямым замерам не менее 1200 С, или такая же, что и при возникновении магмы. Это пример вечного двигателя второго (теплового) типа, когда не учитываются потери тепла при теплопроводности вещества. Вечный двигатель первого (механического) типа воображается без потерь энергии от трения. Ни одна академия наук не принимает проекты вечных двигателей, а вулканизм объясняется с его помощью, и нелепости этой люди не замечают.
Температура лавы в изливающемся потоке по прямым замерам не менее 1200 С, или такая же, что и при возникновении магмы. Это пример вечного двигателя второго (теплового) типа, когда не учитываются потери тепла при теплопроводности вещества. Вечный двигатель первого (механического) типа воображается без потерь энергии от трения. Ни одна академия наук не принимает проекты вечных двигателей, а вулканизм объясняется с его помощью, и нелепости этой люди не замечают.
Вымыслы относятся не только к содержанию физической стороны общепринятого представления механизма и причин вулканизма, но и химии.
Магма не расплав, а раствор
Прежде всего, магма на всем пути своего длительного подъема и контакта с вмещающими породами иного состава не меняет своего химического состава. Как была базальтовой при возникновении в верхней мантии, такой и изливается на поверхность литосферы. Объяснение этому видится в том, что магму называют расплавов, хотя она таковым не является.
Расплав, по физической химии, — это индивидуальное стехиометрической вещество в жидком состоянии, кристаллизующееся при температуре плавления. В естествознание понятие ‘расплав’ не пользуется уважением, не востребовано, поэтому, например, в БСЭ третьего издания такое слово отсутствует.
В естествознание понятие ‘расплав’ не пользуется уважением, не востребовано, поэтому, например, в БСЭ третьего издания такое слово отсутствует.
Индивидуальное, означает чистое вещество. Железо в расплавленном состоянии — это расплав. Но стоит в него попасть немного углерода, оно станет жидким раствором углерода в железе: сталью или чугуном. Остынув, сталь или чугун будет твердым раствором углерода в железе. А так как в природе нет чистых веществ, то нет и расплавов. Даже хлорид натрия в расплавленном состоянии (жидком, но без участия воды) будет расплавом только в том случае, если соотношение катионов натрия к анионам хлора точно соответствует 50:50 (соблюдение требования стехиометрии), чего в реальности не бывает. Расплав, в отличие от раствора, всегда сохраняет свой химический состав постоянным. Для раствора это не применимо.
Магму, как сложное силикатное вещество, к тому же содержащее пары воды и газы, нельзя называть расплавом. Это, по химии, высоконагретый жидкий раствор. Поэтому химический состав его при подъеме обязательно должен был бы изменяться. Следовательно, по химическому составу лавы нельзя было бы говорить о химическом составе магмы в верхней мантии, даже если бы магма и возникала.
Следовательно, по химическому составу лавы нельзя было бы говорить о химическом составе магмы в верхней мантии, даже если бы магма и возникала.
Из базальтовой лавы получить слоистую оболочку среднего состава невозможно
Из верхней мантии, по современной геологии, поднимается базальтовая магма, становящаяся затем лавой того же состава. Ничто иное, кроме небольших порций магмы ультраосновного состава, глубины земного шара не покидает. На поверхности литосферы базальт и его туфы разрушаются, что приводит к формированию реально наблюдаемой слоистой оболочки из слоев аргиллитов, песчаников, известняков и других пород. Спрашивается, каким будет химический состав вещества слоистой оболочки, если он образуется из базальта? Ответ только один: базальтовым. Но он другой!
Химические составы базальта и слоистой оболочки существенно различаются. Состав базальта основной, а слоистой оболочки — средний. В базальте больше глинозема, оксидов железа. Оксида магния больше чем в 2,5 раза, оксида кальция — в 3 раза, оксида натрия — в 2 раза. В то же время кремнезема и оксида калия в базальте меньше, чем в веществе слоистой оболочки. Ничего подобного не могло быть, если вещество слоистой оболочки формировалось за счет базальта.
В то же время кремнезема и оксида калия в базальте меньше, чем в веществе слоистой оболочки. Ничего подобного не могло быть, если вещество слоистой оболочки формировалось за счет базальта.
Получается, базальт в образовании химического состава слоистой оболочки участия не принимает, или первичная базальтовая магма (лава) на поверхность каменной оболочки земного шара не поднимается. Из общепринятого представления причин вулканизма выходит: из глубины поступает гречневая крупа (базальт), из которой на поверхности при гипергенезе приготавливается манная каша (слоистая оболочка). Это — вымысел!
Как же такое вымышленное представление о вулканизме сформировалось?
В.М. Дуничев
Ответить
Alexis 27.05.2007 16:30 Ответить
История взглядов на причины вулканизма
Все неизвестное у человека вызывает страх, дискомфорт. Выяснив неясное, человек чувствует облегчение, и не имеет значение, научное это объяснение или нет. Величие вулканов и мощь вулканических извержений всегда свидетельствовали человеку о могуществе природы, побуждая выяснить причину этого грозного явления.
Величие вулканов и мощь вулканических извержений всегда свидетельствовали человеку о могуществе природы, побуждая выяснить причину этого грозного явления.
Что думали о вулканах древние греки и римляне?
На раннем этапе истории человечества, когда люди еще не отделяли себя от природы (не называли себя Homo sapiens), одухотворенным (живым) воспринимался весь окружающий мир. Духи были добрыми и злыми. Последних обычно помещали под землю, в связи с чем сложилось представление о страшном, пугающем подземном мире. Добрые духи обитали на небе, откуда приходили солнечное тепло и живительная сила дождя. Помимо событий повседневной жизни обожествлялись и могущественные явления природы, такие как извержения вулканов и землетрясения. Постепенно возникали и затем длительное время существовали различные мифы, в которых не только отражались грозные природные явления, но и делались попытки еще наивного (непосредственного) их объяснения.
Почти 10 тысяч лет назад Гомер рассказывал о встрече Одиссея с циклопом — громадным истуканом с горящим глазом, вставленным в лоб. В гневе циклоп швыряет огромные глыбы, производя страшный грохот. Кого напоминает циклоп? Да, это вулкан со светящимся на вершине кратером, из которого с шумом вылетают вулканические бомбы.
В гневе циклоп швыряет огромные глыбы, производя страшный грохот. Кого напоминает циклоп? Да, это вулкан со светящимся на вершине кратером, из которого с шумом вылетают вулканические бомбы.
Познакомимся с древнегреческим мифом ‘Борьба богов-олимпийцев с титанами’. Сначала существовал лишь вечный безграничный темный Хаос. Из него возникли мир и бессмертные боги, в том числе богиня Земли — Гея. В неизмеримой глубине под землей родился мрачный Тартар — ужасная бездна, полная вечной тьмы.
Могучая Земля породила беспредельное голубое небо — Урана. Уран взял себе в жены Гею. У них родились шесть сыновей и шесть дочерей — могучие и грозные титаны. Еще Гея породила трех великанов — циклопов, и трех громадных, как горы, сторуких великанов — гекатонхейров. Невзлюбил Уран своих детей-великанов и заключил их в глубокий мрак Тартара в недра богини Земли. Один из сыновей Урана, Крон, хитростью низверг своего отца и отнял у него власть. В свою очередь, сын Крона, Зевс, когда вырос и возмужал, восстал против деспотии своего отца. Вместе с другими детьми Крона Зевс начал борьбу с отцом и титанами за власть над миром. На помощь Зевсу пришли циклопы, выковавшие ему громы и молнии, которые он метал в титанов.
Вместе с другими детьми Крона Зевс начал борьбу с отцом и титанами за власть над миром. На помощь Зевсу пришли циклопы, выковавшие ему громы и молнии, которые он метал в титанов.
Борьба длилась десять лет, но победа не приходила ни к одной из сторон. Тогда Зевс освободил из недр сторуких великанов — гекатонхейров. Выйдя из недр земли, они отрывали от гор целые скалы и бросали их в титанов. Грохот наполнил воздух, земля стонала, все кругом колебалось. Даже Тартар сотрясался от этой борьбы. Зевс метал свои огненные молнии и рокочущие громы. Всю землю охватил огонь, дым и смрад заволокли все густой пеленой.
Не выдержали, дрогнули титаны. Сила их была сломлена. Зевс с богами Олимпа сковали их и низвергли в мрачный Тартар, поставив у ворот стражу из гекатонхейров, чтобы не вырвались на свободу могучие титаны.
Гея разгневалась на Зевса за столь жестокую участь своим побежденным детям — титанам. Вступив в брак с Тартаром, она произвела на свет ужасное стоголовое чудище — Тифона. Горой поднялся он из недр Земли, диким воем содрогая воздух. Яркое пламя клубилось вокруг Тифона. Под его тяжелыми ногами колебалась сама земля. Но Зевса не устрашил вид Тифона. Он вступил с ним в бой, выпуская свои огненные стрелы и раскаты грома. Земля и небесный свод сотрясались до основания. Ярким пламенем вспыхнула земля, как и во время борьбы с титанами. Моря кипели от одного приближения Тифона. Сотнями сыпались огненные стрелы-молнии громовержца Зевса. Казалось, от их огня горят даже воздух и темные грозовые тучи.
Яркое пламя клубилось вокруг Тифона. Под его тяжелыми ногами колебалась сама земля. Но Зевса не устрашил вид Тифона. Он вступил с ним в бой, выпуская свои огненные стрелы и раскаты грома. Земля и небесный свод сотрясались до основания. Ярким пламенем вспыхнула земля, как и во время борьбы с титанами. Моря кипели от одного приближения Тифона. Сотнями сыпались огненные стрелы-молнии громовержца Зевса. Казалось, от их огня горят даже воздух и темные грозовые тучи.
Зевс испепелил все сто голов чудовища. Рухнул Тифон на землю. От тела его исходил такой жар, что плавилось все кругом. Зевс поднял тело Тифона и низверг его в Тартар. Но и оттуда грозит еще Тифон богам и всему живому. Он вызывает бури и извержения.
Очень образно в мифе описано извержение сначала пирокластического материала, а затем и излияние лавы.
Со времен древних римлян в сознании людей утвердились основные термины, характеризующие вулкан и саму вулканическую деятельность: пепел, шлак, потухший вулкан, вулканический очаг и другие. Древние римляне по конической форме с отверстием наверху, из которого выходит дым и пепел, изливается лава, видели в вулкане громадную кузницу. Внутри ее работает бог-кузнец — Вулкан. В кузнице, как известно, есть очаг. Твердыми продуктами горения являются пепел или зола и шлаки, оплавленные тугоплавкие остатки. Кузница бывает действующей и потухшей.
Древние римляне по конической форме с отверстием наверху, из которого выходит дым и пепел, изливается лава, видели в вулкане громадную кузницу. Внутри ее работает бог-кузнец — Вулкан. В кузнице, как известно, есть очаг. Твердыми продуктами горения являются пепел или зола и шлаки, оплавленные тугоплавкие остатки. Кузница бывает действующей и потухшей.
Объяснение механизма вулканической деятельности горением в близповерхностных пустотах горючих веществ
С окончанием мифологического восприятия окружающего мира началось время логоса, когда по наблюдаемым явлениям делались логически выдержанные заключения. Древние греки, исходя из широкого развития на их территории пещер, воронок и углублений — проявления карста, считали Землю пронизанную на глубине пустотами и соединяющими их каналами. По пустотам циркулируют воздух, вода и огонь. Движения воды и воздуха сотрясают поверхность Земли, вызывая землетрясения. Огонь, движущийся по пустотам и каналам, при прорыве на поверхность приводит к извержению вулканов.
Древние греки считали мир таким, каким его видели. Знания о любом предмете соответствуют сути самого предмета. Мир везде одинаков. Такие представления послужили основой создания чувственно-наглядных образов видимого мира природы.
Энциклопедическое описание мира с этих позиций дано Аристотелем (384-322 гг. до н. э.). Он принимал движущей силой извержения вулканов сжатый в глубине Земли воздух, выбрасывающий золу (пепел) и поднимающий лаву.
Не подходя близко к действующему вулкану, древние греки видели, особенно ночью, выбросы из него огня. На самом деле выбрасывается раскаленный пепел. Если ветер дул от вулкана, то чувствовался специфический запах, принимавшийся за запах серы, вернее, горящей серы. С тех пор утвердилось представление, что суть вулканизма в выходе огня из кратера. Считалось, что горели сера или асфальт (горючая земля).
Обычно считается, что Помпеи и другие города и виллы в 79 г. были засыпаны продуктами извержения вулкана Везувий. Но такого вулкана тогда не было. Была гора Сомма, не принимавшаяся за вулкан, потому что на памяти людей извержений ее не было. После катастрофического извержения Соммы в 79 г. на вершине ее образовалась кальдера. В этой кальдере через 93 г. произошло следующее извержение, в результате которого появился конус, названный Везувием, почти полностью перекрывший в настоящее время Сомму. Полное название вулкана близ Неаполя — Сомма-Везувий (Монте-Сомма-Везувий).
Была гора Сомма, не принимавшаяся за вулкан, потому что на памяти людей извержений ее не было. После катастрофического извержения Соммы в 79 г. на вершине ее образовалась кальдера. В этой кальдере через 93 г. произошло следующее извержение, в результате которого появился конус, названный Везувием, почти полностью перекрывший в настоящее время Сомму. Полное название вулкана близ Неаполя — Сомма-Везувий (Монте-Сомма-Везувий).
С тех пор до начала XIX в. считалось, если найди причину выхода огня из кратера, можно объяснить механизм вулканизма. Например, в 1684 г. М. Листер сформулировал гипотезу, по которой деятельность вулканов вызывалась воспламенением в земных недрах под действием морской воды серного колчедана (с современных понятий при окислении пирита — FeS2).
В 1700 г. ее экспериментально подтвердил профессор химии Сорбонского университета в Париже Н. Лемери (1645-1715) моделированием извержения вулкана путем самовозгорания смеси из увлажненной серы и железных опилок. Он приготавливал при публике в своем саду смесь из серы, железных опилок и воды и просил даму зарыть смесь в землю. Через определенное время смесь настолько сильно разогревалась, что появлялся небольшой конус, через разрывы в котором выходили языки пламени. Особый эффект опыт производил ночью — публика наблюдала извержение небольшого искусственного вулкана. Людям тогда казалось, что механизм вулканизма полностью выяснен. На этих же позициях объяснения сущности вулканизма стояли М.В. Ломоносов (1711-1765) и первый исследователь Камчатки С.П. Крашенинников (1711-1755). Как отмечал С.П. Крашенинников, по частым землетрясениям можно говорить о нахождении в недрах Камчатки пустот и горючего материала. Причина горения сопок виделась им в соприкосновении соленой морской воды, проникающей в глубины по трещинам, с рудами железа и горючей серы, что и приводило к воспламенению.
Через определенное время смесь настолько сильно разогревалась, что появлялся небольшой конус, через разрывы в котором выходили языки пламени. Особый эффект опыт производил ночью — публика наблюдала извержение небольшого искусственного вулкана. Людям тогда казалось, что механизм вулканизма полностью выяснен. На этих же позициях объяснения сущности вулканизма стояли М.В. Ломоносов (1711-1765) и первый исследователь Камчатки С.П. Крашенинников (1711-1755). Как отмечал С.П. Крашенинников, по частым землетрясениям можно говорить о нахождении в недрах Камчатки пустот и горючего материала. Причина горения сопок виделась им в соприкосновении соленой морской воды, проникающей в глубины по трещинам, с рудами железа и горючей серы, что и приводило к воспламенению.
Во второй половине XVIII в. и в самом начале XIX в. вулканизм объясняли горением пластов каменного угля. Обосновал это профессор Фрейбергской горной академии в Саксонии А.Г. Вернер (1750-1817) — основоположник первой в геологии гипотезы нептунизма.
Объяснения вулканизма поднятием глубинной энергии и вещества (излиянием лавы)
Наблюдения за действующими вулканами Южной Америки и Индонезии привели ученых в начале XIX в. к выводу, что сущность вулканизма не в выходе огня из кратера, а в излиянии лавы. Первым в этом удалось убедить людей немецкому естествоиспытателю А. Гумбольдту (1769-1859), обосновавшему глубинную природу вулканизма. В то время на вооружение науки была принята гипотеза Канта-Лапласа образования Земли из раскаленного огненно-жидкого шара. Остывая, земной шар покрылся корой охлаждения — земной корой, мощностью 10 миль, ниже которой сохранился первичный расплавленный материал базальтового состава. Сквозь трещины, рассекающие растрескивающуюся земную кору, расплав поднимается вверх, вызывая извержение вулкана. А. Гумбольдт делал вывод, что вулканические явления есть результат постоянной или временной связи между расплавленной внутренней частью и поверхностью земного шара. Сначала людям казались странными такие объяснения причин вулканизма, когда с древних греков было ясно, что это результат возгорания горючих веществ. Что преподавать студентам, как быть с учебниками? Но постепенно с ними согласились и стали считать их единственно возможными.
Что преподавать студентам, как быть с учебниками? Но постепенно с ними согласились и стали считать их единственно возможными.
Одной из обязательных черт, характеризующих науку, является приемлемость. Выражается это в том, что предыдущее объяснение должно входить составной частью в…
Ответить
Alexis 27.05.2007 17:10 Ответить
ПРОДОЛЖЕНИЕ… последующее. Если же новое объяснение игнорирует ранее существовавшее, то новое, как и старое представления нельзя называть научными знаниями. В данном случае сначала вулканизм объяснялся горением в поверхностных условиях горючих веществ, а затем — поднятием из глубин расплавленного материала. Никакой приемлемости не наблюдается. Следовательно, отношения к науке ни первое, ни второе представление не имеют.
Между тем, к середине XIX в. было выяснено, что расплавленных внутренностей Земли нет, а земная кора вообще не могла образоваться на расплавленном шаре. Дело в том, что остывшее твердое вещество имеет большую плотность (более тяжелое), чем расплавленное, в котором расстояния между атомами больше, чем в твердом кристаллическом. Если бы твердые глыбы и появлялись, они погружались бы вниз, и затвердевание планеты должно было бы начаться с центра. Земная кора, стало быть, исходно ложное, ненаучное представление. Потому этот термин мной и не употребляется, кроме как в исторических справках. Нужно говорить не ‘земная кора’, а литосфера — каменная оболочка. Не называют же водную оболочку конденсационной, а именуют гидросферой по слагающему веществу, исключая представления об ее происхождении.
Дело в том, что остывшее твердое вещество имеет большую плотность (более тяжелое), чем расплавленное, в котором расстояния между атомами больше, чем в твердом кристаллическом. Если бы твердые глыбы и появлялись, они погружались бы вниз, и затвердевание планеты должно было бы начаться с центра. Земная кора, стало быть, исходно ложное, ненаучное представление. Потому этот термин мной и не употребляется, кроме как в исторических справках. Нужно говорить не ‘земная кора’, а литосфера — каменная оболочка. Не называют же водную оболочку конденсационной, а именуют гидросферой по слагающему веществу, исключая представления об ее происхождении.
Кроме того, тогда же выяснилось, что приливы и отливы, возникающие под воздействием Луны и Солнца, проявляются не только в гидросфере, вызывая периодические колебания уровня моря, но и в твердой каменной оболочке. Незначительные колебания земной поверхности от таких приливов и отливов свидетельствовали о большой упругости вещества земного шара, что невозможно при жидком состоянии его недр. Если бы на расплавленной оболочке была твердая кора толщиной 10 миль, то она в течение суток периодически воздымалась бы и опускалась на несколько сантиметров, чего не наблюдается.
Если бы на расплавленной оболочке была твердая кора толщиной 10 миль, то она в течение суток периодически воздымалась бы и опускалась на несколько сантиметров, чего не наблюдается.
Окончательное доказательство твердости недр земного шара было получено начавшимися во второй половине XIX в. сейсмическими исследованиями. Было установлено, что упругие колебания, возникающие от тектонических землетрясений, как продольные, растяжения и сжатия, так и поперечные, типа сдвига, прослеживаются до глубин 3 тысяч километров, что было бы невозможно при наличии внутри Земли пояса расплавленного материала. Деформации типа сдвига, т.е. с нарушением сплошности среды, в жидкостях невозможны; они там гасятся. Почему? Потому что в жидкостях, тем более в газах, как аморфных высокоэнергонасыщенных веществах, атомы постоянно хаотично движутся с большими скоростями (в воздухе, например, при обычных условиях со скоростями несколько сотен метров в секунду) и не допускают возникновения пустоты.
Естествоиспытатели столкнулись с странной ситуацией: жидкого готового расплава в недрах земного шара нет, а вулканы достоверно изливают его, поднятого из глубины. Значит, думалось тогда, нужно придумать механизм получения на глубине расплавленного материала из твердого.
Значит, думалось тогда, нужно придумать механизм получения на глубине расплавленного материала из твердого.
Выход предложил Э. Рейер, издавший в 1887 г. в Вене ‘Физику извержений’, а в 1888 г. в Штутгарде ‘Теоретическую геологию’. Он предположил, что если в вышележащих твердых массах появится при землетрясении трещина и вследствие этого начнет уменьшаться давление, то нагретое глубинное вещество перейдет в жидкое состояние и, вырываясь наружу, вызовет извержение вулкана. Такую возникшую расплавленную массу было предложено называть магмой (Фогельзанг, Розенбуш, 1872), а горные породы, получающиеся при ее остывании изверженными или магматическими. В этом основа современных представлений о причинах и механизме вулканизма.
Итак, выяснилось, что глубинной энергии нет, как и магмы. Если бы магма и возникала, при подъеме бы остывала, как и при дегазации. Из вулканов изливается или выбрасывается лава, которая поднимается снизу. Почему же лава не остывает при контакте с менее нагретыми вмещающими породами и дегазации? Этот вопрос можно сформулировать по другому: может ли температура воды 900 С в ведре сохраняться какое-то продолжительное время в комнате с температурой воздуха 200 С? При всей кажущейся абсурдности вопроса логически доказательный ответ на него прост: может, если вода будет подогреваться внешним источником тепла. Подогрева лавы с низу нет. Погружаться вниз тепло не может. Следовательно, подогревается лава с боков.
Подогрева лавы с низу нет. Погружаться вниз тепло не может. Следовательно, подогревается лава с боков.
Общепринятое объяснение вулканизма подъемом глубинной энергии и вещества ненаучно. Какое же научно непротиворечивое обоснование причин вулканизма? Другое, а значит противоположное. Энергия для извержений вулканов поступает не из глубины литосферы, а на ее поверхность. Это солнечная энергия!
Ответить
00000 18.04.2008 02:55 Ответить
Земля вращается.
Ответить
nastusha 27.04.2008 15:50 Ответить
скажите пожалуйста что в зоне литосферных плит наблюдаются»землетрясение»или»землетрясение и извержение вулканов»??
Ответить
Andi
07. 03.2009 00:40
Ответить
03.2009 00:40
Ответить
«Литосфера-‘скорлупа’ как бы плавает в вязкой мантии, НЕМНОГО ПОГРУЗИВШИСЬ в нее под тяжестью своего веса.» А вулкан , соответственно,есть кусок литосферы НЕМНОГО ВСПЛЫВШИЙ из нее с неизвестными целями.
А вообще страшновато детей пускать- прочтут, поверят по простоте душевной, потом ляпнут где-нибудь… будут дураками выглядеть. Перепутаны все слои — химические, физические переходы. Пересказ прапорщиком «Войны и мира».
Ответить
djanubis Andi 28.09.2009 15:00 Ответить
Да, нет — всё просто — это на самом деле ЛУНА приподнимет вулканы из магмы, и потом саму же магму через них тянет. Происходит так называемый «еффект доения коровы». Вот учёные решили что наша Галактика имела форму коровы, так и тут — принцип доения. Что доказывает ещё раз т.н. теорию «матрёшковой вселенной».
 Ещё одно доказательство — електроны бегают вокруг протона, как стадо коров во время гона за быком гоняется.
Ещё одно доказательство — електроны бегают вокруг протона, как стадо коров во время гона за быком гоняется.
А если ещё сюда приплести древне греческую мифолою о титанах и циклопах — так вапсче ваши дети будут не дураками выглядеть а очень современными людьми, которые в курсах всех современных модных теорий.Ответить
oriss 22.07.2018 08:26 Ответить
Статья конечно интересная, как в общем и теория 18 века, которую она излагает, да впрочем практически вся школьная программа интересна. Но почему проигнорированы мысли 19 века, например Вернадского. Ведь даже малейшей критики, механизмы описанные в статье, не выдерживают, например поднятие на 40км (не говоря уже о 80ти) вверх 1000 градусного расплава, пусть даже со скоростью 1-2 м/сек и с сохранением температуры этого расплава мин — 500 град. Простейшие термодинамические расчеты, невозможность подобного, это ясно покажут.
Ответить
Dik 14.06.2022 20:35 Ответить
Интересная статья, но комменты гораздо интереснее. Нигде мне раньше не попадалось такой фееричной переклички фриков всех мастей, каждый из которых упорно игнорирует бревно в своём глазу.
Ответить
Написать комментарий
Металлическое соединение — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 1989
- Джим Кларк
- Школа Труро в Корнуолле
В начале 1900-х Пауль Дрюде придумал теорию металлических связей «моря электронов», смоделировав металлы как смесь атомных ядер (атомные ядра = положительные ядра + внутренняя оболочка электронов) и валентных электронов. Металлические связи возникают между атомами металла. В то время как ионные связи соединяют металлы с неметаллами, металлические связи соединяют большую часть атомов металлов . Лист алюминиевой фольги и медная проволока — это места, где вы можете увидеть металлическую связь в действии.
Металлические связи возникают между атомами металла. В то время как ионные связи соединяют металлы с неметаллами, металлические связи соединяют большую часть атомов металлов . Лист алюминиевой фольги и медная проволока — это места, где вы можете увидеть металлическую связь в действии.
Металлы, как правило, имеют высокие температуры плавления и кипения, что указывает на сильные связи между атомами. Даже такой мягкий металл, как натрий (температура плавления 97,8°С) плавится при значительно более высокой температуре, чем предшествующий ему элемент (неон) в периодической таблице. Натрий имеет электронную структуру 1s 2 2s 2 2p 6 3s 1 . Когда атомы натрия собираются вместе, электрон на 3s-атомной орбитали одного атома натрия делит пространство с соответствующим электроном соседнего атома, образуя молекулярную орбиталь — почти так же, как образуется ковалентная связь.
Разница, однако, заключается в том, что каждый атом натрия соприкасается с восемью другими атомами натрия, и совместное использование происходит между центральным атомом и 3s-орбиталями всех восьми других атомов. К каждому из этих восьми, в свою очередь, прикасаются восемь атомов натрия, которых, в свою очередь, касаются восемь атомов — и так далее, и так далее, пока вы не поглотите все атомы в этом куске натрия. Все 3s-орбиталей всех атомов перекрываются, образуя огромное количество молекулярных орбиталей, которые охватывают весь кусок металла. Конечно, должно быть огромное количество молекулярных орбиталей, потому что любая орбиталь может содержать только два электрона.
К каждому из этих восьми, в свою очередь, прикасаются восемь атомов натрия, которых, в свою очередь, касаются восемь атомов — и так далее, и так далее, пока вы не поглотите все атомы в этом куске натрия. Все 3s-орбиталей всех атомов перекрываются, образуя огромное количество молекулярных орбиталей, которые охватывают весь кусок металла. Конечно, должно быть огромное количество молекулярных орбиталей, потому что любая орбиталь может содержать только два электрона.
Электроны могут свободно перемещаться внутри этих молекулярных орбиталей, поэтому каждый электрон отрывается от своего родительского атома. Говорят, что электроны делокализованы. Металл удерживается сильными силами притяжения между положительными ядрами и делокализованными электронами (рис. \(\PageIndex{1}\)).
Рисунок \(\PageIndex{1}\): Металлическая связь: модель электронного моря: положительные атомные ядра (оранжевые кружки), окруженные морем делокализованных электронов (желтые кружки). Это иногда описывается как «массив положительных ионов в море электронов». +}\).
+}\).
Пример \(\PageIndex{1}\): металлическая связь в магнии
Используйте модель моря электронов, чтобы объяснить, почему магний имеет более высокую температуру плавления (650 °C), чем натрий (97,79 °C).
Решение
Если вы проработаете тот же аргумент выше для натрия с магнием, вы получите более прочные связи и, следовательно, более высокую температуру плавления.
Магний имеет внешнюю электронную структуру 3s 2 . Оба этих электрона становятся делокализованными, поэтому плотность электронов в «море» вдвое больше, чем в натрии. Остальные «ионы» также имеют вдвое больший заряд (если вы собираетесь использовать именно этот взгляд на металлическую связь), и поэтому притяжение между «ионами» и «морем» будет больше.
Более реалистично, каждый атом магния имеет 12 протонов в ядре по сравнению с 11 атомами натрия. В обоих случаях ядро экранируется от делокализованных электронов одним и тем же числом внутренних электронов — 10 электронов в 1s 2 2s 2 2p 6 орбиталей. Это означает, что будет чистое притяжение от ядра магния 2+, но только 1+ от ядра натрия.
Это означает, что будет чистое притяжение от ядра магния 2+, но только 1+ от ядра натрия.
Таким образом, в магнии будет не только больше делокализованных электронов, но и большее притяжение к ним со стороны ядер магния. Атомы магния также имеют немного меньший радиус, чем атомы натрия, поэтому делокализованные электроны находятся ближе к ядрам. Каждый атом магния также имеет двенадцать ближайших соседей, а не восемь, как у натрия. Оба эти фактора еще больше увеличивают прочность соединения.
Примечание: Переходные металлы обычно имеют особенно высокие температуры плавления и кипения. Причина в том, что они могут вовлекать в делокализацию 3d-электроны так же, как и 4s. Чем больше электронов вы можете задействовать, тем сильнее будет притяжение.
Объемные свойства металлов
Металлы обладают несколькими уникальными качествами, такими как способность проводить электричество и тепло, низкая энергия ионизации и низкая электроотрицательность (поэтому они легко отдают электроны, образуя катионы). Их физические свойства включают блестящий (блестящий) внешний вид, они податливы и пластичны. Металлы имеют кристаллическую структуру, но легко деформируются. В этой модели валентные электроны свободны, делокализованы, подвижны и не связаны с каким-либо конкретным атомом. Эта модель может учитывать:
Их физические свойства включают блестящий (блестящий) внешний вид, они податливы и пластичны. Металлы имеют кристаллическую структуру, но легко деформируются. В этой модели валентные электроны свободны, делокализованы, подвижны и не связаны с каким-либо конкретным атомом. Эта модель может учитывать:
- Проводимость : Поскольку электроны свободны, если электроны из внешнего источника втолкнуть в металлическую проволоку с одного конца (Рисунок \(\PageIndex{2}\)), электроны будут перемещаться по проволоке и приходить на другом конце с той же скоростью (проводимость — это движение заряда).
- Ковкость и Пластичность : Модель металлов электронного моря объясняет не только их электрические свойства, но также их ковкость и пластичность.
 Море электронов, окружающее протоны, действует как подушка, поэтому, например, когда по металлу ударяют молотком, общий состав структуры металла не повреждается и не изменяется. Протоны могут перестраиваться, но море электронов приспосабливается к новому образованию протонов и сохраняет металл неповрежденным. При перемещении одного слоя ионов в электронном море на одно расстояние по отношению к слою под ним кристаллическая структура не разрушается, а только деформируется (рис. \(\PageIndex{3}\)).
Море электронов, окружающее протоны, действует как подушка, поэтому, например, когда по металлу ударяют молотком, общий состав структуры металла не повреждается и не изменяется. Протоны могут перестраиваться, но море электронов приспосабливается к новому образованию протонов и сохраняет металл неповрежденным. При перемещении одного слоя ионов в электронном море на одно расстояние по отношению к слою под ним кристаллическая структура не разрушается, а только деформируется (рис. \(\PageIndex{3}\)).
- Теплоемкость : Это объясняется способностью свободных электронов перемещаться по твердому телу.
- Блеск : Свободные электроны могут поглощать фотоны в «море», поэтому металлы выглядят непрозрачными.
 Электроны на поверхности могут отражать свет с той же частотой, что и свет, падающий на поверхность, поэтому металл кажется блестящим.
Электроны на поверхности могут отражать свет с той же частотой, что и свет, падающий на поверхность, поэтому металл кажется блестящим.
Однако эти наблюдения являются только качественными, а не количественными, поэтому их нельзя проверить. Теория «Море электронов» сегодня существует только как упрощенная модель того, как работает металлическая связь.
В расплавленном металле металлическая связь все еще присутствует, хотя упорядоченная структура нарушена. Металлическая связь не разрывается полностью до тех пор, пока металл не закипит. Это означает, что точка кипения на самом деле является лучшим показателем прочности металлической связи, чем точка плавления. При плавлении связь ослабляется, а не разрывается. Прочность металлической связи зависит от трех факторов:
- Число электронов, которые становятся делокализованными из металла
- Заряд катиона (металл).
- Размер катиона.
Сильная металлическая связь будет результатом большего количества делокализованных электронов, что приведет к увеличению эффективного заряда ядра на электронах катиона, что приведет к уменьшению размера катиона. Металлические связи прочны и требуют много энергии для разрыва, поэтому 9Металлы 0052 имеют высокие температуры плавления и кипения. Теория металлических связей должна объяснить, как такое количество связей может происходить с таким небольшим количеством электронов (поскольку металлы расположены в левой части таблицы Менделеева и не имеют много электронов на своих валентных оболочках). Теория также должна учитывать все уникальные химические и физические свойства металла.
Металлические связи прочны и требуют много энергии для разрыва, поэтому 9Металлы 0052 имеют высокие температуры плавления и кипения. Теория металлических связей должна объяснить, как такое количество связей может происходить с таким небольшим количеством электронов (поскольку металлы расположены в левой части таблицы Менделеева и не имеют много электронов на своих валентных оболочках). Теория также должна учитывать все уникальные химические и физические свойства металла.
Расширение диапазона возможных связей
Ранее мы утверждали, что связи между атомами можно классифицировать как диапазон возможных связей между ионные связи (полный перенос заряда) и ковалентные связи (полностью разделенные электроны). Когда два атома с немного различающимися электроотрицательностями соединяются вместе, образуя ковалентную связь, один атом притягивает электроны больше, чем другой; это называется полярной ковалентной связью. Однако простые «ионные» и «ковалентные» связи являются идеализированными концепциями, и большинство связей существует в двумерном континууме, описываемом треугольником Ван Аркела-Кетелаара (рис. \(\PageIndex{4}\)).
Однако простые «ионные» и «ковалентные» связи являются идеализированными концепциями, и большинство связей существует в двумерном континууме, описываемом треугольником Ван Аркела-Кетелаара (рис. \(\PageIndex{4}\)).
или треугольники ван Аркела – Кетелаара (названные в честь Антона Эдуарда ван Аркеля и Дж. А. А. Кетелара) представляют собой треугольники, используемые для отображения различных соединений с разной степенью ионной, металлической и ковалентной связи. В 1941 ван Аркель выделил три экстремальных материала и связанные с ними типы склеивания. Используя 36 основных групп элементов, таких как металлы, металлоиды и неметаллы, он разместил ионные, металлические и ковалентные связи в углах равностороннего треугольника, а также предложил промежуточные виды. Треугольник связей показывает, что химические связи — это не просто определенные связи определенного типа. Скорее, типы связи взаимосвязаны, и разные соединения имеют разную степень разного характера связи (например, полярные ковалентные связи).
Треугольник связей показывает, что химические связи — это не просто определенные связи определенного типа. Скорее, типы связи взаимосвязаны, и разные соединения имеют разную степень разного характера связи (например, полярные ковалентные связи).
Используя электроотрицательность — два составных средних значения электроотрицательности по оси x рисунка \(\PageIndex{4}\).
\[\sum \chi = \dfrac{\chi_A + \chi_B}{2} \label{sum}\]
и разность электроотрицательностей по оси Y,
\[\Delta \chi = | \чи_А — \чи_Б | \label{diff}\]
мы можем оценить доминирующую связь между соединениями. В правой части рисунка \(\PageIndex{4}\) (от ионных до ковалентных) должны быть соединения с различной разницей в электроотрицательности. Соединения с одинаковой электроотрицательностью, такие как \(\ce{Cl2}\) (хлор), помещаются в ковалентный угол, в то время как в ионный угол входят соединения с большой разницей электроотрицательностей, такие как \(\ce{NaCl}\) ( столовая соль). Нижняя сторона (от металлической до ковалентной) содержит соединения с разной степенью направленности связи. На одном полюсе находятся металлические связи с делокализованным соединением, а на другом — ковалентные связи, в которых орбитали перекрываются в определенном направлении. Левая часть (от ионной к металлической) предназначена для делокализованных связей с различной разницей электроотрицательностей.
Нижняя сторона (от металлической до ковалентной) содержит соединения с разной степенью направленности связи. На одном полюсе находятся металлические связи с делокализованным соединением, а на другом — ковалентные связи, в которых орбитали перекрываются в определенном направлении. Левая часть (от ионной к металлической) предназначена для делокализованных связей с различной разницей электроотрицательностей.
Три крайности в связывании
В целом:
- Металлические связи имеют низкое \(\Delta \chi\) и низкое среднее \(\sum\chi\).
- Ионные связи имеют значения \(\Delta \chi\) от умеренных до высоких и средние значения \(\sum \chi\).
- Ковалентные связи имеют среднее значение \(\sum \chi\) от умеренного до высокого и могут существовать при умеренно низком \(\Delta \chi\).
Пример \(\PageIndex{2}\)
Используйте таблицы электроотрицательностей (Таблица A2) и рисунок \(\PageIndex{4}\) для оценки следующих значений
- разница в электроотрицательности (\(\Delta \chi\))
- средняя электроотрицательность связи (\(\sum \chi\))
- процента ионного характера
- вероятный тип облигации
для выбранных соединений:
- \(\ce{AsH}\) (например, в арсине \(AsH\))
- \(\ce{SrLi}\)
- \(\ce{KF}\).

Раствор
a: \(\ce{AsH}\)
- Электроотрицательность \(\ce{As}\) равна 2,18
- Электроотрицательность \(\ce{H}\) равна 2,22
Использование уравнений \ref{sum} и \ref{diff}:
\[\begin{align*} \sum \chi &= \dfrac{\chi_A + \chi_B}{2} \\[4pt] & =\dfrac{2.18 + 2.22}{2} \\[4pt] &= 2.2 \end{align*}\]
\[\begin{align*} \Delta \chi &= \chi_A — \chi_B \\ [4pt] &= 2,18 — 2,22 \\[4pt] &= 0,04 \end{align*}\]
- Из рисунка \(\PageIndex{4}\) видно, что связь довольно неполярная и имеет низкий ионный характер (10% или менее)
- Связь между ковалентной связью и металлической связью
b: \(\ce{SrLi}\)
- Электроотрицательность \(\ce{Sr}\) равна 0,95
- Электроотрицательность \(\ce{Li}\) равна 0,98
Использование уравнений \ref{sum} и \ref{diff}:
\[\begin{align*} \sum \chi &= \dfrac{\chi_A + \chi_B}{2} \\[4pt] & =\dfrac{0,95 + 0,98}{2} \\[4pt] &= 0,965 \end{align*}\]
\[\begin{align*} \Delta \chi &= \chi_A — \chi_B \\ [4 балла] &= 0,98 — 0,95 \\[4pt] &= 0,025 \end{align*}\]
- Из рисунка \(\PageIndex{4}\) видно, что связь довольно неполярная и имеет низкий ионный характер (~3% или меньше)
- Соединение, вероятно, металлическое.

c: \(\ce{KF}\)
- Электроотрицательность \(\ce{K}\) равна 0,82
- Электроотрицательность \(\ce{F}\) равна 3,98
Использование уравнений \ref{sum} и \ref{diff}:
\[\begin{align*} \sum \chi &= \dfrac{\chi_A + \chi_B}{2} \\[4pt] & =\dfrac{0,82 + 3,98}{2} \\[4pt] &= 2.4 \end{align*}\]
\[\begin{align*} \Delta \chi &= \chi_A — \chi_B \\[4pt] &= | 0,82 — 3,98 | \\[4pt] &= 3,16 \end{align*}\]
- Из рисунка \(\PageIndex{4}\) видно, что связь довольно полярная и имеет высокий ионный характер (~75%)
- Связь, вероятно, ионная.
Упражнение \(\PageIndex{2}\)
Сравните связь \(\ce{NaCl}\) и тетрафторида кремния.
- Ответить
\(\ce{NaCl}\) представляет собой ионную кристаллическую структуру и электролит при растворении в воде; \(\Delta \chi =1,58\), среднее \(\sum \chi =1,79\), тогда как тетрафторид кремния является ковалентным (молекулярный, неполярный газ; \(\Delta \chi =2,08\), среднее \( \сумма \хи =2,94\).

Авторы и ссылки
Джим Кларк (Chemguide.co.uk)
- Дэниел Джеймс Бергер
- Википедия
Эд Витц (Университет Куцтауна), Джон В. Мур (UW-Мэдисон), Джастин Шорб (Колледж Хоуп), Ксавьер Прат-Ресина (Университет Миннесоты в Рочестере), Тим Вендорф и Адам Хан.
Эта страница под названием Metallic Bonding используется в соответствии с лицензией CC BY-SA, автором, ремиксом и/или куратором которой является Джим Кларк.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Автор
- Джим Кларк
- Лицензия
- CC BY-SA
- Показать страницу TOC
- № на стр.

- Теги
- металлическое соединение
- Треугольник ван Аркель-Кетелаар
Объяснение урока: Склеивание металлов | Nagwa
В этом толкователе мы узнаем, как описывать металлическую связь и ее влияние на физические и химические свойства металлов.
Почти все знакомы с металлами, потому что металлы используются во всем мире. Некоторые металлы используются для изготовления электрических проволока и другие металлы превращаются в банки и декоративные украшения. Металлы также используются для изготовления автомобилей и для обеспечения структурной поддержки больших зданий и памятников. Металлы являются основой современной жизни, и было бы трудно представить жизнь без них.
Металлы состоят из относительно неподвижных катионов и очень подвижных делокализованных электронов. Неподвижные катионы расположены
как гигантская трехмерная решетка, и решетка удерживается вместе благодаря притягивающим взаимодействиям между решеткой и
делокализованные электроны. Металлические связи обычно описываются как ненаправленные взаимодействия, поскольку делокализованное
электроны вместе действуют как клей, который одинаково влияет на все катионы металлов. Металлы почти всегда описываются как
плотная, потому что решетка состоит из катионов, которые очень тесно связаны друг с другом.
Неподвижные катионы расположены
как гигантская трехмерная решетка, и решетка удерживается вместе благодаря притягивающим взаимодействиям между решеткой и
делокализованные электроны. Металлические связи обычно описываются как ненаправленные взаимодействия, поскольку делокализованное
электроны вместе действуют как клей, который одинаково влияет на все катионы металлов. Металлы почти всегда описываются как
плотная, потому что решетка состоит из катионов, которые очень тесно связаны друг с другом.
Определение: металлическая связь
Металлическая связь – это сильное электростатическое притяжение, которое существует между положительно заряженными катионами металлов и делокализованные электроны.
Пример 1. Определение доминирующей силы притяжения в гигантской металлической решетке
Какая форма притяжения в металлической связи является преобладающей между решеткой положительных ионов и морем делокализованные электроны?
- Гравитационный
- Ядерный
- Магнитное
- Электростатическое
- Ковалентное
Ответ
Металлическую связь можно определить как электростатическое притяжение, которое существует между относительно неподвижными катионами металлов. и подвижные делокализованные электроны. Катионы имеют положительный электростатический заряд и притягиваются к окружающей среде.
отрицательно заряженные делокализованные электроны. Электростатическое притяжение между противоположно заряженными частицами
доминирующая форма притяжения в гигантской металлической решетчатой структуре. Эти операторы могут быть использованы для определения этого варианта
D — правильный ответ на этот вопрос.
и подвижные делокализованные электроны. Катионы имеют положительный электростатический заряд и притягиваются к окружающей среде.
отрицательно заряженные делокализованные электроны. Электростатическое притяжение между противоположно заряженными частицами
доминирующая форма притяжения в гигантской металлической решетчатой структуре. Эти операторы могут быть использованы для определения этого варианта
D — правильный ответ на этот вопрос.
На следующем рисунке показано, что делокализованные электроны исходят из валентной оболочки атомов металла. Валентные электроны имеют
очень низкие энергии ионизации, и это электроны, которые легче всего удалить из нейтрально заряженных атомов. Делокализованный
электроны относительно не ограничены, когда они отделяются от атомов металла, и они могут перемещаться между катионами, которые
составляют металлическую решетку. Здесь важно понимать, что число делокализованных электронов почти всегда будет
быть точно равным числу валентных электронов в чистом металлическом элементе. Атомы натрия генерируют одиночные электроны, потому что
у них есть один валентный электрон, а атомы магния генерируют два, потому что у них есть два валентных электрона.
Атомы натрия генерируют одиночные электроны, потому что
у них есть один валентный электрон, а атомы магния генерируют два, потому что у них есть два валентных электрона.
Пример 2. Определение наилучшего описания делокализованных электронов
Что из следующего является лучшим описанием делокализованных электронов в металлической связи?
- Электроны остова, связанные с ионами металлов
- Электроны остова и валентные электроны, которые могут свободно перемещаться между ионами металлов
- Электроны остова, которые могут свободно перемещаться между ионами металлов
- Электроны остова, связанные с ионами металлов ионы металлов
Ответ
Атомы металлов имеют как минимум две электронные оболочки, но только валентные электроны отделяются от электронов.
атомы металла в гигантских металлически связанных структурах. Валентные электроны группируются вместе, и они эффективно образуют один
гигантское море делокализованных электронов. Делокализованные электроны относительно не ограничены и могут перемещаться между
неподвижные катионы металлов.
Делокализованные электроны относительно не ограничены и могут перемещаться между
неподвижные катионы металлов.
Мы можем определить, что все варианты A, B и E неверны, потому что они утверждают, что делокализованные электроны являются либо остовными электронов или комбинации остовных и валентных электронов.
Мы также можем определить, что вариант D не может быть правильным ответом, потому что он утверждает, что делокализованные электроны являются частицами которые связаны с ионами металлов. Делокализованные электроны — это относительно неограниченные частицы, которые могут перемещаться по всему гигантскому металлическая решетка.
Мы определили, что вариант C должен быть правильным ответом в процессе исключения, но мы также можем использовать логические
аргументация, подтверждающая этот вывод. Мы можем сделать вывод, что вариант C является правильным ответом, потому что мы уже заявили, что
Делокализованные электроны — это валентные электроны, которые могут перемещаться между неподвижными катионами металлов. Вариант C должен быть правильным
ответ на этот вопрос, потому что он также утверждает, что делокализованные электроны — это валентные электроны, которые могут свободно перемещаться
между ионами металлов.
Вариант C должен быть правильным
ответ на этот вопрос, потому что он также утверждает, что делокализованные электроны — это валентные электроны, которые могут свободно перемещаться
между ионами металлов.
В следующей таблице перечислены некоторые наиболее распространенные физические свойства элементов из чистого металла. Перечисленные свойства могут все можно объяснить с помощью модели моря электронов.
| The Common Physical Properties of Pure Metal Elements |
|---|
| High melting point |
| High boiling point |
| High electrical conductivity |
| High heat conductivity |
| Malleable |
| Ковкий |
| Блестящий |
Температура плавления и кипения любого металла зависит от размера его положительно заряженных катионов. Металлы обычно
имеют высокие температуры плавления и кипения, если они содержат малые катионы. Металлы обычно имеют более низкую температуру плавления и
температуры кипения, если они содержат большие катионы. В следующей таблице показаны значения температуры плавления и атомного радиуса
металлические элементы натрия и лития.
Металлы обычно имеют более низкую температуру плавления и
температуры кипения, если они содержат большие катионы. В следующей таблице показаны значения температуры плавления и атомного радиуса
металлические элементы натрия и лития.
| Element Name | Lithium (Li) | Sodium (Na) |
|---|---|---|
| Electron Shells | (2, 1) | (2, 8, 1) |
| Atomic Radius (pm) | 152 | 186 |
| Печата плавления (∘C) | 181 | 98 |
LITHIUM с более высокой точкой. Атомы лития становятся высококонцентрированными, когда они упаковываются близко друг к другу в решетке лития, и это создает сильное
Силы металлического сцепления. Требуется много энергии, чтобы преодолеть сильные силы притяжения между катионами лития и
окружающие делокализованные электроны. Требуется гораздо меньше энергии, чтобы преодолеть силы притяжения между более крупными натриевыми
катионы и окружающие делокализованные электроны.
На температуры плавления и кипения также влияет состояние электростатического заряда катионов в металлической решетке. Катионы сильно взаимодействуют с электронами, если они имеют высокое зарядовое состояние, и более слабые взаимодействия, если они имеют более низкое состояние заряда. Катионы имеют относительно сильные взаимодействия с электронами, если они имеют 2+ или зарядовое состояние 3+ и относительно слабые взаимодействия, если они имеют зарядовое состояние 1+. Это утверждение подтверждается данными в следующей таблице. Таблица доказывает, что натрий имеет более низкую температуру плавления и температура кипения выше, чем у магния. Это также доказывает, что магний имеет более низкую температуру плавления и кипения, чем алюминий.
| Название элемента | натрия (NA) | Магний (MG) | Алюминий (AL) |
|---|---|---|---|
| Electron Shells | (2, 8, | ||
| . | (2, 8, 3) | ||
| Точка плавления (∘C) | 98 | 650 | 659 |
. 470 470 |
Ионы натрия относительно слабо взаимодействуют с окружающими делокализованными электронами, потому что они имеют 1+ состояние заряда. Ионы магния сильнее взаимодействуют с делокализованными электронами, потому что они имеют 2+ состояние заряда. Ионы алюминия еще сильнее взаимодействуют с делокализованными электронами, поскольку имеют 3+ состояние заряда.
Важно понимать, что на температуры кипения и плавления также влияет концентрация делокализованных
электроны в металлической решетке. Алюминий имеет такую исключительно высокую температуру кипения отчасти потому, что он содержит такое высокое
концентрация делокализованных электронов. Каждый атом алюминия генерирует три делокализованных электрона, а каждый атом натрия и магния
атом может генерировать только один или два делокализованных электрона. На следующем рисунке показано, что атомы алюминия генерируют больше
делокализованных электронов, чем атомы натрия.
В предыдущих абзацах указано, что существует множество различных свойств частиц и решеток, влияющих на плавление. температура и температура кипения металла. В параграфах поясняется, что металлы, как правило, имеют относительно высокие температуры плавления. и температуры кипения, если они содержат малые катионы. Предполагается, что металлический литий имеет более высокую температуру плавления, чем натрий. потому что ионы лития меньше ионов натрия. В предыдущих абзацах также объясняется, что металлы, как правило, имеют высокую температуры плавления и кипения, если они содержат высокую концентрацию делокализованных электронов и катионов, имеющих состояние высокого заряда. Предполагается, что алюминий имеет гораздо более высокую температуру кипения, чем натрий, поскольку алюминий содержит более высокая концентрация делокализованных электронов, и он состоит из катионов с более высоким зарядом.
Пример 3: Идентификация системы с самой высокой температурой плавления
Какой из следующих атомов образует твердый металл с самой высокой температурой плавления?
Ответ
В этом вопросе нам предлагается определить, какой атом образует твердый металл с самой высокой температурой плавления. Мы можем немедленно
систему B, потому что она имеет полную валентную оболочку электронов и является благородным газом. Атомы благородных газов имеют тенденцию образовывать
газы с невероятно низкой температурой плавления. Другие варианты нужно тщательно сравнивать, потому что все они сделаны из металлов.
и мы не можем так быстро сбрасывать со счетов их как возможные ответы на этот вопрос.
Мы можем немедленно
систему B, потому что она имеет полную валентную оболочку электронов и является благородным газом. Атомы благородных газов имеют тенденцию образовывать
газы с невероятно низкой температурой плавления. Другие варианты нужно тщательно сравнивать, потому что все они сделаны из металлов.
и мы не можем так быстро сбрасывать со счетов их как возможные ответы на этот вопрос.
Металлы обычно имеют высокие температуры плавления, когда они имеют большое количество валентных электронов. Металлы, как правило, имеют
относительно низкая температура плавления, если они имеют один валентный электрон, и они, как правило, имеют более высокую температуру плавления, если
они имеют два или даже три валентных электрона. Это говорит о том, что системы А и С имеют более высокие температуры плавления, чем системы
D и E. Обе системы A и C имеют по два валентных электрона, а системы D и E имеют только один валентный электрон. Эта линия
рассуждений помогло нам определить, что правильным ответом должна быть система А или система С. Теперь нам нужно сравнить другие
атомные свойства, чтобы определить, имеет ли система A или C более высокую температуру плавления.
Эта линия
рассуждений помогло нам определить, что правильным ответом должна быть система А или система С. Теперь нам нужно сравнить другие
атомные свойства, чтобы определить, имеет ли система A или C более высокую температуру плавления.
Металлы обычно имеют высокие температуры плавления, если они состоят из небольших атомов, и более низкие температуры плавления, если они состоят из крупных атомов. Система А имеет три электронных оболочки, а система С — две электронные оболочки. Электронные оболочки принимают пространстве, и это предполагает, что система C меньше, чем система A. Наша линия рассуждений предполагает, что система C должна формировать твердый металл, который имеет более высокую температуру плавления, чем системы A и B или системы D и E. Мы можем заключить, что система C имеет быть правильным ответом на этот вопрос.
Металлы хорошо проводят электричество, потому что они содержат делокализованные электроны. Делокализованные электроны могут переносить
заряд при приложении напряжения к металлической решетке. Делокализованные электроны движутся к положительному полюсу, и
отрицательный терминал производит больше электронов. Металлы имеют тенденцию быть лучшими проводниками электричества, когда они имеют много
делокализованные электроны. Алюминий — лучший проводник электричества, чем магний, а магний — лучший электрический проводник.
проводник, чем натрий.
Делокализованные электроны могут переносить
заряд при приложении напряжения к металлической решетке. Делокализованные электроны движутся к положительному полюсу, и
отрицательный терминал производит больше электронов. Металлы имеют тенденцию быть лучшими проводниками электричества, когда они имеют много
делокализованные электроны. Алюминий — лучший проводник электричества, чем магний, а магний — лучший электрический проводник.
проводник, чем натрий.
Определение: Электропроводность
Электропроводность — это мера того, насколько легко электрический заряд проходит через материал.
Пример 4. Понимание того, как валентные электроны влияют на электропроводность
На гистограмме показаны электропроводности алюминия, магния и натрия.
- Используя символы элементов, определите металлы X,
Y и Z.
- X=Al, Y=мг, Z=Na
- Х=Na, Y=Al, Z=Mg
- X=Mg, Y=Al, Z=Na
- X=Mg, Y=Na, Z=Al
- X=Na, Y=мг, Z=Al
- Какое из следующих атомных свойств больше всего отвечает за изменение проводимости между
металлы X, Y и Z?
- Атомная масса
- Энергия связи
- Энергия ионизации
- Количество остовных электронов
- Количество валентных электронов
Ответ
Часть 1
Натрий, магний и алюминий имеют одинаковое количество остовных электронов, но у них разное количество электронов
валентных электронов. Металлы, как правило, имеют более высокие значения электропроводности, когда они содержат больше переносящих заряд
валентные электроны. Атомы натрия имеют один валентный электрон, а атомы магния и алюминия – двух- и трехвалентные.
электроны. Система Y должна быть натриевой, потому что у нее самая низкая электропроводность.
ценность. Система Z должна быть алюминиевой, поскольку она имеет самое высокое значение электропроводности. Система X должна состоять из магния, потому что его электропроводность равна
между этими двумя крайностями. Эти утверждения можно использовать для определения того, что вариант D является правильным ответом для
этот вопрос.
Металлы, как правило, имеют более высокие значения электропроводности, когда они содержат больше переносящих заряд
валентные электроны. Атомы натрия имеют один валентный электрон, а атомы магния и алюминия – двух- и трехвалентные.
электроны. Система Y должна быть натриевой, потому что у нее самая низкая электропроводность.
ценность. Система Z должна быть алюминиевой, поскольку она имеет самое высокое значение электропроводности. Система X должна состоять из магния, потому что его электропроводность равна
между этими двумя крайностями. Эти утверждения можно использовать для определения того, что вариант D является правильным ответом для
этот вопрос.
Часть 2
Металлы обычно имеют высокие значения электропроводности, когда они содержат много валентных электронов, несущих заряд. Алюминий имеет три валентных электрона на атом и имеет самое высокое значение электропроводности из трех перечисленных.
опции. Натрий имеет только один валентный электрон на атом и имеет самое низкое значение электропроводности из трех.
перечисленные варианты. Мы можем использовать эти утверждения, чтобы определить, что вариант E является правильным ответом на этот вопрос.
Натрий имеет только один валентный электрон на атом и имеет самое низкое значение электропроводности из трех.
перечисленные варианты. Мы можем использовать эти утверждения, чтобы определить, что вариант E является правильным ответом на этот вопрос.
Металлы лучше проводят тепло, чем неметаллы, потому что металлические решетки содержат делокализованные электроны. Тепло проводится в неметаллических материалах, когда некоторые из атомов неметалла вступают в контакт с источником тепла. Источник тепла делает некоторые атомы неметаллов энергично колеблются вокруг одной и той же точки решетки. Затем эта кинетическая энергия передается другим атомы неметалла, когда один из вибрирующих атомов сталкивается с другими соседними атомами неметалла. Кинетическая энергия медленно передается через неметаллический материал, когда атомы неметалла вибрируют и сталкиваются друг с другом.
Атомы металлов могут передавать тепло через аналогичные медленные процессы вибрации и столкновения. Некоторые катионы металлов колеблются, когда они
нагреваются, и эти катионы в конечном итоге сталкиваются с другими соседними катионами металлов. Тепловая энергия может перемещаться по всей металлической
решетки, когда кинетическая энергия передается вдоль длинной цепи колеблющихся катионов металлов.
Некоторые катионы металлов колеблются, когда они
нагреваются, и эти катионы в конечном итоге сталкиваются с другими соседними катионами металлов. Тепловая энергия может перемещаться по всей металлической
решетки, когда кинетическая энергия передается вдоль длинной цепи колеблющихся катионов металлов.
Металлы также содержат высокоподвижные делокализованные электроны, которые могут очень быстро передавать тепло. Электроны относительно свободно, и они могут перемещаться между катионами металлов. Делокализованные электроны могут скользить по металлической решетке. и быстро передавать тепло между различными частями гигантской металлической конструкции. На следующем рисунке сравнивается тепло (красные стрелки) процессы переноса в гигантских неметаллических и металлических структурах.
Чистые металлы обычно пластичны и пластичны. Металлы описываются как пластичные, потому что их можно волочить.
на тонкие провода. Металлы описываются как податливые, потому что их можно ковать или прессовать в различные формы. формы без поломок и трещин. Металлы обычно пластичны и ковки, потому что они содержат делокализованные
электроны.
формы без поломок и трещин. Металлы обычно пластичны и ковки, потому что они содержат делокализованные
электроны.
Определение: Ковкий
Ковкий материал можно вытягивать в тонкую проволоку.
Гигантские металлические структуры состоят из слоев катионов металлов, удерживаемых вместе морем делокализованных электронов. Это позволяет одному слою катионов металлов легко скользить по другому слою без необходимости разрушения или восстановления решетки. любые химические связи. Море делокализованных электронов будет менять свою форму по мере того, как слои катионов металлов будут скользить по каждому из них. Другой.
Определение: Ковкий
Ковкий материал можно спрессовать или придать ему форму без разрушения или растрескивания.
Элементы из чистого металла почти всегда можно описать как блестящие (блестящие), когда они существуют в виде большого блока или
камень среднего и крупного размера. Блестящий вид металла можно объяснить делокализованными электронами. Говорят, что делокализованные электроны на поверхности металла непрерывно поглощают, а затем отражают.
пакеты световой энергии. Отражение света делокализованным морем электронов — это то, что делает металлическим
поверхность выглядит такой блестящей или блестящей. Некоторые металлы имеют тенденцию быть очень ценными, потому что они блестящие. Золото, как правило,
продается по высокой цене отчасти потому, что он такой блестящий и редкий.
Говорят, что делокализованные электроны на поверхности металла непрерывно поглощают, а затем отражают.
пакеты световой энергии. Отражение света делокализованным морем электронов — это то, что делает металлическим
поверхность выглядит такой блестящей или блестящей. Некоторые металлы имеют тенденцию быть очень ценными, потому что они блестящие. Золото, как правило,
продается по высокой цене отчасти потому, что он такой блестящий и редкий.
Определение: Блестящие
Блестящие материалы могут равномерно и эффективно отражать свет без мерцания или блеска.
Не всегда желательно иметь ковкие или пластичные металлы, и иногда мы хотим реформировать чистые металлы.
в сплавы, чтобы сделать их более жесткими. Мы можем производить сплавы, смешивая один чистый металл с другим металлом или неметаллическим элементом. На следующем рисунке показано, как можно получить сплав путем смешивания одного чистого металлического элемента с совершенно другим веществом. Сплавы, как правило, обладают необычными физическими свойствами из-за такого нерегулярного расположения атомов и ионов.
Сплавы, как правило, обладают необычными физическими свойствами из-за такого нерегулярного расположения атомов и ионов.
Определение: Сплав
Сплав можно получить путем соединения одного металлического элемента с одним или несколькими другими элементами.
Пример 5. Определение правильной классификации композитного материала
Свойства металла можно изменить, смешав этот металл с другим элементом. Который из перечисленных как называется полученная смесь?
- Гель
- Сплав
- Эмульсия
- Суспензия
- Металлоид
Ответ
Атомы любого металлического элемента могут быть объединены с атомами другого элемента для создания нового композитного материала. Новый композиционный материал обычно имеет совершенно другой набор физических свойств. Новый композитный материал может
быть менее податливым, а может быть более твердым и ломким. Процесс создания новых композиционных материалов из металла
элементов теперь хорошо известно, и люди разработали термины для описания процесса создания новых композитных материалов. и условия для самих композиционных материалов. Процесс обычно называют легированием, а конечный продукт легирования
процесс почти всегда называют сплавом. Мы можем использовать эти утверждения, чтобы определить, что вариант B должен быть правильным ответом.
для этого вопроса.
и условия для самих композиционных материалов. Процесс обычно называют легированием, а конечный продукт легирования
процесс почти всегда называют сплавом. Мы можем использовать эти утверждения, чтобы определить, что вариант B должен быть правильным ответом.
для этого вопроса.
Ключевые моменты
- Металлическая связь — это сильное электростатическое притяжение, которое существует между относительно неподвижными катионами. и подвижные делокализованные электроны.
- Большинство металлов имеют высокие температуры плавления и кипения из-за сильного электростатического притяжения, которое существует между их катионами и делокализованными электронами.
- Металлы, как правило, являются хорошими проводниками тепла и электричества, поскольку они имеют делокализованные электроны.
- Чистые металлы обычно ковкие и пластичные, потому что они содержат слои атомов, которые легко могут
проходить друг над другом.

- Чистые металлы обычно блестят, потому что они содержат море делокализованных электронов.
- Чистые металлы можно смешивать с другими элементами для получения металлических сплавов.
Металлическая связка | Определение, факторы и объяснение
Металлическая связкаВы, должно быть, читали о металлах и других металлических предметах. Даже вы видели много предметов, сделанных из металлов. Задумывались ли вы когда-нибудь, что вызывает различные формы и вариации металлических предметов? Почему мы можем делать листы, проволоку или любую другую форму металла? Почему они светятся на свету?
Какая связь между одним атомом металла и другим и что их связывает? В металлах так много всего интересного. Но причиной большинства из этих причин является металлическая связь.
В этой статье вы узнаете о склеивании металлов и ответите на поставленные выше вопросы. Взглянуть.
Что такое металлическое соединение?
Металлическая связь – это сила притяжения между валентными электронами и ионами металлов. Химическая связь возникает из-за электростатической силы притяжения между электронами проводимости и положительно заряженными ионами металлов.
Химическая связь возникает из-за электростатической силы притяжения между электронами проводимости и положительно заряженными ионами металлов.
Что такое металлическое соединение? Это описывается как совместное использование свободных электронов в решетке положительно заряженных ионов (или катионов). Металлическая связь — это удар, который удерживает ионы металла вместе в металлическом объекте. Это сила притяжения между катионами металлов и делокализованными электронами, и эта сила прочно связывает атомы в металлическом объекте.
Металлическая связь является электростатической и существует только в металлических предметах. Металлическая связь описывает многие физические характеристики металлов, такие как блеск, гибкость, электро- и теплопроводность, удельное сопротивление, непрозрачность и прочность.
Как образуется металлическая связь?
В случае металлического объекта интегральные частицы представляют собой фиксированные катионы металлов, окруженные морем подвижных электронов. Они производятся из металлических объектов, потому что такие объекты имеют низкую энергию ионизации и могут легко терять свои валентные электроны, оставляя после себя положительно заряженные ионы (ядра).
Они производятся из металлических объектов, потому что такие объекты имеют низкую энергию ионизации и могут легко терять свои валентные электроны, оставляя после себя положительно заряженные ионы (ядра).
Эти электроны могут легко проникать сквозь металлическую решетку, как вода в море. Поэтому их называют «морем свободных электронов».
Каждый атом металла вносит один или несколько электронов в это море делокализованных электронов. Эти подвижные электроны одновременно притягиваются положительными ионами и удерживают эти положительные ионы вместе электростатической силой притяжения.
Притяжение между ядром и мобильными электронами, удерживающими ядро вместе, и эта сила притяжения известна как металлическая связь. Существенными частицами в металлических кристаллах являются атомы металла, удерживаемые вместе металлической связью.
Следующая диаграмма металлических связей показывает металлические твердые положительные ионы в море подвижных электронов.
Примеры металлической связи Как правило, все металлы являются примерами металлической связи. Но вот объяснение металлической связи в некоторых металлах, то есть алюминии, магнии и натрии.
Но вот объяснение металлической связи в некоторых металлах, то есть алюминии, магнии и натрии.
Электронная конфигурация алюминия (Al): 1s 2 2s 2 2p 6 3s 2 3p 1 . Всего у него три валентных электрона. Из-за своей электроположительной природы и делокализованных электронов он может потерять эти три валентных электрона и стать ионами металла Al+3. При таком положительном заряде отдельные ионы Al могут сильно отталкиваться друг от друга. Но море или облако электронов удерживало их вместе. Из-за большей величины заряда и плотности электронов температура плавления алюминия становится выше, чем у магния и натрия.
In the case of magnesium (Mg), electronic configuration 1s 2 2s 2 2p 6 3s 2 , and sodium (Na), electronic configuration 1s 2 2s 2 2p 6 3s 1 , число валентных электронов равно 2 и 1 соответственно. В результате их электронная плотность и величина заряда ниже, чем у алюминия. Следовательно, их температура плавления также ниже, чем у алюминия.
В результате их электронная плотность и величина заряда ниже, чем у алюминия. Следовательно, их температура плавления также ниже, чем у алюминия.
Следовательно, металлическая связь алюминия будет прочнее, чем у магния и натрия. На самом деле из-за малого количества свободных электронов натрий мягкий и имеет более низкую температуру плавления, чем два других.
Факторы образования металлических связей
Факторы, способствующие образованию металлических связей:
- Энергия ионизации металла должна быть низкой, чтобы валентные электроны свободно удерживались ядром и, таким образом, становились подвижными.
- Металлы должны иметь высокую электроположительность, чтобы они не принимали электроны и образовывали анионы.
- Свободная орбиталь должна быть больше числа валентных электронов, чтобы подвижные электроны могли легко перемещаться по вакантным орбиталям.
Характерные свойства металлических связей
Некоторые важные характерные свойства твердых тел, содержащих металлические связи:
- Электрические проводники:
Металлические связующие кристаллы обычно являются хорошими проводниками электричества. Это из-за моря свободных электронов в их структуре. Их металлический кристалл имеет подвижные или делокализованные электроны. Когда один конец этого кристалла входит в контакт с электрическим полем, присутствующий там подвижный электрон движется к положительному концу кристалла. Когда он движется, другой электрон захватывает его положение и сталкивается с той же ситуацией. Таким образом происходит движение электронов, приводящее к протеканию электричества в кристалле. Следовательно, твердые тела, имеющие металлические связи, являются хорошими проводниками электричества.
Это из-за моря свободных электронов в их структуре. Их металлический кристалл имеет подвижные или делокализованные электроны. Когда один конец этого кристалла входит в контакт с электрическим полем, присутствующий там подвижный электрон движется к положительному концу кристалла. Когда он движется, другой электрон захватывает его положение и сталкивается с той же ситуацией. Таким образом происходит движение электронов, приводящее к протеканию электричества в кристалле. Следовательно, твердые тела, имеющие металлические связи, являются хорошими проводниками электричества.
- Теплопроводники:
Как и электропроводность, металлические кристаллы являются хорошими проводниками тепла. Это связано с тем, что когда тепло передается одной части металлической решетки, делокализованные электроны на этом конце начинают поглощать тепловую энергию. После этого эти электроны начинают двигаться к холодному концу решетки. Таким образом, тепло передается от одного конца решетки к другому. Следовательно, это делает их хорошими теплопроводниками. Теплопроводность металлических предметов уменьшается с повышением температуры.
Следовательно, это делает их хорошими теплопроводниками. Теплопроводность металлических предметов уменьшается с повышением температуры.
- Блестящий:
В некоторых случаях они обладают блеском и цветом. Это также объясняется наличием подвижных электронов в металлической решетке. Свет сталкивается со свободными электронами, когда падает на поверхность решетки. В результате эти электроны возбуждаются и возвращаются из исходного положения. Во время этого движения они выделяют некоторую энергию в виде света.
- Непрозрачный:
Они непрозрачные. Это потому, что когда свет падает на металлические предметы, свет полностью поглощается электронным переходом моря электронов. Следовательно, свет не может проходить через них.
- Ковкий и пластичный:
Они очень податливы (превращаются в тонкие листы) и пластичны (превращаются в тонкую проволоку). Когда металлический кристалл бьют, верхний слой положительных ионов металла движется. После этого его место занимает еще один слой. Из-за своей подвижной природы в металлических объектах электроны также движутся вместе с положительным металлическим слоем.
После этого его место занимает еще один слой. Из-за своей подвижной природы в металлических объектах электроны также движутся вместе с положительным металлическим слоем.
Поэтому положение положительных ионов изменяется без нарушения структуры вещества, а свободно движущиеся электроны обеспечивают равномерное распределение зарядов. По этой причине они легко деформируются.
- Высокая температура кипения и плавления:
Поскольку позиционные ионы плотно упакованы в веществах, содержащих металлические связи, большинство из них имеют высокие температуры кипения и плавления и высокую плотность.
- Формование сплава:
Смеси металлов называются сплавами. Металлические предметы могут легко образовывать сплавы. В этих сплавах сферические ионы разных атомов делят одно и то же море электронов.
Вывод
Металлическая связь — это химическая связь, возникающая при соединении атомов металлических объектов. Главная сила удерживает вместе атомы металлического кристалла. Металлические связи возникают в результате совместного использования переменного числа электронов с переменным числом атомов. Это придает металлам их отличительные свойства.
Главная сила удерживает вместе атомы металлического кристалла. Металлические связи возникают в результате совместного использования переменного числа электронов с переменным числом атомов. Это придает металлам их отличительные свойства.
Q1. Каковы области применения металлической связки?
Ответ: Металлические связи удерживают металл вместе, но они также генерируют то море электронов, которое позволяет электронам течь. Без этого моря электронов, созданных металлическими связями, у нас не было бы всех приятных вещей, которые приносит электричество.
Q2. Чем металлическая связь отличается от ионной связи?
Ответ: Важные различия между металлическими связями и ионными связями:
| Металлическая связь | Ионная связь |
Эта связь образуется за счет одновременного взаимодействия притяжения между ядрами (положительно заряженными атомами металла) и подвижными электронами в металлическом кристалле. | Эта связь возникает в результате переноса электронов между двумя разнородными атомами. |
| Металлы ковкие. | Ионные соединения хрупкие. |
| Это слабая связь. | Это прочная связь из-за сильной электростатической силы притяжения. |
| Металлы являются хорошими проводниками в твердом состоянии. | Ионные соединения являются плохими проводниками в твердом состоянии. |
Q3. Чем металлическая связь отличается от ковалентной связи?
Ответ: Различия между металлическими и ковалентными связями:
| Металлическая связь | Ковалентная связь |
| Эта связь образуется за счет одновременного взаимодействия притяжения между ядрами и подвижными электронами в металлическом кристалле. | Эта связь образуется путем обмена электронами между двумя одинаковыми или разными атомами. |
| Это слабая связь, потому что многие ядра одновременно притягивают подвижные электроны. | Это сильная связь, потому что ядра сильно притягивают связанную электронную пару (или пары). |
| Металлы обычно твердые. | Ковалентные соединения обычно представляют собой жидкости и газы. |
| Металлы являются хорошими проводниками электричества. | Как правило, ковалентные твердые вещества являются плохими проводниками электричества (графит является исключением). |
| Эта облигация является ненаправленной. | Эта облигация является направленной. |
Q4. Как металлическая связь отвечает за более высокую температуру плавления и кипения переходных металлов, чем у щелочных металлов?
Ответ: Прочность металлической связи зависит от числа валентных электронов и заряда ядра. По мере увеличения числа валентных электронов и заряда прочность металлической связи увеличивается. Из-за этой реальности щелочные металлы мягкие и имеют низкие температуры плавления и кипения, а переходные металлы твердые и имеют высокие температуры плавления и кипения.
Из-за этой реальности щелочные металлы мягкие и имеют низкие температуры плавления и кипения, а переходные металлы твердые и имеют высокие температуры плавления и кипения.
Научные принципы
Научные принципыСтруктура металлов:
Металлы составляют около двух третей всех элементов и около 24% массы планеты. Они окружают нас повсюду в таких формах, как стальные конструкции, медные провода, алюминиевая фольга и золотые украшения. Металлы широко используются из-за их свойств: прочности, пластичности, высокой температуры плавления, тепло- и электропроводности, ударной вязкости.
Эти свойства также дают представление о структуре металлов. Как и все элементы, металлы состоят из атомов. Прочность металлов предполагает, что эти атомы удерживаются вместе сильными связями. Эти связи также должны позволять атомам двигаться; иначе как можно было бы металлы ковать в листы или вытягивать в провода? Разумной моделью была бы та, в которой атомы удерживаются вместе сильными, но делокализованными связями.
Склеивание
Такие связи могут образовываться между атомами металлов, которые имеют низкую электроотрицательность и не сильно притягивают свои валентные электроны. Это позволило бы разделить внешние электроны со всеми окружающими атомами, в результате чего положительные ионы ( катионы ) были окружены морем электронов (иногда называемым электронным облаком).
Поскольку эти валентные электроны являются общими для всех атомов, они не считаются связанными с каким-либо одним атомом. Это очень отличается от ионных или ковалентных связей, где электроны удерживаются одним или двумя атомами. Таким образом, металлическая связь является прочной и однородной. Поскольку электроны притягиваются ко многим атомам, они обладают значительной подвижностью, что обеспечивает хорошую тепло- и электропроводность, характерную для металлов.
При температуре выше точки плавления металлы являются жидкостями, а их атомы расположены случайным образом и относительно свободно перемещаются. Однако при охлаждении ниже точки плавления металлы перестраиваются, образуя упорядоченные кристаллические структуры.
Однако при охлаждении ниже точки плавления металлы перестраиваются, образуя упорядоченные кристаллические структуры.
Кристаллы
Для образования самых прочных металлических связей металлы упаковываются как можно плотнее. Возможны несколько вариантов упаковки. Вместо атомов представьте шарики, которые нужно упаковать в коробку. Шарики клали на дно коробки аккуратными ровными рядами, а затем начинали второй слой. Второй слой шариков не может быть размещен непосредственно поверх других шариков, поэтому ряды шариков в этом слое перемещаются в промежутки между шариками в первом слое. Первый слой мрамора может быть обозначен как A, а второй слой — как B, что дает двум слоям обозначение AB.
| Слой «A» | Слой «B» | Упаковка AB |
|---|
 Обратите внимание, что сферы слоя B подходят к отверстиям слоя A.
Обратите внимание, что сферы слоя B подходят к отверстиям слоя A.Для упаковки мрамора в третий слой требуется решение. Снова ряды атомов будут гнездиться в пустотах между атомами во втором слое, но существуют две возможности. Если ряды шариков уложены так, что они находятся непосредственно над первым слоем (А), то такое расположение можно описать как АВА. Такое насадочное устройство с чередующимися слоями будет обозначаться как АВАВАВ. Такое расположение ABAB называется гексагональной плотной упаковкой (HCP).
Если ряды атомов упакованы в этом третьем слое так, что они не лежат над атомами ни в слое A, ни в слое B, то третий слой называется C. Эта последовательность упаковки будет обозначаться ABCABC, а также известна как гранецентрированная кубическая (ГЦК). Обе компоновки дают максимально плотную упаковку сфер, оставляя лишь около четверти доступного пространства пустым.
Наименьший повторяющийся массив атомов в кристалле называется элементарной ячейкой. Третье распространенное устройство упаковки в металлах, объемно-центрированная кубическая (ОЦК) элементарная ячейка имеет атомы в каждом из восьми углов куба плюс один атом в центре куба. Поскольку каждый из угловых атомов является углом другого куба, угловые атомы в каждой элементарной ячейке будут общими для восьми элементарных ячеек. Элементарная ячейка ОЦК состоит из двух атомов, одного в центре и восьми восьмых от углов.
Третье распространенное устройство упаковки в металлах, объемно-центрированная кубическая (ОЦК) элементарная ячейка имеет атомы в каждом из восьми углов куба плюс один атом в центре куба. Поскольку каждый из угловых атомов является углом другого куба, угловые атомы в каждой элементарной ячейке будут общими для восьми элементарных ячеек. Элементарная ячейка ОЦК состоит из двух атомов, одного в центре и восьми восьмых от углов.
В конфигурации FCC снова восемь атомов по углам элементарной ячейки и по одному атому в центре каждой из граней. Атом на грани является общим с соседней клеткой. Элементарные ячейки ГЦК состоят из четырех атомов, восьми восьмых в углах и шести половинок на гранях. В таблице 1 показаны стабильные кристаллические структуры при комнатной температуре для нескольких элементарных металлов.
| Aluminum | FCC | Nickel | FCC | |
|---|---|---|---|---|
| Cadmium | HCP | Niobium | BCC | |
| Chromium | BCC | Platinum | FCC | |
| Кобальт | HCP | Серебро | FCC | FCC | Titanium | HCP |
| Gold | FCC | Vanadium | BCC | |
| Iron | BCC | Zinc | HCP | |
| Свинец | FCC | Цирконий | HCP | |
| Магний |
| Объемно-центрированный куб | Гранецентрированный куб |
|---|
Когда атомы расплавленного металла начинают собираться вместе, образуя кристаллическую решетку при температуре замерзания, группы этих атомов образуют крошечные кристаллы. Эти крошечные кристаллы увеличиваются в размерах за счет постепенного добавления атомов. Полученное твердое тело представляет собой не один кристалл, а множество более мелких кристаллов, называемых зернами. Эти зерна растут до тех пор, пока не столкнутся с соседними растущими кристаллами. Поверхность раздела, образующаяся между ними, называется границей зерна. Зерна иногда бывают достаточно большими, чтобы их можно было увидеть в обычный световой микроскоп или даже невооруженным глазом. Блестки, которые видны на только что оцинкованных металлах, представляют собой зерна. (См. Модель активности металлов в частицах.) На рис. 5 показан типичный вид поверхности металла с множеством зерен или кристаллов.
Поверхность раздела, образующаяся между ними, называется границей зерна. Зерна иногда бывают достаточно большими, чтобы их можно было увидеть в обычный световой микроскоп или даже невооруженным глазом. Блестки, которые видны на только что оцинкованных металлах, представляют собой зерна. (См. Модель активности металлов в частицах.) На рис. 5 показан типичный вид поверхности металла с множеством зерен или кристаллов.
Кристалл Дефекты:
Металлические кристаллы не идеальны. Иногда есть пустые пространства, называемые вакансиями, где отсутствует атом. Другим распространенным дефектом металлов являются дислокации, представляющие собой линии дефектного соединения. На рис. 6 показан один тип дислокации.

Эти и другие дефекты, а также наличие зерен и границ зерен определяют многие механические свойства металлов. Когда к металлу прикладывается напряжение, дислокации генерируются и перемещаются, позволяя металлу деформироваться.
Механические свойства:
При приложении малых нагрузок (напряжений) к металлам они деформируются, а при снятии нагрузки возвращаются к исходной форме. Изгиб листа стали является примером, когда связи изгибаются или растягиваются лишь на небольшой процент. Это называется упругой деформацией и связано с временным растяжением или изгибом связей между атомами.
При приложении более высоких напряжений возникает остаточная (пластическая) деформация. Например, если скрепку сильно согнуть, а затем отпустить, она останется частично согнутой. Эта пластическая деформация включает разрыв связей, часто за счет движения дислокаций. См. рис. 8. Дислокации легко перемещаются в металлах из-за делокализованной связи, но не так легко перемещаются в керамике. Это во многом объясняет, почему металлы пластичны, а керамика хрупка.
См. рис. 8. Дислокации легко перемещаются в металлах из-за делокализованной связи, но не так легко перемещаются в керамике. Это во многом объясняет, почему металлы пластичны, а керамика хрупка.
При слишком большом напряжении металлы будут механически разрушаться или ломаться. Это также может произойти с течением времени из-за множества небольших стрессов. Наиболее распространенной причиной (около 80%) разрушения металла является усталость. Из-за приложения и снятия небольших напряжений (до миллионов раз) по мере использования металла в металле образуются и медленно растут мелкие трещины. В конце концов металл необратимо деформируется или ломается (разламывается). (См. Деятельность по обработке металлов)
Обработка:
В промышленности расплавленный металл охлаждают до твердого состояния. Затем твердому металлу придают механическую форму для получения определенного продукта. То, как выполняются эти шаги, очень важно, потому что тепловая и пластическая деформация могут сильно повлиять на механические свойства металла.
То, как выполняются эти шаги, очень важно, потому что тепловая и пластическая деформация могут сильно повлиять на механические свойства металла.
Зернистость Эффект:
Давно известно, что свойства некоторых металлов можно изменить путем термообработки. Зерна в металлах имеют тенденцию к увеличению по мере нагревания металла. Зерно может увеличиваться за счет миграции атомов из другого зерна, которое в конечном итоге может исчезнуть. Дислокации не могут легко пересекать границы зерен, поэтому размер зерен определяет, насколько легко могут двигаться дислокации. Как и ожидалось, металлы с мелкими зернами прочнее, но менее пластичны. На рис. 5 показан пример зеренной структуры металлов.
Закалка и закалка:
Существует множество способов термической обработки металлов. Отжиг — это процесс размягчения, при котором металл нагревается, а затем медленно охлаждается. Большинство сталей можно закалить путем нагревания и закалки (быстрого охлаждения). Этот процесс использовался довольно рано в истории обработки стали. На самом деле считалось, что биологические жидкости являются лучшими закалочными жидкостями, и иногда использовалась моча. В некоторых древних цивилизациях раскаленные лезвия мечей иногда вонзались в тела незадачливых заключенных! Сегодня металлы закаливают в воде или масле. На самом деле закалка в растворах соленой воды происходит быстрее, так что древние не совсем ошибались.
Этот процесс использовался довольно рано в истории обработки стали. На самом деле считалось, что биологические жидкости являются лучшими закалочными жидкостями, и иногда использовалась моча. В некоторых древних цивилизациях раскаленные лезвия мечей иногда вонзались в тела незадачливых заключенных! Сегодня металлы закаливают в воде или масле. На самом деле закалка в растворах соленой воды происходит быстрее, так что древние не совсем ошибались.
В результате закалки металл становится очень твердым, но в то же время хрупким. Осторожно нагревая закаленный металл и позволяя ему медленно остывать, можно получить металл, который все еще остается твердым, но при этом менее хрупким. Этот процесс известен как закалка. (См. Деятельность по обработке металлов). Это приводит к множеству мелких выделений Fe 3 C в стали, которые блокируют движение дислокаций, тем самым обеспечивая упрочнение.
Холодная обработка:
Поскольку пластическая деформация возникает в результате движения дислокаций, металлы можно упрочнить, препятствуя этому движению. Когда металл изгибается или формуется, дислокации генерируются и перемещаются. По мере увеличения количества дислокаций в кристалле они запутываются или скрепляются и не могут двигаться. Это укрепит металл, затруднит его деформацию. Этот процесс известен как холодная обработка. При более высоких температурах дислокации могут перестраиваться, поэтому упрочнение происходит незначительно.
Когда металл изгибается или формуется, дислокации генерируются и перемещаются. По мере увеличения количества дислокаций в кристалле они запутываются или скрепляются и не могут двигаться. Это укрепит металл, затруднит его деформацию. Этот процесс известен как холодная обработка. При более высоких температурах дислокации могут перестраиваться, поэтому упрочнение происходит незначительно.
Вы можете попробовать это с помощью скрепки. Разогните скрепку и согните один из прямых участков несколько раз вперед и назад. Представьте, что происходит на атомном уровне. Обратите внимание, что согнуть металл в одном и том же месте труднее. Вывихи образовались и запутались, увеличивая прочность. Скрепка в конце концов сломается на изгибе. Холодная обработка, очевидно, работает только до определенной степени! Слишком сильная деформация приводит к клубку дислокаций, которые не могут двигаться, поэтому вместо этого ломается металл.
Нагрев устраняет последствия холодной обработки. При нагреве холоднодеформированных металлов происходит рекристаллизация. Новые зерна формируются и растут, чтобы потреблять холодную обработанную часть. В новых зернах меньше дислокаций и восстанавливаются исходные свойства.
Новые зерна формируются и растут, чтобы потреблять холодную обработанную часть. В новых зернах меньше дислокаций и восстанавливаются исходные свойства.
Сплавы:
Присутствие в металле других элементов также может изменить его свойства, иногда кардинально. Расположение и вид связи в металлах позволяет добавлять в структуру другие элементы, образуя смеси металлов, называемые сплавами. Даже если добавленные элементы являются неметаллами, сплавы могут иметь металлические свойства.
Медные сплавы производились очень рано в нашей истории. Бронза, сплав меди и олова, была первым известным сплавом. Его было легко изготовить, просто добавив олово в расплавленную медь. Инструменты и оружие из этого сплава были прочнее, чем из чистой меди. Добавление цинка к меди дает другой сплав, латунь. Хотя латунь труднее производить, чем бронзу, она также была известна в древние времена. (См. «Золотая» копейка.) Типичный состав некоторых сплавов приведен в таблице 2.

| Alloy | Composition |
|---|---|
| Brass | Copper, Zinc |
| Bronze | Copper, Zinc, Tin |
| Pewter | Tin, Copper, Bismuth, Antimony |
| Припой | Свинец, олово |
| Альнико | Алюминий, никель, кобальт, железо |
| Cast iron | Iron, Carbon, Manganese, Silicon |
| Steel | Iron, Carbon (plus small amounts of alloying elements) |
| Stainless Steel | Iron, Chromium, Nickel |
Сплавы являются смесями и их процентный состав может варьироваться. Это полезно, потому что свойствами сплавов можно управлять, изменяя состав. Например, электрикам нужен припой с другими свойствами, чем у сантехников. Электрический припой затвердевает очень быстро, обеспечивая почти мгновенное соединение. Это было бы нецелесообразно для сантехников, которым нужно некоторое время, чтобы установить соединение. Электрический припой содержит около 60% олова, тогда как припой для сантехники содержит около 30%.
Это полезно, потому что свойствами сплавов можно управлять, изменяя состав. Например, электрикам нужен припой с другими свойствами, чем у сантехников. Электрический припой затвердевает очень быстро, обеспечивая почти мгновенное соединение. Это было бы нецелесообразно для сантехников, которым нужно некоторое время, чтобы установить соединение. Электрический припой содержит около 60% олова, тогда как припой для сантехники содержит около 30%.
Первоначально олово содержало свинец, а поскольку олово использовалось для изготовления тарелок и кубков, вероятно, оно было источником отравления свинцом. Олово, сделанное сегодня, не содержит свинца. Расширение знаний о свойствах металлов также приводит к новым сплавам. Некоторые латуни образуют сплавы с памятью формы, которые можно сгибать и возвращать свою первоначальную форму при осторожном нагревании. Цинковые сплавы, используемые в качестве покрытия на стали, замедляют коррозию (оцинкованная сталь). Сплавы кадмия находят широкое применение в солнечных элементах. Способность мельхиора противостоять накоплению отложений делает его полезным для садков в рыбоводстве.
Способность мельхиора противостоять накоплению отложений делает его полезным для садков в рыбоводстве.
Железо и сталь:
Углеродистые стали различаются по процентному содержанию углерода. Количество углерода влияет на свойства стали и ее пригодность для конкретных целей. Стали редко содержат более 1% углерода. Конструкционная сталь содержит около 0,1-0,2% углерода по весу; это делает его немного более пластичным и менее склонным к разрушению во время землетрясений. Сталь, используемая для инструментов, содержит около 0,5-1% углерода, что делает ее более твердой и износостойкой. Чугун содержит от 2,5 до 4% углерода и находит применение в недорогих приложениях, где его хрупкость не является проблемой. Удивительно, но чистое железо чрезвычайно мягкое и используется редко. Увеличение количества углерода приводит к увеличению твердости металла, как показано на следующем графике. В медленно охлаждаемых сталях углерод увеличивает количество твердого Fe 3 С; в закаленных сталях он также увеличивает твердость и прочность материала.
Невидимые шпильки и скрепки обрабатываются практически одинаково, но содержат разное количество углерода. Невидимые шпильки и скрепки изготовлены из стальной проволоки холодной обработки. Скрепка для бумаг, содержащая мало углерода, в основном состоит из чистого Fe с небольшим количеством Fe 9.1236 3 С частицы. Невидимка содержит больше углерода и, следовательно, содержит большее количество Fe 3 C, что делает ее намного тверже и прочнее.
Свойства стали могут быть адаптированы для специального использования путем добавления в сплав других металлов. Титан, ванадий, молибден и марганец входят в число металлов, добавляемых в эти специальные стали. Нержавеющая сталь содержит минимум 12% хрома, который останавливает дальнейшее окисление, образуя на поверхности защитный оксид.
Коррозия:
Коррозия металлов может быть серьезной проблемой, особенно для долгосрочных структурных применений, таких как автомобили, мосты и корабли. Большинство коррозий носит электрохимический (гальванический) характер. Чтобы иметь коррозию, должны присутствовать анод (более легко окисляемая область) и катод (менее легко окисляемая область). Это могут быть разные типы металлов или просто разные участки на одном и том же металле. Также должен присутствовать какой-то электролит, который может обеспечить перенос электронов. Коррозия включает высвобождение электронов на аноде из-за высокого окислительного потенциала атомов на аноде. По мере высвобождения электронов образуются катионы металлов, и металл распадается. В то же время катод, имеющий более высокий восстановительный потенциал, принимает электроны, либо образуя отрицательные ионы, либо нейтрализуя положительные ионы.
В случае ряда активности или электродвижущей силы такой металл, как цинк, реагирует с водородом и служит как анодом, так и катодом. (См. ряд действий.) Уравнение этой реакции:
(См. ряд действий.) Уравнение этой реакции:
Пузырьки водорода на катоде при разрушении анода. Дефекты поверхности, наличие примесей, ориентация зерен, локальные напряжения и изменения окружающей среды — вот некоторые из факторов, определяющих, почему один кусок металла может служить обоими электродами. Например, шляпка и острие гвоздя были подвергнуты холодной обработке и могут служить анодом, а тело — катодом. (См. Коррозия активности железа)
Хотя окисление на аноде и восстановление на катоде являются одновременными процессами, коррозия обычно возникает на аноде. Катод почти никогда не разрушается. В 1824 году Дэви разработал метод защиты корпусов кораблей от коррозии с помощью периодически заменяемого цинка. Цинк более активен, чем сталь в корпусе, он будет служить анодом и подвергаться коррозии; он приносится в жертву для защиты стальной конструкции. Сталь, которая была бы и анодом, и катодом, обычно служит катодом. Это называется катодной защитой. Трубопроводы также защищены более активным металлом магнием. Иногда электрические токи поддерживаются на коротких участках трубопроводов с такой же металлической проволокой, которая служит расходуемым анодом.
Это называется катодной защитой. Трубопроводы также защищены более активным металлом магнием. Иногда электрические токи поддерживаются на коротких участках трубопроводов с такой же металлической проволокой, которая служит расходуемым анодом.
Коррозия является серьезной проблемой, которую необходимо решить, чтобы эффективно использовать металлы. Железо соединяется с кислородом в воздухе, образуя оксид железа (ржавчину), в конечном итоге разрушая полезность металла. (См. Необязательно: Химические грелки для рук.) К счастью, некоторые металлы, такие как алюминий и хром, образуют защитное оксидное покрытие, которое предотвращает дальнейшее окисление (коррозию). Точно так же медь соединяется с серой и кислородом, образуя знакомую зеленую патину.
Понимание химии металлов приводит к разработке методов уменьшения и предотвращения коррозии. Атомы хрома имеют примерно такой же размер, как атомы железа, и могут замещать их в кристаллах железа. Хром образует оксидный слой, который позволяет нержавеющей стали противостоять коррозии. Металлы могут быть окрашены или покрыты другими металлами; например, оцинкованная (оцинкованная) сталь. Когда эти два металла используются вместе, более активный цинк подвергается коррозии, жертвуя собой ради спасения стали.
Металлы могут быть окрашены или покрыты другими металлами; например, оцинкованная (оцинкованная) сталь. Когда эти два металла используются вместе, более активный цинк подвергается коррозии, жертвуя собой ради спасения стали.
Металлические руды:
Золото, серебро и медь были первыми используемыми металлами, потому что они находятся в свободном или элементарном состоянии. Большинство металлов, встречающихся в природе, сочетаются с другими элементами, такими как кислород и сера. Энергия необходима для извлечения металлов из этих соединений или руд. Исторически сложилось так, что легкость, с которой тот или иной металл можно было извлечь из руды, наряду с его доступностью, определялась временем его использования, отсюда и раннее использование меди, олова и железа. Формулы для некоторых руд приведены ниже:
| Hematite | Fe 2 O 3 | Rutile | TiO 2 |
|---|---|---|---|
| Magnetite | Fe 3 O 4 | Zircon | ZrSiO 4 |
| Pyrite | FES 2 | Касситерит | SNO 2 |
| Chalcocit0996 Al 2 O 3 | |||
| Киноварь | HgS | Галенит | PbS |
Эти руды представляют собой ионные соединения, в которых металлы существуют в виде положительных ионов. Например, степень окисления железа в гематите +3; степень окисления меди в халькозине +1. Извлечение металлов из их руд представляет собой окислительно-восстановительную (окислительно-восстановительную) реакцию. В элементарном состоянии металлы состоят из атомов, а не ионов. Поскольку атомы не имеют общего заряда, ионы металлов в реакции приобретают электроны; они уменьшены.
Например, степень окисления железа в гематите +3; степень окисления меди в халькозине +1. Извлечение металлов из их руд представляет собой окислительно-восстановительную (окислительно-восстановительную) реакцию. В элементарном состоянии металлы состоят из атомов, а не ионов. Поскольку атомы не имеют общего заряда, ионы металлов в реакции приобретают электроны; они уменьшены.
Общая реакция восстановления меди из халькоцита:
Это только общая реакция. Полный процесс не так прост. Восстановление металлов из их руд обычно требует ряда химических и механических процессов. Обычно они энергетически дороги, потребляют большое количество тепла и/или электроэнергии. Например, около пяти процентов электроэнергии, потребляемой в США, используется для производства алюминия. Производство алюминиевой банки из-под руды стоит примерно в сто раз дороже, чем плавление и формирование переработанного алюминия. При извлечении металлов из руд также могут образовываться загрязняющие вещества, такие как двуокись серы, описанная выше. Когда это возможно, переработка и переработка металлов имеет смысл.
При извлечении металлов из руд также могут образовываться загрязняющие вещества, такие как двуокись серы, описанная выше. Когда это возможно, переработка и переработка металлов имеет смысл.
Относительная сложность извлечения металлов из их руд указывает на то, что это их предпочтительное состояние. После извлечения из руд и в элементарном состоянии большинство металлов проявляют значительную склонность вступать в реакцию с кислородом и серой и возвращаться в свое естественное состояние; они ржавеют! При коррозии металл окисляется. Он теряет электроны, превращаясь в положительный ион. (См. активность коррозии металлов)
Краткое описание металлов
Металлы обладают полезными свойствами, включая прочность, пластичность, высокие температуры плавления, тепло- и электропроводность и ударную вязкость. Они широко используются для структурных и электрических применений. Понимание структуры металлов может помочь нам понять их свойства.
Атомы металлов связаны друг с другом прочными делокализованными связями. Эти связи образованы облаком валентных электронов, которые распределяются между положительными ионами металлов (катионами) в кристаллической решетке. При таком расположении валентные электроны обладают значительной подвижностью и способны легко проводить тепло и электричество. В кристаллической решетке атомы металла плотно упакованы, чтобы максимизировать прочность связей. Настоящий кусок металла состоит из множества крошечных кристаллов, называемых зернами, которые соприкасаются границами зерен.
Эти связи образованы облаком валентных электронов, которые распределяются между положительными ионами металлов (катионами) в кристаллической решетке. При таком расположении валентные электроны обладают значительной подвижностью и способны легко проводить тепло и электричество. В кристаллической решетке атомы металла плотно упакованы, чтобы максимизировать прочность связей. Настоящий кусок металла состоит из множества крошечных кристаллов, называемых зернами, которые соприкасаются границами зерен.
Из-за делокализованной природы связей атомы металла могут скользить друг относительно друга, когда металл деформируется, а не разрушаться, как хрупкий материал. Это движение атомов осуществляется за счет образования и движения дислокаций в решетке. Методы обработки, которые изменяют связь между атомами или влияют на количество или подвижность дислокаций, могут иметь большое влияние на механические свойства металла.
Упругая деформация металла представляет собой небольшое изменение формы при низком напряжении, которое восстанавливается после снятия напряжения. Этот тип деформации включает растяжение металлических связей, но атомы не скользят друг относительно друга. Пластическая деформация возникает, когда напряжение достаточно, чтобы необратимо деформировать металл. Этот тип деформации включает разрыв связей, обычно за счет движения дислокаций.
Этот тип деформации включает растяжение металлических связей, но атомы не скользят друг относительно друга. Пластическая деформация возникает, когда напряжение достаточно, чтобы необратимо деформировать металл. Этот тип деформации включает разрыв связей, обычно за счет движения дислокаций.
Пластическая деформация приводит к образованию большего количества дислокаций в металлической решетке. Это может привести к уменьшению подвижности этих дислокаций из-за их склонности к запутыванию или закреплению. Пластическая деформация при температурах, достаточно низких, чтобы атомы не могли перегруппироваться (холодная обработка), может упрочнить металл в результате этого эффекта. Одним из побочных эффектов является то, что металл становится более хрупким. По мере использования металла трещины имеют тенденцию образовываться и расти, что в конечном итоге приводит к его поломке или разрушению.
Дислокации не могут легко пересекать границы зерен. Если металл нагреть, зерна могут увеличиться, и материал станет мягче. Нагрев металла и его быстрое охлаждение (закалка) с последующим мягким нагревом (отпуском) приводит к получению более твердого материала из-за образования множества мелких выделений Fe 3 C, которые блокируют дислокации.
Нагрев металла и его быстрое охлаждение (закалка) с последующим мягким нагревом (отпуском) приводит к получению более твердого материала из-за образования множества мелких выделений Fe 3 C, которые блокируют дислокации.
Смешивание металлов с другими металлами или неметаллами может привести к получению сплавов с желаемыми свойствами. Сталь, изготовленная из железа и углерода, может существенно различаться по твердости в зависимости от количества добавленного углерода и способа ее обработки. Некоторые сплавы обладают более высокой коррозионной стойкостью.
Коррозия является серьезной проблемой для большинства металлов. Это окислительно-восстановительная реакция, в которой атомы металла образуют ионы, вызывающие ослабление металла. Один из методов, который был разработан для борьбы с коррозией в конструкциях, включает в себя прикрепление расходуемого анода из металла с более высоким потенциалом окисления. При таком расположении анод подвергается коррозии, а катод, конструктивная часть, остается неповрежденным. Образование защитного покрытия на внешней стороне металла также может противостоять коррозии. Стали, содержащие металлический хром, образуют защитное покрытие из оксида хрома. Алюминий также устойчив к коррозии благодаря образованию прочного оксидного покрытия. Медь образует знакомую зеленую патину, реагируя с серой и кислородом в воздухе.
Образование защитного покрытия на внешней стороне металла также может противостоять коррозии. Стали, содержащие металлический хром, образуют защитное покрытие из оксида хрома. Алюминий также устойчив к коррозии благодаря образованию прочного оксидного покрытия. Медь образует знакомую зеленую патину, реагируя с серой и кислородом в воздухе.
В природе можно найти лишь несколько чистых металлов. Большинство металлов существуют в виде руд, соединений металла с кислородом или серой. Отделение чистого металла от руды часто требует больших затрат энергии в виде тепла и/или электричества. Из-за больших затрат энергии имеет смысл по возможности перерабатывать металлы.
Вопросы для обсуждения
1. Как добывают руду из земли?
2. Назовите 4 сплава и металлы, из которых они изготовлены.
3. Какое влияние оказывает «холодная обработка» на металлы?
4. Какой процесс делает металлы твердыми, но хрупкими?
5. Какой процесс делает металлы мягче и легче в обработке?
6. Укажите три метода уменьшения коррозии.
Укажите три метода уменьшения коррозии.
7. Дайте 2 ценные воздействия утилизации.
Проблема
Предположим, что радиус одного атома железа составляет 1,24 ангстрема (1 ангстрем = 1 x 10 -8 см). Какова будет плотность объемно-центрированного кубического (ОЦК) железа в граммах на кубический сантиметр? Подсказка: Найдите массу и объем одной элементарной ячейки. Не забудьте подсчитать только долю каждого атома в ячейке.
Добавочный номер:
Максимальная растворимость углерода в ОЦК-железе составляет один атом на каждые 5000 атомов железа. Какова будет плотность стали при максимальном количестве растворенного углерода?
Решение
= m/V = количество атомов x (масса/атом) / объем ячейки
В ОЦК-железе на элементарную ячейку приходится два атома железа. (8 х 1/8 + 1)
Один атом железа имеет массу 55,85 а.е.м. или 9,27 х 10 -23 грамм.
Общая масса одной элементарной ячейки составляет 1,85 х 10 -22 грамм.
Пусть (r) — радиус атома железа. Атомы в углах контактируют с атомом в середине, делая диагональ коробки равной (4r).
Если мы назовем одну сторону прямоугольника (L), диагональ грани куба будет равна (квадратный корень из 2), умноженный на (L).
Одна сторона, диагональ грани куба и диагональ прямоугольника образуют прямоугольный треугольник. Используя теорему Пифагора, (L) 2 + (квадратный корень 2 x (L)) 2 = (4r) 2 .
Решая для L и подставляя (r), мы находим, что L = 2,86 ангстрема или 2,86 x 10 -8 см.
Объем куба (элементарной ячейки) равен (л) 3 = 2,34 x 10 -23 см 3 . Разделив массу на объем, получим:
Плотность = 7,91 г/см 3 .
Next Topic:References
Металлы Содержание Главная страница МАСТ
Материаловедение
МатериаловедениеМатериаловедение
| Материаловедение | Склеивание в твердых телах | Структуры твердых тел |
Материаловедение
Вы когда-нибудь задумывались, почему серебряное зеркало отражает свет, проходящий через лист? из стекла? Почему металлический корпус автомобиля, оставленный на летнем солнце, кажется намного горячее, чем трава, рядом с которой он был припаркован? Почему стекло разбивается при падении на пол, но не ложка, используемая для размешивания содержимого? Почему металлы проводят и тепло, и электричество, но не керамика, такая как плитка, которая защищает космический шаттл, когда он снова входит в атмосферу?
Ответы на эти и многие другие вопросы лежат в области поля
известный как материаловедение . Борьба за использование материалов не нова,
он восходит к доисторическим временам. Но последние достижения в области синтеза и использования
материалы, основанные на понимании их структуры и свойств, а не
методом проб и ошибок были получены новые материалы с революционными свойствами. Теперь у нас есть
керамическая посуда, которая может попасть прямо из холодильника на горячую конфорку без
ломать. Интегральные схемы, которые сделали компьютеры такими, о которых можно было только мечтать
двадцать лет назад — компьютер на каждом столе. У нас есть новые сплавы для использования в самолетах или
теннисные ракетки, обеспечивающие силу без веса. И мы сделали первые шаги
к сверхпроводящим материалам, которые позволят нам строить поезда, парящие над
поверхности дорожек, по которым они проходят.
Борьба за использование материалов не нова,
он восходит к доисторическим временам. Но последние достижения в области синтеза и использования
материалы, основанные на понимании их структуры и свойств, а не
методом проб и ошибок были получены новые материалы с революционными свойствами. Теперь у нас есть
керамическая посуда, которая может попасть прямо из холодильника на горячую конфорку без
ломать. Интегральные схемы, которые сделали компьютеры такими, о которых можно было только мечтать
двадцать лет назад — компьютер на каждом столе. У нас есть новые сплавы для использования в самолетах или
теннисные ракетки, обеспечивающие силу без веса. И мы сделали первые шаги
к сверхпроводящим материалам, которые позволят нам строить поезда, парящие над
поверхности дорожек, по которым они проходят.
Склеивание в твердых телах
Первый шаг к пониманию этих достижений в материаловедении — это
сформировать базовые представления о строении твердых тел.
Химики обычно классифицируют твердые вещества как металлические , ионные , молекулярные , или ковалентной сети на основе макроскопических различий в их физических свойства, которые являются результатом различий в связи на атомном уровне.
Связь между атомами в твердом теле определяется комбинацией двух факторов: величина электроотрицательности атомов в твердом теле и различия между эти электроотрицательности. В результате треугольник типа связи, показанный на рисунке ниже можно использовать для предсказания классификации, в которую должно попасть твердое тело. Соединения с металлические связи должны быть металлическими твердыми телами, с ионными связями должны быть ионными твердыми телами, а те, у которых есть ковалентные связи, должны быть либо молекулярными, либо сетчатыми ковалентными твердыми телами.
Треугольник типа соединения, показывающий классификацию типов соединения на основе среднего
электроотрицательность и различия в электроотрицательности. |
Металлические твердые вещества ожидаются для комбинаций атомов, электроотрицательность и различия в электроотрицательности помещают их в нижний левый угол типа связи треугольник, показанный на рисунке выше. Ионные соединения находятся в центре, ближе к вершине этого треугольника, а ковалентные материалы находятся в правом нижнем углу.
Твердые тела описываются с точки зрения их точек решетки , которые
определяется как регулярное периодическое расположение частиц в твердом теле. Металлик
твердые тела состоят из плоскостей отдельных атомов металла, удерживаемых вместе
сильная сила притяжения между этими атомами, как показано на рисунке ниже. Атомы металла
не имеют достаточного количества электронов, чтобы заполнить свои валентные оболочки, разделяя электроны со своими
непосредственные соседи. Таким образом, валентные электроны являются общими для многих атомов, делокализация эти электроны над многими атомами. Поскольку эти валентные электроны не связаны прочно с
отдельные атомы, они могут свободно мигрировать в металле. В результате металлы хороши
проводники электричества. Электроны, попадающие в металл с одного края, могут вытеснять с другого
электронов, чтобы вызвать чистый поток электричества через металл.
Поскольку эти валентные электроны не связаны прочно с
отдельные атомы, они могут свободно мигрировать в металле. В результате металлы хороши
проводники электричества. Электроны, попадающие в металл с одного края, могут вытеснять с другого
электронов, чтобы вызвать чистый поток электричества через металл.
Когда твердое тело содержит два или более элементов, для которых существует большое разность электроотрицательности, электроны переходят от одного атома к другому, образуя ионное твердое вещество . Точки решетки в этих твердых телах положительны и отрицательные ионы, такие как ионы Na + и Cl — , показанные на рисунке ниже, которые удерживаются вместе сильными ионными связями.
Ковалентные соединения обычно кристаллизуются в виде молекулярных твердых веществ , в которых
точки решетки заняты отдельными молекулами, например, в структуре сухого льда
показано на рисунке ниже. Отдельные молекулы удерживаются вместе относительно прочными внутримолекулярных связей между атомами, образующими молекулу. Гораздо более слабые межмолекулярные соединения связи между этими молекулами являются результатом относительно слабых ван-дер-ваальсовых сил. Силы Ван-дер-Ваальса
удерживание молекул CO 2 вместе в сухом льду, например, настолько слабое, что сухой
лед возвышается, он проходит прямо
из твердой фазы в газовую
при -78С.
Отдельные молекулы удерживаются вместе относительно прочными внутримолекулярных связей между атомами, образующими молекулу. Гораздо более слабые межмолекулярные соединения связи между этими молекулами являются результатом относительно слабых ван-дер-ваальсовых сил. Силы Ван-дер-Ваальса
удерживание молекул CO 2 вместе в сухом льду, например, настолько слабое, что сухой
лед возвышается, он проходит прямо
из твердой фазы в газовую
при -78С.
Сетчатые ковалентные твердые вещества представляют собой уникальный класс материалов, которые можно
рассматривается как единая гигантская молекула, состоящая из почти бесконечного числа ковалентных связей,
такие как структура алмаза, показанная на рисунке ниже. Поскольку все облигации в
эта структура одинаково сильна, ковалентные твердые тела часто очень тверды, и они
известно, что его трудно расплавить. Алмаз — самое твердое природное вещество, плавится при
3550С.
Алмаз — самое твердое природное вещество, плавится при
3550С.
Строение твердых тел
Структура материала определяется тем, как простейшие повторяющиеся единицы расположены в пространстве. Когда эти простые повторяющиеся единицы встречаются регулярно от одного конца твердого тела к другому говорят, что материал кристаллический . Наилучшая связь между физическими свойствами материала и его структурой иллюстрируется различными элементарными формами углерода.
Углерод встречается в виде различных аллотропов. Существуют две кристаллические формы алмаза и графита и ряд аморфных форм. (некристаллические) формы, такие как древесный уголь, кокс и сажа.
Ссылки на характеристическую твердость алмаза (от греческого adamas ,
«непобедимый») насчитывают не менее 2600 лет. Однако только в 1797 г.
что Смитсон Теннант смог показать, что алмазы состоят исключительно из углерода.
свойства алмаза замечательны. Он имеет одну из самых высоких температур плавления ( МП = 3550 o С) и температурах кипения ( л.н. = 4827 o С) любых природных
встречающееся вещество. Это также самое твердое природное вещество, и оно меньше расширяется при
нагрев, чем любой другой материал.
Однако только в 1797 г.
что Смитсон Теннант смог показать, что алмазы состоят исключительно из углерода.
свойства алмаза замечательны. Он имеет одну из самых высоких температур плавления ( МП = 3550 o С) и температурах кипения ( л.н. = 4827 o С) любых природных
встречающееся вещество. Это также самое твердое природное вещество, и оно меньше расширяется при
нагрев, чем любой другой материал.
Характерные свойства алмаза являются прямым результатом его структуры. углерод,
с четырьмя валентными электронами образует ковалентные связи с четырьмя соседними атомами углерода
расположены по углам тетраэдра, как показано на рисунке ниже. Каждый из них
атомы затем связаны с четырьмя другими атомами углерода, которые образуют связи с четырьмя другими атомами, и
скоро. В результате идеальный алмаз представляет собой единую гигантскую молекулу. Сила
отдельные облигации CC и их
расположение в пространстве порождают необычные свойства алмаза.
В некотором смысле графит по своим свойствам подобен алмазу. Оба соединения кипят при 4827 o C, например. Но графит также сильно отличается от алмаза. Графит намного менее плотный, чем алмаз. Принимая во внимание, что алмаз является самым твердым из известных веществ, графит — один из самых мягких. Алмаз — отличный изолятор, графит — хороший изолятор. проводник электричества, что графитовые электроды используются в электрических элементах.
Физические свойства графита можно понять по структуре твердого тела
показано на рисунке ниже. Графит состоит из вытянутых плоскостей атомов углерода, в которых
каждый углерод образует прочные ковалентные связи с тремя другими атомами углерода. (крепкие связи
между атомами углерода внутри каждой плоскости объясняют исключительно высокую температуру плавления
точка и точка кипения графита.) Эти плоскости атомов, однако, удерживаются вместе
относительно слабые силы Ван-дер-Ваальса. Потому что облигации между плоскостями атомов слабы, легко деформировать твердое тело, позволив одной плоскости атомов двигаться относительно
другому. Таким образом, графит достаточно мягкий, чтобы его можно было использовать в карандашах и в качестве смазки для
моторное масло.
Потому что облигации между плоскостями атомов слабы, легко деформировать твердое тело, позволив одной плоскости атомов двигаться относительно
другому. Таким образом, графит достаточно мягкий, чтобы его можно было использовать в карандашах и в качестве смазки для
моторное масло.
Характерные свойства графита и алмаза могут привести вас к
ожидать, что алмаз будет более стабильным, чем графит. Это не то, что наблюдается
экспериментально. Графит при 25°С и давлении 1 атм несколько более стабилен, чем алмаз.
(Энтальпия соединения атомов графита составляет -5557 кДж/моль RXN и тот из
алмаз составляет -5523 кДж/моль rxn ). Однако при очень высоких температурах и давлениях
алмаз становится более стабильным, чем графит. В 1955 году General Electric разработала процесс
производить алмазы промышленного качества путем обработки графита металлическим катализатором при температуре
от 2000 до 3000 К и давления выше 125000 атм. Примерно 40% промышленного качества
бриллианты теперь синтетические. Хотя алмазы ювелирного качества можно синтезировать, затраты
участие являются запретительными.
Примерно 40% промышленного качества
бриллианты теперь синтетические. Хотя алмазы ювелирного качества можно синтезировать, затраты
участие являются запретительными.
И алмаз, и графит встречаются в виде правильно упакованных кристаллов. Другие формы углерода аморфные им не хватает регулярная структура. Древесный уголь получается при нагревании древесины в отсутствие кислорода. Чтобы получить сажу , природный газ сжигается в ограниченном количестве воздуха, чтобы получить густой черный дым, содержащий чрезвычайно мелкие частицы углерода, которые можно собрать когда газ охлаждается и проходит через электрофильтр. Кокс это более регулярно структурированный материал, более близкий по структуре к графиту, чем любой древесный уголь или сажа, которая сделана из угля.
В 1985 году путем испарения графита с
лазер. Продуктом этой реакции является молекула с формулой C 60 , которая
имеет структуру с симметрией футбольного мяча. Поскольку эта структура напоминает
геодезический купол, изобретенный Р. Бакминстером Фуллером, C 60 был назван бакминстерфуллерен ,
или «бакибол» для краткости.
Поскольку эта структура напоминает
геодезический купол, изобретенный Р. Бакминстером Фуллером, C 60 был назван бакминстерфуллерен ,
или «бакибол» для краткости.
Некоторое очарование C 60 можно понять, сопоставив эту форму чистый углерод с алмазом и графитом. C 60 уникален, потому что существует как отдельные молекулы, а не протяженные массивы атомов. Не менее важно, C 60 может быть получается как чистое вещество, тогда как поверхности алмаза и графита неизбежно загрязнены атомами водорода, которые связываются с атомами углерода на поверхности.
В настоящее время известно, что C 60 является членом семейства соединений, известных как фуллерены .
C 60 может быть самым важным из фуллеренов, потому что он наиболее
возможна идеально симметричная молекула, вращающаяся в твердом теле со скоростью более 100
миллионов раз в секунду. Из-за своей симметрии молекулы C 60 упаковываются как
регулярно как шарики для пинг-понга. Полученное твердое вещество обладает необычными свойствами. Изначально это
мягкий, как графит, но при сжатии на 30% становится тверже алмаза. Когда это
давление сбрасывается, твердое тело возвращается к своему первоначальному объему. С 60 поэтому обладает замечательным свойством отскакивать назад при попадании в металлическую поверхность в
высокие скорости.
Полученное твердое вещество обладает необычными свойствами. Изначально это
мягкий, как графит, но при сжатии на 30% становится тверже алмаза. Когда это
давление сбрасывается, твердое тело возвращается к своему первоначальному объему. С 60 поэтому обладает замечательным свойством отскакивать назад при попадании в металлическую поверхность в
высокие скорости.
C 60 также обладает замечательной способностью образовывать соединения, в которых он является
изолятор, проводник, полупроводник или сверхпроводник. Сам по себе C 60 является
полупроводник. При смешивании с достаточным количеством калия, чтобы получить соединение с
эмпирическая формула K 3 C 60 , он проводит электричество, как металл. Когда
добавляется избыток калия, это твердое вещество становится изолятором. Когда К 3 С 60 охлаждается до 18 К, в результате получается сверхпроводник. Потенциал химии фуллеренов
как для практических материалов, так и для лабораторных диковин, достаточно велика, чтобы объяснить, почему
эта молекула была описана как «экзохармическая», она излучает очарование.
Материаловедение
Материаловедение | Металлы и элементарные ячейки | Подробнее о материаловедении | Керамика
Периодический Таблица | Глоссарий | Прохладный Апплеты
Если вы видите это, ваш браузер не поддерживает JavaScript. Периодическая таблица
Тематический обзор Gen Chem | Главная страница справки по общей химии | Поиск: Сайт общей химии.
Металлическая связь и структура железа | 14-16 лет | План урока
Узнайте, как связывание железа связано с его физическими свойствами, и развейте распространенные заблуждения, используя этот план урока с заданиями для детей 14–16 лет
В этом упражнении учащиеся решают, верны или нет ряд утверждений о связи в железе. Это приводит к дальнейшим размышлениям и дискуссиям о связи в металлах.
Это упражнение проверяет ошибочные представления о том, что:
- Структура железа является примером гигантской молекулы.

- Атомы железа удерживаются вместе ионными связями.
- Железо проводит электричество, потому что атомы железа движутся через твердое тело.
- Железо расширяется при нагревании, потому что атомы становятся больше.
- Металлическое железо — это серебро, потому что атомы железа — это серебро.
Цели обучения
Учащиеся смогут:
- Описать связь в железе и использовать это для объяснения физических свойств металла.
Последовательность действий
Введение
- Дайте каждому учащемуся гвоздь или скрепку, чтобы он посмотрел и потрогал их в качестве стимула для концентрации внимания.
- Поделитесь со студентами тем, что они собираются:
- Опишите соединение в железе.
- Объясните свойства металла, используя их представления о связи.
Упражнение: этап 1
Раздайте каждому учащемуся лист вопросов «Связь металлов и структура железа», содержащий 10 утверждений о структуре и свойствах железа. Попросите их работать индивидуально по телефону:
Попросите их работать индивидуально по телефону:
- Прочитайте вопросы.
- Запишите в таблицу, считают ли они утверждения верными или ложными.
Упражнение: этап 2
Объедините учащихся в группы по три человека, чтобы:
- Рассмотрите каждый вопрос по очереди.
- Поделитесь своими отзывами и идеями.
- Согласовать групповой ответ.
- Запишите каждый ответ.
- Запишите индивидуально, как они изменили свои идеи в результате обсуждения.
Упражнение: этап 3
Выдайте мини-доски и спросите:
- Каждый учащийся должен нарисовать рисунок, изображающий соединение железа.
- Некоторые ученики делятся своими идеями.
Продемонстрируйте с помощью информационного проектора электронную анимацию структуры металла и того, что с ним происходит при нагревании или подключении к батарее. Задайте вопросы:
- . Сделайте явную картину металлической связи с точки зрения внешней оболочки электронов, свободно перемещающихся через гигантскую решетку положительных ионов.

- Объясните использование этой модели металлической связи для объяснения физических свойств, включая проводимость электричества, расширение при нагревании и внешний вид.
- Распространите представления о связи (и, следовательно, их физических свойствах) на металлы в целом.
Перед окончанием
Предоставьте учащимся возможность:
- Добавить к тому, что уже есть в вопроснике «Металлическая связь и структура железа».
- Напишите их имя.
Обратная связь
Просмотрите листы и прокомментируйте, как развивались их идеи, и обратите внимание на пути дальнейшего развития учащегося.
Тактильный стимул помогает учащимся оценить цели занятия.
Работая в группах, учащиеся сравнивают свои идеи с другими, переоценивают свои первоначальные идеи и при необходимости развивают их. Наводящие вопросы имеют основополагающее значение для устранения неверных представлений и их замены правильной моделью. На протяжении всего урока учащимся предлагается проверить свое понимание.
На протяжении всего урока учащимся предлагается проверить свое понимание.
Финальная проверка на этапе обратной связи сопровождается указанием дальнейших шагов, которые должен предпринять студент.
Оборудование
Для демонстрации (если возможно):
- Электронная анимация, показывающая структуру металла и что с ним происходит при нагревании металла или при подключении к батарее.
- Проектор данных.
Для каждого учащегося:
- Гвоздь или скрепка.
- Мини-доска.
Ответы и примечания к ответам
- Железо имеет тип связи, называемый металлической связью.
- ИСТИНА. Железо — это металл, и все металлы имеют тип связи, называемый металлической связью, которая отличается от ковалентной или ионной связи. При металлической связи внешние оболочки соседних атомов перекрываются, и электроны внешних оболочек могут свободно перемещаться по решетке. Металл состоит из катионов металла и уравновешивающего числа этих «свободных» электронов.

- ИСТИНА. Железо — это металл, и все металлы имеют тип связи, называемый металлической связью, которая отличается от ковалентной или ионной связи. При металлической связи внешние оболочки соседних атомов перекрываются, и электроны внешних оболочек могут свободно перемещаться по решетке. Металл состоит из катионов металла и уравновешивающего числа этих «свободных» электронов.
- Структура железа является примером гигантской молекулы.
- ЛОЖЬ. В железе положительные ионы упакованы вместе в гигантскую решетку, но мы используем слово «молекула», чтобы подразумевать, что структура содержит ковалентные связи, которых нет в железе.
- В структуре железа есть положительные ионы.
- ИСТИНА. Поскольку электроны во внешней оболочке могут свободно перемещаться по решетке, они оставляют после себя положительные ионы железа.
- Атомы железа удерживаются вместе ионными связями.
- ЛОЖЬ. Связь в железе металлическая. Это отличается от ионной связи, поскольку в ней отсутствуют отрицательные анионы.
- В структуре железа некоторые электроны могут двигаться вокруг твердого тела.
- ИСТИНА. Электроны с внешней оболочки атомов могут свободно перемещаться через решетку положительных ионов.
- Если железо нагреть до очень высокой температуры, оно станет газом.

- ИСТИНА. Если железо нагреть, оно расплавится. Если расплавленное железо нагреть до достаточно высокой температуры, оно закипит.
- Железо может проводить электричество, потому что атомы железа могут скользить по своим соседям и двигаться сквозь твердое тело.
- ЛОЖЬ. Катионы железа обычно зафиксированы в своих позициях в решетке и не могут перемещаться.
- Железо проводит электричество, потому что оно содержит «море» электронов.
- ИСТИНА. Электроны из внешних оболочек атомов могут двигаться и проходить через металл, когда он подключен к батарее.
- Железо расширяется при нагревании, потому что атомы железа становятся больше.
- ЛОЖЬ. При нагревании железа положительные катионы вибрируют сильнее и отдаляются друг от друга.
- Железо — серебристо-серый металл, потому что атомы железа серебристо-серые.

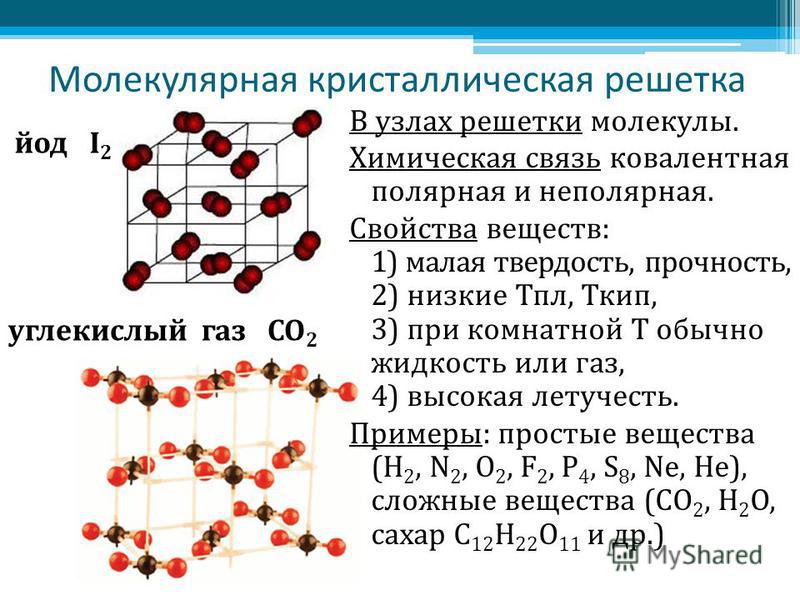
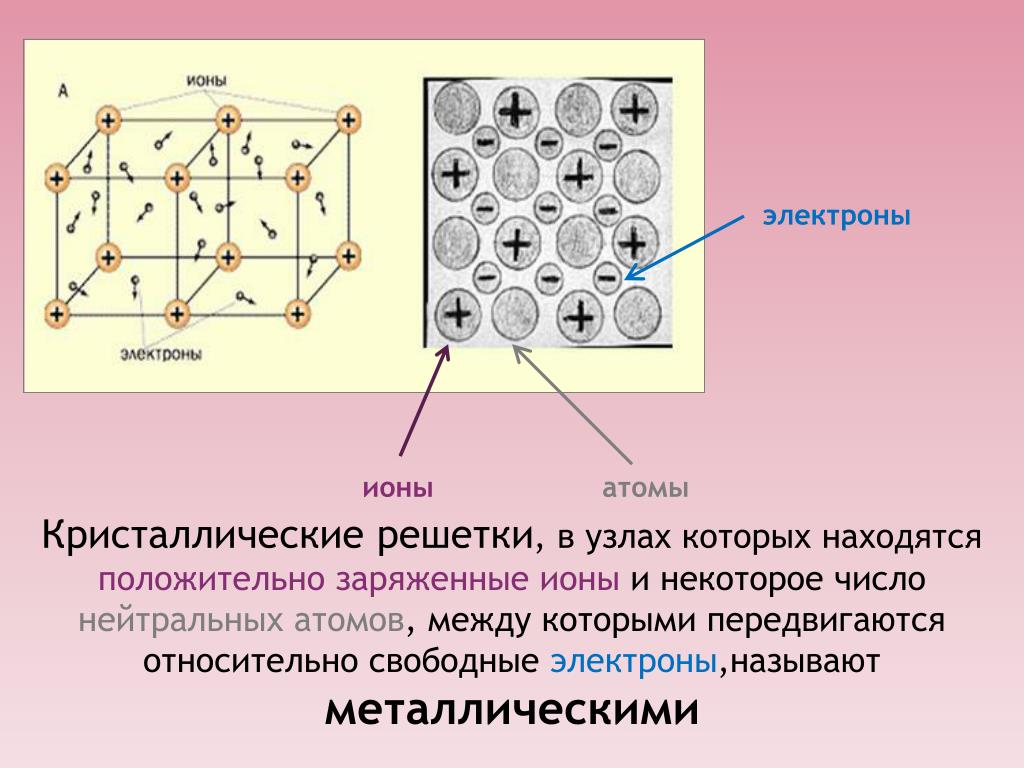
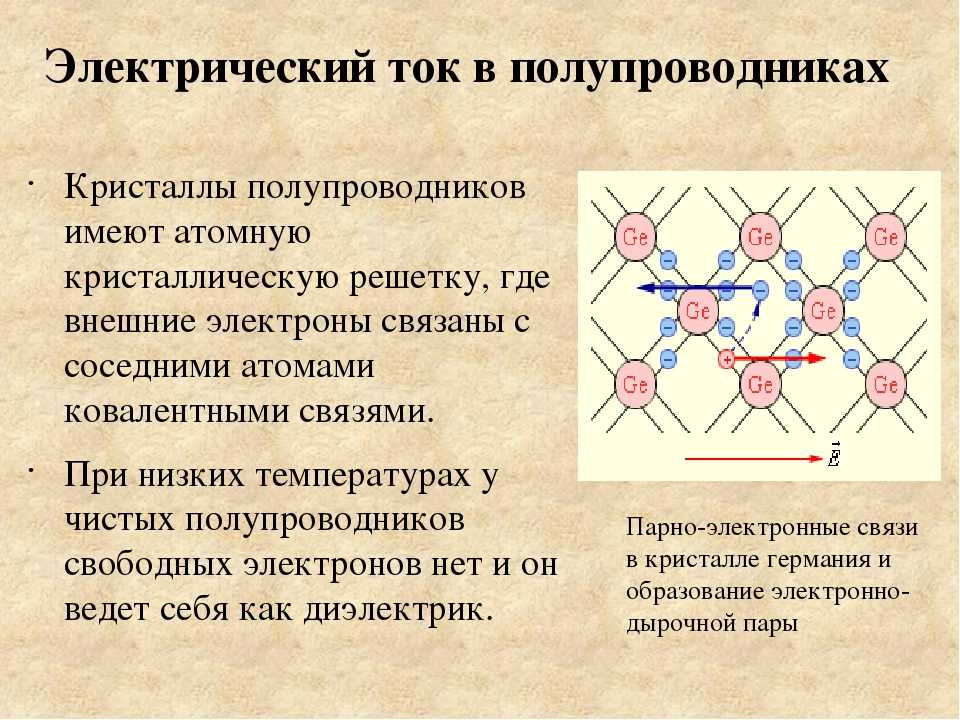 Такая
связь называется ковалентной. Также атомы-неметаллы характеризуются ещё и тем,
насколько сильно они притягивают к себе электроны. Эта способность называется
электроотрицательностью – она растёт снизу вверх по группе (от иода к фтору), и
слева направо по периоду (от лития к фтору). Если связь образована двумя
одинаковыми неметаллами – в простом веществе – то их э.о. одинакова,
электронная пара не смещена, и она будет называться ковалентной неполярной.
Если же образуется соединение из разных атомов-неметаллов, то их э.о. будет
разной и общая электронная пара будет смещена в направлении более э.о.
элемента. Из-за того, что в одной части молекулы электронов – носителей
отрицательного заряда – больше, чем в другой, молекула приобретает положительно
и отрицательно заряженный полюс – становится
Такая
связь называется ковалентной. Также атомы-неметаллы характеризуются ещё и тем,
насколько сильно они притягивают к себе электроны. Эта способность называется
электроотрицательностью – она растёт снизу вверх по группе (от иода к фтору), и
слева направо по периоду (от лития к фтору). Если связь образована двумя
одинаковыми неметаллами – в простом веществе – то их э.о. одинакова,
электронная пара не смещена, и она будет называться ковалентной неполярной.
Если же образуется соединение из разных атомов-неметаллов, то их э.о. будет
разной и общая электронная пара будет смещена в направлении более э.о.
элемента. Из-за того, что в одной части молекулы электронов – носителей
отрицательного заряда – больше, чем в другой, молекула приобретает положительно
и отрицательно заряженный полюс – становится 