что такое? Нитраты: формула, получение, применение, действие
Среди информации, посвященной проблеме правильного питания, можно выделить сегмент, раскрывающий влияние на организм человека таких веществ, как нитраты. Действие их на наше здоровье неоднозначно. Как не вспомнить известное выражение Парацельса: «Всё есть яд и всё есть лекарство; тем или иным его делает только доза». Действительно, для правильного обмена веществ необходимо присутствие в цитоплазме клеток анионов NO3— NO4+. В то же время избыток соединений, содержащих эти ионы, в продуктах питания опасен для здоровья человека. Роль солей азотной кислоты, их получение, применение нитратов будут рассмотрены в данной статье.
Положение нитратов в классификации неорганических веществ
Многие знают, что соли азотной кислоты, хорошо растворимые в воде – это нитраты. Что такое селитра, известно не всем. Оказывается, так ранее в химии называли особые вещества – соли нитратной кислоты. До сих пор мы можем слышать этот термин применительно к химии минеральных удобрений. В селитрах нитрат-ион связан с катионами калия, кальция, натрия и аммония. Они представляют собой средние соли. Оказалось, что нитраты натрия, калия и другие соли при нагревании разлагаются, причем продукты реакции зависят от того, какой катион входит в состав молекулы. Так, нитраты, формула которых KaNO3 илиNaNO3, термически разлагаются до соответствующего нитрита и свободного кислорода, а азотнокислый магний при нагревании образует оксид, двуокись азота и кислород.

Получение нитратов
Основной способ – переработка природных минералов, содержащих соли азотной кислоты. Так, чилийская селитра, представляющая собой минерал нитронатрит, – один из главных источников их получения. На заводах туковой промышленности горную породу, содержащую нитрат натрия, мелко измельчают и в расфасованном виде поставляют сельхозпредприятиями фермерского хозяйства в качестве азотного удобрения. Применяют его прежде всего для прироста вегетационной массы овощных, зерновых и плодово-ягодных культур, а также для повышения их урожайности. В лабораторных условиях соли азотной кислоты получают реакцией обмена между щелочами и нитратной кислотой или же взаимодействием металлов с концентрированной HNO3. Применение азотных удобрений, таких как калийная селитра, нитрат аммония, – необходимое условие для получения стабильных высоких урожаев основных сельскохозяйственных культур.
Агротехнические условия внесения азотных удобрений (нитратов)
К ним относят прежде всего соблюдение норм внесения препаратов в почву. Например, для аммиачной селитры, содержащей до 35 % азота, допустимая норма составляет не более 25 г на один квадратный метр. Кальциевая селитра, в которую входит до 15,5 % азота, вносится из расчета до 50 г на 1 м. Нарушение агротехнических норм азотной подкормки растений приводит не только к загрязнению почвы и снижению её восстановительной функции, но и к опасной концентрации таких соединений, как нитраты, в овощах и фруктах. На этом вопросе мы остановимся далее.

Как нитраты попадают в растения
Рассмотрим, какими именно путями поступают в почву нитраты, что такое допосевное внесение, стартовое удобрение и подкормка. В сельском хозяйстве основное внесение удобрений проводят весной и при этом обращают внимание на состав почвы и особенности климата. Цель – обеспечение азотного питания в период вегетации растения.
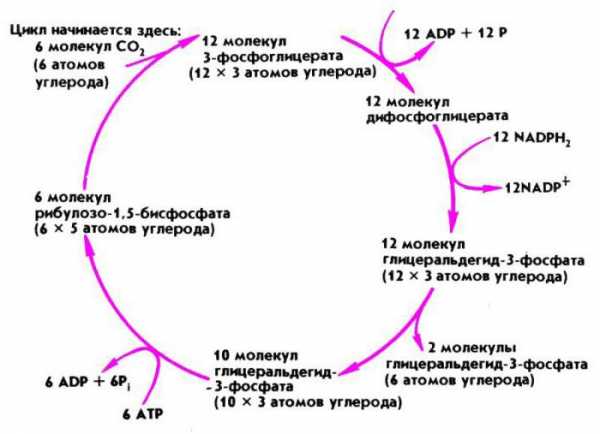
При использовании стартового способа селитру вносят непосредственно в ряды или лунки, используя нитраты в минимальных дозах, чтобы «не обжечь» хрупкие корни высаживаемой рассады. Подкормка осуществляется во время наиболее интенсивного поглощения растениями питательных элементов. Её проводят в форме вегетирующих культур или как корневую подкормку растворами нитратов. В почвенном субстрате ионы аммония или нитрат ионы путем диффузии легко поглощаются корневыми волосками и далее поступают в ксилему. Из нее состоят проводящие элементы растений. У голосеменных это трахеиды, а у цветковых – сосуды (трахеи). Атомы азота, входящие в состав нитратов, включаются в цикл Кальвина, осуществляемый в темновой фазе фотосинтезом, и в дальнейшем входят в состав синтезируемых аминокислот и далее в растительные белки.
Чем опасно избыточное содержание солей нитратной кислоты
Если концентрация вышеназванных соединений превышает допустимую норму, это может определить прибор для измерения нитратов в продуктах. Он доступен в продаже и используется во многих семьях, ответственно относящихся к своему здоровью. Исследования медицины доказали, что избыток солей HNO3 в желудочно-кишечномтракте превращается в нитриты. Именно они вызывают раздражение слизистых оболочек желудка и двенадцатиперстной кишки, симптоматически проявляющиеся явлениями диспепсии и пищевого отравления. Также установлено, что избыток солей HNO2 плохо выводиться почками, поэтому они накапливаются в почечной паренхиме. Известно, что сами почки играют ведущую роль в метаболизме и выведении вредных продуктов обмена. Снижение фильтрационной функции почек является очень опасным осложнением, возникающим в результате отравления солями азотной и азотистой кислот. В результате употребления продуктов с высоким содержанием нитратов страдает также и печень, являющаяся еще одним детоксикационным органом. Ее повреждение нитратами чревато тяжелыми повреждениями вплоть до перерождения гепатоцитов в жировую ткань.

Кислородное голодание тканей как последствие их отравления нитратами
Питательные вещества (жиры, углеводы) могут сохраняться в качестве запасного источника энергии и расходуются организмом постепенно. Именно поэтому человек способен в течение 5-7 дней обходиться без пищи. Но кислород, в отличие от углеводов и жиров, не может длительно сохраняться в клетках или тканях, поэтому гипоксия в течение 5-15 минут приводит к гибели сначала клеток головного мозга, а затем и всего организма человека в целом. Кажущиеся на первый взгляд безобидными, нитраты в фруктах, овощах, молочных детских смесях способны вызывать разрушение дыхательных цепей в митохондриях, нарушать образование связи пигмента эритроцитов – гемоглобина – с молекулами кислорода.

И препятствовать его переносу к органам и тканям. Поэтому избыточная концентрация в цитозоле клетки таких соединений, как нитраты (формула — Me(NO3)N1), может привести к серьезным нарушениям функций со стороны таких физиологических систем, как пищеварительная, выделительная, а также нервная.
Какие продукты могут быть загрязнены солями нитратной кислоты
У большинства людей избыточное содержание этих веществ ассоциируется с овощами или фруктами, например арбузом, картофелем, редисом или клубникой. Но оказывается, что загрязнение почвы и особенно воды азотными удобрениями, попавшими туда в связи с нарушением норм их внесения, напрямую влечет за собой «оседание нитратов» в организмах домашних животных. Поэтому бесконтрольное и нерациональное применение нитратов влечет за собой их высокое содержание в продуктах животноводства: мясе, молоке и даже в меде. Опрыскивание растений-медоносов (гречихи, рапса) растворами солей азотной кислоты в качестве жидкого удобрения приводит к появлению токсинов и в продуктах пчеловодства.

Как определить содержание солей азотной кислоты в продуктах
Давайте уточним, как же практически можно узнать о концентрации в пищевых веществах таких соединений, как нитраты. Что такое нитрат-тестер, рассмотрим более подробно. Чтобы выявить присутствие солей азотной кислоты, нужно погрузить щуп прибора в мякоть арбуза или другого продукта. Приспособление имеет две части: положительно и отрицательно заряженную. А сам нитратомер определяет электропроводность раствора клеточного сока. Полученные результаты сравниваются с ПДК исследуемого продукта, и прибор для измерения нитратов в продуктах выводит на дисплей результат с содержанием солей в мг/кг. Особенно желательным будет тестирование пищевых продуктов, используемых в питании маленьких детей, беременных и кормящих женщин, а также людей, страдающих хроническими заболеваниями ЖКТ и почек.

Отравление солями нитратной кислоты и его профилактика
Пик регистрируемых случаев интоксикаций, связанных с отравлениями солями азотной кислоты, проходится на конец зимы – начало весны. Вследствие дефицита солнечного света и энергии, человеческий организм в этот период остро нуждается в витаминах, содержащихся в свежих овощах и фруктах. Поэтому в супермаркетах не залеживаются тепличные огурцы, помидоры, пряно-вкусовые приправы (сельдерей, петрушка, укроп), а также клубника. Агротехнологии их выращивания предусматривают обязательное применение таких веществ, как нитраты. Что такое минеральные удобрения и как их избыток влияет на организм человека, было уже рассмотрено нами ранее. Сейчас мы остановимся на приемах первой помощи, способных облегчить состояние больного с симптомами отравления нитратами. В первую очередь нужно вызвать рвоту, чтобы удалить из желудка токсичный продукт. Для этого применяют обильное питье. Затем принимают препараты-энтеросорбенты и продолжают соблюдать водно-солевой режим. При сложных симптомах, таких как падение кровяного давления, потеря сознания, судороги, вызванных поражением центральной нервной системы и почек, следует срочно вызвать «скорую помощь».
fb.ru
Формула Нитрата натрия структурная химическая
Структурная формула
Истинная, эмпирическая, или брутто-формула: NNaO3
Химический состав Нитрата натрия
| Символ | Элемент | Атомный вес | Число атомов | Процент массы |
|---|---|---|---|---|
| N | Азот | 14,007 | 1 | 16,5% |
| Na | Натрий | 22,99 | 1 | 27% |
| O | Кислород | 15,999 | 3 | 56,5% |
Молекулярная масса: 84,994
Нитрат натрия(азотноки́слый на́трий, натриевая селитра, чилийская селитра, натронная селитра) — натриевая соль азотной кислоты с формулой NaNO3
Свойства
Физические свойства
Молекулярная масса — 85. Это бесцветные длинные кристаллы, плотностью 2,257 г/см3. tпл 308 °C, при t выше 380 °С разлагается.
Растворимость (г в 100 г) в:
- воде — 72,7 (0°С), 87,6 (20°С), 91,6 (25 °С), 114,1 (50 °C), 124,7 (60°С), 176,0 (100°С)
- жидком аммиаке — 127 (25 °С)
- гидразине — 100 (25 °С)
- этаноле — 0,036 (25 °С)
- метаноле — 0,41 (25 °С)
- пиридине — 0,35 (25 °С).
Химические свойства
ри нагревании до 380°С разлагается с выделением кислорода и нитрита натрия:2NaNO3 → 2NaNO2+O2
Может вступать в реакции обмена с солями щелочных металлов. Благодаря меньшей, по сравнению с нитратом натрия, растворимости образующихся нитратов, равновесие указанных реакций смещено вправо:
NaNO3+KCl → KNO3+NaCl
NaNO3+RbI → RbNO3+NaI
Проявляет сильные окислительные свойства в твердом агрегатном состоянии и в расплавах.
В процессе разложения выделяет кислород, вследствие чего может взаимодействовать с неметаллами:
2NaNO3+S → 2NaNO2+SO2
2NaNO3+C → 2NaNO2+CO2
Реакция с серой проходит с большим выделением света и тепла, таким, что стеклянный сосуд, в котором проводится опыт, может лопнуть или расплавиться.
Его окислительные свойства близки к свойствам нитрата калия, поэтому он может использоваться аналогично в некоторых направлениях, например в пиротехнике.
Получение
В лаборатории нитрат натрия можно получить следующими способами:
- Взаимодействием металлического натрия или его оксида с азотной кислотой:
21Na + 26HNO3 → 21NaNO3 + NO+N2O + N2 + 13H2O
Na2O + 2HNO3 → 2NaNO3 + H2O - Гидроксида натрия или кислых солей натрия с азотной кислотой:
NaOH + HNO3 → NaNO3 + H2O
NaHCO3 + HNO3 → NaNO3 + CO2 +H2O
Также вместо азотной кислоты можно использовать нитрат аммония:
NaOH + NH4NO3 → NaNO3 + NH3 + H2O
NaHCO 3 + NH4NO3 → NaNO3 + NH3 + CO2 + H2O - Взаимодействием нитрата серебра с пищевой солью (качественная реакция на ион Cl-): AgNO3 + NaCl → NaNO3 + AgCl
Применение
Применяется как удобрение; в пищевой, стекольной, металлообрабатывающей промышленности; для получения взрывчатых веществ, ракетного топлива и пиротехнических смесей для придания огню жёлтого цвета. Получается из природных залежей выщелачиванием горячей водой и кристаллизацией; абсорбцией раствором соды окислов азота; обменным разложением кальциевой или аммиачной селитры с сульфатом, хлоридом или карбонатом натрия.
formula-info.ru
Формула нитрата аммония в химии
Определение и формула нитрата аммония
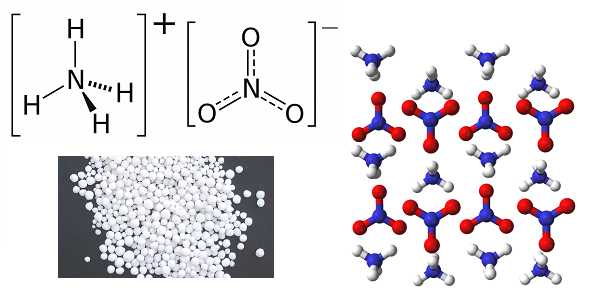
Химическая формула –
Молярная масса равна г/моль.
Физические свойства – белое кристаллическое вещество.
Гигроскопичная соль, термически неустойчивая.
Хорошо растворяется в воде с большим поглощением тепла.
Гидролизуется по катиону, не образует кристаллогидратов.
Химические свойства нитрата аммония
- При нагревании разлагается различными путями. Например, разложение при температуре выше протекает по уравнению:
- Реагирует с концентрированным раствором гидроксида натрия:
- Реагирует с таким окислителем как диоксид марганца:
Получение
Нитрат аммония можно получить по реакции раствора аммиака с азотной кислотой:
Применение
Основной областью применения нитрата аммония является его использование в качестве удобрения.
Еще одна отрасль промышленности использует смеси аммиачной селитры с различными материалами в качестве взрывчатых веществ.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Нитрат Калия (Селитра Калиевая, Селитра Калийная): применение, формула, цена
Читайте нас и будьте здоровы! Пользовательское соглашение о портале обратная связь- Врачи
- Болезни
- Кишечные инфекции (5)
- Инфекционные и паразитарные болезни (27)
- Инфекции, передающиеся половым путем (6)
- Вирусные инфекции ЦНС (3)
- Микозы (10)
- Протозойные болезни (1)
- Гельминтозы (5)
- Злокачественные новообразования (9)
- Доброкачественные новообразования (7)
- Болезни крови и кроветворных органов (9)
- Болезни щитовидной железы (6)
- Болезни эндокринной системы (13)
- Недостаточности питания (1)
- Нарушения обмена веществ (1)
- Психические расстройства (31)
- Воспалительные болезни ЦНС (3)
- Болезни нервной системы (19)
- Двигательные нарушения (5)
- Болезни глаза (20)
- Болезни уха (4)
- Болезни системы кровообращения (10)
- Болезни сердца (11)
- Цереброваскулярные болезни (2)
- Болезни артерий, артериол и капилляров (9)
- Болезни вен, сосудов и лимф. узлов (8)
- Болезни органов дыхания (35)
- Болезни полости рта и челюстей (16)
- Болезни органов пищеварения (30)
- Болезни печени (2)
- Болезни желчного пузыря (9)
- Болезни кожи (32)
- Болезни костно-мышечной системы (49)
- Болезни мочеполовой системы (14)
- Болезни мужских половых органов (8)
- Болезни молочной железы (3)
- Болезни женских половых органов (27)
- Беременность и роды (5)
- Болезни плода и новорожденного (4)
- Симптомы
- Амнезия (потеря памяти)
- Анальный зуд
- Апатия
- Афазия
- Афония
- Ацетон в моче
- Бели (выделения из влагалища)
- Белый налет на языке
- Боль в глазах
- Боль в колене
- Боль в левом подреберье
- Боль в области копчика
- Боль при половом акте
- Вздутие живота
- Волдыри
- Воспаленные гланды
- Выделения из молочных желез
- Выделения с запахом рыбы
- Вялость
- Галлюцинации
- Гнойники на коже (Пустула)
- Головокружение
- Горечь во рту
- Депигментация кожи
- Дизартрия
- Диспепсия (Несварение)
- Дисплазия
- Дисфагия (Нарушение глотания)
- Дисфония
- Дисфория
- Жажда
- Жар
- Желтая кожа
- Желтые выделения у женщин
- …
- ПОЛНЫЙ СПИСОК СИМПТОМОВ>
- Лекарства
- Антибиотики (211)
- Антисептики (123)
- Биологически активные добавки (210)
- Витамины (192)
- Гинекологические (183)
- Гормональные (155)
- Дерматологические (258)
- Диабетические (46)
- Для глаз (124)
- Для крови (77)
- Для нервной системы (385)
- Для печени (69)
- Для повышения потенции (24)
- Для полости рта (68)
- Для похудения (40)
- Для суставов (161)
- Для ушей (15)
- Другие (306)
- Желудочно-кишечные (314)
- Кардиологические (149)
- Контрацептивы (48)
- Мочегонные (32)
- Обезболивающие (280)
- От аллергии (102)
- От кашля (137)
- От насморка (91)
- Повышение иммунитета (123)
- Противовирусные (113)
- Противогрибковые (126)
- Противомикробные (145)
- Противоопухолевые (65)
- Противопаразитарные (49)
- Противопростудные (90)
- Сердечно-сосудистые (351)
- Урологические (89)
- ДЕЙСТВУЮЩИЕ ВЕЩЕСТВА
- Справочник
- Аллергология (4)
- Анализы и диагностика (6)
- Беременность (25)
- Витамины (15)
- Вредные привычки (4)
- Геронтология (Старение) (4)
- Дерматология (3)
- Дети (15)
- Другие статьи (22)
- Женское здоровье (4)
- Инфекция (1)
- Контрацепция (11)
- Косметология (23)
- Народная медицина (17)
- Обзоры заболеваний (27)
medside.ru
Нитрат аммония — это… Что такое Нитрат аммония?
Нитра́т аммо́ния (аммонийная (аммиачная) селитра) — химическое соединение NH
Физические свойства
Кристаллическое вещество белого цвета. Температура плавления 169,6 °C, при нагреве выше этой температуры начинается постепенное разложение вещества, а при температуре 210 °C происходит полное разложение. Температура кипения при повышенном давлении — 235 °C. Молекулярная масса 80,04 а. е. м.. Скорость детонации 2570 м/с.
Растворимость
Растворимость в воде:
| Температура, °C | Растворимость, г/100мл |
|---|---|
| 0 | 119 |
| 25 | 212 |
| 50 | 346 |
| 100 | 1024 |
При растворении происходит сильное поглощение тепла (аналогично нитрату калия), что значительно замедляет растворение. Поэтому для приготовления насыщенных растворов нитрата аммония применяется нагревание, при этом твёрдое вещество засыпается небольшими порциями.
Также соль растворима в аммиаке, пиридине, метаноле, этаноле.
Состав
Содержание элементов в нитрате аммония в массовых процентах:
- O — 60 %,
- N — 35 %,
- H — 5 %.
Методы получения
Основной метод
В промышленном производстве используется безводный аммиак и концентрированная азотная кислота:
Реакция протекает бурно с выделением большого количества тепла. Проведение такого процесса в кустарных условиях крайне опасно (хотя в условиях большого разбавления водой нитрат аммония может быть легко получен). После образования раствора, обычно с концентрацией 83 %, лишняя вода выпаривается до состояния расплава, в котором содержание нитрата аммония составляет 95—99,5 % в зависимости от сорта готового продукта. Для использования в качестве удобрения расплав гранулируется в распылительных аппаратах, сушится, охлаждается и покрывается составами для предотвращения слёживания. Цвет гранул варьируется от белого до бесцветного. Нитрат аммония для применения в химии обычно обезвоживается, так как он очень гигроскопичен и процентное количество воды в нём () получить практически невозможно.
Метод Габера
По способу Габера из азота и водорода синтезируется аммиак, часть которого окисляется до азотной кислоты и реагирует с аммиаком, в результате чего образуется нитрат аммония:
- при давлении, высокой температуре и катализаторе
- .
Нитрофосфатный метод
Этот способ также известен как способ Одда, названный так в честь норвежского города, в котором был разработан этот процесс. Он применяется непосредственно для получения азотных и азотно-фосфорных удобрений из широко доступного природного сырья. При этом протекают следующие процессы:
- Природный фосфат кальция (апатит) растворяют в азотной кислоте:
- .
- Полученную смесь охлаждают до 0 °C, при этом нитрат кальция кристаллизуется в виде тетрагидрата — Ca(NO3)2·4H2O, и его отделяют от фосфорной кислоты.
- На полученный нитрат кальция и не удалённую фосфорную кислоту действуют аммиаком, и в итоге получают нитрат аммония:
- .
А также амфотерный метод.
Химические свойства
Реакции разложения
Термическое разложение нитрата аммония может происходить по-разному, в зависимости от температуры:
- Температура ниже 270 °C:
- .
- Температура выше 270 °C, или детонация:
- .
Кристаллические состояния нитрата аммония
Изменения кристаллического состояния нитрата аммония под воздействием температуры и давления меняют его физические свойства. Обычно различают следующие состояния:
| Система | Диапазон температур (°C) | Состояние | Изменение объёма (%) |
|---|---|---|---|
| — | > 169.6 | жидкость | |
| I | 169.6 — 125.2 | кубическая | +2.1 |
| II | 125.5 — 84.2 | тетрагональная | −1.3 |
| III | 84.2 — 32.3 | α-ромбическая | +3.6 |
| IV | 32.3 — −16.8 | β-ромбическая | −2.9 |
| V | < −16.8 | тетрагональная |
Фазовый переход от IV к III при 32,3 °C приносит неприятности производителям удобрений, потому как изменения плотности приводят к разрушению частиц при хранении и применении. Это особенно важно в тропических странах, где нитрат аммония испытывает циклические изменения, приводящие к разрушению гранул, слёживанию, повышенному пылению и риску возникновения взрыва.
Применение
Взрывчатые вещества
Наиболее широко в промышленности и горном деле применяются смеси аммиачной селитры с различными видами углеводородных горючих материалов, других взрывчатых веществ, а также многокомпонентные смеси:
Удобрения
Бо́льшая часть нитрата аммония используется либо непосредственно как хорошее азотное удобрение, либо как полупродукт для получения прочих удобрений.
Аварии и взрывы
- 21 сентября 1921 года в Оппау в Германии на складе завода фирмы BASF при работах по дроблению небольшими взрывами слежавшихся масс нитрата аммония произошёл катастрофический взрыв примерно 4500 тонн удобрения и мощностью в 1-2 килотонны тротилового эквивалента. На месте склада образовалась воронка удлинённой формы размером более 160 метров и глубиной более 10 метров. По официальным данным, в результате взрыва погиб 561 человек[1].
- 16 апреля 1947 года во время погрузки аммиачной селитры на пароход «Гранкан» в гавани города Техас-сити (англ.) произошёл пожар, который в результате неграмотных действий по его тушению, привёл к катастрофическому по последствиям взрыву приблизительно 2300 тонн удобрения. В результате взрыва были разрушены портовые сооружения, несколько судов, многие предприятия и жилые дома. Погибло более полутора тысяч человек, сотни пропали без вести и их тела не были найдены. Травмы получили более трёх с половиной тысяч человек.[2]
- 22 июля 2011 год в Правительственном квартале Осло, Норвегия, прогремел взрыв. Заложенная в автомобиль «Volkswagen Crafter» радиоуправляемая бомба была изготовлена из сельскохозяйственных удобрений на основе аммиачной селитры и дизельного топлива. Вследствие этого взрыва 8 человек погибли, пятнадцать получили ранения. Виновником теракта был объявлен Андерс Беринг Брейвик.
Дополнительная информация
Мировое производство аммиачной селитры на 1980 год составляло 14 млн т, в пересчёте на азот.
См. также
Примечания
Ссылки
Литература
- Технология аммиачной селитры, под ред. В. М. Олевского, М., 1978.
- Соли азотной кислоты, Миниович М. А., М., 1964.
- Олевский В. М., Ферд М. Л., «Ж. Всес. хим. о-ва им. Д. И. Менделеева», 1983, т. 28, № 4, с. 27—39.
dic.academic.ru
NO3 название вещества
Вещества, химический состав которого отображался бы формулой не существует (NO3 название вещества), однако, есть анион , получающийся в результате диссоциации азотной кислоты — нитрат-ион:
В обычных условиях нитраты представляют собой твердые вещества с ионной кристаллической решеткой, хорошо растворимые в воде.
Качественной реакцией на является выделение бурого газа при подкислении раствора и его взаимодействии с металлической медью:
Все нитраты по их термической устойчивости можно разделить на четыре группы:
— нитраты щелочных металлов при нагревании разлагаются на нитриты и кислород
— большинство нитратов активных металлов (от щелочно-земельных до меди) разлагаются на оксид металла, и кислород
— нитраты наиболее тяжелых металлов разлагаются на свободный металл, и кислород
— нитрат аммония разлагается до
ru.solverbook.com
Формула нитрата калия в химии
Определение и формула нитрата калия
Химическая формула –
Молярная масса равна г/моль.
Физические свойства – это твёрдое кристаллическое вещество, представляющее из себя бесцветные ромбические или гексагональной кристаллы, с плотностью 2,11 г/см, хорошо растворяется в воде 31,6 г/100 г (), температура плавления , при разлагается.
Химические свойства нитрата калия
Получение
Нитрат калия получают с помощью следующих реакций:
Качественная реакция
Качественной реакцией на ионы калия является образование жёлтого кристаллического осадка гексанитрокобальтата (III) калия-натрия при добавлении к раствору гексанитрокобальтата (III) натрия:
Применение
Нитрат калия в основном применяют в качестве удобрения, используют также в пиротехнике, в создании дымного пороха, производстве прочного стекла, в переработке никелевой руды, в пищевой промышленности как консервант.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
