Угольная кислота | это… Что такое Угольная кислота?
У́гольная кислота́ — слабая двухосновная кислота с химической формулой . В чистом виде неустойчива[2]. Образуется в малых количествах при растворении углекислого газа в воде[1], в том числе и углекислого газа из воздуха. Образует ряд устойчивых неорганических и органических производных: соли (карбонаты и гидрокарбонаты), сложные эфиры, амиды и др.
Содержание
|
Физические свойства
Молекула угольной кислоты имеет плоское строение. Центральный углеродный атом имеет sp²-гибридизацию. В гидрокарбонат- и карбонат-анионах происходит делокализация π-связи. Длина связи C—O в карбонат-ионе составляет 129 пм.
Длина связи C—O в карбонат-ионе составляет 129 пм.
Химические свойства
Равновесие в водных растворах и кислотность
Угольная кислота существует в водных растворах в состоянии равновесия с гидратом диоксида углерода:
- , константа равновесия при 25 °C
Скорость прямой реакции 0,039 с
В свою очередь растворённый гидрат диоксида углерода находится в равновесии с газообразным диоксидом углерода:
Данное равновесие при повышении температуры сдвигается вправо, а при повышении давления — влево (подробнее см. Абсорбция газов).
Угольная кислота подвергается обратимому гидролизу, создавая при этом кислую среду:
- , константа кислотности при 25 °C
Однако, для практических расчётов чаще используют кажущуюся константу кислотности, учитывающую равновесие угольной кислоты с гидратом диоксида углерода:
Гидрокарбонат-ион подвергается дальнейшему гидролизу по реакции
- , константа кислотности при 25 °C
Таким образом, в растворах, содержащих угольную кислоту, создается сложная равновесная система, которую можно изобразить в общем виде следующим образом:
Значение pH в такой системе, соответствующей насыщенному раствору диоксида углерода в воде при 25 °C и давлении 760 мм рт.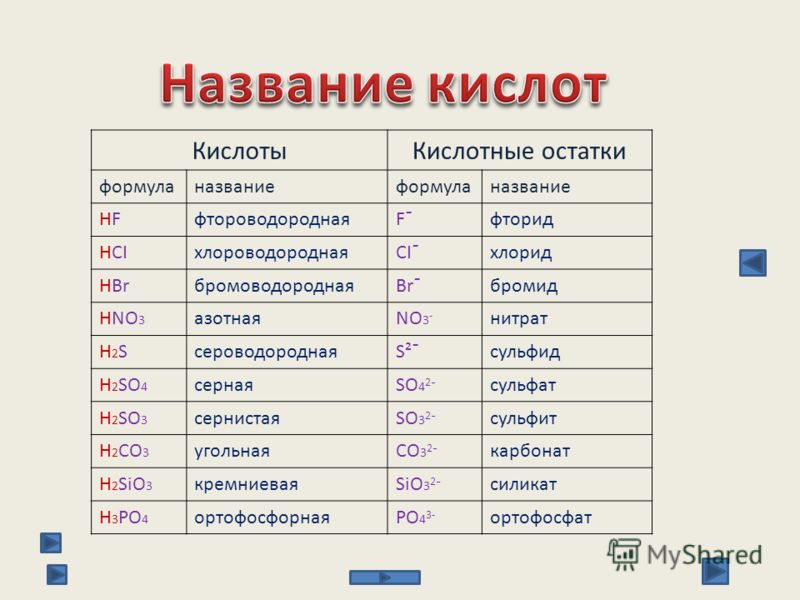
- , где L = 0,034 моль/л — растворимость CO2 в воде при указанных условиях.
Разложение
При повышении температуры раствора и/или понижении парциального давления диоксида углерода равновесие в системе смещается влево, что приводит к разложению части угольной кислоты на воду и диоксид углерода. При кипении раствора угольная кислота разлагается полностью:
Взаимодействие с основаниями и солями
Угольная кислота вступает в реакции нейтрализации с растворами оснований, образуя средние и кислые соли — карбонаты и гидрокарбонаты соответственно:
- (конц.)
- (разб.)
При взаимодействии угольной кислоты с карбонатами образуются гидрокарбонаты:
Получение
Угольная кислота образуется при растворении в воде диоксида углерода:
Содержание угольной кислоты в растворе увеличивается при понижении температуры раствора и увеличении давления углекислого газа.
Также угольная кислота образуется при взаимодействии её солей (карбонатов и гидрокарбонатов) с более сильной кислотой. При этом бо́льшая часть образовавшейся угольной кислоты, как правило, разлагается на воду и диоксид углерода:
Применение
Угольная кислота всегда присутствует в водных растворах углекислого газа (см. Газированная вода).
В биохимии используется свойство равновесной системы изменять давление газа пропорционально изменению содержания ионов оксония (кислотности) при постоянной температуре. Это позволяет регистрировать в реальном времени ход ферментативных реакций, протекающих с изменением pH раствора.
Органические производные
Угольную кислоту формально можно рассматривать как карбоновую кислоту с гидроксильной группой вместо углеводородного остатка. В этом качестве она может образовывать все производные, характерные для карбоновых кислот[3].
Некоторые представители подобных соединений перечислены в таблице.
| Класс соединений | Пример соединения |
|---|---|
| Сложные эфиры | поликарбонаты |
| Хлорангидриды | фосген |
| Амиды | мочевина |
| Нитрилы | циановая кислота |
| Ангидриды | пироугольная кислота |
См. также
- Оксид углерода(IV)
- Карбонаты
- Гидрокарбонаты
- Карбоновые кислоты
- Газированная вода
Примечания
- ↑ 1 2 3 В водном растворе бо́льшая часть угольной кислоты обратимо переходит в гидрат диоксида углерода по реакции H2CO3 ⇄ CO2·H2O
- ↑ Угольная кислота теперь обнаружена и в газовой фазе — пора снова переписывать учебники
- ↑ Нейланд О. Я. Органическая химия. — М.: Высшая школа, 1990. — С. 640—652. — 751 с. — ISBN 5-06-001471-1
Литература
- Лидин Р.
 А., Молочко В. А., Андреева Л. Л. Реакции неорганических веществ: справочник / Под ред. Р. А. Лидина. — 2-е изд., перераб. и доп. — М.: Дрофа, 2007. — 637 с. — ISBN 978-5-358-01303-2
А., Молочко В. А., Андреева Л. Л. Реакции неорганических веществ: справочник / Под ред. Р. А. Лидина. — 2-е изд., перераб. и доп. — М.: Дрофа, 2007. — 637 с. — ISBN 978-5-358-01303-2 - Лидин Р.А., Андреева Л. Л., Молочко В. А. Константы неорганических веществ: справочник / Под ред. Р. А. Лидина. — 2-е изд., перераб. и доп. — М.: Дрофа, 2006. — 685 с. — ISBN 5-7107-8085-5
Растворимость кислот, оснований и солей в воде
| H+ | Li+ | K+ | Na+ | NH4+ | Ba2+ | Ca2+ | Mg2+ | Sr2+ | Al3+ | Cr3+ | Fe2+ | Fe 3+ | Ni2+ | Co2+ | Mn2+ | Zn2+ | Ag+ | Hg2+ | Hg22+ | Pb2+ | Sn2+ | Cu+ | Cu2+ | |
| OH− | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F− | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl− | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р | |
| Br− | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I− | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | — | Н | Н | Н | Н |
| SO32− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO42− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3− | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | |
| NO2− | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO43− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO32− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | — | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN− | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO32− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Сравнение эффективности и безопасности ингибиторов карбоангидразы для местного применения
Сравнение эффективности и безопасности ингибиторов карбоангидразы для местного применения
01 января 1970
Поделиться материалом Распечатать Добавить в избранное- Егоров Е.
 А.
1 ,
А.
1 , - Хлобыстов А.А. ,
- Ставицкая Т.В.
1
РНИМУ им. Н.И. Пирогова Минздрава России, Москва, Россия
История применения ингибиторов карбоангидразы в медицине начинается с 1954 года, когда был разработан первый препарат из группы ингибиторов КА – ацетазоламид. Сначала он использовался в качестве диуретического средства. Однако вскоре была установлена способность ацетазоламида снижать внутриглазное давление (ВГД) у больных глаукомой.
Однако вскоре была установлена способность ацетазоламида снижать внутриглазное давление (ВГД) у больных глаукомой.
Карбоангидраза (угольная ангидраза) – фермент, участвующий в процессе гидратации и дегидратации угольной кислоты. Карбоангидраза– фермент, являющийся цинкопротеидом. Как правило, КА сосредоточена в клеточных элементах, она не найдена в тканевых жидкостях.
В организме человека данный фермент, который представлен двумя изоферментами КАI и КАII, встречается в эритроцитах, клетках поджелудочной железы, слизистой оболочки желудка, околоушной слюнной железы, почках, ресничного тела глаза.
Карбоангидраза катализирует превращение карбоксида в угольную кислоту (СО2 + h3O = h3CO3). Угольная кислота впоследствии диссоциирует на гидроксильный ион и бикарбонат (H+ + HCO3–). Эта реакция – ключ к секреторным физиологическим процессам во многих тканях в том числе и в глазу.
В процессе образования водянистой влаги глаза бикарбонат–ионы активно транспортируются в заднюю камеру из цитоплазмы беспигментных клеток, чтобы компенсировать градиент положительных ионов, обусловленный активным транспортом ионов Na+. Ингибиторы КА блокируют образование угольной кислоты, таким образом снижая продукцию HCO3–. В отсутствие достаточного количества ионов HCO3– увеличевается позитивный ионный градиент, что вызывает снижение секреции водянистой влаги. Вероятно, это механизм, за счет которого ИКА снижают ВГД.
Ингибиторы КА блокируют образование угольной кислоты, таким образом снижая продукцию HCO3–. В отсутствие достаточного количества ионов HCO3– увеличевается позитивный ионный градиент, что вызывает снижение секреции водянистой влаги. Вероятно, это механизм, за счет которого ИКА снижают ВГД.
Однако применение таких пероральных ИКА, как ацетазоламид и метазоламид, сопровождается побочными явлениями. Побочные эффекты включают симптомы недомогания, парестезии, желудочно–кишечные расстройства (тошнота, рвота и другие симптомы), потерю веса, депрессию, анорексию и потерю либидо.
Возникновение побочных эффектов системного характера ограничивает применение пероральных ингибиторов карбоангидразы для длительного лечения глаукомы. В основном они используются для лечения острого приступа глаукомы, купирования реактивного повышения ВГД после лазерных вмешательств или в течение короткого времени для подготовки больного перед антиглаукоматозной операцией.
Поэтому в течение многих лет исследователи пытались разработать местный ингибитор КА, чтобы избежать нежелательных системных проявлений. В 1986 г. впервые были опубликованы данные о возможном местном применении 10% раствора ацетазоламида. Экпериментальное исследование, проведенное у кроликов, показало, что инстилляции 10% раствора ацетазоламида снижают ВГД в среднем на 1,9–2,3 мм рт.ст. Однако прошло около 40 лет между демонстрацией гипотензивного эффекта перорального ацетазоламида в отношении ВГД и разработкой первых достаточно эффективных и безопасных местных ингибиторов КА. Трудности заключались в невозможности достичь достаточно высокой концентрации препарата, необходимой для значительного ингибирования КА цилиарного тела. Так как, чтобы добиться фармакологического эффекта необходимо практически 100% подавление человеческой КА II, которая играет важную роль в секреции внутриглазной жидкости.
В 1986 г. впервые были опубликованы данные о возможном местном применении 10% раствора ацетазоламида. Экпериментальное исследование, проведенное у кроликов, показало, что инстилляции 10% раствора ацетазоламида снижают ВГД в среднем на 1,9–2,3 мм рт.ст. Однако прошло около 40 лет между демонстрацией гипотензивного эффекта перорального ацетазоламида в отношении ВГД и разработкой первых достаточно эффективных и безопасных местных ингибиторов КА. Трудности заключались в невозможности достичь достаточно высокой концентрации препарата, необходимой для значительного ингибирования КА цилиарного тела. Так как, чтобы добиться фармакологического эффекта необходимо практически 100% подавление человеческой КА II, которая играет важную роль в секреции внутриглазной жидкости.
В настоящее время для больных доступны два ингибитора человеческой карбоангидразы местного применения. Данные препараты обладают хорошей биодоступностью, высокой селективностью и мощной ингибиторной активностью по отношению к изоферменту КА II, к тому же, обладая выраженным гипотензивным эффектом, они лишены побочных системных проявлений. К ним относятся 2% раствор дорзоламида гидрохлорида (Трусопт) – первый ингибитор карбоангидразы предназначенный для местного лечения глаукомы, а также новый препарат– 1% офтальмологическая суспензия бринзоламида (Азопт).
К ним относятся 2% раствор дорзоламида гидрохлорида (Трусопт) – первый ингибитор карбоангидразы предназначенный для местного лечения глаукомы, а также новый препарат– 1% офтальмологическая суспензия бринзоламида (Азопт).
Местные ингибиторы КА, специфически подавляя КА II цилиарного тела, не оказывают других значимых фармакологических эффектов. Это объясняется тем, что терапевтическая доза и низкая системная адсорбционная способность этих препаратов не позволяют достичь уровня для системного угнетения КА. Низкий период их полувыведения из тканей, в частности, из цилиарного тела обеспечивает пролонгированный гипотензивный эффект.
Мировой опыт и исследования проведенные в нашей клинике позволяют утверждать, что оба препарата (Азопт и Трусопт) обладают сопоставимым гипотензивным эффектом (рис. 1) при применении 3 раза в день.
При сравнении влияния исследуемых препаратов на офтальмотонус у больных с ПОУГ, можно отметить, что оба препарата обладают выраженным гипотензивным эффектом. Большая степень снижения ВГД после применения дорзоламида по сравнению с бринзоламидом статистически недостоверна (p
Снижение ВГД (в среднем) на фоне применения бринзоламида составило 25,5% (2 раза в день) и 27,1% (3 раза в день) соответственно.
Большая степень снижения ВГД после применения дорзоламида по сравнению с бринзоламидом статистически недостоверна (p
Снижение ВГД (в среднем) на фоне применения бринзоламида составило 25,5% (2 раза в день) и 27,1% (3 раза в день) соответственно.
Многие исследования показывают, что различные проявления глазного дискомфорта после применения бринзоламида возникают примерно в 2 раза реже, чем при использовании дорзоламида. Степень глазной переносимости – важный показатель для больных, которые вынуждены применять препараты длительно. С целью определения переносимости местных ингибиторов КА нами была разработана анкета, которая включала 14 вопросов. Степень выраженности жалоб пациентов оценивалась в баллах от 0 до 3, где 0 – отсутствие симптома, 1 – слабая выраженность симптома, 2 – умеренная, 3 – сильная.
Всего было обследовано 20 больных ПОУГ. До начала исследования они получали различную гипотензивную терапию. Наиболее часто (в 50% случаев) применялось сочетание тимолола 0,5% и пилокарпина 1%. После оценки переносимости базовой терапии средний балл составлял 6,15. Среди наиболее частых жалоб встречались: покалывание, зуд, жжение – у 11 больных, покраснение глаза – у 10 больных, нечеткость зрения – у 10 больных.
После оценки переносимости базовой терапии средний балл составлял 6,15. Среди наиболее частых жалоб встречались: покалывание, зуд, жжение – у 11 больных, покраснение глаза – у 10 больных, нечеткость зрения – у 10 больных.
После месячного применения дорзоламида средний балл составлял 5,5. Наиболее частые жалобы: покалывание, зуд, жжение – 15 больных, горький привкус во рту – 11 больных, нечеткость зрения – 8 больных.
Через 1 месяц применения бринзоламида средний балл составил 0,97. Наиболее частые жалобы: скапливание отделяемого в углу глаза – 7 больных, покалывание, зуд, жжение – 3 больных, нечеткость зрения – 1 больной (см. рис. 3). Больше 50% пациентов вовсе не отмечают какого–либо глазного дискомфорта при применении бринзоламида в сравнении с дорзоламидом.
Вывод
Благодаря меньшему количеству инстилляций, а также более хорошей глазной переносимости, чем у дорзоламида (бринзоламид обладает оптимальным составом суспензии и физиологическим pH – у бринзоламида – 7,5, у дорзоламида – 5,6), бринзоламид лучше влияет на качество жизни пациентов.
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Получите pdf-версию статьи
Скачать статью Все статьи номераКакое химическое название у h3co3?
Химическое название для h3co3 это угольная кислота, известная под другими названиями, такими как триоксокарбоновая кислота IV, триоксикарбонат дигидрогена, но давайте узнаем больше об этом химическом соединении.
Характеристики
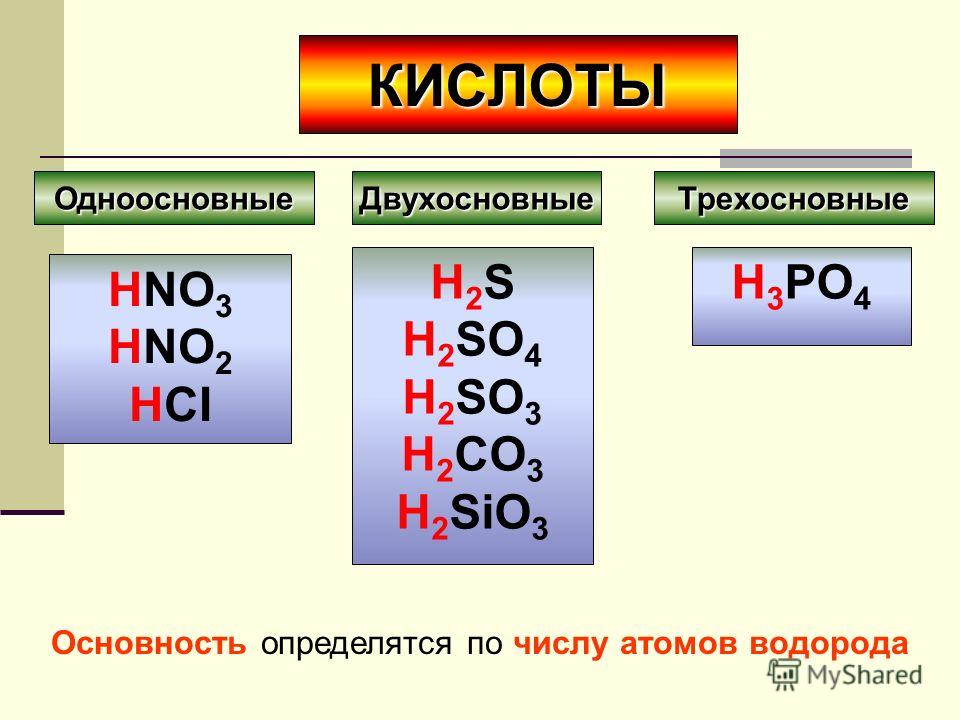
h3co3 Углекислота, Химическое название h3co3 , представляет собой вещество неорганического характера, считающееся оксокислотой, которое способно отдавать два положительных иона водорода в водную среду с образованием двух молекулярные катионы вида h4O+, а также CO32-, поэтому ее также считают двухосновной кислотой.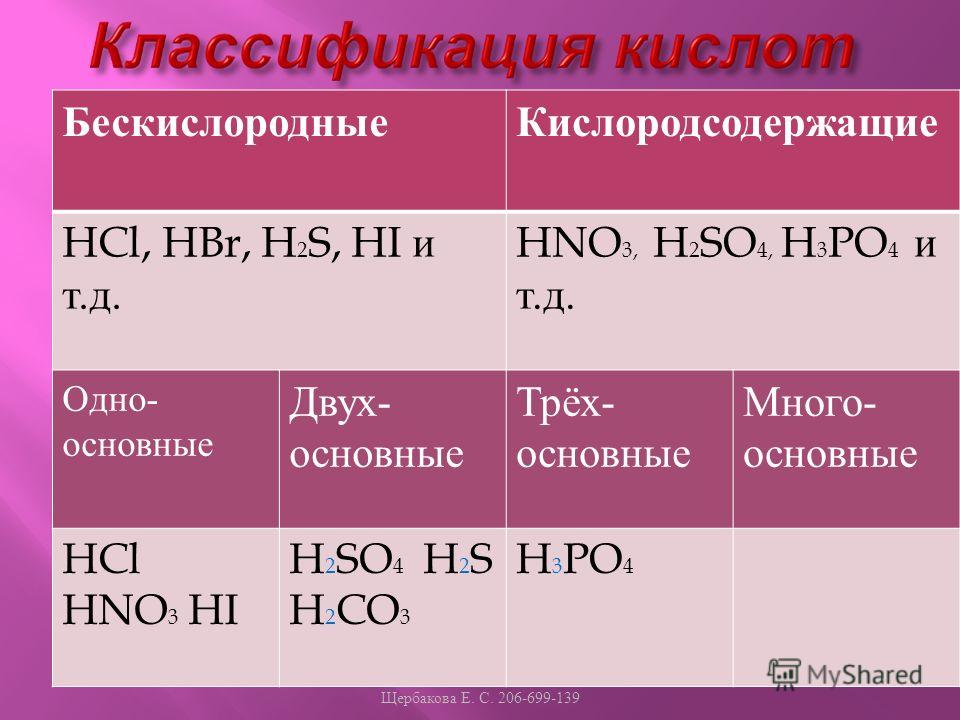
Это слабая кислота с константой ионизации Ka = 4,5-10, которая считается небольшой, ее образование происходит при объединении двух основных неорганических молекул, таких как вода и CO2.
Свойства угольной кислоты,
Химическое название h3co3- Не имеет цвета, это бесцветное вещество.
- Его три компонента: водород, состоящий из 2 атомов, углерод, состоящий из 1 атома, и кислород, состоящий из 3 атомов, являются неметаллическими химическими элементами.
https://upload.wikimedia.org/wikipedia/commons/thumb/b/b4/Carbonic-acid-3D-balls.png/245px-Carbonic-acid-3D-balls.png
Химическое название для h3co3 графически представлена черной сферой, атом углерода соединен двойной связью с атомом кислорода, красной сферой, и двумя одинарными связями, которые соединяют его с двумя другими атомами кислорода, а те, в свою очередь, соединены с одинарные связи с 2 атомами водорода.
Соответственно, мы можем выразить угольную кислоту другой формулой в виде CO(OH)2, где C=O представляет собой карбонильную группу, связанную с двумя гидроксильными группами OH.
- Кислотность 6,352 pKa.
- Плотность 1 г/см 3 .
- Молярная масса h3co3 составляет 62,03 г/моль.
- Агрегатное состояние углекислоты жидкое.
- Он очень изменчив, его время жизни чрезвычайно короткое, всего 300 наносекунд.
- В растворах эта кислота теряет один или два протона, при потере первого образуется ион бикарбоната, а при потере второго протона образуется ион карбоната, это происходит при соединении с положительными атомами радикалов или с основаниями, представляющими собой соли, такие как карбонаты и бикарбонаты.
- Когда эта кислота соединяется с оксидом кальция, широко известным как известь, образуется карбонат кальция в форме мрамора и мела.
Применение
h3co3 Углекислота, Химическое название h3co3 само по себе представляет собой вещество, которое имеет очень мало применений в промышленности, коммерции и повседневной жизни, но из-за его производных и растворения они разнообразны. можно наблюдать.
можно наблюдать.
На основе его пар, таких как HCO3-/CO32- и h3CO3/HCO3-, готовят растворы, в которых используется фермент карбоангидраза. Известно, что этот фермент присутствует в гемоглобине живых существ, при транспортировке через эритроциты он достигает легких. Этот СО2 используется в производстве безалкогольных напитков, где он используется для придания им того приятного шипения, которое производит такое большое удовлетворение во вкусе множества людей, которые глотают их ежедневно.
Примером полезности h3co3 является продукт, известный как карбогидразид, от Echemi.
https://www.echemi.com/produce/pr2112152844-water-treatment-carbohydrazide-cas-497-18-7.html
Это порошок кристаллического беловатого цвета, который можно использовать при лечении водного карбогидразида, обозначенного как CAS 497-18-7, который доступен в упаковках по 25 грамм, 100 грамм и 1 килограмм.
Это вещество марки Zhishang Chemicals и имеет плотность 1,3±0,1 г/см 3 , с температурой плавления от 150 до 153 ℃, показателем преломления 1,537, растворим в воде и стабилен при хранении в условиях от 0 до 6 ℃, при превышении этой температуры может возникнуть риск взрывоопасности, он также не совместим ни с веществами, обладающими сильными окислительными свойствами, ни с сильными кислотами.
Карбогидразид Echemi обладает высокой восстановительной способностью и особенно подходит для использования в производстве энергетических материалов, в качестве компонента взрывчатых материалов и ракетного топлива.
Это также эффективное средство для борьбы с ржавчиной в котлах, кроме того, оно обладает большим преимуществом, поскольку является продуктом с очень низкой токсичностью, не представляющим серьезной опасности для окружающей среды, и существует множество полезных свойств, среди которых промышленность химических волокон, медицинская промышленность, сельское хозяйство, где он используется в производстве гербицидов, в продуктах для регулирования роста растений, в производстве красителей и во множестве других применений.
Отказ от ответственности: ECHEMI оставляет за собой право окончательного объяснения и пересмотра всей информации.

 0111.10101010101010101010101010101010101010101010101010101010101010101011101110101.10111.10111.10111.10111.10111.10111.10111.1011098
0111.10101010101010101010101010101010101010101010101010101010101010101011101110101.10111.10111.10111.10111.10111.10111.10111.1011098 У людей гидрокарбонат участвует в метаболическом расстройстве, называемом путем расстройства Хартнапа. Вне человеческого тела карбонат водорода был обнаружен, но не определен количественно, в нескольких различных продуктах, таких как любисток, лимская фасоль, древовидный папоротник, горный ямс и налим. Это может сделать гидрокарбонат потенциальным биомаркером потребления этих продуктов. Таким образом, он является важным поглотителем в углеродном цикле. Он изоэлектронен азотной кислоте HNO3.
У людей гидрокарбонат участвует в метаболическом расстройстве, называемом путем расстройства Хартнапа. Вне человеческого тела карбонат водорода был обнаружен, но не определен количественно, в нескольких различных продуктах, таких как любисток, лимская фасоль, древовидный папоротник, горный ямс и налим. Это может сделать гидрокарбонат потенциальным биомаркером потребления этих продуктов. Таким образом, он является важным поглотителем в углеродном цикле. Он изоэлектронен азотной кислоте HNO3. 6
6 0248
0248
 /МС Спектр — 20В, Положительный
/МС Спектр — 20В, Положительный