Цитрат натрия E331 – вред, применение
Среди огромного количества консервантов, которые в наши дни с успехом используются в пищевой промышленности, особое место занимает цитрат натрия, известный как Е331. Он представляет собой белый порошок с довольно характерным кисловато-соленым вкусом, который получают синтезированным путем из лимонной кислоты. Впервые это вещество было искусственно создано более 100 лет назад, однако в промышленности получило широкое распространение лишь в середине прошлого века.
В чем польза Е331?
Цитрат натрия является прекрасным консервантом, который способен защитить от порчи многие продукты питания. Помимо всего прочего, Е331 усиливает вкусовые качества различных блюд, делая их более пряными и острыми. Это особенно важно, когда нужно подчеркнуть вкус нейтральных продуктов. Современные сыры и колбасы, в которые добавляется цитрат натрия, вряд ли были бы столь аппетитными без этой кисло-соленой добавки.
Примечательно, что еще в 1914 году цитрат натрия впервые был применен для стабилизации состава крови при ее переливании, что стало настоящей сенсацией в медицинском мире. Кроме этого, данное вещество помогает в лечении многих заболеваний,
Область применения цитрата натрия
Изначально консервант Е331 использовался в медицинских целях, да и в наши дни он входит в состав различных лекарственных препаратов, которые используются при лечении внутренних воспалительных процессов и, в частности, цистита. Кроме этого, цитрат натрия нередко применяют для того, чтобы нейтрализовать последствия алкогольного опьянения и снять симптомы похмелья.
Однако область применения этого вещества в пищевой промышленности гораздо более широка. Так, цистит натрия помогает усилить вкус газированных напитков и придать особую пикантность всевозможным специям. Кроме этого, в качестве консерванта Е331 добавляют в мясные блюда и молочные продукты, которые нуждаются в продолжительной термической обработке. Желе и варенье, конфеты и йогурты, различные виды консервов, в том числе и соки – во всех этих продуктах в наши дни нередко используется цитрат натрия, который считается практически безвредной добавкой. Кроме этого, данное вещество сегодня добавляют в кофемашины для стабилизации кислотности напитка и приданию ему особого аромата.
Чем опасен цитрат натрия и стоит ли им злоупотреблять?
Производители, применяющие Е331, едины во мнении, что этот консервант абсолютно безвреден. Однако независимые исследования все же показывают, что побочных эффектов у цитрата натрия все же довольно много. Это вещество не накапливается в организме и легко выводится естественным путем вместе с мочой. Однако если концентрация Е331 в крови человека превышает допустимую норму, которая составляет 1,5 г для взрослого человека, то возможны побочные эффекты в виде резкого повышения артериального давления, тошноты и рвоты, диареи, болей в животе, головокружения и кратковременной потери сознания.
Конечно же, в продуктах питание содержание Е331 незначительно, однако в некоторых лекарственных препаратах может быть довольно высоким. Поэтому при злоупотреблении подобными препаратами проблем со здоровьем избежать вряд ли удастся. Тем не менее, консервант Е331 официально разрешен к использованию во многих странах мира, включая Россию, и его применение считается нормой, когда речь заходит о пищевой и фармацевтической промышленности.
onwomen.ru
Цитрат — это… Что такое Цитрат?
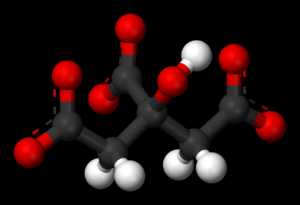 Цитрат ион
Цитрат ионЦитра́т (ион) (C3H5O(COO)33−) — ион лимонной кислоты, фактически лимонная кислота, лишенная трех ионов водорода.
Цитраты
Цитраты — соединения, имеющие в своем составе ион цитрата, соединения с ионными связями такие как соли или соединения с ковалентными связями, такие как эфиры. Например, соль цитрат натрия и эфир триметил цитрат.
Иные ионы лимонной кислоты
Так как лимонная кислота многоосновная кислота, существуют и промежуточные ионы гидроген цитрат-ион HC6H5O72− и дигидроген цитрат-ион H2C6H5O7−. Они также образуют соли, называемые кислые соли.
pH
Соли иона гидроген цитрата дают слабо выраженную кислую реакцию, в то время как соли иона цитрата (с внутренним ионом-заместителем, таким как натрий-ион) сами по себе — дают слабо выраженную основную реакцию.
Буферные свойства
Цитрат ион — основной компонент часто применяемого натриево цитратного 20х концентрированного буфера гибридизации. В существующей авторской литературе (Maniatis некорректно указано, что приготовление этого буфера включает 3 моля NaCl и 0,3 моля цитрата натрия, титрируемого далее в щелочную сторону NaOH до pH 7. В то время как два первых компонента уже смешаны, их реакция уже слабо основная и pH должен быть титрирован в кислую сторону HCl до тех же pH 7.
Этот раздел является переводом английской версии статьи, поэтому оставляю этот спор на совести авторов оригинальной статьи. —SSsilver 13:14, 7 декабря 2007 (UTC)
Лимонная кислота может применяться как слабая хелатная добавка.
В метаболизме
Цитратный цикл (АТФ цикл, цикл Кребса)
Цитрат-ион — посредник в цитратном цикле (АТФ, Кребса).
Роль в гликолизе
Высокая концентрация цитрата может ингибировать энзим фосфофруктокиназу (англ. phosphofructokinase) — участника цепи гликолиза.
См. также
dic.academic.ru
Е339 – Фосфаты натрия, применение, влияние, вред и польза

Вещество, выступающее в классификационной таблице пищевых добавок под маркировочным шифром Е 339 является искусственно получаемым консервантом-эмульгатором. Его уровень опасности для здоровья человека расценивается учеными-медиками как крайне низкий, то есть добавка практически безопасна.
Происхождение: 3-искусственное;
Категория добавки: консервант-эмульгатор;
Опасность: крайне низкого уровня;
Синонимические названия: Е 339, монофосфат натрия, фосфат натрия, Е-339, фосфат натрію, фосфати натрію.
Общая информация
Фосфаты натрия или проще говоря, Е-339, кроме того, что может выступать как эмульгатор, регулятор кислотности и стабилизатор, еще может играть роль влагоудерживающего агента, вещества, фиксирующего цвет продукта и усиливающего антиоксидантные свойства других веществ.
Вообще под обще название Фосфаты натрия вмещаются сразу несколько видом солей, получаемых из гидроксида натрия и кислоты фосфорной.
В физическом отношении эта добавка представляет собой белый гранулированный порошок с высокой степенью устойчивости к повышенным температурам и хорошей растворимостью в водной среде.
В пищевых производствах вполне применимы сразу три вида натриевых фосфатов. И маркируются эти вещества так: Е 339i (в виде химической формулы можно записать так: NaH2PO4), Е339ii (с химическим выражением в виде Na2HPO4), и Е339iii (который можно выразить химическими значениями в виде Na3PO4).

Влияние на организм
Вред
Добавка Е 339 является в фармакологии активным действующим веществом тех препаратов, которые призваны расслаблять кишечник при запорах. То есть, продукты с высоким содержанием данной добавки могут приводить к тому же эффекту. Следовательно, не стоит «увлекаться» фосфатами натрия и употреблять с ними продукты в больших количествах.
Польза
Особой пользы, кроме как слабительный эффект в случаях терапии запоров, данная добавка не несет.
Использование
В пищевых производствах добавка Е 339 применяется как разрыхлитель теста в хлебопекарных и кондитерских цехах. Кроме того, ее добавляют в напитки безалкогольные, молочную продукцию, сыры, сухое молоко и сливки, супы, бульоны, соусы и пасты, растворимые чаи, рабные и мясные консервы.
Раньше фосфаты натрия имели широчайшее применение в стиральных порошках и разной бытовой химии. Но с конце прошлого столетия многие страны запретили в своих производствах порошков и средств для уборки дома и стирки белья использование Е 339 любого вида. Цель такого запрета – снижение эвтрофикации водоемов.

Законодательство
Многие страны Евросоюза, Украина и Российская Федерация разрешают применять консервант Е 339 в производствах продуктов питания человека.
nebolet.com
| азелаил (от азелаиновой к-ты) | -ОС(СН2)7СО- | валерил* (пентаноил) | СН3(СН2)3СО- |
| азидо | N3— | валил (от валина) | (CH3)2CHCH(NH2)CO- |
| азино | =N-N= | винил (этенил) | СН2=СН- |
| азо | -N=N- | винилиден (этенилиден) | CH2=С= |
| азокси | -N(O)=N- | гексадеканоил | СН3(СН2)14СО- |
| акрилоил* (1 -оксо-2-пропенил) | CH2=CHCO- | гексаметилен (1,6-гександиил) | -(СН2)6— |
| аланил (от аланина) | CH3CH(NH2)CO- | гександиоил | -ОС(СН2)4СО- |
| 3-аланил | H2N(CH2)2CO- | гептадеканоил | СН3(СН2)15СО- |
| аллил (2-пропенил) | CH2=CHCH2— | гептанамидо | CH3(CH2)5CONH- |
| аллилиден (2-пропенилиден) | CH2=CHCH= | гептандиоил | -ОС(СН2)5СО- |
| амидино (аминоиминометил) | H2NC(=NH)- | гептаноил | СН3(СН2)5СО- |
| амил*(пентил) | CH3(CH2)4— | гидразино | H2NNH- |
| амино | H2N- | гидразо | -HNNH- |
| анизидино | CH3OC6H4NH- | гидрокси | HO- |
| анилино (фениламино) | C6H5NH- | гидроксиамино | HONH- |
| антраноил (2-аминобензоил) | 2-H2NC6H4CO- | гидроперокси | НОО- |
| арсино | AsH2— | гидроциннамоил | С6Н5(СН2)2СО- |
| ацетамидо (ацетиламино) | CH3CONH- | гиппурил (N-бензоилглицил) | C6H5CONHCH2CO- |
| ацетил | CH3CO- | гликолоил;гликолил (гидроксиацетил) | НОСН2СО- |
| ацетоацетил | CH3COCH2CO- | глиоксилоил; глиоксилил (оксоацетил) | НСОСО- |
| ацетонил | CH3COCH2— | глицил (аминоацетил) | H2NCH2CO- |
| бензаль* (бензилиден) | C6H5CH= | глициламино | H2NCH2CONH- |
| бензамидо (бензоиламино) | C6H5CONH- | глутамоил (от глутаминовой к-ты) |
-OC(CH2)2CH(NH2)CO- |
| бензгидрил (дифенилметил) | (C6H5)2CH- | глутарил (от глутаровой к-ты) |
-ОС(СН2)3СО- |
| бензил | C6H5CH2— | гуанидино | H2NC(=NH)NH- |
| бензилиден | C6H5CH= | гуанил (аминоиминометил) | H2NC(=NH)- |
| бензилидин | C6H5CHΞ | декандиоил | -OC(CH2)8CO- |
| бензоил | C6H5CO- | деканоил | CH3(CH2)8CO- |
| бензокси* (бензоилокси) | C6H5COO- | диазо | N2= |
| бифенилен | -C6H4—C6H4— | диазоамино | -NHN=N- |
| бифенилил | C6H5C6H5— | дисиланил | H3SiSiH2— |
| бутил | CH3(CH2)3— | дисилоксанилокси | H3SiOSiH2O- |
| втор-бутил (1-метилпропил) | CH3CH2CH(CH3)- | дисульфинил | -S(O)S(O)- |
| mpem—бутил (1,1-диметилэтил) | (CH3)3C- | дитио | -SS- |
| бутирил (1 -оксобутил) | CH3(CH2)2CO- | изоамил* (изопентил; 3-метилбутил) | (CH3)2CH(CH2)2— |
| бутокси | C4H9O- | изобутенил (2-метил-1 -пропенил) | (CH3)2C=CH- |
| втор-бутокси (1-метилпропокси) | C2H5CH(CH3)O- | изобутил (2-метилпропил) | (CH3)2CHCH2— |
| mpem—бутокси (1,1 -диметилэтокси) |
(CH3)3CO- | изобутилиден (3-метилпропилиден) | (СН3)2СНСН= |
| изобутирил (2-метил-1 -оксопропил) |
(СН3)2СНСО- | мезитил | 2,4,6-(СН3)3С6Н2— |
| изобутокси (2-метилпропокси) | (СН3)2СНСН2O- | меркапто | HS- |
| изовалерил* (3-метил-1 -оксобутил) | (СН3)2СНСН2СО- | метакрилоил (от метакриловой к-ты) |
СН2=С(СН3)СО- |
| изогексил (4-метилпентил) | (СН3)2СН(СН2)3— | металлил (2-метил-2-пропенил) | СН2=С(СН3)СН2— |
| изолейцил (от изолейцина) | C2H5CH(CH3)CH(NH2)CO- | метионил (от метионина) |
CH3SCH2CH2CH(NH2)CO- |
| изонитрозо* (гидроксиамино) | HON= | метокси | CH3O- |
| изопентил (3-метилбутил) | (СН3)2СН(СН2)2— | метил | Н3С- |
| изопентилиден (3-метилбутилиден) |
(СН3)2СНСН2СН= | лейцил (от лейцина) | (CH3)2CHCH2CH(NH2)CO- |
| изопропенил (1-метилэтенил) | СН2=С(СН3)- | малонил (от малоновой к-ты) |
-ОССН2СО- |
| изопропокси (1-метилэтокс) | (СН3)2СНО- | метилен | H2C= |
| изопропил (1-метилэтил) | (СН3)2СН- | метилтио | CH3S- |
| изопропилиден (1 -метилэтилиден) |
(СН3)2С= | миндалоил (от миндальной к-ты) |
С6Н5СН(ОН)СО- |
| изотиоцианато (изотиоциано) | SCN- | миристил (тетрадецил) | СН3(СН2)13— |
| изоцианато | OCN- | миристоил (от миристиновой к-ты) |
СН3(СН2)12СО- |
| изоциано | CN- | нафтил | -(С10Н7)- |
| имино | HN= | нафтилен | -(С10Н6)- |
| иодил | O2I- | неопентил (2,2-диметилпропил) |
(СН3)3ССН2— |
| иодозо* (иодозил) | OI- | нитроамино | O2NNH- |
| каприл* (деканоил) | СН3(СН2)8СО- | нитро | O2N- |
| каприлоил* (октаноил) | СН3(СН2)бСО- | нитрозоамино | ONNH- |
| капроил* (гексаноил) | СН3(СН2)4СО- | нитрозоимино | ONN= |
| карбазоил (гидразинокарбонил) | H2NNHCO- | нитрозо | ON- |
| карбамидо (карбамоиламино) | H2NCONH- | нонаноил (от нонановой к-ты) |
CH3(CH2)7CO- |
| карбамоил (аминокарбонил) | H2NCO- | оксалил (от щавелевой к-ты) |
-OCCO- |
| карбокси | НООС- | олеоил (от олеиновой к-ты) | CH3(CH2)7CH=CH(CH2)7CO- |
| карбонил | =С=O | оксо | O= |
| карбэтокси (этоксикарбонил) | С2Н5ОСО- | пальмитоил (от пальмитиновой к-ты) | CH3(CH2)14CO- |
| крезил* (гидроксиметилфенил) | НО(СН3)С6Н4— | пентаметилен (1,5-пентандиил) | -(CH2)5— |
| кротил (2-бутенил) | СН3СН=СНСН2— | пентил | CH3(CH2)4— |
| кротоноил | СН3СН=СНСО- | трет-пентил | CH3CH2C(CH3)2— |
| ксилидино [(диметилфенил)амино] | (CH3)2C6H3NH- | пивалоил (от пивалиновой к-ты) |
(CH3)3CCO- |
| ксилил (диметилфенил) | (СН3)2С6Н3— | пикрил (2,4.6-тринитрофенил) | 2,4,6-(NO2)3C6H2— |
| ксилилен [фениленбис(метилен)] | —СН2С6Н4СН2— | пимелоил(от пимелиновой к-ты) | OC(CH2)5CO- |
| лактоил (от молочной к-ты) | СН3СН(ОН)СО- | пиперидино (1-пиперидинил) | C5H10N- |
| лаурил (додецил) | СН3(СН2)11— | пиррил (пирролил) | C3H4N- |
| лауроил (от лауриновой к-ты) | СН3(СН2)10СО- | пренил (З-метил-2-бутенил) | (CH3)2C=CHCH2— |
| левулиноил (от левулиновой к-ты) |
СН3СО(СН2)2СО- | пропаргил (2-пропинил) | НС=ССН2— |
| 1-пропенил | -СН=СНСН3 | толуоил (метилбензоил) | СН3С6Н4СО- |
| 2-пропенил (аллил) | СН2=СНСН2— | треонил (от треонина) | CH3CH(OH)CH(NH2)CO- |
| пропионил* (пропанил) | СН3СН2СО- | триазано | H2NNHNH- |
| пропил | СН3СН2СН2— | триметилен (1,3-пропандиил) | -(СН2)3— |
| пропилиден | СН3СН2СН= | тритил (трифенилметил) | (C6H5)3C- |
| пропокси | СН3СН2СН2О- | фенацил | С6Н5СОСН2— |
| салицилоил (2-гидроксибензоил) | 2-НОС6Н4СО- | фенацилиден | С6Н5СОСН= |
| селенил* (селанил; гидроселено) | HSe- | фенетил (2-фенилэтил) | С6Н5CH2CH2— |
| серил (от серина) | HOCH2CH(NH2)CO- | фенил | С6Н5— |
| силил | H3Si- | фенилен (бензолдиил) | -C6H4— |
| силилен | H2Si= | фенокси | C6H5O- |
| силокси | H3SiO- | формамидо (формиламино) | HCONH- |
| сорбоил (от сорбиновой к-ты) | CH3CH=CHCH=CHCO- | формил | HCO- |
| стеарил (октадецил) | CH3(CH2)17— | фосфинил* (фосфиноил) | Н2Р(O)- |
| стеароил (от стеариновой к-ты) | CH3(CH2)14CO- | фосфино* (фосфанил) | Н2Р- |
| стирил (2-фенилэтенил) | C6H5CH=CH— | фосфо | O2Р- |
| субероил (от субериновой к-ты) | -OC(CH2)6CO- | фосфоно | (HO)2P(O)- |
| сукцинил (от сукциновой к-ты) | -OCCH2CH2CO- | фталоил (от фталевой к-ты) | 1,2-С6Н4(СО-)2 |
| сульфамоил (сульфамид) | H2NSO2— | фумароил (от фумаровой к-ты) | -ОССН=СНСО- |
| сульфамино (сульфоамино) | HOSO2NH- | фурфурил (2-фуранилметил) | ОС4Н3СН2— |
| сульфанилил [(4-аминофенил) сульфонил] | 4-H2NC6H4SO2— | фурфурилиден (2-фуранилметилен) | ОС4Н3СН= |
| сульфено | HOS- | хлорформил (хлоркарбонил) | СlСО- |
| сульфгидрил (меркапто) | HS- | цетил* (гексадецил) | СН3(СН2)15— |
| сульфинил | OS= | циано | NC- |
| сульфо | HO3S- | цианамидо (цианоамино) | NCNH- |
| сульфонил (сульфурил) | -SO2— | цианато | NCO- |
| терефталоил | 1,4-C6H4(CO-)2 | циннамил (З-фенил-2-пропенил) | C6H5СН=СНСН2— |
| тетраметилен | -(CH2)4— | циннамилиден | С6Н5СН=СНСН= |
| тиенил (от тиофена) | (C4H3S)- | циннамоил | С6Н5СН=СНСО- |
| тиокарбокси | HOSC- | этантоил* (гептаноил) | СН3(СН2)5СО- |
| тиокарбонил (карботионил) | =CS | эпокси | -O- |
| тионил* (сульфинил) | -SO- | этенил(винил) | CH2= CH- |
| тиоцианато (тиоциано) | NCS- | этил | СН3СН2— |
| тозил [(4-метилфенил) сульфонил] | 4-CH3C6H4SO2— | этилен | -СН2СН2— |
| толил (метилфенил) | СН3С6Н4— | этилиден | СН3СН= |
| а-толил (бензил) | C6H5CH2— | этилтио | C2H5S- |
| толилен (метилфенилен) | -(CH3C6H3)- | этинил | HC=C- |
| толуидино [(метилфенил)амино] | CH3C6H4NH- | этокси | C2H5O- |
tehtab.ru
Свойства фенолов | Дистанционные уроки
20-Авг-2012 | комментария 2 | Лолита Окольнова
это органические спирты, в которых группа -OH непосредственно связана с бензольным ядром — из этого строения вытекают все химические свойства фенолов.
Классификация фенолов
Как и не ароматические спирты, фенолы бывают однотомные и многоатомные.
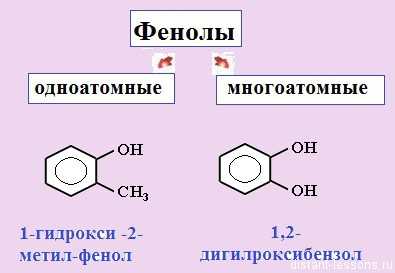
Понятно, что изомерия у них будет структурная.
Вот на что надо особенно обратить внимание, так это на
Cтроение фенолов
 У самого бензольного кольца занятное строение — на 6 атомов углерода приходится всего 6 атомов водорода, система связей сопряженная и очень ненасыщенная.
У самого бензольного кольца занятное строение — на 6 атомов углерода приходится всего 6 атомов водорода, система связей сопряженная и очень ненасыщенная.
Поэтому атом кислорода со своей свободной электронной парой приходится очень кстати.
Это означает, что атом кислорода довольно крепко связан с бензольным кольцом, его электронная плотность смещена к бензольной структуре. Что это означает химически?
Химические свойства фенолов
- Если атом кислорода «привязан» к бензольному кольцу, то фенол больше проявляет кислотные свойства — он легче отдает протон водорода, чем всю группу -OH (в отличие от алифатических спиртов)
- А вот с HCl фенолы не реагируют!!! Это отличие химических свойств фенолов от неароматических спиртов!!!
- Реакции по кольцу у фенолов такие же, как у бензолов. Единственное, что надо учитывать — ориентирование заместителей.
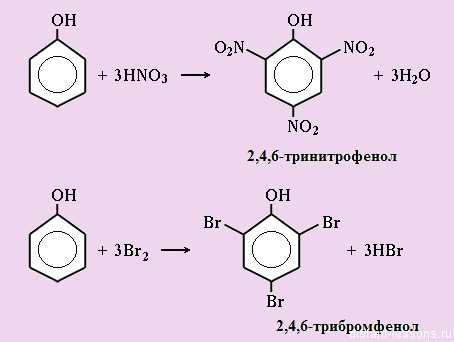
Кстати, последняя реакция — качественная на фенолы, точнее на бензольное кольцо.
И еще одна качественная реакция на фенол:
с солями Fe (3+) образуется фиолетовый комплекс
6C6H5OH + FeCl3 → [Fe(C6H5OH)6]CI3
Получение фенолов
Способы получения фенолов разнообразием не отличаются, основной метод — так называемый «Кумольный способ»:
Вот, кстати, несколько фенолов, названия которых желательно знать наизусть — встречаются в заданиях ЕГЭ:
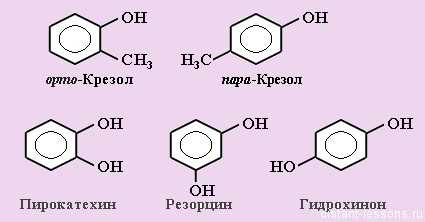
- в ЕГЭ это вопрос А14 — Свойства предельных одноатомных и многоатомных спиртов, фенола
Категории: |
Обсуждение: «Свойства фенолов»
(Правила комментирования)distant-lessons.ru
