Конструкционный металл — Большая Энциклопедия Нефти и Газа, статья, страница 1
Конструкционный металл
Cтраница 1
Конструкционные металлы и сплавы, которые используют в технике низких температур, по хладостойкости могут быть разделены на четыре основные группы. [1]
Конструкционные металлы представляют собой сплавы многих рдзнородных металлов. При наличии внешних растягивающих нагрузок в конце концов возникает трещина, которая может развиваться в дальнейшем за счет электрохимического механизма растворения анодного металла на дне трещины и локального разрушения ослабленного материала. [2]
Конструкционные металлы и сплавы применяют совместно с графитом в машинах и аппаратах, различающихся как по назначению, так и по рабочим параметрам эксплуатации. [3]
Конструкционные металлы имеют различные механические свойства, зависящие от их химического состава и структурного состояния. Сочетание таких характеристик, как химический состав, механические свойства и структурное состояние металла, определяет его сопротивление обработке резанием. Обрабатываемость металлов резанием находит свое проявление в общих закономерностях процессов стружкообразования, формирования новых поверхностей и качества обработанных поверхностей. [4]
Конструкционные металлы, работающие в области высоких температур, должны обладать жаропрочностью и жаростойкостью. [6]
Конструкционные металлы и сплавы, которые используют в технике низких температур, по хладостойкости могут быть разделены на четыре основные группы. [7]
Конструкционные металлы являются конгломератом спаянных, но случайно ориентированных анизотропных кристаллических зерен. Пластическое деформирование начинается сначала только в отдельных, наиболее неблагоприятно ориентированных зернах, в которых касательные напряжения значительно выше средних значений, и лишь при дальнейшем увеличении напряжений зона пластических деформаций распространяется на значительные объемы. Совокупность пластических сдвигов в отдельных зернах создает полосы скольжения, проходящие через конгломерат многих зерен и приблизительно совпадающие по направлению с плоскостями действия наибольших касательных напряжений, определяемых обычными методами механики сплошной среды. Схематически этот процесс показан на рис. 1.2. Под действием сдвигающих усилий отдельные слои материала скользят относительно друг друга, причем объем деформируемого материала остается постоянным. В результате получается угол пластического сдвига — утах — Полосы скольжения являются местами концентрации микротрещин, из множества которых на определенном этапе деформирования формируется одна или несколько магистральных ( микроскопических) трещин вязкого разрушения, которые могут быть [6, 54] трещинами сдвига или трещинами нормального отрыва. [9]
Машиноподелочные конструкционные металлы, естественно, не являются монокристаллами, а состоят из большого количества связанных между собой зерен. Между зернами располагаются узкие прослойки — границы зерен. Границы зерен могут быть представлены как нарушения упорядоченного расположения атомов в кристаллической решетке. При значительном отклонении углов ориентации дислокации взаимодействуют между собой. [10]
Как конструкционный металл уран не используется. В реакторы элемент уран вводится в различных видах, не обязательно в виде металла. Однако преобладающим видом ядерного горючего остается металическип уран, легированный и нелегированный. [11]
Все технические конструкционные металлы
( сталь, чугун, медь и др.) могут быть покрыты гальваническим методом. Гальваническое покрытие алюминия разработано и технически опробовано, но еще не имеет широкого практического распространения вследствие значительных технологических трудностей. [12]Все основные промышленные конструкционные металлы и сплавы ( черные и цветные) хорошо обрабатываются в растворе хлорида натрия. [14]
Из конструкционных металлов титан по своему распространению в природе находится на четвертом месте после железа, алюминия и магния. Техническое значение титана и сплавов на его основе определяется следующими данными: удельный вес титана 4 5 и, таким образом, титан и его сплавы по этой характеристике являются переходными между легкими сплавами на основе магния и алюминия, и сталями. Высокопрочные титановые сплавы имеют удельную прочность ( отношение прочности к единице веса), соизмеримую с самыми высокопрочными сталями. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
Тема 3. Конструкционные металлы и сплавы
3.1. Конструкционные стали.
Сталь является сложным по составу железо – углеродистым сплавом. Кроме железа и углерода – основных компонентов, а также возможных легирующих элементов, сталь содержит некоторое количество постоянных и случайных примесей, влияющих на ее свойства.
Углерод, концентрация которого в конструкционных сталях достигает 0,8 %, оказывает определяющее влияние на их свойства. Степень его влияния зависит от структурного состояния стали, ее термической обработки.
После отжига или в горячекатаном состоянии без термической обработки углеродистые конструкционные стали имеют ферритно-перлитную структуру, состоящую из двух фаз – феррита и цементита. Количество цементита, который имеет высокую твердость и хрупкость, увеличивается пропорционально концентрации углерода. В связи с этим, по мере повышения содержания углерода, повышается прочность и твердость, но снижаются пластичность и вязкость стали (рисунок 3.1).
Кроме снижения ударной вязкости углерод заметно повышает верхний порог хладноломкости, расширяя температурный интервал перехода стали в хрупкое состояние (рисунок 3.2). Каждая 0,1 % С повышает верхнюю границу этого перехода примерно на 20 С.
При 0,4 % С порог хладноломкости равен 0 С.
При большей концентрации углерода температура хрупкости достигает 20 С; сталь становится менее надежной в работе.
Влияние
углерода еще более значительно после
закалки стали. Например,
При большей концентрации углерода в становится нестабильным из-за хрупкого разрушения стали.
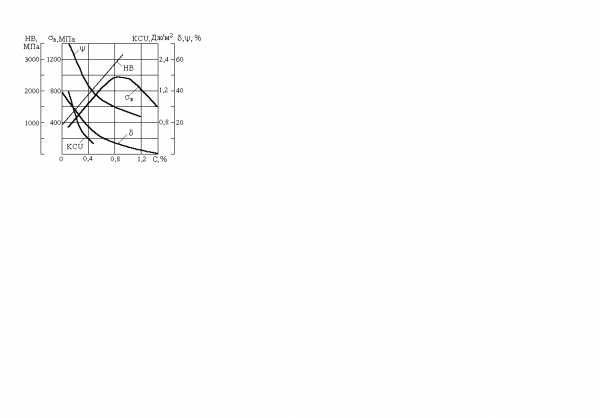
Рисунок 3. 1. Влияние углерода на механические свойства горячекатаных сталей
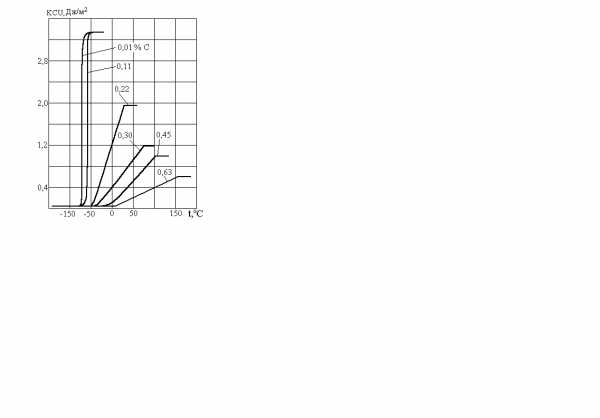
Рисунок 3. 2. Влияние углерода на хладноломкость стали
Углерод изменяет и технологические свойства стали. При увеличении его содержания снижается способность сталей деформироваться в горячем и, особенно в холодном состоянии, затрудняется свариваемость.
Постоянными примесями в стали являются марганец, кремний, сера, фосфор и такие газы, как кислород, азот, водород.
Марганец — полезная примесь вводится в сталь для раскисления и остается в ней в количестве 0,3…0,8 %. Марганец уменьшает вредное влияние кислорода и серы.
Кремний – полезная примесь, вводится в сталь в качестве активного раскислителя и остается в ней в количестве до 0,4 %, оказывая упрочняющее действие.
Сера – вредная примесь, вызывающая красноломкость стали – хрупкость при горячей обработке давлением. В стали она находится в виде сульфидов FeS, которые образуют с железом эвтектику с низкой температурой плавления (988 С) и располагаются по границам зерен. При горячей деформации границы зерен оплавляются, и сталь хрупко разрушается.
Введение марганца устраняет красноломкость за счет связывания серы в сульфиды MnS, которые при этом снижают пластичность и вязкость стали.
Положительное влияние серы проявляется лишь в улучшении обрабатываемости резанием.
Фосфор – вредная примесь. Он растворяется в феррите, упрочняет его, но вызывает хладноломкость – снижение вязкости по мере понижения температуры. Каждая 0,01 % Р повышает порог хладноломкости на 25 С.
Кислород, азот и водород – вредные примеси. Их влияние наиболее сильно проявляется в снижении пластичности и повышении склонности стали к хрупкому разрушению.
По концентрации углерода стали подразделяют на низкоуглеродистые (< 0,3 % C), среднеуглеродистые (0,3…0,7) %С) и высокоуглеродистые (> 0,7 % С).
По качеству стали классифицируют на стали обыкновенного качества, качественные, высококачественные и особовысококачественные. Качество стали определяется содержанием вредных примесей. Стали обыкновенного качества содержат до 0,055 % S и 0,045 % P, качественные – не более 0,04 %S и 0,035 %P, высококачественные – не более 0,025 %S и 0,025 %P, особо высококачественные — не более 0,015 % S и 0,025 % P.
По степени раскисления и характеру затвердевания стали классифицирую на спокойные, полуспокойные и кипящие.
Раскисление – процесс удаления из жидкого металла кислорода, проводимый для предотвращения хрупкого разрушения стали при горячей деформации.
Спокойные стали раскисляют марганцем, кремнием и алюминием. Они содержат мало кислорода и затвердевают спокойно без газовыделения. Кипящие стали раскисляют только марганцем. Перед разливкой в них содержится повышенное количество кислорода, который при затвердевании, частично взаимодействуя с углеродом, удаляется в виде пузырей CO. Кипящие стали дешевы, их производят низкоуглеродистыми и практически без кремния (Si 0,07 %), но с повышенным количеством газообразных примесей. Полуспокойные стали по степени раскисления занимают промежуточное положение между спокойными и кипящими.
Углеродистые конструкционные стали выпускают обыкновенного качества и качественные.
Стали обыкновенного качества (ГОСТ 380) выпускают в виде проката и поковок. В зависимости от гарантируемых свойств их поставляют трех групп А, Б, В. Их маркируют сочетанием букв «Ст» и цифрой от 0 до 6, показывающей номер марки.
Стали групп Б и В имеют перед маркой буквы Б и В, указывающие на их принадлежность к этим группам. Группа А в обозначении марки не указывается.
Степень раскисления обозначается добавлением индексов: «сп» — спокойная, «пс» — полуспокойная, «кп» — кипящая. Например, Ст3сп, БСт3пс, ВСт3кп. Спокойными и полуспокойными производят стали Ст1…Ст6, кипящими – Ст1…Ст4 всех трех групп. Сталь Ст0 по степени раскисления не разделяют.
Стали группы А поставляют с гарантированными механическими свойствами, химический состав не указывают. Стали группы Б поставляют с гарантированным химическим составом, механические свойства не гарантируются. Стали группы В поставляют с гарантированными механическими свойствами и химическим составом.
Углеродистые стали обыкновенного качества предназначены для изготовления различных металлоконструкций, а также слабонагруженных деталей машин и приборов.
Соответствие некоторых отечественных марок сталей обыкновенного качества с зарубежными аналогами представлены в таблице 3.1.
Таблица 3.1
Аналоги зарубежных сталей обыкновенного качества
Россия (ГОСТ) | Германия (DIN) | США (ASTM) | Япония (JIS) | Китай (GB) |
Ст2сп | RSt34-2- | К02502 | — | Q215A |
Cт3Гпс, Ст5Гпс | St52-3I S235J2G3 | A572/42 | SM41B | — |
Cт3Гпс | — | A131/B, A573/58 | SM41B | — |
Ст2кп, Ст2пс | Rst34-2 | — | SS34 | Q215 |
Ст3сп | RSt37-2 | A283/C | — | — |
Ст3кп, Ст3пс | Ust37-2 | A283/C | — | — |
Ст4сп | Ust42-2 St44-2 | А283/D, A131/A | SS41, SM41A | — |
Ст5сп | St50-2 | — | SS50 | Q275 |
Ст6сп | St60-2 | — | — | — |
Углеродистые качественные стали поставляют в виде проката, поковок и других полуфабрикатов с гарантированным химическим составом и механическими свойствами.
Эти стали маркируются двухзначными числами 05, 08, 10, 15, 20, …, 85, обозначающими среднее содержание углерода по массе в сотых долях процента (ГОСТ 1050).
Спокойные стали маркируют без индекса, полуспокойные и кипящие – с индексом.
Качественные стали для станков – автоматов маркируют с указание буквы А впереди: А11, А12, А20.
Качественные стали для котлов маркируют с указание буквы «К» позади: 12К, 15К…и т. д.
Низкоуглеродистые стали 05, 08, 10 применяют для холодной штамповки различных изделий.
Без термической обработки в горячекатаном состоянии их используют для шайб, прокладок, кожухов и других деталей, изготавливаемых холодной деформацией и сваркой.
Стали 15, 20, 25 – цементуемые, предназначены для деталей небольшого размера, от которых требуется твердая, износостойкая поверхность и вязкая сердцевина (кулачки, шестерни и т. д.), а также горячекатаные и после нормализации для изготовления деталей машин и приборов невысокой прочности (крепежные детали, втулки, штуцеры, трубы, змеевики и т. д.).
Среднеуглеродистые стали 30…55 применяют после улучшения для изготовления деталей небольшого размера, работоспособность которых определяется сопротивлением усталости (шатуны, коленчатые валы, оси и т. п.).
Стали 40 … 50 после нормализации и поверхностной закалки применяют для изготовления крупных деталей, работающих при невысоких циклических и контактных нагрузках, например, валы, ходовые винты, кулачки распределительных валиков и т. д.
Стали с высоким содержанием углерода (60 … 85), а также с увеличенным содержанием марганца (60Г, 65Г и 70Г) преимущественно применяют в качестве рессорно-пружинных после закалки и среднего отпуска, а также для прокатных валков, шпинделей станков и других крупных деталей после нормализации.
Соответствие некоторых отечественных марок конструкционных сталей с зарубежными аналогами представлены в таблице 3.2.
Таблица 3.2
Аналоги зарубежных углеродистых сталей
Страны СНГ (ГОСТ) | Евронормы | США (стандарты) | Япония (JIS) | Китай (GB) |
10 | С10Е (1.1121)* | 1010 | S10C | 10 |
15 | С15Е (1.1141)* | 1015 | S15C | 15 |
20 | С22Е (1.1151)* | 1020 | S20C | 20 |
25 | С25Е (1.1158)* | 1025 | S25C | 25 |
30 | С30Е (1.1178)* | 1030 | S28C | 30 |
35 | С35Е (1.1181)* | 1035 | S35C | ML35 |
40 | С40Е (1.1186)* | 1040 | S40C | 40 |
45 | С45Е (1.1191)* | 1045 | S48C | 45H |
50 | С50Е (1.1206)* | 1050 | S50C | 55 |
Примечание: * — цифровое обозначение.
Контрольные вопросы:
1. Каким параметром характеризуются доэвтектоидные, эвтектоидные и заэвтектоидные стали?
2. Какие марки сталей применяются для холодной штамповки?
3. Как классифицируются стали по степени раскисления?
4. Какие марки сталей относятся к улучшаемым после закалки?
5. Что означает буква «Ш» в конце марки стали?
6. Что обозначает буква перед маркой стали Ст3кп?
7. С какой целью проводят раскисление сталей?
8. Как классифицируются стали по качеству?
9. Какие существуют аналоги зарубежных сталей отечественным марка?
studfiles.net
Металлы конструкционные — Справочник химика 21
Гибка двухслойных листов, плакированных коррозионно-стойкой сталью, может производиться как в холодном, так и в горячем состоянии, плакирующим слоем внутрь или наружу. Прокладки, соприкасающиеся при гибке с плакирующим слоем, изготовляют из коррозионно-стойкой стали, чтобы предотвратить налипание на поверхность плакирующего слоя частиц металла, что возможно при использовании обычной конструкционной стали. Холодная гибка двухслойной стали должна производиться при температуре не ниже 20° С. При гибке в горячем состоянии заготовки должны быть нагреты до 1150—1200 С их обработка должна завершаться при температуре не ниже 900—850° С. Заготовки, обработанные методом горячей деформации, должны быть подвергнуты последующей термической обработке, режимы которой приведены в табл. 10, а. [c.42]
Для борьбы с коррозией теплообменников внутреннюю или наружную поверхность металлических труб и внутреннюю поверхность кожухов облицовывают стеклом применяют плакировку, сочетающую механическую прочность одного металла с коррозионной стойкостью другого. Так, тонкий слой нержавеющей сталп прокаткой соединяют с листом обычной углеродистой стали. Применяют иногда электролитические или химические покрытия, образующие противокоррозионную пленку на конструкционных материалах. При случае несовместимости прокачиваемой жидкости с материа.1 ами труб используют биметаллические трубы, например из никелевого сплава с одной стороны и алюминиевого — с другой. [c.270]
Сборник составлен в основном из статей, направленных авторами в журнал Атомная энергия , и частично из работ, представленных на первом Всесоюзном совещании по экстракции, состоявшемся в декабре 1959 г. Ввиду большого числа статей представлялось целесообразным распределение материала по отдельным выпускам. При этом для удобства читателей материал по каждому из сборников распределен более или менее равномерно, т. е. в каждом из выпусков имеются работы по теории экстракции, применению экстракционных процессов для получения чистых редких металлов, конструкционных материалов и ядерного горючего, отчасти — по переработке облученных тепловыделяющих элементов, а также работы по расчету и описанию экстракционной аппаратуры. [c.3]
Двухслойный металл, состоящий из основного слоя черного металла (конструкционного) и тонкого слоя нержавеющей стали или другого легированного сплава, соприкасающегося с корродирующем раствором. [c.15]
Физико-механические характеристики новых конструкционных металлов приведены в табл. 2.8. [c.65]
Концентрация растворенного в металле газа помимо температуры зависит от парциального давления атомарного водорода, которое определяется общим давлением. Зависимость растворимости водорода от давления для ряда конструкционных сталей имеет следующий вид [48] [c.143]
Максимально возможная температура нагревания кислорода определяется свойствами применяемого конструкционного металла. При применении легированных сталей обычно ограничиваются нагреванием до 650°С. [c.95]
Металлы и сплавы. Сталь. Благодаря широкому спектру свойств, определяемых составом и химико-термической обработкой, сталь — наиболее распространенный конструкционный материал. [c.97]
Ванадиевая коррозия в процессе эксплуатации и испытаний авиационных ГТД не отмечалась. Это обусловлено низким — не более 10 —10 (масс.)—содержанием ванадия в реактивных топливах. Пентаоксид ванадия имеет температуру плавления 685 °С и с конструкционными материалами образует легкоплавкие соединения. Кроме того, ванадий имеет переменную валентность, что делает его способным переносить кислород из газа к поверхности металла. [c.182]
Стальные свободные фланцы на отбортовке (рис. 29, е) применяют на аппаратах из цветных металлов, из некоторых пластмасс, поддающихся отбортовке, и при необходимости максимально экономить дефицитный конструкционный материал, например титан и. и высоколегированную сталь. Фланцы на отбортовке применяют для условного давления до 0,6 МПа. [c.54]
К частям трубопроводных систем относятся трубы и их фасонные части, детали для соединения и крепления трубопроводов, компенсаторы температурных удлинений, трубопроводная арматура. Трубы — основная часть трубопроводов. Их изготовляют из стали, чугуна, цветных металлов, стекла, керамики, фарфора, пластмасс, т. е. практически из всех конструкционных материалов химического машиностроения. Наиболее широко применяют стальные трубы [13]. [c.254]
Свойства алюминия, обусловившие его широкое использование, перечислены в табл. 11.9. После железа алюминий — наиболее широко используемый металл. Как автомобильная, так и аэрокосмическая промышленность широко используют алюминий в качестве конструкционного материала из-за его прочности и легкости. Уменьшение массы автомобиля и самолета приводит к значительной экономии топлива. [c.160]
Полимерные материалы (пластмассы, резина) отличаются разнообразными эксплуатационными и хорошими технологическими свойствами, благодаря чему в ряде случаев не только успешно заменяют металлы, но и как конструкционные материалы имеют самостоятельное значение. [c.102]
В условиях хранения и эксплуатации углеводородное топливо С растворенным в нем кислородом находится в контакте с металлической поверхностью стенками баков для хранения, трубопроводов, насосов. Известно, что металлы, их оксиды и соли катализируют окисление углеводородов. В связи с этим необходимо определить влияние поверхности конструкционных материалов на окисление топлива в условиях хранения соотношение между процессами окисления топлива в объеме и на стенке стадии окисления, на которые воздействует металлическая стенка ингибиторы, которые следует применять для стабилизации топлива в присутствии металлической поверхности и др. Наряду с гетерогенным катализом в топливе. может протекать и гомогенный окислительный катализ, вызываемый растворенными в нем солями металлов. Роль металлов в окислении углеводородов неоднократно исследовалась. Достаточно подробные данные имеются о механизме гомогенного катализа окисления углеводородов растворенными солями жирных кислот. [c.192]
Жаропрочность, как и жаростойкость, зависит от свойств конструкционных материалов она ухудшается с повышением температуры и скорости газового потока. Соответствующие зависимости на рис. 5.32 представлены временем до разрушения испытуемых образцов металлов. [c.180]Применительно к наиболее важному и распространенному металлическому конструкционному материалу — сплавам на железной основе и наиболее распространенному процессу химической коррозии металлов — газовой коррозии — можно отметить следующее. [c.137]
Полиэфиры на основе оксиалкилированного дифенилолпропана применяются в основном в виде слоистых пластиков, как покрытия для металлов или других конструкционных материалов и в виде литых изделий. Они могут найти широкое применение в химической, целлюлозной, бумажной, нефтяной и текстильной промышленности, а также в гальванотехнике. [c.54]
Эта теория в ее современном виде объясняет не только общую величину коррозии, но и влияние гетерогенности поверхности корродирующих металлов (включая и структурную гетерогенность) на характер и скорость (увеличение и уменьшение ее, равно как и отсутствие влияния в ряде случаев) коррозионного разрушения. Она была широко использована для объяснения коррозионного поведения конструкционных металлов и сплавов в различных условиях [c.187]
В морской воде, коррозия в которой протекает с катодным контролем и условия для пассивности металлов неподходящи, катодные контакты являются вредными, а часто и опасными для ответственных конструкционных узлов с малой поверхностью. [c.402]
Стеклопластики найдут широкое применение в машиностроении и, в частности, при изготовлении крупногабаритных изделий, таких, как кузовы автомобилей, корпусы мелких судов, детали вагонов. По прочности армированные стеклопластики превосходят сталь, при этом имеют значительно более низкий удельный вес (в 1,5 раза по сравнению с дюралюминием и в 4 раза—со сталью), а также высокую коррозийную стойкость, не требуют окраски. Трудоемкость изготовления деталей из них, благодаря возможности получения изделий даже сложной конфигурации, за одну операцию значительно ниже, чем изготовление соответствующих деталей из металлов. Совокупность этих свойств делает стеклопластики одним из основных конструкционных материалов, производство которых все время увеличивается. Создание в республике производства стеклопластиков позволит высвободить значительное количество металла и обеспечить потребности машиностроения, а также развить новые заводы по выпуску кузовов автомобилей и других крупногабаритных изделий- [c.372]
Склеивание металлов в конструкциях несилового назначения контровка болтов Склеивание сталей, алюминиевых и титановых сплавов Склеивание металлов конструкционных неме таллических материа лов и для изготовле Н1 я клеесварных сое динений [c.479]
Новые конструкционные металлы и сплавы. Условия эксплуатации оборудования в химической промышленности иногда оказываются СЛИН1К0М жесткими даже для высоколегированных сталей. В этом случае для его изготовления требуется применение дефи-цигиых металлов и их сплавов. Интенсификация отдельных процессов является также предпосылкой необходимости применения таких материалов, например, для ответственных частей аппарата, где в результате наиболее острой фазы реакции имеют место максимальная температура и химическая активность, а также в условиях резких колебаний температуры и теплообмена в агрессивных [c.64]
Фланцы литые применяют для литой стальной или чугунной арматуры плоские приварные — для сварной арматуры фланцы с шейкой рекомендуется применять для штуцеров ответственных апг[аратов из углеродистой и легированных сталей, так как шейка повышает прочность фланца н обеспечивает качественную сварку его с трубой. Стальные свободные фланцы на отбортовке (ГОСТ 12822 80) следует применять для входных и выходных штуцеров у аппаратов и машин из алюминия, меди и других цветных металлов или керамики, фсрросилида и других пеметалличсских и хрупких материалов. Кроме того, стальные свободные фланцы рекомендуется применять в целях экономии дефицитных и дорогостоя-ии-1х конструкционных материалов, например высоколегированной хромоникелевой стали, титана, сплава цветных металлов и др. Для штуцеров из двухслойных металлов желательно применять свободные фланцы из углеродистой стали на приварном кольце. [c.80]
Камеральный метод зактночается в переносе размеров на материал по предварительным эскизам развертки. Эскизы содержат размеры, вычисленные по данным рабочих чертежей деталей, и выполняются в технолог ических шт конструкционных бюро. Плазовый метод разметки заключается в том, что развертка вьнюдняется в натуральную величину на специально подготовленной плоскости, называемой плазом, или непосредственно на металле. Для плазового метода предварительная разработка эскизов заготовки отпадает. [c.100]
Нафтеновые кислоты (главным образом низкомолекулярные) оказывают значительное корродирующее влияние на металлы, особенно цветные и их сплавы. Однако следует заметить, что дюралюминий довольно устойчив к воздействию нафтеновых кислот. В результате воздействия нафтеновых кислот па конструкционные материалы в процессе применения топлив образуются соли нафтеновых кислот, которые являются одной из составных частей образующихся в топливах нерастворимых осадков, отрицательпо влияющих на эксплуатационные свойства топлив. [c.54]
Из поликарбонатов можно получать пленки и волокна, перерабатывать в изделия разными методами. Поликарбонаты в качестве конструкционного материала успешно конкурируют с металлом, древесиной, стеклом. Потребителями поликарбонатов являются электротехническая и электронная промышленность, производство изделий технического и бытового назначения, где поликарбонаты вытесняют металлы их используют в производстве пленочных и ли-стошх материалов, а также красок и noKpbiTHH.J [c.51]
Н пкель. Он обладает хорошими литейными свойствами, легко куется и штампуется. Его сваривают никелевыми электродами в атмос(1)ере инертного газа. Аппаратуру из никеля применяют для процессов щелочного плавления, при переработке органических кислот, а также в тех случаях, когда требуется высокая чистота продукта или недопустимо применение кислотостойких сталей пследствпе нх действия как катализатора, ускоряющего ход нежелательных реакций. Никель — очень дефицитный металл, и для химической аппаратуры как самостоятельный конструкционный материал он применяется редко. [c.21]
Прибавка на коррозию равна скорости коррозии v (мм/год), умноженной на срок службы т аппарата (обычно 10—12 лет) с = = ит. Скорость коррозии определяют по справочникам или По лабораторным испытаниями. Прибавку на коррозию обычно принимают I—2 мм, что соответствует скорости 0,1—0,2 мм/год. При более интенсивной коррозии стенки аппарата необходимо защищать антикоррозионными покрытиями или заменять конструкционный материал другим, более коррозионно-стойким. Для неответственных частей аппаратов скорость коррозии может быть принята и большей. Если стенка подвергается коррозии с двух сторон, то необходимо ввести две прибавки на коррозию. Для чугунных отливок прибавку на коррозию и возмолшую разностенность отливок принимают равной 5—9 мм. Для аппаратов из двухслойной стали в расчет принимается только слой основного металла, а плакирующий слой может быть учтен только в качестве прибавки на коррозию. Прибавки С2 и Сз учитывают только тогда, когда сумма их превышает 5% от расчетной толщины листа. [c.39]
Это объясняется чрезвычайнЪ большим ассортиментом перерабатываемого сырья, широким диапазоном производительности и различным гидравлическим режимом колонн [1, 30]. В качестве конструкционного материала для изготовления колонных аппаратов наиболее широко применяют углеродистую и кислотостойкую сталь, реже цветные металлы и чугун. В настоящее время осваиваются тарельчатые колонны из неметаллических материалов—керамики, графита и фторопласта. [c.137]
Чистые щелочноземельные металлы имеют более высокие температуры плавления и кипения по сравнению с щелочными металлами, потому что для образования металлических связей в них имеется по два электрона на атом. По той же причине они обладают большей твердостью, хотя их тоже можно резать острым стальньгм ножом. Бериллий и магний-единственные элементы этой группы, широко используемые как конструкционные. металлы благодаря своей легкости они используются в чистом виде или в составе сплавов в авиастроительной и космической промышленности, где вес является очень важным фактором. [c.436]
Установлено [175], что окисление реактивных топлив катализируется конструкционными материалами по скорости окисления их можно расположить в следующем порядке чистые металлы — РЬ>Си>8п>Сг>Ре>А1 стали — 12Х18Н9Т> [c.161]
Металлы и их сплавы являются наиболее важными современными конструкционными материалами. Всюду, где эксплуатируются металлические конструкции, есть вещества, которые, взаимодействуя с металлами, постепенно их разрушают ржавление металлических конструкций (железных кровель зданий, стальных мостов, станков и оборудования цехов) в атмосфере ржавление наружной металлической обшивки судов в речной и морской воде разрушение металлических баков и аппаратов растворами кислот, солей и щелочей на химических и других заводах ржавление стальных трубопроводов в земле окисление металлов при их нагревании и т. п. У большинства металлов в условиях их эксплуатации более устойчивым является окисленное (ионное) состояние, в которое они переходят в результате коррозии. Слово коррозия происходит от латинского согго(1еге , что означает разъедать . [c.8]
Неоднородность металлической фазы, жидкой коррозионной средй и физических условий (см. с. 188), а также конструкционные особенности металлических сооружений (их полиметаллич-ность, наличие узких зазоров и др.) делают поверхность металл-электролит электрохимически гетерогенной, что часто оказывает влияние на скорость электрохимической коррЬзии металлов и ее распределение, изменяя характер коррозионного разрушения. Даже сплошная коррозия металлов бывает по этим причинам неравномерной или избирательной. Кроме того, встречается местная коррозия различных видов, опасность которой обычно тем больше, чем больше локализовано коррозионное разрушение. Местная коррозия не определяется общей скоростью коррозионного процесса. [c.414]
Существующие нормы и методы расчета на прочность [1-3] не учитывают наличия трещиноподобных образований в основном металле и в сварных соединениях, несмотря на то, что дефекты типа микроскопических трещин, способных в определенных условиях к росту, являются обязательным показателем современных конструкционных материалов. Поэтому в практике эксплуатации сварных конструкций нередко встречаются случаи их разрущения. Достаточно упомянуть такие случаи в Урта-Булаке (разрушение пылеуловителей из стали 10Г2ФР, на Оренбургском и Астраханском газоперерабатывающих заводах, разрушение продуктопровода ШФЛУ в Башкирии (август 1989 г.), газопровода в Норильске (ноябрь 1989 г.). [c.237]
Достигнутый к настоящему времени уровень развития механики разрушения позволяет эффективно решать задачи, связанные с определением трещиностойкости высокопрочных материалов. Однако, применительно к сталям средней и низкой прочности с Ов = 500-600 Н/мм , являющимся основным конструкционным материалом в газонефтехимическом машиностроении, использовании положений линейной механики разрушения оказывается в ряде случаев необоснованным из-за значительной пластической деформации в этих материалах в области неупругого деформирования вблизи контура трещины. Отмеченное обстоятельство предопределяется типом напряженного состояния, зависящим также от толщины металла. [c.237]
chem21.info
Неблагородные конструкционные металлы и их сплавы
На свойствах сплава, его «поведении» на этапах изготовления протеза и при пользовании последним сказывается качество проведения технологического процесса. Свойства неблагородных конструкционных сплавов в большей степени зависят от вида, процентного содержания элементов, входящих в сплав. Вещества, которые добавляются для исправления тех или иных свойств сплава в нужном направлении, на-
зываются легирующими, а сам сплав — легированным. В первую очередь характеристику того или иного конструкционного материала данной группы определяют следующие материалы: железо, хром, никель, кобальт, молибден, марганец.
Железо. Металл синевато-серебристого цвета. Плотность- 7,86. Температура плавления — 1535°С. Твердость по Брннел- лю — 65 кгс/мм\ Мягкий, пластичный материал. Химически очень активный, может вступать в химические соединения с углеродом. Сплав железа, содержащий от 4,5 до 1,7% углерода, называется чугуном: содержащий от 1.7 до 0,1% — сталью. В виде оксидов железо применяется для изготовления полировочных паст.
Хром. Белый с синеватым опенком металл. Плотность — 7,2. температу ра плавления — 1910″С. Твердость по Бринеллю — 450. Хром обладает твердостью, равной твердости корунда, а последний уступает по твердости лишь азмазу. Хром имеет малую усадку. В полости рта не изменяется. В чистом виде применяется для хромирования инструментов. Входит в состав нержавеющей хромоникелевой стали и кобалыохромо- вых сплавов (КХС). Придает им устойчивость к коррозии и твердость. Например, для того, ч тобы сталь стала нержавеющей, требуется 11-13% хрома. Для полной гарантии его вводят, как правило, 18%. Отрицательные качества хрома, в том числе чрезмерную твердость, исправляют другими меташа- ми. В виде оксидов хром применяется для приготовления полировочных паст.
Никель. Серебристо-белый металл. Плотность — 8,У. Температура плавления — Твердость по Бринеллю — 70.
Имеет очень маленькую усадку. В чистом виде применяют для покрытия инструментов защитной пленкой. Сплав никеля с хромом (нихром) используют для изготовления электронагревательных приборов, применяемых в зуботехнической лаборатории. В состав стали входит в количеелве 8-10%, придавая ей дополнительные антикоррозийные свойства. Смягчает негативные качества хрома.
Кобальт. Белый с красноватым оттенком металл. Плотность — 8,8. Температура плавления — 1490°С. Твердость по Бринеллю — 124. Это твердый и, наряду с этим, ковкий, ibi v- чий металл. В обычных условиях, на воздухе он не окисляе!- ся. При нагревании до 300°С покрывается оксидной пленкой. В растворах кислот медленно растворяется. Входит в сплавы, придавая им высокие механические качества.
Молибден. Светлосерый металл. Плотность — 10,2. Температура плавления — 2620°С (самая высокая из всех металлов, применяемых для зуботехнических целей). Твердость по Бринеллю — 155. На воздухе, в щелочах и некоторых кислотах устойчив против окисления. Растворяется в азотной кислоте и царской водке. Входит в состав КХС и подобных ему сплавов. улучшая их межкристаллитную структуру.
Марганец. Серебристо-белый металл. Плотность 2,3. Температура плавления — 1215°С. При комнатной температуре, на воздухе, не окисляется. При нагревании реагирует с кислородом, углеводом, азотом, серой. Легко растворим в соляной и разбавленной серной кислотах. Введенный в сплав, уменьшает содержание в нем серы, раскисляет сплав и повышает ею износостойкость.
Нержавеющая хромоникелевия снкгчь — это сплав, основными элементами которого являются железо, хром и никель. Для обозначения марки стали применяют цифровые и буквенные обозначения, которые отражают вид и процентное содержание легирующего элемента. Например, сталь марки 1Х18Н9Т содержит 0,1% углерода, 18%-хрома, 9% -никеля с добавлением тигана. Это сплав блестящего цвета. Плотность — около 7,6. Температура плавления — около 1450°С. Из него делают гильзы (заготовки) для штампованных коронок.
Для литых зубов применяют сталь марки ЭИ-95, в которой до 2,5% увеличено содержание кремния, улучшающего жидкотекучесть и жаростойкость сплава.
Нержавеющая сталь хорошо штампуется, паяется, мало истирается. После тщательной полировки приобретает металлический блеск с синеватым отливом. Под влиянием механических воздействий сталь теряет мелкозернистую структуру, образуется «наклеп». Для возвращения стали первоначально заданных свойств, ее подвергают термической обработке при температуре 1050-1100°С. Однако, сталь имеет и существенные недостатки: абсолютно не соответствует цвету
естественных зубов, имеет большgt;ю (3-5%) усадку и высокую температуру плавления.
В настоящее время взамен литейной нержавеющей стали ЭИ-95 выпускается хромированный сплав «Дентан» с уменьшенным содержанием железа и повышенным содержанием никеля. Выпускается в четырех модификациях. Имеет температуру плавления от 1200 до 1380°С.
С целью облегчения работы специалистов выпускают заготовки или полуфабрикаты из нержавеющей стали. Гильзы имеют диаметр от 6 до 18 мм. Размеры меняются через 0,5 мм. Они укладываются в коробки по 100 штук одного размера. Толщина гильз для «постоянных» коронок равняется 0,25 — 0,27 мм.(Для «временных» коронок, применяемых в ортодонтии, гильзы делаются толщиной 0,17 — 0,19 мм. Ортодонтическая проволока поставляется в мотках по 5 м длиной, диаметром 0,6: 0,8; 1,0; 1,2; 1,5 и 2 мм. Кламмерные заготовки (кламмеры) имеют длину 27 мм (для передних) и 32 мм (для боковых зубов), диаметр 1,0 и 1,2 мм. Упаковываются по 250 штук. Металлические блоки для литейных работ весят 30 и 50 граммов.
Кпбшьпюхролювые ставы (КХС). Основу КХС составляет кобальт, хром и никель. С целью улучшения структуры сплава и его свойств добавляются легирующие элементы: молибден, марганец, железо и даже вольфрам. Кобальтохромовые сплавы имеют, в среднем, плотность — 8,3, температуру плавления 1400°С, твердость по Бринеллю 370 кгс/мм\ Усадка КХС колеблется в пределах 1.8 — 2,0%. Сплав прочный, обладает хорошей текучестью, хорошо штампуется, паяется припоем типа припоя Цитрина и припоем для золотых сплавов. Полированная поверхность в обычных условиях не тускнеет. Сплав не коррозируется. КХС легче золотоплатинового сплава в 2,5 раза и тверже хромоникелевой стали примерно в 1,5 раза. Эти качества, дополненные хорошей текучестью в расплавленном состоянии, позволяет создавать легкие ажурные детали. Применяется для изготовления каркасов бюгельных протезов различной сложности, съемных шинирующих конструкций и других протезов и аппаратов.
КХС вып\ скается в ви ie дегятиграммовых заготовок, упакованных в пачки по 15 штук.
Для изготовления стандартных деталей зубных протезов (зубы, каркасы и т.п.) КХС не используют из-за большой твердости и трудностей припасовки. Также, как и нержавеющая хромоникелевая сталь, кобальтохромовый сплав не соответствует цвету естественных зубов. Изделия из КХС трудно полирмотся механическим способом, для придания им зеркального блеска требуется электрополировка.
Учитывая отрицательные качества применяемых в ортопедической стоматологии основных или конструкционнь..\ сплавов, идет постоянный поиск новых материалов. В настоящее время созданы сплавы, имеющие меньшую усадку, повышенную удельную прочность, химическую стойкость к многим агрессивным средам и биологическую инертность в полости рта. К таким материалам относятся сплавы на основе титана ВГ5л и ВТ1-00 (Пермь. Г. И. Рогожников).
С целью придания протезам лучших декоративных свойств предложены материалы внешне имитирующие протезы из золотых сплавов. В качестве зашигно-декоратиыюго покрытия используют, в основном, нитрид-титановые и ти- тан-цирконевые соединения, напыленные в вакууме на протез из стали или КХС. Несмотря на повышенную износостойкость, индифферентность к биологическим средам, эти материалы не решают одну из главных задач зубного протезирования — восстановление эстетической нормы.
Данная задача может быть почти полностью и достаточно успешно решена, если в одной конструкции протеза соединить эстетичную пластмассу или керамику с прочными металлическими сплавами. Соединение, например, фарфоровой массы, восстанавливающей в полном объеме эстетические нормы с металлической основой, заключенной внутри протеза, достигается, главным обоазом, путем спекания их в вакууме во время обжига фарфора.
(‘питы для металлок-рамических и метаиппластмиссо- вых протезов
К материалам, применяемым в качестве основы, предъявляются следующие требования:
а) обладать достаточной прочностью,
б) иметь лорошие литейные качества;
в) иметь температуру плавления выше температуры обжига облицовочной массы:
г) иметь коэффициент термического расширения, равный
или близкий к таковому у керамической массы:
д) хорошо сцепляться с фарфором.
Ь настоящее время возможно применение более 100 различных видов сплавов, относящихся к трём группам: благородные, полублагородные (с низким содержанием золота) и неблагородные.
Из благородных используются золотые, золотоплатиновые, золото-палладиевые и серебряно-палладиевые сплавы. При хорошей коррозийной стойкости, жидкотекуче- сти, они, вместе с тем, непрочны, реформируясь, могут способствовать сколам фарфоровой облицовки. Соединение их с облицовкой не всегда оказывается прочным, надежным. Из неблагородных чаше применяются сплавы на основе кобальта и никеля, с уменьшенным по сравнению с КХС. содержанием кобальта. Введение в сплав молибдена и алюминия улучшает соединение металлической основы с фарфоровой массой. Этому же способствуют и оксиды неблагородных металлов, которые образуются на металлической основе во время обжига. Определённый интерес представляет пре дложенный в последнее время кобальтохромовый сплав «Эст- мет». Полублагородные металлы занимают среднее положение.
Из зарубежных предложений большой интерес представляет ЬЕГО-система (Германия). Составной частью системы являются золотые сплавы «Понтостар Г», «БегоЦер Г», «Бе- гоПал 300» и другие материалы, позволяющие получать вместо основы с темными окислами металлический остов светлого и желтого оттенков, значительно улучшающих эстетический вид облицовки. Несмотря на высокое содержание золота в сплавах, последние способны к нажиганию оксидов.
Австрийская фирма «Комеса», рекламируя систему ЭСПЕ РОКАТЕК предлагает в адгезионной системе соединения металла с облицовочным материалом ЭСПЕ ВИЗИО-ГЕМом без механической ретенции применить силановый агент сцепления ЭСПЕ-СИЛ. благодаря которому образуется химическая связь между поверхностью металла и облицовочным слоем.
www.med24info.com
3.2 Конструкционные металлы и сплавы на основе железа, титана и цветных металлов. Классификация.
КМС на Feпредставлены чугунами и сталями. Масштабы производства стали в значительной степени характеризуют технико-экономический уровень государства. Сталь служит материальной основой практически всех отраслей техники, в том числе и радиоэлектроники.
Сталь получают из смеси чугуна, выплавляемого в домнах, со стальным ломом.
Классификация сталей определяется (по 6 критериям)
типом печей: конверторная, мартеновская, электросталь;
типом футеровки печей: основная сталь, кислая сталь;
характером застывания металла в изложнице: спокойная сталь, полуспокойная сталь, кипящая сталь;
химическим составом: углеродистая, легированная;
назначением: конструкционная, инструментальная;
требованием специального качества: ст. рафинировнного пеоеплава, нержавеющая.
Стали обозначаются (маркируются) буквенно-цифровыми многопозицион-ными кодами (СССР): ____ ___ ___ ___ ___
1 2 3 4 5 6
Позиции 1 и 2 – сотые доли %С для конструкционных ст. или десятые доли %С для инструментальных ст.;
Позиции 3, 5 – буквенные обозначения легирующих элементов;
Позиции 4, 6 — % содержание легирующих элементов слева от цифр.
Примеры: марка 3Х13 – 0,3% С и 13% Сr– инструментальная ст.; марка 2Х17Н2 – 0,2% С, 17%Cr, 2%Ni– инструментальная ст.; марка 12ХН3А – ст. содержит 0,12% С, менее 1,5%Cr, 3%Niи является высококачественной сталью.
Таблица условных обозначений компонентов:
Компонента | УО | Компонента | УО | Компонента | УО |
Алюминий | Ю | Кремний | С | Ниобий | Б |
Бор | Р | Марганец | Г | Титан | Т |
Ванадий | Ф | Медь | Д | Углерод | У* |
Вольфрам | В | Молибден | М | Хром | Х |
Кобальт | К | Никель | Н | Высококач. сталь | А |
Стальные конструкции относительно легкие, прочные, сочетаются с другими материалами без электрокоррозии (cAl), не подвержены коррозии и снижают прочность при нагреве. Наиболее распространены в машиностроении.
3.3. Конструкционные сплавы на основе титана и цветных металлов (Al, Cu).
Титан по виду похож на сталь, но легче стали (плотность 4500 кг/м³), туго-плавкий (1665ºС), мало распространен в природе. Конструкционные материалы на основе титана применяются в авиа- и судостроении, имеют высокую стойкость против коррозии и эррозии в морской воде, склонны к окислению при нагреве в воздухе.Алюминий и конструкционные сплавы из алюминия наиболее широко применяются в электронике, электротехнике и многих других областях промышленности. Алюминий – самый распространенный металл в природе, легкий, легкоплавкий (получают электролизом), ковкий, устойчивый против коррозии благодаря защитной пленке окисла на поверхности.
Алюмель – алюм. сплав с никелем (2%), марганцем (2%) и кремнием (1%) с добавкой циркония и кобальта. Применяется в паре с хромелем для термопар, измеряющих температуру в интервале 20÷1000ºС;
Термит – смесь Al c железной окалиной – интенсивно сгорает при воспла-менении (1300ºС). При горенииtº>2000ºC. Применяется в военном деле (зажи-гательная смесь) и для термичной сварки конструкций большого сечения.
Дюралюмин (Düren- город) – сплавAlиCu(2÷5%),Mg(0,2÷2,7%) иMn(0,2÷1,0%). Подвергается закалке в воде (после нагрева доtº=500º) и упрочняющему старению. Коррозионные свойства невелики, поэтому применяется плакирование чистым алюминием, а в морской воде применяют протекторы (Zn). Хрупок. Используется в судостроении и электронике.
Ряд конструкционных сплавов по массовости применения:
Стали>алюминевые сплавы>титановые сплавы.
Температурные пределы термической обработки цветных сплавов существенно ниже tº плавления основных металлов:
Таблица
Для алюминиевых сплавов tºпл.Al660ºС | Д1, АК8 АК1, АК4, АК5 | 470÷400ºС 490÷380ºС |
Для магниевых сплавов tºпл.Mg650ºС | МА1, МА2 МА5 | 430÷350ºС 370÷300ºС |
Для медных сплавов tºпл. Сu1083ºС | БрАЖ9-4, БрАЖ МЦ10-3-1,5 ЛС59 | 830÷700ºС 750÷600ºС |
Специальные сплавы Сплав Вуда (Wood) (пожарные датчики) | Висмут 50% Свинец 25% Олово 12,5% Кадмий 12,5% | 68ºС |
studfiles.net
легкие конструкционные металлы лаб.раб
Лабораторная работа
ЛЕГКИЕ КОНСТРУКЦИОННЫЕ МЕТАЛЛЫ
Цель работы: Изучение химических свойств некоторых легких конструкционных металлов(Mg,Al) и их соединений.
Легкими металлами и сплавами, в отличие от стали, чугуна и других металлических материалов, принято считать все металлы и сплавы, плотность которых составляет примерно половину плотности железа. К этим металлам условно можно причислить алюминий, магний, титан, бериллий, а также литий, натрий, калий.
Литий, натрий, калий были бы идеальными конструкционными материа-лами, если бы не их чрезвычайно высокая химическая активность с кисло-родом. Бериллий, плотность которого 1,84 г/см3, обладает высокой прочностью и другими важными техническими свойствами. Однако сплавы бериллия весьма дорогостоящие и поэтому находят применение только для специальных целей.
В качестве наиболее применяемых конструкционных материалов во многих отраслях промышленности являются алюминий, магний, титан, а также сплавы на их основе.
Атомные характеристики и некоторые физико-химические
свойства Be, Mg, Al, Ti
Атом элемента |
|
|
|
|
Распределение валентных электронов по подуровням | …2s2 | …3s2 | …3s23p1 | …3d24s2 |
Радиус атома, нм | 0,113 | 0,160 | 0,143 | 0,147 |
Стандартный электродный потенциал, В, | -1,85 | -2,37 | -1,66 | -1,63 |
Степени окисления в соединениях | +2 | +2 | +3 | +2, +3, +4 |
Плотность, г/см3 | 1,85 | 1,74 | 2,70 | 4,51 |
Температура плавления, 0С | 1284 | 651 | 660 | 1677 |
Температура кипения, 0С | 2967 | 1110 | 2494 | 3330 |
Содержание в земной коре, масс. % | 210-4 | 2,09 | 8,13 | 0,44 |
Цвет в компактном состоянии | свинцово-серый | серебристо-белый | серебрис-тый | серебрис-то-белый |
Магний – химически активный металл. В атмофере сухого воздуха он теряет металлический блеск, так как покрывается плотной защитной пленкой оксида. Во влажном воздухе магний быстро покрывается белым слоем, состоящем из оксида MgO и гидроксида Mg(OH)2, защитные свойства пленки ухудшаются. При нагревании до 600 °С магний горит с интенсивным выделением света и тепла: Mg + 1/2O2 = MgO.
Освобожденный от оксидной пленки металлический магний взаимо-
действует с водой при нагревании, при этом в зависимости от соотношения
реагентов образуются различные продукты:
Mg + 2H2O = Mg(OH)2↓ + H2.
Разбавленные минеральные кислоты HCl, H2SO4 и HNO3 растворяют магний с образованием солей. Благодаря химической активности, металлический магний вытесняет многие элементы из растворов
Сплавы на основе магния характеризуются малой плотностью (1,5-
1,8 г/см 3), высокой удельной прочностью, способностью к поглощению энергии удара и вибрационных колебаний. Сплавы магния, являются самым лёгким металлическим конструкционным материалом. Наименьшую плотность имеют магний-литиевые сплавы. Сплавы магния легко обрабатываются резанием, свариваются различными видами сварки, паяются, склеиваются. Основные легирующие элементы магниевых сплавов — Al, Zn, Zr, Mn, РЗЭ (Се, La, Nd, Y) и др. Общее количествово добавок в сплавы составляет 10-14% по массе. Среди магниевых сплавов, обладающих высокой прочностью при комнатной температуре, преобладают сплавы с Аl, Zn, Zr, при повышенной-сплавы с РЗЭ. Необходимые свойства данных сплавов достигаются комплексным легированием, различием методов выплавки и технологии изготовления узлов и деталей. Литейные высокопрочные сплавы предназначены для длительной эксплуатации при
температурах до 150-200 °С.
Магний и его соединения не ядовиты и играют значительную роль в животном и растительном мире. Магний образует порфириновый комплекс, называемый хлорофиллом, отвечающий за фотосинтез в растительных клетках.
Во всех устойчивых соединениях степень окисления магния +2, а кординационное число 6. По химической природе соединения Mg(II) – преимущественно основные. Гироксид магния слабо, а большинство его солей хорошо растворимы в воде. Соли магния гидролизуются при повышенной температуре.
Из соединений магния наибольшее применение нашел оксид магния MgO (жженная магнезия) – высокоплавкое вещество (Тпл.=2800 оС). Мелкокристаллический MgO химически активен, является основным соединением. Он взаимодействует с водой, поглощает СО2, легко растворяется в кислотах. Но сильно прокаленный MgO становится очень твердым, теряет химическую активность. MgO применяют при производстве магния, в качестве наполнителя при производстве резины, для очистки нефтепродуктов, в производстве огнеупоров и строительных материалов.
Гидроксид магния Mg(OН)2 в воде растворяется незначительно, является основанием средней силы.
Кроме оксида широкое применение находит хлорид магния MgCl2 для получения магния и в производстве магнезиального цемента.
Алюминий – самый распространенный элемент в земной коре (после
кислорода и кремния), весьма активен, поэтому в природе в свободном виде не встречается, а находится в виде различных соединений.
Металлический алюминий – легкий металл, он почти в три раза легче
железа, парамагнитный. После серебра и меди металлический алюминий –
лучший проводник тепла и электричества.
Алюминий, не содержащий примесей, устойчив на воздухе, в горячей
и холодной воде. Не растворяется в концентрированных серной и азотной
кислотах на холоде, так как на его поверхности образуется тонкая и очень
прочная оксидная пленка Al2O3. Эта пленка препятствует дальнейшему его
разрушению, поскольку не растворяется в кислотах, тем самым происходит
пассивирование алюминия. Реакция алюминия с разбавленными кислотами
приводит к соответствующим солям и выделению водорода. При взаимодействии алюминия с растворами щелочей происходит образование алюминатов и выделение водорода:
2Al + 6H2O + 2OH– = 3H2 + 2[Al(OH)4]–,
причем нужно иметь в виду, что алюминий выделяет водород из воды, а щелочь нужна лишь для растворения образующегося гидроксида.
Алюминий, введенный в виде стружки или порошка в пламя, ярко го-
рит, выделяя большое количество энергии – тепловой и световой. Поэтому алюминиевый порошок часто применяют вместо магния для фотовспышек. Однако более важным в практическом применении, несомненно, оказывается процесс алюмотермии – восстановление многих, особенно тугоплавких, металлов из их оксидов.
Оксид алюминия Al2O3 проявляет амфотерные свойства, взаимодейст-
вуя с кислотами и щелочами. Температура плавления Al3O3 2042 ºС; кипения 3025 ºС.
Гидроксид алюминия Al(OH)3 образуется в виде белого студенистого осадка в результате обменной реакции между растворами его соли и щелочами. При нагревании гидроксид алюминия теряет молекулы воды и переходит в оксид гидроксид Al(OH)O, а при прокаливании – в оксид. Легко растворяется в кислотах и щелочах. Β последнем случае образуются растворимые гидроксоалюминаты, содержащие ионы [Al(OH)4]– или [Al(OH)6]3–.
Соли алюминия гидролизуются в растворах, вследствие этого некоторые соли слабых кислот (сульфид, карбонат) невозможно получить из водных растворов.
Многие соединения алюминия неустойчивы и при соприкосновении с водой выделяют легко воспламеняющиеся газы. Например: (AlH3)n – полиалюмогидрид, Al4C3 – карбид, Al4Si3 – силицид, LiAlH4 – алюмогидрид лития. Пыль алюмогидрида лития и сплав алюминия с ферросилицидами взрывоопасны. К взрывоопасным относятся и многие органические соединения: трибутилалюминат Al(C4H9)3, триэтилалюминат Al(C2H5)3 и др.
Алюминий – один из наиболее применяемых металлов в современной
технике. Его используют как простое вещество, так и в многочисленных и
разнообразных сплавах и соединениях. В частности, его сплавы с магнием
применяют как конструкционный материал для низкотемпературных ядер-
ных реакторов. Алюминий, будучи хорошим проводником электричества,
применяется для изготовления электрических кабелей, в различных электро-
технических приборах.
Путем прессования спеченного алюминиевого порошка (САП) начали получать материалы, отличающиеся высокой жаропрочностью. САП применяют при изготовлении оболочек для урановых стержней, используемых в ядерных реакторах.
Алюминиевые сплавы подразделяются на деформируемые и литейные. Деформируемые отличаются высокой пластичностью и механической прочностью, но коррозионная стойкость их сравнительно невелика (дюралюмин). Литейные сплавы содержат легирующих добавок больше предельной растворимости. Из них готовят различные фасонные отливки. Алюминиевые сплавы применяют в самолетостроении, судостроении, ракетостроении, промышленном и гражданском строительстве, химической промышленности.
Алюминий не токсичен для человека и животных и находит широкое
применение в пищевой и фармацевтической промышленности для упаковки
продуктов и препаратов. Но пыль алюминия и его оксида поражают главным образом легкие и слизистые оболочки носа, рта и глаз. Накопление алюминия в костях при недостатке кальция приводит к их разрушению, а так же к развитию заболеваний ЦНС.
Экспериментальная часть
Опыт 1. Взаимодействие магния с водой.
Положите в две пробирки с 5-6 каплями воды по хорошо зачищенному кусочку магния или один микрошпатель порошка магния. Что наблюдаете? Нагрейте одну пробирку. Прибавьте к раствору 1-2 капли фенолфталеина. Как изменилась окраска раствора? Какие ионы получены при взаимодействии воды с магнием? Какой газ при этом выделяется? В другую пробирку добавьте 6 капель насыщенного раствора хлорида аммония Nh5Cl. Объясните активное растворение магния в этой пробирке. Напишите уравнение реакции.
Опыт 2. Действие кислот на металлический магний
В три пробирки положите по кусочку металлического магния, добавьте по 10 капель разбавленных растворов кислот: в первую – соляной, во вторую – серной, в третью – азотной. Какие газы выделяются при взаимодействии магния с этими кислотами? Напишите уравнения реакций
Опыт 3. Изучение свойств гидроксида магния
В три пробирки внесите по 5 капель раствора хлорида магния. В первую и вторую пробирки добавьте такой же объем гидроксида натрия, а в третью – гидроксида аммония. Наблюдайте образование осадка. В первую пробирку внесите несколько капель раствора HCl, во вторую – избыток NaOH, в третью – раствор хлорида аммония. В каких пробирках растворился осадок? Чем это можно объяснить? Каков химический характер Mg(OH)2?
Примечание: раствор гидроксида аммония не осаждает ионов магния из водных растворов, содержащих соли аммония, так как в этих растворах образуется аммиачный буфер (NH4OH + NH4Cl), pH которого равен 9,2, то есть в растворе создается такая концентрация ионов водорода, при которой Mg(OH)2 не выпадает в осадок.
Опыт 3. Действие кислот на металлический алюминий
Испытайте действие 2 н растворов соляной, серной и азотной кисло на алюминий. Во всех ли случаях протекает реакция на холоду? Осторожно нагрейте пробирки. Что наблюдаете? Напишите уравнения реакций.
Аналогично проделайте опыт с концентрированными кислотами. С какими из них реакция на холоду не протекает? Почему? Напишите уравнения реакций. Укажите условия их протекания.
Опыт 4. Взаимодействие алюминия с раствором щелочи
В пробирку поместите один кусочек предварительно зачищенного алюминия, прибавьте 5-6 капель концентрированного раствора NaOH. Отметьте интенсивное выделение водорода. Запишите уравнения реакций. Составьте электронные схемы. Укажите окислитель и восстановитель, процессы окисления и восстановления.
Опыт 5. Восстановительные свойства алюминия
В пробирку налейте 10 капель раствора серной кислоты, каплю раствора перманганата калия и положите небольшой кусочек алюминия. Через некоторое время наблюдайте изменение окраски раствора при нагревании. Напишите уравнение реакции и подберите коэффициенты в уравнении с помощью метода электронного баланса.
Опыт 6.Получение гидроксида алюминия и изучение его свойств
Получите гидроксид алюминия и исследуйте его отношение к кислоте, щелочи и NH4OH. Напишите уравнения реакций и сделайте вывод о химических свойствах гидроксида алюминия.
Сделайте вывод о химической активности магния и алюминия, о характере их гидроксидов.
Контрольные вопросы
1. К раствору, содержащему соли бериллия и магния, добавили избыток гидроксида натрия. Напишите молекулярные и ионные уравнения всех
реакций, которые при этом произошли. Какое вещество выпало в осадок? Ка-
кие ионы находятся в растворе?
2. Почему горящий магний нельзя тушить водой? Напишите соответствующие уравнения.
3. Напишите уравнения реакций взаимодействия Mg и Al с разбавленным, концентрированными кислотами h3SO4, HNO3 и c водным раствором NaOH.
4. Как практически убедиться в амфотерных свойствах гидроксида алюминия? Напишите уравнения соответствующих реакций.
5. Какая реакция будет протекать в водном растворе, содержащем одновременно ионы Al3+ и ионы S2–? Напишите уравнение реакции
6
studfiles.net
§ 2.2 Конструкционные металлы и сплавы на основе железа.
КМС на Fe представлены чугунами и сталями. Масштабы производства стали в значительной степени характеризуют технико-экономический уровень государства. Сталь служит материальной основой практически всех отраслей техники, в том числе и радиоэлектроники.
Сталь получают из смеси чугуна, выплавляемого в домнах, со стальным ломом.
Классификация сталей определяется (по 6 критериям)
типом печей: конверторная, мартеновская, электросталь;
типом футеровки печей: основная сталь, кислая сталь;
характером застывания металла в изложнице: спокойная сталь, полуспокойная сталь, кипящая сталь;
химическим составом: углеродистая, легированная;
назначением: конструкционная, инструментальная;
требованием специального качества: ст. рафинировнного пеоеплава, нержавеющая.
Стали обозначаются (маркируются) буквенно-цифровыми многопозицион-ными кодами (СССР): ____ ___ ___ ___ ___
1 2 3 4 5 6
Позиции 1 и 2 – сотые доли %С для конструкционных ст. или десятые доли %С для инструментальных ст.;
Позиции 3, 5 – буквенные обозначения легирующих элементов;
Позиции 4, 6 — % содержание легирующих элементов слева от цифр.
Примеры: марка 3Х13 – 0,3% С и 13% Сr – инструментальная ст.; марка 2Х17Н2 – 0,2% С, 17% Cr, 2% Ni – инструментальная ст.; марка 12ХН3А – ст. содержит 0,12% С, менее 1,5% Cr, 3% Ni и является высококачественной сталью.
Таблица условных обозначений компонентов:
Компонента
УО
Компонента
УО
Компонента
УО
Алюминий
Ю
Кремний
С
Ниобий
Б
Бор
Р
Марганец
Г
Титан
Т
Ванадий
Ф
Медь
Д
Углерод
У*
Вольфрам
В
Молибден
М
Хром
Х
Кобальт
К
Никель
Н
Высококач. сталь
А
Стальные конструкции относительно легкие, прочные, сочетаются с другими материалами без электрокоррозии (c Al), не подвержены коррозии и снижают прочность при нагреве. Наиболее распространены в машиностроении.
§2.3 Конструкционные сплавы на основе титана и цветных металлов (Al, Cu).
Титан по виду похож на сталь, но легче стали (плотность 4500 кг/м³), туго-плавкий (1665ºС), мало распространен в природе. Конструкционные материалы на основе титана применяются в авиа- и судостроении, имеют высокую стойкость против коррозии и эррозии в морской воде, склонны к окислению при нагреве в воздухе.
Алюминий и конструкционные сплавы из алюминия наиболее широко применяются в электронике, электротехнике и многих других областях промышленности. Алюминий – самый распространенный металл в природе, легкий, легкоплавкий (получают электролизом), ковкий, устойчивый против коррозии благодаря защитной пленке окисла на поверхности.
Алюмель – алюм. сплав с никелем (2%), марганцем (2%) и кремнием (1%) с добавкой циркония и кобальта. Применяется в паре с хромелем для термопар, измеряющих температуру в интервале 20÷1000ºС;
Термит – смесь Al c железной окалиной – интенсивно сгорает при воспла-менении (1300ºС). При горении tº>2000ºC. Применяется в военном деле (зажи-гательная смесь) и для термичной сварки конструкций большого сечения.
Дюралюмин (Düren — город) – сплав Al и Cu (2÷5%), Mg (0,2÷2,7%) и Mn (0,2÷1,0%). Подвергается закалке в воде (после нагрева до tº=500º) и упрочняющему старению. Коррозионные свойства невелики, поэтому применяется плакирование чистым алюминием, а в морской воде применяют протекторы (Zn). Хрупок. Используется в судостроении и электронике.
Ряд конструкционных сплавов по массовости применения:
Стали>алюминевые сплавы>титановые сплавы.
Температурные пределы термической обработки цветных сплавов существенно ниже tº плавления основных металлов:
Для алюминиевых сплавов tºпл. Al 660ºС
Д1, АК8
АК1, АК4, АК5
470÷400ºС
490÷380ºС
Для магниевых сплавов tºпл. Mg 650ºС
МА1, МА2
МА5
430÷350ºС
370÷300ºС
Для медных сплавов tºпл. Сu 1083ºС
БрАЖ9-4, БрАЖ МЦ10-3-1,5
ЛС59
830÷700ºС
750÷600ºС
Специальные сплавы
Сплав Вуда (Wood) (пожарные датчики)
Висмут 50%
Свинец 25%
Олово 12,5%
Кадмий 12,5%
68ºС
studfiles.net






