Таблица Температуры плавления металлов
Температура плавления вещества — это температура перехода тела в жидкое состояние.
Таблица температуры плавления металлов представлена ниже:
| Ртуть | -38,9 |
| Цезий | 28,4 |
| Легкоплавкий сплав | 60,5 |
| Калий | 63,6 |
| Натрий | 97,8 |
| Олово | 231,9 |
| Свинец | 327,4 |
| Цинк | 419,5 |
| Магний | 650 |
| Дуралюмин | ~650 |
| Алюминий | 660,4 |
| Германий | 937 |
| Серебро | 961,9 |
| Латунь | ~1000 |
| Золото | 1064 |
| Медь | 1084,5 |
| Нейзильбер | ~1100 |
| Чугун | 1100-1300 |
| Константин | |
| Сталь | 1300-1500 |
| Нихром | ~1400 |
| Кремний | 1415 |
| Инвар | 1425 |
| Никель | 1455 |
| Фехраль | ~1460 |
| Железо | 1539 |
| Иридий | 2447 |
| Осмий | 3030 |
| Титан | 3150 |
| Вольфрам | 3420 |
| Цирконий | 3530 |
| Ниобий | 3760 |
| Карбиды гафния | 3890 |
| Платина | 17772 |
Из всех металлов, представленных на таблице, стоит отметить Ртуть, которая в обычных ословиях является жидкостью.
Еще интересный металл — Вольфрам, из которого изготавливают нити накала в лампах. Температура вольфрамовой нити в лампах накаливания достигает 2000 градусов, что значительно ниже температуры плавления Вольфрама.
Еще интересный металл, который используют при пайке — олово. Температура его плавления чуть больше 230 градусов. Температура паяльника в рабочем режиме обычно составляет от 250-400 градусов.
energy.clcnet.ru
Таблица температуры плавления (tпл) металлов и сплавов при нормальном атмосферном давлении
| Металл или сплав | tпл. С |
|---|---|
| Алюминий | 660,4 |
| Вольфрам | 3420 |
| Германий | 937 |
| Дуралюмин | ~650 |
| Железо | 1539 |
| Золото | 1064?4 |
| Инвар | 1425 |
| Иридий | 2447 |
| Калий | 63,6 |
| Карбиды гафния | 3890 |
| ниобия | 3760 |
| титана | 3150 |
| циркония | 3530 |
| Константин | ~1260 |
| Кремний | 1415 |
| Латунь | ~1000 |
| Легкоплавкий сплав | 60,5 |
| Магний | 650 |
| Медь | 1084,5 |
| Натрий | 97,8 |
| Нейзильбер | ~1100 |
| Никель | 1455 |
| Нихром | ~1400 |
| Олово | 231,9 |
| Осмий | 3030 |
| Платина | 17772 |
| Ртуть | — 38,9 |
| Свинец | 327,4 |
| Серебро | 961,9 |
| Сталь | 1300-1500 |
| Фехраль | ~1460 |
| Цезий | 28,4 |
| Цинк | 419,5 |
| Чугун | 1100-1300 |
Вернуться в раздел аналитики
Запись опубликована автором admin в рубрике Полезные материалы. Добавьте в закладки постоянную ссылку.zaozmi.ru
Мир современных материалов — Самый тугоплавкий материал
Используя мощные компьютерные модели, исследователи из Университета Брауна определили материал с температурой плавления выше, чем у любого из известных веществ. Расчеты показывают, что материал, изготовленный из гафния, азота и углерода будет иметь температуру плавления более чем 4400 К. Это примерно две трети от температуры на поверхности Солнца и на 200 К выше, чем самая высокая точка плавления из когда-либо зарегистрированных в ходе эксперимента.
Раньше было экспериментально подтверждено, что рекордной температурой плавления обладает вещество из элементов гафния, тантала, и углерода (HF-Та-C).Расчеты, представленные в журнале Physical Review B, показали, что материал, изготовленный с определенным составом из гафния, азота и углерода (HF-N-C) будет иметь температуру плавления более 4400 К, что на 200 К выше, чем экспериментальный результат. Проведенные расчеты показывают, что оптимальный состав материала из гафния, азота и углерода — HfN0.38C0.51. Следующим шагом исследователей станет синтез материала для подтверждения выводов лаборатории.
«Преимуществом вычислительного подхода является то, что можно с небольшими затратами посмотреть много различных комбинаций и найти те, которые стоят эксперимента в лаборатории,» — сказал Аксель ван де Валле, соавтор исследования.
Исследователи использовали вычислительный метод, при котором температура плавления рассчитывается путем моделирования физических процессов на атомном уровне, следуя закону квантовой механики. Динамика плавления изучается на наноуровне, в блоках около 100 атомов. Исследователи начали с анализа материала HF-Та-C, для которого точка плавления уже определена экспериментально. Моделирование смогло прояснить некоторые из факторов, которые вносят вклад в способность материала выдерживать тепло.
Работа показала, что в HF-Та-С сочетается высокая теплота плавления (энергия выделяется или поглощается, когда он переходит из твердого состояния в жидкое) с небольшой разницей между энтропией твердой и жидкой фаз.
Затем исследователи использовали эти выводы для поиска соединений, которые могут максимально соответствовать таким требованиям. Они обнаружили, что соединение гафния, азота и углерода будет иметь аналогичную высокую температуру плавления, но меньшую разницу между энтропией твердого вещества и жидкости. Когда они рассчитали точку плавления, она получилась на 200 К выше, чем получена в эксперименте для HF-Та-C.
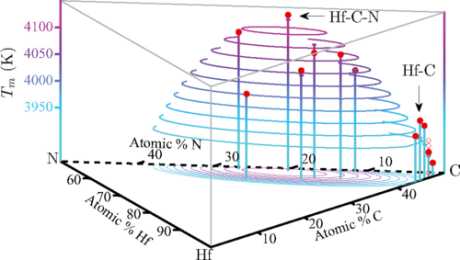
Температуры плавления Та-HF-C-N сплавов. Закрашенные кружки обозначают рассчитанные температуры плавления в системах HF-C и Hf-C-N, а незакрашенные кружки показывают данные для системы Та-HF-C для сравнения.
Работа в конечном итоге может указать на новые высококачественные материалы для различных применений, от покрытий для газовых турбин до деталей высокоскоростных самолетов. Станет или нет этим новым материалом HfN0.38C0.51 пока не ясно, говорят исследователи.
Источник: Prediction of the material with highest known melting point from ab initio molecular dynamics calculations.Qi-Jun Hong and Axel van de Walle // Phys. Rev. B 92, 020104(R) – Published 20 July 2015. http://dx.doi.org/10.1103/PhysRevB.92.020104.
Вас также может заинтересовать:
worldofmaterials.ru
Плотность, температура плавления и кипения простых веществ: таблицы для элементов
В таблице приводятся основные физические свойства простых веществ: плотность при температуре 20°С (в случае, если плотность измерена при другой температуре, последняя указана в скобках), температура плавления и температура кипения веществ в градусах Цельсия.
Указаны плотность и температуры плавления и кипения следующих простых веществ: азот N2, актиний Ac, алюминий Al, америций Am, аргон Ar, астат At, барий Ba, бериллий Be, бор B, бром Br, ванадий V, висмут Bi, водород H2, вольфрам W, гадолиний Gd, галлий Ga, гафний Hf, гелий He, германий Ge, гольмий Ho, диспрозий Dy, европий Eu, железо Fe, золото Au, индий In, йод (иод) J, иридий Ir, иттербий Yb, иттрий Y, кадмий Cd, калий K, кальций Ca, кислород O
Следует отметить, что плотность веществ в таблице выражена в размерности кг/м 3. В таблице можно выделить вещества (химические элементы) с минимальной и максимальной плотностью. Наименьшей плотностью из химических элементов обладают газы — например, плотность водорода равна всего 0,08987 кг/м3 — это самый легкий газ на планете. Из тяжелых элементов высокой плотностью отличаются вольфрам, уран, нептуний, осмий и другие металлы.
Цифры в скобках означают, что вещество при данной температуре разлагается. Сокращения: г. — газ, ж. — жидкость, тв. — твердое вещество, возг. — возгоняется, ромб. — ромбическая структура.
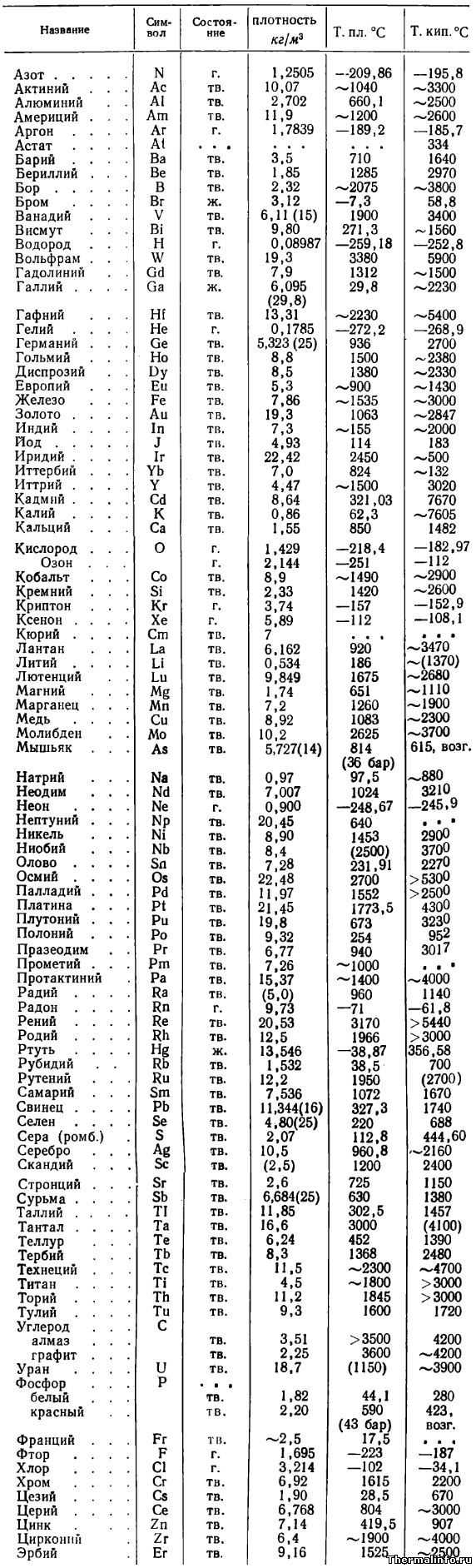
По данным таблицы можно выделить вещества, обладающие минимальной и максимальной температурой плавления и кипения. Самую низкую температуру плавления имеет химический элемент гелий — его температура плавления равна минус 272,2 °С. Гелий также обладает и самой низкой температурой кипения.
Самую высокую температуру плавления среди простых веществ имеет такой химический элемент, как углерод в виде графита. Он начинает плавиться при температуре 3600°С. Другая модификация углерода — алмаз также относится к тугоплавким веществам с температурой плавления 3500°С.
Самую высокую температуру кипения имеет элемент кадмий, он кипит при температуре не ниже 7670°С, хотя начинает плавиться всего лишь при 321°С.
Атомная масса и плотность простых веществ
В таблице приведена атомная масса и плотность следующих химических элементов: азот ,актиний, алюминий, америций, аргон, астат, барий, бериллий, берклий, бор, бром, ванадий, висмут, водород, вольфрам, гадолиний, галлий, гафний, гелий, германий, гольмий, диспрозий, европий, железо, золото, индий, йод, иридий, иттербий, иттрий, кадмий, калий, калифорний, кальций, кислород, кобальт, кремний, криптон, ксенон, кюрий, лантан, литий, лютеций, магний, марганец, медь, менделевий, молибден, мышьяк, натрий, неодим, неон, нептуний, никель, ниобий, олово, осмий, палладий, платина, плутоний, полоний, празеодим, прометий, протактиний, радий, радон, рений, родий, ртуть, рубидий, рутений, самарий, свинец, селен, сера, серебро, скандий, стронций, сурьма, таллий, тантал, теллур, тербий, технеций, титан, торий, тулий, углерод (графит, алмаз), уран, фермий, фосфор, франций, фтор, хлор, хром, цезий, церий, цинк, цирконий, эйнштейний, эрбий.
Указанные значения плотности соответствуют плотности веществ при температуре 20°С и атмосферном давлении, за исключением тех случаев, когда в скобках указана другая температура.
Плотность элементов дана в размерности тонна на кубометр. Например, плотность жидкого азота при температуре -195,8°С равна 0,808 т/м3 или 808 кг/м3; плотность хлора в газообразном состоянии равна 3,214 кг/м3, жидкого — 1557 кг/м3. Значения плотности веществ приведены для их естественного молекулярного и агрегатного состояний при указанной температуре.
 Источники:
Источники:
1. Писаренко В.В. Справочник лаборанта-химика. Справ. пособие для проф.-техн. учебн. заведений. М., «Высшая школа», 1970. — 192 стр. с илл.
2. Физические величины. Справочник. А.П. Бабичев, Н.А. Бабушкина, А.М. Братковский и др.; Под ред. И.С. Григорьева, Е.З. Мейлихова. — М.: Энергоатомиздат, 1991. — 1232 с.
thermalinfo.ru
Рекорды ХИМИИ — Мастерок.жж.рф

Самым сильным стабильным окислителем, является комплекс дифторида криптона и пентафторида сурьмы. Из-за сильного окисляющего действия (окисляет все элементы в высшие степени окисления, в том числе кислород и азот воздуха) для него очень трудно измерить электродный потенциал. Единственный растворитель, который реагирует с ним достаточно медленно — безводный фтористый водород.
Самым плотным веществом, является осмий. Его плотность составляет 22,5 г/см3.
Самый легкий металл — это литий. Его плотность составляет 0,543 г/см3.
Самый дорогой металл — это калифорний. Его стоимость в настоящее время составляет 6 500 000 долларов за 1 грамм.
Самый распространенный элемент в земной коре — это кислород. Его содержание составляет 49% от массы земной коры.
Самый редкий элемент в земной коре — это астат. Его содержание во всей земной коре, по оценкам специалистов составляет всего 0,16 грамм.
Самым горючим веществом, является по-видимому мелкий порошок циркония. Для того чтоб он не мог гореть, необходимо поместить его в атмосферу инертного газа на пластину из материала не содержащего неметаллов.
Веществом с наименьшей температурой кипения, является гелий. Его температура кипения равна -269 градусов по Цельсию. Гелий — единственное вещество не имеющее температуры плавления при обычном
давлении. Даже при абсолютном нуле он остается жидким. Жидкий гелий широко используется в криогенной технике.
Самый тугоплавкий металл — это вольфрам. Его температура плавления составляет +3420 градусов по Цельсию. Из него изготавляют нити накаливания для электрических лампочек.
Самый тугоплавкий материал — это сплав карбидов гафния и тантала (1:1). Он имеет температуру плавления +4215 С.
Самым легкоплавким металлом,является ртуть. Ее температура плавления равна -38,87 градусов по Цельсию. Она же является самой тяжелой жидкостью, ее плотность составляет 13,54 г/см3.
Самую высокую растворимость в воде среди твердых веществ имеет моногидрат иодата уранила. Растворимость его бета-формы при +18°С составляет 12140 грамм на литр.
Самым легким газом, является водород. Масса 1 литра составляет всего 0,08988 грамм.
Самым тяжелым газом при комнатной температуре, является гексафторид вольфрама (т. кип. +17 С). Его масса составляет 12,9 г/л, т.е. в нем могут плавать некоторые виды пенопласта.
Самым стойким к кислотам металлом, является иридий. До сих пор не известно ни одной кислоты или их смеси, в которых он бы растворялся.
Самый широкий диапазон концентрационных пределов взрываемости имеет сероуглерод. Взрыватся могут все смеси паров сероуглерода с воздухом содержащие от 1 до 50 объемных процентов сероуглерода.
Самой сильной стабильной кислотой является раствор пентафторида сурьмы во фтористом водороде. В зависимости от концентрации пентафторида сурьмы эта кислота может иметь показатель Гаммета до -40.
Самым необычным анионом в соли является электрон. Он входит в состав электрида 18-краун-6 комплекса натрия.
Веществом с наименьшей плотностью являются кремниевые аэрогели, в которых сферы связанных атомов кремния и кислорода образуют разделённые воздушными прослойками длинные пряди. В феврале 1990 г. в
Национальной лаборатории им. Лоуренса, Ливермор, штат Калифорния, США, был получен самый легкий из таких аэрогелей с плотностью всего 0,005 г/см3. Это вещество использовалось в космических исследованиях при сборе микрометеоритов, присутствующих в хвостах комет.
Вещество с самой высокой температурой сверхпроводимости. В марте 1988 г. в Исследовательском центре компании ИБМ в Сан-Хосе, штат Калифорния, США, при температуре –148°С было получено явление сверхпроводимости. Проводником служила смесь оксидов таллия, кальция, бария и меди – Тl2Са2Ва2Сu3Оx.
Самым горьким веществом, является денатония сахаринат. Его получили случайно, во время исследования денатония бензоата. Сочетание последнего с натриевой солью сахарина дало вещество в 5 раз более горькое, чем предыдущий рекордсмен (денатония бензоат). В настоящее время оба этих вещества используются для денатурации спирта и других непищевых продуктов.
Самым сильным ядом, является ботулинический токсин типа А. Его летальная доза для мышей (ЛД50, внутрибрюшинно) составляет 0,000026 мкг/кг веса. Это белок с молекулярной массой 150 000, продуцируемый бактерией Clostridium botulinum.
Самым нетоксичным органическим веществом, является метан. При увеличении его концентрации интоксикация возникает из-за недостатка кислорода, а не в результате отравления.
Самый сильный адсорбент, был получен в 1974 году из производного крахмала, акриламида и акриловой кислоты. Это вещество способно удерживать воду, масса которой в 1300 раз превосходит его собственную.
Самыми зловонными соединениями, являются этилселенол и бутилмеркаптан – их запах напоминает комбинацию запахов гниющей капусты, чеснока, лука и нечистот одновременно. По оценкам минимальная концентрация которая еще чувствуется человеком составляет 2 нанограмма на кубометр воздуха.
Веществом, обнаруживаемым по запаху в наименьшей концентрации, является один из изомеров винного лактона, который, как показал в 1996 году швейцарский химик Х.Гут, придает красным и белым винам сладковатый «кокосовый» аромат. Поразительна чувствительность носа к этому веществу: его можно почувствовать при концентрации 0,01 пикограмма (или одна стотриллионная грамма) в 1 л воздуха.
Предыдущим рекордсменом был ванилин, который чувствуется при концентрации в воздухе 20 пг/л.
Самым сильным галлюциногенным веществом, является диэтиламид l-лизергиновой кислоты. Доза всего в 100 микрограмм вызывает галлюцинации продолжающиеся около суток.
Самым сладким веществом, является N-(N-циклонониламино(4-цианофенилимино)м
токсичности, применения в качестве подсластителя, по видимому не найдет. Из промышленных веществ самым сладким является талин (комплекс тауматина и солей алюминия), который в 3 500 — 6 000 раз слаще сахарозы.
Самым медленным ферментом, является нитрогеназа, катализирующая усвоение клубеньковыми бактериями атмосферного азота. Полный цикл превращения одной молекулы азота в 2 иона аммония занимает полторы секунды.
Самым сильным наркотическим анальгетиком является, по видимому вещество, синтезированное в Канаде в 80-х годах. Его эффективная анальгетическая доза для мышей (подкожное введение) составляет всего 3,7 нанограмма на килограмм веса, то есть он в 500 раз сильнее эторфина.
Органическим веществом с самым большим содержанием азота является бис(диазотетразолил)гидразин. Он содержит 87,5% азота. Это взрывчатое вещество черезвычайно чувствительно к удару, трению и теплу.
Веществом с самой большой молекулярной массой является гемоцианин улитки (переносит кислород). Его молекулярная масса составляет 918 000 000 дальтон, что больше молекулярной массы даже ДНК.
Самое длинное химическое название опубликованное в Chemical Abstracts насчитывает 1578 знаков в английском написании и является модифицированной нуклеотидной последовательностью. Это вещество называется:
Adenosene. N-[4-(dimethylethyl)benzoyl]-2′-O-(tetra
Самым длинным химическим названием обладает ДНК выделенное из митохондрии человека и состоящая из 16569 пар нуклеотидов. Полное название этого соединения, расчитанное теоретически, должно содержать около 207 000 знаков.
Самый долгоживущий гальванический элемент — серно-цинковая батарея, изготовленная в Лондоне в 1840 г. Подключенный к ней звонок работает и по сей день в Кларендонской лаборатории в Оксфорде (Англия)
Самый распространенный элемент в литосфере — кислород (46,60% по массе)
Самый распространенный элемент в атмосфере — азот (78,09%)
Самый распространенный элемент вне Земли — водород (90%)
Самое тяжелое из газообразных веществ — радон (10,05 г/л при 0 оС), а самое легкое — водород (0,08929 г/л)
Самый дорогой — калифорний (10$ за 0,001 мг)
Самый долгоживущий из изотопов — 128Te (период полураспада 1,5 . 1024 лет)
Самый долгоживущий изотоп среди альфа-активных — 148Sm (8 . 1015 лет )
Самый долгоживущий изотоп среди бета-активных — 113Cd (9 . 1015 лет)
Самый нестабильный изотоп — 5Li (4,4 . 10—22 сек)
Самое большое число изотопов у Xe и Cs (по 36)
Самый ковкий металл — золото (из 1 г можно вытянуть проволоку длиной 2,4 км)
Самый тугоплавкий — вольфрам (т. пл. 3420 оС)
Самые необычные теплофизические свойства у — плутония (в интервале температур от 320 до 540 оС этот металл, в отличие от всех других, сжимается, причем наиболее сильно в интервале температур 500-540 оС)
Самый большой положительный коэффициент температурного расширения у цезия (97 . 10—6 К—1)
Самые зловонные соединения — этилмеркаптан С2Н9SH и бутилселеномеркаптан С4Н9SeH. Их запах напоминает комбинацию запахов гниющей капусты, чеснока, лука и нечистот одновременно
Самый сильный нервный яд — газ VX (о-этиловый эфир S-2-(диизопропиламиноэтил)метилфосфоноти
Самое ядовитое из всех синтезированных соединений — TCDD (2,3,7,8-тетрахлордибензо-n-диоксин), оно в 150000 раз токсичнее цианида калия
Самое сильное биологически активное соединение — диэтиламид d-лизергиновой кислоты (LSD) и тартрат диэтиламида d-лизергиновой кислоты (LSD—25)
Самый сильный анальгетик — вещество R33799 , по своему действию напоминает морфин, но в 12000 раз превосходит его
Самое дорогое вещество — интерферон (10-6 мкг стоит 10 $)
Самая низкая температура, прикоторой идет химическая реакция, равна -269 оС — это реакция полимеризации формальдегида под джействием ионизирующего излучения
Еще всякую кучу полезной мелочи МОЖНО ПОЧИТАТЬ в прошлых постах Оригинал статьи находится на сайте ИнфоГлаз.рф Ссылка на статью, с которой сделана эта копия — http://infoglaz.ru/?p=13833
masterok.livejournal.com
У какого металла самая высокая температура плавления?
На сколько я знаю — вольфрам. Сейчас уточним.. . Да. Не ошибся. <a rel=»nofollow» href=»http://all-met.narod.ru/fiz.html» target=»_blank»>http://all-met.narod.ru/fiz.html</a> <a rel=»nofollow» href=»http://ru.wikipedia.org/wiki/Металл» target=»_blank»>http://ru.wikipedia.org/wiki/Металл</a> <a rel=»nofollow» href=»http://www.periodictable.ru/074W/W.html» target=»_blank»>http://www.periodictable.ru/074W/W.html</a>
вольфрам кажись
Да, наверное, в лампочках вольфрам
Только на воздухе он сгорит к ядрене фене, гораздо раньше.
А чё в таблице написано платина 17772 С ?
вольфрам, рений, осмий, тантал. К единому мнению который самый тугоплавкий не придут. Из полуметаллов — углерод, по квантомеханическим расчетам более 8000 град, но начинает испаряться при 4000 град.
touch.otvet.mail.ru
ФИЗИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ ТЕМПЕРАТУРА ПЛАВЛЕНИЯ
СВОЙСТВА МЕТАЛЛОВ
Астицы любого тела — атомы или молекулы — находятся в постоянном беспорядочном движении. В твёрдых телах это движение практически ограничивается к о — лебанием атомов вокруг определённого положения равновесия. Чем выше температура тела, тем оживлённее ато движение. При определённой температуре твёрдое тело плавится, переходит в жидкость.
Аморфные тела — воск, смола, янтарь, стекло — при нагревании постепенно размягчаются, а затем становятся жидкими. Переход воска из твёрдого состояния в жидкое совершается плавно, и мы не можем сказать точно, какова температура плавления воска.
Иное дело — кристаллические вещества. При нагревании ионы, закреплённые в узлах кристаллической решётки, колеблются всё энергичнее, но, пока решётка сохраняется, кристалл остаётся твёрдым. Только когда колебания ионов усиливаются настолько, что решётка разрушается, появляются первые следы жидкости. Вот почему все кристаллические вещества, в том числе и металлы, имеют совершенно определённую температуру плавления.
Среди металлов встречаются такие, для расплавления которых строят специальные высокотемпературные электрические печи; есть такие, которые плавятся от теплоты руки, а есть и такие, которые плавятся при температуре ниже нуля.
Наиболее легкоплавкие металлы — ртуть и цезий, а самые тугоплавкие — рений и вольфрам. Ниже мы приводим таблицу температур плавления различных металлов:
Металл | Температура плавления в градусах Цельсия | Д’еталл | Температура плавления в градусах Цельсия |
Ртуть………………… | — 38,9 | Алюминий…. | 658 |
Цезий………………… | 28,5 | Серебро……………. | 960 |
Рубидий……………. | 39,0 | Золото…… | 1063 |
Натрий……………… | 97,9 | Медь…………………. | 1083 |
Литий………………… | 173 | Кобальт……………. | 1490 |
Олово……………….. | 231,8 | Железо………………. | 1532 |
Свинец……………… | 327 | Молибден…. | 2600 |
Цинк…………………. | 419 | Рений…… | 3000 |
Сурьма…………….. | 632 | Вольфрам…. | 3400 |
ТЕПЛОПРОВОДНОСТЬ
Передача теплоты от одного тела к другому — это переход энергии беспорядочного движения от одних молекул к другим.
Вода, стекло, воздух, дерево, кирпич передают тепло медленно, теплопроводность их низка. Металлы же проводят тепло очень быстро. Чем это объяснить?
Мы уже знаем, что в пространственной решётке металлических кристаллов находятся положительно заряженные атомы металлов — ионы. Они более или менее прочно удерживаются на своих местах. Вокруг ионов беспорядочно движутся свободные электроны. Их можно представить в виде «электронного газа», омывающего кристаллическую решётку. Свободные электроны легко перемещаются внутри решётки и служат хорошими переносчиками теп — ловой энергии от нагретых слоёв металла к холодным.
Высокую теплопроводность металла всегда легко обнаружить. Прикоснитесь в холодную погоду рукой к стене деревянного дома и к железной ограде: железо на ощупь всегда гораздо холоднее, чем дерево, так как железо быстро отводит тепло от руки, а дерево — в сотни раз медленнее. Лучше всех других металлов проводят тепло серебро и золото, затем идут медь, алюминий, вольфрам, магний, цинк и другие. Самые плохие металлические проводники тепла — свинец и ртуть.
Теплопроводность измеряют количеством тепла, которое проходит по металлическому стержню сечением в
1 квадратный сантиметр за 1 минуту. Если теплопроводность серебра условно принять за 100, то теплопроводность меди будет 90, алюминия 27, железа 15, свинца 12, ртути 2, а теплопроводность дерева всего 0,05.
Чем больше теплопроводность металла, тем быстрее и равномернее он нагревается.
Благодаря своей высокой теплопроводности металлы широко используются в тех случаях, когда необходимо быстрое нагревание или охлаждение. Паровые котлы, аппараты, в которых протекают различные химические процессы при высоких температурах, батареи центрального отопления, радиаторы автомобилей — всё это делается из металлов. Аппараты, которые должны отдавать или поглощать много тепла, чаще всего изготовляются из хороших проводников тепла — меди, алюминия.
Эта листовая продукция надежно устраняет скольжение на поверхности материала. На гладкую сторону листа наносят различные рифления в виде ромба, дуэта, чечевицы, квинтета или любого другого рисунка. Но рифление квинтет и …
Низкоуглеродистую сталь марки aisi 310s купить в интернете по выгодной цене и с оперативной доставкой можно исключительно через онлайн-сервис производителей с репутацией ответственного партнера. Только в таком случае можно рассчитывать …
Изготавливаемые из стали 12х18н10т круг нержавеющий, лист зеркальный — пластичные материалы с ударновязкой структурой, устойчивые к межкристаллитной коррозии.
msd.com.ua
