Назовите лёгкий металл, который плавает в воде, как пробка ???? — Обсуждай
Любовь
Назовите лёгкий металл, который плавает в воде, как пробка ???? металл вода пробка
1739
239
3
Александр
Две подружки вечерком
Пробавлялись коньячком.
И, как принято в кругах,
Речь вели о мужиках…
— Как бы мне так исхитриться,-
Говорит одна девица, —
Чтоб в толпе, наверняка,
Набрести на мужика?..
Ныне стал мужик другой:
То импот, то — голубой.
Угадай-ка под личиной
Настоящего мужчину!!!
— Эх, подруженька родная!
Раньше, дура, их не зная,
Многим сердце я дарила,
Пока их не раскусила. ..
..
И теперь могу сказать,
С виду все они похожи,
Словно тапочки из кожи,
Лишь размер их различает,
Да по-разному воняют…
Пахнут водкою и потом
Алкоголик с обормотом.
С ними — не построишь рай,
А жильё их — как сарай!..
Вонь соляры и мотора
Выдаст с головой шофера.
С ним на счастье не надейся —
Проведет пол жизни в рейсах…
Пахнут властью и деньгами
Парни с хваткими руками.
Их любовью не проймёшь,
Только время зря убьёшь…
Парфюмерией и гелем
Пахнут пидоры и геи.
Тут нам нечего ловить,
Лучше сразу отвалить…
Запахом овец и мулов
Пахнут горцы из аулов.
Спесь и наглость так и прут,
Развелось их много тут…
Вот идет навстречу парень.
У него лицо, как камень…
Запах страха уловила?
— Убегай что было силы!.
—————————-
Но, встречаются (по слухам)
Те, кто пахнут Русским Духом.
Вот такие — по душе!
С ними рай — и в шалаше!!!\
0
Любовь
Вот коза !!
1
Александр
С одной, я помню, сладкой дурой
Я, было, начал с увертюры…..
Ну там нормально всё, вступленье,
ГОрмоний разных разведенье.
Чин-чинарем все, пару септим.
(Я ж аккуратно с делом с энтим)
Тут позволяю я легато.
Интеллигентно, элегантно.
Вроде прошло. Иду к мажору.
Она всё семечки. (Обжора!)
Уж я поспел для главных арий,
Я ей «Диез», а мне «Бемоль»!
Ну нет, красавица, уволь!
Ну не выходит с нею терций
Из всех моих крутейших скерций!
Тогда устал я изгаляться
И вмазал пару модуляций!
Сорвал с нее покровы мантий,
Весь в абсолютной доминанте!. ..
..
Грустны финальные аккорды,-
Я получил за это в морду!(((((((
Ну как в экстазе тут сливаться?????????!
Всё. Буду лепкой заниматься.
1
Любовь
Хи..хи… ОБЛОМ !!!
1
Александр
Черная,как видно полоса нашла.
Собрала я вещи от тебя ушла.
И в мою ты сторону вовсе не глядишь.
Нет уж сил смотреть мне на твои носки
Как на все я гляну- вою от тоски
Вышла из подъезда-осмотрелась вдруг
Кажется я много слушала подруг.
Как тебя такого можно оставлять
Кто тебя с дивана будет поднимать
Кто от телевизора будет отрывать
Сигаретный пепел будет вытирать
Черную я полосу властно отведу
Поверну назад я и в подъезд войду
Если девкам нравишься я не удивлюсь
Да.
 Я передумаю,возьму да и вернусь
Я передумаю,возьму да и вернусьБыстро забежала, сумку теребя
Слушай мой ты котик,я люблю тебя!.
1
Любовь
1
Alexander Titov
Что тут сказать?Товарищ 7 лет назад
Мастер (2093)
Есть такие лёгкие металлы, которые плавают в воде, как пробка. Один из них называется ЛИТИЙ. Он легче воды вдвое и в 15 раз легче железа. Он есть почти в каждом камне и поэтому получил такое название: греческое «литос» означает «камень». Этот серебристо-белый металл в жарких печах расплавляют и смешивают с другими металлами. Получаются сплавы. Аллюминий не очень прочен, но если его сплавить с литием, получается металл куда прочнее!
0
Alexander Titov
Ну что я могу сказать, я всегда волнуюсь и за дочь и сына,а вот сейчас и за внуков уже! И конечно хочется пожить,ведь как сказала моя дочь,папа живи ведь твоя пенсия 12100,нам не как не помешает!
1
Любовь
Ты с детьми вместе живёшь ??? Я бы на такое высказывание обиделась.
1
Alexander Titov
Ну мой сын живет на квартире,моя мать по моей просьбе,завещала свою однокомнатную дочери! Когда мне было плохо и я выли тал из тела! Жена попросила дочь переехать к нам в трех комнатную,а дочь свою сдала квартирантам! Вот сейчас дочь купила дачу и построила там дом с баней! Это нам,что бы мы пользу приносили! Так что все просчитано до мелочей! Хотя банка мне нравится! Весной посадили две яблони,а осенью малину! Виноград от соседей растет на заборе, старая яблоня в этом году дала урожай яблок! Помидоры свои но мы не сильно упираемся,главное нам хватает!
1
Любовь
Лишь бы у тебя на душе был комфорт.
1
Alexander Titov
1
ОС
Олег Сорокин
Гугля в помощь ))) Самый легкий металл в мире – литий. При комнатной температуре его плотность является самой низкой. Она уступает воде практически в два раза и составляет 0,533 грамма на кубический сантиметр. Благодаря маленькой плотности он всплывает в воде и керосине.
При комнатной температуре его плотность является самой низкой. Она уступает воде практически в два раза и составляет 0,533 грамма на кубический сантиметр. Благодаря маленькой плотности он всплывает в воде и керосине.
0
Любовь
ХОРОШО ))))
1
Ми
Михаил
Литий?
1
Любовь
Да это он. Спасибо )))
1
Ми
Михаил
Это хорошо
1
Любовь
1
НИ
Николай Иванов
 Литий, в отличие от натрия и калия, хранят в вазелине. Литий — самый легкий из металлов. Он легче керосина и в отличие от других металлов всплывает в нем, поэтому его хранят в вазелине.
Литий, в отличие от натрия и калия, хранят в вазелине. Литий — самый легкий из металлов. Он легче керосина и в отличие от других металлов всплывает в нем, поэтому его хранят в вазелине.0
НИ
Николай Иванов
дело в том, что мы очень часто считаем себя правыми….. даже когда не правы
1
Любовь
Смотря в чём ! В профессионализме —да. В жизненных ситуациях не всегда.
1
НИ
Николай Иванов
В профессионализме от начальства зависит разрешит оно поспорить или нет. А в жизненных ситуациях иногда полезно дать успокоиться взрывному человеку, особенно если этот человек ты сам1
Любовь
Мне надо выходить. БУДУ ПОЗЖЕ….ЕДУТ ГОСТИ. НЕ СКУЧАЙ ))))
БУДУ ПОЗЖЕ….ЕДУТ ГОСТИ. НЕ СКУЧАЙ ))))
1
НИ
Николай Иванов
ОК
1
Яков Махортов
Ну не как пробка, пробка плавает, а вот этот метал кипит, или как еще назвать, ну короче реакция с водой.
0
Любовь
Натрий в воде сразу вступает в реакцию, выделяет газ и тепло, в результате чего, насятся с большой скоростью, но не плавает. КАЛИЙ при соединенении с водой просто взрывется и самовоспламеняются !
1
Яков Махортов
Калий взрывается когда в лужу бросаешь, а потом башмаком придавил, в 10 классе наверное весь запас щелочных металлов извели, в школьной лаборатории
1
Любовь
Смеюсь. ……………а лужа—не вода ???
……………а лужа—не вода ???
1
Яков Махортов
Лужа вода, я к тому, какие мы были беспечные
1
Любовь
Да, с этим я согласна. Беречь себя надо, а мы не умеем ))))
1
ВЛ
Владимир Логвинов
Из уроков химии не помню, но где-то слышал что Литий, он намного легче воды,может и ошибаюсь
0
Любовь
Верно. Литий
1
RS
Rishat Shakirov
Наверну умняк литий, и признаюсь подсмотрел, потому что самому стало интересно
0
Любовь
ой. …вот этого не ведаю !
…вот этого не ведаю !
1
RS
Rishat Shakirov
Сейчас скорее у вас ревность вижу
1
Любовь
Смеюсь………как я могу ревновать…не зная тебя ???
1
RS
Rishat Shakirov
И я смеюсь)))
1
Любовь
Вот и замечательный позитивчик )))
1
Alexandr Galkin
Значит так корабль плавает по воде, а он из железа. Отсюда и вывод железо
Отсюда и вывод железо
0
Alexandr Galkin
1
Alexandr Galkin
Самая мирная профессия
1
Любовь
Да, это верно )
1
Alexandr Galkin
У нас уже утро! Пойду новости смотреть да управляться по хозяйству
1
Любовь
Хорошего тебе дня !
1
Cергей Свириденко
ЦЕЗИЙ. НО И НАТРИЙ БРОСЬ УТОНУТЬ НЕ УСПЕЕТ, ГОРИТ СО ВЗРЫВНОЙ СКОРОСТЬЮ!
НО И НАТРИЙ БРОСЬ УТОНУТЬ НЕ УСПЕЕТ, ГОРИТ СО ВЗРЫВНОЙ СКОРОСТЬЮ!
0
Любовь
Это….ЛИТИЙ
1
Cергей Свириденко
КАлий и другие
1
Любовь
)))
1
**
***
не знаю…знаю..что алюминий один из легких металлов..но он тонет в воде…
0
Любовь
ЛИТИЙ, он в 2 раза легче воды !
1
**
***
спасибо!
1
Любовь
1
Сергей Кащик
Литий, конечно. В своё время с ним опыты проводили по химии интересные.
В своё время с ним опыты проводили по химии интересные.
0
Любовь
Спасибо !!! Верно !!
1
Сергей Кащик
Токмо нужно быть крайне осторожным — взрывоопасная сие штука….. Пары грамм достаточно, чтобы весьма неплохой взрыв создать….
1
Любовь
Это натрий кипит, а литий просто плавает
1
Сергей Кащик
Поверьте моему многолетнему опыту — литий не то. что кипит, он взрывается тут же с хлопком и искрами разлетается, и куда как активнее, чем натрий — сам лично сие проделывал неоднократно.
1
Любовь
Помню с урока, он быстро плавал по воде, происходила реакция и он таял в воде
1
Сергей Кащик
Либо сие был не литий, либо у нас разные металлы были…..
1
Любовь
Это у натрия очень бурная реакция при соприкосновении с водой ))
1
Роберт Иванов
..есть один «материал» который плавает.. Но, не металл точно.. Не угадал?
0
AP
Alex Pech
Он ещё и вступает в химическую реакцию с водой. Причём в очень бурную
Причём в очень бурную
0
Любовь
Калий и натрий не плавают, а результате реакции с водой они просто носятся по поверхности потому как выделяется газ
1
AP
Alex Pech
Да как скажете. Плотность воды 1.их плотность 0.96 и 0.9- конечно они тяжелее воды
1
Любовь
Спасибо !!! Ты прав, тяжелее
1
AP
Alex Pech
Вы очаровательны!
1
Любовь
Благодарю тебя !!! И ещё. …………..С Добрым Утром !!!
…………..С Добрым Утром !!!
1
ВМ
Виктор М
Не знаю, но корабли в сотни тысяч тонн — не тонут. А самолёты — летают.
0
Любовь
Ну и сравнил ! Прежде чем начать строительство корабля конструкторы составляют проект корабля, тщательно просчитывают нагрузки, водоизмещение и т д. А мой вопрос очень простой, назвать металл
1
ВМ
Виктор М
Не знаю, легче аллюминия.
1
Любовь
ЛИТИЙ ОН В 2 РАЗА ЛЕГЧЕ ВОДЫ
1
ВМ
Виктор М
Понял, спасибо. Я это раньше читал, но забыл.
Я это раньше читал, но забыл.
1
Любовь
Конечно, в памяти не всё удерживается !
1
АС
Андрей Симон
может это наша мужская воля иногда мы совершаем такие глупости
0
Любовь
Хихикаю……………….так мужчины состоят из металла ???
1
АС
Андрей Симон
думаю из множества разных металлов некоторых нет даже в таблице менделеева
1
Любовь
Это те, которые создали искусственно ?
1
Николай Ходосевич
Я видел, как натрий плавает, но он с водой вступает в реакцию. ..
..
0
Любовь
Это —ЛИТИЙ. Он в 2 раза легче воды.
1
Николай Ходосевич
Кстати, литий тоже с водой вступает в реакцию
1
Любовь
Он просто в воде растворяется
1
Николай Ходосевич
Нет. Идёт реакция и получается щёлочь — LiOH
1
Любовь
Верно.
1
МА
Мирошниченко Александр
литий, калий и натрий. изотопы лития самые легкие из них.
изотопы лития самые легкие из них.
0
Любовь
ЛИТИЙ !! Спасибо ))))
1
Ken Kiзi
Лёгкий крейсер черноморского флота «Вездесссущий» )))
0
Любовь
Внушительно !!! Но……………..не он ))))
1
Ken Kiзi
)) Литий и калий. В школе нужно было не прогуливать химию.
1
Любовь
Смеюсь. На свои вопросы я знаю ответы !!!
На свои вопросы я знаю ответы !!!
1
Ken Kiзi
)) Тоже смеюсь. …Задавать вопросы и знать ответы -похоже на маразм. ))))
1
Любовь
ненавижу хамов уйди с моих вопросов
1
Ken Kiзi
))…
1
СИ
Скорпион Иванович
Но с контактом с водой выделяет водород, нагреваясь!
0
Любовь
Смеюсь. ..Ты свою эрудицию проверь. Массу я тебе дала ! Вот тебе ещё для твоей эрудиции………………………………Легче воды литий (плотность 0,5), калий (0,9) и натрий (0,968 )
..Ты свою эрудицию проверь. Массу я тебе дала ! Вот тебе ещё для твоей эрудиции………………………………Легче воды литий (плотность 0,5), калий (0,9) и натрий (0,968 )
1
СИ
Скорпион Иванович
С этого и надо было бы начинать, а то шпаргалишь, как начинающая студентка 1 курса!
1
Любовь
Я тебе и так, как первокласснику всё разжевала !
1
СИ
Скорпион Иванович
Мне жвачку сознательность запрещает!
1
Любовь
Ничего !! Сейчас это модно !!! Идёт такой амбал и как ребёнок жвачку жуёт !
1
ОБ
Олег Борисович
Люба, Ты — Крассавчик!!!!! Всегда — интересные вопросы!
0
Любовь
Почему не спишь ???
1
ОБ
Олег Борисович
Боюсь пропустить Твои вопросы
1
Любовь
А знаешь как увидеть мои все вопросы ???
1
ОБ
Олег Борисович
На Твоей странице. Смотрел, но пока не добрался
Смотрел, но пока не добрался
1
Любовь
Да, там их много.
1
Есть ли металлы легче алюминия? | Техника и Интернет
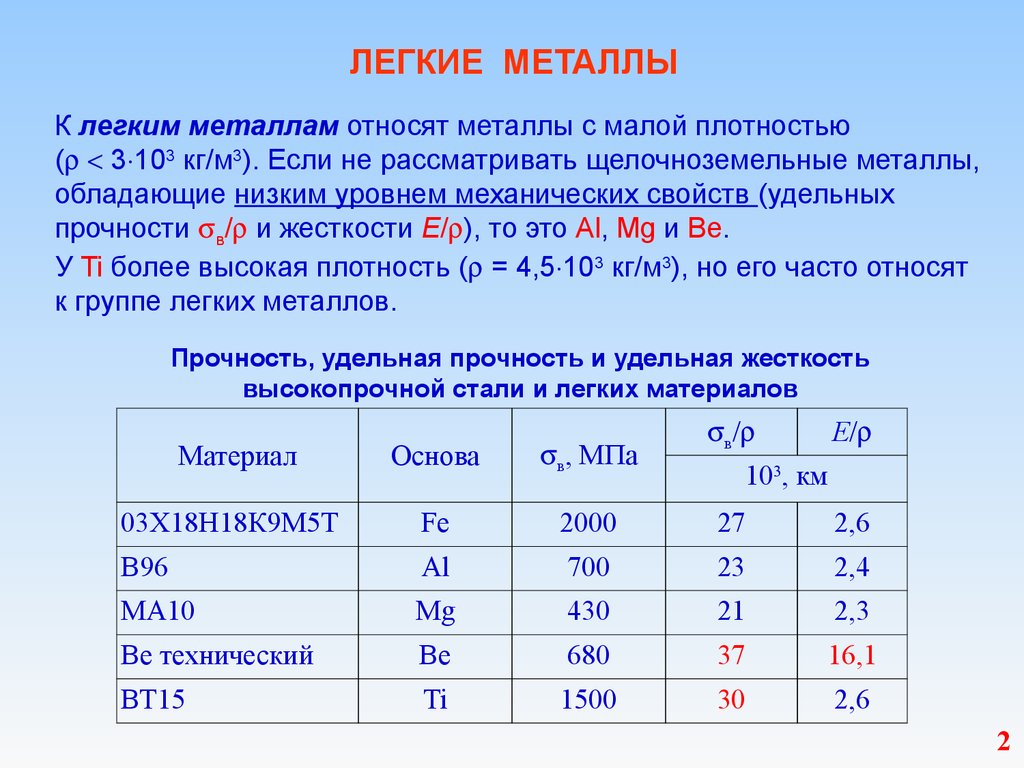
Развитие производства полимерных и композиционных материалов отнюдь не отодвигает легкие металлы на второй план. Объем их производства продолжает расти, особенно это относится к алюминию и его сплавам. Но есть и «более другие» легкие металлы и сплавы.
Самые легкие — все щелочные металлы: литий, натрий, калий, рубидий, цезий и франций. Но в промышленности из них в качестве легкого материала применяют только литий, да и то в сплавах.
Литий — самый легкий из металлов, он почти вдвое легче воды. Но, к сожалению, в чистом виде применить его в качестве конструкционного материала невозможно — он слишком активен, вступает во взаимодействие и с водой, и с воздухом. А вот в сплавах, например, с алюминием, — пожалуйста.
Но, к сожалению, в чистом виде применить его в качестве конструкционного материала невозможно — он слишком активен, вступает во взаимодействие и с водой, и с воздухом. А вот в сплавах, например, с алюминием, — пожалуйста.
Современные алюмо-литиевые сплавы по многим параметрам превосходят традиционные сплавы, и в ряде случаев конкурируют с пластмассами, упрочненными волокнами. Необходимую вязкость таких сплавов обеспечивают введением в них легирующих элементов — марганца, циркония и меди, соответствующей технологией изготовления материала, приводящей к образованию мелкозернистой структуры, а также применением термомеханической обработки, влияющей на равномерность выделения дисперсных фаз.
Благодаря этому достигают необходимой комбинации прочности и вязкости, что при малой плотности и высокой жесткости позволяет рассматривать алюмо-литиевые сплавы как наиболее перспективный материал для легких конструкций.
Алюмо-литиевые сплавы интересны для авиакосмической промышленности. Это вызвано тем, что добавка лития одновременно повышает модуль упругости и понижает плотность сплава, тем самым способствуя уменьшению массы конструкций.
Из щелочноземельных металлов в конструкционных материалах используют только магний и бериллий. Кальций и стронций, несмотря на то, что они легче алюминия, практически не используют.
Сплавы магния многочисленны и делятся на две группы: литейные и деформируемые.
Благодаря низкой плотности и высокой удельной прочности их используют в авиакосмической технике в качестве конструкционных материалов. Магний придает им легкость — магниевые сплавы на треть легче алюминия.
Магний придает им легкость — магниевые сплавы на треть легче алюминия.
Около пятой части выплавляемого магния используют в автомобилестроении.
Магний предпочтителен и при изготовлении композитов с металлической матрицей. Расплавленный алюминий, например, реагирует с армирующими волокнами карбида кремния, образуя карбид алюминия. Магний в отношении этих волокон инертен.
Бериллий одновременно относится и к легким, и к редким металлам, а следовательно, и к дорогим. Но основной недостаток этого металла, препятствующий его применению в технике, — высокая токсичность.
Еще один отрицательный фактор — хрупкость бериллия. Однако плюсов у него значительно больше.
Однако плюсов у него значительно больше.
Бериллий — один из наиболее легких металлов. Он в 1,5 раза легче алюминия и в 4 раза легче нержавеющей стали. По модулю упругости он превосходит и сталь, и титан, и алюминий. Важно, что его прочностные свойства не утрачиваются вплоть до температуры 800 градусов.
Несмотря на высокую стоимость и токсичность, бериллий используют там, где он незаменим. Так, в США из него были изготовлены панели серии космических кораблей «Аджена», части антенны на спутнике связи «Тэксэт-1» и отражатель ядерного ракетного двигателя «Нерва-1».
Алюминий находится в третьей группе элементов. Других металлов легче алюминия в этой группе нет. В четвертой группе легче алюминия только кремний. Но значение его столь велико, что он заслуживает отдельной статьи.
В четвертой группе легче алюминия только кремний. Но значение его столь велико, что он заслуживает отдельной статьи.
Подведем итоги. Металлов легче алюминия много, больше десятка. Но не все из них, увы, могут его заменить или дополнить.
Однако все меняется…
Теги: творческая мысль, польза, физика, интересный факт, металл, химия
в России превзошли Японию в создании непотопляемых судов » Экономическое обозрение
newinform. com
com
- 5 420
Российские разработчики создали инновационный материал с уникальными свойствами, которых не смогли достичь даже в Японии….
Читать полностью…
[is-owner] Аукцион[/is-owner]
Из Европы потянулся ручеёк мигрантов в РФ. Причём, люди не бедные. Покупают, зачастую, не просто недвижимость, но, некоторые, и земли сельхозназначения….
[author-avatar] [/author-avatar] трымава.рф
- 4 016
[is-owner] Аукцион[/is-owner]
Новый союзник Путина обеспечит России серьезное преимуществе в борьбе со странами Запада. Таким мнением поделился журналист британских СМИ Энтони Ашкеназ….
[author-avatar]
[/author-avatar]
politros. com
com
- 3 598
[is-owner] Аукцион[/is-owner]
ЕС не удалось согласовать потолок цен на российский газ. Тем не менее, вопрос ограничения доходов нашей страны от экспорта «голубого топлива» не вычеркнут из…
[author-avatar] [/author-avatar] k-politika.ru
- 3 386
[is-owner] Аукцион[/is-owner]
Соединенные Штаты готовятся совершить очередную глупость в отношении России. Такими выводами поделился американский финансовый эксперт, экс-советник ЦРУ Джеймс…
[author-avatar] [/author-avatar] politros.com
- 3 365
[is-owner] Аукцион[/is-owner]
Большинство импортных самолётов в России находятся в лизинге, платить по которому невозможно. Минтранс предложил использовать национальный кошелёк для того,…
Минтранс предложил использовать национальный кошелёк для того,…
[author-avatar] [/author-avatar] k-politika.ru
- 2 991
[is-owner] Аукцион[/is-owner]
Германский концерн Uniper готовит иск в Стокгольмский арбитраж, а Siemens врет, изображая невиновного…
[author-avatar] [/author-avatar] svpressa.ru
- 2 934
[is-owner] Аукцион[/is-owner]
Областное государственное учреждение «Облкоммунэнерго» старается делать всё для потребителя, а ему все вставляют палки в колеса. Именно к такому выводу уже не…
[author-avatar]
[/author-avatar]
k-politika. ru
ru
- 2 671
[is-owner] Аукцион[/is-owner]
Проблемы Евросоюза из-за газа достигнут пика не предстоящей зимой и не будут связаны с отоплением. Такое мнение выразил заместитель генерального директора…
[author-avatar] [/author-avatar] rueconomics.ru
- 2 418
[is-owner] Аукцион[/is-owner]
После конфискации имущества россиян в Финляндии инвестиционный климат страны ухудшится, ведь ни одно другое государство не захочет иметь дела с нарушающей…
[author-avatar] [/author-avatar] inforeactor.ru
- 2 260
[is-owner] Аукцион[/is-owner]
Ждать, что Европа замерзнет и все само собой образуется без необходимости напрягаться и побеждать на поле боя – опасная иллюзия и маниловщина. …
…
[author-avatar] [/author-avatar] politnavigator.net
- 2 242
Золото или Уран? Не торопитесь с ответом!
Если задать этот вопрос 10 человекам, то 9 из них уверенно ответят, что, конечно же, уран тяжелее, притом намного. Но такой ответ – результат широко распространенного заблуждения. То же самое, наверняка, случится, если попросить назвать самый распространённый на Земле металл. Наверное, вы уже догадались, это отнюдь не железо. В честь отмечаемого сегодня Дня металлурга мы собрали для вас ТОП-6 самых любопытных фактов о металлах.
1. Самые лёгкие и тяжёлые
Если в школе по химии у вас была не пятёрка, то вы, наверняка, удивитесь тому факту, что существует целых три металла, которые легче …воды! Это литий (0,53 г/см3), калий (0,85 г/см3) и натрий (0,97 г/см3). Это значит, что вся эта прекрасная троица категорически отзывается тонуть и плавает в воде!
Что касается самых тяжёлых металлов, то таковыми являются иридий (22,65 г/см3), осмий (22,61 г/см3) и платина (21,46 г/см3). Наверняка о первых двух вы никогда не слышали, и знаете только платину. Так вот, знайте, все эти три металла-рекордсмена на 10% тяжелее золота (19,3 г/см3), которое превосходит по тяжести даже радиоактивный уран (19,05 г/см3). Если и это сравнение для вас слишком сложное, то просто запомните, что иридий, осмий и платина в 3 раза тяжелее железа и в 2 раза тяжелее свинца!
Наверняка о первых двух вы никогда не слышали, и знаете только платину. Так вот, знайте, все эти три металла-рекордсмена на 10% тяжелее золота (19,3 г/см3), которое превосходит по тяжести даже радиоактивный уран (19,05 г/см3). Если и это сравнение для вас слишком сложное, то просто запомните, что иридий, осмий и платина в 3 раза тяжелее железа и в 2 раза тяжелее свинца!
2. Легкоплавкие и тугоплавкие
С первым рекордсменом вы хорошо знакомы – это ртуть, которая плавится (т.е. становится жидкой) уже при минус 39 градусах Цельсия. На втором месте стоит металл франций – он плавится уже при комнатной температуре – при плюс 27 градусах. Третье место у цезия – для плавления его достаточно нагреть до плюс 28 градусов. К слову, это норма максимальной температуры в рабочих (офисных) помещениях. Так вот, если принесённый вами на рабу кусочек цезия расплавился, значит, вы смело можете требовать сокращения продолжительности рабочего дня!
Тяжелее всего расплавить вольфрам (3422 градуса), рений (3186 градусов) и уже знакомый вам осмий (3033 градуса). К слову, именно из-за феноменальной тугоплавкости почти все нити накаливания в электрических лампочках делают именно из вольфрама. Название этого чудо-металла в переводе с немецкого языка означает «волчья пена». Когда волк долго бежит за добычей, у его рта появляется обильная белая пена. Совсем как при плавлении вольфрама на металлургическом заводе…
К слову, именно из-за феноменальной тугоплавкости почти все нити накаливания в электрических лампочках делают именно из вольфрама. Название этого чудо-металла в переводе с немецкого языка означает «волчья пена». Когда волк долго бежит за добычей, у его рта появляется обильная белая пена. Совсем как при плавлении вольфрама на металлургическом заводе…
3. Проводники и не очень
Из всех металлов наиболее высокую электропроводимость имеет серебро – поэтому в самых ответственных приборах проводники делают из «аргенутма», в честь которого получило название целое государство – Аргентина. На второй позиции стоит медь, с которой произошла противоположная история – этот металл назвали «купрум» в честь острова Кипр, где его добывали ещё с незапамятных времён. Третье место по проводимости у золота (ну, это вообще элемент-уникум по целому ряду параметров, который является самым известным драгоценным металлом). А вот алюминий находится лишь на четвёртом месте, но именно из него во всём мире делают львиную долю электрических проводов.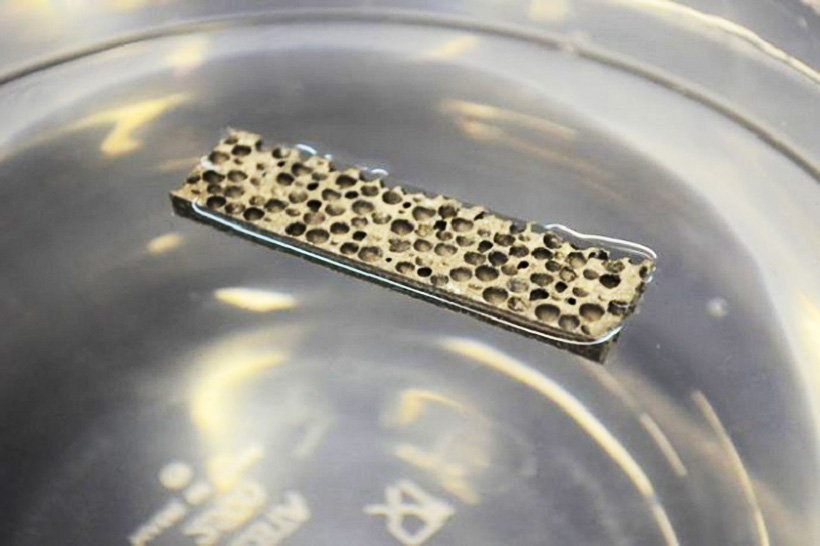 Почему? Ответ на этот вопрос вы найдете в следующем разделе.
Почему? Ответ на этот вопрос вы найдете в следующем разделе.
Все металлы являются хорошими проводниками электрического тока – этот параметр является отличительным признаком ВСЕХ металлов от НЕметаллов. Однако, «как говорят в народе, в семье не без урода»! По своей проводимости марганец, гадолиний и висмут отстают от серебра в 7-10 раз!
4. Распространённые и редкие
Самым распространённым металлом на Земле является, конечно же, …алюминий. Его оксид составляет весьма значительную долю самой обычной глины. К слову, наиболее дорогой бриллиант — это аламаз, который доводится близким родственником заурядному каменному углю. Так и тут, непосредственной роднёй красной глины является драгоценный камень под названием «рубин». Но вернёмся к металлам. На втором месте по распространённости в коре Земли находится железо – из него сделаны корабли, мосты, железные дороги, автомобили и «скелеты» почти всех наших домов. А третьим по частоте нахождения в природе стоит кальций, который является строительным материалом наших костей и зубов.
Что касается наиболее редких металлов на нашей планете – это рений, иридий и родий. Впрочем, есть и искусственно создаваемые элементы, которые живут всего доли секунды. Но не о них сегодня речь, поскольку от таковых для человечества пока нет почти никакой практической пользы…
5. Твёрдые и мягкие
Для определения этого параметра существует специальная шкала, придуманная немцем Фридрихом Моосом. Она далеко не только про металлы, но всё же, ознакомьтесь, чтобы вам было понятно, о чём идёт речь. Так, вот, по этой 10-бальной шкале самым мягким веществом является тальк (1 балл), а самым твёрдым – уже упомянутый сегодня алмаз (10 баллов).
Если говорить только о металлах, то среди них есть ещё более мягкие, чем тальк! Это церий (0,2), рубидий (0,3) и калий (0,4). На другой чаше весов – рекордсмены по твёрдости. Это ванадий (7,0), наш хороший друг вольфрам (7,5) и хром (8,5).
6. Чёрные и цветные
К чёрным металлам относят всего четыре: железо, марганец, хром и ванадий. С железом всё ясно – в холодном состоянии оно, как правило, имеет чёрный цвет (существуют оттенки от серебристого до иссиня-чёрного – «воронёного»). А вот последние три металла широко используются для легирования (т.е. улучшения физических свойств) стали. Все остальные металлы, вне зависимости от их цвета, являются цветными!
С железом всё ясно – в холодном состоянии оно, как правило, имеет чёрный цвет (существуют оттенки от серебристого до иссиня-чёрного – «воронёного»). А вот последние три металла широко используются для легирования (т.е. улучшения физических свойств) стали. Все остальные металлы, вне зависимости от их цвета, являются цветными!
Если вы дочитали этот материал до конца, то теперь понимаете и сможете популярно рассказать другим, почему самые важные детали в лобовой части вашего автомобиля хромированы (покрыты слоем хрома), почему в градусники заливают ртуть, а не цезий, и почему сердечники бронебойных снарядов начиняют слаборадиоактивными изотопами урана, а не более тяжёлым золотом)))
Так крикнем «УРА!» металлургам мы дружное,
За то, что те варят нам всё самое нужное!!!
- новости
- общество
- металлургия
- тяжелые металлы
- профессиональный праздник
- драгоценные металлы
- день металлурга
- 17 июля
- металлы
- цветные металлы
- железо
Литиевые батареи
Внимательно прочтите эти правила перед использованием батарей! |
Литий — наиболее легкий металл, он вдвое легче воды и всплывает даже в керосине. Одновременно с этим, литий обладает огромным электрохимическим потенциалом, что делает его одним из самых активных металлов. Это свойство лития дает возможность создавать на его основе батареи и аккумуляторы с очень высокой плотностью энергии при минимальных размерах и массе.
Одновременно с этим, литий обладает огромным электрохимическим потенциалом, что делает его одним из самых активных металлов. Это свойство лития дает возможность создавать на его основе батареи и аккумуляторы с очень высокой плотностью энергии при минимальных размерах и массе.
Преимущества, которыми обладают литиевые аккумуляторы
Еще одно преимущество литиевых аккумуляторов — очень низкий ток саморазряда. Это означает, что батарея может пролежать «на полке» или в выключенном приборе на годы дольше щелочных батареек. Для литиевых аккумуляторов это означает, что в малопотребляющих приборах не придется периодически подзаряжать аккумулятор (что придется сделать с никель-металлгидридными (NiMh), никель-кадмиевыми (NiCd) или свинцовокислотными (Lead Acid) аккумуляторами), или придется это делать намного реже.
Литиевые аккумуляторы также обладают еще одним важным преимуществом — они практически не теряют емкость при отрицательных температурах: большинство выпускаемых батарей спокойно работают от -40° а некоторые типы — от -60°. В условиях русской зимы и особенно Крайнего севера — литиевые батареи незаменимы.
В условиях русской зимы и особенно Крайнего севера — литиевые батареи незаменимы.
Все эти параметры становятся особенно важными при использовании в устройствах выживания — к примеру, в фонарях, аварийных маячках или рациях.
Можно один раз «заправить» фонарь комплектом литиевых батарей, и более десяти лет не беспокоиться о том, что батареи (или аккумуляторы) разрядились, и требуют замены.
При этом, они легче других батарей, работают дольше, и не теряют емкость при отрицательных температурах.
Литиевые батареи и аккумуляторы производятся с разнообразными химическими формулами, что дает разное рабочее напряжение и энергоемкость.
Наиболее распространены:
- Li-MnO2 (батареи с префиксом «CR»).
Номинальное напряжение: 3В.Наиболее распространенный вид литиевых батарей. К батареям такого типа относятся, например, батареи CR123 или CR2. Батарея такой системы обладает большой емкостью, может отдавать большой ток, обладает широким температурным диапазоном (от -40 до +60).

К батареям этого типа относится также совместимая батарея типа «Корунд» (тип ISO «1604») напряжением 9В, которая физически состоит из трех элементов (обычные щелочные — из 6) - Li-FeS2 (литий-железодисульфидные батареи)
Номинальное напряжение: 1.5В.Современные литиевые батареи, призванные заменить традиционные щелочные и солевые батарейки.
Напряжение 1.5В позволяет напрямую вставлять их в приборы, предназначенные для работы с обычными батарейками.При этом за счет литиевой химии, они обладают преимуществами по сравнению с щелочными батареями и Ni-Mh аккумуляторами:
- Работают до 3-4 раз дольше. Литиевые батареи АА обладают эффективной емкостью 2900 мАч.
- Имеют массу на 35% меньше.
- Могут отдавать большой ток, что делает их применение возможным в «прожорливых» устройствах.
- Рабочий температурный диапазон — от -40° до +60°
- Низкий саморазряд: срок хранения — более десяти лет.

К недостаткам можно отнести сравнительно высокую цену, но наращивание объемов производства таких батарей с каждым годом сокращает разрыв цены с щелочными батареями, и для работы в устройствах с большим энергопотреблением покупать такие батареи выгоднее, чем щелочные. - Li-Ion (литий-ионные батареи (аккумуляторы))
Номинальное напряжение: 3.6-3.7В.
В этих элементах металлический литий заменен на ионы лития, что сделало батарею более безопасной. Эти батареи являются перезаряжаемыми (аккумуляторами).В отличие от аккумуляторов других систем, они не подвержены «эффекту памяти», и обладают превосходными энергетическими характеристиками.
Саморазряд этих батарей — около 5% в месяц, по сравнению с 30% Ni-Mh аккумуляторов (новейшие типы Ni-Mh аккумуляторов имеют более низкие, чем 30%, токи саморазряда), и 10% Ni-Cd.
Однако, литий-ионные аккумуляторы теряют емкость по мере старения, вне зависимости от заряда и количества циклов заряда-разряда. В среднем, это старение составляет около 20-30% в год, и усиливается при высоких температурах.
В среднем, это старение составляет около 20-30% в год, и усиливается при высоких температурах.
Сильная электрохимическая активность лития, наряду с огромным энергетическим потенциалом, создает дополнительные инженерные проблемы производителям батарей. Например, литий вступает в сильную реакцию с водой, с образованием щелочи и водорода.
Как известно, водород в смеси с кислородом воздуха, при определенной пропорции смеси, становится взрывоопасным. А тепло, выделяющееся при реакции, может воспламенить эту смесь.
Впрочем, эта проблема присуща также и свинцовокислотным аккумуляторам.
По этой причине все литиевые элементы упаковываются в герметичную оболочку.
В высокоэнергетических литиевых батареях и литий-ионных аккумуляторах при коротком замыкании или неправильной эксплуатации повышается температура и давление. Поэтому в конструкцию элементов добавляют предохранительные клапаны и контакты («PTC» — Positive Temperature Coefficient), размыкающиеся при повышении температуры. Эти меры позволяют предотвратить взрыв батарей, при неправильном с ними обращении.
Поэтому в конструкцию элементов добавляют предохранительные клапаны и контакты («PTC» — Positive Temperature Coefficient), размыкающиеся при повышении температуры. Эти меры позволяют предотвратить взрыв батарей, при неправильном с ними обращении.
Литий-ионные и литий-полимерные аккумуляторы очень чувствительны к процессу заряда и разряда,
поэтому в 99% случаев вместе с собственно элементом питания в батарее присутствует также и плата электроники, которая следит за «здоровьем» батареи, контролирует процесс заряда, разряда, а также предотвращает взрыв при коротком замыкании или превышении тока заряда.
Именно поэтому большинство литий-ионных аккумуляторов имеет не два, а три или четыре контакта — через дополнительные контакты микроконтроллер платы защиты общается с основным устройством.
Использование незащищенных литий-ионных аккумуляторов не рекомендуется по следующим причинам:
- Короткое замыкание, неправильная полярность, превышение напряжения или тока заряда могут вызвать взрыв.

- Слишком сильный разряд аккумулятора «убьет» его, сделав невозможным его дальнейшее использование. Не все устройства содержат защиту от глубокого разряда вставленных в них аккумуляторов. Обычно критическое напряжение глубокого разряда составляет 2.4-2.7В, в зависимости от химической формулы.
Меры предосторожности при работе с литиевыми аккумуляторами.
Проведенные исследования режимов эксплуатации на пожаро- и взрывобезопасность, а также миллиарды использованных литиевых батарей (в том числе батареи Вашего мобильного телефона, плеера, компьютера и т.п.), установили, что современные конструкции литиевых элементов практически безопасны при их правильной эксплуатации, и более того — вполне рассчитаны на «дурака».
Но, следуя принципу «предупрежден — значит вооружен», мы публикуем основные моменты работы
с литиевыми батареями. В общем-то все, написанное ниже, применимо и обязательно для выполнения при использовании и обычных щелочных батареек.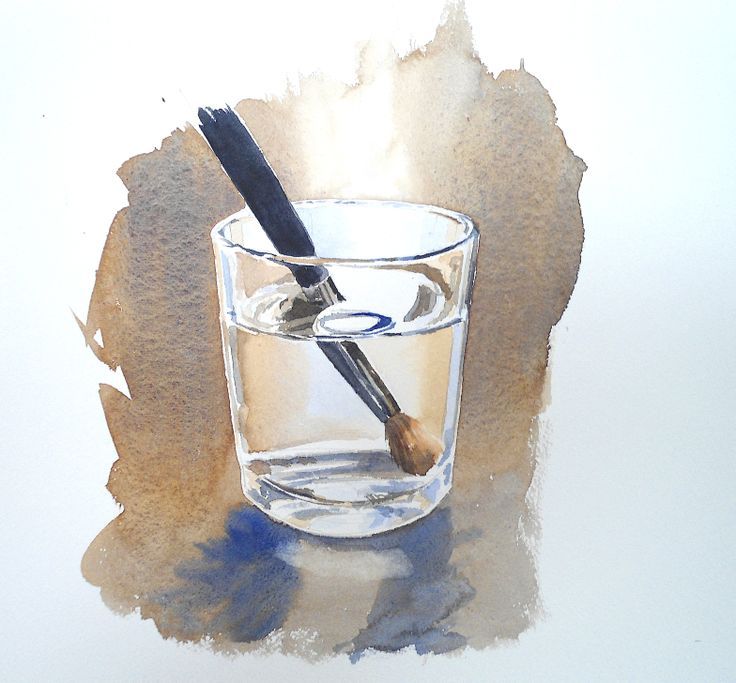 (и всегда пишется на упаковке)
(и всегда пишется на упаковке)
Используя в бытовой технике батареи и аккумуляторы литиевой системы, вы должны осознавать, что их повышенные по сравнению с щелочными батареями и Ni-Mh аккумуляторами потребительские свойства — энергоемкость, масса — взяты не «с потолка», а являются следствием использования более активного материала.
Как показывает практика, потребители редко читают инструкцию по эксплуатации батарей и аккумуляторов, и еще реже её соблюдают, надеясь на русский «авось».
И хотя правила эксплуатации литиевых батарей ничем не отличаются от правил эксплуатации щелочных батарей и других аккумуляторов, их соблюдение особенно важно, т.к. несоблюдение может привести к более серьезным последствиям.
Итак:
Не перезаряжать, не нагревать.
В литиевой батарее есть т.н. пассивирующий слой на литиевом аноде. Эта защитная пленка соединений лития, в обычных условиях, препятствует прямым химическим реакциям металлического лития с электролитом и основными продуктами реакции. Зарядка литиевых батарей (не аккумуляторов, а именно неперезаряжаемых батарей, к примеру CR123) разрушает эту пленку и категорически запрещена. Это приводит к высвобождению и накоплению в батарее металлического лития, его реакции с электролитом, росту температуры и давления, и, как следствие, утечке токсичного газа (через предохранительный клапан), электролита, и может привести к воспламенению или взрыву батареи.
Зарядка литиевых батарей (не аккумуляторов, а именно неперезаряжаемых батарей, к примеру CR123) разрушает эту пленку и категорически запрещена. Это приводит к высвобождению и накоплению в батарее металлического лития, его реакции с электролитом, росту температуры и давления, и, как следствие, утечке токсичного газа (через предохранительный клапан), электролита, и может привести к воспламенению или взрыву батареи.
К этому также может привести закорачивание батареи или её нагревание. К батарее нельзя припаивать провода бытовыми паяльниками и паяльными станциями — это нарушит или сплавит защиту от перегрева батареи, и она станет небезопасна. Нельзя оставлять батарею под прямыми солнечными лучами.
То же самое относится к превышению тока заряда и напряжения заряда литиевых аккумуляторов. Используйте только качественные зарядные устройства, не стоит подключать «вот эту батарейку» к «вон тому заряднику» от «вон того прибора». Это опасно.
Некоторые компании даже выпускают спец. оболочки-пакеты для зарядки литиевых элементов на предельных режимах:
Не смешивать бывшие в употреблении и новые батареи; батареи разных типов или производителей.
Установка элементов с разным напряжением (например, новый и бывший в употреблении) приведет к тому, что один элемент (новый) будет стремиться отдавать больший ток, и станет заряжать другой (старый). Батареи разных производителей, во-первых, могут иметь разное внутреннее сопротивление, а во-вторых, незначительно отличающийся химический состав. По описанной в п.1 схеме, и то, и другое может привести к взрыву.
Согласно исследованиям, смешивание Б/У и новых батарей или батарей разных производителей, явилось причиной №1 случаев возгорания и взрыва литиевых батарей в фонарях и других приборах. Наихудшее с точки зрения безопасности соотношение — это использование новой батареи и
на 20% использованной. И хотя таких случаев зарегистрировано менее десяти на сотни тысяч случаев беспроблемного использования, делать этого не стоит.
Наихудшее с точки зрения безопасности соотношение — это использование новой батареи и
на 20% использованной. И хотя таких случаев зарегистрировано менее десяти на сотни тысяч случаев беспроблемного использования, делать этого не стоит.Не разбирать, не сжигать, не использовать батареи со следами повреждений или протечек.
Прокол элементов или смятие может привести к внутреннему короткому замыканию, с последующим возгоранием и взрывом; Расплавление лития от высокой температуры также приводит к взрыву.
При разгерметизации внутрь элемента может попасть вода или сконденсироваться атмосферная влага, что может привести к реакции с выделением водорода и возгоранию.Не закорачивать.
 Соблюдать полярность.
Соблюдать полярность.
При разряде большими токами или коротком замыкании из-за некоторой неоднородности структуры батареи и наличия примесей могут возникать локальные «горячие точки», которые лавинообразно вызывают разогрев всей батареи.
Результат — взрыв.Не утилизировать с бытовыми отходами.
Хотя это общепринятая практика в нашей стране, но, вопреки ей, элементы питания нельзя выкидывать вместе с бытовым мусором.К примеру, остатки соленой воды в кухонных отходах могут закоротить элемент.
И хотя у нас не создано никаких условий для правильной утилизации таких отходов — позаботьтесь хотя бы о том, чтобы литиевый элемент не контактировал с другими отходами.
Например, поместив его в индивидуальный полиэтиленовый пакет, и завязав его.Хранить в сухом, прохладном месте.
 Влага, кроме прямого закорачивания контактов, может вызвать коррозию внешней оболочки
батареи, заткнуть вентиляционные клапаны или нарушить герметичность. Батарею с признаками коррозии использовать нельзя.
Высокая температура, близость к батареям отопления, духовым шкафам, печным трубам
или прямые солнечные лучи могут вызвать повышение давления внутри батареи.
Влага, кроме прямого закорачивания контактов, может вызвать коррозию внешней оболочки
батареи, заткнуть вентиляционные клапаны или нарушить герметичность. Батарею с признаками коррозии использовать нельзя.
Высокая температура, близость к батареям отопления, духовым шкафам, печным трубам
или прямые солнечные лучи могут вызвать повышение давления внутри батареи.
Современные литиевые батареи содержат множество элементов конструкции, которые призваны повысить степень защиты — сбросить нарастающее давление, разъединить электрическую цепь при превышении тока или температуры, а также разнообразную защитную электронику, но их лучше рассматривать как средства «последнего эшелона», и надеяться не на них, а на разумное соблюдение правил безопасности.
Соблюдение этих правил почти наверняка избавит вас от неприятных моментов использования литиевых батарей. И хотя случаи возгорания или взрыва батарей в фонарях очень редки (в Интернет-сообществе описано менее 10 случаев за все время на весь мир), мы считаем важным упомянуть основные сценарии развития событий.
- В большинстве редких случаев возгорания литиевых батарей в фонарях, фонарь «тухнет» или теряет яркость на сравнительно свежем комплекте батарей. В любом случае, это должно вас насторожить.
Часто после этого, иногда через значительное время (20-30 мин.) слышится шипение клапана сброса давления батареи. Если вы слышите шипение этого клапана или фонарь неожиданно потускнел или нагрелся — ни в коем случае не направляйте фонарь стеклом или торцом к себе.
Настороженность также должно вызвать ненормальное для данного режима работы фонаря нагревание батарейного отсека, особенно в выключенном состоянии (выше 60-70 градусов).
При возникновении описанных симптомов — если фонарь у вас в руках — немедленно выключите его и положите подальше от людей, домашних животных и легковоспламеняемых предметов.
Если фонарь не в руках — не подходите к нему как минимум 3-4 часа.Шипение клапана сброса давления часто сопровождается выделением едкого белого дыма с характерным «электрическим» запахом.
 Этот дым токсичен — старайтесь не вдыхать его и проветрить
помещение.
Этот дым токсичен — старайтесь не вдыхать его и проветрить
помещение.
Если из батареи вылился электролит — не допускайте его контактов с кожей.
Пролитый электролит следует засыпать пищевой содой или опилками, и вытереть насухо.
Взрыв батареи иногда происходит через 1-2 секунды, а иногда через 20-30 минут после шипения клапана.
При возгорании и взрыве литиевых батарей запрещается тушить их углекислотными огнетушителями: литий бурно реагирует с углекислотой.
Эффективно применение порошковых огнетушителей (напр. ОП-10).Тушение горящих элементов и их обломков можно производить, накрывая очаги горения плотной термостойкой тканью (асбестовым полотном).
Можно тушить сухим песком, покрывалом, сухой поваренной солью.
Вода неэффективна при тушении горящего лития, и предотвращает главным образом распространение пожара. Наоборот, реакция лития с водой может вызвать выделение водорода, который усилит горение.
Не берите в руки фонарь, обломки или батареи ранее, чем через несколько часов после прекращения любых проявлений реакции. Не приближайтесь к взорвавшимся или вытекшим батареям, пока они не остынут.
Защищайте кожу от контактов с электролитом резиновыми перчатками.
Засыпьте батареи, а также обломки, пищевой содой, для нейтрализации электролита. Поместите в полиэтиленовый пакет и утилизируйте.
Помните телефон пожарной охраны: В России это 101, или 112, или 911 (с мобильного телефона).
- Чаще взрываются фонари на двух CR123-элементах (в большинстве случаев ксеноновые, а не светодиодные), чем на одном. Поэтому при использовании фонаря, работающего на двух элементах, старайтесь или использовать защищенный аккумулятор 18650 или 17670, если он допустим конструкцией фонаря, или особенно тщательно подходите к вопросу выбора пары батарей. Старайтесь ставить вместе батареи из одной партии.
Если у вас есть возможность измерить внутреннее сопротивление батарей — старайтесь совмещать батареи по внутреннему сопротивлению.
Естественно, ни в коем случае не ставьте разные батареи или использованные совместно с новыми.
- Чаще взрываются фонари на галогеновых (ксеноновых галогенных) лампах без электроники, чем светодиодные с электроникой.
Причина — описанные выше в п.4 «горячие точки», которые возникают при неконтролируемом
разряде большим током.
- Старайтесь использовать качественный фонарь, нежели безымянный.
Плохая конструкция и используемые материалы могут служить причиной закорачивания батарей. Особенно это относится к дешевым галогеновым фонарям на элементах CR123.
Старайтесь использовать водонепроницаемый фонарь — это также предотвратит нештатные ситуации при использовании литиевых батарей. - Старайтесь использовать алюминиевый фонарь, нежели пластиковый.
Пластиковый фонарь может разлететься в непредсказуемых направлениях.
У алюминиевых фонарей «вышибает» стекло и торцевую кнопку (если такая есть). Так что, при взрыве в руке в большинстве описанных случаев (3 случая) обошлось без травм.
Так что, при взрыве в руке в большинстве описанных случаев (3 случая) обошлось без травм.
Одновременно, пластиковый корпус менее стоек к разогреву батарей и может обеспечить меньше защиты батареям от внешнего тепла.
А остальные миллиарды случаев успешного использования литиевых батарей без каких-либо эксцессов подтверждают: за этими элементами ближайшее будущее. И если век топливных или био-элементов еще не наступил, то для лития — самое время.
В реальности же с безопасностью дело обычно обстоит так:
Ссылки по теме:
Статья про элементы питания на HPC.RU
Лабораторные опыты по Химии, видео: реакция лития с водой (опыт 12)
Реакция лития с водой, видео (другой опыт)
Статья на сайте FlashLightReviews про батарейки вообще(англ.)
Статья на сайте FlashLightReviews про батарейки подробнее(англ.)
Статья на сайте FlashLightReviews про взрывы батарей (англ. )
)
Сравнение разных типов и марок батарей (с графиками)
Взаимодействие щелочных металлов с водой (передача «Мозголомы»), видео
ЩЕЛОЧНЫЕ МЕТАЛЛЫ | это… Что такое ЩЕЛОЧНЫЕ МЕТАЛЛЫ?
ТолкованиеПеревод
- ЩЕЛОЧНЫЕ МЕТАЛЛЫ
ПОДГРУППА IА. ЩЕЛОЧНЫЕ МЕТАЛЛЫ
ЛИТИЙ, НАТРИЙ, КАЛИЙ, РУБИДИЙ, ЦЕЗИЙ, ФРАНЦИЙ
Электронное строение щелочных металлов характеризуется наличием на внешней электронной оболочке одного электрона, относительно слабо связанного с ядром. С каждого щелочного металла начинается новый период в периодической таблице. Щелочной металл способен отдавать свой внешний электрон легче, чем любой другой элемент этого периода. Разрез щелочного металла в инертной среде имеет яркий серебристый блеск. Щелочные металлы отличаются невысокой плотностью, хорошей электропроводностью и плавятся при сравнительно низких температурах (табл. 2).
2).
Благодаря высокой активности щелочные металлы в чистом виде не существуют, а встречаются в природе только в виде соединений (исключая франций), например с кислородом (глины и силикаты) или с галогенами (хлорид натрия). Хлориды являются сырьем для получения щелочных металлов в свободном состоянии. Морская вода содержит ЩЕЛОЧНЫЕ МЕТАЛЛЫ3% NaCl и следовые количества других солей. Очевидно, что озера и внутренние моря, а также подземные отложения солей и рассолы содержат галогениды щелочных металлов в больших концентрациях, чем морская вода. Например, содержание солей в водах Большого Соленого озера (шт. Юта, США) составляет 13,827,7%, а в Мертвом море (Израиль) до 31% в зависимости от площади зеркала воды, изменяющейся от времени года. Можно полагать, что незначительное содержание KCl в морской воде по сравнению с NaCl объясняется усвоением иона K+ морскими растениями.
В свободном виде щелочные металлы получают электролизом расплавов таких солей, как NaCl, CaCl2, CaF2 или гидроксидов (NaOH), так как нет более активного металла, способного вытеснить щелочной металл из галогенида. При электролизе галогенидов необходимо изолировать выделяющийся на катоде металл, так как одновременно на аноде выделяется газообразный галоген, активно реагирующий с выделяющимся металлом.
При электролизе галогенидов необходимо изолировать выделяющийся на катоде металл, так как одновременно на аноде выделяется газообразный галоген, активно реагирующий с выделяющимся металлом.
См. также ЩЕЛОЧЕЙ ПРОИЗВОДСТВО
Поскольку у щелочных металлов на внешнем слое всего один электрон, каждый из них является наиболее активным в своем периоде, так, Li самый активный металл в первом периоде из восьми элементов, Na соответственно во втором, а K самый активный металл третьего периода, содержащего 18 элементов (первый переходный период). В подгруппе щелочных металлов (IA) способность отдавать электрон возрастает сверху вниз.
Химические свойства. Все щелочные металлы активно реагируют с кислородом, образуя оксиды или пероксиды, отличаясь в этом друг от друга: Li превращается в Li2O, а другие щелочные металлы в смесь M2O2 и MO2, причем Rb и Cs при этом возгораются. Все щелочные металлы образуют с водородом солеподобные термически стабильные при высоких температурах гидриды состава M+H, являющиеся активными восстановителями; гидриды разлагаются водой с образованием щелочей и водорода и выделением теплоты, вызывающей воспламенение газа, причем скорость этой реакции у лития выше, чем у Na и K.
См. также ВОДОРОД; КИСЛОРОД.
В жидком аммиаке щелочные металлы растворяются, образуя голубые растворы, и (в отличие от реакции с водой) могут быть выделены снова при испарении аммиака или добавлении соответствующей соли (например, NaCl из его аммиачного раствора). При реакции с газообразным аммиаком реакция протекает подобно реакции с водой:Амиды щелочных металлов проявляют основные свойства подобно гидроксидам. Большинство соединений щелочных металлов, кроме некоторых соединений лития, хорошо растворимы в воде. По атомным размерам и зарядовой плотности литий близок к магнию, поэтому свойства соединений этих элементов похожи. По растворимости и термической устойчивости карбонат лития подобен карбонатам магния и бериллия элементов подгруппы IIA; эти карбонаты разлагаются при относительно невысоких температурах вследствие более прочной связи МО. Соли лития лучше растворимы в органических растворителях (спиртах, эфирах, нефтяных растворителях), чем соли других щелочных металлов.
 Литий (как и магний) непосредственно реагирует с азотом, образуя Li3N (магний образует Mg3N2), тогда как натрий и другие щелочные металлы могут образовывать нитриды только в жестких условиях. Металлы подгруппы IA реагируют с углеродом, но наиболее легко протекает взаимодействие с литием (очевидно, благодаря его малому радиусу) и наименее легко с цезием. И наоборот, активные щелочные металлы непосредственно реагируют с СО, образуя карбонилы (например, K(CO)x), а менее активные Li и Na только в определенных условиях.
Литий (как и магний) непосредственно реагирует с азотом, образуя Li3N (магний образует Mg3N2), тогда как натрий и другие щелочные металлы могут образовывать нитриды только в жестких условиях. Металлы подгруппы IA реагируют с углеродом, но наиболее легко протекает взаимодействие с литием (очевидно, благодаря его малому радиусу) и наименее легко с цезием. И наоборот, активные щелочные металлы непосредственно реагируют с СО, образуя карбонилы (например, K(CO)x), а менее активные Li и Na только в определенных условиях.
Применение. Щелочные металлы применяются как в промышленности, так и в химических лабораториях, например для синтезов. Литий используется для получения твердых легких сплавов, отличающихся, однако, хрупкостью. Большие количества натрия расходуются для получения сплава Na4Pb, из которого получают тетраэтилсвинец Pb(C2H5)4 антидетонатор бензинового топлива. Литий, натрий и кальций используются как компоненты мягких подшипниковых сплавов. Единственный и поэтому подвижный электрон на внешнем слое делает щелочные металлы прекрасными проводниками тепла и электричества. Сплавы калия и натрия, сохраняющие жидкое состояние в широком интервале температур, применяют как теплообменную жидкость в некоторых типах ядерных реакторов и благодаря высоким температурам в ядерном реакторе используются для производства пара. Металлический натрий в виде подводящих электрических шин используется в электрохимической технологии для передачи токов большой мощности. Гидрид лития LiH является удобным источником водорода, выделяющегося в результате реакции гидрида с водой. Литийалюминийгидрид LiAlh5 и гидрид лития используются в качестве восстановителей в органическом и неорганическом синтезе. Благодаря малому ионному радиусу и соответственно высокой зарядовой плотности литий активен в реакциях с водой, поэтому соединения лития сильно гигроскопичны, и хлорид лития LiCl используется для осушки воздуха при эксплуатации приборов. Гидроксиды щелочных металлов сильные основания, хорошо растворимые в воде; они применяются для создания щелочной среды. Гидроксид натрия как наиболее дешевая щелочь находит широкое применение (только в США ее расходуется в год более 2,26 млн.
Сплавы калия и натрия, сохраняющие жидкое состояние в широком интервале температур, применяют как теплообменную жидкость в некоторых типах ядерных реакторов и благодаря высоким температурам в ядерном реакторе используются для производства пара. Металлический натрий в виде подводящих электрических шин используется в электрохимической технологии для передачи токов большой мощности. Гидрид лития LiH является удобным источником водорода, выделяющегося в результате реакции гидрида с водой. Литийалюминийгидрид LiAlh5 и гидрид лития используются в качестве восстановителей в органическом и неорганическом синтезе. Благодаря малому ионному радиусу и соответственно высокой зарядовой плотности литий активен в реакциях с водой, поэтому соединения лития сильно гигроскопичны, и хлорид лития LiCl используется для осушки воздуха при эксплуатации приборов. Гидроксиды щелочных металлов сильные основания, хорошо растворимые в воде; они применяются для создания щелочной среды. Гидроксид натрия как наиболее дешевая щелочь находит широкое применение (только в США ее расходуется в год более 2,26 млн. т).
т).
Литий. Самый легкий металл, имеет два стабильных изотопа с атомной массой 6 и 7; более распространен тяжелый изотоп, его содержание составляет 92,6% от всех атомов лития. Литий был открыт А.Арфведсоном в 1817 и выделен Р.Бунзеном и А.Матисеном в 1855. Он используется в производстве термоядерного оружия (водородная бомба), для увеличения твердости сплавов и в фармацевтике. Соли лития применяют для увеличения твердости и химической стойкости стекла, в технологии щелочных аккумуляторных батарей, для связывания кислорода при сварке.
Натрий. Известен с древности, выделил его Х.Дэви в 1807. Это мягкий металл, широко применяются такие его соединения, как щелочь (гидроксид натрия NaOH), пищевая сода (бикарбонат натрия NaHCO3) и кальцинированная сода (карбонат натрия Na2CO3). Находит применение и металл в виде паров в неярких газоразрядных лампах уличного освещения.
Калий. Известен с древности, выделил его также Х.Дэви в 1807. Соли калия хорошо известны: калиевая селитра (нитрат калия KNO3), поташ (карбонат калия K2CO3), едкое кали (гидроксид калия KOH) и др. Металлический калий также находит различное применение в технологии теплообменных сплавов.
Металлический калий также находит различное применение в технологии теплообменных сплавов.
Рубидий был открыт методом спектроскопии Р.Бунзеном в 1861; содержит 27,85% радиоактивного рубидия Rb-87. Рубидий, как и другие металлы подгруппы IA, химически высокоактивен и должен храниться под слоем нефти или керосина во избежание окисления кислородом воздуха. Рубидий находит разнообразное применение, в том числе в технологии фотоэлементов, радиовакуумных приборов и в фармацевтике.
Цезий. Соединения цезия широко распространены в природе, обычно в малых количествах совместно с соединениями других щелочных металлов. Минерал поллуцит силикат содержит 34% оксида цезия Cs2O. Элемент был открыт Р.Бунзеном методом спектроскопии в 1860. Основным применением цезия является производство фотоэлементов и электронных ламп, один из радиоактивных изотопов цезия Cs-137 применяется в лучевой терапии и научных исследованиях.
Франций. Последний член семейства щелочных металлов франций настолько радиоактивен, что его нет в земной коре в более чем следовых количествах. Сведения о франции и его соединениях основаны на исследовании ничтожного его количества, искусственно полученного (на высокоэнергетическом ускорителе) при a-распаде актиния-227. Наиболее долгоживущий изотоп 22387Fr распадается за 21 мин на 22388Ra и b-частицы. Согласно приблизительной оценке, металлический радиус франция составляет 2,7 . Франций обладает большинством свойств, характерных для других щелочных металлов, и отличается высокой электронодонорной активностью. Он образует растворимые соли и гидроксид. Во всех соединениях франций проявляет степень окисления I.
Сведения о франции и его соединениях основаны на исследовании ничтожного его количества, искусственно полученного (на высокоэнергетическом ускорителе) при a-распаде актиния-227. Наиболее долгоживущий изотоп 22387Fr распадается за 21 мин на 22388Ra и b-частицы. Согласно приблизительной оценке, металлический радиус франция составляет 2,7 . Франций обладает большинством свойств, характерных для других щелочных металлов, и отличается высокой электронодонорной активностью. Он образует растворимые соли и гидроксид. Во всех соединениях франций проявляет степень окисления I.Энциклопедия Кольера. — Открытое общество. 2000.
- ИНЕРТНЫЕ ГАЗЫ
- ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ
Нужно решить контрольную?
Полезное
| SPECULATIVE SCIENCE Литий — один из самых легких элементов, легче кислорода, но твердый. Майкл Андерсон, Лондон
| ||||||||||||||||||||||||||||
Легкие металлические композитные поплавки на воде
Легкие композиционные материалы с полимерной матрицей все чаще используются для замены материалов на основе металлов для снижения веса промышленных изделий, особенно автомобилей и самолетов. Однако большинство композитов с полимерной матрицей могут выдерживать температуры только 150°C или ниже, что делает их непригодными для компонентов двигателя и выхлопной системы.
Однако теперь композит с магниевой матрицей, изобретенный исследователями Политехнической инженерной школы Нью-Йоркского университета в сотрудничестве с Deep Springs Technology и Военной исследовательской лабораторией, может обратить эту тенденцию обратно в сторону металлических композитов. Новый материал примечателен по нескольким параметрам: он не только достаточно легкий, чтобы плавать на воде, но и такой же прочный, как и другие композитные материалы, используемые сегодня, и может выдерживать температуры свыше 400°C.
Новый материал примечателен по нескольким параметрам: он не только достаточно легкий, чтобы плавать на воде, но и такой же прочный, как и другие композитные материалы, используемые сегодня, и может выдерживать температуры свыше 400°C.
Карбид кремния имеет значение
Под руководством Нихила Гупты, адъюнкт-профессора машиностроения и аэрокосмической инженерии Политехнической инженерной школы Нью-Йоркского университета в Бруклине, исследовательская группа из его отдела и Deep Springs Technology разработала новый материал из матрицы из магниевого сплава, известный как AZ91D, литой магний. сплав, содержащий 9 весовых процентов алюминия, 1 весовой процент цинка, 0,3 весовых процента марганца.
Магниевые сплавы обладают огромным потенциалом для чувствительных к весу приложений, особенно в автомобильной, аэрокосмической, оборонной и электронной промышленности. Хотя магний является многообещающим металлом с низкой плотностью, несколько лет назад возникли первоначальные опасения по поводу воспламеняемости и проблем с обработкой. Однако новые магниевые сплавы и методы обработки решили эти проблемы. Полые сферы из карбида кремния. Изображение: Нихил Гупта / NYU Polytechnic School of Engineering
Однако новые магниевые сплавы и методы обработки решили эти проблемы. Полые сферы из карбида кремния. Изображение: Нихил Гупта / NYU Polytechnic School of Engineering
Плотность нового композитного материала с магниевой матрицей составляет всего 0,92 грамма на кубический сантиметр по сравнению с плотностью воды 1,0 г/куб. см, что означает, что он будет плавать на воде.
«Испытания его высокотемпературных свойств показывают, что механические свойства сохраняются примерно до 400°C», — заявляет Гупта. «Кроме того, прочность на сжатие при низкой и высокой скорости деформации сравнима с другими существующими матричными композитами из алюминия и магния, которые имеют плотность в диапазоне от 1,2 до 1,5 г/см3».
Секрет этой прочности заключается в полых частицах карбида кремния, которые были разработаны и изготовлены компанией DST. Внешняя оболочка отдельной частицы может выдержать давление, превышающее 25 000 фунтов на квадратный дюйм, прежде чем разорвется, что в сто раз превышает максимальное давление в пожарном шланге. Полые частицы также обеспечивают защиту от ударов, поскольку каждая оболочка (если она выходит из строя) поглощает часть энергии удара.
Полые частицы также обеспечивают защиту от ударов, поскольку каждая оболочка (если она выходит из строя) поглощает часть энергии удара.
«Одной из самых сложных задач было определение оптимальной концентрации частиц», — говорит Гупта. «Частицы, которые были смешаны в больших количествах в матрице, имели тенденцию разрушаться, что приводило к более высокой, чем ожидалось, плотности. С другой стороны, чем меньше частиц используется, тем выше плотность материала».
Композит можно настроить по плотности и другим свойствам, добавив больше или меньше оболочек в металлическую матрицу в соответствии с требованиями приложения.
Будущие приложения
Этот новый композитный материал с магниевой матрицей является прочным, термостойким и легче воды. Например, лодка из этого материала не утонет, даже если ее конструкция будет повреждена.
«Это первый случай, когда кому-либо удалось добиться такой низкой плотности композиционного материала с металлической матрицей», — говорит Гупта. Он также достаточно прочен, чтобы выдерживать суровые условия эксплуатации, что делает его привлекательным для настила лодок, автомобильных деталей, модулей плавучести и оборонных приложений, таких как броня транспортных средств.
Он также достаточно прочен, чтобы выдерживать суровые условия эксплуатации, что делает его привлекательным для настила лодок, автомобильных деталей, модулей плавучести и оборонных приложений, таких как броня транспортных средств.
Новый композитный материал Гупты может быть готов к испытаниям прототипа всего через три года. Поиск приложений для военной техники является первоочередной задачей. Например, более новые или экспериментальные платформы, такие как сверхтяжелый амфибийный соединитель (UHAC), могут особенно выиграть от легких металлических материалов. Однако, отмечает Гупта, предстоит еще много исследований, в том числе определение подходящей термообработки для дальнейшего улучшения механических свойств, эксперименты с различными типами частиц в композите и определение коррозионной стойкости.
«Хотя плотность и важна, но это лишь малая часть большого набора свойств, определяющих применимость материала в любых промышленных целях», — говорит Гупта. «Прочность, пластичность, модуль упругости, коррозионная стойкость и многие другие свойства могут иметь отношение к фактическому применению. Мы также будем стремиться расширить границы как можно большего количества этих объектов».
Мы также будем стремиться расширить границы как можно большего количества этих объектов».
Марк Кроуфорд — независимый писатель.
Впервые кому-либо удалось добиться такой низкой плотности композитного материала с металлической матрицей. Проф. Нихил Гупта, Инженерная политехническая школа Нью-Йоркского университета
Плотность
Плотность4-4 Плотность
Плотность — это количество вещества в данной единице объема. Его можно измерить в граммах. на кубический сантиметр (г/см 3 ). Это мера того, насколько плотно упакованы атомы вещества. Когда мы говорим, что лед менее плотный чем вода, мы имеем в виду, что молекулы воды более плотно упакованы, когда они находятся в жидком состоянии. Формула для определения плотности:
или же
Всегда можно услышать, что мышцы плотнее жира.
Это означает, что я могу тренироваться, не худеть и при этом терять лишние сантиметры. мою талию. Это потому, что 1 фунт
мышц займет меньше места, чем 1 фунт жира.
мою талию. Это потому, что 1 фунт
мышц займет меньше места, чем 1 фунт жира.
Масса обычно измеряется в граммах. Объем обычно измеряется в мл, что соответствует см 3 (или кубические сантиметры cc. 1 мл = 1 см 3 = 1 см3)
Плотность воды 1,00 г/мл. Плотность некоторых общих элементов показана ниже:
Плотность выбранных элементов
элемент | плотность (г/см 3 ) | внешний вид |
алюминий | 2,70 | серебристый белый, металлик |
сурьма | 6,68 | серебристый белый, металлик |
кадмий | 8,64 | серебристый белый, металлик |
углерод (графит) | 2,25 | черный, тупой |
хром | 7. | сталь серый, твердый |
кобальт | 8,9 | серебристый серый, металлик |
Медь Золото | 8,92 19,3 | красноватый, металлический желтый, металлический |
железо | 7,86 | серебро , металлический |
свинец | 11,3 | серебристо-голубоватый белый, мягкий, металлик |
марганец | 7. | серый розовый, металлик |
Никель Платина | 8,9 21,4 | серебро , металлический серебро, металлический |
кремний | 2,32 | сталь серый, кристаллический |
серебро | 10,5 | серебро , металлический |
банка (серый) | 5,75 | серый |
банка (белый) | 7,28 | белый металлический |
Цинк | 7,14 | голубоватый белый, металлик |
Пример задачи: Твердое тело имеет массу 128 г. Это
представляет собой прямоугольное тело размером 1,0 см на 2,0 см на 3,0 см.
Какова плотность твердого тела и что это за металл?
Это
представляет собой прямоугольное тело размером 1,0 см на 2,0 см на 3,0 см.
Какова плотность твердого тела и что это за металл?
Объем = длина x ширина x высота = 1 см x 2 см x 3 см = 6 см 3 или 6 мл.
D= M/V = 128 г / 6 мл= 21,4 г/мл
Металл должен быть платиновым!
Можно видеть полезность плотностей для определения видов металлов на этом сайте:
http://www.24carat.co.uk/densityofgoldandothermetals.html
Какой элемент легче воды? Разъяснено в блоге часто задаваемых вопросов
Последнее обновление: 30 мая 2022 г.
Этот вопрос время от времени задают наши эксперты. Теперь у нас есть полное подробное объяснение и ответ для всех, кто заинтересован!
Вопрос задан: Девонте Ланг
Оценка: 4,3/5 (72 голоса)
Самым легким или наименее плотным металлом, который является чистым элементом, является литий , плотность которого составляет 0,534 г/см3. Это делает литий почти вдвое менее плотным, чем вода, поэтому, если бы литий не был таким реакционноспособным, кусок металла плавал бы в воде.
Это делает литий почти вдвое менее плотным, чем вода, поэтому, если бы литий не был таким реакционноспособным, кусок металла плавал бы в воде.
Кальций легче воды?
Образующиеся пузырьки прилипают к поверхности металлического кальция и делают ее легче . Поэтому кальций плавает на воде.
Плотность какого металла меньше плотности воды?
литий, натрий и калий имеют меньшую плотность, чем вода, поэтому они плавают на поверхности воды. металлы движутся по поверхности воды и шипят, когда образуется газообразный водород.
Мг легче воды?
Плотность нового композитного материала с магниевой матрицей составляет всего 0,92 грамма на кубический сантиметр по сравнению с плотностью воды 1,0 г/куб. см, что означает, что он будет плавать на воде.
Какие щелочные металлы легче воды?
Примечание. Щелочные металлы энергично реагируют с водой с образованием гидроксида металла и газообразного водорода. Литий реагирует менее энергично, чем натрий и калий, натрий и калий также легче воды и взрывоопасно реагируют с водой. -литий наименее реакционноспособен среди всех щелочных металлов.
-литий наименее реакционноспособен среди всех щелочных металлов.
Плотнее, чем вы думаете — научный эксперимент
Найдено 19 связанных вопросов
Титан легче алюминия?
Титан высоко ценится в металлургической промышленности за его высокую прочность на растяжение, а также малый вес, коррозионную стойкость и способность выдерживать экстремальные температуры. Он крепок как сталь, но на 45 % легче и в два раза прочнее алюминия, но только на 60 % тяжелее.
Какой самый легкий металл на земле?
Литий считается самым легким или наименее плотным металлом на земле с плотностью 0,534 г/см 3 .
Алюминий легче воды?
В своей обычной форме алюминий плотнее воды . Алюминиевая ложка опустится на дно, если ее бросить в воду. … Материал имеет плотность всего 0,61 грамма на кубический сантиметр, в отличие от обычной плотности алюминия 2,7 грамма на кубический сантиметр.
Меркурий легче воды?
Ртуть — очень плотный, тяжелый серебристо-белый металл, который при комнатной температуре является жидкостью. Ртуть имеет плотность 13,5 г/мл, что примерно в 13,5 раз плотнее воды (1,0 г/мл), поэтому такое небольшое количество ртути кажется неожиданно тяжелым. …
Какой металл имеет низкую плотность?
При стандартных условиях литий является самым легким металлом и наименее плотным твердым элементом.
Какой металл самый легкий и прочный?
Новый Сплав на основе магния как самый прочный и легкий металл в мире, который изменит мир. Исследователи из Университета штата Северная Каролина разработали материал с использованием магния, который легкий, как алюминий, но такой же прочный, как титановые сплавы. Этот материал имеет самое высокое отношение прочности к весу, известное человечеству.
Является ли ртуть самым легким металлом?
Его атомный номер 82. Он имеет символ Pb и его атомный вес 207,2 ед. Итак из всего вышеперечисленного самый легкий металл это Литий с атомным весом 6,941 ед., поэтому вариант С верен. Дополнительная информация: — Ртуть широко известна как ртуть, а ранее называлась гидраргирум.
Итак из всего вышеперечисленного самый легкий металл это Литий с атомным весом 6,941 ед., поэтому вариант С верен. Дополнительная информация: — Ртуть широко известна как ртуть, а ранее называлась гидраргирум.
Почему калий легче воды?
Два других металлических элемента имеют меньшую плотность, чем вода. Калий имеет плотность 0,862 г/см 90 258 3 90 259, а натрий имеет плотность 0,971 г/см 90 258 3 90 259 . Все остальные металлы периодической таблицы тяжелее воды. Хотя литий, калий и натрий достаточно легкие, чтобы плавать на воде, они также имеют высокореактивный .
Какой металл самый тяжелый?
Самым тяжелым металлом является осмий , который почти в два раза тяжелее свинца. Удельный вес золота составляет около 19 1/4, а осмия — почти 22 1/2.
Натрий легче фосфора?
Утверждение 1: Натрий имеет наибольший атомный радиус в период после аргона. Утверждение 2: Натрий легче фосфора .
Какие металлы легче алюминия?
Магний . Всплеск интереса за последнее десятилетие показал, как магниевые сплавы и методы нанесения покрытий могут максимально использовать его привлекательные свойства: магний чрезвычайно легкий: он на 75 % легче стали, на 50 % легче титана и на 33 % легче алюминия. .
Всплеск интереса за последнее десятилетие показал, как магниевые сплавы и методы нанесения покрытий могут максимально использовать его привлекательные свойства: магний чрезвычайно легкий: он на 75 % легче стали, на 50 % легче титана и на 33 % легче алюминия. .
Почему лед легче воды?
Когда вода замерзает, молекулы воды образуют кристаллическую структуру, поддерживаемую водородными связями. … Лед менее плотный, чем вода , потому что ориентация водородных связей заставляет молекулы отталкиваться дальше друг от друга , что снижает плотность.
Является ли алюминий самым легким металлом?
Первыми семью металлами в периодической таблице являются литий, бериллий, натрий, магний, алюминий, калий и кальций, известные под общим названием « самый легкий металл ».
Мел легче воды?
Обратите внимание, что меловой порошок не легче, а тяжелее воды . Кроме того, он нерастворим в воде. Таким образом, когда меловой порошок смешивается с водой, то, будучи более тяжелым, он оседает на дно.
Почему лед легче воды класса 9?
Полный ответ:
Лед твердый, поэтому он плавает на воде потому что молекулы воды расширяются при замерзании и образуют открытую структуру, подобную клетке. Это приводит к уменьшению плотности льда. Это означает, что для данной массы лед будет иметь больший объем по сравнению с жидкой водой. Таким образом, более легкий лед плавает по воде.
Какой металл самый прочный в мире?
Вольфрам обладает самой высокой прочностью на растяжение среди всех чистых металлов – до 500 000 фунтов на квадратный дюйм при комнатной температуре. Даже при очень высоких температурах свыше 1500°C он обладает высочайшей прочностью на растяжение. Однако металлический вольфрам хрупок, что делает его менее пригодным для использования в чистом виде.
Какой металл легче воздуха?
Микрорешетка из никель-фосфорного сплава является самым легким металлом, поскольку состоит из полых трубок. Это воздух на 99,99%!
Какой металл самый мягкий?
* Цезий — самый мягкий металл с твердостью по шкале Мооса 0,2.
Титан легче нержавеющей стали?
Титан на 40% легче стали и обладает большей прочностью, чем большинство сплавов из нержавеющей стали серии 300. … В отличие от большинства стальных сплавов, титан не подвержен охрупчиванию при очень низких криогенных температурах.
Плотность | Общая наука | Visionlearning
- Закладка
- Глоссарий терминов
Где-то около 250 г. до н.э. греческий математик Архимед получил задание определить, не обманул ли ремесленник царя Сиракуз, заменив часть золота в царской короне серебром. Архимед думал о проблеме, отдыхая в бассейне. Войдя в бассейн, он заметил, что вода переливается через борта бассейна. У Архимеда был момент прозрения. Он понял, что количество пролитой воды было равно по объему пространству, которое занимало его тело. Этот факт внезапно дал ему метод отличить смешанную серебряную и золотую корону от короны из чистого золота. Поскольку мера серебра занимает больше места, чем эквивалентная мера золота, Архимед поместил корону ремесленника и корону из чистого золота эквивалентной массы в два сосуда с водой. Он обнаружил, что больше воды пролилось по бокам ванны, когда корона мастера была погружена в воду. Выяснилось, что мастер обманывал короля! Легенда гласит, что Архимед был так взволнован своим открытием, что пробежал голым по улицам Сицилии с криками «Эврика! Эврика!» (греческое слово «Я нашел это!»).
Он обнаружил, что больше воды пролилось по бокам ванны, когда корона мастера была погружена в воду. Выяснилось, что мастер обманывал короля! Легенда гласит, что Архимед был так взволнован своим открытием, что пробежал голым по улицам Сицилии с криками «Эврика! Эврика!» (греческое слово «Я нашел это!»).
Что такое плотность?
Архимед использовал концепцию плотности, чтобы разоблачить мошенничество. Плотность — это физическое свойство материи, выражающее отношение массы к объему. Чем больше массы предмет содержит в данном пространстве, тем он плотнее. Однако важно помнить, что эта взаимосвязь заключается не только в том, насколько плотно упакованы атомы элемента или молекулы соединения. На плотность также влияет атомная масса элемента или соединения. Поскольку разные вещества имеют разную плотность, измерение плотности является полезным средством идентификации веществ.
Например, как вы могли бы отличить метрическую тонну перьев от метрической тонны кирпичей, показанных на рисунке 1, если бы вы их не видели?
Рисунок 1: Кирпичи и перья.
Одна метрическая тонна перьев или кирпичей будет иметь одинаковую массу 1000 килограммов (одна метрическая тонна). Однако метрическая тонна перьев займет объем почти 400 миллионов см 90 258 3 90 259 (размером примерно четыре тягача с прицепом), а метрическая тонна кирпичей займет всего полмиллиона см 9 .0258 3 (размером с большой телевизор). Кирпичи плотнее перьев, потому что их масса упакована в меньший объем. Это соотношение между массой и объемом вещества определяет физическое свойство плотности:
Плотность = масса/объем
Плотность определяется как отношение массы объекта к его объему, как показано в уравнении выше. Поскольку это отношение, плотность материала остается неизменной независимо от того, сколько этого материала присутствует. Поэтому плотность называется интенсивное свойство материи. Масса — это количество вещества, содержащегося в объекте, и обычно измеряется в граммах (г). Объем — это количество пространства, занимаемое количеством материи, и обычно выражается в кубических сантиметрах (см 90 258 3 90 259) или в миллилитрах (мл) (1 см 90 258 3 90 259 = 1 мл). Таким образом, общепринятыми единицами измерения плотности являются граммы на миллилитр (г/мл) и граммы на кубический сантиметр (г/см 3 ).
Таким образом, общепринятыми единицами измерения плотности являются граммы на миллилитр (г/мл) и граммы на кубический сантиметр (г/см 3 ).
Давайте рассмотрим пример. Типичный кирпич имеет массу 2268 г и занимает объем 1230 см 3 . Используя приведенное выше уравнение, мы можем рассчитать плотность кирпича:
Плотность кирпич = Масса кирпич / Объем кирпич
Плотность кирпич = 2,268 г/1,230 см 3
Плотность кирпич = 1,84 г/см 3
Плотность иногда можно спутать в нашем сознании с весом, потому что более плотный из двух объектов одинакового объема будет тяжелее. Помните, однако, что именно соотношение между массой и объемом определяет плотность, а не только объем или массу, или даже то, насколько плотно упакованы атомы или молекулы. Посмотрите на таблицу 1 для примеров плотности обычных веществ.
| Плотность некоторых обычных веществ | ||
| Вещество | Плотность (г/см 3 ) | |
| Воздух | 0,0013 | |
| Перья | 0,0025 | |
| Сосна | 0,5 | 908:45|
| Лед | 0,92 | |
| Вода | 1,00 | |
| Кирпичи | 1,84 | |
| Алюминий | 2,70 | |
| Сталь | 7,80 | |
| Серебро | 10,50 | |
| Золото | 19,30 | |
Таблица 1: Плотность обычных веществ.
Контрольно-пропускной пункт понимания
Одна метрическая тонна перьев и одна метрическая тонна кирпичей имеют
- а. тот же объем разной плотности.
- б. та же масса, но другой объем.
Плавучесть
Когда Архимед вошел в свой бассейн для купания, он не только осознал, что вода переливается через края, но и заметил то, что мы все замечаем, когда плаваем, — ему стало легче. Способность объекта «плавать», когда он помещен в жидкость, называется выталкивающей силой и связана с плотностью. Если объект менее плотный, чем жидкость, в которой он находится, он будет плавать. Если он более плотный, чем жидкость, он утонет.
Эта концепция объясняет, почему одни объекты плавают на воде, а другие тонут. Например, большинство видов древесины плавают на воде, потому что они менее плотные; сталь, напротив, тонет, потому что она плотнее воды. Как же тогда большие стальные круизные лайнеры могут оставаться на плаву? В больших кораблях огромное количество пространства, заполненного воздухом (вдумайтесь: каюты, кинотеатры, бортовые казино и т. д.). В то время как сталь плотнее воды, воздух намного менее плотный, чем вода (см. Таблицу 1). Металлические корабли могут плавать, потому что их общая плотность — сталь плюс воздух — меньше, чем у воды, по которой они плавают. Когда металлический корпус корабля пробивает пробоину, например, когда Титаник столкнулся с айсбергом, вода устремляется внутрь и заменяет воздух в корпусе корабля. В результате общая плотность корабля меняется и заставляет корабль тонуть.
Например, большинство видов древесины плавают на воде, потому что они менее плотные; сталь, напротив, тонет, потому что она плотнее воды. Как же тогда большие стальные круизные лайнеры могут оставаться на плаву? В больших кораблях огромное количество пространства, заполненного воздухом (вдумайтесь: каюты, кинотеатры, бортовые казино и т. д.). В то время как сталь плотнее воды, воздух намного менее плотный, чем вода (см. Таблицу 1). Металлические корабли могут плавать, потому что их общая плотность — сталь плюс воздух — меньше, чем у воды, по которой они плавают. Когда металлический корпус корабля пробивает пробоину, например, когда Титаник столкнулся с айсбергом, вода устремляется внутрь и заменяет воздух в корпусе корабля. В результате общая плотность корабля меняется и заставляет корабль тонуть.
Концепция изменения плотности обычно используется на судах другого типа — подводных лодках. Подводная лодка имеет постоянный объем, но она может изменять свою массу, набирая воду в балластные цистерны. При наборе воды в балластные цистерны масса (и, следовательно, плотность) подводной лодки увеличивается, и подводная лодка приобретает отрицательную плавучесть, что позволяет ей погружаться в океанские глубины. И наоборот, когда вода сбрасывается из балластных цистерн, плотность судна уменьшается, позволяя ему всплыть.
При наборе воды в балластные цистерны масса (и, следовательно, плотность) подводной лодки увеличивается, и подводная лодка приобретает отрицательную плавучесть, что позволяет ей погружаться в океанские глубины. И наоборот, когда вода сбрасывается из балластных цистерн, плотность судна уменьшается, позволяя ему всплыть.
Смешивание материалов различной плотности дает предсказуемые результаты. Вы когда-нибудь замечали, что происходит с бутылкой масла и уксусной заправки для салата, когда ее оставляют стоять на месте после того, как ее встряхнули? Масло поднимется наверх, а уксус осядет на дно бутылки. Это происходит потому, что масло менее плотное, чем уксус. Когда материалы разной плотности соприкасаются друг с другом, их относительная плотность будет определять, как они упорядочиваются. Это явление, когда материалы наслаиваются друг на друга в соответствии со своей плотностью, называется суперпозиция .
Контрольно-пропускной пункт понимания
Круизные лайнеры плавают, потому что
- а.
 Их общая плотность меньше, чем у воды.
Их общая плотность меньше, чем у воды. - б. они сделаны из стали, которая менее плотна, чем вода.
Плотность и другие интенсивные свойства
Плотность материала тесно связана с другими интенсивными свойствами, особенно с температурой (см. наш модуль «Температура»). Многие материалы расширяются при нагревании. Поскольку расширяющийся материал занимает больший объем, его плотность уменьшается. Это явление происходит во всех формах материи: например, в твердых телах, жидкостях и газах. Тесно связанная зависимость между плотностью и температурой объясняет, как работают воздушные шары. Когда воздух внутри воздушного шара нагревается, он расширяется и его плотность уменьшается. Таким образом, воздушный шар приобретает положительную плавучесть по отношению к окружающему его более холодному воздуху и взлетает в небо.
Плотность — это фундаментальное физическое свойство материи. Он обычно используется как средство классификации и идентификации различных материалов. Кроме того, полное понимание концепции плотности имеет решающее значение для строительства кораблей и летательных аппаратов легче воздуха, таких как воздушные шары.
Резюме
Плотность — фундаментальное физическое свойство материи. Этот модуль вводит понятие плотности, объясняет, как рассчитывается плотность, и перечисляет плотности обычных веществ. Обсуждается связь между плотностью и плавучестью. Модуль связывает понятие плотности с эксплуатацией больших кораблей, подводных лодок и воздушных шаров.
Основные понятия
Плотность — это физическое свойство материи, выражающее отношение массы к объему.
Когда материалы разной плотности соприкасаются друг с другом, их плотность определяет порядок их расположения.
Плавучесть объекта определяется его плотностью по отношению к плотности окружающей жидкости.

вода — Почему металлическая лодка плавает?
спросил
Изменено 1 год, 4 месяца назад
Просмотрено 12 тысяч раз
$\begingroup$
Я был в классе, изучая плотность и прочее. Наш учитель сказал нам, что то, что плотнее воды, тонет в воде, а то, что менее плотно, плавает.
Тогда наш учитель спросил нас, почему металлические лодки плавают в воде, хотя они плотнее воды. Это из-за поверхностного натяжения воды? Что-то еще?
Будем признательны за любую помощь.
- вода
- плотность
- плавучесть
- гидростатика
$\endgroup$
5
$\begingroup$
Это потому, что вся лодка вместе с воздухом в лодке легче вытесняемой ею воды.
Например, если небольшая лодка вмещает 1 кубометр воды, то она должна быть тяжелее, чем вес 1 кубометра воды. Это объясняется в этом посте What If здесь.
По той же причине, по которой плавают шары для боулинга (поскольку соленая вода размером с шар для боулинга весит больше), лодки плавают (поскольку общий вес лодки меньше, чем общий вес соленой воды размером с лодку.
$\endgroup$
1
$\begingroup$
Два фактора:
Общая плотность. Лодка бывает не только из металла. Он содержит большое количество пластика и дерева, плотность которых ниже, чем у воды. Вы должны рассчитать общую плотность объекта, а не только металла.
Форма: Если бы лодки были сделаны в удобной форме, они бы обязательно утонули (независимо от дерева и всего прочего). Инженеры разрабатывают лодки так, чтобы они были как можно более плавучими и не тонули. Представьте себе лодку, имеющую крутую V-образную форму с очень узким углом. У этой лодки гораздо больше шансов утонуть, чем у той, которая также имеет V-образную форму, но имеет гораздо более широкий внутренний угол.
Представьте себе лодку, имеющую крутую V-образную форму с очень узким углом. У этой лодки гораздо больше шансов утонуть, чем у той, которая также имеет V-образную форму, но имеет гораздо более широкий внутренний угол.
$\endgroup$
$\begingroup$
Кажется, что они должны утонуть, потому что мы привыкли видеть, как все падает. Но чтобы корабль затонул, он должен оттолкнуть часть воды, которой некуда идти, кроме как вверх. Итак, возникает вопрос: «хочет» ли корабль утонуть больше, чем вода «хочет» не подниматься? Оказывается, от этого как раз зависит, весит ли корабль больше или меньше того количества воды, которое заполнило бы то же пространство. В настоящих кораблях много воздуха, поэтому они весят меньше, чем такой же объем воды, поэтому плавают.
Вот классный эксперимент, который ты мог бы провести. Наполните раковину водой, затем поставьте в нее миску.
Теперь посмотрите, какой вес вы можете положить в чашу, прежде чем она утонет. Можно было даже налить воду в качестве веса. Если вы используете воду, посмотрите, как высоко вода поднимается внутри и снаружи чаши, когда вы добавляете больше воды. Это то же самое или другое?
И кстати, разве не круто, что неважно, глубокая или мелкая вода? Если что-то плавает на глубине 2 футов, оно будет плавать на глубине 2000 футов!
Надеюсь, это имеет смысл.
(Источник)
$\endgroup$
5
$\begingroup$
Смещение. Пока вес судна превышает объем вытесняемой им воды, оно будет оставаться на плаву. Проделайте в нем очень большую дыру.. Айсберг, торпеда или в случае с Costa Concordia Sightseeing, он, скорее всего, утонет. Представьте воздушный шар, наполненный водородом. Он весит меньше, чем объем воздуха, который он вытесняет, поэтому он поднимается. Проделайте дыру в корабле, пораженная область больше не вытесняет воду, но вес судна не изменился.
Проделайте дыру в корабле, пораженная область больше не вытесняет воду, но вес судна не изменился.
$\endgroup$
$\begingroup$
Если вы поместите что-то в воду с большей плотностью, чем вода, оно утонет. Если эта штука со всем, что внутри, имеет меньшую плотность, чем вода, она будет плавать. Из какого материала сделана эта вещь, значения не имеет.
Обычная лодка в основном наполнена воздухом, который намного менее плотный, чем вода, поэтому даже если лодка сделана из свинца, она будет плавать. Если заменить воздух в лодке водой, она утонет.
На дне морей и океанов лежало множество деревянных кораблекрушений. Само по себе это дерево может плавать, но поскольку оно является частью корабля с более высокой плотностью, чем вода, оно все равно утонет.
То же самое и с самой водой. «Тяжелая» вода высокой плотности тонет, а легкая всплывает на поверхность. Пресная вода имеет самую высокую плотность примерно при 4 градусах Цельсия.

 Почему мы не можем построить из него вещи, которые плавают?
Почему мы не можем построить из него вещи, которые плавают? 
 Литий плавает на воде, но стоит далеко позади…
Литий плавает на воде, но стоит далеко позади… Гораздо более интересными были бы калий или натрий, которые оба загорятся.
Гораздо более интересными были бы калий или натрий, которые оба загорятся.
 2
2 2
2