Толуидины — это… Что такое Толуидины?
Толуидины (аминотолуолы, метиланилины, толиламины) — ароматические органические соединения, амминопроизводные толуола. Жидкости или твёрдые вещества, хорошо растворяются в этаноле, диэтиловом эфире, ацетоне, хлороформе, плохо — в воде.
Получение
Физические свойства
Толуидины хорошо растворимы в этаноле, диэтиловом эфире, ацетоне, хлороформе, плохо — в воде. Перегоняются с водяным паром, при хранении на свету в присутствии воздуха, как и анилин, темнеют.
| о-толуидин 2-аминотолуол | м-толуидин 3-аминотолуол | п-толуидин 4-аминотолуол | |
|---|---|---|---|
| Структурная формула | |||
| Температура плавления, °С | -24,4 (α-форма) -14,7 (β-форма) | -31,5 | 44,5-45 |
| Температура кипения, °С | 200,3 | 203,0 | 200,5 |
| Плотность, г/см³ | 0,9984 | 0,9891 | 0,9619 |
| Коэффициент диссоциации, pKα | 9,61 | 9,41 | 8,83 |
| Растворимость в воде, % | 1,59 | — | 0,74 |
| Регистрационный номер CAS | 95-53-4 | 108-44-1 | 106-49-0 |
Химические свойства
Толуидины обладают свойствами ароматических аминов. Легко образуют соли, окисляются, диазотируются, вступают в реакции электрофильного замещения.
Применение
- Для получения аминотолуолсульфокислот, крезолов, азокрасителей, трифенилметановых и сернистых красителей.
- п-толуидин входит в состав ингибиторов коррозии.
- м-толуидин используют для получения 3-хлортолуола.
Физиологическое действие
Сильный яд.
Признаки отравления: чувство жжения в лице, сильная головная боль, поражение органов мочеотделения, кровь и метгемоглобин в моче, задержка выделения мочи, иногда причиняющая сильные боли.
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4. — 639 с. — ISBN 5-82270-092-4
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
dic.academic.ru
Толуидин орто, мета и пара
Толуидин орто. . . мета. . . пара. -. [c.47]Вместо диэтиланилина можно пользоваться диметиланилином, орто-, мета- или пара-толуидинами, мета- или пара-нитроанилинами, а-нафтиламином. При этом образуются красители несколько других оттенков. [c.477]
Орто-мета- и пара-толуидины и анилин. Результаты опытов обмена между толуидинами и разбавленной окисью дейтерия приведены в табл. 6. Полученные данные однозначно указывают на отсутствие обмена ядерных атомов водорода толуидинов (и анилина) на дейтерий из тяжелой воды при катализе основаниями. В этих условиях протекает только быстрый обмен атомов водорода аминогрупп этих соединений. Среднее К в опытах с основным катализатором составляет 2,1, что соответствует коэффициенту распределения дейтерия между атомами водорода N—Н-связей толуидинов и О—Н-связей воды, равному 1,05. Эта величина хорошо согласуется с найденной другими исследователями [17].
НИЯ всех углеводородов ароматического ряда оканчивать суффиксом ен (т. е. не бензол , а бензен это трудно внедряется, но это логично). Разрешено использовать тривиальные названия основных гомологов и производных (толуол, ксилолы, фенол, анилин, толуидины и др.), которые служат основой для наименования более сложных структур. Положение заместителей у дизамещенных производных бензола обозначается с помощью приставок орто, мета- и пара- [c.37]
Так же, как анилин, диазотируют амины, близкие к анилину по строению, — орто-толуидин, пара-толуидин н мета-ксилидин. По этому же способу диазотируют орто-анизидин, крезидин и пара-аминодиметиланилин. Строение этих продуктов приведено в Приложении 5. [c.74]
Анилин СйНаКНз Этил-анилин 8H N Метил-анилин 7H9N Толуидин (орто-, мета-, пара-) [c.506]
Простейшими гомологами анилина являются аминопроизводные толуола СНз— eHi—NHj, называемые толуидинами они существуют в виде орто-, мета- и пара-изомеров [c.385]
Ароматические амины, являющиеся производными толуола и получающиеся путем замещения атома водорода в бензольном ядре на аминогруппу, называются толуидинами СвН4(СНз)НН2. То-луидины существуют в виде трех нзомеров — орто-, мета- и пара-. [c.339]
Толуидины (моноаминотолуолы, толиламины) существуют в трех изомерных формах орто-, мета- и пара-. Их общая формула [c.258]
Как указано в примерах, для простейших, наиболее часто встречающихся соединений используются тривиальные или полутривиаль-ные названия вроде фенол , пара-крезол (но не пара-метилфенол ) орто-толуидин (но не орто-метиланилин ). Для тризамещенных с одинаковыми заместителями используют названия симметричный , несимметричный и рядовой либо вицинальный виц.). Для неодинаковых заместителей используют приставки орто , мета и пара .
Хорошее разделение орто-, мета- и пара-изомеров толуидина достигают методом газоадоорбционной хроматографии на монтмориляояи-тоБой глине, в которой природные неорганические ионы заменены ионами диметилдиоктадециламмония [150], Удерживаемые объемы о-, м-, В Толуидинов равны 1,03, 1,24 и 1,60 соответственно (удельный объем фенола равен I), [c.18]
Анилин образует при действии диазосоединений только диазоаминосоединения, которые в определенных условиях могут превращаться в -ами-ноазосоединения. Орто- и пара-замещенные анилина (о- и и-толуидины, сульфаниловая кислота, антраниловая и т. д.) также образуют диазоаминосоединения. Только Б тех случаях, когда в мета-положении к аминогруппе расположена метильная группа ( -толуидин, и-ксилидин и др.), сочетание проходит нормально с непосредственным образованием /г-аминоазокрасителя. [c.126]
Поэтому в отличие от толуидина в ряду изомерных фенилендиаминов облегчение окисления наблюдается в пара-, орто-, мета-направлении. [c.163]
К условиям диазотирования пара-нитранилина близки условия диазотирования следующих нитраминов орто- и мета-нитр-анилина, мета-иитро-пара-толуидина, пара-хлор-орто-нитранн-лина, орто-хлор-пара-нитранилииа, мета-нитро-орто-анизидина, пара-нитранилин-орто-сульфокислоты. [c.75]
Хотя реакция Скраупа является общим методом получения производных хинолина, однако гомологи и производные анилина обычно реагируют труднее и с меньшим выходом, чем сам анилин. Например, о-толуидин дает 8-метилхинолин с выходом 47% от теоретического, а реакции с нитроанилинами протекают с еще меньшими выходами, В зависимости от химической природы и положения заместителя в анилине получают производные хинолина, замещенные в положениях 5, 6, 7 или 8. Из орто-однозамещенных анилинов получают производные хинолина, замещенные в положении 8, из пара-однозамещенных анилинов—в положении 6. Мета-замещенные анилины дают смесь двух изомерных продуктов реакции, содержащих заместители в положении 5 и 7. Когда мета-заместитель в анилине принадлежит к ориентантам первого рода, образуются пре-
При нагревании ароматических аминов с метиловым спиртом и соляной кислотой в автоклаве до 200 — 250 наблюдается постепенное метилирование ядра, причем СН3 становится преимущественно в пара- и орто-места к азоту. Прн нагревании смеси до более высокой температуры (250 — 300 ) становится более заметной мета-ориеи-тация так, из о-толуидина (I) получается мезидин (II) и некоторое количество изо-дуридина (III) [c.310]
Физические свойства основность. — Наиболее распространенные амины ряда бензола и дифенила приведены в табл. 19. Среди изомерных толуидинов, нитроанилинов и фенилендиаминов симметрично построенные пара-изомеры неизменно имеют наиболее высокие температуры плавления. Метил- и диметиланилин кипят почти при одной и той же температуре, которая лишь немного превышает температуру кипения анилина орто-изомеры в ряду толуидинов, фениленди- [c.226]
Изомеры толуидина на ПЭГ-20М, а также мета- и пара-хлораш-лины не разделяются, а анизидины и нитроанилины разделяются хорошо. Трифторацетилирование, понижая основность толуидинов, позволяет в этих же условиях отделить орто-изомер от мета- и пщ)а-изомеров, разделение которых намечается. Трифторацетилирование меняет порядок выхода изомеров анизидина по сравнению с порад-ком выхода свободвых оснований. [c.50]
В случае орто-толуидина смещение незначительнее, чем в случае с анилином. Слабое влияние СНз-груп-пы в этом случае следует, по-видимому, объяснить нарушением сопряжения за счет пространственных эффектов. Незначительное смещение Е1/, в сторону меньших значений потенциалов объясняется в этом случае индукционным влиянием метильной группы. Как и следовало ожидать, в ряду изомеров толуидина в пара-, мета-, орто-направлении наблюдается незначительное облегчение окислительной способности с переходом из кислой в щелочную обласгь pH. Особенно резко проявляется влияние аминогруппы, введенной в пара-положение в молекулу анилина. В этом случае за счет высоких электронно-до-норных свойств аминогр
www.chem21.info
м-толуидин ⌬ органические растворители на Chemical Region
Синонимы:
м-толуидин, м-аминотолуол, м-метиланилин, з-толуидин T замерзания: -30.40 °СТолуидины характеризуются приблизительно теми же химическими реакциями, что и анилин. Они образуют соли с большинством кислот; в воде они ведут себя как слабые основания, а в уксусной кислоте и в других органических растворителях — как сильные основания. Методы очистки анилина могут быть, как правило, использованы также и в случае толуидинов.
Адкинс и Биллика восстанавливали п-нитротолуол специально приготовленным катализатором (никелем Ренея). (См. раздел, посвященный изопропиловому спирту.)
Берлинер и Мей очищали каждый из трех изомеров толуидина, используя для этого следующие способы.
о-Толуидин. Исходный реактив дважды перегоняли, после чего растворяли в четырехкратном объеме этилового эфира. Для получения диоксалата к раствору добавляли эквивалентное количество эфирного раствора щавелевой кислоты и отделяли образующиеся кристаллы диоксалата п-толуидина фильтрованием. Эфирный раствор упаривали и образующиеся кристаллы чистого Диоксалата о-толуидина отфильтровывали, а затем пять раз пере-кристаллизовывали из воды, в которую предварительно добавляли Для предотвращения гидролиза небольшое количество щавелевой Кислоты. Очищенные кристаллы обрабатывали разбавленным раствором карбоната натрия и амин отделяли; затем его сушили хлористым кальцием и трижды перегоняли при пониженном давлении. Температура кипения составляла 199.84°.
м-Толуидин. Амин дважды перегоняли, а затем нагревали с небольшим избытком соляной кислоты. Образующийся гидрохлорид пять раз подвергали дробной кристаллизации из 95%-ного этилового спирта и два раза из дистиллированной воды. При этом каждый раз отбрасывали часть препарата, которая выкристаллизовывалась первой. Из полученной соли регенерировали амин и три раза перегоняли его так, как это описано выше. Температура кипения была равна 202.86°.
п-Толуидин. Исходный амин три раза перегоняли и дважды сублимировали при 30°. После этого его растворяли в пятикратном объеме этилового эфира и добавляли эквивалентное количество щавелевой кислоты, растворенной в эфире. Отфильтрованные и промытые кристаллы трижды перекристаллизовывали из горячей дистиллированной воды и регенерировали основание раствором карбоната натрия. В заключение амин трижды перекристаллизовывали из дистиллированной воды. Температура плавления составляла 43.5°. Семикратная перекристаллизация из этилового спирта не приводила к изменениям температуры плавления препарата.
Критерии чистоты. Превосходным критерием чистоты толуидинов является их температура плавления. Дрейсбах и Мартин характеризовали чистоту орто- и.мета-соединений по кривой их замерзания. Берлинер и Мей пользовались в качестве критерия чистоты постоянством температуры плавления при многократной перекристаллизации.
Токсикология. В отношении токсических свойств толуидины мало отличаются от анилина.
Дипольный момент:
1.45Диэлектрическая проницаемость:
5.95 при 18 °СПлотность:
0.99302 при 15 CПоказатель преломления:
1.56811 при 20 °Сwww.chemistry.org.ua
метил метиланилин — Справочник химика 21
Так, при взаимодействии метилиодида с диазотатом натрия образуется Л/-нитрозо-Л -метиланилин (88). Реакция протекает по одностадийному механизму 5м2, и, следовательно, диазотат-анион атакует электронодефицитный атом углерода в метил-иодиде атомом азота, обладающим большей нуклеофильной реакционной способностью [c.450]Реакция алкилирования. Атомы водорода в аминогруппе могут замещаться алкильными радикалами в результате образуются вторичные и третичные жирно-ароматические амины. Так, при действии иодистого метила (СНд ) на анилин вначале получается иодистоводородная соль метиланилина ее разлагают щелочью и получают метиланилин [c.389]
К-метил-Ы-хлороанилин, который перегруппировывается (по реакции 11-37) в смесь N-метиланилинов, хлорированных в ароматическое кольцо, среди которых преобладает орго-изомер [170]. [c.347]
Какие общие свойства и различия наблюдаются в следующих парах соединений а) ж-толуидин и Л -метиланилип б) амидогидроксибензойной (салициловой) кислоты и о-аминобензойная (антраниловая) кислота в) N,N-J i -метиланилин и Л -метил-о-толуидин г) /V,//-диэтиланилин и 3,5-диэтиланилин [c.14]
Расположите приведенные ниже соединения в порядке возрастания их скорости взаимодействия с эквимолярным количеством азотистой кислоты а) Ы,Ы-диэтиланилин, ЛГ,Л -диэтил-о-анизидин, Л ,Л -диэтил-2,6-диметиланилин1 б) фенол, о-метоксифенол, о-крезол, о-хлорфенол в) Л/-метиланилин, л-метил-о-толуидин, л-метил-о-хлоранилин. [c.100]
При пропускании хлороводорода в спиртовый раствор смеси Л -метил-Л -фенилнитрозамина и дифениламина получается п-нитрозо-Л -метиланилин и га-ни-трозодифениламин. Предложите возможный механизм образования и-нитрозо-дифениламина. [c.100]
Для каждой пары соединений предложите химические реакции, которые выявили бы а) их различие УУ-метиланилин и п-толуидин, Л -нитрозо-Л -метилани-лин и и-нитрозо-Л -метиланилин, фенокснуксусная кислота и фениловый эфир уксусной кислоты б) их сходство -фенил-З-метил-5-пиразолон и фенол, диазоами-нобензол и Л -нитрозо-Л -метиланилин, iV-нитрозоацетанилид и бензолдиазосуль-фонат. [c.268]
Тетрил. — 2,4,6,Ы-Тетранитро-Ы-метиланилин широко применяется в качестве взрывчатого вещества (сокращенное название — тетрил называется также метил-2,4,6-тринитрофенилнитрамином). В этом соединении одна нитрогруппа присоединена к азоту в результате замещения водорода метиламинной группы [c.209]
З-Нитро-М-метиланилин. При добавлении 20 з метил-(З-нитрофенил)-нитрозамипа к нагретому до 50° С раствору 15 в мочовииы в 75 мл воды и 75 мл На 04 сразу начинается выделение газов (N2v 04 и N0). Реакционную массу нагревают при 100° С еще 15 мин. После охлаждения вторичный амин осаждают аммиаком и перекристаллшовывают из лигроина выход продукта 15,5 г т. пл. 67, 5° С. [c.531]
Впервые получен в 1928 г. в медицине применяют с 1931 г. При синтезе исходят из л-диметилаыинофепола, который получают а) из резорцина н водного раствора днметиламина прн нагревании под давлением, б) из ди-метиланилина. переходя через ж-нитро- и л-аминопроизводные, которые после дназотирования превращают в л-диметиламинофенол или в) из мета-ниловой кислоты, которую вначале метилируют и затем N. Ы-диметилпро- [c.250]
Первоначальный водный слой и кислые вытяжки соединяют вместе, охлажданзт и делают раствор сильно щелочным путем прибавления к нему 450 млАО% -ного раствора едкого натра. Выделившийся М-метиланилин экстрагируют тремя порциями эфира по 200 мл. Эфирные вытяжки соединяют вместе, промывают водой (100 мл), сушат над безводным сернокислым натрием и упаривают. Перегонкой остатка из колбы емкостью200 снабженной елочным дефлегматором высотой 11 см, получают 95,6 г (89% теоретич.) М-метил-анилина г. кип. 96—100° (27 мм)-, 1,5717. [c.476]
Реакция 2,4-дииитрофторбензола с К-метиланилином, приводящая к Ы-метил-2,4-динитродифениламину, катализируется слабыми основаниями типа ацетат-иоиа. Реакция соответствующего бромпроизводиого происходит быстрее и не катализируется основаниями. Как вы объясните эти наблюдения (Указание разберите подробно каждую стадию механизма.) [c.808]
Роданированием о-толуидина синтезирован 2-метил-4-родап-анилин 1575, 579, 582, 584, 606, 626—628, 645]. Из ж-толуидина получен как 4-родан-З-метиланилин [582. 584, 606, 659], так п [c.44]
www.chem21.info
Ароматические амины
Ароматическими аминами называют производные ароматических углеводородов, в которых один или несколько атомов водорода бензольного кольца замещены на аминогруппы (NH2).
Ароматические амины можно также рассматривать как производные аммиака, в молекуле которого один или несколько атомов водорода замещены ароматическими радикалами.
Как и в алифатическом (жирном) ряду, ароматические амины могут быть первичными, вторичными и третичными.
В зависимости от того, какие радикалы (только ароматические или ароматические и алифатические) связаны с атомом азота, различают чисто ароматические и жирноароматические.
Аминогруппа может быть непосредственно связана с ядром или находиться в боковой цепи.
Анилин является родоначальником класса ароматических аминов, в которых аминогруппа непосредственно связана с бензольным кольцом:
анилин (фениламин, аминобензол)
Номенклатура ароматических аминов
Для названия ароматических аминов обычно используют тривиальную номенклатуру.
Например, анилин, толуидин.
По систематической (заместительной) номенклатуре названия аминов образуют из названий радикалов с добавлением окончания –амин или приставки амино- и названия соответствующего углеводорода:
Тривиальная: орто-толуидин мета-толуидин пара-толуидин
Заместительная: орто-толиламин мета-толиламин пара-толиламин
орто-аминотолуол мета-аминотолуол пара-аминотоуол
(2-аминотоуол) (3-аминотолуол) ( 4-аминотолуол)
В ароматическом кольце может быть две и более аминогрупп.
Названия соединений с двумя аминогруппами (диамины) образуют из названия двухвалентного углеродного остатка и окончания –диамин или приставки диамино- и названия соответствующего углеводорода:
о-фенилендиамин м-фенилендиамин п-фенилендиамин
о-диаминобензол м-диаминобензод п-диаминобензол
(1,2-диаминобензол) (1,3-диаминобензол) (1,4-диаминобензол)
В зависимости от числа радикалов, связанных с атомом азота, различают также вторичные и третичные ароматические амины.
Названия вторичных и третичных аминов чаще всего образуют по принципам рациональной номенклатуры, перечисляя имеющиеся в соединении радикалы и добавляя окончание –амин:
дифениламин (вторичный амин)
трифениламин (третичный амин)
Если в молекуле амина с атомом азота связаны одновременно и ароматические и алифатические радикалы, то такие амины называют жирноароматическими.
В случае жирноароматических аминов за основу названия берется слово «анилин» и, чтобы показать, что радикал расположен у атома азота, а не в бензольном кольце, перед названием радикала ставится буква N:
N-метиланилин N,N-диметиланилин
Рациональная: метилфениламин диметилфениламин
Заместительная: N-метиламинобензол N,N-диметиламинобензол
Амины с аминогруппой в боковой цепи:
бензиламин
α-аминотолуол
Ароматические амины с аминогруппой в боковой цепи обладают свойствами алифатических аминов.
studfiles.net
Добавка к бензину и композиция, ее содержащая
Настоящее изобретение относится к области нефтепереработки и нефтехимии, конкретно — к составу октаноповышающей добавки к бензину и композиции, содержащей эту добавку, предназначенной для использования в двигателях внутреннего сгорания. Октаноповышающая добавка к бензину на основе толуидинов и спирта содержит синергетическую композицию смеси мета- и орто-толуидинов, изобутилового спирта и продукта конденсации растительного масла, диэтаноламина и борной кислоты при мольном соотношении компонентов растительного масла, диэтаноламина и борной кислоты 0,75 — 1:3:0,5 — 1 и при следующем соотношении компонентов, масс. %: мета-толуидин — 49-54, орто-толуидин — 24-27, изобутиловый спирт — 16-22, продукт конденсации — 3-5. Композиция на основе бензина содержит октаноповышающую добавку, включающую вышеуказанную добавку в количестве 1-3 об. %. Техническим результатом является разработка добавки для повышения октанового числа и использование добавки с высокими антидетонационными свойствами в составе композиции на основе бензина, создание синергетической композиции, а также получение качественной добавки, не содержащей металлорганических добавок и ММА, в которой используемые бораты имеют аминное число не более 30 мг HCl/г. 2 н.п. ф-лы, 6 табл.
Настоящее изобретение относится к области нефтепереработки и нефтехимии, конкретно — к составу октаноповышающей добавки к бензину и композиции, содержащей эту добавку, предназначенной для использования в двигателях внутреннего сгорания. Добавка к бензину на основе ароматических аминов и спирта включает, масс.%: 49-54 — мета-толуидина, 24-27 — орто-толуидина, 16-22 — изобутилового спирта, 3-5 — продукта конденсации растительного масла, диэтаноламина и борной кислоты при мольном соотношении 0,75-1,0:3:0,5-1.
Композиция на основе бензина содержит вышеуказанную добавку в количестве 1-3% об.
Предлагаемое изобретение относится к добавке, повышающей антидетонационную стойкость углеводородных горючих топлив-бензинов, в частности автомобильных бензинов. Известно, что бензины прямой перегонки состоят из устойчивых углеводородов. Они могут храниться в бензохранилищах без заметного смолообразования. Однако использование таких бензинов в двигателях внутреннего сгорания вызывает детонацию, что способствует преждевременному его износу, уменьшению мощности, увеличению расхода топлива и неполному его сгоранию.
Современные требования к автомобильным бензинам существенно ограничивают возможности улучшения антидетонационных свойств топлива, поскольку предусматривают запрет на применение металлорганических добавок и ограничивают содержание в бензинах высокооктановых ароматических углеводородов. Все присутствующие на рынке РФ октаноповышающие присадки («Каскад3», «Каскад4», «БВД-премиум») в своем составе содержат N-метиланилин (ММА), не позволяющий согласно ГОСТ P5 1105-97 получать бензин марки Регуляр-92 экологического класса 5 и ГОСТ Р5 1866-2002 бензин марки Премиум-95.
С 01.01.2016 года ММА запрещен во всех марках бензина. В связи с этим разработка октаноповышающей добавки, не содержащей ММА, — является актуальной. Наиболее близкой к заявленному техническому решению является добавка к бензину, содержащая, масс.%: 16 — смесь толуидинов, 1,5 — кротоновый альдегид, 2,0 — уксусный альдегид, 0,5 — Фероз (производное дициклопентадиенил железа), этиловый спирт до 100 (Патент RU 2161639 С1, опубл. 10.01.2001, взят в качестве прототипа).
Однако данная добавка из-за содержания металлорганики не может быть использована для повышения октанового числа бензина.
Предлагаемая добавка разработана с целью создания синергетической композиции, не содержащей метиланилин, металлорганические соединения и проявляющей высокую антидетонационную активность, позволяющей выпускать бензины высокого класса. В известном патенте РФ 2161639 сама смесь толуидинов (без указания процентного содержания изомеров) и этилового спирта не показывает высокого антидетонационного эффекта, а только при наличии железосодержащей присадки Фероз и концентрации — 5 масс.%. В заявленном техническом решении указано строгое соотношение мета- и орто-толуидинов для получения нужного синергетического эффекта. Присутствие в составе добавки изобутилового спирта позволяет улучшить растворимость бората и приводит к синергетическому повышению октанового числа.
В известных патентах RU 2355733 С1 (опубл. 20.05.2009), RU 2355734 С1 (опубл. 20.05.2009), RU 2355735 С1 (опубл. 20.05.2009), RU 2400528 С1 (опубл. 27.09.2010) продукты конденсации растительных масел, диэтаноламина и борной кислоты используются в качестве противокоррозионных, моющих добавок к бензину, а также для снижения давления насыщенных паров бензина и потерь бензина от испарения.
Несмотря на то, что детонационная стойкость бензина и его испаряемость тесно связаны между собой, однако точной закономерности такого влияния не выявлено. Использование данных соединений для повышения октанового числа бензина или его стойкости к детонации неизвестно. Кроме того, во всех вышеуказанных патентах получаемые бораты имели аминные числа 60-80 мг HCl/г и при анализе по ГОСТ 6307 на содержание водорастворимых щелочей дают положительную реакцию, что недопустимо при использовании в составе бензина. Кроме того, бораты по патентам RU 2355733 и RU 2355734 имеют высокие показатели по смоле и сере. Авторами настоящей заявки был получен борат согласно патенту RU 2400528. Полученный продукт имел аминное число 75 мг HCl/г и положительную реакцию на водорастворимую щелочь. В техническом решении согласно настоящей заявке аминное число достигается не более 30 мг HCl/г и дает отрицательную реакцию на содержание водорастворимых щелочей. Это является неотъемлемым условием получения качественной добавки.
Задачей настоящего изобретения является разработка добавки для повышения октанового числа и использование добавки с высокими антидетонационными свойствами в составе композиции на основе бензина, создание синергетической композиции, а также получение качественной добавки, не содержащей металлорганических добавок и ММА, в которой используемые бораты имеют аминное число не более 30 мг HCl/г, что дает отрицательную реакцию на содержание водорастворимых щелочей, в отличие от вышеуказанных известных композиций бензина.
Для решения поставленной задачи предлагается октаноповышающая добавка к бензину на основе толуидинов и спирта, которая содержит синергетическую композицию смеси мета- и орто-толуидинов, изобутилового спирта и продукта конденсации растительного масла, диэтаноламина и борной кислоты при мольном соотношении компонентов растительного масла, диэтаноламина и борной кислоты 0,75-1:3:0,5-1 при следующем соотношении компонентов, масс.%: мета-толуидин — 49-54, орто-толуидин — 24-27, изобутиловый спирт — 16-22, продукт конденсации — 3-5.
Предлагается также композиция на основе бензина, содержащая вышеуказанную добавку в количестве 1-3 об.%. Отличием заявляемого технического решения является содержание в составе добавки изобутанола и продукта конденсации растительного масла, диэтаноламина, борной кислоты и соотношения компонентов.
Используемые вещества в составе добавки являются продуктами промышленного производства. Орто- и мета-толуидины применялись по ТУ 6-09-2949-88 с массовой долей основного вещества не менее 99%. Изобутиловый спирт — по ГОСТ 6016.
Предлагаемую октаноповышающую добавку готовят по безотходной технологии с использованием стандартного оборудования путем смешивания компонентов для получения однородного раствора.
В качестве растительного масла используют: подсолнечное, соевое, льняное, оливковое и др. Способ получения продукта конденсации заключается в следующем: на примере соевого масла — в реактор, снабженный ловушкой для воды и термометром, механической мешалкой, загружается один моль соевого масла и три моля диэтаноламина. Реакционную массу нагревают при перемешивании до 100 и добавляют один моль борной кислоты. Температуру поднимают до 180 градусов и выдерживают до получения продукта с аминным числом не более 30 мг HCl/г и растворимым в бензине. Для иллюстрации заявляемого технического решения было подготовлено 2 образца добавки путем смешения компонентов при комнатной температуре и постоянном перемешивании (Таблица 1). Приготовленные образцы были испытаны в составе топливной композиции, содержащей предлагаемую добавку.
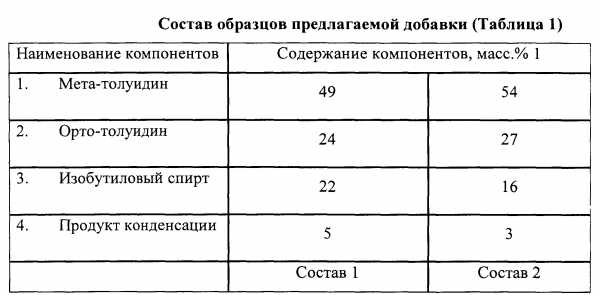
Образец №2 под торговым наименованием «Октаноповышающая добавка «R&T®Octane» выпускается по ТУ 0257-00663538901-2014.
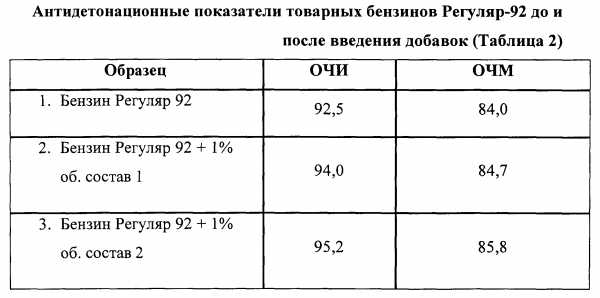

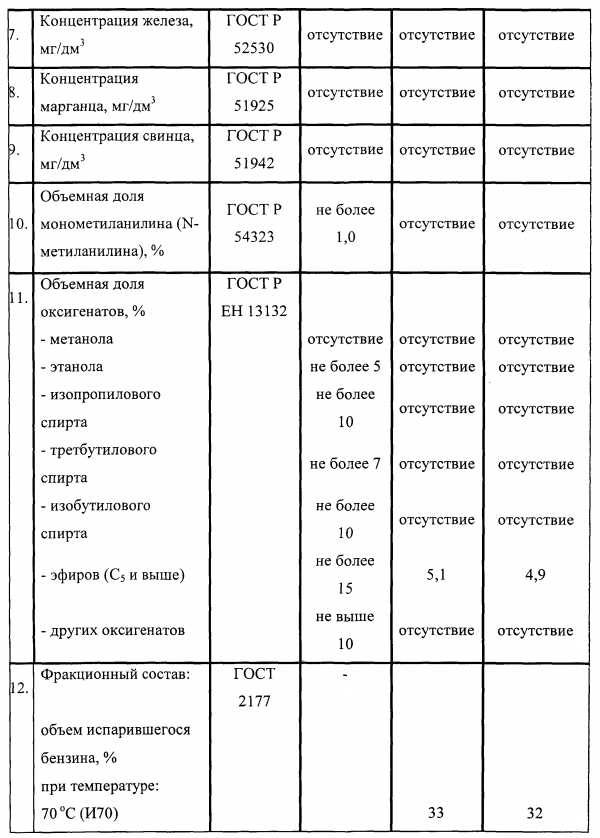
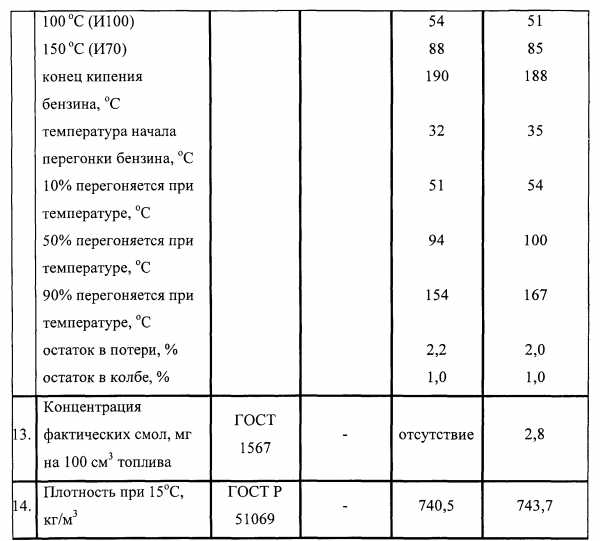
Результаты испытаний, приведенные в Таблицах 2 и 3, показывают высокую эффективность предлагаемой октаноповышающей добавки и позволяют получать бензины класса 5 без ММА.
Кроме того, для иллюстрации настоящего технического решения были также приготовлены образцы предлагаемой добавки и добавки, содержащей борат согласно патенту RU 2400528, состав которых приведен в таблице 4.
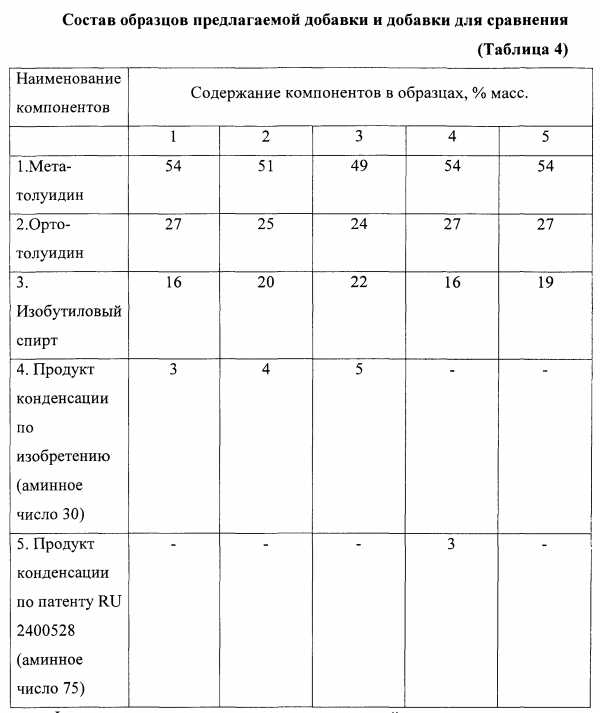
Функциональные и эксплуатационные свойства приготовленных образцов представлены в таблице 5. Влияние добавки на детонационную стойкость оценивалось по АСТМ Д 2700-95 (ГОСТ 511-82) на установке УИТ-85 по приросту октанового числа эталонной смеси «70 изооктана и н-гептана», взятых в соотношении 70:30 (по объему). Чем больше прирост октанового числа, тем выше антидетонационные свойства добавки.
Для испытанных образцов прирост составляет от 4,1 до 4,3 в сравнении с эталонной смесью (добавкой для сравнения).
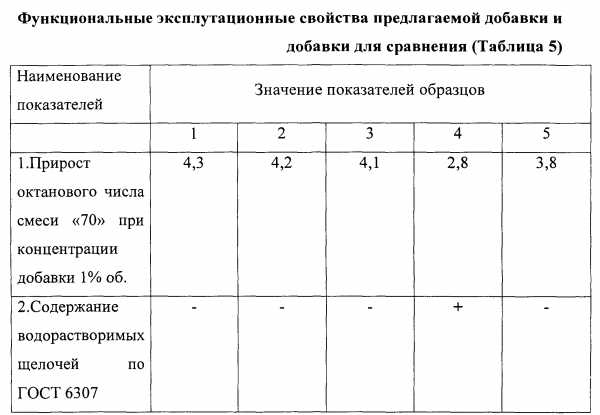
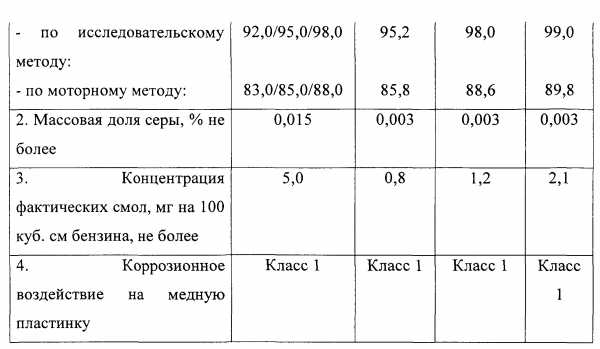
Образец №1 был испытан в составе бензинов. Физико-химические показатели представлены в таблице 6.
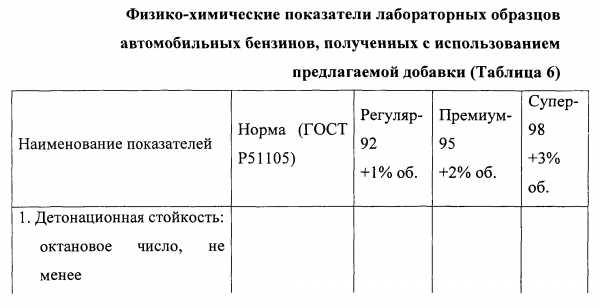
1. Октаноповышающая добавка к бензину на основе толуидинов и спирта, отличающаяся тем, что содержит синергетическую композицию смеси мета- и орто-толуидинов, изобутилового спирта и продукта конденсации растительного масла, диэтаноламина и борной кислоты при мольном соотношении компонентов растительного масла, диэтаноламина и борной кислоты 0,75 — 1:3:0,5 — 1 и при следующем соотношении компонентов, масс. %: мета-толуидин — 49-54, орто-толуидин — 24-27, изобутиловый спирт — 16-22, продукт конденсации — 3-5.
2. Композиция на основе бензина, содержащая октаноповышающую добавку, отличающаяся тем, что она содержит добавку по п. 1 в количестве 1-3 об. %.
findpatent.ru
Метиланилин, свойства — Справочник химика 21
Рассматривая какое-либо органическое соединение, невозможно сказать, к какому гомологическому ряду оно принадлежит. Гомологами анилина могут быть и толуидин, и М-метиланилин, и нафтиламин, и аминобифенил. Место вещества в систематике органических соединений определено группой гомологических рядов, к которым оно принадлежит. Поскольку препаративная химия широко использует синтетические гомологи для получения веществ с изменяемыми свойствами, то широкое понимание гомологии безусловно стимулирует творческую фантазию исследователя. [c.15]В России допущены к применению экст-ралин и присадка АДА на основе М,М-ме-тиланилина. При их концентрации 1-2 об. % увеличение октанового числа составляет 2-6 пунктов и зависит от группового состава бензина, а также исходного значения октанового числа. Экстралин наиболее эффективен в бензинах парафинового основания и менее — в бензинах, содержащих повышенные количества ароматических углеводородов. Экстралин представляет собой технический монометиланилин, содержащий до 90 % основного вещества и около 10 % смеси анилина и диметиланилина. Присадка АДА содержит практически чистый монометиланилин. Амины имеют ряд преимуществ перед ТЭС не оказывают отрицательного влияния на работоспособность свечей зажигания, не образуют нагаров, они хорошо совмещаются с метало-содержащими антидетонаторами. В некоторых случаях наблюдается синергизм — взаимное усиление антидетонационных свойств присадок в смеси. Токсичность аминов гораздо меньше, чем ТЭС. Амины действуют на радикал гидроперекиси (на примере ТУ-метиланилина) [c.359]
При взаимодействии дифениламина, дибензиламина, а также бензил-амина с перекисью бензоила реакции осложняются, потому и в качестве конечных продуктов, кроме бензойной кислоты, получаются другие вещества, отличные от продуктов реакций алифатических аминов с перекисью бензоила (ПБ) [4—6]. Впоследствии Л. Хорнером с сотр. [7, 8] было показано, что бензольные растворы диметиланилина и ПБ поглощают кислород и что эта система инициирует полимеризацию стирола, между тем как анилин и метиланилин этими свойствами не обладают. Последние скорее ингибируют инициированную перекисью бензоила полимеризацию стирола. В нашей лаборатории было показано [9], что система ПБ-дифениламин поглощает окись азота и с малой эффективностью инициирует полимеризацию винилацетата, а также метилметакрилата. [c.260]
Алкилирование анилина метанолом исследовано в присутствии цеолитов типа У и X, модифицированных катионами Ма , К , КЬ , при 400°С. Установлено, что активность и селективность цеолита сильно зависят от его кислотно-основных свойств на более основных катализаторах, содержащих К , КЬ , в основном образуется К-метиланилин, а на более кислых цеолитах — л- и о-толуидины [517]. [c.183]
Интересно, что метиланилин, и особенно диметиланилин, обладают более сильными основными свойствами, чем сам анилин. Это легко объяснить в соответствии с теорией А. М. Бутлерова. Если представить анилин как аммиак, где водород замещен ароматическим радикалом фенилом, который усиливает кислотные свойства органических соединений и ослабляет основные, то станет ясно, что анилин — более слабое основание, чем аммиак. Замещение водорода в аммиаке или ароматическом амине жирным радикалом усиливает их основные свойства. [c.165]
Небольшая основность пиридина объясняется влиянием на атом азота двойной связи 1—2. Неподеленные электроны атома азота вследствие геометрических причин имеют плоскую триго-нальную орбиту, т. е. в значительной степени являются -электронами. Таким образом, рКа пиридина (5,2) лежит между р/(а типичных алифатических аминов (например, триметиламина с р/Са=9,7), основные свойства которых обусловлены неподеленны-ми электронами, занимающими тетраэдрическую орбиту, и рКа молекулярного азота или соединений циана, где неподеленные электроны занимают чистую s-орбиту, вследствие чего эти соединения не имеют основных свойств. Эти факты служат подтверждением, что s-электроны расположены ближе к атомному ядру, чем р-электроны. То, что основность пиридина близка к основности ди-метиланилина (р/Со=5,1), является простой случайностью, так как [c.31]
Реакция проводилась в присутствии бензола (13 объема. %) Термомеханические свойства обсуждается эффект пластификации Проведена прививка на волокно описаны кинетика реакции и свойства сополимеров Облучение проведено в присутствии системы перекись бензоила — ди-метиланилин [c.77]
Наблюдается ускорение реакции в присутствии метилового спирта Изучены кинетика реакции и физические свойства сополимера Описано влияние растворителей и температуры приведены кинетические данные Облучение проведено в присутствии системы перекись бензоила — ди-метиланилин Осуществлена прививка на полиэтиленовый латекс обсуждается влияние окислительно-восстанови-тельной инициирующей системы Облучение проведено на воздухе [c.82]
Химические свойства. Отличается слабым основным характером и не образует с минеральными кислотами солей, устойчивых в водных растворах. При смешении с уксусным ангидридом не вступает с ним в реакцию и не дает поэтому повышения температуры. Повышение температуры при таком смешении может служить мерилом содержания метиланилина в техническом продукте. В Д. 3 сорта допускается 2% примесей (главным образом анилина). [c.444]
Авторы работы [249] в диапазоне частот 102—105 Гц в температурном интервале 100—310 К изучили диэлектрические свойства кристаллических N-этиланилина, о-нитро-М-метиланилина, анилина и фенола. При температурах значительно ниже точки плавления веществ наблюдается увеличение диэлектрической проницаемости, которое связано с межслоевой поляризацией, возникающей из-за подвижности молекул вблизи дефектов кристаллической структуры и присутствия в образце жидкой фазы в результате наличия примесей. Интересно, что для исследованных соединений не обнаружено фазовых переходов в твердой фазе. Проведенные оценки с учетом наблюдающихся изменений величины диэлектрической проницаемости показали, что объемная доля молекул, подвижность которых характеризуется звуковыми и более высокими частотами, в феноле и о-нитро-М-метиланилине составляет менее 3—4% при температурах до 260 К- В анилине доля подвижных молекул до температуры 250 К несколько выше 6—8%. [c.62]
Уокер исследовал влияние промотирования К,4-динитрозо-Ы-метиланилином на физико-механические свойства и гистерезис вулканизатов бутадиен-стирольного и натурального каучуков, а также вулканизатов на основе комбинации этих каучуков (1 1), [c.222]
При ароматизации соединений П1 и IV поддействием безводной фосфорной кислоты и уксусного ангидрида в обоих случаях были получены диалкиланилины, что свидетельствует о сохранении алкильных групп при перегруппировке. Из соединения III получен известный 3,4—диметиланилин, который был идентифицирован сравнением с аутентичн
www.chem21.info
