Пропеновая кислота | это… Что такое Пропеновая кислота?
ТолкованиеПеревод
- Пропеновая кислота
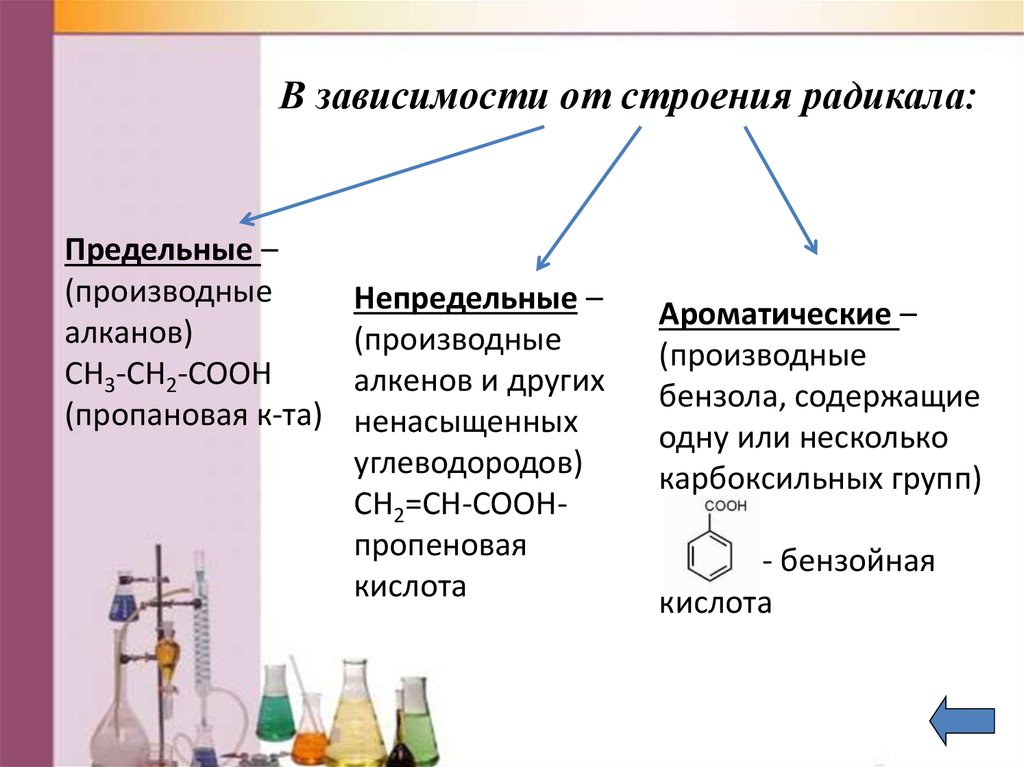
Акриловая кислота (пропеновая кислота, этенкарбоновая кислота) СН2=СН–СООН – простейший представитель одноосновных непредельных карбоновых кислот. Бесцветная жидкость с резким запахом, растворима в воде, диэтиловом эфире, этаноле, хлороформе. Легко полимеризуется с образованием полиакриловой кислоты. С другими мономерами образует сополимеры.
Содержание
- 1 Синтез
- 2 Химические свойства
- 3 Применение
- 4 Безопасность
- 5 Примечания
- 6 См. также
Синтез
Сейчас применют парофазное окисление пропилена кислородом воздуха на висмутовых, кобальтовых или молибденовых катализаторах.

СН2
Раньше использовалась реакция ацетилена, оксида углерода (II) и воды:
СН≡СН + СО + Н2О → СН2=СН–СООН
или кетена с формальдегидом.
СН2=С=О + H2C=O → СН2=СН–СООН
Компанией Rohm and Haas разрабатывается технология синтеза акриловой кислоты из пропана.
Химические свойства
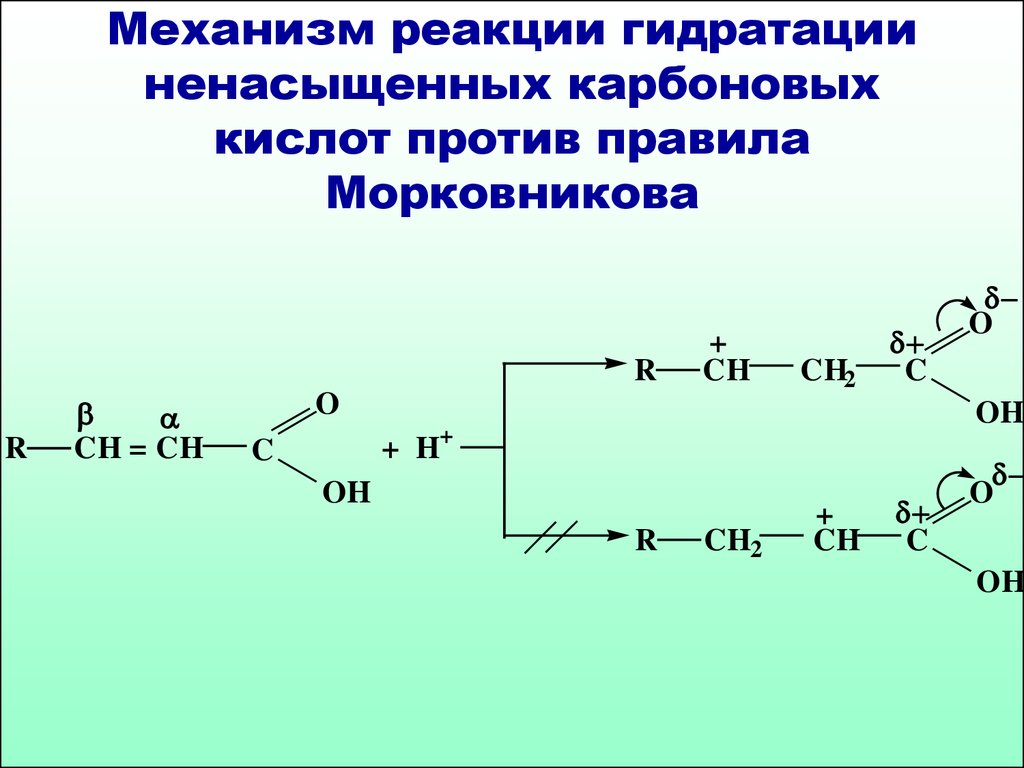
Акриловая кислота образует соли, хлорангидрид, ангидриды, сложные эфиры, амиды и пр. Она вступает в реакции присоединения, характерные для этиленовых углеводородов. При действии амальгамы натрия в водном растворе и гидрировании в жидкой фазе в присутвии Ni, Pt, Pd в пропионовую кислоту. Присоединение протонных кислот, воды и NH3 происходит против правила Марковникова с образованием замещенных производных. Как диенофил акриловая кислота участвует в диеновом синтезе. Конденсируется с солями арилдиазония (реакция Меервейна):
n-ClC6H
4N2Cl + СН2=СНСООН n-СlС6Н4СН=СНСООН + НСl + N2.
При УФ-облучении или в кислых водных растворах (рН=1), а также присутствии инициаторов полимеризации образует полиакриловую кислоту ([—СН2—СН(СООН)—]n).
Применение
Для предотвращения полимеризации при хранении добавляют ингибитор-гидрохинон. Перед использованием перегоняют с особой осторожностью — возможна взрывоподобная полимеризация.
Акриловая кислота и ее производные используются при производстве акриловых эмульсий для лакокрасочных материалов, пропитки тканей и кожи, в качестве сырья для полиакрилонитрильных волокон и акрилатных каучуков, строительных смесей и клеев. Значительная часть акриловой кислоты используется так же при производстве суперабсорбентов. В производстве полимеров широко применяют сложные эфиры акриловой и метакриловой кислот, главным образом метиловые эфиры: метилакрилат и метилметакрилат.
Безопасность
Акриловая кислота сильно раздражает кожные покровы. Раздражает слизистую оболочку глаз (порог раздражающего действия 0,04 мг/л).
 При попадании в глаза вызывает сыльные ожоги роговицы глаза и может вызвать необратимые повреждения. Вдыхание паров может вызвать раздражение дыхательных путей, головную боль,при больших концентрациях или экспозиции — отёк лёгких. Хотя наличие запаха ещё не означает какой либо угрозы здоровью, необходим мониторинг воздуха. ПДК 5 мг/м3
При попадании в глаза вызывает сыльные ожоги роговицы глаза и может вызвать необратимые повреждения. Вдыхание паров может вызвать раздражение дыхательных путей, головную боль,при больших концентрациях или экспозиции — отёк лёгких. Хотя наличие запаха ещё не означает какой либо угрозы здоровью, необходим мониторинг воздуха. ПДК 5 мг/м3Примечания
- Kirk-Othmer encyclopedia, 3 ed., v. I, N.Y.-[a.o.], 1978, p. 330-54. А. В. Девекки.
- Рабинович В.А., Хавин З.Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 121
См. также
- Акрилаты
- Акролеин
- Акрилонитрил
- Метакриловая кислота
Wikimedia Foundation. 2010.
Игры ⚽ Поможем написать курсовую
- Пропеллер
- Пропен
Полезное
Пропеновая кислота | это… Что такое Пропеновая кислота?
ТолкованиеПеревод
- Пропеновая кислота
Акриловая кислота (пропеновая кислота, этенкарбоновая кислота) СН2=СН–СООН – простейший представитель одноосновных непредельных карбоновых кислот.
 Бесцветная жидкость с резким запахом, растворима в воде, диэтиловом эфире, этаноле, хлороформе. Легко полимеризуется с образованием полиакриловой кислоты. С другими мономерами образует сополимеры.
Бесцветная жидкость с резким запахом, растворима в воде, диэтиловом эфире, этаноле, хлороформе. Легко полимеризуется с образованием полиакриловой кислоты. С другими мономерами образует сополимеры.Содержание
- 1 Синтез
- 2 Химические свойства
- 3 Применение
- 4 Безопасность
- 5 Примечания
- 6 См. также
Синтез
Сейчас применют парофазное окисление пропилена кислородом воздуха на висмутовых, кобальтовых или молибденовых катализаторах.
СН2=СН–СН3 + O2 → СН2=СН–СООН
Раньше использовалась реакция ацетилена, оксида углерода (II) и воды:
СН≡СН + СО + Н2О → СН2=СН–СООН
или кетена с формальдегидом.
СН2=С=О + H2C=O → СН2=СН–СООН
Компанией Rohm and Haas разрабатывается технология синтеза акриловой кислоты из пропана.

Химические свойства
Акриловая кислота образует соли, хлорангидрид, ангидриды, сложные эфиры, амиды и пр. Она вступает в реакции присоединения, характерные для этиленовых углеводородов. При действии амальгамы натрия в водном растворе и гидрировании в жидкой фазе в присутвии Ni, Pt, Pd в пропионовую кислоту. Присоединение протонных кислот, воды и NH
3 происходит против правила Марковникова с образованием замещенных производных. Как диенофил акриловая кислота участвует в диеновом синтезе. Конденсируется с солями арилдиазония (реакция Меервейна):n-ClC6H4N2Cl + СН2=СНСООН n-СlС6Н4СН=СНСООН + НСl + N2.
При УФ-облучении или в кислых водных растворах (рН=1), а также присутствии инициаторов полимеризации образует полиакриловую кислоту ([—СН2—СН(СООН)—]n).
Применение
Для предотвращения полимеризации при хранении добавляют ингибитор-гидрохинон. Перед использованием перегоняют с особой осторожностью — возможна взрывоподобная полимеризация.

Акриловая кислота и ее производные используются при производстве акриловых эмульсий для лакокрасочных материалов, пропитки тканей и кожи, в качестве сырья для полиакрилонитрильных волокон и акрилатных каучуков, строительных смесей и клеев. Значительная часть акриловой кислоты используется так же при производстве суперабсорбентов. В производстве полимеров широко применяют сложные эфиры акриловой и метакриловой кислот, главным образом метиловые эфиры: метилакрилат и метилметакрилат.
Безопасность
Акриловая кислота сильно раздражает кожные покровы. Раздражает слизистую оболочку глаз (порог раздражающего действия 0,04 мг/л). При попадании в глаза вызывает сыльные ожоги роговицы глаза и может вызвать необратимые повреждения. Вдыхание паров может вызвать раздражение дыхательных путей, головную боль,при больших концентрациях или экспозиции — отёк лёгких. Хотя наличие запаха ещё не означает какой либо угрозы здоровью, необходим мониторинг воздуха. ПДК 5 мг/м3
Примечания
- Kirk-Othmer encyclopedia, 3 ed.
 , v. I, N.Y.-[a.o.], 1978, p. 330-54. А. В. Девекки.
, v. I, N.Y.-[a.o.], 1978, p. 330-54. А. В. Девекки. - Рабинович В.А., Хавин З.Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 121
См. также
- Акрилаты
- Акролеин
- Акрилонитрил
- Метакриловая кислота
Wikimedia Foundation. 2010.
Игры ⚽ Нужен реферат?
- Пропеллер
- Пропен
Полезное
Поли(пропеновая кислота) (Полиакриловая кислота)
За исключением
За исключением
Существует группа полимеров, акрилы, которые можно рассматривать как основанные на акриловой кислоте, формально называемой пропеновой кислотой.
Кислота полимеризуется путем полимеризации присоединения к поли(пропеновой кислоте) (полиакриловой кислоте).
Другие соединения на основе кислоты, образующие акрилы, включают метиловый, этиловый и бутиловый эфиры пропеновой кислоты.
Каждый из этих сложных эфиров может быть полимеризован, например, метиловый эфир образует этот акрил:
Двумя другими важными мономерами на основе кислоты являются пропенитрил (акрилонитрил) и пропенамид (акриламид).
Можно видеть, что полимеры имеют базовую структуру акриловых материалов, показанных выше.
Поли(метил-2-метилпропеноат, (поли(метилметакрилат)) — еще один важный полимер, известный просто как акриловое или акриловое стекло. Он основан на метиловом эфире 2-метилпропионовой кислоты (метакриловой кислоты).
Этот веб-сайт содержит три единицы акриловых материалов:
Поли(пропеновая кислота) (Полиакриловая кислота)
Поли(пропенонитрил) (Полиакрилонитрил)
Поли(метил-2-метилпропеноат) (поли(метилметакрилат))
Эта единица касается пропеновой кислоты (акриловой кислоты), ее сложных эфиров и полимеров, полученных из них.
Использование поли(пропеновой кислоты) (полиакриловой кислоты)
Поли(пропеновая кислота) используется в моющих средствах для удаления ионов кальция и магния из воды, тем самым смягчая ее. Это означает, что для этой цели не нужно использовать фосфаты, что позволяет производить более экологически чистое моющее средство.
|
Второе применение – производство так называемых суперабсорбентов.
1. Market Research Store по данным GlobeNewswire 2018
Использование полипропеноатов (полиакрилатов)
Полимеры, полученные из сложных эфиров пропеновой кислоты, используются в качестве основы во многих красках и лаках. Полимеры этил- и бутилпропеноатов используются в водоэмульсионных красках, а также сополимеры бутилпропеноата и метил-(2-метилпропеноата).
Метилпропеноат используется для производства сополимера с пропенонитрилом , который является одним из наиболее широко используемых «акриловых» волокон.
Метил- и этилпропеноаты сополимеризуются с метил-2-метилпропеноатом, чтобы помочь в производстве поли(метил-2-метилпропеноата), ряда полимеров, таких как плексиглас.
Использование пропеновой кислоты (акриловой кислоты)
Около 50% используется для получения сложных эфиров, в основном метил-, этил- и бутилпропеноатов. Они, в свою очередь, полимеризуются (см. ниже).
Около 30% используется для производства поли(пропеновой кислоты) и, таким образом, суперабсорбентов.
Годовое производство пропеновой кислоты (акриловой кислоты)
| Мир | 5,9 млн тонн 2 |
2. В 2014 году Market Research Store цитирует GlobeNewswire 2018
Производство пропеновой кислоты (акриловой кислоты)
Пропеновая кислота производится из пропилена в два этапа.
Первая стадия – окисление пропена в пропеналь (акролеин). Алкен и воздух смешивают и пропускают через нагретый гетерогенный катализатор, часто смесь оксидов висмута (III) и молибдена (VI) на кремнеземе, при ca 650 K:
Вторая стадия происходит при пропускании пропеналя и воздуха над другим катализатором, смесью оксидов ванадия(V) и молибдена(VI) на кремнеземе при ca 550 K:
3
3
3
3
3
Производство поли(пропеновой кислоты) (полиакриловой кислоты)
Полимеризация пропеновой кислоты представляет собой свободнорадикальный процесс с использованием органического пероксида в качестве инициатора. Ее можно проводить с чистым мономером (так называемая полимеризация в массе), но чаще полимеризуют в водном растворе или в виде эмульсии, а также в воде:
Производство полипропеноатов (полиакрилатов)
Пропеновая кислота взаимодействует со спиртом (например, метанолом, этанолом, бутан-1-олом) в жидкой фазе с небольшим количеством серной кислоты в качестве катализатора для получения сложные эфиры. Например:
Например:
Затем сложные эфиры полимеризуют свободнорадикальным способом с использованием органического пероксида в качестве инициатора. Можно использовать чистый мономер (известный как полимеризация в массе), но опять же чаще реакцию проводят в водном растворе или в эмульсии в воде. Например:
Если требуются сополимеры сложных эфиров, два мономера смешивают перед реакцией полимеризации в аналогичных условиях. Рис. ) и поли(пропенонитрил) из пропилена.
Дата последнего изменения: 29 октября 2018 г.



 При попадании в глаза вызывает сыльные ожоги роговицы глаза и может вызвать необратимые повреждения. Вдыхание паров может вызвать раздражение дыхательных путей, головную боль,при больших концентрациях или экспозиции — отёк лёгких. Хотя наличие запаха ещё не означает какой либо угрозы здоровью, необходим мониторинг воздуха. ПДК 5 мг/м3
При попадании в глаза вызывает сыльные ожоги роговицы глаза и может вызвать необратимые повреждения. Вдыхание паров может вызвать раздражение дыхательных путей, головную боль,при больших концентрациях или экспозиции — отёк лёгких. Хотя наличие запаха ещё не означает какой либо угрозы здоровью, необходим мониторинг воздуха. ПДК 5 мг/м3 Бесцветная жидкость с резким запахом, растворима в воде, диэтиловом эфире, этаноле, хлороформе. Легко полимеризуется с образованием полиакриловой кислоты. С другими мономерами образует сополимеры.
Бесцветная жидкость с резким запахом, растворима в воде, диэтиловом эфире, этаноле, хлороформе. Легко полимеризуется с образованием полиакриловой кислоты. С другими мономерами образует сополимеры.
 , v. I, N.Y.-[a.o.], 1978, p. 330-54. А. В. Девекки.
, v. I, N.Y.-[a.o.], 1978, p. 330-54. А. В. Девекки. 0211
0211