Химическая формула Физические свойства
Спецификация
| ||||||
osayt.ru
Карбонат натрия | khimie.ru
Карбонат натрия Na2СО3 в безводном состоянии представляет собой белый порошок удельного веса 2,4-2,54, который плавится около 850 °С. В воде сода легко растворяется, причем вследствие образования гидратов растворение сопровождается разогреванием. Важнейший из гидратов, получаемых в твердом состоянии, кристаллическая сода, Nа2СО3
Помимо декагидрата, существует ромбический гептагидрат, устойчивый при соприкосновении с раствором в температурном интервале 32,017-35,3 °C, а также ромбический моногидрат, который, согласно Вальдеку, находясь под раствором; при 112,5 °C и давлении 1,27 атм., переходит в безводную соль. Гептагидрат существует также еще в другой модификации, которая при соприкосновении с водным раствором не устойчива ни при какой температуре.
Сода встречается иногда в природе в водах озер, например в озере Оуэнс в шт. Калифорния, общее содержание соды в котором достигает 100 млн. т; сода, правда достаточно грязная, добывается из этого озера в результате испарения воды на солнце. Содовые озера наряду с нейтральным карбонатом содержат прежде всего гидрокарбонат. В некоторых местах осаждается двойное соединение гидрокарбоната натрия с нормальным карбонатом Nа 2СО3∙NаНСO3, называемое троной. В водах щелочных источников, например в Карловых Барах, такте содержатся Nа2СО3 и NаНСO3.
Карбонат натрия содержится в золе некоторых морских водорослей. 100 лет назад соду добывали главным образом из золы растений.
Теперь соду получают почти исключительно способом Солъве (аммиачный способ получения соды). Более старый способ Леблана теперь, по крайней мере в Германии, совершенно не используют. Производство соды путем карбонизации полученной электролизом натровой щелочи в противоположность осуществляемому таким путем производству поташа имеет ограниченное значение. Как было указано, едкий натр, наоборот, часто получают каустификацией соды. В США соду отчасти получают из криолита.
По способу Леблана каменную соль обрабатывали сначала концентрированной серной кислотой; получая сульфат натрия (называемый обычно в технике коротко сульфат) и в качество важнейшего побочного продукта соляную кислоту
2NaCl + Н2SO4 = Na2SO4 + 2НС1.
Затем для получения соды сульфат смешивали с карбонатом кальция (известняк) и углем, и сплавляли в пламенной печи. При этом происходили следующие реакции:
Na2SO4 + 2C = Na2S + 2CO2
Na2S + CaCO3 = Na2CO3 + CaS
Соду извлекали из охлажденного сплава выщелачиванием водой, в то время как нерастворимый СаS оставался в качестве малоценного отброса. Способ был разработан Лебланом в 1791 г. на премию Франдузской академии. Вскоре после этого, сначала в Англии, затем в Германии и Франции, развилась содовая промышленность, которая до 1870 г. основывалась исключительно на процессе Леблана. Только в последнее время процесс Леблана был вытеснен рентабельным способом Сольве.
Способ получения соды по Сольве, или аммиачный способ, основал на образовании сравнительно трудно растворимого гидрокарбоната натрия NаНСО3 взаимодействием хлорида натрия с гидрокарбонатом аммония в водном растворе:
NaCl + NH4НСO3= NaНСO3+NH4С1.
В технике почти в насыщенный раствор поваренной соли пропускают сначала аммиак, затем диоксид углерода. Образующийся, NaНСО3 отфильтровывают и нагреванием (кальцинирование) переводят в Na2СО3 (кальцинированная сода)
2NаHСО3 = Nа2СO3+СO2 + Н2О.
При этом выделяется половина первоначально взятого диоксида углерода, и его снова направляют в процесс. Чтобы обратно получить NН3, в маточный раствор, из которого осаждали гидрокарбонат, пропускают аммиак и водяной пар. Благодаря этому содержащийся там гидрокарбонат аммония переходит сначала в нейтральный карбонат и последний при температурах выше 58 °C разлагается на диоксид углерода, воду и аммиак.
NH4HCO3 + NH3 = (NH4)2HCO3
Аммиак, содержащийся в маточном растворе в виде NH4Cl (около 75% общего количества), выделяется оттуда при добавлении нзвесткового молока:
2NН4С1+Са(ОН)2 = СаС12 + 2Н2O + 2NН3.
так что наряду с не прореагировавшим хлоридом натрия единственным отходом является хлорид кальция, который обычно спускают в реки.
Сода является одним яз важнейших продуктов химической промышленности. В больших количествах ее используют в стекольном и мыловаренном производствах. Она является также исходным продуктом для получения многих других важных соединений натрия, таких, как едкий натр. бура, фосфат натрия, растворимое стекло и др. Большое количество соды употребляют, кроме того, в прачечных, на бумажных фабриках, в красильном производстве, а также для смягчения воды паровых котлов. В домашнем хозяйстве сода применяется как средство для чистки.
Ваш отзыв
Вы должны войти, чтобы оставлять комментарии.
khimie.ru
Натрия карбонат, применение — Справочник химика 21
Кроме сульфата алюминия в НИИнефтеотдача исследована возможность использования для ограничения добычи воды некоторых других химических отходов, таких как лигносульфонаты, кремнефтористоводородная кислота, соли железа и алюминия, сульфат натрия, карбонат и бикарбонат натрия, аммиачная вода, жидкое стекло и др. Лигносульфонаты, как было отмечено в предыдущих разделах, являются многотоннажными и дешевыми отходами целлюлозно-бумажных комбинатов, вполне доступны и транспортабельны. Поэтому они представляют большой интерес для применения в качестве осадкообразующих реагентов. Известно, что лигносульфонаты выпадают в осадок при контакте с сильно минерализованными пластовыми водами плотностью выше 1150—1160 кг/м . [c.306]Добавки минеральных солей к кормовым рационам ускоряют развитие животных, увеличивают продуктивность скотоводства и птицеводства. Кормовыми средствами являются хлорид натрия, карбонат кальция, фосфаты кальция, натрия, аммония, соли железа, меди, цинка, кобальта, марганца и другие карбамид (мочевина). Консервантами, т. е. средствами, сохраняющими ценные питательные вещества в кормах, служат дисульфит натрия NagSaOg, гидросульфит натрия NaHSOs, фосфаты и карбонаты аммония и др. Применение в сельском хозяйстве минеральных удобрений и других солей, наряду с механизацией и передовыми методами агротехники, дает нашему народному хозяйству большой экономический эффект. [c.18]
Даны хлорид натрия, карбонат кальция, кокс, вода, воздух. Как получить из них не менее 20 веществ (органических и неорганических), имеющих практическое применение [c.76]
Растворы поликарбонатов, получаемые методом межфазной поликонденсации, содержат нежелательные примеси (хлористый натрий, карбонат натрия и едкий натр), которые при контакте с водой приводят к образованию эмульсии, что затрудняет выделение поликарбоната из раствора при переработке. Кроме того, наличие этих примесей в поликарбонате может привести к окрашиванию конечного продукта и ухудшению его свойств. Поэтому перед осаждением поликарбоната из растворов необходимо удалить эти примеси. Для этого раствор поликарбоната промывают очищенной водой с удельной электропроводностью 1—2 мВ/см. Промывка организована в виде многоступенчатого циклического процесса или многократной противоточной системы с применением мешалок различных конструкций, например турбинных, лопастных, пропеллерных и др. [c.75]
Мытье с применением моющих средств. Для удаления не растворяющихся в воде загрязнений органического происхождения, особенно жировых и смолистых веществ, рекомендуется применение различных моющих растворов. В лабораториях чаще всего используют растворы хозяйственного мыла, стиральных паст и порошков, соды (карбоната натрия), фосфата натрия. [c.22]
Эрссон [108] использовал этот метод для газохроматографического определения карбоновых кислот и фенолов. Метод включает экстракцию кислоты в форме ионной пары в метиленхлорид и получение производного с пентафторбензилбромидом. Скорость реакции увеличивается в зависимости от структуры противоиона и при увеличении его концентрации. Для повышения скорости реакции гораздо лучше использовать вместо тетрабутиламмониевых солей более липофильные соли тетра-н-пен-тиламмония. Имеется обзор, посвященный применению экстрактивного алкилирования для анализа фармацевтических препаратов [1052], а недавно описана микромодификация этого метода с твердофазной системой МФК и использованием в каче- стве щелочи карбоната натрия [1053]. [c.128]
В гидразобензоле связь N—Н существенно более кислая, поэтому небольшая равновесная концентрация аниона может образоваться в присутствии карбоната калия или водной щелочи. С К2СО3 в этаноле или ДМФА моноалкилирование идет плохо. Применение техники экстрактивного алкилирования с метиленхлоридом в качестве растворителя в присутствии 0,5— 1 моля тетрабутиламмония гидроксида и 0,5—1 моля водного гидроксида натрия при кипячении в течение 1—24 ч до нейтральной реакции позволяет значительно увеличить выход. Первичные иодиды, бензилбромид и аллилбромид дают хорошие выходы, вторичные иодиды — хуже [253] (схема 3.48 см. также [1548]). Аналогично можно проалкилировать фенилгидра-зон С при этом образуется О с выходом 43—98%. Условия реакции перемешивание с 50%-ным водным раствором гидрокси- [c.161]
Исследовано влияние количества и свойств растворенных солей на разделение суспензий глинистых сланцев [220]. Опыты проведены с применением анионоактнвного, катионоактивного и неионогенного флокулянтов в присутствии хлоридов натрия, кальция и магния, карбонатов натрия, кальция и магния, сульфатов натрия, магния, железа и алюминия при концентрации 100—5000 ч. на 1 млн. Установлено, что эффективность действия флокулянтов зависит от концентрации и валентности ионов солей, причем влияние этих факторов на каждый флокулянт различно. [c.196]
На этом свойстве перекиси натрия основано применение ее в качестве отбеливающего средства для различных материалов тканей, соломки, костей, волосяных изделий и пр. Она входит в состав мыльных стиральных порошков. При взаимодействии с двуокисью углерода перекись натрия переходит в карбонат, освобождая при этом кислород [c.39]
Применение. В производстве сахара, пива, газированных вод, для изготовления сухого льда для получения гидрокарбоната натрия, карбоната и гидрокарбоната аммония, свинцовых белил, карбамида и гидроксикарбоновых кислот как инертная среда при проведении некоторых реакций как теплоноситель в графитовых реакторах как нагнетающий газ для перекачки легковоспламеняющихся жидкостей в металлургии. [c.326]
Напишите уравнения реакции регенерации пермутита кальция карбонатом натрия в исходный пермутит натрия. Какое применение имеет пермутит натрия в технике [c.221]
Клинкер из камеры 10 направляют на хранение в бункер 15. По мере необходимости клинкер смешивают с добавками, регулирующими схватываем ость, например ангидридом или гипсом, другими соединениями, такими как оксид алюминия, сульфат алюминия, сульфаты калия и натрия, карбонат калия или бура. Эти соединения добавляются в достаточных количествах, чтобы обеспечить требуемые свойства цемента. Клинкер, добавки, регулирующие схватываемость, а также другие добавки измельчаются в порошок в мельнице 16. Порошкообразный цемент, который готов к применению, направляют на хранение в бункер 17. [c.292]
ЧТО некоторые элементы дают после сплавления с ним более растворимые продукты, чем после сплавления с карбонатом натрия. Карбонат калия применяют чаще всего в некоторых методах анали.за танталатов и ниобатов, а в смеси с карбонатом натрия — в тех случаях, когда надо иметь сплав с более низкой температурой плавления, чем у обоих карбонатов в отдельности. Перед применением карбоната калия его, конечно, надо обезвоживать. [c.918]
Карбонат этаноламина и различные другие соединения рассматриваются в качестве летучих ингибиторов в [35, 45]. Смесь мочевины и нитрита натрия также нашла практическое применение, в частности в виде пропитки для бумаги. В присутствии» влаги компоненты смеси, вероятно, взаимодействуют друг с другом с образованием нитрита аммония, который летуч, хотя мало устойчив, и обеспечивает подвод ингибирующих ионов N0 к поверхности металла. [c.274]
При применении третьего способа берут 100 г гидроксида натрия, помещают в колбу из термостойкого стекла или в фарфоровую чашку и растворяют в 100 мл дистиллированной воды. Добавление воды следует вести осторожно, небольшими порциями, при постоянном помешивании. При растворении гидроксида натрия карбонат натрия остается в виде суспензии, которая при стоянии опускается на дно. Полученный раствор нагревают и кипятят в течение 2—3 ч, охлаждают и сливают в другую колбу, стараясь не взмутить осадок, или фильтруют через стеклянный фильтр. Концентрированный раствор гидроксида натрия сохраняют в склянках, закрытых резиновыми пробками. Склянки для хранения концентрированных щелочей рекомендуется покрывать внутри слоем церезина или парафина последнее время применяют сосуды из пластмассы. [c.361]
Промышленный ПАВ ДС-РАС — это вязкая хорошо растворяющаяся в воде масса от желтого до светло-коричневого цвета плотностью = = 1,16 с температурой застывания /=50 °С, которая в своем составе помимо основного вещества (45%) и растворителя имеет определенное количество несульфированных соединений (1 % ), сульфата натрия (5%) и карбоната натрия (3%). Обладает высокой пенообразующей и смачивающей способностью даже в морской воде, что стимулирует его широкое применение помимо нефтяной промышленности также в текстильной, горнорудной и строительной в качестве технических моющих средств, фло-тореагента и пластификатора бетонов и цементов. Аналогами реагента являются 51апу1 40 (Франция), Тепзепе Д40 (Бельгия), А1капо1 V.XN (США). [c.78]
Как правило, не имеет значения, какой карбонат взят для сплавления. Наиболее часто используют карбонат натрия. Карбонат калия находит меньшее применение из-за более высокой температуры плавления и гигроскопичности, его используют для [c.119]
Данные о вытеснении нефти водными растворами других типов ПАВ из карбонатных и терригенных пористых сред приведены на рис. 35 и 36. Эти данные — результат многочисленных опытов на образцах с различной проницаемостью. Из рисунков видно, что применение анионного ПАВ сульфанал НП-36 в смеси с карбонатом натрия эффективно в карбонатных коллекторах любой проницаемости, но особенно при малой. Для вытеснения нефти из терригенных коллекторов смеси реагентов НП-3 и МазСОз, а также алкилсульфонат и неонол 2В1315-9 малоэффективны. Это связано с различием структуры порового пространства и молекулярно-поверхностных свойств (в частности, смачиваемости) терригенных и карбонатных пород. [c.82]
Отходы от регенерации катионообменника, работавшего в натриевом цикле, содержат хлориды кальция, магния и натрия, а также хлориды железа и марганца, если два последних иона содержатся в сырой воде. В отходах регенератов после катионита, работавшего в водородном циме, содержатся сульфаты натрия, кальция и магния и избыток кислоты. При регенерации слабоосновных анионитов получаются сульфат и хлорид натрия и избыток регенерирующей щелочи и дополнительно силикат и карбонат натрия при применении сильноосновных анионитов. Отходы от регенерации и промывки могут часто составлять 10 и возможно более процентов от количества обрабатываемой в установке воды. [c.261]
Осадительно-фильтрующие центрифуги нашли применение в различных производствах химической промышленности при разделении солевых суспензий (хлориды калия и натрия, сульфат и сульфид натрия, карбонат и бикарбонат натрия), суспензий поливинилхлорида, полистирола и др. [c.152]
Процесс Стретфорд [28, 600, 601] нашел широкое применение со времени успешных экспериментов на пилотной установке в 1959 г. Достоинством процесса является возможность исключить-очень токсичные арсениты и уменьшить содержание сероводорода в широком диапазоне первоначальных концентраций (от 100 до 10 000 млн ) до конечной концентрации 1 млн в отходящих газах. Построенные установки имели мощность 60 000 м /ч. В процессе Стретфорд сероводород абсорбируется щелочным раствором (pH = 8,5—9,5), содержащим кроме карбоната натрия эквимолекулярные количества ванадата натрий-аммоний и антрахинон-2,6 к 2,7-дисульфоната (ADA) [на первых установках применяли метава-надат вместо ванадата аммония]. Кроме того, к раствору добавляется соль Рошеля (натрий-калиевая соль винной кислоты), чтобы ванадат не выпадал в осадок. [c.149]
Ванадиевые минералы также легко сплавляются с карбонатом натрия (или калия) и с перекисью натрия. При применении карбоната целесообразно прибавить немного селитры. Если пользуются перекисью натрия, то нет необходимости нагревать до полного расплавления смеси, так как реакция проходит полностью и в случае спекания. [c.465]
В ПВХ-пластизолях неорганические ХГО не растворяются и плохо диспергируются, в связи с чем они долго не находили применения, особенно для изготовления жестких ПВХ-пен. Положение изменилось после того, как Берлин с сотр. (см. [93]) предложил использовать иизкомолекулярные реакционноспособные пластификаторы-сшиватели, хорошо совмещающиеся и с минеральными ХГО, и с ПВХ. Этот метод позволил использовать для вспенивания ПВХ-композиций все общедоступные минеральные ХГО карбонат [94] и гидрокарбонат [16] натрия карбонат кальция [94, 95] перборат натрия [17, 41] смеси карбоната и гидрокарбоната натрия и аммония [16] и др. Жесткие ПВХ-пенопласты вспененные с помощью минеральных ХГО, могут быть изготовлены и без применения реакционноспособных олигомеров и пизкомолеку-лярных пластификаторов [96]. [c.245]
Карбонат калия. Гигроскопичность карбоната калия делает его для сплавления минералов менее пригодным, чем карбонат натрия. Однако карбонат калия изредка применяют, главным образом потому, что некоторые элементы дают после сплавления с ним более растворимые продукты, чем после сплавления с карбонатом натрия. Карбонат калия применяют чаще всего в некоторых методах анализа танталатов и ниобатов, а в смеси с карбонатом натрия—в тех случаях, когда надо иметь сплав с более низкой температурой плавления, чем у обоих карбонатов в отдельности. Перед применением карбоната калия его, конечно, надо обезвоживать. [c.840]
Кинетику осаждения ПВС изучали по изменению мутности раствора после введения электролита, концентрация которого превышала пороговую [18]. На рис. 15.7 и 15.8 показаны кривые зависимости мутности как функции времени при различных концентрациях растворов сульфата натрия и сульфата аммония. Аналогичные кривые получены при применении растворов хлорида натрия, карбоната натрия, сульфата цинка, ацетата натрия и нитрата натрия. [c.213]
Важное практическое применение ионообмепного метода состоит в определении фтора в органических веществах после сплавления их в никелевой бомбе с перекисью натрия, карбонатом натрия-калия или металлическим натрием. Плав растворяют в воде и пропускают раствор через колонку с катионитом в Н-форме. Фтор определяют в вытекающем растворе либо путем титрования нитратом тория с али-заринсульфонатом натрия в качестве индикатора [50, 51, 105], либо алкалиметрическим титрованием [8, 188]. Если в растворе присутствует хлор, то алкалиметрическое титрование дает сумму галогенидов после оиределения хлора содержание фтора может быть вычислено но разности [8 ]. При микроопределении фтора в органических веществах вытекающий из ионообменной колонки раствор лучше анализировать колориметрическим методом, нанример с применением хлоранилата лантана [53]. Во фториде алюминия, криолите и плавиковом шпате фтор можно легко определить после сплавления пробы со смесью карбоната щелочного металла и кремнезема [194]. В этой связи уместно упомянуть также о колориметрических методах оиределения фтора в шлаках и фосфатных породах [74, 192]. [c.247]
Натрий и его производные имеют важнейшее значение. Сплав металлического натрия со свинцом используют для получения тетралкилсвинца (см. разд. 29.9), а сам натрий имеет и другие промышленные применения. Гидроксид (едкий натр), карбонат (сода), сульфат, триполифосфат и силикат (растворимое стекло) натрия входят в число 50 промышленных химических препаратов, которые производились в США в 1972 г, в количествах от одного до десяти миллионов тонн ежегодно. Калиевые соли, обычно сульфат, используют как удобрения. Литий в основном применяют для получения литийорганических соединений (см. разд. 29.3). [c.258]
Щелочные растворы. Поглощение двуокиси углерода щелочными растворами (карбонатами натрия и калия, едкой щелочью, этаноламинами) является примером абсорбции, сопровождающейся химической реакцией. Сложность явления, вытекающая из различия в механизме и скорости реакции, поверхностного натяжения растворов и действительной межфазовой поверхности, ограничивает анализ процесса по существу только эмпирическими методами. В последнее время разработан метод извлечения СО2 из предварительно сжатых газов (10—20 ат) горячими растворами. карбонатов Применение этого метода ограничено концентрацией СО2 в газе не ниже, чем 0,5%, однако применять его совместно с другими процессами щелочной абсорбции экономически выгодно. [c.57]
Наиболее изеестная соль — это хлористый натрий, употребляемый в пищу и широко применяемый в промышленности. В крови человека содержится 0,9% хлористого натрия. Фтористый натрий — очень ядовитый инсектицид. Бикарбонат натрия (питьевая сода) применяется в медицине и в кондитерской промышленности. Бикарбонат натрия играет важную роль в процессе обмена углекислый газ — кислород в организме человека. Карбонат натрия находит применение в бумажном, стекольном, текстильном и мыловаренном производствах. Гипохлорит натрия ЫаСЮ — отбеливающее и дезинфицирующее средство. [c.104]
Применение натриевых солей обширно. Помимо поваренной соли, следует назвать карбонат натрия Na2 0a, гидрокарбонат натрия NaH Os и натриевую селитру NaNOa. [c.145]
Кислотно-основной характер системы определяется типом заместителей и электроноакцепторные группы усиливают кислотность соли или основность соответствующего илида. В этих случаях для отрыва а-протона пригодны слабые основания, например карбонат калия. В более общем случае, когда заместителей, сильно повышающих кислотность, мало или они отсутствуют, используют, как правило, сильные щелочи литий-органические соединения, амид натрия в жидком аммиаке, ал-ко сиды щелочных металлов в гидроксильных растворителях или в диметилсульфоксиде либо димсильный анион в ДМСО. Стабилизованные (наличием групп Р = СООР, СМ и др.) илиды можно выделить. В то же время хорошо известно, что обычные фосфониевые илиды чувствительны и к воде, и к кислороду, поэтому стандартная методика требует применения тщательно высушенных растворителей и инертной атмосферы. Под действием воды происходит необратимый распад с образованием ал-килдифенилфосфина и бензола. На воздухе протекают следующие реакции [c.251]
Некоторые виды сырья после добычи и очистки сразу готовы к применению (например, карбонат натрия Ыа2СОз используется для смягчения воды). Но многие виды неорганического сырья превращаются сначала в промежуточные вещсстпа, которые затем используются для синтеза потребительских продуктов или других реактивов. На рис. VIII. 1 показано, как неорганические ископаемые комбинируются для получения неорганических промежуточных вещестн. [c.505]
Ввшо наличия в производстве вискозных волокон кислых и шелочных стоков нейтрализация сточных вод осушествляется путем применения метода взаимной нейтрализации. В случае наличия после смешения в сточных водах избытка серной кислоты (зависят от вида волокна, особенностей технологического процесса и др.) для нейтрализации применяют такие щелочные реагенты, как гидроксид натрия, карбонат натрия или чаше известковое молоко. [c.135]
Основными ингредиентами древнеегипетской синей глазури были щелочь, небольшое количество какого-то соединения меди в качестве окрашивающего вещества, немного карбоната кальция (частичный анализ додинастической глазури показал следы кальция , а в глазури римской эпохи — 3,8% извести оба эти вещества, почти наверное, присутствовали первоначально в виде карбоната кальция, который во время обжига превратился в силикат кальция) и большое количество окиси кремния. Поскольку как толченый, так и цельный, кусковой кварц являются формами кремнезема и поскольку при высокой температуре окись кремния приобретает свойства кислоты и соединяется с такими веществами, как [278] карбонат натрия, карбонат калия и карбонат кальция, добавление кремнезема было, по-видимому, излишне. Кроме того, некоторое количество окиси кремния содержится в щелочах, как в растительной золе, так и в низкокачественной соде. Например, в четырех подвергнутых анализу образцах соды кварцевого песка оказалось 2,2 %, 6,7 %, 7,6 % и 9,6 %. Поскольку некоторое количество карбоната кальция всегда содержится в соде и растительной золе (в четырех вышеупомянутых образцах соды оказалось 0,9 %>, 1,3 %), 1,4 %) и 1,2 %) карбоната кальция) и даже в кварце (в исследованной белой кварцевой гальке его оказалось 0,2 %), мы пришли к выводу, что добавлять карбопат кальция в опытную смесь не нужно. Поэтому опыты производились только с малахитом и с щелочью, и в результате при сильном прокаливании карбоната калия (главная составная часть обычной растительной золы) или толченой соды, смешанных с небольшим количеством мелкоистолченного малахита, каждый раз получалась великолепная синяя глазурь. Реакция заключалась не только в сплавлении щелочи и окрашивании ее малахитом, но также и во взаимодействии щелочи с кварцем. Когда мы удаляли глазурь путем растворения, поверхность гальки оказывалась сильно изъеденной и шероховатой. Несомненно, щелочи, соединяясь с частью кварца, образовывали силикат калия или натрия (в зависимости от состава примененной в каждом отдельном случае щелочи). Заметивший это Петри нишет Плавка глазури на камне частично растворяет его поверхность даже после того, как глазурь открошится, следы ее действия все еще остаются видны на камне, приобретающем вид выветренного мрамора или обсахаренного леденца . [c.153]
Иодометрическое титрование. 800 мг вещества (точная навеска) прибавляют к 10 мл 2 н. раствора карбоната натрия и 40 мл воды. Через 5 мин фильтруют через пористый стеклянный фильтр, осадок промывают (три раза по 10 мл воды). К фильтрату приливают 25 мл 10 н. раствора едкого натра и в течение 1,5 ч отгоняют 95 мл. Приемником при перегонке служит мерная колба вместимостью 100 мл, охлаждаемая ледяной водой. Дистиллят разбавляют до 100 мл, отбирают пипеткой 25 мл и прибавляют 25 мл 0,1 н. раствора бихромата калия. Затем осторожно приливают 25 мл серной кислоты и смесь кипятят с обратным холодильником в течение 30 мин. После охлаждения приливают 100 мл воды и 25 мл 0,5 и. раствора иодида калия и через 4 мин титруют 0,1 н. раствором тиосульфата натрия с применением в качестве лндикатора крахмала. [c.197]
В качестве растворителя для проведения реакции дегидрохлорирования был выбран глицерин. Выбор его обусловлен тем, что он инертен в отношении исходных реагентов, хорошо растворяет карбонат натрия и ограниченно — побочно образующийся хлорид натрия. Щелочной гидролиз и дегидрохлорирование ЭПХГ в среде глицерина представляет также большой практический интерес, так как глицерин является конечным продуктом реакции и применение его в качестве среды исключает необходимость введения в реакционную систему новых компонентов. [c.118]
Все летучие ингибиторы (НДА, фосфатный, бензоатный, уротропи-иовый, карбонат и бензоат моноэтаноламина) используют в виде ингибированной бумаги, порошка или растворов. Нелетучий ингибитор — нитрит натрия — применяют в виде загущенного 30 %-ного водного раствора бензоат натрия — в виде ингибированной бумаги. Приведенные способы применения ингибиторов атмосферной коррозии целесообразно использовать в основном для консервации запасных частей и инструментов. [c.191]
Абсорбция НаЗ и СОа этаноламипами целесообразна, когда концентрация этих примесей в газе не превышает 2—2,5 мол. %. При более высоких концентрациях выгодно применение таких дешевых абсорбентов, как вода или водные растворы карбонатов натрия (Г а СОз) или калия (К2СО3) — поташа. Подобные абсорбенты обычно используют для предварительной очистки газов с доведением концентрации Н З и СО до 2—2,5 мол. %, а окончательная их очистка от Н38 и СО2 осуществляется этаноламипами. [c.162]
chem21.info
Натрия карбонат — это… Что такое Натрия карбонат?
Карбона́т на́трия — химическое соединение Na2CO3, натриевая соль угольной кислоты.
Сода — общее название технических натриевых солей угольной кислоты.
Название «сода» происходит от растения Salsola Soda, из золы которого её добывали. Кальцинированной соду называли потому, что для получения её из кристаллогидрата приходилось его кальцинировать (то есть нагревать до высокой температуры).
Каустической содой называют гидроксид натрия (NaOH).
Оксиды и гидроксиды
| Вид | Для Na | Для С |
|---|---|---|
| Гидроксид | NaOH | h3CO3 |
| Оксид | Na2O | CO2 |
Нахождение в природе
В природе сода встречается в золе некоторых морских водорослей, а также в виде следующих минералов:
- нахколит NaHCO3
- трона Na2CO3·NaHCO3·2H2O
- натрон (сода) Na2CO3·10H2O
- термонатрит Na2CO3·Н2O.
Современные содовые озёра известны в Забайкалье и в Западной Сибири; большой известностью пользуется озеро Натрон в Танзании и озеро Сирлс в Калифорнии. Трона, имеющая промышленное значение, открыта в 1938 в составе эоценовой толщи Грин-Ривер (Вайоминг, США). Вместе с троной в этой осадочной толще обнаружено много, ранее считавшихся редкими, минералов, в том числе давсонит, который рассматривается как сырьё для получения соды и глинозёма. В США природная сода удовлетворяет более 40% потребности страны в этом полезном ископаемом. В России из-за отсутствия крупных месторождений сода из минералов не добывается.
Получение
До начала XIX века карбонат натрия получали преимущественно из золы некоторых морских водорослей и прибрежных растений.
Способ Леблана
В 1791 году французский химик Никола Леблана получил патент на «Способ превращения глауберовой соли в соду». По этому способу при температуре около 1000°C запекается смесь сульфата натрия («глауберовой соли»), мела или известняка (карбоната кальция) и древесного угля. Уголь восстанавливает сульфат натрия до сульфида:
Na2SO4 + 2C → Na2S + 2CO2↑Сульфид натрия реагирует с карбонатом кальция:
Na2S + СаСО3 → Na2CO3 + CaS
Полученный расплав обрабатывают водой, при этом карбонат натрия переходит в раствор, сульфид кальция отфильтровывают, затем раствор карбоната натрия упаривают. Сырую соду очищают перекристаллизацией. Процесс Леблана даёт соду в виде кристаллогидрата (см. выше), поэтому полученную соду обезвоживают кальцинированием.
Сульфат натрия получали обработкой каменной соли (хлорида натрия) серной кислотой:
2NaCl + H2SO4 → Na2SO4 + 2HCl↑
Выделявшийся в ходе реакции хлороводород улавливали водой с получением соляной кислоты.
Первый содовый завод такого типа в России был основан промышленником М. Прангом и появился в Барнауле в 1864 году.
После появления более экономичного (не остаётся в больших количествах побочный сульфид кальция) и технологичного способа Сольве, заводы, работающие по способу Леблана, стали закрываться. К 1900 90% предприятий производили соду по методу Сольве, а последние фабрики, работающие по методу Леблана закрылись в начале 1920-х.
Промышленный аммиачный способ (способ Сольве)
В 1861 году бельгийский инженер-химик Эрнест Сольве запатентовал метод производства соды, который используется и по сей день.
В насыщенный раствор хлорида натрия пропускают эквимолярные количества газообразных аммиака и диоксида углерода, то есть как бы вводят гидрокарбонат аммония NH4HCO3:
Выпавший остаток малорастворимого (9,6 г на 100 г воды при 20°C) гидрокарбоната натрия отфильтровывают и кальцинируют (обезвоживают) нагреванием до 140—160°C, при этом он переходит в карбонат натрия:
2NaHCO3 →(t) Na2CO3 + CO2↑ + H2OОбразовавшийся диоксид углерода и аммиак, выделенный из маточного раствора на первой стадии процесса по реакции:
возвращают в производственный цикл.
Первый содовый завод такого типа в мире был открыт в 1863 в Бельгии; первый завод такого типа в России был основан в районе уральского поселка Березники фирмой «Любимов, Сольве и Ко» в 1883 году. Его производительность составляла 20 тысяч тонн соды в год.
До сих пор этот способ остаётся основным способом получения соды во всех странах.
Способ Хоу
Разработан китайским химиком Хоу (Hou Debang) в 1930-х годах. Отличается от процесса Сольве тем, что не использует карбонат кальция.
По способу Хоу в раствор хлорида натрия при температуре 40 градусов подается диоксид углерода и аммиак. Менее растворимый гидрокарбонат натрия в ходе реакции выпадает в осадок (как и в методе Сольве). Затем раствор охлаждают до 10 градусов. При этом выпадает в осадок хлорид аммония, а раствор используют повторно для производства следующих порций соды.
В настоящее время в ряде стран практически весь искусственно производящийся карбонат натрия вырабатывается по методу Хоу.
Свойства
Кристаллогидраты карбоната натрия существуют в разных формах: бесцветный моноклинный Na2CO3·10H2O, при 32,017°С переходит в бесцветный ромбический Na2CO3·7H2O, последний при нагревании до 35,27°C бесцветный переходит в ромбический Na2CO3·H2O.
Безводный карбонат натрия представляет собой бесцветный кристаллический порошок.
| Параметр | Безводный карбонат натрия | Декагидрат Na2CO3·10H2O |
|---|---|---|
| Молекулярная масса | 105,99 а.е.м. | 286,14 а.е.м. |
| Температура плавления | 852°C (по другим источникам, 853°C) | 32°С |
| Растворимость | Не растворим в ацетоне, и сероуглероде, мало растворим в этаноле хорошо растворим в глицерине, и воде (см. таблицу ниже) | растворим в воде, не растворим в этаноле |
| Плотность ρ | 2,53 г/см3 (при 20°C) | 1,446 г/см3 (при 17°C) |
| Стандартная энтальпия образования ΔH | −1131 кДж/моль (т) (при 297 К) | −4083,5 кДж/моль ((т) (при 297 К) |
| Стандартная энергия Гиббса образования G | −1047,5 кДж/моль (т) (при 297 К) | −3242,3 кДж/моль ((т) (при 297 К) |
| Стандартная энтропия образования S | 136,4 Дж/моль·K (т) (при 297 К) | |
| Стандартная мольная теплоёмкость Cp | 109,2 Дж/моль·K (жг) (при 297 К) |
| Температура, °C | 0 | 10 | 20 | 25 | 30 | 40 | 50 | 60 | 80 | 100 | 120 | 140 |
| Растворимость, г Na2CO3 на 100 г H2O | 7 | 12,2 | 21,8 | 29,4 | 39,7 | 48,8 | 47,3 | 46,4 | 45,1 | 44,7 | 42,7 | 39,3 |
В водном растворе карбонат натрия гидролизуется, что обеспечивает щелочную реакцию среды. Уравнение гидролиза (в ионной форме):
CO32- + H2O ↔ HCO3— + OH—
Первая константа диссоциации угольной кислоты равна 4,5·10-7. Все кислоты, более сильные, чем угольная, вытесняют её в реакции с карбонатом натрия. Так как угольная кислота крайне нестойкая, она тут же разлагается на воду и углекислый газ:
Na2CO3 + H2SO4 → Na2SO4 + CO2↑ + H2O
Применение
Карбонат натрия используют в стекольном производстве, мыловарении и производстве синтетических моющих средств, эмалей, для получения ультрамарина. Также он применяется для умягчения воды паровых котлов и вообще устранения жёсткости воды, для обезжиривания металлов и десульфатизации доменного чугуна. Карбонат натрия — исходный продукт для получения NaOH, Na2B4O7, Na2HPO4.
В пищевой промышленности зарегистрирован в качестве пищевой добавки E500, регулятора кислотности, разрыхлителя, препятствующего комкованию и слёживанию.[1]
Ссылки
Wikimedia Foundation. 2010.
dic.academic.ru
(i) Карбонат натрия | |
Органолептические свойства | кристаллический или гранулированный порошок белого цвета либо же бесцветные кристаллы |
Эмпирическая формула | Na2CO3(б/в), Na2CO3·xh3O (гидротированный), где х принимает значение либо единицы, либо десяти |
Естественные источники | минералы термонатрит и натрон, а также рапе соленых озер и грунтовый рассол |
Получение | карбонат натрия получают посредствам прокаливания гидрокарбоната натрия, добытого из залежей соляных рассолов, встречающихся в природе |
Разрешение для применения в пищевой промышленности | разрешен |
Функции, выполняемые при производстве продуктов питания | стабилизатор, регулятор кислотности, а также средство для снятия кожицы с овощей и фруктов |
Применение в пищевой промышленности | как правило, карбонат натрия применяется в качестве стабилизатора в мясные продукты; также его можно встретить в тех продуктах, что содержат какао-порошок, например, в шоколаде, а также в продуктах с наличием в них сухого молока |
Альтернативное применение | применяют карбонат натрия также в изготовлении моющих средств и мыла, целлюлозы, стекла, а также в производстве алюминия, а кроме того в производстве пигментов, необходимых в нефтеперарботке |
Синонимичные названия | натрий углекислый, sodium carbonate, динатрий карбонат, сода кальцинированная, soda ash, sodium salt of carbonic acid |
(ii) Гидрокарбонат натрия | |
Органолептические свойства | либо кристаллический порошок белого цвета, либо же кристаллы вовсе не имеющие цвет |
Эмпирическая формула | NaHCO3 |
Получение | получают гидрокарбонат натрия посредствам взаимодействия насыщенного водного раствора обыкновенной поваренной соли с аммиаком и углекислым газом или же посредствам насыщения углекислым газом раствора карбоната натрия |
Разрешение для применения в пищевой промышленности | разрешен |
Функции, выполняемые при производстве продуктов питания | стабилизатор, регулятор кислотности, средство для снятия кожицы с овощей и фруктов, а также разрыхлитель и средство против слеживания и комкования |
Применение в пищевой промышленности | наиболее широкое применение гидрокарбонат натрия получил в изготовлении всевозможной выпечки, в качестве разрыхлителя теста, однако встретить его можно еще и в таких продуктах: желе, мармелады из цитрусовых, джемы, сухое молоко, сухие сливки, сгущенное молоко, маргарин, твердые сорта сыров, плавленые сыры, томатный концентрат, мясные продукты, а также продукты, изготовленные с применением какао-порошка (в т.ч. шоколад) |
Альтернативное применение | применяют гидрокарбонат натрия для изготовления наполнителя огнетушителей, а также данную пищевую добавку используют в качестве лекарственного средства |
Синонимичные названия | бикарбонат натрия, сода питьевая (пищевая), двууглекислый натрий, натрий кислый углекислый, bicarbonate of soda, sodium bicarbonate, baking soda, sodium hydrogen carbonate, sodium salt of carbonic acid |
(iii) Смесь карбоната натрия с его гидрокарбонатом | |
Органолептические свойства | данная смесь может принимать форму, кристаллов, хлопьев либо же кристаллического порошка белого цвета |
Эмпирическая формула | Na2CO3·NaHCO3·2H2O |
Естественные источники | природными источниками смеси являются карбонат и гидрокарбонат натрия |
Получение | получают вещество посредствам прокаливания гидрокарбоната натрия при определенных условиях |
Разрешение для применения в пищевой промышленности | разрешен |
Функции, выполняемые при производстве продуктов питания | стабилизатор, регулятор кислотности, средство для снятия кожицы с овощей и фруктов, а также разрыхлитель и средство против слеживания и комкования |
Применение в пищевой промышленности | наиболее широкое применение смесь карбоната и гидрокарбоната натрия получила в изготовлении всевозможной выпечки, в качестве разрыхлителя теста, однако встретить ее можно еще и в таких продуктах: желе, мармелады из цитрусовых, джемы, сухое молоко, сухие сливки, сгущенное молоко, маргарин, сливочное масло, твердые сорта сыров, плавленые сыры, томатный концентрат, а также продукты, изготовленные с применением какао-порошка (в т.ч. шоколад) |
Альтернативное применение | применяют данную добавку еще и для производства наполнителя в огнетушители |
Синонимичные названия | сесквикарбонат натрия, sodium sesquicarbonate, натриевые соли угольной кислоты, sodium salts of carbonic acid |
xcook.info
Карбонаты натрия (Е500): полезные свойства и вред
 Вещества относятся к ненастоящим разрыхлителям, имеют незначительную опасность. Е500 – элементы, которые используют в разных качествах. Сода препятствует комкованию. В жизни карбонат натрия именуют содой. По химическим составляющим это ни что другое, как обычные производные угольной кислоты.
Вещества относятся к ненастоящим разрыхлителям, имеют незначительную опасность. Е500 – элементы, которые используют в разных качествах. Сода препятствует комкованию. В жизни карбонат натрия именуют содой. По химическим составляющим это ни что другое, как обычные производные угольной кислоты.
Раствор чаще всего применяют при готовке блюд в виде карбоната натрия, гидрокарбоната, их смеси.
Краткие сведения
Название походит из латыни, от наименования растения. В прошлые века ее усердно получали из золы. Кальцинированная сода была создана в конце 18-го века Лебланом, однако пищевая – в 1861 г. Сольвэ.
Карбонат натрия кислота получается несколькими способами. Наиболее распространенный из них – методика Сольве. Так добывают более 90% всех объемов промышленного вещества. Для этого нужен хлорид натрия, аммиак.
Вещество получается в процессе кальцинирования (увеличение температурных значений). От этого оно именуется кальцинированным. Ряд стран получает из месторождений. Также изготавливается промышленным способом в тех регионах, где отсутствуют залежи минералов.
Методики синтеза
Используют «сухой» и «мокрый» способы. В основе процесса – карбонизация (присоединение углекислоты). Отмечают перекристаллизационные преображения. Методики отличаются готовкой раствора. При сухом – кальцинированные элементы растворяются водой, а при мокром применяют технический бикарбонат.
Разложение вещества при постепенном возрастании температуры именуют декарбонизацией.
Содовые элементы раствора под влиянием диоксида углерода осаждаются. Чистая пищевая содовая часть отделяется, а маточные компоненты вновь идут на получение первичного раствора.
Главные свойства
| Систематическое наименование | Карбонат натрия |
|---|---|
| Традиционные наименования | Кальцинированная сода |
| Молекулярная масса | 105,99 г/моль |
| Плотность | 2,53 г/см3 |
| Растворимость | 21,8 г/100 мл |
Масса уникальных характеристик определила ценную роль элемента для человека. Внешний облик являет собой бесцветные кристаллические элементы. Иногда встречаются формы порошкообразного элемента беловатого окраса.
По общеобразовательным качествам пищевой эмульгатор отличается немаленькой температурой плавления (853 градуса).
Вещество не теряет своей способности отменно растворяться в водных структурах (в отличие от этанола). Особенность кроется в способности поглощать углекислоту.
Применение
Массовая доля карбоната натрия довольно весомая в кондитерстве и в кулинарии в целом. Ведь вещество просто незаменимо при приготовлении выпечки. Зачастую Е500 входит как в готовую продукцию, так и в смеси.
 Соду можно встретить в:
Соду можно встретить в:
- колбасе;
- мясной продукции;
- сухом молоке;
- продуктах, что содержат какао-порошок.
Сода также применяется в различных секторах промышленности. Больше всего ее применяют в стекольной промышленности, цветной металлургии, химическом производстве.
Особенности использования в кулинарии
Пищевая сода – незаменимый элемент добавки, который используется в составе изделий в роли разрыхлителя. Обнаружить ее возможно в сгущенном молоке, мармеладе, джеме, маргарине.
Взаимодействие карбоната натрия с продуктами используется во время приготовления брецелей и рулетов. Технология подобной нестандартной обработки разведенным щелочным веществом целиком оправдана. Так можно безопасно изменить кислотность продукции. В итоге это приводит к возникновению необычайно хрусткой корочки на поверхности продукции. Карбонат натрия — незаменимый элемент. Без него никогда не получится идеальная лапша. Все дело в том, что нежность содового элемента в рассоле сохраняет вкусовое качество макарон. Добавка используется при готовке шербета. Так действует карбонат и несильные кислотные элементы. При этом образуется углекислота из-за слюны.
Карбонат натрия серная кислота содержится в большинстве паст по уходу за ротовой полостью и зубными элементами. Это пенообразователь, абразив, который на время минимизирует кислотность во рту. Подобным образом предупреждаются многие недуги.
Влияние
По итогам численных мировых исследований, реакции карбоната натрия не причиняют никакого вреда клеткам организма. То есть вещество числится в категории неопасных добавок. Без передозировки никогда и никому не наносит вред.
Но определенный вред кислота карбоната все же несет.
Существуют доказанные факты, согласно которым чувствительный организм плохо переносит вещество. Возникает затруднение дыхания, обмороки.
В экспериментах показано, что формула данного вещества неблагоприятно влияет на печень и мозг живого организма. Длительное потребление продуктов с Е500 увеличивает риски появления аллергических реакций на руках и голове.
Карбонат натрия и соляная кислота – самые известные антагонисты. Об их противоположном влиянии ведомо давно. Существует даже старинный способ победить изжогу – размешать в воде соду. «Пожар» исчезнет в считанные минуты. Это никак не методика терапии. Методика действенно и скоро позволяет избавиться от изжоги на непродолжительный период. Переизбыток соды способен провоцировать рези, даже аллергические признаки.
На территории многих стран разрешено применение Е500 в качестве пищевой добавки.
Упаковка, транспортировка
Перемещают данное вещество любым транспортом, но исключительно в плотно закрытых объектах. Элемент совершенно безопасен, поскольку лишен даже минимальной токсичности. Сохраняется содовый элемент только в закрытых упаковках. Крайне важно не допустить присутствия влаги в данной структуре. На протяжении года истекает гарантийный срок на сохранение содового раствора. При этом общий срок пригодности не лимитирован.
Содовый элемент можно по праву назвать главным разрыхлителем при выпечке. Данное вещество при нагревании выделяет углекислоту. За счет этого тесто становится мягким, пушистым. Сода выступает как самостоятельное вещество для разрыхления либо в комплексном составе пекарского порошка. При этом важно не переусердствовать с дозировкой. Содовый элемент оставляет в готовом продукте довольно неприятный, но безвкусный привкус. Соду важно добавлять в муку, кислые компоненты – только в жидкость.
foodandhealth.ru
Карбонат натрия — Википедия (с комментариями)
Материал из Википедии — свободной энциклопедии
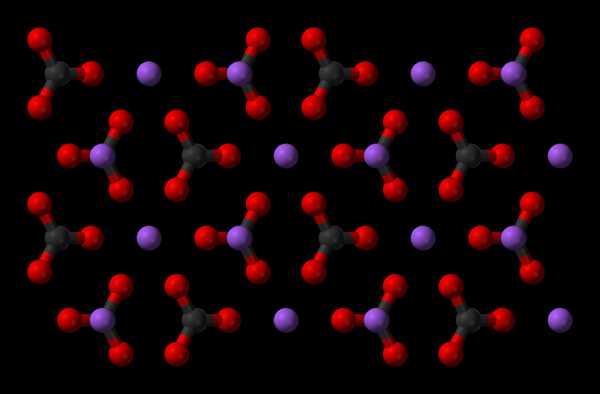
Карбона́т на́трия Na2CO3 — химическое соединение, натриевая соль угольной кислоты.
Сода — общее название технических натриевых солей угольной кислоты.
- Na2CO3 (карбонат натрия) — кальцинированная сода, бельевая сода
- Na2CO3·10H2O (декагидрат карбоната натрия, содержит 62,5 % кристаллизационной воды) — стиральная сода; иногда выпускается в виде Na2CO3·H2O или Na2CO3·7H2O
- NaHCO3 (гидрокарбонат натрия) — пищевая сода, натрий двууглекислый (устар.), бикарбонат натрия
Название «сода» происходит от растения солянка содоносная[en] (лат. Salsola soda), из золы которого её добывали. Кальцинированной соду называли потому, что для получения её из кристаллогидрата приходилось его кальцинировать (то есть нагревать до высокой температуры).
Каустической содой называют гидроксид натрия (NaOH).
Оксиды и гидроксиды
| Вид | Для Na | Для С |
|---|---|---|
| Гидроксид | NaOH | H2CO3 |
| Оксид | Na2O | CO2 |
Нахождение в природе
В природе сода встречается в золе некоторых морских водорослей, а также в виде следующих минералов:
Современные содовые озёра известны в Забайкалье и в Западной Сибири; большой известностью пользуется озеро Натрон в Танзании и озеро Сирлс в Калифорнии. Трона, имеющая промышленное значение, открыта в 1938 в составе эоценовой толщи Грин-Ривер (Вайоминг, США). Вместе с троной в этой осадочной толще обнаружено много ранее считавшихся редкими минералов, в том числе давсонит, который рассматривается как сырьё для получения соды и глинозёма. В США природная сода удовлетворяет более 40 % потребности страны в этом полезном ископаемом.
Получение
До начала XIX века карбонат натрия получали преимущественно из золы некоторых морских водорослей и прибрежных растений.
Способ Леблана
В 1791 году французский химик Никола Леблан получил патент на «Способ превращения глауберовой соли в соду». По этому способу при температуре около 1000 °C запекается смесь сульфата натрия («глауберовой соли»), мела или известняка (карбоната кальция) и древесного угля. Уголь восстанавливает сульфат натрия до сульфида:
- Na2SO4 + 2C → Na2S + 2CO2↑.
Сульфид натрия реагирует с карбонатом кальция:
- Na2S + СаСО3 → Na2CO3 + CaS.
Полученный расплав обрабатывают водой, при этом карбонат натрия переходит в раствор, сульфид кальция отфильтровывают, затем раствор карбоната натрия упаривают. Сырую соду очищают перекристаллизацией. Процесс Леблана даёт соду в виде кристаллогидрата (см. выше), поэтому полученную соду обезвоживают кальцинированием.
Сульфат натрия получали обработкой каменной соли (хлорида натрия) серной кислотой:
- 2NaCl + H2SO4 → Na2SO4 + 2HCl↑.
Выделявшийся в ходе реакции хлороводород улавливали водой с получением соляной кислоты.
Первый содовый завод такого типа в России был основан промышленником М. Прангом и появился в Барнауле в 1864 году.
После появления более экономичного (не остаётся в больших количествах побочный сульфид кальция) и технологичного способа Сольве, заводы, работающие по способу Леблана, стали закрываться. К 1900 году 90 % предприятий производили соду по методу Сольве, а последние фабрики, работающие по методу Леблана закрылись в начале 1920-х.
Промышленный аммиачный способ (способ Сольве)
 В 1861 году бельгийский инженер-химик Эрнест Сольве запатентовал метод производства соды, который используется и по сей день.
В 1861 году бельгийский инженер-химик Эрнест Сольве запатентовал метод производства соды, который используется и по сей день.
В насыщенный раствор хлорида натрия пропускают эквимолярные количества газообразных аммиака и диоксида углерода, то есть как бы вводят гидрокарбонат аммония NH4HCO3:
- NH3 + CO2 + H2O + NaCl → NaHCO3 + NH4Cl.
Выпавший остаток малорастворимого (9,6 г на 100 г воды при 20 °C) гидрокарбоната натрия отфильтровывают и кальцинируют (обезвоживают) нагреванием до 140—160 °C, при этом он переходит в карбонат натрия:
- 2NaHCO3 →(t) Na2CO3 + CO2↑ + H2O.
Образовавшийся CO2 возвращают в производственный цикл. Хлорид аммония NH4Cl обрабатывают гидроксидом кальция Ca(OH)2:
- 2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3↑ + 2H2O,
и полученный NH3 также возвращают в производственный цикл.
Таким образом, единственным отходом производства является хлорид кальция, не имеющий широкого промышленного применения, кроме использования в качестве противообледеняющего реагента для посыпания улиц.
Первый содовый завод такого типа в мире был открыт в 1863 в Бельгии; первый завод такого типа в России был основан в районе уральского города Березники фирмой «Любимов, Сольве и Ко» в 1883 году. Его производительность составляла 20 тысяч тонн соды в год. В 2010 году ФАС России отказала фирме Solvay в покупке этого завода, разрешив покупку группе Башкирская химия (ей также принадлежит завод Сода).К:Википедия:Статьи без источников (тип: не указан)[источник не указан 2431 день]
До сих пор этот способ остаётся основным способом получения соды во всех странах.
Способ Хоу
Разработан китайским химиком Хоу (Hou Debang) в 1930-х годах. Отличается от процесса Сольве тем, что не использует гидроксид кальция.
По способу Хоу в раствор хлорида натрия при температуре 40 градусов подается диоксид углерода и аммиак. Менее растворимый гидрокарбонат натрия в ходе реакции выпадает в осадок (как и в методе Сольве). Затем раствор охлаждают до 10 градусов. При этом выпадает в осадок хлорид аммония, а раствор используют повторно для производства следующих порций соды.
Сравнение способов
По методу Хоу в качестве побочного продукта образуется NH4Cl вместо CaCl2 по методу Сольве.
Способ Сольве был разработан до появления процесса Габера, в то время аммиак был в дефиците, поэтому регенерировать его из NH4Cl было необходимо. Метод Хоу появился позже, необходимость регенерации аммиака уже не стояла так остро, соответственно, аммиак можно было не извлекать, а использовать его как азотное удобрение в виде соединения NH4Cl.
Тем не менее NH4Cl содержит хлор, избыток которого вреден для многих растений, поэтому использование NH4Cl в качестве удобрения ограничено. В свою очередь рис хорошо переносит избыток хлора, и в Китае, где применяется NH4Cl для рисоводства, метод Хоу, дающий NH4Cl в качестве побочного продукта, более широко представлен по сравнению с другими регионами.
В настоящее время в ряде стран практически весь искусственно производящийся карбонат натрия вырабатывается по методу Сольве (включая метод Хоу как модификацию), а именно в Европе 94 % искусственно производимой соды, во всем мире — 84 % (2000 год)[1].
Свойства
Кристаллогидраты карбоната натрия существуют в разных формах: бесцветный моноклинный Na2CO3·10H2O, при 32,017 °C переходит в бесцветный ромбический Na2CO3·7H2O, последний при нагревании до 35,27 °C бесцветный переходит в ромбический Na2CO3·H2O.
Безводный карбонат натрия представляет собой бесцветный кристаллический порошок.
| Параметр | Безводный карбонат натрия | Декагидрат Na2CO3·10H2O |
|---|---|---|
| Молекулярная масса | 105,99 а. е. м. | 286,14 а. е. м. |
| Температура плавления | 852 °C (по другим источникам, 853 °C) | 32 °C |
| Растворимость | Не растворим в ацетоне, и сероуглероде, мало растворим в этаноле хорошо растворим в глицерине, и воде (см. таблицу ниже) | растворим в воде, не растворим в этаноле |
| Плотность ρ | 2,53 г/см³ (при 20 °C) | 1,446 г/см³ (при 17 °C) |
| Стандартная энтальпия образования ΔH | −1131 кДж/моль (т) (при 297 К) | −4083,5 кДж/моль ((т) (при 297 К) |
| Стандартная энергия Гиббса образования G | −1047,5 кДж/моль (т) (при 297 К) | −3242,3 кДж/моль ((т) (при 297 К) |
| Стандартная энтропия образования S | 136,4 Дж/моль·K (т) (при 297 К) | |
| Стандартная мольная теплоёмкость Cp | 109,2 Дж/моль·K (жг) (при 297 К) |
| Температура, °C | 0 | 10 | 20 | 25 | 30 | 40 | 50 | 60 | 80 | 100 | 120 | 140 |
| Растворимость, г Na2CO3 на 100 г H2O | 7 | 12,2 | 21,8 | 29,4 | 39,7 | 48,8 | 47,3 | 46,4 | 45,1 | 44,7 | 42,7 | 39,3 |
В водном растворе карбонат натрия гидролизуется, что обеспечивает щелочную реакцию среды. Уравнение гидролиза (в ионной форме):
CO32− + H2O ↔ HCO3− + OH−
Первая константа диссоциации угольной кислоты равна 4,5·10−7. Все кислоты, более сильные, чем угольная, вытесняют её в реакции с карбонатом натрия. Так как угольная кислота крайне нестойкая, она тут же разлагается на воду и углекислый газ:
Na2CO3 + H2SO4 → Na2SO4 + CO2↑ + H2O
Применение
Карбонат натрия используют в стекольном производстве; мыловарении и производстве стиральных и чистящих порошков; эмалей, для получения ультрамарина. Также он применяется для смягчения воды паровых котлов и вообще уменьшения жёсткости воды, для обезжиривания металлов и десульфатизации доменного чугуна. Карбонат натрия — исходный продукт для получения NaOH, Na2B4O7, Na2HPO4. Может использоваться в сигаретных фильтрах[2].
В пищевой промышленности карбонаты натрия зарегистрированы в качестве пищевой добавки E500, — регулятора кислотности, разрыхлителя, препятствующего комкованию и слёживанию. Карбонат натрия (кальцинированная сода, Na2CO3) имеет код 500i, гидрокарбонат натрия (пищевая сода, NaHCO3) — 500ii, их смесь — 500iii.
Также используется для приготовления проявителя фотоматериалов.
Напишите отзыв о статье «Карбонат натрия»
Примечания
- ↑ [www.webcitation.org/5W0IxdohY WebCite query result]
- ↑ [bd.patent.su/2292000-2292999/pat/servl/servlet3466.html Патент на изобретение]
Отрывок, характеризующий Карбонат натрия
– Он на козлы. Ведь ты на козлы, Петя? – кричала Наташа.Соня не переставая хлопотала тоже; но цель хлопот ее была противоположна цели Наташи. Она убирала те вещи, которые должны были остаться; записывала их, по желанию графини, и старалась захватить с собой как можно больше.
Во втором часу заложенные и уложенные четыре экипажа Ростовых стояли у подъезда. Подводы с ранеными одна за другой съезжали со двора.
Коляска, в которой везли князя Андрея, проезжая мимо крыльца, обратила на себя внимание Сони, устраивавшей вместе с девушкой сиденья для графини в ее огромной высокой карете, стоявшей у подъезда.
– Это чья же коляска? – спросила Соня, высунувшись в окно кареты.
– А вы разве не знали, барышня? – отвечала горничная. – Князь раненый: он у нас ночевал и тоже с нами едут.
– Да кто это? Как фамилия?
– Самый наш жених бывший, князь Болконский! – вздыхая, отвечала горничная. – Говорят, при смерти.
Соня выскочила из кареты и побежала к графине. Графиня, уже одетая по дорожному, в шали и шляпе, усталая, ходила по гостиной, ожидая домашних, с тем чтобы посидеть с закрытыми дверями и помолиться перед отъездом. Наташи не было в комнате.
– Maman, – сказала Соня, – князь Андрей здесь, раненый, при смерти. Он едет с нами.
Графиня испуганно открыла глаза и, схватив за руку Соню, оглянулась.
– Наташа? – проговорила она.
И для Сони и для графини известие это имело в первую минуту только одно значение. Они знали свою Наташу, и ужас о том, что будет с нею при этом известии, заглушал для них всякое сочувствие к человеку, которого они обе любили.
– Наташа не знает еще; но он едет с нами, – сказала Соня.
– Ты говоришь, при смерти?
Соня кивнула головой.
Графиня обняла Соню и заплакала.
«Пути господни неисповедимы!» – думала она, чувствуя, что во всем, что делалось теперь, начинала выступать скрывавшаяся прежде от взгляда людей всемогущая рука.
– Ну, мама, все готово. О чем вы?.. – спросила с оживленным лицом Наташа, вбегая в комнату.
– Ни о чем, – сказала графиня. – Готово, так поедем. – И графиня нагнулась к своему ридикюлю, чтобы скрыть расстроенное лицо. Соня обняла Наташу и поцеловала ее.
Наташа вопросительно взглянула на нее.
– Что ты? Что такое случилось?
– Ничего… Нет…
– Очень дурное для меня?.. Что такое? – спрашивала чуткая Наташа.
Соня вздохнула и ничего не ответила. Граф, Петя, m me Schoss, Мавра Кузминишна, Васильич вошли в гостиную, и, затворив двери, все сели и молча, не глядя друг на друга, посидели несколько секунд.
Граф первый встал и, громко вздохнув, стал креститься на образ. Все сделали то же. Потом граф стал обнимать Мавру Кузминишну и Васильича, которые оставались в Москве, и, в то время как они ловили его руку и целовали его в плечо, слегка трепал их по спине, приговаривая что то неясное, ласково успокоительное. Графиня ушла в образную, и Соня нашла ее там на коленях перед разрозненно по стене остававшимися образами. (Самые дорогие по семейным преданиям образа везлись с собою.)
На крыльце и на дворе уезжавшие люди с кинжалами и саблями, которыми их вооружил Петя, с заправленными панталонами в сапоги и туго перепоясанные ремнями и кушаками, прощались с теми, которые оставались.
Как и всегда при отъездах, многое было забыто и не так уложено, и довольно долго два гайдука стояли с обеих сторон отворенной дверцы и ступенек кареты, готовясь подсадить графиню, в то время как бегали девушки с подушками, узелками из дому в кареты, и коляску, и бричку, и обратно.
– Век свой все перезабудут! – говорила графиня. – Ведь ты знаешь, что я не могу так сидеть. – И Дуняша, стиснув зубы и не отвечая, с выражением упрека на лице, бросилась в карету переделывать сиденье.
– Ах, народ этот! – говорил граф, покачивая головой.
Старый кучер Ефим, с которым одним только решалась ездить графиня, сидя высоко на своих козлах, даже не оглядывался на то, что делалось позади его. Он тридцатилетним опытом знал, что не скоро еще ему скажут «с богом!» и что когда скажут, то еще два раза остановят его и пошлют за забытыми вещами, и уже после этого еще раз остановят, и графиня сама высунется к нему в окно и попросит его Христом богом ехать осторожнее на спусках. Он знал это и потому терпеливее своих лошадей (в особенности левого рыжего – Сокола, который бил ногой и, пережевывая, перебирал удила) ожидал того, что будет. Наконец все уселись; ступеньки собрались и закинулись в карету, дверка захлопнулась, послали за шкатулкой, графиня высунулась и сказала, что должно. Тогда Ефим медленно снял шляпу с своей головы и стал креститься. Форейтор и все люди сделали то же.
– С богом! – сказал Ефим, надев шляпу. – Вытягивай! – Форейтор тронул. Правый дышловой влег в хомут, хрустнули высокие рессоры, и качнулся кузов. Лакей на ходу вскочил на козлы. Встряхнуло карету при выезде со двора на тряскую мостовую, так же встряхнуло другие экипажи, и поезд тронулся вверх по улице. В каретах, коляске и бричке все крестились на церковь, которая была напротив. Остававшиеся в Москве люди шли по обоим бокам экипажей, провожая их.
Наташа редко испытывала столь радостное чувство, как то, которое она испытывала теперь, сидя в карете подле графини и глядя на медленно подвигавшиеся мимо нее стены оставляемой, встревоженной Москвы. Она изредка высовывалась в окно кареты и глядела назад и вперед на длинный поезд раненых, предшествующий им. Почти впереди всех виднелся ей закрытый верх коляски князя Андрея. Она не знала, кто был в ней, и всякий раз, соображая область своего обоза, отыскивала глазами эту коляску. Она знала, что она была впереди всех.
В Кудрине, из Никитской, от Пресни, от Подновинского съехалось несколько таких же поездов, как был поезд Ростовых, и по Садовой уже в два ряда ехали экипажи и подводы.
Объезжая Сухареву башню, Наташа, любопытно и быстро осматривавшая народ, едущий и идущий, вдруг радостно и удивленно вскрикнула:
– Батюшки! Мама, Соня, посмотрите, это он!
– Кто? Кто?
– Смотрите, ей богу, Безухов! – говорила Наташа, высовываясь в окно кареты и глядя на высокого толстого человека в кучерском кафтане, очевидно, наряженного барина по походке и осанке, который рядом с желтым безбородым старичком в фризовой шинели подошел под арку Сухаревой башни.
– Ей богу, Безухов, в кафтане, с каким то старым мальчиком! Ей богу, – говорила Наташа, – смотрите, смотрите!
– Да нет, это не он. Можно ли, такие глупости.
– Мама, – кричала Наташа, – я вам голову дам на отсечение, что это он! Я вас уверяю. Постой, постой! – кричала она кучеру; но кучер не мог остановиться, потому что из Мещанской выехали еще подводы и экипажи, и на Ростовых кричали, чтоб они трогались и не задерживали других.
Действительно, хотя уже гораздо дальше, чем прежде, все Ростовы увидали Пьера или человека, необыкновенно похожего на Пьера, в кучерском кафтане, шедшего по улице с нагнутой головой и серьезным лицом, подле маленького безбородого старичка, имевшего вид лакея. Старичок этот заметил высунувшееся на него лицо из кареты и, почтительно дотронувшись до локтя Пьера, что то сказал ему, указывая на карету. Пьер долго не мог понять того, что он говорил; так он, видимо, погружен был в свои мысли. Наконец, когда он понял его, посмотрел по указанию и, узнав Наташу, в ту же секунду отдаваясь первому впечатлению, быстро направился к карете. Но, пройдя шагов десять, он, видимо, вспомнив что то, остановился.
Высунувшееся из кареты лицо Наташи сияло насмешливою ласкою.
– Петр Кирилыч, идите же! Ведь мы узнали! Это удивительно! – кричала она, протягивая ему руку. – Как это вы? Зачем вы так?
Пьер взял протянутую руку и на ходу (так как карета. продолжала двигаться) неловко поцеловал ее.
– Что с вами, граф? – спросила удивленным и соболезнующим голосом графиня.
– Что? Что? Зачем? Не спрашивайте у меня, – сказал Пьер и оглянулся на Наташу, сияющий, радостный взгляд которой (он чувствовал это, не глядя на нее) обдавал его своей прелестью.
– Что же вы, или в Москве остаетесь? – Пьер помолчал.
– В Москве? – сказал он вопросительно. – Да, в Москве. Прощайте.
– Ах, желала бы я быть мужчиной, я бы непременно осталась с вами. Ах, как это хорошо! – сказала Наташа. – Мама, позвольте, я останусь. – Пьер рассеянно посмотрел на Наташу и что то хотел сказать, но графиня перебила его:
– Вы были на сражении, мы слышали?
– Да, я был, – отвечал Пьер. – Завтра будет опять сражение… – начал было он, но Наташа перебила его:
– Да что же с вами, граф? Вы на себя не похожи…
– Ах, не спрашивайте, не спрашивайте меня, я ничего сам не знаю. Завтра… Да нет! Прощайте, прощайте, – проговорил он, – ужасное время! – И, отстав от кареты, он отошел на тротуар.
Наташа долго еще высовывалась из окна, сияя на него ласковой и немного насмешливой, радостной улыбкой.
Пьер, со времени исчезновения своего из дома, ужа второй день жил на пустой квартире покойного Баздеева. Вот как это случилось.
Проснувшись на другой день после своего возвращения в Москву и свидания с графом Растопчиным, Пьер долго не мог понять того, где он находился и чего от него хотели. Когда ему, между именами прочих лиц, дожидавшихся его в приемной, доложили, что его дожидается еще француз, привезший письмо от графини Елены Васильевны, на него нашло вдруг то чувство спутанности и безнадежности, которому он способен был поддаваться. Ему вдруг представилось, что все теперь кончено, все смешалось, все разрушилось, что нет ни правого, ни виноватого, что впереди ничего не будет и что выхода из этого положения нет никакого. Он, неестественно улыбаясь и что то бормоча, то садился на диван в беспомощной позе, то вставал, подходил к двери и заглядывал в щелку в приемную, то, махая руками, возвращался назад я брался за книгу. Дворецкий в другой раз пришел доложить Пьеру, что француз, привезший от графини письмо, очень желает видеть его хоть на минутку и что приходили от вдовы И. А. Баздеева просить принять книги, так как сама г жа Баздеева уехала в деревню.
– Ах, да, сейчас, подожди… Или нет… да нет, поди скажи, что сейчас приду, – сказал Пьер дворецкому.
Но как только вышел дворецкий, Пьер взял шляпу, лежавшую на столе, и вышел в заднюю дверь из кабинета. В коридоре никого не было. Пьер прошел во всю длину коридора до лестницы и, морщась и растирая лоб обеими руками, спустился до первой площадки. Швейцар стоял у парадной двери. С площадки, на которую спустился Пьер, другая лестница вела к заднему ходу. Пьер пошел по ней и вышел во двор. Никто не видал его. Но на улице, как только он вышел в ворота, кучера, стоявшие с экипажами, и дворник увидали барина и сняли перед ним шапки. Почувствовав на себя устремленные взгляды, Пьер поступил как страус, который прячет голову в куст, с тем чтобы его не видали; он опустил голову и, прибавив шагу, пошел по улице.
wiki-org.ru

 Его можно получить несколькими способами, все они разные, но в этой статье будет рассказано лишь об одном. Необходимо смешать мел и древесный уголь с сульфатом натрия, а потом запечь эту смесь при температуре около 1000 о С. Уголь будет восстанавливать последний до сульфида, который при реакции с карбонатом кальция образует расплав сернистого кальция и искомого вещества. Его необходимо обработать водой, затем отфильтровать ненужный сульфид и упарить получившийся раствор. Образовавшийся сырой карбонат натрия очищается посредством перекристаллизации, а затем обезвоживается с помощью кальцинирования. Данный метод называется способом Леблана.
Его можно получить несколькими способами, все они разные, но в этой статье будет рассказано лишь об одном. Необходимо смешать мел и древесный уголь с сульфатом натрия, а потом запечь эту смесь при температуре около 1000 о С. Уголь будет восстанавливать последний до сульфида, который при реакции с карбонатом кальция образует расплав сернистого кальция и искомого вещества. Его необходимо обработать водой, затем отфильтровать ненужный сульфид и упарить получившийся раствор. Образовавшийся сырой карбонат натрия очищается посредством перекристаллизации, а затем обезвоживается с помощью кальцинирования. Данный метод называется способом Леблана. Отрасли, производящие стекло, стиральные порошки, мыло и эмали не обходятся без карбоната натрия, где его используют, чтобы получить ультрамарин. Также с помощью него устраняют жесткость воды, обезжиривают металлы и проводят десульфатизацию, объектом которой является доменный чугун. Карбонат натрия является хорошим окислителем и регулятором кислотности, его содержат моющие посуду средства, сигареты и пестициды. Также он известен как пищевая добавка E500, не дающая ингредиентам комковаться и слёживаться. Обсуждаемое сейчас вещество необходимо и для того, чтобы приготовить проявитель фотографий.
Отрасли, производящие стекло, стиральные порошки, мыло и эмали не обходятся без карбоната натрия, где его используют, чтобы получить ультрамарин. Также с помощью него устраняют жесткость воды, обезжиривают металлы и проводят десульфатизацию, объектом которой является доменный чугун. Карбонат натрия является хорошим окислителем и регулятором кислотности, его содержат моющие посуду средства, сигареты и пестициды. Также он известен как пищевая добавка E500, не дающая ингредиентам комковаться и слёживаться. Обсуждаемое сейчас вещество необходимо и для того, чтобы приготовить проявитель фотографий.