Те, кто увлекается химией или работает на химическом производстве, знают, насколько опасна серная кислота. При работе с этим видом яда требуется специальные средства защиты. В составе с другими элементами действие может либо усиливаться, либо уменьшаться, как, например, в случае взаимодействия серной кислоты и карбоната натрия.
Серная кислота
Любая кислота — это всегда сложное сочетание элементов нескольких видом веществ. Серная кислота — это два атома водорода и кислотная субстанция. Ее формула h3SO4. В чистом виде серная кислота — это жидкость, тяжелая и вязкая, напоминающая масло, имеющая кисловатый запах. Серная кислота хорошо взаимодействует с металлами и водой, является сильным окислителем почти для всех металлов, кроме золота, железа и алюминия. Именно поэтому промышленную серную кислоту транспортируют в стальных бочках или цистернах. Кислота образует среднюю и кислую соли.

Взаимодействие с карбонатом натрия
Химическая реакция карбоната натрия с серной кислотой всегда предсказуема. При взаимодействии:
- Выпадает осадок.
- Изменяется цвет.
- Выделяется газ.
- Выделяется свет.
Химическая формула реакции выглядит как Na2CO3 + h3SO4 → Na2SO4 + CO2 + h3O. В итоге образуется сульфат натрия и угольная кислота, а угольная кислота путем взаимозамещения разлагается на воду и углекислый газ.

Напомним, что карбонат натрия — это белое порошкообразное вещество, в народе известное как кальцинированная сода, которая может быть технической и пищевой. Само по себе это вещество неопасно и применяется даже в кулинарии и хлебопечении. Однако взаимодействие с серной кислотой карбонат натрия превращается в один из сильнейших ядов, которые используют в цветной и черной металлургии, в текстильном производстве, нефтегазовой отрасли и химической промышленности.
В школьной программе описание этих химических соединений можно найти в учебниках восьмого и девятого классов.
применение и формула — OneKu
Содержание статьи:- Серная кислота
- Взаимодействие с карбонатом натрия
Те, кто увлекается химией или работает на химическом производстве, знают, насколько опасна серная кислота. При работе с этим видом яда требуется специальные средства защиты. В составе с другими элементами действие может либо усиливаться, либо уменьшаться, как, например, в случае взаимодействия серной кислоты и карбоната натрия.
Серная кислота
Любая кислота — это всегда сложное сочетание элементов нескольких видом веществ. Серная кислота — это два атома водорода и кислотная субстанция. Ее формула h3SO4. В чистом виде серная кислота — это жидкость, тяжелая и вязкая, напоминающая масло, имеющая кисловатый запах. Серная кислота хорошо взаимодействует с металлами и водой, является сильным окислителем почти для всех металлов, кроме золота, железа и алюминия. Именно поэтому промышленную серную кислоту транспортируют в стальных бочках или цистернах. Кислота образует среднюю и кислую соли.
Вам будет интересно:Каково лексическое значение слова «классический»?
Взаимодействие с карбонатом натрия
Химическая реакция карбоната натрия с серной кислотой всегда предсказуема. При взаимодействии:
Химическая формула реакции выглядит как Na2CO3 + h3SO4 → Na2SO4 + CO2 + h3O. В итоге образуется сульфат натрия и угольная кислота, а угольная кислота путем взаимозамещения разлагается на воду и углекислый газ.
Напомним, что карбонат натрия — это белое порошкообразное вещество, в народе известное как кальцинированная сода, которая может быть технической и пищевой. Само по себе это вещество неопасно и применяется даже в кулинарии и хлебопечении. Однако взаимодействие с серной кислотой карбонат натрия превращается в один из сильнейших ядов, которые используют в цветной и черной металлургии, в текстильном производстве, нефтегазовой отрасли и химической промышленности.
В школьной программе описание этих химических соединений можно найти в учебниках восьмого и девятого классов.
Источник
Те, кто увлекается химией или работает на химическом производстве, знают, насколько опасна серная кислота. При работе с этим видом яда требуется специальные средства защиты. В составе с другими элементами действие может либо усиливаться, либо уменьшаться, как, например, в случае взаимодействия серной кислоты и карбоната натрия.
Серная кислота
Любая кислота — это всегда сложное сочетание элементов нескольких видом веществ. Серная кислота — это два атома водорода и кислотная субстанция. Ее формула h3SO4. В чистом виде серная кислота — это жидкость, тяжелая и вязкая, напоминающая масло, имеющая кисловатый запах. Серная кислота хорошо взаимодействует с металлами и водой, является сильным окислителем почти для всех металлов, кроме золота, железа и алюминия. Именно поэтому промышленную серную кислоту транспортируют в стальных бочках или цистернах. Кислота образует среднюю и кислую соли.

Взаимодействие с карбонатом натрия
Химическая реакция карбоната натрия с серной кислотой всегда предсказуема. При взаимодействии:
- Выпадает осадок.
- Изменяется цвет.
- Выделяется газ.
- Выделяется свет.
Химическая формула реакции выглядит как Na2CO3 + h3SO4 → Na2SO4 + CO2 + h3O. В итоге образуется сульфат натрия и угольная кислота, а угольная кислота путем взаимозамещения разлагается на воду и углекислый газ.

Напомним, что карбонат натрия — это белое порошкообразное вещество, в народе известное как кальцинированная сода, которая может быть технической и пищевой. Само по себе это вещество неопасно и применяется даже в кулинарии и хлебопечении. Однако взаимодействие с серной кислотой карбонат натрия превращается в один из сильнейших ядов, которые используют в цветной и черной металлургии, в текстильном производстве, нефтегазовой отрасли и химической промышленности.
В школьной программе описание этих химических соединений можно найти в учебниках восьмого и девятого классов.
Задание №1
Для выполнения заданий 30, 31 используйте следующий перечень веществ: перманганат калия, гидрокарбонат калия, сульфит натрия, сульфат бария, гидроксид калия. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
KHCO3 + KOH = K2CO3 + H2O
K+ + HCO3— + K+ + OH— = 2K+ + CO32- + H2O
HCO3— + OH— = H2O + CO32-
Комментарий: формулы слабых кислот, а также формулы водородсодержащих кислотных остатков слабых кислот в ионных уравнениях записываются целиком.
Задание №2
Для выполнения заданий 30, 31 используйте следующий перечень веществ: гидрокарбонат натрия, алюминат натрия, бромид калия, углекислый газ, концентрированная серная кислота. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
2NaHCO3 + H2SO4 = Na2SO4 + 2H2O + 2CO2
2Na+ + 2HCO3— + 2H+ + SO42- = 2Na+ + SO42- + 2H2O + 2CO2
HCO3— + H+ = H2O + CO2
Комментарий: формулы слабых кислот, а также формулы водородсодержащих кислотных остатков слабых кислот в ионных уравнениях записываются целиком.
Задание №3
Для выполнения заданий 30, 31 используйте следующий перечень веществ: азот, хлороводород, оксид фосфора (V), диоксид марганца, ацетат калия. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
CH3COOK + HCl = CH3COOH + KCl
CH3COO— + K+ + H+ + Cl— = CH3COOH + K+ + Cl—
CH3COO— + H+ = CH3COOH
Комментарий: формулы слабых кислот, а также формулы водородсодержащих кислотных остатков слабых кислот в ионных уравнениях записываются целиком.
Задание №4
Для выполнения заданий 30, 31 используйте следующий перечень веществ: серная кислота, оксид серы (VI), гидроксид натрия, бром, силикат натрия. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеПервый вариант ответа:
Na2SiO3 + H2SO4 = Na2SO4 + H2SiO3↓
2Na+ + SiO32- + 2H+ + SO42- = 2Na+ + SO42- + H2SiO3↓
SiO32- + 2H+ = H2SiO3↓
Комментарий: формулы нерастворимых веществ в ионных уравнениях реакций записывают целиком.
Второй вариант ответа:
2NaOH + H2SO4 = Na2SO4 + H2O
2Na+ + 2OH
OH— + H+ = H2O
Комментарий: формулы нерастворимых веществ в ионных уравнениях реакций записывают целиком.
Задание №5
Для выполнения заданий 30, 31 используйте следующий перечень веществ: углекислый газ, сульфат натрия, бром, бромоводород, сульфит калия. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
2HBr + K2SO3 = 2KBr + H2O + SO2↑
2H+ + 2Br— + 2K+ + SO32- = 2K+ + 2Br—
+ H2O + SO22H+ + SO32- = SO2 + H2O
Задание №6
Для выполнения заданий 30, 31 используйте следующий перечень веществ: гидрокарбонат кальция, углерод, сульфид меди, азотная кислота, тетрагидроксоалюминат натрия. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
2HNO3 + Ca(HCO3)2 = Ca(NO3)2 + 2CO2 + 2H2O
2H+ + 2NO3— + Ca2+ + 2HCO3— = Ca2+ + 2NO3— + 2CO2 + 2H2O
H+
Задание №7
Для выполнения заданий 30, 31 используйте следующий перечень веществ: пероксид водорода, фосфат лития, гидрокарбонат калия, гидроксид хрома (III), гидроксид калия. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеПервый вариант ответа:
KOH + KHCO3 = K2CO3 + H2O
K+ + OH— + K+ + HCO3— = 2K+ + CO32- + H2O
OH— + HCO3— = CO32- + H2O
Задание №8
Для выполнения заданий 30, 31 используйте следующий перечень веществ: карбонат натрия, иодоводородная кислота, оксид серы (IV), гидроксид железа (III), хлорид алюминия. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
2HI + Na2CO3 = 2NaI + H2O + CO2
2H+ + 2I— + 2Na+ + CO32- = 2Na+ + 2I— + H2O + CO2
2H+ + CO32- = H2O + CO2.
Задание №9
Для выполнения заданий 30, 31 используйте следующий перечень веществ: сульфид железа (II), гидроксид натрия, гидроксид алюминия, нитрит натрия, хлорид аммония. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
NaOH + NH4Cl = NaCl + NH3 + H2O
Na+ + OH— + NH4+ + Cl— = Na+ + Cl— + NH3 + H2O
OH— + NH4+ = NH3 + H2O.
Задание №10
Для выполнения заданий 30, 31 используйте следующий перечень веществ: иодид натрия, ацетат бария, уксусная кислота, серная кислота, угарный газ. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
H2SO4 + (CH3COO)2Ba = BaSO4↓ + 2CH3COOH
2H+ + SO42- + Ba2+ + 2CH3COO— = BaSO4↓ + 2CH3COOH
Так как в левой и правой частях полного ионного уравнения не обнаруживаются одинаковые ионы, сокращенное ионное уравнение будет совпадать с полным ионным.
Задание №11
Для выполнения заданий 30, 31 используйте следующий перечень веществ: оксид железа (II), хлорид бария, гидроксид натрия, оксид кремния (IV), концентрированная азотная кислота. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
HNO3 + NaOH = NaNO3 + H2O
H+ + NO3— + Na+ + OH— = Na+ + NO3— + H2O
H+ + OH— = H2O.
Задание №12
Для выполнения заданий 30, 31 используйте следующий перечень веществ: гидроксид натрия, дихромат калия, хлорид бария, диоксид кремния, соляная кислота. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
HCl + NaOH = NaCl + H2O
H+ + Cl— + Na+ + OH— = Na+ + Cl— + H2O
H+ + OH— = H2O.
Задание №13
Для выполнения заданий 30, 31 используйте следующий перечень веществ: дихромат калия, сульфат меди, серная кислота, бромид калия, гидроксид алюминия. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
3H2SO4 + 2Al(OH)3 = Al2(SO4)3 + 6H2O
6H+ + 3SO42- + 2Al(OH)3 = 2Al3+ + 3SO42- + 6H2O
3H+ + Al(OH)3 = Al3+ + 3H2O.
Задание №14
Для выполнения заданий 30, 31 используйте следующий перечень веществ: азотная кислота, гидроксид калия, бром, гидроксид хрома (III), серная кислота. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
Первый вариант ответа:
HNO3 + KOH = KNO3 + H2O
H+ + NO3— + K+ + OH— = K+ + NO3— + H2O
H+ + OH— = H2O
Второй вариант ответа:
2KOH + H2SO4 = K2SO4 + 2H2O
2K+ + 2OH— + 2H+ + SO42- = 2K+ + SO42- + 2H2O
OH— + H+ = H2O
Третий вариант ответа:
Cr(OH)3 + 3HNO3 = Cr(NO3)3 + 3H2O
Cr(OH)3 + 3H+ + 3NO3— = Cr3+ + 3NO3— + 3H2O
Cr(OH)3 + 3H+ = Cr3+ + 3H2O.
Задание №15
Для выполнения заданий 30, 31 используйте следующий перечень веществ: карбонат бария, оксид меди (I), концентрированная серная кислота, гидрокарбонат натрия, дихромат натрия. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеПервый вариант ответа:
H2SO4 + BaCO3 = BaSO4 + H2O + CO2
2H+ + SO42- + BaCO3 = BaSO4 + H2O + CO2
Так как в левой и правой частях полного ионного уравнения не обнаруживаются одинаковые ионы, сокращенное ионное уравнение будет совпадать с полным ионным.
Второй вариант ответа:
2NaHCO3 + H2SO4 = Na2SO4 + 2H2O + 2CO2
2Na+ + 2HCO3— + 2H+ + SO42- = 2Na+ + SO42- + 2H2O + 2CO2
HCO3— + H+ = H2O + CO2.
Задание №16
Для выполнения заданий 30, 31 используйте следующий перечень веществ: нитрат калия, углекислый газ, алюминий, гидрофосфат калия, гидроксид калия. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
KOH + K2HPO4 = K3PO4 + H2O
K+ + OH— + 2K+ + HPO42- = 3K+ + PO43- + H2O
OH— + HPO42- = PO43- + H2O.
Задание №17
Для выполнения заданий 30, 31 используйте следующий перечень веществ: оксид фосфора (III), азотная кислота, оксид железа (III), оксид серы (IV), карбонат кальция. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
2HNO3 + CaCO3 = Ca(NO3)2 + H2O + CO2
2H+ + 2NO3— + CaCO3 = Ca2+ + 2NO3— + H2O + CO2
2H+ + CaCO3 = Ca2+ + H2O + CO2.
Задание №18
Для выполнения заданий 30, 31 используйте следующий перечень веществ: гидроксид алюминия, сульфат меди (II), нитрат железа (II), концентрированная азотная кислота, гидроксид калия |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеПервый вариант ответа:
3HNO3 + Al(OH)3 = Al(NO3)3 + 3H2O
3H+ + 3NO3— + Al(OH)3 = Al3+ + 3NO3— + 3H2O
3H+ + Al(OH)3 = Al3+ + 3H2O
Второй вариант ответа:
Fe(NO3)2 + 2KOH = Fe(OH)2 + 2KNO3
Fe2+ + 2NO3— + 2K+ + 2OH— = Fe(OH)2 + 2K+ + 2NO3—
Fe2+ + 2OH— = Fe(OH)2
Третий вариант ответа:
CuSO4 + 2KOH = Cu(OH)2 + K2SO4
Cu2+ + SO42- + 2K+ + 2OH— = Cu(OH)2 + 2K+ + SO42-
Cu2+ + 2OH— = Cu(OH)2
Задание №19
Для выполнения заданий 30, 31 используйте следующий перечень веществ: сульфат бария, сульфид калия, сульфат натрия, ацетат бария, перманганат калия. Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
Na2SO4 + (CH3COO)2Ba = BaSO4 + 2CH3COONa
2Na+ + SO42- + 2CH3COO— + Ba2+ = BaSO4 + 2CH3COO— + 2Na+
SO42- + Ba2+ = BaSO4.
Задание №20
Для выполнения заданий 30, 31 используйте следующий перечень веществ: раствор серной кислоты, гидроксид меди (II), дихромат калия, диоксид кремния, сульфат железа (II). Допустимо использование водных растворов веществ. |
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
РешениеВариант ответа:
Cu(OH)2 + H2SO4 = CuSO4 + 2H2O
Cu(OH)2 + 2H+ + SO42- = Cu2+ + SO42- + 2H2O
Cu(OH)2 + 2H+ = Cu2+ + 2H2O.
NaHCO3 + h3SO4 = ? уравнение реакции
В результате взаимодействия гидрокарбоната натрия с раствором разбавленной серной кислоты (NaHCO3 + h3SO4 = ?) происходит образование средней соли – сульфата натрия и угольной кислоты, которая мгновенно разлагается на углекислый газ и воду. Молекулярное уравнение реакции имеет вид:
Диоксид углерода (углекислый газ) при обычных условиях представляет собой бесцветный газ, который в 1,5 раза тяжелее воздуха, что позволяет переливать его, как жидкость, из одного сосуда в другой. Растворимость диоксида углерода в воде невелика.
Под давлением диоксид углерода при комнатной температуре превращается в жидкость. А при быстром выливании его из баллона он превращается в твердую белую снегообразную массу.
Углекислый газ проявляет кислотные свойства (именно поэтому реакция между азотной кислотой и диоксидом углерода HNO3 + CO2 = ? невозможна): реагирует со щелочами, гидратом аммиака. Восстанавливается активными металлами, водородом, углеродом.
В промышленных условиях углекислый газ получают из дымовых газов или в качестве побочного продукта многих химических реакций, например при разложении природных карбонатов – известняка и доломита.
Карбонат натрия и серная кислота
Для просмотра онлайн кликните на видео ⤵

Взаимодействие карбоната натрия и серной кислоты Подробнее

распознавание растворов карбоната натрия, хлорида натрия и сульфата натрия Подробнее

Взаимодействие карбоната натрия и соляной кислоты К Подробнее

Изучаем химические свойства концентрированной серной кислоты! Подробнее

Карбонат натрия из пищевой соды Подробнее

Карбонат натрия и сульфат натрия в домашних условиях. Подробнее

ЕГЭ химия 2020 | ВАЖНЫЕ СВОЙСТВА КИСЛЫХ СОЛЕЙ НА ЕГЭ | PARTA Подробнее

Делаем очень чистый нитрат натрия (химия) Подробнее

СЕРНАЯ КИСЛОТА | h3SO4 | Химические свойства разбавленной и концентрированной СЕРНОЙ КИСЛОТЫ | Химия Подробнее

Получение карбоната натрия (кальцинированной соды) из гидрокарбоната натрия (пищевой соды)!!! Подробнее

Разбираем 31 задание ЕГЭ 2019 по Химии Подробнее

КАЧЕСТВЕННАЯ РЕАКЦИЯ НА ИОН КАЛЬЦИЯ С КАРБОНАТОМ НАТРИЯ Подробнее

Получение сильной щёлочи. Едкий натрий для восстановления золота. Подробнее

распознавание растворов хлорида бария, сульфата натрия и серной кислоты Подробнее

Тест состава: Карбонат натрия и ПАМ. Na2CO3 и MgAl Подробнее

Опыты по химии. Взаимодействие муравьиной кислоты с карбонатом натрия Подробнее

Получение сульфата никеля Подробнее

Серная кислота! Где достать! С чем реагирует! Подробнее

КАЧЕСТВЕННЫЕ РЕАКЦИИ НА КАРБОНАТ-ИОН (КАРБОНАТ НАТРИЯ) Подробнее

Реакции ионного обмена. Часть 1
Реакции ионного обмена. Часть 1 | Подготовка к ЦТ и ЕГЭ по химии Skip to contentЗадание 31
Из предложенного перечня веществ выберите вещества, между которыми может протекать реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения только одной из возможных реакций. Дан следующий перечень веществ:
Перманганат калия, аммиак, сульфат калия, сульфат железа(III), фосфат кальция. Допустимо использование водных растворов этих веществ.
Фосфид кальция, перманганат натрия, оксид азота(IV), гидроксид меди(II), хлороводород. Допустимо использование водных растворов этих веществ.
Нитрат кальция, гидрокарбонат натрия, медь, алюминий, серная кислота (конц.). Допустимо использование водных растворов этих веществ.
Серная кислота, иодид калия, оксид марганца(IV), нитрат магния, гидроксид алюминия. Допустимо использование водных растворов этих веществ.
Перманганат калия, нитрит калия, гидроксид калия, оксид меди(II), сульфат аммония. Допустимо использование водных растворов этих веществ.
Перманганат калия, гидрокарбонат калия, сульфит натрия, сульфат бария, гидроксид калия. Допустимо использование водных растворов веществ.
Нитрат железа(II), концентрированная азотная кислота, оксид кремния(IV), углекислый газ, гидроксид алюминия. Допустимо использование водных растворов веществ.
Cернистый газ, перманганат натрия, гидроксид натрия, углекислый газ, ортофосфорная кислота. Допустимо использование водных растворов этих веществ.
Иодид калия, оксид кремния, гидроксид калия, углекислый газ, серная кислота. Допустимо использование водных растворов этих веществ.
Иодид калия, сульфат натрия, гидроксид железа(II), иодоводородная кислота, гидроксид железа(III). Допустимо использование водных растворов этих веществ.
Хлорид бария, сульфит натрия, фосфат кальция, сульфат бария, хлорид железа(III). Допустимо использование водных растворов этих веществ.
Гипохлорит калия, сульфат калия, гидрофосфат калия, гидроксид калия, гидроксид хрома(III). Допустимо использование водных растворов этих веществ.
Бром, сульфат калия, сульфит калия, нитрат натрия, соляная кислота. Допустимо использование водных растворов этих веществ.
Иодид калия, нитрат бария, сульфат бария, карбонат натрия, пероксид водорода. Допустимо использование водных растворов этих веществ.
Оксид меди(I), разбавленный раствор серной кислоты, перманганат калия, фторид натрия, азот. Допустимо использование водных растворов этих веществ.
Сульфид меди(II), концентрированная азотная кислота, гидроксид алюминия, нитрат меди(II), сульфат хрома(III). Допустимо использование водных растворов этих веществ.
Дихромат натрия, серная кислота, иодид натрия, силикат калия, нитрат магния. Допустимо использование водных растворов веществ.
Хлорат калия, серная кислота, аммиак, сульфат железа (II), хлорид калия. Допустимо использование водных растворов веществ.
Перманганат калия, соляная кислота, аммиак, хлорид железа (II), сульфит бария. Допустимо использование водных растворов этих веществ.
Оксид марганца (IV), серная кислота, сульфид меди (II), хлорид калия, гидрокарбонат калия. Допустимо использование водных растворов этих веществ.
Азотная кислота (разбавленная), гидроксид железа (II), нитрат меди (II), карбонат кальция, хлорид лития. Допустимо использование водных растворов этих веществ.
Дихромат калия, цинк, серная кислота (разбавленная), хлорид бария, ацетат аммония. Допустимо использование водных растворов этих веществ.
Пероксид водорода, нитрат серебра, гидроксид натрия, оксид хрома (III), фторид аммония. Допустимо использование водных растворов этих веществ.
Cерная кислота, сульфит натрия, дихромат натрия, оксид меди (II), нитрат калия. Допустимо использование водных растворов этих веществ.
Марганцевая кислота, фторид натрия, сернистый газ, нитрат бария, пероксид водорода. Допустимо использование водных растворов этих веществ.
Силикат натрия, серная кислота, углекислый газ, иодид калия, оксид марганца (IV). Допустимо использование водных растворов этих веществ.
Нитрат натрия, медь, оксид фосфора (V), серная кислота (концентрированная), ацетат калия. Допустимо использование водных растворов этих веществ.
Плавиковая кислота, хлорит калия, фосфин, гидроксид калия, нитрат серебра. Допустимо использование водных растворов этих веществ.
Хлорид железа (II), хромит калия, аммиак, серная кислота (концентрированная), угарный газ. Допустимо использование водных растворов этих веществ.
Гидроксид калия, хлорат калия, дигидрофосфат аммония, сульфат бария, фосфин. Допустимо использование водных растворов этих веществ.
Возможные варианты ответа:
Fe2(SO4)3 + 6NH3∙H2O = 2Fe(OH)3 + 3(NH4)2SO4
2Fe3+ + 3SO42ˉ + 6NH3∙H2O = 2Fe(OH)3 + 6NH4+ + 3SO42ˉ
Fe3+ + 3NH3∙H2O = Fe(OH)3 + 3NH4+
Cu(OH)2 + 2HCl = CuCl2 + 2H2O
Cu(OH)2 + 2H+ + 2Cl— = Cu2+ + 2Cl— + 2H2O
Cu(OH)2 + 2H+ = Cu2+ + 2H2O
2NaHCO3 + H2SO4 = Na2SO4 + 2CO2 + 2H2O
2Na+ + 2HCO3— + 2H+ + SO42- = 2Na+ + SO42- + 2CO2 + 2H2O
HCO3ˉ + H+ = CO2 + H2O
2Al(OH)3 + 3H2SO4 = Al2(SO4)3 + 6H2O
2Al(OH)3 + 6H+ + 3SO42ˉ = 2Al3+ + 3SO42- + 6H2O
Al(OH)3 + 3H+ = Al3+ + 3H2O
2KOH + (NH4)2SO4 = K2SO4 + 2NH3 + 2H2O
2K+ + 2OHˉ + 2NH4+ + SO42ˉ = 2K+ + SO42ˉ + 2NH3 + 2H2O
OHˉ + NH4+ = NH3 + H2O
KHCO3 + KOH = K2CO3 + H2O
2K+ + HCO3— +OH— = 2K+ + CO32- + H2O
HCO3— +OH— = CO32- + H2O
Al(OH)3 + 3HNO3 = Al(NO3)3 + 3H2O
Al(OH)3 + 3H+ + 3NO3ˉ = Al3+ + 3NO3ˉ + 3H2O
Al(OH)3 + 3H+ = Al3+ + 3H2O
H3PO4+ 3NaOH = Na3PO4 + 3H2O
H3PO4 + 3Na+ + 3OHˉ = 3Na+ + PO43ˉ + 3H2O
H3PO4 + 3OHˉ = PO43ˉ + 3H2O
2KOH + H2SO4= K2SO4 + 2H2O
2K+ + 2OHˉ + 2H+ + SO42ˉ = 2K+ + SO42ˉ + 2H2O
OHˉ + H+ = H2O
Fe(OH)2+ 2HI = FeI2 + 2H2O
Fe(OH)2 + 2H+ + 2Iˉ = Fe2+ + 2Iˉ + 2H2O
Fe(OH)2 + 2H+ = Fe2+ + 2H2O
BaCl2+ Na2SO3 = BaSO3 + 2NaCl
Ba2+ + 2Clˉ + 2Na+ + SO32ˉ = BaSO3 + 2Na+ + 2Clˉ
Ba2+ + SO32ˉ = BaSO3
K2HPO4+ KOH = K3PO4 + H2O
3K+ + HPO42ˉ + OHˉ = 3K+ + PO43ˉ + H2O
HPO42ˉ + OHˉ = PO43ˉ + H2O
K2SO3+ 2HCl = 2KCl + SO2 + H2O
2K+ + SO32ˉ + 2H+ + 2Clˉ = 2K+ + 2Clˉ + SO2 + H2O
SO32ˉ + 2H+ = SO2 + H2O
Ba(NO3)2+ Na2CO3 = BaCO3 + 2NaNO3
Ba2+ + 2NO3ˉ + 2Na+ + CO32ˉ = BaCO3 + 2Na+ + 2NO3ˉ
Ba2+ + CO32ˉ = BaCO3
2NaF + H2SO4= Na2SO4 + 2HF
2Na+ + 2Fˉ + 2H+ + SO42ˉ = 2Na+ + SO42ˉ + 2HF
Fˉ + H+ = HF
Al(OH)3+ 3HNO3 = Al(NO3)3 + 3H2O
Al(OH)3 + 3H+ + 3NO3ˉ = Al3+ + 3NO3ˉ + 3H2O
Al(OH)3 + 3H+ = Al3+ + 3H2O
H2SO4 + K2SiO3 = H2SiO3 + K2SO4
2H+ + SO42- + 2K+ + SiO32- = H2SiO3 + 2K+ + SO42-
2H+ + SiO32- = H2SiO3
FeSO4 + 2NH3∙H2O = Fe(OH)2 + (NH4)2SO4
Fe2+ + SO42ˉ + 2NH3∙H2O = Fe(OH)2 + 2NH4+ + SO42ˉ
Fe2+ + 2NH3∙H2O = Fe(OH)2 + 2NH4+
2HCl + BaSO3 = SO2 + H2O + BaCl2
2H+ + 2Cl— + BaSO3 = SO2 + H2O + Ba2+ + 2Cl—
2H+ + BaSO3 = SO2 + H2O + Ba2+
2KHCO3 + H2SO4 = 2CO2 + 2H2O + K2SO4
2K+ + 2HCO3— + 2H+ + SO42- = 2CO2 + 2H2O + 2K+ + SO42-
HCO3— + H+ = CO2 + H2O
2HNO3 + CaCO3 = CO2 + H2O + Ca(NO3)2
2H+ + 2NO3— + CaCO3 = CO2 + H2O + Ca2+ + 2NO3—
2H+ + CaCO3 = CO2 + H2O + Ca2+
H2SO4 + BaCl2 = BaSO4 + 2HCl
2H+ + SO42- + Ba2+ 2Cl— = BaSO4 + 2H+ + 2Cl—
SO42- + Ba2+ = BaSO4
2NaOH + 2AgNO3 = 2NaNO3 + Ag2O + H2O
2Na+ + 2OH— + 2Ag+ + 2NO3— = 2Na+ + 2NO3— + Ag2O + H2O
2OH— + 2Ag+ = Ag2O + H2O
H2SO4 + Na2SO3 = Na2SO4 + SO2 + H2O
2H+ + SO42- + 2Na+ + SO32- = 2Na+ + SO42- + SO2 + H2O
2H+ + SO32- = SO2 + H2O
HMnO4 + NaF = NaMnO4 + HF
H+ + MnO4— + Na+ + F— = Na+ + MnO4— + HF
H+ + F— = HF
H2SO4 + Na2SiO3 = H2SiO3 + Na2SO4
2H+ + SO42- + 2Na+ + SiO32- = H2SiO3 + 2Na+ + SO42-
2H+ + SiO32- = H2SiO3
2CH3COOK + H2SO4 = K2SO4 + 2CH3COOH
2CH3COO— + 2K+ + 2H+ + SO42- = 2K+ + SO42- + 2CH3COOH
CH3COO— + H+ = CH3COOH
KOH + HF = KF + H2O
K+ + OH— + HF = K+ + F— + H2O
OH— + HF = F— + H2O
FeCl2 + 2NH3 + 2H2O = 2NH4Cl + Fe(OH)2
Fe2+ + 2Cl— + 2NH3 + 2H2O = 2NH4+ + 2Cl— + Fe(OH)2
Fe2+ + 2NH3 + 2H2O = 2NH4+ + Fe(OH)2
NH4H2PO4 + 3KOH = K3PO4 + NH3 + 3H2O
NH4+ + H2PO4— + 3K+ + 3OH— = 3K+ + PO43- + NH3 + 3H2O
NH4+ + H2PO4— + 3OH— = PO43- + NH3 + 3H2O
Также предлагаем вам плейлист видео-уроков и видео-объяснений заданий на эту тему:
карбонат натрия | 497-19-8
Карбонат натрия Химические свойства, применение, Производство
Описание
Карбонат натрия, Na2CO3, является натриевой солью углекислоты. Чистый продукт представляет собой какое-то время порошок без запаха с сильным щелочным вкусом. Обладает высокой гигроскопичностью. Он может быть легко растворен в воде с образованием водного раствора с умеренной щелочностью.Карбонат натрия имеет широкое применение в различных областях по всему миру.Одним из наиболее важных применений карбоната натрия является производство стекла. Согласно статистическим данным, около половины общего производства карбоната натрия используется для производства стекла. Во время производства стекла карбонат натрия действует как флюс при плавлении кремнезема. Кроме того, в качестве прочной химической основы он используется в производстве целлюлозы и бумаги, текстиля, питьевой воды, мыла и моющих средств, а также в качестве очистителя для слива. Кроме того, он также может быть использован для пищеварения тканей, растворения амфотерных металлов и соединений, приготовления пищи, а также в качестве моющего средства.
Как правило, есть два способа производства карбоната натрия. Один из них заключается в реакциях между хлоридом натрия и карбонатом кальция (через процесс с аммиачной содой (Solvay)). Другая — из карбонатных и гидрокарбонатных руд натрия (троны и нахколиты).
Физические свойства
Карбонат натрия является неорганической солью, поэтому давление пара можно считать незначительным. Он имеет температуру плавления 851 ° C (CRC Handbook, 1986; Merck Index, 1983), он разлагается при нагревании до> 400 ° C и, следовательно, температура кипения не может быть определена.растворим в воде; нерастворим в спирте; растворяется в кислотах, выделяя СО2. Коэффициент распределения октаноловой воды (log Pow) не имеет отношения к неорганическому веществу, которое диссоциирует. Средний диаметр частиц (d50) легкого карбоната натрия находится в диапазоне от 90 до 150 мкм, а плотного карбоната натрия находится в диапазоне от 250 до 500 мкм.
Моногидрат состоит из мелких кристаллов без цвета и запаха или из кристаллического порошка; ромбическая структура; показатель преломления 1.420; твердость 1,3 Мосса; плотность 2,25 г / см3; теряет воду при 100 ° С, становясь безводным; очень растворим в воде; нерастворим в этаноле.
Декагидрат состоит из прозрачных кристаллов; выцветания на воздухе; плотность 1,46 г / см3; разлагается при 34 ° С; очень растворим в воде; нерастворим в этаноле.
Водный раствор карбоната натрия сильно щелочной.
Химические свойства
Карбонат натрия представляет собой белый кристаллический и гигроскопичный порошок с чистотой> 98%.Доступны две формы карбоната натрия: легкая сода и густая сода. Примеси карбоната натрия могут включать воду (Карбонат натрия представляет собой сильное щелочное соединение с рН 11,6 для 0,1 М водного раствора (The Merck Index, 1983; Johnson and Swanson, 1987). PKa CO3 2- составляет 10,33, что означает, что при pH 10,33 карбонат и бикарбонат присутствуют в равных количествах.
Использует
Карбонат натрия является важным сырьем для химической промышленности с широким применением.Это важное сырье для производства стекла, мыла, моющих средств, текстиля, кожи, специй, красителей, лекарств и т. Д.Может использоваться для аналитических реагентов, а также для фармацевтической промышленности и фотогравировки.
Широко используется в стекольной, химической, бумажной, металлургической, фармацевтической и текстильной промышленности, а также в пищевой промышленности.
Это ТВ выделенный реагент.
Может использоваться для пищевой промышленности в качестве нейтрализующего агента, разрыхлителей, таких как аминокислоты, соевый соус и макаронные изделия, такие как хлеб, хлеб и так далее.Это может также быть приготовлено, чтобы дублировать щелочь и добавить в пасту, чтобы увеличить гибкость и пластичность.
В качестве моющего средства его можно использовать для полоскания шерсти. Его также можно применять для солей для ванн и фармацевтического применения, а также в качестве щелочного агента дубления.
Карбонат натрия наиболее широко используется в промышленности, а небольшая часть используется гражданскими лицами. Что касается кальцинированной соды промышленного назначения, она в основном применяется в легкой промышленности, строительных материалах и химической промышленности, составляя около 2/3: за ней следуют металлургия, текстиль, нефть, оборона и фармацевтика.Стекольная промышленность является крупнейшим сектором потребителей соды, каждая тонна стекла потребляет 0,2 тонны кальцинированной соды. В химической промышленности его можно использовать для производства силиката натрия, дихромата натрия, нитрата натрия, фторида натрия, пищевой соды, буры и тринатрийфосфата. В металлургической промышленности он в основном используется для флюсования, минерального флотационного агента и десульфурирующего агента для стали и сурьмы. Он также может быть использован в качестве смягчителя воды в полиграфической и красильной промышленности. В кожевенной промышленности его можно использовать для обезжиривания сырых шкур, нейтрализации хромированной дубленой кожи и улучшения щелочности хромовой жидкости.Он также используется в производстве синтетических моющих добавок триполифосфата натрия и других натриевых солей.
Может использоваться в качестве буфера, нейтрализующего агента и кондиционера для теста. Это может использоваться в пирогах и пастах. Используйте его в соответствии с фактическими требованиями производства.
В основном применяется для флоат-стекла, воронок, оптического стекла. Он также может быть использован в других секторах химической промышленности и металлургии. Это может уменьшить летающее щелочную пыль путем применения тяжелой кальцинированной соды, и, таким образом уменьшая расход материала, улучшение условий труда, а также повышение качества продукции при одновременном снижении ее эрозии на огнеупорном материале, чтобы продлить срок службы печи.
Это разновидность основного химического сырья, которое широко используется в медицине, бумажной промышленности, металлургии, стекольной, текстильной, красильной и других отраслях промышленности и может использоваться в качестве разрыхлителя в пищевой промышленности.
Может использоваться в качестве аналитических реагентов, дегидратирующих агентов и добавок для аккумуляторов.
Биологические функции
Карбонат натрия используется в качестве буферного компонента в таких областях, как хроматография, капиллярный электрофорез и ферментативный катализ. Карбонат натрия широко используется для выделения клеточных мембран, мембранных белков и гидрофобных белков.Был опубликован протокол для выделения полиаминов из среды для культивирования клеток.Токсичность
ADI (допустимая суточная доза) не имеет ограничений (ФАО / ВОЗ в 1985 г.). LD50 (средняя летальная доза) составляет около 6 г / кг (для мышей орально).Пыль кальцинированной соды оказывает раздражающее воздействие на кожу, органы дыхания и глаза. Длительное воздействие раствора соды может вызвать экзему и дерматит. Его концентрированные растворы могут вызвать ожоги, некроз и даже непрозрачность роговицы. Предельно допустимая концентрация кальцинированной содовой пыли в воздухе составляет 2 мг / м3.Операторы должны носить комбинезоны, дверные чехлы, перчатки, ботинки и другую защитную одежду для защиты органов дыхания и кожи.
Способ производства
Карбонат натрия в настоящее время добывается в основном из природных месторождений. Это также произведено синтетически процессом Solvay (или сода аммиака). Естественное производство карбоната натрия в настоящее время превысило его синтетическое производство.Процесс Сольве включает в себя ряд частичных реакций. Первым этапом является прокаливание карбоната кальция с образованием извести и CO2.Известь превращается в гидроксид кальция. Наиболее важная стадия процесса включает взаимодействие рассола с диоксидом углерода и аммиаком с образованием бикарбоната натрия и хлорида аммония. Бикарбонат натрия превращается в карбонат натрия. Гидроксид кальция и хлорид аммония реагируют с образованием хлорида кальция в качестве побочного продукта. Частичные реакции показаны ниже:
CaCO3 → CaO + CO2
CaO + h3O → Ca (OH) 2
2NaCl + 2CO2 + 2Nh4 + 2h3O → 2NaHCO3 + 2Nh5Cl
2NaHCO3 → Na2CO3 + h3O + CO2
Ca (OH) 2 + 2Nh5Cl → CaCl2 + 2Nh4 + 2h3O
Общая реакция:
CaCO3 + 2NaCl → Na2CO3 + CaCl2
Карбонат натрия исторически получался методом Леблана.Первое коммерческое производство было осуществлено по процессу Леблана. В этом процессе хлорид натрия обрабатывали серной кислотой с получением сульфата натрия и соляной кислоты. При нагревании сульфата натрия с углем и известняком образуется «черная зола», которая содержит карбонат натрия, сульфид кальция, непрореагировавший уголь и карбонат кальция. Карбонат натрия отделяли от черной золы выщелачиванием водой. Общая реакция выглядит следующим образом:
Na2SO4 + 2C + CaCO3 → Na2CO3 + CaS + 2CO2
Список литературы
https: // эн.wikipedia.org/wiki/Sodium_hydroxide#Useshttp://www.essentialchemicalindustry.org/chemicals/sodium-carbonate.html
Описание
Карбонат натрия известен как кальцинированная сода или промывочная сода и является широко используемым неорганическим соединением. Приблизительно 45 миллионов тонн кальцинированной соды производится в мире как естественным, так и синтетическим путем. Кальцинированная сода получается естественным образом главным образом из минеральной троны, но ее также можно получить из месторождений нахколита (NaHCO3) и соляного раствора.Trona — это пресноводный эвапорит карбонат-бикарбонат натрия с формулой Na3CO3HCO3 .2h3O. Самое большое из известных месторождений троны находится в районе Грин-Ривер в штате Вайоминг, а другие крупные месторождения находятся в египетской долине Нила и калифорнийском бассейне Сирлс вокруг города Трона. Кальцинированная сода производится из добытой троны путем дробления и сортировки руды, а затем ее нагревания. Это производит кальцинированную соду, смешанную с примесями. Чистую кальцинированную соду получают путем растворения продукта и осаждения примесей в сочетании с процессами фильтрации.Химические свойства
Карбонат натрия, Na2CO3, также известный как сода или кальцинированная сода, является наиболее важным из промышленных щелочей. Это белый или серовато-белый комковатый водорастворимый порошок, который теряет кристаллическую воду при нагревании. Разлагается при температуре около 852 ° C (1560 ° F). Он существует только в решении. Это подготовлено комбинацией углекислого газа и воды.Происшествие
Ясень — дерево, найденное в регионах Северной АмерикиИстория
Карбонат натрия, Na 2 CO 3 , исторически использовался для изготовления стекла, мыла и пороха.Наряду с карбонатом калия, известным как калий, карбонат натрия был основой щелочной промышленности, которая была одной из первых крупных химических отраслей промышленности. На протяжении всей истории щелочи были получены из природных источников. Кальцинированную соду также производили путем сжигания древесины и выщелачивания золы водой, чтобы получить раствор, который давал кальцинированную соду при выпаривании воды. Название кальцинированная сода происходит от завода бариллы, который был использован для производства кальцинированной соды. Научное название этого растения — сода сальсола, но оно носит общие названия: содовая или стекловидная, потому что сода, полученная из нее, использовалась при изготовлении стекла.Барилла — обычное растение, которое можно найти в соленых водах вдоль Средиземного моря в Испании и Италии. Барилла была высушена и сожжена для производства кальцинированной соды. Истощение европейских лесов и В результате международных споров наличие солей щелочных металлов в течение последняя часть 18-го века. Леблан предложил процедуру в 1783 году, а завод, основанный на методе Леблана, был открыт в 1791 году. К сожалению, ассоциация LeBlanc с французским лицензионным платежом привела к конфигации завода во времена французской революции.Кроме того, конфликтующие претензии к методу Леблана были сделаны несколькими другими химиками, и он так и не получил награду.Использует
Кальцинированная сода используется в производстве стекла, в производстве химических веществ натрия (таких как хроматы, фосфаты и силикаты натрия), в целлюлозно-бумажной промышленности, в производстве мыла и моющих средств, в переработке нефти, в умягчении воды и в рафинировании Цветные металлы. В своей кристаллизованной водной форме (Na 2 CO 3 · 10 · 3 O) он известен как сода, промывочная сода или кристаллы соды, которую не следует путать с пищевой содой, которой является гидрокарбонат натрия или бикарбонат натрия (NaHCO3).Его моногидратная форма (Na2CO3 · h30) является стандартным соединением для чистящих растворов.В растворе карбонат натрия создает меньшую щелочность, чем гидроксиды. 0,1% раствор создает рН 11, полностью насыщенный раствор — 35%, который имеет рН 12,5.
Требования безопасности для карбоната натрия из-за его более низкой щелочности могут считаться менее строгими, чем требования для соответствующих бикарбонатов.
Использует
Карбонат натрия представляет собой щелочь, которая существует в виде кристаллов или кристаллических порошок и легко растворим в воде.имеет множество функций: антиоксидант, отвердитель и травление, ароматизатор, технологическая помощь, секвестрант и агент для контроля рН. это используется в супы быстрого приготовления для нейтрализации кислотности. используется в альгинатной воде Сер-гели для секвестрации кальция, позволяющие альгинату раствориться. он также используется в пудингах, соусах и выпечке.Использует
Карбонат натрия также известен как промывка соды или карбонат натрия, натрия карбонат представляет собой белый кристалл или порошок, полученный путем преобразования соли в сульфат натрия с последующим обжигом с известняк и уголь.Растворим в воде и глицерине, но не алкоголь Карбонат натрия был использован в качестве модификатора рН в тонизирующие ванны и в качестве основной щелочи в проявителях, используемых для желатиновые эмульсии.Определение
двухосновная кислота, образующаяся в небольших количествах в растворе когда углекислый газ растворяется в вода: CO 2 + H 2 O? H 2 CO 2 Образует две серии солей: гидрокарбонаты (HCO 3 -) и карбонаты (CO 3 2-).Чистая кислота не может быть выделена.Определение
карбонат натрия: безводный карбонат натрия (кальцинированная сода, соляная сода) представляет собой белый порошок, который спекается и агрегирует на воздухе из-за образования гидратов. Моногидрат Na 2 CO 3 · H 2 O представляет собой белый кристаллический материал, который растворим в воде и нерастворим в спирте; R.D. 2,532; теряет воду при 109 ° С; т.пл. 851 ° С.Декагидрат, Na 2 CO 3 · 10H 2 O (промывочная сода), представляет собой полупрозрачное полупрозрачное кристаллическое твердое вещество; р.д. 1,44; теряет воду при 32–34 ° C, чтобы получить моногидрат; т.пл. 851 ° С.
Карбонат натрия может быть получен способом Сольве или с помощью подходящих процедур кристаллизации из любого из ряда природных месторождений, таких как:
трона (Na 2 CO 3 · NaHCO 3 · 2H 2 O ),
натрона (Na 2 CO 3 · 10H 2 O),
ранксита (2Na 2 CO 3 · 9Na 2 SO 4 · KCl),
пирсоннита (Na2CO ) 3 · CaCO 3 · 2H 2 O),
гайлюссит (Na2CO3 · CaCO 3 · 5H 2 O).
Метод добычи очень чувствителен к относительным затратам на энергию и транспортным расходам в данном регионе. Карбонат натрия используется в фотографии, при очистке, контроле pH воды, при обработке текстиля, стекол и глазурей, а также в качестве пищевой добавки и объемного реагента.
Методы производства
Карбонат натрия производится на всех континентах мира из его минералов. Он присутствует в крупных месторождениях в Африке и Соединенных Штатах в виде карбоната или троны, смешанной руды равные молярные количества карбоната и бикарбоната.Тем не мение, около 70% мирового производства карбоната натрия составляет изготовлено по технологии Solvay (аммиачная сода), посредством чего аммиак добавляют к раствору хлорида натрия. Диоксид углерода затем барботируется для осаждения бикарбонат (NaHCO3), который разлагается при производстве тепла карбонат натрия. В Соединенных Штатах. вся продукция на основе минералов, которые содержат карбонат натрия. Разные Качества карбоната натрия выпускаются: технические, пищевые и фармацевтические сорта.Профиль безопасности
Яд внутрибрюшинным путем. Умеренно токсичен при вдыхании и подкожных путях. Ядовито при приеме внутрь. Экспериментальные репродуктивные эффекты. Раздражитель кожи и глаз. Мигрирует в еду из упаковочных материалов. Может бурно реагировать с Al, P2O5, h3SO4, F2, Li, 2,4,6-тринитротолуолом. При нагревании до разложения выделяет токсичные пары Na2OМетоды очистки
Он кристаллизуется из воды в виде декагидрата, который растворяется в воде, давая почти насыщенный раствор.При барботировании CO2 выделяется NaHCO3. Его отфильтровывают, промывают и поджигают в течение 2 часов при 280 ° С [MacLaren & Swinehart J Am Chem Soc 73 1822 1951]. Перед использованием в качестве объемного стандарта материал аналитического качества должен быть высушен путем нагревания при 260-270 ° С в течение 0,5 часа и оставлен для охлаждения в эксикаторе. Он имеет точку перехода при 450 ° С, и его растворимость в воде составляет 21,58% при 20 ° С (декагидрат в твердой фазе), 49,25% при 35 ° (гептагидрат в твердой фазе) и 44,88% при 75 ° С (моногидрат в твердой фазе) [D.в справочнике по препаративной неорганической химии (ред. Брауэр), Academic Press Vol I p 987-988 1963]. После трех перекристаллизаций техническая чистота Na2CO3 имела Cr, Mg, K, P, Al, W, Sc и Ti при 32, 9,4, 6,6, 3,6, 2,4, 0,6, 0,2 и 0,2 ч / млн соответственно; другой технический источник содержал Cr, Mg, Mo, P, Si, Sn и Ti при 2,6, 0,4, 4,2, 13,4, 32, 0,6, 0,8 м.д. соответственно.Продукты и сырье для приготовления карбоната натрия
Сырье
Продукты для приготовления
,Наука
- Анатомия и физиология
- астрономия
- астрофизика
- Биология
- Химия
- наука о планете Земля
- Наука об окружающей среде
- Органическая химия
- физика
математический
- Алгебра
- Исчисление
- Геометрия
- Prealgebra
Серная кислота
Серная кислота является одним из наиболее важных соединений, производимых химической промышленностью. Он используется для производства буквально сотен соединений, необходимых практически каждой отрасли.
Использование серной кислоты
На сегодняшний день наибольшее количество серной кислоты используется для производства фосфорной кислоты, которая, в свою очередь, используется для производства фосфатных удобрений, дигидрофосфата кальция и фосфатов аммония. Он также используется для приготовления сульфата аммония, который является особенно важным удобрением при дефиците серы.
Рисунок 1 Использование серной кислоты.
Он широко используется при обработке металла, например, при производстве меди и цинка, а также при очистке поверхности стального листа, известного как «травление», перед тем как его покрыть тонким слоем олова, используемого для изготовления банки для еды.
Он также используется для производства капролактама, который превращается в полиамид 6, и при производстве диоксида титана, используемого, например, в качестве пигмента.
Среди множества других применений — производство плавиковой кислоты и фенола с пропаноном, которые используются во многих отраслях промышленности.
Годовой объем производства серной кислоты
| Мир | 231 млн. Тонн |
| Китай | 74 миллиона тонн |
| США | 37 миллионов тонн |
| Индия | 16 миллионов тонн |
| Россия | 14 миллионов тонн |
| Марокко | 7 миллионов тонн |
По оценкам:
Merchant Research & Consulting Ltd.
Эти цифры относятся к 2011 — 2012 гг. Ожидалось, что к 2012 г. мировое производство составит более 250 млн. Тонн (mcgroup.com) и 260 млн. Тонн к 2018 г. (marketsandmarkets.com), при этом прогнозируется тенденция роста как минимум до 2023 г. (transparencymarketresearch.com).
Производство серной кислоты
Процесс получения серной кислоты состоит из четырех стадий:
а) извлечение серы
б) превращение серы в диоксид серы
в) превращение диоксида серы в триоксид серы
г) превращение триоксида серы в серную кислоту
(а) Извлечение серы
Несомненно, самым важным источником серы является ее извлечение из природного газа и нефти.Они содержат соединения серы, как органические, так и сероводород, которые должны быть удалены перед использованием в качестве топлива или химического сырья.
Другим важным источником серы является двуокись серы при переработке металлов. Многие металлические руды встречаются в виде сульфидов и обжигаются с образованием оксида и диоксида серы, например, при производстве свинца:
Другие металлы, произведенные из их сульфидных руд, включают медь, никель и цинк.
Во всем мире около 35% серы получают в виде диоксида серы при обжиге сульфидной руды, и это увеличивается, поскольку заводы, которые традиционно выделяли диоксид серы в атмосферу, извлекают его в виде серной кислоты.В частности, Китай производит большую часть своей серной кислоты из пирита, железорудной руды.
Серную кислоту также получают из сульфата аммония, побочного продукта при производстве поли (метил 2-метилпропеноата), а также извлекают из «отработанной» (т.е. использованной) серной кислоты.
(b) Превращение серы в диоксид серы
Если сера является исходным сырьем, ее сначала необходимо преобразовать в диоксид серы. Расплавленная сера распыляется в печь и сгорает во взрыве сухого воздуха при температуре около 1300 К.Сера горит характерным синим пламенем:
В качестве избытка воздуха используется выходящий газ, содержащий около 10-12% диоксида серы и 10% кислорода по объему. Газы очень горячие и поэтому пропускаются через теплообменники (котлы-утилизаторы).
Газы охлаждаются примерно до 700 К, а вода в окружающих котельных трубах превращается в пар. При производстве одной тонны серной кислоты также производится одна тонна пара высокого давления.
(c) Превращение диоксида серы в триоксид серы (контактный процесс)
Типичная установка содержит один цилиндрический сосуд, который действует как реактор с неподвижным слоем с четырьмя отдельными слоями катализатора, известного как конвертер, с нагревом до 700 К, через который проходят диоксид серы и воздух:
Катализатор, оксид ванадия (V) на диоксиде кремния, как правило, находится в форме небольших гранул, к которым в качестве промотора был добавлен сульфат цезия (рис. 2).Функция промотора состоит в том, чтобы понизить температуру плавления оксида ванадия (V), чтобы он расплавился при 700 К.
| Рисунок 2. Катализатор на основе оксида ванадия (v), используемый для производства серной кислоты. Канал подачи газа можно увидеть в середине картины. С любезного разрешения Хальдора Топсе. |
Рисунок 3 Блок-схема процесса контакта.Как показано выше, это экзотермическая реакция, поэтому для удовлетворительного выхода триоксида серы (требуется конверсия выше 99,5%) используется настолько низкая температура, насколько это экономически возможно. Таким образом, тепло отводится из газа, выходящего из каждого слоя, с помощью теплообменников. Полученный триоксид серы удаляется между третьим и четвертым слоями и поступает на следующую стадию превращения триоксида серы в серную кислоту. |
(d) Превращение триоксида серы в серную кислоту
Триоксид серы, образовавшийся из третьего слоя (и небольшое количество из четвертого слоя), теперь превращается в
серную кислоту.
Триоксид серы реагирует с водой, и реакция может быть выражена как:
Однако сама вода не может быть использована для абсорбции, так как происходит значительное повышение температуры, и образуется туман серной кислоты, с которым трудно справиться.Вместо этого используется серная кислота с концентрацией около 98%. Это сохраняется в этой концентрации путем добавления воды и удаления кислоты в этой концентрации.
Чтобы поддерживать температуру около 400 К, тепло отводится теплообменниками, Рисунок 4.
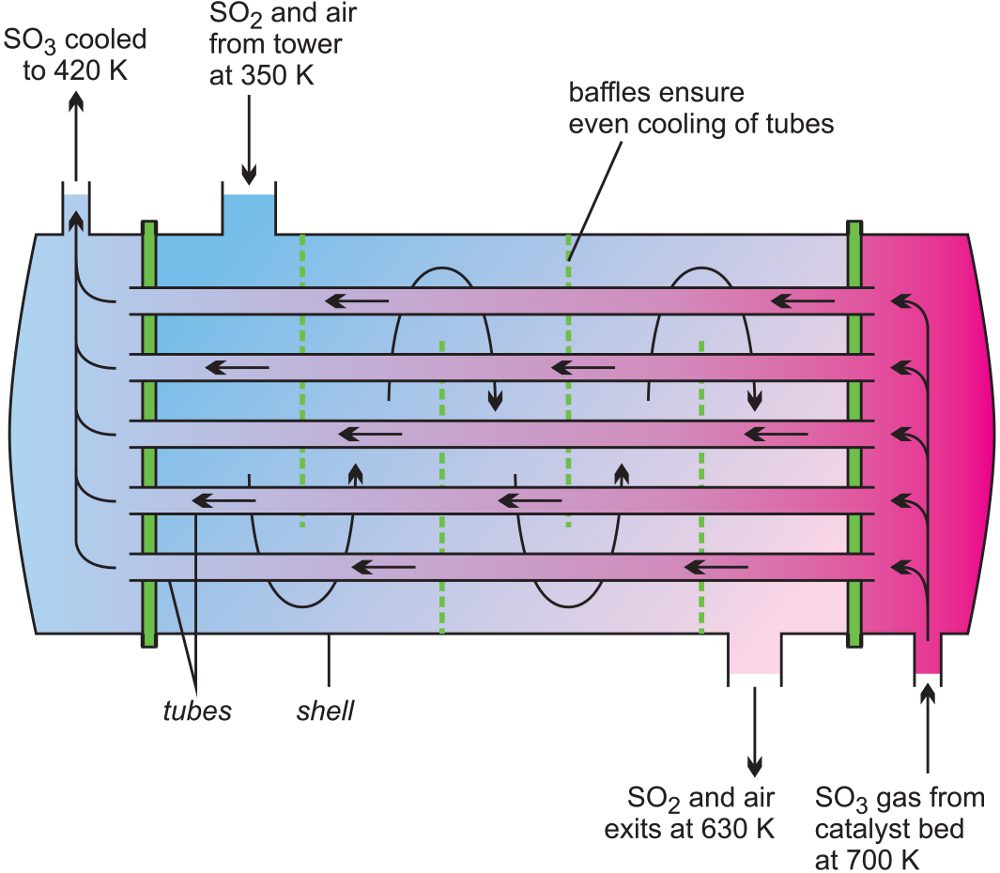
Рисунок 4 Линейная диаграмма, иллюстрирующая теплообменник, используемый при производстве триоксида серы.
Не поглощенные газы содержат около 95% азота, 5% кислорода и следы диоксида серы. Поток газа фильтруется, чтобы удалить любые следы сернокислого тумана, и возвращается в атмосферу, используя высокий стек.
Дата последнего изменения: 9 октября 2016 г.
,Оксикислота | химическое соединение | Британика
Азотная кислота, HNO 3 , была известна алхимикам 8-го века как «aqua fortis» (сильная вода). Он образуется в результате реакции как пятиокиси диоксида азота (N 2 O 5 ), так и диоксида азота (NO 2 ) с водой. Небольшие количества азотной кислоты обнаруживаются в атмосфере после грозы, и ее соли, называемые нитратами, широко распространены в природе. Огромные залежи нитрата натрия, NaNO 3 , также известного как чилийская селитра, обнаружены в пустынном регионе недалеко от границы Чили и Перу.Эти отложения могут иметь ширину 3 км (2 мили), длину 300 км (200 миль) и толщину до 2 метров (7 футов). Нитрат калия, KNO 3 , иногда называемый бенгальской селитрой, встречается в Индии и других странах Восточной Азии. Азотная кислота может быть приготовлена в лаборатории путем нагревания нитратной соли, такой как упомянутые выше, с концентрированной серной кислотой; например, NaNO 3 + H 2 SO 4 + тепло → NaHSO 4 + HNO 3 . Поскольку HNO 3 кипит при 86 ° C (187 ° F) и H 2 SO 4 кипит при 338 ° C (640 ° F), а NaNO 3 и NaHSO 4 являются нелетучими солями, азотная кислота легко удаляется перегонкой.
Получите эксклюзивный доступ к контенту из нашего первого издания 1768 года с вашей подпиской. Подпишитесь сегодняКоммерчески азотная кислота производится с помощью процесса Оствальда. Этот процесс включает окисление аммиака NH 3 до оксида азота NO, дальнейшее окисление NO до диоксида азота NO 2 , а затем превращение NO 2 в азотную кислоту (HNO 3 ) , Это проточный процесс, в котором смесь аммиака и избытка воздуха нагревают до 600-700 ° C (от 1100 до 1300 ° F) и пропускают через платиново-родиевый катализатор.(Катализатор увеличивает скорость реакции, не расходуя себя на реакцию.) Когда происходит окисление до NO, эта газообразная смесь буквально горит пламенем. Дополнительный воздух добавляется для окисления NO до NO 2 . NO 2 , избыток кислорода и нереакционноспособный азот из воздуха пропускаются через разбрызгиватель воды, где HNO 3 и NO образуются в результате диспропорционирования NO 2 . Газообразный NO рециркулируется в процессе с большим количеством воздуха, а жидкий HNO 3 отводится и концентрируется.Около 7 миллиардов кг (16 миллиардов фунтов) HNO 3 ежегодно производится в Соединенных Штатах на коммерческой основе, при этом основная его часть производится с помощью процесса Оствальда.
В чистом виде азотная кислота представляет собой бесцветную жидкость, которая кипит при 86 ° C (187 ° F) и замерзает при -42 ° C (-44 ° F). При воздействии света или тепла он разлагается с образованием кислорода, воды и смеси оксидов азота (прежде всего NO 2 ). 4HNO 3 + свет (или тепло) → 4ΝΟ 2 + 2H 2 O + O 2 Следовательно, азотная кислота часто имеет желтый или коричневый цвет из-за NO 2, который образуется при разложении.Азотная кислота является стабильной в водном растворе, и 68% -ные растворы кислоты (то есть 68 г HNO 3 на 100 г раствора) продаются в виде концентрированной HNO 3 . Это одновременно сильный окислитель и сильная кислота. Неметаллические элементы, такие как углерод (C), йод (I), фосфор (P) и сера (S), окисляются концентрированной HNO 3 до их оксидов или оксикислот с образованием NO 2 ; например, S + 6HNO 3 → H 2 SO 4 + 6NO 2 + 2H 2 O.Кроме того, многие соединения окисляются HNO 3 . Соляная кислота, водная HCl, легко окисляется концентрированной HNO 3 до хлора, Cl 2 и диоксида хлора, ClO 2 . Aqua regia («королевская вода»), смесь одной части концентрированной HNO 3 и трех частей концентрированной HCl, активно реагирует с металлами. Использование этой смеси алхимиками для растворения золота зарегистрировано еще в 13 веке.
Воздействие азотной кислоты на металл обычно приводит к уменьшению кислоты (т.е.уменьшение степени окисления азота). Продукты реакции определяются концентрацией HNO 3 , вовлеченным металлом (т.е. его реакционной способностью) и температурой. В большинстве случаев образуется смесь оксидов азота, нитратов и других продуктов восстановления. Относительно нереакционноспособные металлы, такие как медь (Cu), серебро (Ag) и свинец (Pb), снижают концентрацию HNO 3 прежде всего до NO 2 . В результате реакции разбавленной HNO 3 с медью образуется NO, в то время как более химически активные металлы, такие как цинк (Zn) и железо (Fe), реагируют с разбавленной HNO 3 с образованием N 2 O.При использовании чрезвычайно разбавленной HNO 3 может образовываться либо газообразный азот (N 2 ), либо ион аммония (NH 4 + ). Азотная кислота реагирует с белками, такими как в коже человека, с образованием желтого материала, называемого ксанопротеином.
Нитраты, которые представляют собой соли азотной кислоты, образуются, когда металлы или их оксиды, гидроксиды или карбонаты реагируют с азотной кислотой. Большинство нитратов растворимы в воде, и основным применением азотной кислоты является производство растворимых нитратов металлов.Все нитраты разлагаются при нагревании и могут взрываться. Например, при нагревании нитрата калия (KNO 3 ) образуется нитрит (соединение, содержащее NO 2 — ), и выделяется газообразный кислород. 2KNO 3 + тепло → 2KNO 2 + O 2 Когда нитраты тяжелых металлов нагревают, получают оксид металла, как, например, в 2Cu (NO 3 ) 2 + тепло → 2CuO + 4NO 2 + O 2 . Аммиачная селитра, (NH 4 ) 2 NO 3 , образует закись азота N 2 O и особенно опасна для нагревания или детонации.
Азотная кислота интенсивно используется в лабораториях и в химической промышленности в качестве сильной кислоты и в качестве окислителя. Производство взрывчатых веществ, красителей, пластмасс и лекарств широко использует кислоту. Нитраты ценны как удобрения. Порох представляет собой смесь нитрата калия, серы и древесного угля. Ammonal, взрывчатка, представляет собой смесь нитрата аммония и алюминиевой пудры.
