сульфит натрия, карбонат натрия, хлорид аммония, безводный сульфат меди. Идентифицировать названные вещества, не прибегая к другим реактивам.
8 класс
В восьми склянках находятся вода, растворы умеренно концентрированной серной кислоты, гидроксида калия и четыре сухие соли: сульфит натрия, карбонат натрия, хлорид аммония, безводный сульфат меди. Идентифицировать названные вещества, не прибегая к другим реактивам.
Анализ следует проводить, добавляя растворы к твердым веществам.
Раствором серной кислоты можно обнаружить: сульфит натрия — по выделению бесцветного газа о резким запахом:
$Na_{2}SO_{3} + H_{2}SO_{4} = Na_{2}SO_{4} + SO_{2} \uparrow + H_{2}O$
карбонат натрия — по выделению газа без цвета и запаха:
$Na_{2}CO_{3} + H_{2}SO_{4} = Na_{2}SO_{4} + CO_{2} \uparrow + H_{2}O$
хлорид аммония — по выделению бесцветного газа с резким запахом:
$NH_{4}Cl + H_{2}SO_{4} = NH_{4}HSO_{4} + HCl \uparrow $
Хлороводород и оксид серы (IV) различаются по запаху.
В результате добавления раствора серной кислоты к безводному сульфату меди появляется голубая окраска.
Взаимодействие серной кислоты с гидроксидом калия и водой сопровождается разогреванием растворов:
$2KOH + H_{2}SO_{4} = K_{2}SO_{4} + 2H_{2}O$
$nH_{2}O + H_{2}SO_{4} = H_{2}SO_{4} \cdot nH_{2}O$.
Раствор гидроксида калия и воду можно разделить, добавляя их к безводному сульфату меди. В первом случае образуется голубой осадок гидроксида меди:
$CuSO_{4} + 2KOH = Cu (OH)_{2} \downarrow + K_{2}SO_{4}$
во втором — идет растворение сульфата меди и раствор становится голубым.
Дополнительно гидроксид калия можно идентифицировать, добавляя его к хлориду аммония:
$KOH + NH_{4}Cl = KCl + NH_{3} \uparrow + H_{2}O$
8 класс Химия Средняя 96
Ещё по теме
Некоторое количество углеводорода состава $C_{n}H_{2n — 2}$ дает с избытком хлора 21,0 г тетрахлорида.
8 класс Химия Средняя 33
Смесь стружек цинка и железа обработали избытком раствора гидроксида калия. При этом выделился газ объемом 2,24 л (н.у.). Затем такой же образец смеси обработали избытком соляной кислоты, в результате чего выделился газ объемом 8,96 л (н.у.). Определите массу железа в образце.
8 класс Химия Средняя 104
Рассчитайте объем ацетилена (н.у.), полученного из 40 г карбида кальция, содержащего 20 % примесей.
8 класс Химия Средняя 39
а) Изотоп какого элемента образуется при испускании изотопом $^{209}{81} Tl$ ($\beta$ — частицы? б) Изотоп какого элемента образуется при испускании изотопом $^{213}_{84}Po$ $\alpha$ — частицы? Напишите уравнения ядерных превращений для (а) и (б).
8 класс Химия Средняя 23
Определите молекулярную формулу оксида фосфора, содержащего 43,7 % фосфора. Плотность по воздуху паров этого оксида 9,8.
8 класс Химия Средняя 37
В атоме какого элемента при его образовании из субатомных частиц последним займет свое место в электронной оболочке электрон с таким набором квантовых чисел: $n = 3, l = 2, m = -1, s = +1/2$? Напишите полную электронную формулу атома этого элемента.
8 класс Химия Средняя 48
При бромировании некоторого ароматического соединения в присутствии катализатора $AlBr_{3}$ в темноте образуется только одно монобромпроизводное, причем из 1,00 г исходного соединения можно получить 1,57 г этого монобромпроизводного. { \circ } С$ составляет 1,097 г/л. Определите формулу алкадиена.
{ \circ } С$ составляет 1,097 г/л. Определите формулу алкадиена.
8 класс Химия Средняя 43
Если материал понравился Вам и оказался для Вас полезным, поделитесь им со своими друзьями!
Задания 32 ЕГЭ по химии-2020
Задачи 32 из реального ЕГЭ по химии-2020, все задачи на неорганическую химию (мысленный эксперимент) из реального экзамена ЕГЭ по химии, задания 32 из реального ЕГЭ 2020 (основная волна и резервные дни — 16 июля 2020 года, 24 июля 2020) с текстовыми решениями и ответами.
1. Карбид алюминия сожгли. Полученное твёрдое вещество поместили в раствор гидроксида натрия. Через образовавшийся прозрачный раствор пропустили газ, полученный при действии на магний концентрированной серной кислоты. При пропускании газа происходило выпадение белого осадка и образование соли бескислородной кислоты.
2. Натрий растворили в воде. Образовавшееся газообразное вещество при нагревании пропустили через железную окалину. Получившееся простое вещество при нагревании растворили в необходимом количестве концентрированной серной кислоты, при этом образовался бесцветный газ с резким запахом. К полученному раствору добавили раствор карбоната калия.
Натрий растворили в воде. Образовавшееся газообразное вещество при нагревании пропустили через железную окалину. Получившееся простое вещество при нагревании растворили в необходимом количестве концентрированной серной кислоты, при этом образовался бесцветный газ с резким запахом. К полученному раствору добавили раствор карбоната калия.
3. Натрий сгорел в избытке кислорода. Образовавшееся при этом вещество поместили в раствор, содержащий перманганат калия и серную кислоту. Полученное простое вещество при нагревании прореагировало с пиритом. Образовавшееся при этом твёрдое вещество растворили в иодоводородной кислоте.
4. Алюминий добавили к раствору гидроксида калия. Через образовавшийся прозрачный раствор пропустили газ, полученный при растворении магния в концентрированной серной кислоте. Образовавшийся осадок отделили, а к полученному раствору добавили раствор перманганата калия. При этом наблюдали образование осадка простого вещества.
5. Железную окалину растворили в разбавленной серной кислоте. Полученный раствор обработали дихроматом калия. Полученное соединение хрома выделили и поместили в раствор карбоната натрия. Образовавшийся осадок отделили и нагрели с хлоратом калия в присутствии гидроксида калия.
6. Оксид меди(I) растворили в концентрированном растворе азотной кислоты. Полученный в результате бурый газ поглотили холодным раствором гидроксида натрия. К образовавшемуся раствору добавили подкисленный серной кислотой раствор дихромата натрия. Образовавшееся соединение хрома выделили и поместили в раствор карбоната калия.
7. К раствору дигидрофосфата калия добавили избыток раствора гидроксида кальция. Образовавшийся осадок отделили, высушили и нагрели с кремнезёмом и углём. Полученное простое вещество вступило в реакцию с хлоратом калия. Полученный при этом оксид поместили в избыток раствора гидроксида натрия.
8. Фосфид алюминия растворили в соляной кислоте. К полученному при этом раствору добавили раствор сульфита калия и наблюдали образование белого осадка и выделение бесцветного газа. Полученный газ разделили на две части, одну часть поглотили раствором дихромата натрия, подкисленным серной кислотой. Другую часть газа поглотили концентрированным раствором азотной кислоты.
9. К раствору сульфата хрома(III) добавили раствор сульфита натрия и наблюдали образование осадка и выделение бесцветного газа. Полученный газ поглотили раствором перманганата калия, подкисленным серной кислотой, а осадок обработали раствором, содержащим пероксид водорода и гидроксид натрия, и нагрели. В полученный при этом жёлтый раствор добавили раствор серной кислоты.
10. Провели электролиз раствора нитрата серебра. Выделившееся на аноде простое вещество при нагревании прореагировало с железом. Образовавшееся при этом твёрдое вещество черного цвета поместили в раствор иодоводородной кислоты. Полученное при этом простое вещество при нагревании прореагировало с раствором гидроксида натрия.
Полученное при этом простое вещество при нагревании прореагировало с раствором гидроксида натрия.
11. Нитрат хрома(III) прокалили. Образовавшееся при этом твёрдое вещество нагрели с хлоратом натрия и гидроксидом натрия. Одно из полученных веществ прореагировало с концентрированным раствором хлороводородной кислоты. Образовавшуюся при этом соль хрома выделили, растворили в воде и полученный раствор прилили к раствору карбоната натрия.
12. Перхлорат натрия сплавили с оксидом хрома(III) и гидроксидом натрия. Полученное соединение хрома поместили в разбавленный раствор серной кислоты. В образовавшийся раствор добавили серную кислоту и поместили иодид натрия. Образовавшееся простое вещество при нагревании прореагировало с гидроксидом калия.
13. Дихромат аммония прокалили. Образовавшееся при этом твёрдое вещество нагрели с пероксидом водорода и гидроксидом калия. Одно из полученных веществ прореагировало с концентрированным раствором бромоводородной кислоты. Образовавшуюся при этом соль хрома выделили, растворили в воде и полученный раствор прилили к раствору карбоната калия.
Образовавшуюся при этом соль хрома выделили, растворили в воде и полученный раствор прилили к раствору карбоната калия.
14. Пероксид натрия поместили в раствор, содержащий перманганат калия и серную кислоту. Полученное простое вещество при нагревании прореагировало с железом. Образовавшееся при этом твёрдое вещество черного цвета поместили в раствор иодоводородной кислоты. Образовавшуюся при этом соль железа выделили, растворили в воде и полученный раствор прилили к раствору карбоната натрия.
15. К раствору дигидрофосфата кальция добавили избыток раствора гидроксида калия. Образовавшийся осадок отделили, высушили и нагрели с кремнезёмом и углём. Полученное простое вещество вступило в реакцию с хлоратом калия. Полученную соль растворили в воде и подвергли электролизу.
16. Оксид меди(I) растворили в концентрированном растворе азотной кислоты. Образовавшуюся в результате соль выделили и прокалили. Образовавшийся твёрдый остаток прореагировал при нагревании с газом, полученным при нагревании смеси гидрофосфата аммония и гидроксида кальция.
Образовавшийся твёрдый остаток прореагировал при нагревании с газом, полученным при нагревании смеси гидрофосфата аммония и гидроксида кальция.
17. К раствору сульфата цинка добавили избыток раствора гидроксида калия. Через полученный раствор пропустили сероводород. Образовавшийся при этом осадок обработали горячей концентрированной азотной кислотой. Выделившийся бурый газ пропустили через раствор гидроксида бария.
18. Оксид хрома(VI) поместили в раствор гидроксида натрия. В полученный при этом жёлтый раствор добавили раствор серной кислоты. Образовавшийся раствор дополнительно подкислили серной кислотой и пропустили через этот раствор фосфин. Образовавшуюся при этом соль хрома выделили, растворили в воде и полученный раствор прилили к раствору карбоната калия.
19. Хлорную кислоту нейтрализовали гидроксидом натрия. Образовавшуюся при этом соль выделили, высушили и сплавили с оксидом хрома(III) и гидроксидом натрия. Полученное соединение хрома поместили в разбавленный раствор серной кислоты. Образовавшийся раствор дополнительно подкислили серной кислотой и пропустили через этот раствор сероводород.
Полученное соединение хрома поместили в разбавленный раствор серной кислоты. Образовавшийся раствор дополнительно подкислили серной кислотой и пропустили через этот раствор сероводород.
20. Через раствор силиката натрия пропустили углекислый газ. Полученный при этом осадок отделили, а оставшийся раствор смешали с раствором хлорида железа(III). Выпавший при этом осадок отделили и прокалили. Твёрдый остаток растворили в иодоводородной кислоте.
21. Алюминат калия растворили в серной кислоте. К полученному при этом раствору добавили раствор сульфита натрия. Выделившийся газ разделили на две части, одну часть поглотили раствором дихромата натрия, подкисленным серной кислотой. Другую часть газа поглотили бромной водой.
22. Оксид железа(III) поместили в раствор бромоводородной кислоты. Через получившийся раствор пропустили аммиак. Образовавшийся при этом осадок отделили и прокалили.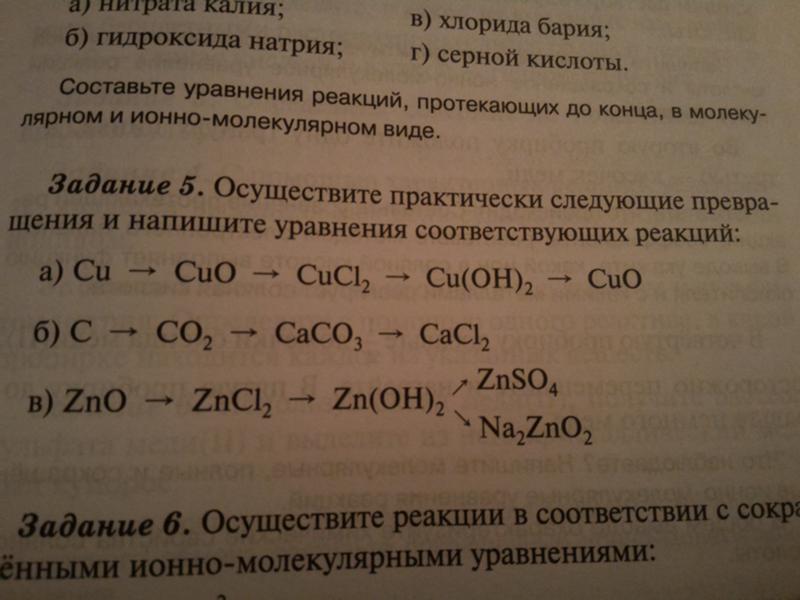 Полученное бурое вещество сплавили с твёрдым гидроксидом калия.
Полученное бурое вещество сплавили с твёрдым гидроксидом калия.
23. Карбонат калия сплавили с оксидом цинка. Выделившийся газ прореагировал с избытком твёрдого гидроксида натрия. Полученную соль растворили в воде и добавили раствор хлорида алюминия. Образовавшийся при этом осадок отделили и поместили в раствор гидроксида калия.
24. Через раствор силиката калия пропустили углекислый газ. Полученный при этом осадок отделили, а оставшийся раствор смешали с раствором сульфата железа(III). Выпавший при этом осадок отделили и прокалили. Полученное бурое вещество сплавили с твёрдым карбонатом натрия.
25. Алюминат натрия растворили в серной кислоте. К полученному при этом раствору добавили раствор сульфида натрия. Выделившийся газ разделили на две части, одну часть поглотили раствором дихромата натрия, подкисленным серной кислотой. Другую часть газа поглотили бромной водой.
26. Медь нагрели с оксидом меди(II), при этом образовалось вещество красного цвета. Это вещество растворили в концентрированном растворе азотной кислоты. Полученный в результате бурый газ поглотили холодным раствором гидроксида калия. К образовавшемуся раствору добавили подкисленный серной кислотой раствор дихромата калия.
Медь нагрели с оксидом меди(II), при этом образовалось вещество красного цвета. Это вещество растворили в концентрированном растворе азотной кислоты. Полученный в результате бурый газ поглотили холодным раствором гидроксида калия. К образовавшемуся раствору добавили подкисленный серной кислотой раствор дихромата калия.
27. Цинк сплавили с твёрдым гидроксидом калия. Полученное в результате твёрдое вещество растворили в необходимом количестве раствора серной кислоты. В образовавшийся раствор добавили сульфид калия, в результате чего образовался белый осадок. Осадок отделили и при нагревании растворили в концентрированной серной кислоте, при этом образовался бесцветный газ с резким запахом.
28. Нитрат железа(II) прокалили. Полученное твердое вещество сплавили с твердым гидроксидом калия. Образовавшийся твердый продукт растворили в необходимом количестве бромоводородной кислоты. Через полученный раствор пропустили аммиак.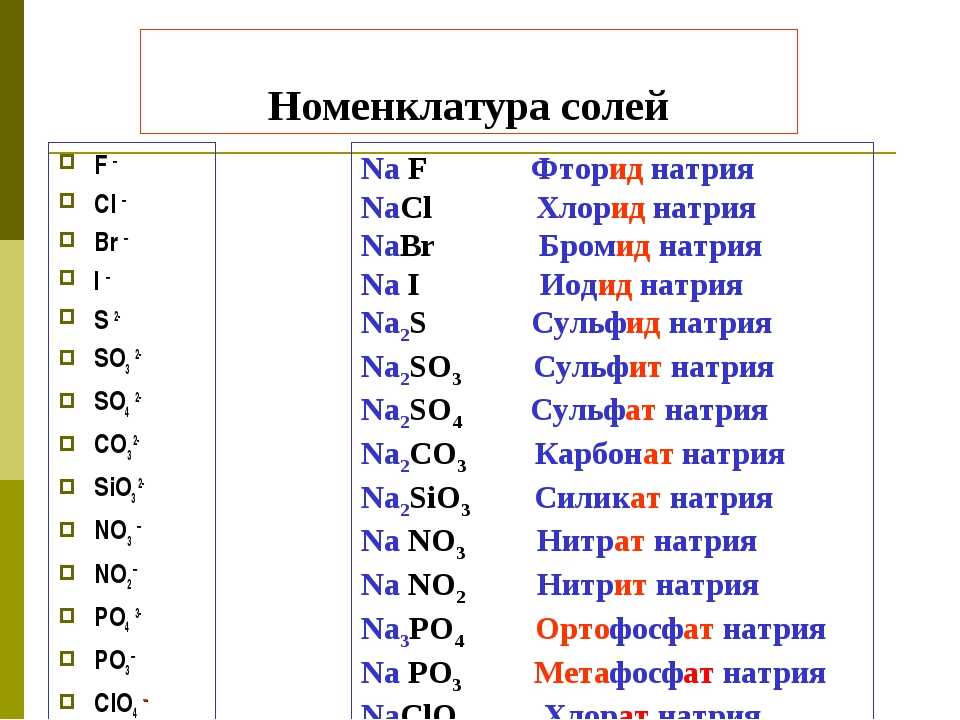
29. Карбонат натрия сплавили с оксидом цинка. Выделившийся газ пропустили через раствор силиката натрия. Образовавшийся осадок отделили, а оставшийся раствор смешали с раствором хлорида железа(III), при этом наблюдали образование осадка и выделение газа. Полученный осадок отделили и поместили в раствор иодоводородной кислоты.
30. Нитрат цинка прокалили. Полученное простое вещество прореагировало с оксидом азота(II). Полученный продукт прореагировал с холодным раствором гидроксида натрия. К образовавшемуся раствору прилили раствор, содержащий дихромат натрия и серную кислоту.
31. К раствору сульфата цинка добавили избыток раствора гидроксида натрия. Через полученный раствор пропустили сероводород. Образовавшийся при этом осадок при нагревании растворили в концентрированной серной кислоте, при этом образовался бесцветный газ с резким запахом. Полученный газ поглотили раствором перманганата калия, подкисленным серной кислотой.
32. К раствору нитрата алюминия добавили раствор сульфида натрия. Полученный газ поглотили раствором перманганата калия, подкисленным серной кислотой, при этом наблюдали образование осадка. Осадок отделили и обработали горячим концентрированным раствором гидроксида калия. Полученную при этом кислородосодержащую соль добавили в раствор, содержащий дихромат калия и серную кислоту.
33. Оксид хрома(VI) поместили в раствор гидроксида калия. В полученный при этом раствор добавили раствор серной кислоты. Образовавшийся раствор дополнительно подкислили серной кислотой и пропустили через этот раствор сероводород. Образовавшийся при этом осадок отделили и поместили в горячий концентрированный раствор гидроксида калия.
34. Фосфид цинка растворили в соляной кислоте. Полученный газ поглотили концентрированным раствором азотной кислоты при нагревании, при этом наблюдали выделение бурого газа. Бурый газ пропустили через раствор гидроксида натрия. К полученному раствору добавили раствор, содержащий дихромат натрия и серную кислоту.
Бурый газ пропустили через раствор гидроксида натрия. К полученному раствору добавили раствор, содержащий дихромат натрия и серную кислоту.
35. Алюминий добавили к раствору гидроксида натрия. Через образовавшийся прозрачный раствор пропустили газ, полученный при растворении серы в концентрированной серной кислоте. Образовавшийся осадок отделили, а к полученному раствору добавили раствор перманганата калия.
Понравилось это:
Нравится Загрузка…
Сравнение бок о бок: гидроксид калия и гидроксид натрия — сходства, различия и варианты использования
Иногда выбор подходящего химического вещества для вашего проекта может оказаться сложным. Химический мир огромен, и в нем так много похожих соединений, что иногда у вас есть выбор между несколькими химическими веществами, которые подойдут для вашего проекта. Но какой из них будет работать лучше ?
Два соединения, которые часто одинаково жизнеспособны, — это гидроксид калия и гидроксид натрия. Если вы застряли между этими двумя составами, эта статья поможет вам определить, какой из них будет для вас лучшим выбором.
Если вы застряли между этими двумя составами, эта статья поможет вам определить, какой из них будет для вас лучшим выбором.
Гидроксид калия (KOH) и гидроксид натрия (NaOH) являются гидроксидами щелочных металлов. Как и большинство соединений, гидроксид калия и гидроксид натрия имеют общие названия, с которыми вы, вероятно, знакомы. Вы можете знать гидроксид натрия как щелочь или едкий натр; в то время как гидроксид калия широко известен как поташ.
Использование гидроксида калия и гидроксида натрия
Гидроксид калия и гидроксид натрия используются во многих производственных областях. Они очень похожи — подробнее об этом чуть позже — и часто могут использоваться в одних и тех же приложениях.
При производстве мыла гидроксид калия и гидроксид натрия используются для омыления — процесса, в ходе которого жиры превращаются в мыло. Точно так же оба соединения могут быть использованы для производства биодизеля. Гидроксид калия и гидроксид натрия реагируют с триглицеридами таким же образом, растворяя триглицериды, что позволяет метанолу связываться с жирными кислотами, основой биодизельного топлива. И оба одобрены FDA в качестве загустителя и стабилизатора в обработанных пищевых продуктах.
Гидроксид калия и гидроксид натрия реагируют с триглицеридами таким же образом, растворяя триглицериды, что позволяет метанолу связываться с жирными кислотами, основой биодизельного топлива. И оба одобрены FDA в качестве загустителя и стабилизатора в обработанных пищевых продуктах.
Несмотря на их сходство, есть несколько применений, в которых вы не можете поменять одно на другое. Гидроксид калия используется в качестве электролита в щелочных батареях. Между тем, гидроксид натрия используется для очистки воды.
Но чтобы лучше понять, когда лучше выбрать один из них, вам необходимо понять сходства и различия между гидроксидом калия и гидроксидом натрия.
Сходство гидроксида калия и гидроксида натрия
Гидроксид калия и гидроксид натрия являются сильно коррозионными сильными основаниями. Оба образуются путем ионного связывания щелочного металла с гидроксильной группой. Из всех соединений группы гидроксидов наиболее химически сходны гидроксид калия и гидроксид натрия.
Их сильное химическое сходство позволяет им легко заменять друг друга в ряде применений. Соответственно, их химические реакции удивительно похожи. Поскольку гидроксид калия и гидроксид натрия являются сильными основаниями, они реагируют с водой с выделением тепла. Таким образом, они оба сильно экзотермичны.
Их химическое сходство приводит и к физическому сходству. В твердой форме они представляют собой белый порошок или хлопья. При растворении каждый из них можно использовать в виде водного раствора.
Различия между гидроксидом калия и гидроксидом натрия
Хотя гидроксид натрия и гидроксид калия очень похожи, они существенно различаются. Начнем с того, что калий и натрий вносят разное количество протонов. Натрий приносит 11 протонов, а калий отдает 19.. Точно так же металл в гидроксиде натрия легче, чем в гидроксиде калия. Это способствует тому, что их атомные массы сильно различаются: 39,997 г/моль и 56,106 г/моль соответственно.
Но на самом деле их различия начинаются на молекулярном уровне. Гидроксид калия немного меньше, чем гидроксид натрия, что означает, что он прорезает молекулы масла быстрее, чем гидроксид натрия. Это делает гидроксид калия отличным выбором для мыла, которое необходимо для удаления затвердевшего масла.
Их реакции также немного отличаются. И гидроксид натрия, и гидроксид калия выделяют тепло при взаимодействии с водой. Но химический состав гидроксида калия выделяет немного меньше тепла, чем гидроксид натрия при воздействии воды.
Из-за производственных затрат гидроксид калия обычно дороже, чем гидроксид натрия. Гидроксид натрия производится с использованием хлорида натрия, также известного как обычная поваренная соль. Тогда как хлорид калия, более дорогое соединение, используется для производства гидроксида калия.
При выборе между гидроксидом калия и гидроксидом натрия нужно учитывать множество факторов. Свяжитесь с нами, чтобы поговорить с нашей командой знающих штатных химиков, которые могут предоставить техническую помощь на основе спецификаций вашего проекта.
Или, если вы уже выбрали идеальное соединение для своего проекта, просмотрите наш обширный онлайн-каталог, и вам доставят идеальное химическое вещество для вашего проекта.
КУПИТЕ ЭТИ ХИМИКАТЫ В NOAH CHEMICALS
Компания Noah Chemicals предлагает клиентам самые чистые химикаты. Купите эти химикаты прямо из нашего обширного онлайн-каталога. Чтобы поговорить с квалифицированным химиком о нестандартных химикатах и оптовом заказе, свяжитесь с нами сегодня!
КАЛИЯ ГИДРОКСИД
КАЛИЯ ГИДРОКСИД, чистота 99,9%, чешуйки, KOH
0005
SODIUM HYDROXIDE
SODIUM HYDROXIDE, 50% SOLUTION, Reagent, (Caustic Soda), NaOH
SODIUM HYDROXIDE, 99% pure, beads, (Caustic Soda), NaOH
ГИДРОКСИД НАТРИЯ, чистота 99,99%, гранулы, (каустическая сода), NaOH
ГИДРОКСИД НАТРИЯ, реагент ACS, гранулы, (каустическая сода), NaOH
0015 химическое сырье
, используемое в промышленности, одним из наиболее известных, но наименее изученных, является карбонат калия .
Карбонат калия имеет химическую формулу K2CO3 , но также называется дикалий карбонат , карбонат калия , зола жемчужная , соль винного камня, соль полыни 905 901 или просто калиевая соль 9016.
Слово поташ используется для всех видов добываемых и промышленных солей, содержащих калий в водорастворимой форме . Это связано с тем, что до индустриализации эти продукты производились путем замачивания растительной или древесной золы в горшке.
В настоящее время карбонат калия получают путем взаимодействия гидроксида калия с диоксидом углерода . При кристаллизации раствор образует гидрат калия , который при нагревании более чем до 200°C образует K2CO3 . Это безводная соль т – и вкус у нее соленый.
В этой базовой форме 9Карбонат калия 0015 выглядит как бесцветные кристаллы, но обычно поставляется в виде белого порошка.
Это такой известный химический продукт , потому что он имеет очень много применений. Например, его можно найти в огнетушителях, как источник калия для сельскохозяйственных культур и домашнего скота, как осушающий агент в фармацевтической промышленности, как смягчитель воды , как технологическое вещество при приготовлении пищи и в производство стекла . Однако чаще всего он используется в производстве мыла .
Его эффективность в качестве ингредиента моющего средства основана на том, как карбонат калия образует щелочную среду, которая делает его способным удалять нежелательные нерастворимые пятна. Он также действует как строитель из-за его более высокой растворимости при низких температурах.
В самом простом определении мыло представляет собой химическую реакцию между гидроксидом натрия и жиром или маслом. Продуктом этой реакции является глицерин (увлажнитель) и натриевые соли жирных кислот (мыло). Полезность карбоната калия в качестве сырья для мыла заключается в том, что вместо сжигания щелочей и последующего превращения жирных кислот в мыло жиры нейтрализуются как натрием , так и калием . Этого процесса достаточно для удаления даже нерастворимых масел, таких как растительное масло, пятна пота и моторная смазка, даже в особенно кислой среде или в жесткой воде.
Продуктом этой реакции является глицерин (увлажнитель) и натриевые соли жирных кислот (мыло). Полезность карбоната калия в качестве сырья для мыла заключается в том, что вместо сжигания щелочей и последующего превращения жирных кислот в мыло жиры нейтрализуются как натрием , так и калием . Этого процесса достаточно для удаления даже нерастворимых масел, таких как растительное масло, пятна пота и моторная смазка, даже в особенно кислой среде или в жесткой воде.
Beyond мыло и моющие средства для рук , карбонат калия также является практичным ингредиентом для
Тем не менее, именно в моющих средствах наиболее примечателен карбонат калия , хотя для стирки одежды требуется нечто большее, чем простое смешивание некоторых K2CO3 .
Например, размер частиц может играть важную роль в очищающих свойствах карбоната калия , так как это ключ к эффективному дозированию, диспергированию и растворению порошкообразных моющих средств для стирки .
Медленное дозирование порошка позволяет образовывать осадок в ящике многих автоматических стиральных машин. Эта проблема обычно возникает из-за порошка с насыпной плотностью от средней до высокой.
Исследование по этой теме показало, что «конкретные сорта карбоната калия при добавлении в качестве отдельного ингредиента в виде частиц (постдозированного) к уже 9Состав 0015 на основе моющей основы в виде частиц значительно сокращает время дозирования всей моющей композиции ».
Хотя последствия эвтрофикации в результате попадания остатков моющего средства в реки и ручьи вынуждают некоторых производителей моющих средств увеличивать использование карбонатов щелочных металлов (особенно карбоната натрия ), карбонат калия остается важным ингредиентом для стирки . Это особенно актуально для районов с жесткой водой, так как K2CO3 является отличным средством для смягчения воды r.
Это особенно актуально для районов с жесткой водой, так как K2CO3 является отличным средством для смягчения воды r.
Несмотря на то, что был известен как полезный чистящий ингредиент
Это химический продукт , которым люди пользуются ежедневно, но каким-то образом он остается анонимным. Малоизвестный химикат в повседневной современной жизни — тот, который делает нашу еду вкуснее, — это сырье для производства стекла и помогает тушить пожары. Но, в конечном счете, карбонат калия — это буквально раствор для стирки белья.
Если вы хотите узнать больше об очищающей способности карбоната калия или если вы хотите получить качественные промышленные химикаты, такие как K2CO3, посетите AG CHEMI GROUP.
