Влияние карбида кальция в качестве раскислителя на химический состав и загрязненность неметаллическими включениями
Journals → Черные металлы → 2019 → #5 → Back
| 55 лет кафедре «Технология материалов» Волгоградского государственного технического университета | |
| ArticleName | Влияние карбида кальция в качестве раскислителя на химический состав и загрязненность неметаллическими включениями |
| ArticleAuthor | Д. В. Руцкий, Н. А. Зюбан, И. В. Неклюдов, А. Ю. Агарков |
| ArticleAuthorData | Волгоградский государственный технический университет, Волгоград, Россия:
АО «Волжский трубный завод» (АО «ВТЗ»), г. А. Ю. Агарков, ведущий инженер-технолог лаборатории выплавки и разливки стали ЦЗЛ |
| Abstract | Приведены результаты исследования загрязненности углеродистой стали марки Д неметаллическими включениями в пробах, отобранных на всех этапах металлургического передела в условиях электросталеплавильного цеха (ЭСПЦ) АО «ВТЗ». Исследования показали, что использование алюминия в качестве раскислителя приводит к образованию в стали преимущественно тугоплавких недеформируемых включений корунда (Al2O3), имеющих неблагоприятную для дальнейшей обработки давлением форму. Внепечная обработка способствует снижению загрязненности стали неметаллическими включениями, а также модификации и глобуляризации включений корунда. Использование в качестве раскислителя алюминия приводит к повышению загрязненностью неметаллическими включениями непрерывнолитой заготовки. Исследование выполнено при финансовой поддержке РФФИ в рамках научного проекта № 18-08-00050\18. |
| keywords | Раскисление, алюминий, карбид кальция, неметаллические включения, химический состав, форма, выплавка, внепечная обработка, непрерывнолитая заготовка |
| References | 1. 5. Григорович К.  В. Исследование структуры и металлургического качества рельсовых сталей различных производителей // Металлы. 2006. № 5. С. 1–16. В. Исследование структуры и металлургического качества рельсовых сталей различных производителей // Металлы. 2006. № 5. С. 1–16.6. Gamanyuk S. B., Zyuban N. A., Rutskii D. V., Babin G. V. Understanding the effect of deoxidation regime on the formation and arrangement of sulphide inclusions and on mechanical properties in steel // CIS Iron and Steel Review. 2018. Vol. 16. P. 44–48. 7. Агбоола О. Ф., Морозова Т. В., Дуб А. В. Неметаллические включения в низколегированной трубной стали // Металлург. 2005. № 4. С. 67–73. 9. Кислинг Р., Ланге Н. Неметаллические включения в стали : пер. с англ. / под. ред. В. М. Розенберга. — М. : Металлургия, 1968. — 124 с. 10. Григорович К. В., Гарбер А. К. Анализ процессов внепечной обработки углеродистых сталей // Перспективные материалы.  2011. № 13. С. 13–25. 2011. № 13. С. 13–25.11. Шахпазов Е. Х., Зайцев А. И., Шапошников Н. Г., Родионова И. Г., Рыбкин Н. А. К проблеме физико-химического прогнозирования типа неметаллических включений. Комплексное раскисление стали алюминием и кальцием // Металлы. 2006. № 2. С. 3–13. 12. Takashi Kimura, Hideaki Suito. Calcium Deoxidation Equilibrium in liquid iron // MMTB, 1994. Vol. 25B. P. 33–42. 13. Котельников Г. И., Зубарев К. А., Мовенко Д. А. и др. Построение кривой раскисления железа кальцием // Электрометаллургия. 2016. № 6. С. 10–18. 14. Fujiwara H., Tano M., Yamamoto K., Ichise E. Solubility and activity of calcium in molten iron in equilibrium with lime and thermodynamics of calcium containing iron melts // ISIJ Int. 1996. Vol. 35, No. 9. P. 1063–1071. 15. Кудрин В. А. Теория и технология производства стали : учеб. для вузов. — М. : Мир, ООО «Издательство ACT», 2003. — 528 с. 16. Лаптев Д.  М. Задачи и упражнения по термодинамике растворов. — М. : Металлургия, 1965. М. Задачи и упражнения по термодинамике растворов. — М. : Металлургия, 1965.17. Shin J. H., Park J. H. 18. Ерошкин С. Б., Прудов К. Э., Попов О. В. и др. Повышение чистоты металла при внепечной обработке карбидом кальция // Сталь. 2007. № 12. С. 26–28. 19. Чайкин В. А., Чайкин А. В., Косимов А. Д. и др. Новый материал для диффузионного раскисления в агрегате комплексной обработки сталей // Черные металлы. 2018. № 9. С. 10–15. 20. Котельников Г. И., Зубарев К. А., Мовенко Д. А. и др. Построение кривой раскисления железа кальцием // Электрометаллургия. 2016. № 6. С. 10–18. 21. Свяжин А. А., Крушке Э., Свяжин А. Г. Применение карбида кальция при выплавке низкоуглеродистой стали // Металлург. 2004. № 11. С.  43–45. 43–45.22. ГОСТ 1778–70 (ISО 4967). Сталь. Металлографические методы определения неметаллических включений (Steel. Metallographic methods for the determination of nonmetallic inclusions). — Введ. 29.07.2011. 23. Lis T. Modification of oxygen and sulphur inclusions in steel by calcium treatment // Metalurgija. 2009. Vol. 2, No. 48. P. 95–98. 24. Huemer K., Wolf G., Sormann A., Frank G. Auswirkungen einer Kalziumbehandlung auf die Entstehung und Zusammensetzung von nichtmetallischen EinschlOssen bei der Erzeugung von aluminiumberuhigten Stahlen für Langprodukte // BHM. 2005. 150. Heft 7. S. 237–242. 25. Поживанов М. А., Шахпазов Е. Х., Свяжин А. Г. Выплавка стали для автолиста. — М. : Интерконтакт Наука, 2006. — 166 с. 26. Воскобойников В. Г., Кудрин В. А., Якушев A. M. Общая металлургия. — М. : Академкнига, 2002. — 168 с. 27. Шахпазов Е. Х., Зайцев А. И., Шапошников Н.  28. Бигеев А. М., Бигеев В. А. Металлургия стали. Теория и технология плавки стали : учеб. для вузов — 3-е изд. перераб. и доп. — Магнитогорск : МГТУ, 2000. — 544 с. 29. Айзатулов Р. С., Харлашин П. С., Протопопов Е. В., Назюта Л. Ю. Теоретические основы сталеплавильных процессов : учеб. пособие для вузов. — М. : МИСиС, 2004. — 320 с. 30. Pires J. C. S., Garcia A. Study of the Nature of Non-Metallic Inclusions in Samples of Aluminum and Silicon Killed Low Carbon Steels, Collected in the Refining Treatment and Continuous Casting Stages // Materials Research. 2004. Vol. 7. No. 4. P. 517–521. |
| Language of full-text | russian |
| Full content | Buy |
Back
Опыт использования карбида кальция для раскисления стали взамен алюминия в условиях ОАО «БМЗ – управляющая компания холдинга «БМК» | Грудницкий
О. М. Грудницкий
М. Грудницкий
https://doi.org/10.21122/1683-6065-2020-2-53-58
Полный текст:
- Аннотация
- Об авторе
- Список литературы
Аннотация
В статье рассматриваются вопросы, связанные с использованием в сталеплавильном производстве карбида кальция, взамен алюминия вторичного и других раскисляющих материалов с целью снижения стоимости раскисления стали и шлака.
Предполагалось, что снижение содержания алюминия в металле арматурного сортамента сталей улучшит его разливаемость, а за счет улучшения разливаемости повысится выход годного металла. Также ожидалось, что в результате использования карбида кальция для раскисления покровного шлака в стальковше произойдет снижение степени загрязнения стали кордового назначения неметаллическими включениями.
В ходе проведения испытаний определяли оптимальное количество присадки материала. В целом в результате проведенных работ было установлено, что карбид кальция может быть использован для раскисления шлака и металла при внепечной обработке стали.
В целом в результате проведенных работ было установлено, что карбид кальция может быть использован для раскисления шлака и металла при внепечной обработке стали.
Подробно описаны способы присадки материала. Приведены результаты проведенной работы.
Ключ. слова
раскисление, карбид кальция, стальковш, шлак, расплав, внепечная обработка,
Об авторе
О. М. Грудницкий
БМЗ– управляющая компания холдинга «БМК»
Россия
Список литературы
1. Свяжин A.A. Применение карбида кальция при выплавке низкоуглеродистой стали / A.A. Свяжин [и др.] // Металлург. 2004.
2. Попов А. В. Разработка и внедрение технологии внепечной обработки стали с применением карбида кальция в условиях ЭСПЦ ЧерМК ОАО «Северсталь» // Диссертация. 2008.
2008.
Дополнительные файлы
Для цитирования: Грудницкий О.М. Опыт использования карбида кальция для раскисления стали взамен алюминия в условиях ОАО «БМЗ – управляющая компания холдинга «БМК». Литье и металлургия. 2020;(2):53-58. https://doi.org/10.21122/1683-6065-2020-2-53-58
For citation: Grudnitsky О.M. The experience of using calcium carbide for the deoxidation of steel to replace aluminum in the conditions of OJSC «BSW – Management company of the holding «BMC». Litiyo i Metallurgiya (FOUNDRY PRODUCTION AND METALLURGY). 2020;(2):53-58. (In Russ.) https://doi.org/10.21122/1683-6065-2020-2-53-58
Просмотров: 458
Обратные ссылки
- Обратные ссылки не определены.
Контент доступен под лицензией Creative Commons Attribution 4. 0 License.
0 License.
ISSN 1683-6065 (Print)
ISSN 2414-0406 (Online)
Карбид кальция – универсал во вторичной металлургии
13.07.2022, Alzchem, Металлургия
Не все стали одинаковы: в принципе универсальный и почти вездесущий металл всегда состоит из железа и небольшого количества углерода. Различные дополнительные сопутствующие легирующие элементы существенно влияют на свойства материала. Однако существует множество способов производства стали из чугуна. Их всех объединяет то, что весьма специфическое качество конечного продукта определяется последующей обработкой, так называемой вторичной металлургией.
Основное внимание во вторичной металлургии уделяется эффективному снижению уровня побочных продуктов, снижающих качество, таких как сера и кислород. Здесь в игру вступает карбид кальция: благодаря своему высокому сродству к кислороду и сере карбид кальция используется в качестве высокоэффективного реагента в различных областях вторичной металлургии. В качестве сильного восстановителя он особенно подходит для десульфурации и раскисления стали, где требуется низкое содержание серы и кислорода, а также отлично подходит для обработки шлака.
В качестве сильного восстановителя он особенно подходит для десульфурации и раскисления стали, где требуется низкое содержание серы и кислорода, а также отлично подходит для обработки шлака.
Для раскисления и десульфурации добавляют карбид кальция в виде мелкодисперсного порошка; однако для обработки шлака действующее вещество проявляет наибольшую эффективность в более грубой форме.
Преимущества карбида кальция во вторичной металлургии с первого взгляда:
Высокий потенциал для экономии затрат
Улучшенная чистота металлов благодаря эффективному деоксидированию и Desulfurization
REDECATED SLETITITETS и DESULFURICATION
- 2 REDECATED SYTETITITET SLITITITITETS и DESULFURICATIO формирователи
извлечение окисленных металлов, таких как хром, марганец, кремний, железо шлак
Alzchem предлагает другие продукты на основе карбида кальция. Это продукты CaD ® для десульфурации чугуна, а также CalciPro 9.0045 ® , разработанный для обработки кальция порошковой проволокой. Кроме того, в нашем портфеле продуктов для сталелитейной промышленности есть Calzot ® : этот продукт основан на цианамиде кальция и используется для легирования азотом.
Это продукты CaD ® для десульфурации чугуна, а также CalciPro 9.0045 ® , разработанный для обработки кальция порошковой проволокой. Кроме того, в нашем портфеле продуктов для сталелитейной промышленности есть Calzot ® : этот продукт основан на цианамиде кальция и используется для легирования азотом.
Здесь вы можете найти дополнительную информацию о карбиде кальция
Более
Вернуться к обзору новостей
Alzchem – глобальная компания по производству специальных химикатов, которая преимущественно входит в число лидеров рынка в своих областях деятельности. В частности, компания Alzchem извлекает выгоду из трех очень разных глобальных тенденций изменения климата, роста населения и увеличения продолжительности жизни. Для достижения поставленных социальных целей продукция Alzchem может предложить привлекательные решения с широким спектром различных применений.
Компания видит для себя интересные перспективы роста, особенно в области питания людей и животных и сельского хозяйства. В результате роста населения необходимо добиться эффективного производства продуктов питания. Фармацевтическое сырье и наши креатиновые продукты могут способствовать здоровому старению по мере увеличения продолжительности жизни. Alzchem стремится к обеспечению устойчивости, связанной с изменением климата, в области возобновляемых источников энергии и во всей компании. Области тонкой химии и металлургии предлагают столь же большие перспективы.
Широкий ассортимент продукции Alzchem Group AG включает пищевые добавки, прекурсоры для тестов на короновирус и фармацевтическое сырье. Эти продукты являются ответом нашей компании на мировые тенденции и разработки. Alzchem находится в идеальном положении в этом отношении и считает себя хорошо подготовленным к экологически ориентированному будущему и глобальным разработкам.
В компании работает около 1630 человек на четырех производственных площадках в Германии и одном заводе в Швеции, а также в двух торговых компаниях в США и Китае. В 2020 году консолидированные продажи Alzchem составили около 379 евро.млн и EBITDA около 53,8 млн евро.
В 2020 году консолидированные продажи Alzchem составили около 379 евро.млн и EBITDA около 53,8 млн евро.
Химические характеристики карбида кальция и его реакция с водой
Похоже, вы зашли на наш сайт из Германия . Пожалуйста, перейдите на наш региональный сайт для получения более актуальных цен, сведений о продуктах и специальных предложениях.
Выбрать другую страну
Почему так бодро?
[Депозитные фотографии]Карбид кальция представляет собой химическое соединение кальция и углерода и в чистом виде представляет собой белое кристаллическое вещество. Его получают по реакции
Ca + 2C → CaC₂
Карбид кальция [Викимедиа] Карбид кальция имеет большое практическое значение. Он также известен как ацетилид кальция.
Он также известен как ацетилид кальция.
Химические характеристики карбида кальция
Карбид кальция не летуч и не растворим ни в одном известном растворителе и реагирует с водой с образованием газообразного ацетилена и гидроксида кальция. Его плотность составляет 2,22 г/см³. Температура плавления 2160°С, температура кипения 2300°С. Поскольку ацетилен, образующийся при контакте с водой, легко воспламеняется, вещество отнесено к классу опасности 4.3.
Ацетилид кальция был впервые получен немецким химиком Фридрихом Вёлером в 1862 году при нагревании сплава цинка и кальция с углем. Ученый описал реакцию карбида кальция с водой. Карбид кальция энергично реагирует даже со следами Н₂O, выделяя большое количество тепла. При недостаточном количестве воды образующийся ацетилид самопроизвольно воспламеняется. Ацетилид кальция бурно реагирует с водными растворами щелочей и разбавленными неорганическими кислотами. Эти реакции высвобождают ацетилид. Благодаря своим сильным восстановительным свойствам CaC₂ восстанавливает все оксиды металлов до чистых металлов или превращает их в карбиды.
Легче получить карбид кальция из его оксида, чем из самого кальция, так как оксид восстанавливается при температуре выше 2000 °C. Соединение металла и углерода:
CaO + 3C → CO↑ + CaC₂
Реакция происходит в электродуговой печи, где нагревается смесь негашеной извести и кокса или антрацита. Технический продукт имеет серый цвет из-за наличия свободного углерода, оксида кальция, фосфида, сульфида и других химических соединений. CaC₂ составляет 80-85% продукта по массе.
Использование карбида кальция
В прошлом карбид кальция использовался в карбидных лампах, где он служил источником ацетиленового пламени. В настоящее время эти лампы все еще используются для питания маяков и маяков, а также при исследовании пещер. CaC₂ также служит сырьем для разработки химических технологий, прежде всего синтетического каучука. Карбид кальция также используется для производства винилхлорида, ацетиленовой сажи, акрилонитрила, уксусной кислоты, ацетона, этилена, стирола и синтетических смол.
В металлургии карбид кальция применяют для раскисления металлов и снижения содержания в них кислорода и серы (десульфурация). Карбид кальция используется для производства порошкообразного карбида, регулятора роста растений. Для получения одной тонны CaC₂ требуется 3000 кВт/ч электроэнергии. По этой причине производство вещества рентабельно только при низких затратах на электроэнергию. В то же время производство карбида кальция во всем мире постоянно увеличивается.
Карбид кальция – реакция с водой
При реакции карбида кальция с водой выделяется ацетилен:
2H₂O + CaC₂ → C₂H₂↑ + Ca(OH)₂
Ацетилен – промышленное вещество с неприятным запахом содержащимися в нем примесями (NH₃, H₂S, PH₃ и др.). В чистом виде ацетилен представляет собой бесцветный газ с характерным слабым запахом, растворяется в воде.
Чтобы продемонстрировать реакцию карбида кальция с водой, можно использовать простой опыт: налить воду в бутыль объемом 1,5 л, быстро добавить несколько кусочков карбида кальция и закрыть бутыль пробкой. В результате последующей реакции между карбидом кальция и водой ацетилен накапливается в бутылке по мере роста давления. Как только реакция прекратится, поместите в бутылку горящую бумажку – это должно вызвать взрыв, сопровождаемый огненным облаком. Поскольку в результате реакции стенки бутылки могут лопнуть, этот эксперимент опасен и должен проводиться только при строгом соблюдении техники безопасности.
Внимание! Не пытайтесь проводить эти эксперименты без профессионального присмотра! Посмотрите здесь эксперименты с пламенем, которые вы можете безопасно проводить дома
Чтобы продемонстрировать реакцию карбида кальция с водой, эксперимент можно повторить в модифицированном виде — с шестилитровой бутылью. При этом компоненты необходимо взвешивать с точностью, ведь чем больше радиус бутылки, тем меньше емкость выдерживает высокое давление (при условии одинакового материала и толщины стенок). Бутылка большой емкости имеет большой радиус, но стенки у нее примерно такие же — соответственно, она менее устойчива к давлению. Чтобы он не взорвался, необходимо заранее рассчитать количество карбида кальция. Молярная масса кальция составляет 40 г/моль, а углерода — 12 г/моль, поэтому молярная масса карбида кальция составляет около 64 г/моль. Соответственно, из 64 г карбида получится 22,4 л ацетилена. Объем баллона 6 л, а давление поднялось примерно на 4 атмосферы.
При этом компоненты необходимо взвешивать с точностью, ведь чем больше радиус бутылки, тем меньше емкость выдерживает высокое давление (при условии одинакового материала и толщины стенок). Бутылка большой емкости имеет большой радиус, но стенки у нее примерно такие же — соответственно, она менее устойчива к давлению. Чтобы он не взорвался, необходимо заранее рассчитать количество карбида кальция. Молярная масса кальция составляет 40 г/моль, а углерода — 12 г/моль, поэтому молярная масса карбида кальция составляет около 64 г/моль. Соответственно, из 64 г карбида получится 22,4 л ацетилена. Объем баллона 6 л, а давление поднялось примерно на 4 атмосферы.
Бутылка должна выдерживать пять атмосфер: для проведения эксперимента берем около 64 г карбида кальция и около 0,5 л воды. Поместите кусок карбида в небольшой пакет. Вставьте пакет в бутылку, затем быстро закройте бутылку пробкой. Реакция карбида кальция с водой продолжается несколько минут, бутылка вздувается и процесс сопровождается громкими хлопками, но бутылка должна это выдержать.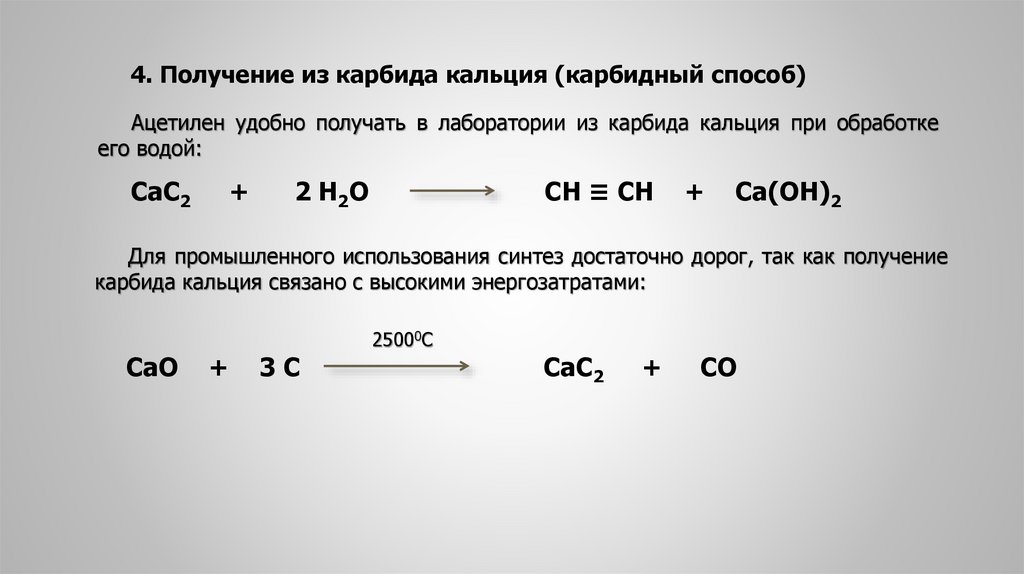

 Волжский, Россия:
Волжский, Россия:
 Кузнецов А. А., Сумин С. Н., Козлов Г. С. Изменение активности кислорода в процессе внепечной обработки стали при раскислении ее алюминием или карбидом кальция // Научно-технический прогресс в металлургии — 2013: мат-лы междунар. науч. сем. — Череповец : ЧГУ, 2014. С. 30–33.
Кузнецов А. А., Сумин С. Н., Козлов Г. С. Изменение активности кислорода в процессе внепечной обработки стали при раскислении ее алюминием или карбидом кальция // Научно-технический прогресс в металлургии — 2013: мат-лы междунар. науч. сем. — Череповец : ЧГУ, 2014. С. 30–33.