Формула хлорида кальция в химии
Определение и формула хлорида кальция
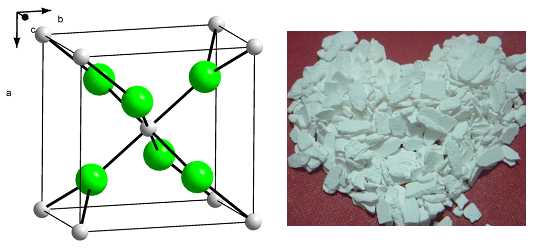
Химическая формула –
Молярная масса равна г/моль.
Физические свойства – белые кристаллы, плавящиеся без разложения.
Расплывается на воздухе из-за энергичного поглощения влаги.
Хорошо растворяется в воде (не гидролизуется).
Образует кристаллогидрат состава .
Химические свойства хлорида кальция
- Хлорид кальция вступает в реакции обмена с кислотами:
- Взаимодействует с щелочами:
- При высокой температуре в присутствии катализатора реагирует с водородом:
Получение
Хлорид кальция можно получить по реакции обмена:
При взаимодействии оксида кальция и хлора при высокой температуре:
Применение
Хлорид кальция находит разнообразное применение, особенно в неорганическом синтезе, в качестве консерванта (при консервировании овощей и фруктов), противогололёдное средство; как отвердитель в продуктах питания.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Хлорид кальция — это… Что такое Хлорид кальция?
Хлори́д ка́льция, CaCl2 — кальциевая соль соляной кислоты. Зарегистрирован в качестве пищевой добавки E509. Считается безвредным (как добавка).
Свойства
Бесцветные кристаллы плотностью 2,51 г/см³, tпл 772 °C. Обладает высокими гигроскопическими свойствами. Растворимость (г на 100 г H 2O): 74 (20 °C) и 159 (100 °C). Водные растворы хлорида кальция замерзают при низких температурах (20%-ный — при −18,57 °C, 30%-ный — при −48 °C).
Кристаллогидраты хлорида кальция
CaCl2 образует гидрат CaCl2·6H2O, устойчивый до 29,8 °C; при более высоких температурах из насыщенного раствора выпадают кристаллогидраты с 4, 2 и 1 молекулами H2O. При смешении CaCl2*6H2O (58,8 %) со снегом или льдом (41,2 %) температура понижается до —55 °C (криогидратная точка).
Природный минерал гексагидрата хлорида кальция, ставший известным как антарктикит[ru], был впервые обнаружен на дне солёного озера Дон-Жуан на Земле Виктории в Антрактиде.
Получение
Хлорид кальция получают как побочный продукт в производстве соды.
В быту можно получить технический хлорид кальция нагреванием хлорной извести.
Применение
Применяют для получения металлического кальция, для осушки и понижения точки росы технологического и импульсного газа:
- На ГРС[прояснить], КС[прояснить] магистральных газопроводов;
- На АГНКС[прояснить];
- На объектах газодобычи при подготовке газа к транспортировке;
- В холодильном деле;
- Как ускоритель схватывания цемента;
- Для обеспыливания гравийных дорог;
- Как противогололёдное средство;
- Как отвердитель в продуктах питания;
- В молокоперерабатывающей промышленности при производстве ферментированных молочных продуктов, и играет большую роль в формировании сгустка. Добавление хлористого кальция ведет к увеличению выхода конечного продукта, а также улучшает его свойства;
- В медицине.
См. также
Источник
Плазмозамещающие и перфузионные растворы — АТХ код: B05| B05A |
| ||
|---|---|---|---|
| B05B |
| ||
| B05C |
| ||
| B05D |
| ||
| B05X |
| ||
| B05Z |
dic.academic.ru
Хлорид кальция: свойства и все характеристики
Характеристики и физические свойства хлорида кальция
Он расплывается на воздухе из-за энергичного поглощения влаги. Хорошо растворяется в воде (не гидролизуется). Кристаллогидратов не образует.

Рис. 1. Хлорид кальция. Внешний вид.
Таблица 1. Физические свойства хлорида кальция.
|
Молекулярная формула |
CaCl2 |
|
Молярная масса |
111 |
|
Плотность (20oС), г/см3 |
2,15 |
|
Температура плавления, oС |
772 |
|
Температура кипения, oС |
1935 |
|
Растворимость в воде (20oС), г/100 мл |
74,5 |
Получение хлорида кальция
Основной способ получения хлорида кальция – взаимодействие хлорида аммония с гидроксидом кальция (промежуточная стадия при производстве соды):
2NH4Cl + Ca(OH)2 = 2NH3↑ + CaCl2 + 2H2O.
Химические свойства хлорида кальция
В водном растворе хлорид кальция диссоциирует на ионы:
CaCl2↔Ca2+ + 2Cl—.
Хлорид кальция взаимодействует с концентрированными растворами сильных минеральных кислот:
CaCl2 + H2SO4 (conc) = CaSO4↓ + 2HCl↑.
Он способен реагировать с щелочами в водных растворах:
CaCl2 + 2NaOHconc = Ca(OH)2↓ + 2NaCl.
Взаимодействие хлорида кальция с другими солями возможно только если продукт взаимодействия выводится из реакционной среды:
CaCl2+ Na2CO3 = CaCO3↓ + 2NaCl;
CaCl2+ 2NH4F = CaF2↓ + 2NH4Cl;
Пропускание водорода через раствор карбонатахлорида кальция приводит к образованию гидрида кальция и соляной кислоты:
CaCl2 + H2↔ CaH2 + 2HCl (t = 600 – 700oC, kat = Pt6 Fe, Ni).
Применение хлорида кальция
Хлорид кальция нашел применение в лабораторной практике (наполнитель осушающих трубок, сырье для получения кальция), пищевой промышленности (смягчение баранины, консервант), медицине, как компонент противогололедных реагентов и т.д.
Примеры решения задач
ru.solverbook.com
Хлористый Кальций: цена в аптеке, инструкция по применению, показания, отзывы косметологов о пилинге лица
Читайте нас и будьте здоровы! Пользовательское соглашение о портале обратная связь- Врачи
- Болезни
- Кишечные инфекции (5)
- Инфекционные и паразитарные болезни (27)
- Инфекции, передающиеся половым путем (6)
- Вирусные инфекции ЦНС (3)
- Вирусные поражения кожи (12)
- Микозы (10)
- Протозойные болезни (1)
- Гельминтозы (5)
- Злокачественные новообразования (9)
- Доброкачественные новообразования (7)
- Болезни крови и кроветворных органов (9)
- Болезни щитовидной железы (6)
- Болезни эндокринной системы (13)
- Недостаточности питания (1)
- Нарушения обмена веществ (1)
- Психические расстройства (31)
- Воспалительные болезни ЦНС (3)
- Болезни нервной системы (19)
- Двигательные нарушения (5)
- Болезни глаза (20)
- Болезни уха (4)
- Болезни системы кровообращения (10)
- Болезни сердца (11)
- Цереброваскулярные болезни (2)
- Болезни артерий, артериол и капилляров (9)
- Болезни вен, сосудов и лимф. узлов (8)
- Болезни органов дыхания (35)
- Болезни полости рта и челюстей (16)
- Болезни органов пищеварения (30)
- Болезни печени (2)
- Болезни желчного пузыря (8)
- Болезни кожи (32)
- Болезни костно-мышечной системы (49)
- Болезни мочеполовой системы (13)
- Болезни мужских половых органов (8)
- Болезни молочной железы (3)
- Болезни женских половых органов (27)
- Беременность и роды (5)
- Болезни плода и новорожденного (4)
- Симптомы
- Амнезия (потеря памяти)
- Анальный зуд
- Апатия
- Афазия
- Афония
- Ацетон в моче
- Бели (выделения из влагалища)
- Белый налет на языке
- Боль в глазах
- Боль в колене
- Боль в левом подреберье
- Боль в области копчика
- Боль при половом акте
- Вздутие живота
- Волдыри
- Воспаленные гланды
- Выделения из молочных желез
- Выделения с запахом рыбы
- Вялость
- Галлюцинации
- Гнойники на коже (Пустула)
- Головокружение
- Горечь во рту
- Депигментация кожи
- Дизартрия
- Диспепсия (Несварение)
- Дисплазия
- Дисфагия (Нарушение глотания)
- Дисфония
- Дисфория
- Жажда
- Жар
- Желтая кожа
- Желтые выделения у женщин
- …
- ПОЛНЫЙ СПИСОК СИМПТОМОВ>
- Лекарства
- Антибиотики (211)
- Антисептики (123)
- Биологически активные добавки (210)
- Витамины (192)
- Гинекологические (183)
- Гормональные (155)
- Дерматологические (258)
- Диабетические (46)
- Для глаз (124)
- Для крови (77)
- Для нервной системы (385)
- Для печени (69)
- Для повышения потенции (24)
- Для полости рта (68)
- Для похудения (40)
- Для суставов (161)
- Для ушей (15)
- Другие (306)
- Желудочно-кишечные (314)
- Кардиологические (149)
- Контрацептивы (48)
- Мочегонные (32)
- Обезболивающие (280)
- От аллергии (102)
- От кашля (137)
- От насморка (91)
- Повышение иммунитета (123)
- Противовирусные (113)
- Противогрибковые (126)
- Противомикробные (145)
- Противоопухолевые (65)
- Противопаразитарные (49)
- Противопростудные (90)
- Сердечно-сосудистые (351)
- Урологические (89)
- ДЕЙСТВУЮЩИЕ ВЕЩЕСТВА
- Справочник
- Аллергология (4)
- Анализы и диагностика (6)
- Беременность (25)
- Витамины (15)
- Вредные привычки (4)
- Геронтология (Старение) (4)
- Дерматология (3)
- Дети (15)
- Другие статьи (22)
- Женское здоровье (4)
- Инфекция (1)
- Контрацепция (11)
- Косметология (23)
- Народная медицина (17)
- Обзоры заболеваний (27)
- Обзоры лекарств (34)
- Ортопедия и травматология (4)
- Питание (103)
- Пласти
medside.ru
Кальция хлорид – инструкция по применению – раствор для внутривенного введения 1 г/10 мл: ампулы 10 шт.
| Раствор для в/в введения | 1 мл | 1 амп. |
| кальция хлорид | 100 мг | 1 г |
10 мл — ампулы (10) — пачки картонные.
Кальций — макроэлемент, участвующий в формировании костной ткани, процессе свертывания крови, необходим для поддержания стабильной сердечной деятельности, процессов передачи нервных импульсов. Улучшает сокращение мышц при мышечной дистрофии, миастении, уменьшает проницаемость сосудов. При в/в введении кальций вызывает возбуждение симпатической нервной системы и усиление выделения надпочечниками адреналина; оказывает умеренное диуретическое действие.
При взаимодействии раствора кальция хлорида с солями магния, щавелевой и фтористой кислотами образуются нерастворимые соединения, что позволяет применять раствор кальция хлорида в качестве антидота.
Как дополнительное средство при лечении аллергических заболеваний (в т.ч. сывороточная болезнь, крапивница, ангионевротический отек, сенная лихорадка) и аллергических реакций на лекарства. Как дополнительное гемостатическое средство при легочных, желудочно-кишечных, носовых, маточных кровотечениях. Как антидот при отравлениях солями магния, щавелевой кислотой и ее растворимыми солями, а также растворимыми солями фтористой кислоты.
При в/в введении разовая доза составляет 0.5-1 мг. При приеме внутрь разовая доза — 0.25-1.5 г. Частота и длительность применения зависят от показаний и клинической ситуации.
Возможно: брадикардия; при быстром введении — фибрилляция желудочков; при в/в введении — ощущение жара в полости рта, а затем во всем теле.
Склонность к тромбообразованию, выраженный атеросклероз, гиперкальциемия.
Не вводить п/к и в/м. При попадании кальция хлорида под кожу или в мышечные ткани развивается сильное раздражение с образованием очагов некроза.
Кальция хлорид несовместим с солями свинца, серебра, одновалентной ртути вследствие образования нерастворимых хлоридов тяжелых металлов и с барбиталом натрия, т.к. при этом образуется малорастворимая кальциевая соль барбитала.
Кальция хлорид при одновременном применении уменьшает действие блокаторов кальциевых каналов. Под влиянием колестирамина абсорбция кальция из ЖКТ снижается. При одновременном применении с хинидином возможно замедление внутрижелудочковой проводимости и повышение токсичности хинидина. Во время лечения сердечными гликозидами парентеральное применение кальция хлорида не рекомендуется, в связи с усилением кардиотоксического действия.
yandex.ru
Кальций хлористый
Упаковка и применение
Применение:
Хлорид кальция применяется
- в пищевой промышленности в качестве эмульгатора (отвердителя) Е509 при производстве сыра, творога, сухого молока; джема, желе, мармелада; консервированных овощей и фруктов;
- в молочной промышленности хлористый кальций (Е-509) используется при производстве ферментированных молочных продуктов и играет большую роль в формировании сгустка. Добавление хлористого кальция ведет к увеличению выхода конечного продукта. Он компенсирует низкий уровень содержания кальция в молоке, а также его потерю после пастеризации, влияет на продолжительность образования и вкусовое качество сгустка, т.к. ионы кальция способствуют связыванию белков.
Известковую воду (насыщенный раствор гидроксида кальция) часто добавляют к сливкам при отделении их от цельного молока, чтобы понизить их кислотность перед пастеризацией и превращением в масло. Снятое молоко затем подкисляют, чтобы отделить казеин, который смешивают с известью для получения казеинового клея. После ферментации оставшегося снятого молока (сыворотки) к нему добавляют известь, чтобы выделить лактат кальция, который используют в медицине или как сырье для последующего получения молочной кислоты. - в холодильных установках в качестве хладагента;
- в химических лабораториях как реактив при анализах;
- при изготовлении резины;
- при изготовлении анатомических перчаток для коагуляции латекса, натурального каучука;
- в качестве сырья для получения металлического кальция;
- в нефтегазовой отрасли для осушки и понижения точки росы технологического и импульсного газа на магистральных газопроводах и объектах газодобычи;
- в строительстве в качестве ускорителя схватывания цемента;
- для обеспыливания гравийных дорог;
- как противогололедное средство;Подробнее об антигололедных реагентах читайте в статье в разделе «Информация»
- в качестве лекарственного средства, восполняющего дефицит кальция в организме.
Упаковка и хранение:
Хлористый кальций хранят в крытых складских помещениях, исключающих попадание влаги.
На открытых площадках допускается хранение хлористого кальция, упакованного в специализированные мягкие контейнеры или мешки, сформированные в транспортные пакеты, скрепленные термоусадочной пленкой. Площадка, где укладываются пакеты и мягкие контейнеры, должна быть очищена от выступающих и острых предметов.
При соблюдении условий хранения и транспортировки ГОСТ регламентирует гарантийный срок хранения равный восьми месяцам со для изготовления.
veleshem.ru
| Температура | гр/100,00 гр воды |
|---|---|
| 0°C 273,15 K | 59,5 |
| 10°C 283,15 K | ~66,2 |
| 15°C 288,15 K | 69,6 |
| 20°C 293,15 K | 74,5 |
| 25°C 298,15 K | 87,3 |
| 30°C 303,15 K | 100 |
| 40°C 313,15 K | ~112 |
| 50°C 323,15 K | ~125 |
| 60°C 333,15 K | 137 |
| 70°C 343,15 K | 142 |
| 80°C 353,15 K | 147 |
| 90°C 363,15 K | 154 |
| 100°C 373,15 K | 159 |
ru.crystalls.info
