Тест по химии по теме «Металлы» (9класс)
ТЕСТ ПО ТЕМЕ «МЕТАЛЛЫ». 9класс
Вариант 1.
1. Самым распространенным металлом в земной коре является: А) Fe, В) Ti, С) Al, D) Са.
2. Назовите металл: Самый тяжелый….. и самый легкий…., самый тугоплавкий …. и самый
легкоплавкий…, самый твердый…. и самый мягкий….
3. В электротехнике для производства ламп накаливания используют металлическую нить:
А) из Al, В) из Сu, C) Мо, D) из W,
поскольку этот металл обладает наибольшей: 1) электропроводностью,
2) теплопроводностью, 3) легкоплавкостью, 4) тугоплавкостью.
4. Какой из металлов активнее всего реагирует с кислородом при комнатной температуре:
А) Fe, В) Нg, С) Ag, D) Сu.
5. С каким из перечисленных веществ может реагировать металлическая медь:
А) водород, В) оксид углерода (IV), С) кислород, D) азот.
Запишите уравнение соответствующей реакции.
6.
7. Атом элемента имеет электронную формулу: 1s22s22p63s23p64s1. Порядковый номер элемента:
A) 10, В) 12, С) 17, D) 19.
8. При электролизе расплава хлорида меди на катоде выделяется:
А) Н2, В) Сl2, С) Сu, D) О2
9. При электролизе раствора сульфата меди на катоде осаждается:
А) Н2, В) О2, С) Сu, D) Н2S.
10. Укажите неверное утверждение:
А) На внешнем уровне атомов металлов чаще всего 1-3 электрона,
В) металлам присуща металлическая связь,
С) Металлы имеют только аморфное строение,
D) Атомы металлов имеют разные значения величины радиусов их атомов.
11. Как изменяются металлические свойства в главных подгруппах сверху вниз. Укажите
правильный ответ. А) Усиливаются, так как растет число электронов в атоме,
В) Усиливаются, так как растет радиус атома, а число внешних электронов не изменяется, С) Не изменяются, так как не изменяется число электронов на внешнем уровне,
D) Ослабевают, так как не изменяется число внешних электронов.
12.Сколько электронов имеется в ионе Fe3+:
А) 26, В) 25, С) 23, D) 22.
13. При электролизе расплава хлорида натрия массой 234г. образуется металлический натрий
массой: А) 23г., В) 46г., С) 69г., D) 92г.
14. При взаимодействии 3,42г. щелочного металла с водой выделилось 448 см3 водорода (н.у.).
Назовите металл: А) Rb, В) Na, С) Li, D) К.
15. Массовая доля железа в оксиде железа (III):
А) 40%, В) 55,8%, С) 68,4% D) 70%.
16. С концентрированной азотной кислотой не будет реагировать:
C) Cr, D) Zn.
17. Металлические свойства в ряду Сr – Mo – W по мере увеличения порядкового номера: А) усиливаются, В) ослабевают, С) не изменяются, D) ослабевают, а потом
усиливаются.
18. В каком из соединений степень окисления марганца равна +6:
А) НМnO4, В) Мn2O3,
C) KMnO4, D) Na2MnO4.
19. Составьте уравнение реакции алюминия с соляной кислотой. Сумма коэффициентов перед
формулами всех электролитов: А) 6, В) 8, С) 10, D) 13.
20. Из железной руды, содержащей 320 кг. Fe2O3 выплавили 134,9 кг. железа. Найдите выход
железа от теоретического (%) :
А) 80%, В) 60%, С) 40%, D) 20%
ТЕСТ ПО ТЕМЕ «МЕТАЛЛЫ» 9 класс
Вариант 2
1. Какой из перечисленных металлов легче всего окисляется на воздухе:
А) Аl, В) Мg,
С) Nа, D) Be.
2. Восстановительными свойствами обладает: А) Fe3+, В) Са2+, C) Na, D) Na+.
3. Какой из перечисленных металлов реагирует с водой при комнатной температуре:
А) Fe, B) Zn, C) Cu, D) Ca.
4. Какой из перечисленных металлов встречается в природе в самородном состоянии:
А) Аl, B) Аu, C) Cr, D) Mg.
5. Степень окисления хрома в соединении SrCrO4:
А) +2, В) +4, С) +6 D) +7.
6. В какой из перечисленных пар оксиды являются кислотным и основным соответственно:
А) Cr2O3 и CrO, B) CrO3 и CrO,
C) CrO и Cr2O3, D) CrO и CrO3.
7. С каким из перечисленных соединений медь реагирует при обычных условиях:
А) АgNO3, B) Zn(NO3)2, C) H
8. Составьте уравнение реакции лития с соляной кислотой. Сумма коэффициентов перед
формулами всех электролитов равна:
А) 7, В) 6, С) 4, D) 2.
9. Сколько молей оксида алюминия образуется из одного моля алюминия по реакции
4Аl + 3О2 = 2Аl2О3:
А) 0,5 В) 2, С) 3, D) 4.
10. Какой объём водорода образуется при взаимодействии 200г. 49%-ной серной кислоты с Zn:
А) 2,24л В) 4,48л С) 22,4л D) 44,8 л.
11. Масса железа, которую можно получить из руды, содержащей 800кг. Fe3O4, если выход
Fe3O4, если выход
железа составляет 80% от теоретического:
А) 193кг В) 579,3кг С) 154,5кг D) 463,4кг.
12. Химическое соединение СаН2 называют:
А) амид кальция, В) гидрид кальция,
С) гидрат кальция, D) гидроксид кальция.13. Какой из указанных металлов самый легкоплавкий:
А) Нg, В) Na, C) Ga D) Cs.
14. При растворении натрия в воде получается раствор:
А) натрия, В) оксида натрия,
С) гидроксида натрия, D) гидрида натрия.
15. С концентрированной серной кислотой не будет взаимодействовать:
А) Сu, B) Fe,
C) Mg, D) Zn.
16. Какие вещества при взаимодействии с НCl могут быть использованы для получения водорода: А) Zn, Mg B) Cu, Hg C) Ag, Au D) C, Si
17. К 400 г. 10%-ного раствора хлорида натрия прибавили 100г. воды. Массовая доля NaCl в
полученном растворе:
А) 8%, В) 5%, С) 6%, D) 4%.
18. При окислении следующих металлов Zn, Cu, Ca, Fe образуются оксиды. Какой оксид
Какой оксид
растворим в воде:
А) ZnO, B) CuO, C) CaO, D) FeO.
19. Какое количество вещества FeS2 потребуется для получения 64г. SO2 по уравнению
4FeS2 +11O2 = 2Fe2O3 +8SO2
А) 0,4 моль В) 0,5 моль, С) 3,2 моль, D) 2 моль.
20. При взаимодействии 13,7 г. металла (II) с водой выделилось 2,24л газа. Какой это металл: А) Мg, B) Ca, C) Sr, D) Ba.
Тугоплавкие металлы: вольфрам, молибден, ниобий, тантал
Свойства тугоплавких металлов
За счёт того, что они расположены в соседних группах периодической таблицы, физические свойства у тугоплавких металлов достаточно близкие:
- Плотность металла колеблется в интервале от 6100 до 10000 кг/м3. По этому показателю выделяется только вольфрам. У него он равен 19000 кг/м3.
- Температура плавления. Она превышает температуру плавления железа и колеблется от 1950 °С у ванадия до 3395 °С у вольфрама.

- Удельная теплоёмкость у них незначительно отличается друг от друга и находится в пределах от 200 до 400 Дж/(кг-град).
- Коэффициент теплопроводности сильно меняется от элемента к элементу. Если у ванадия он равен 31 Вт/(м-град), то у вольфрама он достигает величины в 188 Вт/(м-град).
Физические свойства тугоплавких металлов
Химические свойства также достаточно схожие:
- Очень похожее строение атома.
- Обладают высокой химической активностью. Это свойство определяет основные трудности при сохранении стабильности их соединений.
- Прочность межатомных связей определяет высокую температуру плавления. Это обстоятельство объясняет высокую механическую прочность, твёрдость и электрические характеристики (в частности сопротивление).
- Проявляют хорошую устойчивость при воздействии различных кислот.
К основным недостаткам тугоплавких металлов относятся:
- Низкая коррозийная стойкость. Процесс окисления происходит достаточно быстро.
 Его разделяют на две последовательные стадии. Непосредственное взаимодействие металла с кислородом окружающего воздуха, что приводит к образованию оксидной плёнки. На второй стадии происходит процесс диффузии (проникновения) атомов кислорода через образовавшуюся оксидную плёнку.
Его разделяют на две последовательные стадии. Непосредственное взаимодействие металла с кислородом окружающего воздуха, что приводит к образованию оксидной плёнки. На второй стадии происходит процесс диффузии (проникновения) атомов кислорода через образовавшуюся оксидную плёнку. - Трудности со свариваемостью тугоплавких металлов. Это вызвано высокой химической активностью к окружающему воздуху при высоких температурах, хрупкостью при насыщении различными примесями. Кроме того, трудно определить точку перегрева и практически невозможно контролировать повышение предела текучести.
- Трудности их получения использования в чистом виде без примесей.
- Необходимость применения специальных покрытий от быстрого окисления. Для сплавов, основу которых составляет вольфрам и молибден, разработаны силицидные покрытия.
- Трудности, связанные с механической обработкой. Для качественной обработки их сначала необходимо нагреть.
Таблица характеристик
Металлы и сплавы — непременная основа для ковки, литейного производства, ювелирной продукции и многих других сфер производства. Чтобы не делал мастер (ювелирные украшения из золота, ограды из чугуна, ножи из стали или браслеты из меди), для правильной работы ему необходимо знать температуры, при которых плавится тот или иной элемент.
Чтобы узнать этот параметр, нужно обратиться к таблице. В таблице также можно найти и градус кипения.
Среди наиболее часто применяемых в быту элементов показатели температуры плавления такие:
- алюминий — 660 °C;
- температура плавления меди — 1083 °C;
- температура плавления золота — 1063 °C;
- серебро — 960 °C;
- олово — 232 °C. Олово часто используют при пайке, так как температура работающего паяльника составляет как раз 250–400 градусов;
- свинец — 327 °C;
- температура плавления железо — 1539 °C;
- температура плавления стали (сплав железа и углерода) — от 1300 °C до 1500 °C.
 Она колеблется в зависимости от насыщенности стали компонентами;
Она колеблется в зависимости от насыщенности стали компонентами; - температура плавления чугуна (также сплав железа и углерода) — от 1100 °C до 1300 °C;
- ртуть — -38,9 °C.
Как понятно из этой части таблицы, самый легкоплавкий металл — ртуть, которая при плюсовых температурах уже находится в жидком состоянии.
Градус кипения всех этих элементов почти вдвое, а иногда и ещё выше градуса плавления. Например, у золота он 2660 °C, у алюминия — 2519 °C, у железа — 2900 °C, у меди — 2580 °C, у ртути — 356,73 °C.
У сплавов типа стали, чугуна и прочих металлов расчёт примерно такой же и зависит от соотношения компонентов в сплаве.
Читать также: Как проверить напряжение зарядного устройства мультиметром
Максимальная температура кипения у металлов — у рения — 5596 °C. Наибольшая температура кипения — у наиболее тугоплавящихся материалов.
Бывают таблицы, в которых также указана плотность металлов. Самым лёгким металлом является литий, самым тяжёлым — осмий. У осмия плотность выше, чем у урана и плутония, если рассматривать её при комнатной температуре. К лёгким металлам относятся: магний, алюминий, титан. К тяжёлым относится большинство распространённых металлов: железо, медь, цинк, олово и многие другие. Последняя группа — очень тяжёлые металлы, к ним относятся: вольфрам, золото, свинец и другие.
Самым лёгким металлом является литий, самым тяжёлым — осмий. У осмия плотность выше, чем у урана и плутония, если рассматривать её при комнатной температуре. К лёгким металлам относятся: магний, алюминий, титан. К тяжёлым относится большинство распространённых металлов: железо, медь, цинк, олово и многие другие. Последняя группа — очень тяжёлые металлы, к ним относятся: вольфрам, золото, свинец и другие.
Ещё один показатель, встречающийся в таблицах — это теплопроводность металлов. Хуже всего тепло проводит нептуний, а лучший по теплопроводности металл — серебро. Золото, сталь, железо, чугун и прочие элементы находится посередине между этими двумя крайностями. Чёткие характеристики для каждого можно найти в нужной таблице.
Каждый металл или сплав обладает уникальными свойствами, в число которых входит температура плавления. При этом объект переходит из одного состояния в другое, в конкретном случае становится из твёрдого жидким. Чтобы его расплавить, необходимо подвести к нему тепло и нагревать до достижения нужной температуры. В момент, когда достигается нужная точка температуры данного сплава, он ещё может остаться в твёрдом состоянии. При продолжении воздействия начинает плавиться.
В момент, когда достигается нужная точка температуры данного сплава, он ещё может остаться в твёрдом состоянии. При продолжении воздействия начинает плавиться.
Наиболее низкая температура плавления у ртути – она плавится даже при -39 °C, самая высокая у вольфрама – 3422 °C. Для сплавов (стали и других) определить точную цифру крайне сложно. Все зависит от соотношения компонентов в них. У сплавов она записывается как числовой промежуток.
Производство тугоплавких металлов
Все способы производства тугоплавких металлов основаны на методиках так называемой порошковой металлургии. Сам процесс происходит в несколько этапов:
- На начальном этапе получают порошок металла.
- Затем методами химического восстановления (обычно аммонийных солей или оксидов) выделяют требуемый металл. Такое выделение получается в результате воздействия на порошок водорода.
- На завершающем этапе получают химическое соединение, называемое гексафторидом соответствующего металла, и уже из него сам металл.

Применение тугоплавких металлов
Начиная со второй половины двадцатого века тугоплавкие металлы стали применяться во многих отраслях промышленного производства. Порошки тугоплавких металлов используются для производства первичной продукции. Тугоплавкие металлы вырабатывают в виде проволоки, слитков, арматуры, прокатного металла и фольги.
Отдельное место такие металлы занимают в технологии выращивания лейкосапфиров. Они относятся к классу монокристаллов и называются искусственными рубинами.
Изделия из тугоплавких металлов входят в состав бытовых и промышленных электрических приборов, огнеупорных конструкций, деталей для двигателей авиационной и космической техники. Особое место занимают тугоплавкие металлы при производстве деталей сложной конфигурации.
Среднеплавкие металлы
Среднеплавкие металлы начинают переходить из твердого в жидкое состояние при температуре от 600°C до 1600°C. Они используются для изготовления плит, арматур, блоков и других металлических конструкций, пригодных для строительства. К этой группе металлов относятся железо, медь, алюминий, они также входят в состав многих сплавов. Медь добавляют в сплавы драгоценных металлов, таких как золото, серебро, платина. Золото 750 пробы на 25% состоит из лигатурных металлов, в том числе и меди, которая придает ему красноватый оттенок. Температура плавления этого материала равна 1084 °C. А алюминий начинает плавиться при относительно низкой температуре, составляющей 660 градусов Цельсия. Это легкий пластичный и недорогой металл, который не окисляется и не ржавеет, поэтому широко используется при изготовлении посуды. Температура плавления железа равна 1539 градусов. Это один из самых популярных и доступных металлов, его применение распространено в строительстве и автомобильной промышленности. Но ввиду того, что железо подвергается коррозии, его нужно дополнительно обрабатывать и покрывать защитным слоем краски, олифы или не допускать попадания влаги.
К этой группе металлов относятся железо, медь, алюминий, они также входят в состав многих сплавов. Медь добавляют в сплавы драгоценных металлов, таких как золото, серебро, платина. Золото 750 пробы на 25% состоит из лигатурных металлов, в том числе и меди, которая придает ему красноватый оттенок. Температура плавления этого материала равна 1084 °C. А алюминий начинает плавиться при относительно низкой температуре, составляющей 660 градусов Цельсия. Это легкий пластичный и недорогой металл, который не окисляется и не ржавеет, поэтому широко используется при изготовлении посуды. Температура плавления железа равна 1539 градусов. Это один из самых популярных и доступных металлов, его применение распространено в строительстве и автомобильной промышленности. Но ввиду того, что железо подвергается коррозии, его нужно дополнительно обрабатывать и покрывать защитным слоем краски, олифы или не допускать попадания влаги.
Читать также: Пуск однофазного двигателя с конденсатором
Вольфрам
Этот металл открыли в далёком 1781 г.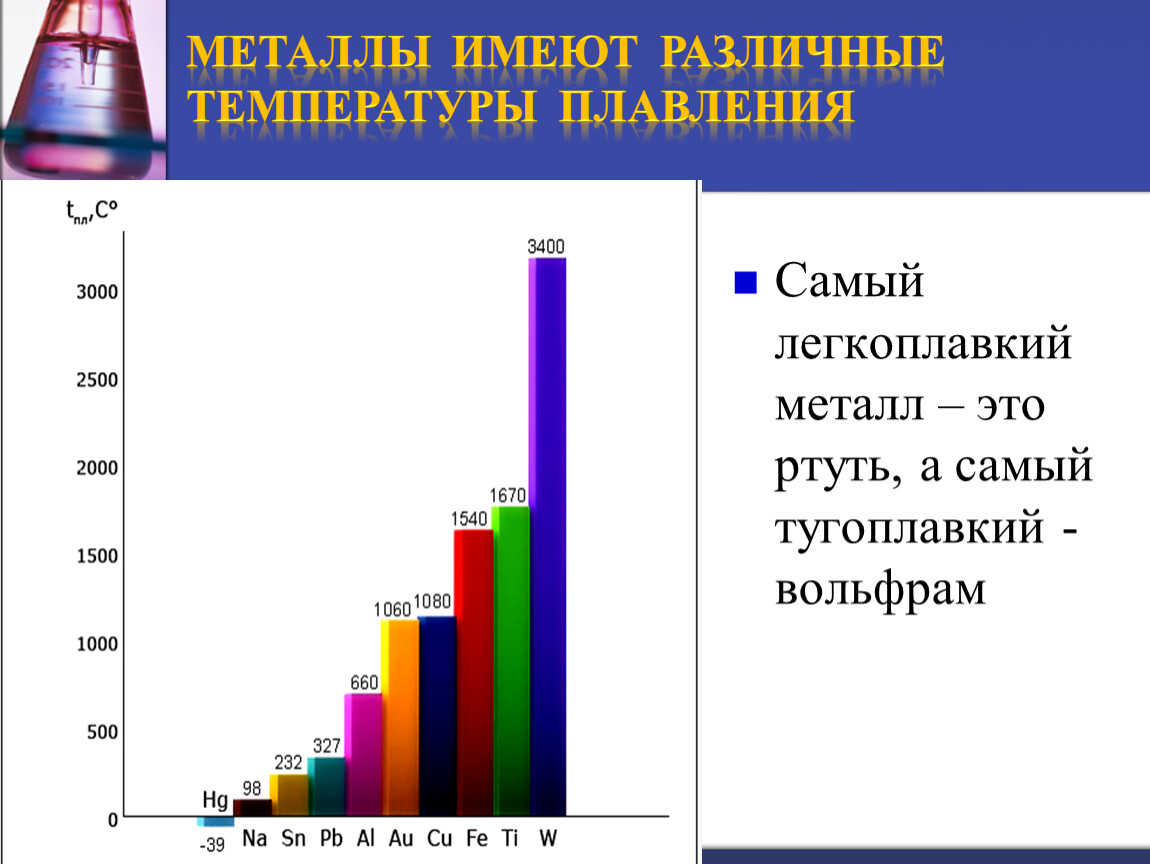 Его температура плавления равна 3380 °С. Поэтому он на сегодняшний день является самым тугоплавким металлом. Получают вольфрам из специального порошка, подвергая его химической обработке. Этот процесс основан на прессовании с последующим спеканием при высоких температурах. Далее его подвергают ковке и волочению на станках. Это связано с его наибольшей тугоплавкостью. Так получают волокнистую структуру (проволоку). Она достаточно прочная и практически не ломается. На конечном этапе его раскатывают в виде тонких нитей или гибкой ленты. Для проведения механической обработки необходимо создать защитную среду из инертного газа. В этой среде температура должна превышать 400 °С. При температуре окружающей среды он приобретает свойства парамагнетика. Ему присущи следующие недостатки:
Его температура плавления равна 3380 °С. Поэтому он на сегодняшний день является самым тугоплавким металлом. Получают вольфрам из специального порошка, подвергая его химической обработке. Этот процесс основан на прессовании с последующим спеканием при высоких температурах. Далее его подвергают ковке и волочению на станках. Это связано с его наибольшей тугоплавкостью. Так получают волокнистую структуру (проволоку). Она достаточно прочная и практически не ломается. На конечном этапе его раскатывают в виде тонких нитей или гибкой ленты. Для проведения механической обработки необходимо создать защитную среду из инертного газа. В этой среде температура должна превышать 400 °С. При температуре окружающей среды он приобретает свойства парамагнетика. Ему присущи следующие недостатки:
- сложность в создании условий для механической обработки;
- быстрое образование на поверхности оксидных плёнок. Если в контакте имеются серосодержащие вещества, образуются сульфидные плёнки;
- создание хорошего электрического контакта между несколькими деталями возможно только при создании большого давление.

Вольфрам
Для улучшения свойств вольфрама (тугоплавкости, устойчивости к коррозии, износостойкости) в него добавляют легирующие металлы. Например, рений и торий.
Металл используется для производства нитей накаливания для осветительных и сушильных ламп. Его добавляют в сварочные электроды, элементы электронных ламп и рентгеновских трубок. Также применяется при производстве элементов ракет, в реактивных двигателях, артиллерийских снарядах.
Таблица характеристик
Металлы и сплавы – непременная основа для ковки
, литейного производства, ювелирной продукции и многих других сфер производства. Чтобы не делал мастер (
Чтобы не делал мастер (
ювелирные украшения из золота
, ограды из чугуна, ножи из стали или
браслеты из меди)
, для правильной работы ему необходимо знать температуры, при которых плавится тот или иной элемент.
Чтобы узнать этот параметр, нужно обратиться к таблице. В таблице также можно найти и градус кипения.
Среди наиболее часто применяемых в быту элементов показатели температуры плавления такие:
- алюминий – 660 °C;
- температура плавления меди – 1083 °C;
- температура плавления золота – 1063 °C;
- серебро – 960 °C;
- олово – 232 °C. Олово часто используют при пайке, так как температура работающего паяльника составляет как раз 250–400 градусов;
- свинец – 327 °C;
- температура плавления железо – 1539 °C;
- температура плавления стали (сплав железа и углерода) – от 1300 °C до 1500 °C. Она колеблется в зависимости от насыщенности стали компонентами;
- температура плавления чугуна (также сплав железа и углерода) – от 1100 °C до 1300 °C;
- ртуть – -38,9 °C.

Как понятно из этой части таблицы, самый легкоплавкий металл – ртуть, которая при плюсовых температурах уже находится в жидком состоянии.
Читать также: Как подключить магнитолу в машине схема проводов
Градус кипения всех этих элементов почти вдвое, а иногда и ещё выше градуса плавления. Например, у золота он 2660 °C, у алюминия
– 2519 °C
, у железа – 2900 °C, у меди – 2580 °C, у ртути – 356,73 °C.
У сплавов типа стали, чугуна и прочих металлов расчёт примерно такой же и зависит от соотношения компонентов в сплаве.
Максимальная температура кипения у металлов – у рения
– 5596 °C
. Наибольшая температура кипения – у наиболее тугоплавящихся материалов.
Бывают таблицы, в которых также указана плотность металлов
. Самым лёгким металлом является литий, самым тяжёлым – осмий.
У осмия плотность выше, чем у урана
и плутония, если рассматривать её при комнатной температуре. К лёгким металлам относятся: магний, алюминий, титан. К тяжёлым относится большинство распространённых металлов: железо, медь, цинк, олово и многие другие. Последняя группа – очень тяжёлые металлы, к ним относятся: вольфрам, золото, свинец и другие.
К тяжёлым относится большинство распространённых металлов: железо, медь, цинк, олово и многие другие. Последняя группа – очень тяжёлые металлы, к ним относятся: вольфрам, золото, свинец и другие.
Ещё один показатель, встречающийся в таблицах – это теплопроводность металлов
. Хуже всего тепло проводит нептуний, а лучший по теплопроводности металл – серебро. Золото, сталь, железо, чугун и прочие элементы находится посередине между этими двумя крайностями. Чёткие характеристики для каждого можно найти в нужной таблице.
Температура плавления, наряду с плотностью, относится к физическим характеристикам металлов
.
Температура плавления металла
– температура, при которой металл переходит из твердого состояния, в котором находится в нормальном состоянии (кроме ртути), в жидкое состояние при нагревании. При плавлении объем металла практически не изменяется, поэтому на температуру плавления нормальное
атмосферное давление не влияет
.
Температура плавления металлов находится в диапазоне от -39 градусов Цельсия до +3410 градусов
. Для большинства металлов температура плавления высокая, однако, некоторые металлы можно расплавить в домашних условиях при нагревании на обычной горелке (олово, свинец).
Классификация металлов по температуре плавления
- Легкоплавкие металлы
, температура плавления которых колеблется
до 600
градусов Цельсия, например
цинк, олово, висмут
. - Среднеплавкие металлы
, которые плавятся при температуре
от 600 до 1600
градусов Цельсия: такие как
алюминий, медь, олово, железо
. - Тугоплавкие металлы
, температура плавления которых достигает
более 1600
градусов Цельсия –
вольфрам, титан, хром
и др. - – единственный металл, находящийся при обычных условиях (нормальное атмосферное давление, средняя температура окружающей среды) в жидком состоянии.
 Температура плавления ртути составляет порядка -39 градусов
Температура плавления ртути составляет порядка -39 градусов
по Цельсию.
Таблица температур плавления металлов и сплавов
650
1000
| Металл | |
| Алюминий | 660,4 |
| Вольфрам | 3420 |
| Дюралюмин | |
| Железо | 1539 |
| Золото | 1063 |
| Иридий | 2447 |
| Калий | 63,6 |
| Кремний | 1415 |
| Латунь | |
| Легкоплавкий сплав | 60,5 |
| Магний | 650 |
| Медь | 1084,5 |
| Натрий | 97,8 |
| Никель | 1455 |
| Олово | 231,9 |
| Платина | 1769,3 |
| Ртуть | –38,9 |
| Свинец | 327,4 |
| Серебро | 961,9 |
| Сталь | 1300-1500 |
| Цинк | 419,5 |
| Чугун | 1100-1300 |
При плавлении металла для изготовления металлических изделий-отливок от температуры плавления зависит выбор оборудования, материала для формовки металла и др. Следует также помнить, что при легировании металла другими элементами температура плавления чаще всего снижается
Следует также помнить, что при легировании металла другими элементами температура плавления чаще всего снижается
.
Не стоит путать понятия «температура плавления металла» и «температура кипения металла» – для многих металлов эти характеристики существенно отличаются: так, серебро плавится при температуре 961 градус по Цельсию, а закипает только при достижении нагрева до 2180 градусов.
Температура плавления металла – это минимальная температура, при которой он переходит из твердого состояния в жидкое. При плавлении его объем практически не изменяется. Металлы классифицируют по температуре плавления в зависимости от степени нагревания.
Ниобий
Температура плавления ниобия составляет 2741 °С. По своим химическим, физическим и механическим свойствам очень напоминает тантал. Он достаточно пластичен. Обладает хорошей свариваемостью и высокой теплопроводностью даже без дополнительного нагрева. Как и все остальные металлы его получают из порошка. Конечные заготовки из ниобия – проволока, лента, труба.
Ниобий
Сам металл и его сплавы демонстрируют эффект сверхпроводимости. Его широко применяют для изготовления анодов, экранных и антидинатронных сеток в электровакуумных приборах. Благодаря хорошей пористости, его успешно применяют в качестве газопоглотителей. В микроэлектронике он идёт на изготовление резисторов в микросхемах.
Ниобий хорошо себя проявил в качестве легирующей добавки. Используется при создании различных жаростойких конструкций, агрегатов работающих в агрессивных и радиоактивных средах. Из сплава стали и ниобия изготавливают некоторые элементы реактивных двигателей. Благодаря его свойству не взаимодействовать с радиоактивными веществами при высоких температурах, например, с ураном, применяется при изготовлении оболочек для урановых элементов, отводящих тепло в реакторах.
Тугоплавкие металлы и сплавы на их основе
К тугоплавким
относят
металлы,
температура плавления которых превышает 1800°С. Наибольшее значение в технике имеют следующие тугоплавкие металлы: Nb, Mo, Cr, W.
Тугоплавкие металлы имеют прочные межатомные связи, что и обеспечивает высокие температуры плавления. Они отличаются малым тепловым расширением, небольшой теплопроводностью, повышенной жесткостью.
Механические свойства тугоплавких металлов зависят от способа производства и содержания примесей, которые увеличивают их хрупкость. Молибден, хром и вольфрам особенно склонны к хрупкому разрушению из-за высокой температуры порога хладноломкости, которую особенно сильно повышают примеси внедрения С, N, Н и О. Наклеп понижает температуру перехода в хрупкое состояние. Жаропрочность тугоплавких металлов может быть повышена как легированием, так и азотированием при 1100… 1200°С в азоте.
Большой недостаток тугоплавких металлов — низкая жаростойкость, поэтому при температуре свыше 400…600°С их нужно защищать от окисления.
Тугоплавкие металлы трудно обрабатываются, так как имеют большое сопротивление пластическому деформированию.
Сплавы на основе тугоплавких металлов обладают более высокой жаропрочностью, чем сами чистые металлы (1500…2000°С).
Тугоплавкие металлы легируют в двух целях: а) для уменьшения их склонности к хрупкому разрушению; б) для повышения прочностных и жаропрочных характеристик.
Сплавы на основе тугоплавких металлов подразделяют на две группы:
1) сплавы со структурой твердого раствора;
2) сплавы, упрочняемые закалкой и старением.
В сплавах первой группы содержание легирующих элементов (Ti, Nb, Zr, Mo, W, Та, Re) выбирают таким, чтобы при увеличении прочности не снизить пластичность и не ухудшить другие свойства.
Сплавы второй группы содержат повышенное количество углерода и карбидообразующие элементы. При старении этой группы сплавов упрочняющей фазой являются карбиды, которые выделяются внутри зерен.
Ниобий— Nb, химический элемент Y группы периодической системы элементов, атомный номер 41, атомная масса 92,9064. Тугоплавкий светло-серый металл, плотность 8570 кг/м3, tnл
= 2500°С, температура перехода в сверхпроводящее состояние 9,25 К.
Ниобий — высокопластичный металл, имеет очень низкий (ниже -196°С) порог хладноломкости. Химически очень стоек. Хорошо сваривается. Для повышения жаропрочности ниобий легируют молибденом, вольфрамом и цирконием. Широкое использование получил как компонент химически стойких и жаростойких сталей, из которых изготовляют детали ракет, реактивных двигателей, химическую и нефтеперегонную аппаратуру. Недостатки ниобия и его сплавов — малый модуль Юнга и большая склонность к окислению при повышенных температурах.
Основными легирующими элементами для сплавов на основе ниобия являются W, Mo, Ti, Та, V, Zr, Hf и элементы внедрения (С, О, N).
Сплавы на основе ниобия (ВН-2А, ВН-4) обладают хорошей технологичностью, свариваемостью и достаточно высокой жаропрочностью до 1300°С (300…850 МПа). Ниобием и его сплавами покрывают тепловыделяющие элементы ядерных реакторов. Станид Nb3Sn, германид Nb3Ge, сплавы ниобия с Sn, Ti и Zr используют в радиоэлектронике для изготовления сверхпроводящих соленоидов (Nb3Ge — сверхпроводник с наиболее высокой температурой перехода в сверхпроводящее состояние).
Как чистый ниобий, так и его сплавы активно взаимодействует при нагреве с атмосферными газами, что требует применения защитных покрытий.
Молибден— Мо, химический элемент YI группы периодической системы элементов, атомный номер 42, атомная масса 95,94. Светло-серый металл, плотность 10200 кг/м3, tпл —
2620 °С. Химичеcки стоек (на воздухе окисляется при температуре выше 400°С). Coединения молибдена обладают значительной окислительно-восстановительной и каталитической способностью. Молибден относится к стратегическим металлам.
Более 75 % молибдена применяют для легирования сталей, используемых в авиа- и автомобилестроении, при изготовлении лопаток турбин и др. Весьма перспективны жаропрочные (для реактивных двигателей) и кислотоупорные (аппараты химической промышленности) сплавы; так, сплав Fe— Ni — Mo стоек ко всем кислотам (кроме HF) до 100°С. Молибден — важнейший конструкционный материал в производстве нитей для электрических ламп и катодов для электровакуумных приборов. Молибдены используются в гальванопластике — молибденирование,
Молибдены используются в гальванопластике — молибденирование,
а также в аналитической химии для определения фосфора, мышьяка, кремния, германия и некоторых других элементов. Природный минерал молибденит MoS2 является лучшей смазкой для трущихся металлических частей при высоких температурах, повышенном или пониженном давлении, в обычной атмосфере и при отсутствии кислорода.
Сплавы молибдена легированы Zr, Ti, Hf, Nb, W, которые образуют с молибденом твердые растворы и упрочняют его. Для увеличения пластичности в сплав могут добавлять Re. Низколегированные сплавы молибдена это — ВМ1, ЦМ2А, ВМ2 (системы Mo — Ti — Zr). Большей жаропрочностью обладают гетерофазные, термически упрочняемые сложнолегированные сплавы — ВМЗ, ЦМВЗО, ЦМВ50, ЦМ10. Длительную прочность молибденовых сплавов повышает вольфрам, вводимый в большом (30 и 50 %) количестве, — сплавы ЦМВЗО и ЦМВ50. Сплав ЦМ10 относится к свариваемым сплавам из-за уменьшения в нем содержания углерода и примесей внедрения.
Хром— Сг, химический элемент YI группы периодической системы элементов, атомный номер 24, атомная масса 51,996. Твердый металл серо-стального цвета; плотность 7190 кг/ 3, tпл =
1903°С. На воздухе не окисляется. Хром — обязательный компонент нержавеющих, кислотоупорных, жаростойких сталей и большого числа других сплавов (нихромы, хромали, стеллит). Применяется для хромирования.
Сплавы хрома, как и чистый хром, обладают очень высокой стойкостью к окислению, вплоть до 1000—1100°С. Хром в этих сплавах легируется W, V, Ni, Ti, Y (сплавы ВХ-1И, ВХ-2, ВХ-4), а также Hf, Mo, Zr, Та. Сплавы хрома, кроме высоколегированного сплава ВХ-4, малопластичные, но обеспечивают высокие значения длительной прочности.
Вольфрам — W, химический элемент VI группы периодической темы элементов, атомный номер 74, атомная масса 183,85. Светло-серый, очень тяжелый (плотность 19300 кг/м3) металл, наиболее тугоплавкий (tпл
= 3410°C) из металлов. Важные свойства вольфрама: высокая электронная эмиссия при накаливании металла и большая мощность излучаемой поверхностью металла энергии при высоких температурах. На воздухе при обычной температуре он устойчив. К недостаткам вольфрама следует отнести высокую склонность к хладноломкости и малое сопротивление окислению даже при не слишком высоких температурах.
Важные свойства вольфрама: высокая электронная эмиссия при накаливании металла и большая мощность излучаемой поверхностью металла энергии при высоких температурах. На воздухе при обычной температуре он устойчив. К недостаткам вольфрама следует отнести высокую склонность к хладноломкости и малое сопротивление окислению даже при не слишком высоких температурах.
В промышленном масштабе применяют в основном нелегированный вольфрам, а число промышленных и полупромышленных сплавов на его основе весьма ограничено.
Сплавы на основе вольфрама могут быть легированы Nb, Та, Мо, Zr, Hf, Re, Сu др. Различают однофазные сплавы вольфрама — твердые растворы и гетерофазные, упрочненные дисперсионными частицами карбидов, боридов и оксидов. К однофазным сплавам относятся сплавы систем W — Nb и W — Мо, к группе гетерофазных — системы W — Та — С (сплав ТСВ).
Главная область применения вольфрама — производство сталей (около 85 %). Он входит в состав жаропрочных сверхтвердых сталей (инструментальные, быстрорежущие) и сплавов (победит, стеллит и др. ). Чистый вольфрам используется в электротехнике (нити ламп накаливания) и радиоэлектронике (катоды и аноды электронных приборов), для спиральных нагревателей в электрических печах, электродов, различных деталей для высоковакуумных и рентгеновских приборов, при атомно-водородной сварке.
). Чистый вольфрам используется в электротехнике (нити ламп накаливания) и радиоэлектронике (катоды и аноды электронных приборов), для спиральных нагревателей в электрических печах, электродов, различных деталей для высоковакуумных и рентгеновских приборов, при атомно-водородной сварке.
Тантал
Внешне имеет светло-серый цвет с небольшим голубоватым оттенком. Температура плавления близка к 3000 °С. Хорошо поддается основным видам обработки. Его можно ковать, прокатывать, производить волочение для изготовления проволоки. Эти операции не требуют значительного нагрева. Для удобства дальнейшего использования тантал изготавливают в форме фольги и тонких листов. Повышение температуры вызывает активное взаимодействие со всеми газами, кроме инертных – с ними никаких реакций не наблюдается.
Тантал
Из тантала производят внутренние элементы генераторных ламп (магнетронов и клистронов). Он активно используется при производстве пластин в электролитических конденсаторах. Очень удобен для изготовления пленочных резисторов. Активно применяется для изготовления так называемых лодочек в испарителях, в которых осуществляется термическое напыление различных материалов на тонкие пленки.
Очень удобен для изготовления пленочных резисторов. Активно применяется для изготовления так называемых лодочек в испарителях, в которых осуществляется термическое напыление различных материалов на тонкие пленки.
Ввиду ряда своих уникальных качеств, считается незаменимым в ядерной, аэрокосмической и радиоэлектронной промышленности.
Рений
Был открыт позже всех из перечисленных ранее металлов. Он полностью оправдывает свое название «редкоземельный металл», потому что находится в небольших количествах в составе руды других металлов, таких как платина или медь. В основном его используют как легирующую добавку. Полученные сплавы приобретают хорошие характеристики прочности и ковкости. Это один из самых дорогих металлов, поэтому его применение приводит к резкому увеличению цены всего оборудования. Те не менее, его применяют в качестве катализатора.
общая характеристика, строение; свойства и получение простых веществ — урок. Химия, 8–9 класс.
Щелочными металлами называются химические элементы-металлы \(IA\) группы Периодической системы Д. И. Менделеева: литий \(Li\), натрий \(Na\), калий \(K\), рубидий \(Rb\), цезий \(Cs\) и франций \(Fr\).
И. Менделеева: литий \(Li\), натрий \(Na\), калий \(K\), рубидий \(Rb\), цезий \(Cs\) и франций \(Fr\).
Электронное строение атомов. На внешнем энергетическом уровне атомы щелочных металлов имеют один электрон ns1. Поэтому для всех металлов группы \(IA\) характерна степень окисления \(+1\).
Этим объясняется сходство свойств всех щелочных металлов.
Для них (сверху вниз по группе) характерно:
- увеличение радиуса атомов;
- уменьшение электроотрицательности;
- усиление восстановительных, металлических свойств.
Нахождение в природе. Из щелочных металлов наиболее широко распространены в природе натрий и калий. Но из-за высокой химической активности они встречаются только в виде соединений.
Основными источниками натрия и калия являются:
- каменная соль (хлорид натрия \(NaCl\)),
- глауберова соль, или мирабилит — декагидрат сульфата натрия Na2SO4 \(·\) 10h3O,
- сильвин — хлорид калия \(KCl\),
- сильвинит — двойной хлорид калия-натрия \(KCl\) \(·\)\(NaCl\) и др.

Соединения лития, рубидия и цезия в природе встречаются значительно реже, поэтому их относят к числу редких и рассеянных.
Физические свойства простых веществ. В твёрдом агрегатном состоянии атомы связаны металлической связью. Наличие металлической связи обусловливает общие физические свойства простых веществ-металлов: металлический блеск, ковкость, пластичность, высокую тепло- и электропроводность.
В свободном виде простые вещества, образованные элементами \(IA\) группы — это легкоплавкие металлы серебристо-белого (литий, натрий, калий, рубидий) или золотисто-жёлтого (цезий) цвета, обладающие высокой мягкостью и пластичностью.
Рис. \(1\). Литий
Рис. \(2\). Натрий
Наиболее твёрдым является литий, остальные щелочные металлы легко режутся ножом и могут быть раскатаны в фольгу.
Только у натрия плотность немного больше единицы ρ=1,01 г/см3, у всех остальных металлов плотность меньше единицы.
Химические свойства. Щелочные металлы обладают высокой химической активностью, реагируя с кислородом и другими неметаллами.
Поэтому хранят щелочные металлы под слоем керосина или в запаянных ампулах. Они являются сильными восстановителями.
Все щелочные металлы активно реагируют с водой, выделяя из неё водород.
Пример:
2Na+2h3O=2NaOH+h3↑.
Взаимодействие натрия с водой протекает с выделением большого количества теплоты (т. е. реакция является экзотермической). Кусочек натрия, попав в воду, начинает быстро двигаться по её поверхности. Под действием выделяющейся теплоты он расплавляется, превращаясь в каплю, которая, взаимодействуя с водой, быстро уменьшается в размерах. Если задержать её, прижав стеклянной палочкой к стенке сосуда, капля воспламенится и сгорит ярко-жёлтым пламенем.
Получение. Металлический натрий в промышленности получают главным образом электролизом расплава хлорида натрия с инертными (графитовыми) электродами.
В расплаве хлорида натрия присутствуют ионы:
NaCl⇄Na++Cl−.
При электролизе
на катоде восстанавливаются катионы Na+, а на аноде окисляются анионы Cl−:
катод (\(–\)): 2Na++2e=2Na,
анод (\(+\)): 2Cl−−2e=Cl2↑.
Суммарное уравнение реакции при электролизе расплава хлорида натрия:
2NaCl→2Na+Cl2↑.
Источники:
Рис. 1. Литий © ЯКласс
Рис. 2. Натрий © ЯКласс
Самый плавкий металл — bankingid.ru
Самый легкоплавкий металл
- Общие сведения
- Самый токсичный металл
- Использование самого легкоплавкого металла в быту
- Использование самого легкоплавкого металла в медицине
Каждый человек множество раз держал в руках самый легкоплавкий металл, причём без всяких последствий. Речь идет о ртути, грозном и загадочном элементе из подгруппы цинка, занимающем в периодической таблице атомный номер 80.
Общие сведения
Название переводится с греческого, как «серебряная вода». На латинском звучит как hydrargyrum, а в русском это толкование праславянского — «катиться». Первая цивилизация шумеров уже вовсю использовала ртуть. Металл добывали из киновари (сульфида ртути) просто обжигая руду, или же из пород, где его видно в виде небольших вкраплений.
Это редкий элемент — общая доля в земных недрах составляет всего 83 мг на одну тонну, причем чаще в рассеянной форме, чем в виде месторождений. Больше всего ее содержится в сульфидах и сланцах, а всего в мире имеется более 20 минералов со ртутью.
Самый легкоплавкий металл
Это единственный из металлов, который может находиться в жидком состоянии при обычной температуре. Такой же и бром, только он относится к галогенам. Твердеет ртуть (и плавится) при -39 °С.
Всего 7 металлов плавятся при минусовой температуре. Литр ртути очень тяжелый — 13,5 кг, а закипит она при +357°С.
Ртуть в природе
Интересно что доказательства ее принадлежности к металлам были опубликованы только в середине XVIII века Брауном и Ломоносовым.
Самый токсичный металл
Ртути принадлежит высочайшая степень токсичности. Это самый ядовитый из всех нерадиоактивных элементов на планете, который начинает распространять свои пары при комнатной температуре. Если рядом присутствует человек, происходит поражение пищеварения, легких и нервной системы, причём первые признаки интоксикации наступают очень быстро, через 8 часов.
Симптомы отравления ртутью
И даже воздействие небольших доз, но длительный период, способно проявить себя в виде хронических заболеваний. Нервная система в первую очередь реагирует раздражением, недосыпанием, головными болями и быстрой усталостью. Выводится ртуть через почки. Начинаются частые позывы к мочеиспусканию, повышение температуры, рвота, слабость, тошнота, дрожь в теле.
Самая известная экологическая трагедия XX века, болезнь Минамата, вызвана отравлением метилртутью. Промышленное загрязнение бухты этого японского города в 1956 году привело к 3 тыс. жертв.
Промышленное загрязнение бухты этого японского города в 1956 году привело к 3 тыс. жертв.
Люди всегда знали о токсических свойствах ртути. Например, при изготовлении фетровых шляп использовались ртутные соединения, но другого способа тогда не было. У мастеров часто развивались поражения нервной системы и слабоумие. Поэтому безумный Шляпник, описанный Льюисом Кэрроллом в «Алисе в стране чудес», совсем не выдуманный персонаж.
Безумный Шляпник из «Алисы в стране чудес»
В обычной жизни пищевые отравления грозят любителям морепродуктов. Ртуть содержится и растворяется в морской воде, накапливаясь в организмах его обитателей.
Симптомы хронического отравления часто встречаются в прибрежных районах по всему миру. Особенно страдают беременные и дети, у которых это основная пища. Умеренная олигофрения диагностируется там намного чаще, чем у тех групп, где морская рыба не является основным источником питания.
Хищники, поедая мелочь, сохраняют и приумножает отраву в своих организмах. У каждой четвертой выловленной рыбы содержание металла превышает допустимые пределы. Особенно много его в тунце и лобстере. Экологи бьют тревогу, а компании по производству рыбных продуктов открещиваются. И никакая тепловая обработка не делает мясо менее токсичным.
У каждой четвертой выловленной рыбы содержание металла превышает допустимые пределы. Особенно много его в тунце и лобстере. Экологи бьют тревогу, а компании по производству рыбных продуктов открещиваются. И никакая тепловая обработка не делает мясо менее токсичным.
Использование самого легкоплавкого металла в быту
Несмотря на токсичность, человечество до сих пор не может отказаться от ртути.
Хорошая электропроводимость делает ее незаменимой в энергосберегающих лампах, паровых турбинах, вакуумных и диффузных насосах. Умение реагировать на малейшие колебания температуры и давления используется в барометрах и термометрах.
Батарейки, энергосберегающие лампы, аккумуляторы, контакты выключателей — везде содержится этот высокоионизированный металл. В градуснике находится от 1 до 2 гр этого металла (в стандартных российских 1 гр). Но и эти несколько граммов полностью испарятся из помещения только в течение 20 лет. При концентрации менее 0,25 мгм3 ртуть оседает в легких. При более высоких дозах организм начинает впитывать яд через кожу. Мужчины менее чувствительны к парам, чем дети и женщины.
При более высоких дозах организм начинает впитывать яд через кожу. Мужчины менее чувствительны к парам, чем дети и женщины.
Вы можете найти ртуть в холодильнике, стиральной машине и кондиционере. Сельское хозяйство чаще всего использует соли ртути в составе пестицидов. Взрывчатка содержит фульминат ртути, антисептики — сульфат.
Фульминат ртути (взрывчатое вещество)
Не могут отказаться от ртути при окрашивании бортов корабля. Морские микроорганизмы всегда селятся там и существенно разрушают обшивку. Только краска на основе «серебряной воды» помогает сохранить судно.
Человечество с самых древних времен использовало ртуть для добычи из руды драгоценных металлов. Ртуть создает сплавы со всеми металлами (амальгамация) и только благодаря ей добыча серебра и золота в Мексике конкистадорами, начиная XVI века, достигла таких впечатляющих размеров и изменила весь мир.
Добыча золота ртутью
Никогда ртуть не транспортируют в самолетах, причем дело не в токсичности. Ртуть хорошо вступает в контакт со всеми металлами, делая их ломкими. Особенно это касается алюминиевых сплавов — случайная авария может повредить самолет.
Ртуть хорошо вступает в контакт со всеми металлами, делая их ломкими. Особенно это касается алюминиевых сплавов — случайная авария может повредить самолет.
Использование самого легкоплавкого металла в медицине
Ядовитый металл чаще всего встречался в эликсирах бессмертия и лекарствах для продления жизни. Алхимики пробовали добывать золото прямо из ртути, только сначала ее надо было нагреть. Ртуть называли праматерью металлов, она входила в теорию трех начал (с серой и солью) и была основным элементом философского камня.
Даже магические действия шаманов не могли обойтись без ртути. Распыляемым порошком киновари отпугивали нечистых духов. Несмотря на токсичность, «серебряную воду» активно использовали древние врачи практически во всех сферах своей деятельности.
Древнеегипетские жрецы клали немного ртути в сосуд и помещали в горло фараона, чтобы обезопасить его в загробной жизни.
В Индии йоги пили ртутно-серный напиток и утверждали, что таким образом можно продлить жизнь. Одним из самых вопиющих случаев в древности было лечение заворота кишок с помощью данного химического элемента.
Одним из самых вопиющих случаев в древности было лечение заворота кишок с помощью данного химического элемента.
Врачи были уверены, что жидкое серебро должно замечательно проходить сквозь человеческие кишки, распрямляя их. Но данный способ почему-то не прижился, так как у пациентов от большого объема высокоплотного «лекарства» происходил разрыв желудка.
Утверждают, что Иван Грозный стал жертвой именно ртути. Предположительно, ему или лечили сифилис, или давали лекарства, содержащие ртуть. То, что русский царь умер в результате ртутной интоксикации и имел деформации костей, свойственные глубоким старикам, уже доказано несколькими учеными.
Историки отмечали, что перед смертью царь очень изменился. Постоянная свирепость, искаженные черты лица, на теле не осталось ни единого волоса. Постоянные эпилептические припадки служили очередным доказательством отравления.
Интересно, что мгновенно покончить с жизнью с помощью ртути ни у кого не получалось. Когда самоубийцы выпивали металл — все они выживали. Самыми опасными являются пары и раствор, а сама ртуть никогда не растворится в желудке и выйдет из организма.
Самыми опасными являются пары и раствор, а сама ртуть никогда не растворится в желудке и выйдет из организма.
В 70-х годах в продаже можно было встретить множество препаратов с ртутью: мочегонные, слабительные, в мазях для отбеливания лица и антисептиках.
Амальгама серебра не так давно была распространенным пломбировочным стоматологическим материалом в России и до сих пор используется в дешевых пломбах за рубежом.
Самый легкоплавкий металл на планете необходим человечеству по-прежнему. А вот смогут ли люди дружить с ним, не отравляя жизнь вокруг — очень спорный вопрос…
Присоединяйся к нам Вконтакте и будешь в курсе всего новго в интернете!
Самый тугоплавкий металл
С древних времен человек научился обрабатывать и использовать в своей жизни металлы. Какие-то из них подходят для изготовления посуды и других товаров народного потребления, из других, например нержавеющая сталь, делают оружие и медицинские инструменты. А некоторые металлы и сплавы используются для строительства сложных технических механизмов, например космический корабль или самолет. Одной из характеристик, на которую обращают внимание при выборе того или иного материала, является его тугоплавкость.
Одной из характеристик, на которую обращают внимание при выборе того или иного материала, является его тугоплавкость.
Тугоплавкость металлов
Внимание этой характеристике уделяют все инженеры и конструкторы, работающие в машиностроении. В зависимости от величины этой характеристики, человек может рассчитать и определить в какую конструкцию можно применить те или иные тугоплавкие материалы.
Материалы, температура плавления который выше температуры плавления железа, равной 1539 °С, называются тугоплавкими. Самые тугоплавкие материалы:
Полный список содержит больше химических элементов, но не все из них получили распространенное применение в производстве и некоторые обладают меньшими температурами плавления или радиоактивны.
Вольфрам – самый тугоплавкий металл. На вид он светло-серого цвета, твердость и вес достаточно велики. Однако, он становится хрупким при низких температурах и его легко сломать (хладноломкость). Если нагреть вольфрам больше 400 °С, он станет пластичным.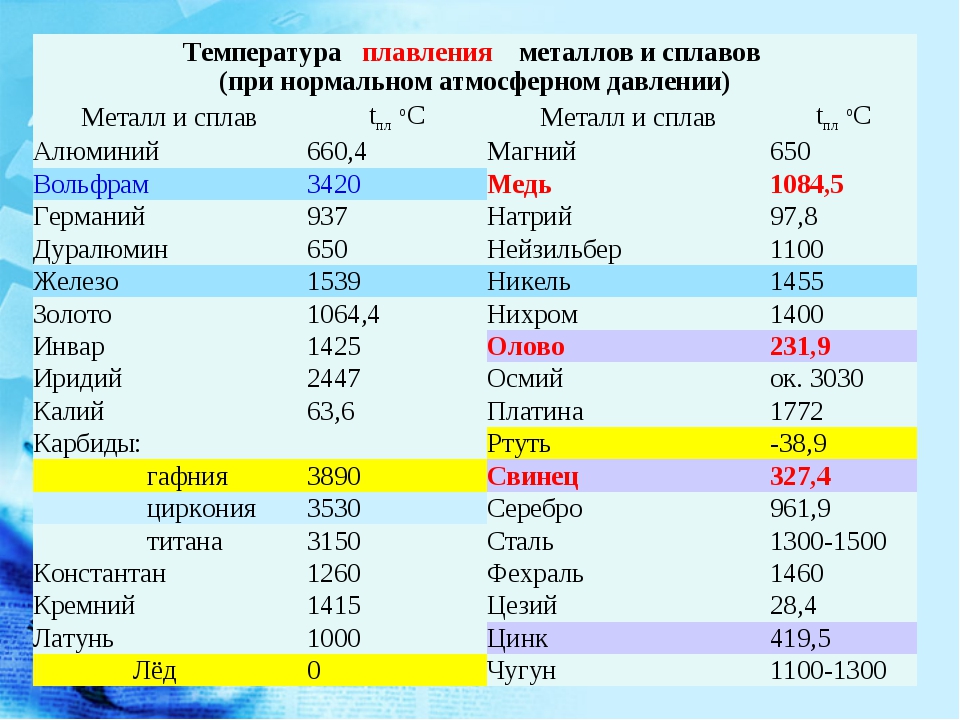 С другими веществами вольфрам плохо соединяется. Добывают его из сложных и редких минералов руд, таких как:
С другими веществами вольфрам плохо соединяется. Добывают его из сложных и редких минералов руд, таких как:
Переработка руды очень сложный и дорогостоящий процесс. Извлеченный материал формируют в бруски или готовые детали.
Вольфрам был открыт в XVIII веке, но долгое время не существовало печей, способных нагреваться до температуры плавления этого тугоплавкого металла. Ученые провели множество исследований и подтвердили, что вольфрам самый тугоплавкий металл. Стоит отметить, что по одной из теорий, сиборгий имеет большую температуру плавления, но не удается провести достаточное количество исследований, т.к. он радиоактивен и нестабилен.
Добавление вольфрама в сталь увеличивает ее твердость, поэтому его стали применять в изготовлении режущего инструмента, что увеличило скорость резания и тем самым привело к росту производства.
Высокая стоимость и трудность обработки этого тугоплавкого металла сказываются на сферах его применения. Он используется в тех случаях, когда нет возможности применить другой. Его достоинства:
Он используется в тех случаях, когда нет возможности применить другой. Его достоинства:
- устойчив к высоким температурам;
- повышенная твердость;
- прочный или упругий при определенных температурах;
Переработка металлической руды
Все эти характеристики помогают вольфраму найти широкое применение в различных сферах, таких как:
- металлургия, для легированных сталей;
- электротехника, для нитей накаливания, электродов и др.;
- машиностроение, в изготовлении узлов зубчатых передач и валов, редукторов и многом другом;
- авиационное производство, в изготовлении двигателей;
- космическая отрасль, применяется в соплах ракет и реактивных двигателях;
- военно-промышленный комплекс, для бронебойных снарядов и патронов, брони военной техники, в устройстве торпед и гранат;
- химическая промышленность, вольфрам обладает хорошей коррозийной стойкостью к действию кислот, поэтому из него делают сетки для фильтров. Кроме того соединения с вольфрамом используют в качестве красителей тканей, в производстве одежды для пожарных и многом другом.
Такой перечень отраслей, где используется этот тугоплавкий металл говорит о том, что его значение для человечества очень велико. Ежегодно по всему миру изготавливают десятки тысяч тон чистого вольфрама и с каждым годом потребность в нем растет.
Получение тугоплавких материалов
Основная трудность, встречающаяся при получении тугоплавких металлов и сплавов, это их высокая химическая активность, которая мешает быть элементу в чистом виде.
Установка для получения тугоплавких металлов
Наиболее распространенной технологией получения считается порошковая металлургия. Существует несколько способов получить порошок тугоплавкого металла.
- Восстановление с помощью триоксида водорода. Такой метод включает в себя несколько этапов, оборудование для обработки — это многотрубные печи, с диапазоном температур от 750 до 950 °С. Данный способ применяется для получения молибдена и вольфрама.
- Восстановление водородом из перрената аммония. При температуре около 500 °С, на заключительном этапе, полученный порошок, отделяют от щелочей с помощью кислот и воды. Применяется для получения рения.
- Соли различных металлов также применяются для получения порошка молибдена. Например, используют соль аммония металла и его порошок не более 15% от общей массы. Смесь нагревается до 500-850 °С при помощи инертного газа, а затем технология производства предусматривает провести восстановление водородом при температуре 850 — 1000 °С.
Производство тугоплавких металлов
Полученный этими способами порошок в дальнейшем подвергают к спеканию в специальные формы, для дальнейшей транспортировки и хранения.
На сегодняшний день, эти способы получения чистых тугоплавких металлов продолжают дорабатываться и применяются новые техники извлечения материала из горных пород. С развитием ядерной энергетики, космической отрасли, металлургии, мы в скором времени сможем наблюдать появление новых методов, возможно более дешевых и простых.
Применение тугоплавких материалов
Сферы, в которых применяются тугоплавкие металлы и сплавы:
- авиация;
- ракетостроение;
- электроника;
- космический и военный комплекс.
Объединяет все эти сферы использование новейших технологий и процессов. В основном используются в электрических приборах, лампах, электродах, катодах, предохранителях и многом другом.
Нашли они свое применение и в ядерной энергетике. Тугоплавкие металлы применяют для производства труб ядерных реакторов, оболочек и других элементов АЭС.
В химической промышленности нашли свое применение вольфрам, для окраски тканей, и тантал, антикоррозионные свойства которого применяются при изготовлении посуды и аппаратуры.
Использование тугоплавких металлов в составе прокатных сталей усиливает определенные свойства тех. Это способствует увеличению прочности, температуре плавления и многим другим свойствам.
Ежегодно выпускается миллионы тонн тугоплавких металлов по всему миру. Они используются в составе различных сплавов и сталей. Без них невозможно изготовить качественный инструмент и материал. Развитие военно-промышленного комплекса, самолетостроения, кораблестроения, создание космических кораблей, безопасность в атомной промышленности невозможна без их применения.
Самый тугоплавкий металл в мире — свойства, получение, применение
Определение «тугоплавкие металлы» не требует дополнительных пояснений в силу исчерпывающей информативности самого термина. Единственным нюансом остается пороговая температура плавления, после которой вещество можно считать тугоплавким.
Исторические сведенияПрежде чем изучать характеристики самых тугоплавких металлов в мире следует ознакомиться с их историей открытия. Металлообработка известна человеку несколько тысяч лет. Однако активное получение тугоплавких металлов началось только со второй половины 19 века.
Изначально они использовались только в электротехнике. С появлением новых технологий в строении самолётов, машин, поездов и ракет детали с высоким показателем плавления начали использоваться активнее. Пик популярности заготовок, выдерживающих температуры более 1000 градусов, пришёлся на середину 20 века.
Где применяется вольфрам?
Широко используют соединения вольфрама. Их применяют в машиностроительной и горнодобывающей промышленностях, для бурения скважин. Из данного металла благодаря его высокой прочности и твердости изготавливают детали двигателей летательных аппаратов, нити накаливания, артиллерийские снаряды, сверхскоростные роторы гироскопов, пули и т.д. Также вольфрам успешно применяется как электрод при аргонно-дуговой сварке. Не обходятся и такие отрасли промышленности без соединений вольфрама – текстильная, лакокрасочная.
Определение
Большинство определений термина тугоплавкие металлы определяют их как металлы имеющие высокие температуры плавления. По этому определению, необходимо, чтобы металлы имели температуру плавления выше 4,000 °F (2,200 °C). Это необходимо для их определения как тугоплавких металлов. Пять элементов — ниобий, молибден, тантал, вольфрам и рений входят в этот список как основные, в то время как более широкое определение этих металлов позволяет включить в этот список ещё и элементы имеющие температуру плавления 2123 K (1850 °C) — титан, ванадий, хром, цирконий, гафний, рутений и осмий. Трансурановые элементы (которые находятся за ураном, все изотопы которых нестабильны и на земле их найти очень трудно) никогда не будут относиться к тугоплавким металлам.
Сравнительная таблица степени тугоплавкости чистых металловСледует отметить, что тугоплавкие материалы не ограничиваются исключительно металлами. К этой категории относится ряд соединений – сплавы и легированные металлы, разработанных, чтобы улучшить определенные характеристики исходного материала. Относительно чистых элементов, можно привести наглядную таблицу степени их температурной устойчивости. Возглавляет ее самый тугоплавкий металл, известный на сегодня, – вольфрам с температурой плавления 3422 0С. Такая осторожная формулировка связана с попытками выделить металлы, обладающие порогом расплава, превосходящим вольфрам. Поэтому вопрос, какой металл самый тугоплавкий, может в будущем получить совсем иное определение.
Пороговые величины остальных соединений приведены ниже:
- рений 3186;
- осмий 3027;
- тантал 3014;
- молибден 2623;
- ниобий 2477;
- иридий 2446;
- рутений 2334;
- гафний 2233;
- родий 1964;
- ванадий 1910;
- хром 1907;
- цирконий 1855;
- титан 1668.
Остается добавить еще один интересный факт, касающийся физических свойств жапропрочных элементов. Температура плавления некоторых из них чувствительная к чистоте материала. Ярким примером этому выступает хром, температура плавления которого может варьироваться от 1513 до 1920 0С, в зависимости от химического состава примесей. Поэтому, данные интернет пространства часто разнятся точными цифрами, однако качественная составляющая от этого не страдает.
Хром в чистом виде
Свойства самых тугоплавких металлов
Так самый тугоплавкий металл в мире (вольфрам) обычно легируется рением, торием, никелем при участии меди и/или железа. Первый делает сплав более коррозионстойким, второй — более надежным, а третий — придает небывалую плотность. Следует обратить внимание, что во всех сплавах вольфрама содержится не более 4/5. Из-за того, что вольфрам одновременно и твердый, и тугоплавкий его обычно применяют в электроснабжении, строении приборов, изготовлении оружия, снарядов, боеголовок и ракет. Более плотные сплавы (на базе никеля) применяют для производства клюшек для игры в гольф. Вольфрам образует и так называемые псевдосплавы. Дело в том, что в них металл не легируется, а наполняется жидким серебром или медью. За счет разницы в температурах расплава получаются лучшие тепло и электропроводные свойства.
Молибден в отличие от вольфрама можно легировать лишь не некоторые сотые долей и получать при этом отличные свойства. Основными легирующими элементами молибдена являются: титан+цирконий и вольфрам. С последним сплав получается чрезвычайно инертным, с большим сопротивлением. Это дает возможность использовать его для изготовления форм для литья цинковых деталей. Особое направления использования молибдена — в качестве легирующего элемента в стальных сплавах. Сплавы сталь+молибден обладают хорошей износостойкостью и невысокими показателями трения. Сталь+молибден применяют в для изготовления труб, трубных конструкций, автомобиле и машиностроении.
Ниобий и тантал как братья, всегда находятся рядом. И тот и другой применяют в изготовлении электролитических конденсаторов .Ниобий иногда также легируют гафнием и титаном, чтобы он не вступал в реакцию с кислородов во время нагрева. Отжиг ниобия позволяет получать металл с разными коэффициентами упругости и твердости. Ниобий можно встретить в электроснабжении, ракето- и судостроении, ядерной промышленности и пр. Тантал же благодаря своей инертности к кислотам используется в медицине и производстве высокоточной электроники.
Самый редкий и самый дорогой металл из представленных — рений. Его сложно добывать, поэтому в сплавах он выступает не в качестве основного элемента, а в качестве легирующего. Нередким является его применение с медью и платиной. Рений упрочняет такие образования и улучшает их способность к ковке. Используется в ядерной, химической (катализатор) и электронной промышленностях.
Использование полезных свойств тугоплавких металлов и сплавов рассматривается учеными всего мира, как весьма перспективное направление научных изысканий.
ВидыВиды металлов и сплавов, обладающие устойчивостью к повышенным температурам:
- Вольфрам. Впервые о нем узнали в 1781 году. Чтобы расплавить, его потребовалось разогреть до 3380 градусов. Вольфрам считается самым тугоплавким. Изготавливается он из порошка, который обрабатывается химическим способом. Сначала смесь разогревается, а затем подвергается давлению. На выходе получаются спрессованные заготовки.
- Ниобий. Плавится при 2500 градусах. Обладает высокой теплопроводностью, обрабатывается не так сложно, как вольфрам. Изготавливается из порошка, который запекают и обрабатывают с помощью высокого давления. Из ниобия делают проволоку, трубы и ленту.
- Молибден. Визуально его можно спутать с вольфрамом. Изготавливается он из порошка при запекании и воздействии давлением. Как и вольфрам обладает парамагнетическими свойствами. Используется в радиоэлектронике, изготовлении промышленного оборудования, печей и электродов.
- Тантал. Плавится при 3000 градусах. Чтобы сделать проволоку из тантала или закалить материал, его не нужно нагревать до критических температур. Используется для изготовления элементов в радиоэлектронике (конденсаторы, пленочные резисторы). Популярен в ядерной промышленности.
- Рений. Материал, который ученые открыли позже остальных. Найти его можно в медной и платиновой руде. Используется на промышленном производстве, как легирующая добавка.
К материалам с высокими температурами плавления относится и хром. Благодаря своим уникальным характеристикам он применяется в различных сферах промышленности. Обладает повышенной устойчивостью к критическим температурам и коррозийным процессам. Однако стоит учитывать его хрупкость.
Технология производства
Поскольку «чистый» вольфрам встретить в природе нельзя (он является составной частью горных пород), то необходима процедура по выделению данного металла. Причем ученые оценивают содержание его в коре Земли так – на 1000 кг породы всего 1,3 грамма вольфрама. Можно отметить, что самый тугоплавкий металл, является довольно редким элементом, если сравнить его с известными видами металлов.
Когда из недр Земли добывается руда, то количество вольфрама в ней составляет только лишь до двух процентов. По этой причине добываемое сырье идет на обогатительные заводы, где специальными способами массовую долю металла приводят к шестидесяти процентам. При получении «чистого» вольфрама процесс делится на несколько технологических этапов. Первый заключается в выделении чистого триоксида из добытого сырья. Для данной цели используется термическое разложение, когда самая высокая температура плавления металла составляет от 500 до 800 градусов. При данном температурном режиме лишние элементы поддаются плавлению, а из расплавленной массы собирается оксид вольфрама.
Далее получившееся соединение проходит этап тщательного измельчения, а затем осуществляется восстановительная реакция. Для этого добавляется водород и используется температура в 700 градусов. В результате получается чистый металл, который имеет порошкообразный вид. Затем идет процесс спрессовывания порошка, для чего применяют высокое давление, и спекания в среде из водорода, где температурный режим составляет 1200-1300 градусов.
Получившуюся массу отправляют в специальную печь для плавления, где масса нагревается электрическим током до отметки более 3000 градусов. То есть вольфрам получается жидким после плавления. Затем масса очищается от примесей и создается монокристаллическая ее решетка. Для этого используют способ зонной плавки – его суть состоит в том, что расплавленной на некотором промежутке времени является лишь часть металла. Этот метод позволяет осуществлять процесс перераспределения примесей, который скапливаются на одном участке, откуда их легко убрать из общей структуры сплава. Необходимый вольфрам имеет вид слитков, которые и применяются для производства необходимых видов продукции в разных отраслях деятельности.
Применение тугоплавких материалов
Применение чистых жаропрочных металлов имеет приоритеты по ряду направлений:
- сверхзвуковая авиация;
- производство космических кораблей;
- изготовление управляемых снарядов, ракет;
- электронная и вакуумная техника.
Последний пункт затрагивает электроды электровакуумных радиоламп. Например, высокочистый ниобий используется для производства сеток, трубок электронных деталей. Также из него изготавливаются электроды – аноды электровакуумных приборов.
Аналогичное применение свойственно молибдену, вольфраму. Эти металлы в чистом виде используются не только как нити накаливания, но и под электроды радиоламп, крючки, подвески электровакуумного оборудования. Монокристаллы вольфрама, напротив, эксплуатируются как подогреватели электродов, в частности катодов, а также при изготовлении электрических контактов, предохранителей.
Чистые ванадий и ниобий используются в ядерной энергетике, где их них изготовлены трубы атомных реакторов, оболочки тепловыделяющих элементов. Область применения высокочистого тантала – химия (посуда и аппаратура), поскольку металл обладает высокой стойкостью к коррозии.
Отдельно следует рассматривать тугоплавкий припой, поскольку он не включает металлов, имеющих высокие температуры плавления. Например, тугоплавкое олово не содержит порошки тугоплавких металлов. В качестве добавок тут используются медь, серебро, никель или магний.
Тугоплавкие металлы и сплавы востребованы как прокат, так и в других сферах. В частности, применение сплавов обусловлено способностью, модифицировать определенные свойства металла: понизить температуру охрупчивания, улучшить жаропорочные характеристики.
Прокат из тугоплавких металлов достаточно широк по ассортименту и включает:
Термоэлектродная проволока вольфрам-рениевая
Наиболее крупным отечественным производителем данного типа продукции выступает опытный завод тугоплавких металлов и твердых сплавов.
Видео — тугоплавкие металлы
Тугоплавкие металлы — характеристики, свойства и применение
Еще с конца 19 века были известны тугоплавкие металлы. Тогда им не нашлось применения. Единственная отрасль, где их использовали, была электротехника и то в очень ограниченных количествах. Но все резко поменялось с развитием сверхзвуковой авиации и ракетной техники в 50-е года прошлого столетия. Производству потребовались новые материалы, способные выдерживать значительные нагрузки в условиях температур свыше 1000 ºC.
Список и характеристики тугоплавких металлов
Тугоплавкость характеризуется повышенным значением температуры перехода из твердого состояния в жидкую фазу. Металлы, плавление которых осуществляется при 1875 ºC и выше, относят к группе тугоплавких металлов. По порядку возрастания температуры плавки сюда входят следующие их виды:
Современное производство по количеству месторождений и уровню добычи удовлетворяют только вольфрам, молибден, ванадий и хром. Рутений, иридий, родий и осмий встречаются в естественных условиях довольно редко. Их годовое производство не превышает 1,6 тонны.
Жаропрочные металлы обладают следующими основными недостатками:
- Повышенная хладноломкость. Особенно она выражена у вольфрама, молибдена и хрома. Температура перехода у металла от вязкого состояния к хрупкому чуть выше 100 ºC, что создает неудобства при их обработке давлением.
- Неустойчивость к окислению. Из-за этого при температуре свыше 1000 ºC тугоплавкие металлы применяются только с предварительным нанесением на их поверхность гальванических покрытий. Хром наиболее устойчив к процессам окисления, но как тугоплавкий металл он имеет самую низкую температуру плавления.
К наиболее перспективным тугоплавким металлам относят ниобий и молибден. Это связано с их распространённостью в природе, а, следовательно, и низкой стоимостью в сравнении с другими элементами данной группы.
Помимо этого, ниобий зарекомендовал себя как металл с относительно низкой плотностью, повышенной технологичностью и довольно высокой тугоплавкостью. Молибден ценен, в первую очередь, своей удельной прочностью и жаростойкостью.
Самый тугоплавкий металл встречаемый в природе — вольфрам. Его механические характеристики не падают при температуре окружающей среды свыше 1800 ºC. Но перечисленные выше недостатки плюс повышенная плотность ограничивают его область использования в производстве. Как чистый металл он применяется все реже и реже. Зато увеличивается ценность вольфрама как легирующего компонента.
Физико-механические свойства
Металлы с высокой температурой плавления (тугоплавкие) являются переходными элементами. Согласно таблице Менделеева выделяют 2 их разновидности:
- Подгруппа 5A – тантал, ванадий и ниобий.
- Подгруппа 6A – вольфрам, хром и молибден.
Наименьшей плотностью обладает ванадий – 6100 кгм3, наибольшей вольфрам – 19300 кгм3. Удельный вес остальных металлов находится в рамках этих значений. Эти металлы отличаются малым коэффициентом линейного расширения, пониженной упругостью и теплопроводностью.
Данные металлы плохо проводят электрический ток, но обладает таким качеством как сверхпроводимость. Температура сверхпроводящего режима составляет 0,05-9 К исходя из вида металла.
Абсолютно все тугоплавкие металлы отличаются повышенной пластичностью в комнатных условиях. Вольфрам и молибден помимо этого выделяются на фоне остальных металлов более высокой жаропрочностью.
Коррозионная стойкость
Жаропрочным металлам свойственна высокая стойкость к большинству видов агрессивных сред. Сопротивление коррозии элементов 5A подгрупп увеличивается от ванадия к танталу. Как пример, при 25 ºC ванадий растворяется в царской водке, между тем как ниобий полностью инертен по отношению к данной кислоте.
Тантал, ванадий и ниобий отличаются устойчивостью к воздействию расплавленных щелочных металлов. При условии отсутствия в их составе кислорода, которые значительно усиливает интенсивность протекания химической реакции.
Молибден, хром и вольфрам имеют большую сопротивляемость к коррозии. Так азотная кислота, которая активно растворяет ванадий, значительно менее воздействует на молибден. При температуре 20 ºC данная реакция вообще полностью останавливается.
Все тугоплавкие металлы охотно вступают в химическую связь с газами. Поглощение водорода из окружающей среды ниобием осуществляется при 250 ºC. Тантал при 500 ºC. Единственный способ остановить эти процессы – проведение вакуумного отжига при 1000 ºC. Стоит заметить, что вольфрам, хром и молибден куда менее склонны к взаимодействию с газами.
Как уже было сказано ранее, лишь хром отличается сопротивляемостью к окислению. Данное свойство обусловлено его способностью образовывать твердую пленку оксида хрома на своей поверхности. Растворение кислорода хромом происходит только при 700 С. У остальных тугоплавких металлов процессы окисления начинаются ориентировочно при 550 ºC.
Хладноломкость
Распространению использования жаропрочных металлов в производстве мешает обладание ими повышенной склонности к хладноломкости. Это означает, что при падении температуры ниже определенного уровня происходит резкое возрастание хрупкости металла. Для ванадия такой температурой служит отметка в -195 ºC, для ниобия -120 ºC, а вольфрама +330 ºC.
Наличие хладноломкости жаропрочными металлами обусловлено содержанием примесями в их составе. Молибден особой чистоты (99,995%) сохраняет повышенные пластические свойства вплоть до температуры жидкого азота. Но внедрение всего 0,1% кислорода сдвигает точку хладноломкости к -20 С.
Области применения
До середины 40-х годов тугоплавкие металлы использовались только как легирующие элементы для улучшения механических характеристик стальных цветных сплавов на основе меди и никеля в электропромышленности. Соединения молибдена и вольфрама применялись также в производстве твердых сплавов.
Техническая революция, связанная с активным развитием авиации, ядерной промышленности и ракетостроения, нашла новые способы использования тугоплавких металлов. Вот неполный перечень новых сфер применения:
- Производство тепловых экранов головного узла и каркасов ракет.
- Конструкционный материал для сверхзвуковых самолётов.
- Ниобий служит материалом сотовой панели космических кораблей. А в ракетостроении его используют в качестве теплообменников.
- Узлы термореактивного и ракетного двигателя: сопла, хвостовые юбки, лопатки турбин, заслонки форсунок.
- Ванадий является основой для изготовления тонкостенных трубок тепловыделяющих элементов термоядерного реактора в ядерной промышленности.
- Вольфрам применяется как нить накаливания электроламп.
- Молибден все шире и шире используется в производстве электродов, применяемых для плавки стекла. Помимо этого, молибден — металл, используемый для производства форм литья под давлением.
- Производство инструмента для горячей обработки деталей.
Оцените статью:
Таблица температур плавления металлов
Каждый металл или сплав обладает уникальными свойствами, в число которых входит температура плавления. При этом объект переходит из одного состояния в другое, в конкретном случае становится из твёрдого жидким. Чтобы его расплавить, необходимо подвести к нему тепло и нагревать до достижения нужной температуры. В момент, когда достигается нужная точка температуры данного сплава, он ещё может остаться в твёрдом состоянии. При продолжении воздействия начинает плавиться.
Наиболее низкая температура плавления у ртути — она плавится даже при -39 °C, самая высокая у вольфрама — 3422 °C. Для сплавов (стали и других) определить точную цифру крайне сложно. Все зависит от соотношения компонентов в них. У сплавов она записывается как числовой промежуток.
Как происходит процесс
Элементы, какими бы они ни были: золото, железо, чугун, сталь или любой другой — плавятся примерно одинаково. Это происходит при внешнем или внутреннем нагревании. Внешнее нагревание осуществляется в термической печи. Для внутреннего применяют резистивный нагрев, пропуская электрический ток или индукционный нагрев в электромагнитном поле высокой частоты. Воздействие при этом примерно одинаковое.
Когда происходит нагревание, усиливается амплитуда тепловых колебаний молекул. Появляются структурные дефекты решётки, сопровождаемые разрывом межатомных связей. Период разрушения решётки и скопления дефектов и называется плавлением.
В зависимости от градуса, при котором плавятся металлы, они разделяются на:
- легкоплавкие — до 600 °C: свинец, цинк, олово;
- среднеплавкие — от 600 °C до 1600 °C: золото, медь, алюминий, чугун, железо и большая часть всех элементов и соединений;
- тугоплавкие — от 1600 °C: хром, вольфрам, молибден, титан.
В зависимости от того, каков максимальный градус, подбирается и плавильный аппарат. Он должен быть тем прочнее, чем сильнее будет нагревание.
Вторая важная величина — градус кипения. Это параметр, при достижении которого начинается кипение жидкостей. Как правило, она в два раза выше градуса плавления. Эти величины прямо пропорциональны между собой и обычно их приводят при нормальном давлении.
Если давление увеличивается, величина плавления тоже увеличивается. Если давление уменьшается, то и она уменьшается.
Таблица характеристик
Металлы и сплавы — непременная основа для ковки, литейного производства, ювелирной продукции и многих других сфер производства. Чтобы не делал мастер (ювелирные украшения из золота, ограды из чугуна, ножи из стали или браслеты из меди), для правильной работы ему необходимо знать температуры, при которых плавится тот или иной элемент.
Чтобы узнать этот параметр, нужно обратиться к таблице. В таблице также можно найти и градус кипения.
Среди наиболее часто применяемых в быту элементов показатели температуры плавления такие:
- алюминий — 660 °C;
- температура плавления меди — 1083 °C;
- температура плавления золота — 1063 °C;
- серебро — 960 °C;
- олово — 232 °C. Олово часто используют при пайке, так как температура работающего паяльника составляет как раз 250–400 градусов;
- свинец — 327 °C;
- температура плавления железо — 1539 °C;
- температура плавления стали (сплав железа и углерода) — от 1300 °C до 1500 °C. Она колеблется в зависимости от насыщенности стали компонентами;
- температура плавления чугуна (также сплав железа и углерода) — от 1100 °C до 1300 °C;
- ртуть — -38,9 °C.
Как понятно из этой части таблицы, самый легкоплавкий металл — ртуть, которая при плюсовых температурах уже находится в жидком состоянии.
Градус кипения всех этих элементов почти вдвое, а иногда и ещё выше градуса плавления. Например, у золота он 2660 °C, у алюминия — 2519 °C, у железа — 2900 °C, у меди — 2580 °C, у ртути — 356,73 °C.
У сплавов типа стали, чугуна и прочих металлов расчёт примерно такой же и зависит от соотношения компонентов в сплаве.
Максимальная температура кипения у металлов — у рения — 5596 °C. Наибольшая температура кипения — у наиболее тугоплавящихся материалов.
Бывают таблицы, в которых также указана плотность металлов. Самым лёгким металлом является литий, самым тяжёлым — осмий. У осмия плотность выше, чем у урана и плутония, если рассматривать её при комнатной температуре. К лёгким металлам относятся: магний, алюминий, титан. К тяжёлым относится большинство распространённых металлов: железо, медь, цинк, олово и многие другие. Последняя группа — очень тяжёлые металлы, к ним относятся: вольфрам, золото, свинец и другие.
Ещё один показатель, встречающийся в таблицах — это теплопроводность металлов. Хуже всего тепло проводит нептуний, а лучший по теплопроводности металл — серебро. Золото, сталь, железо, чугун и прочие элементы находится посередине между этими двумя крайностями. Чёткие характеристики для каждого можно найти в нужной таблице.
Урок 13. сплавы металлов — Химия — 11 класс
Химия, 11 класс
Урок № 13. Сплавы металлов
Перечень вопросов, рассматриваемых в теме: урок посвящён изучению сплавов чёрных и цветных металлов, роли легирующих добавок, зависимости свойств сплавов от состава.
Глоссарий
Бронза – сплав на основе меди; оловянная бронза содержит до 8,5% олова. Может содержать также алюминий, кремний, свинец. Используется для изготовления деталей машин, инструментов, при ударе не образующих искр.
Баббиты – сплавы на основе олова и свинца. Применяются для изготовления подшипников, так как отличаются высокой устойчивостью к истиранию.
Дюралюминий – высокопрочные сплавы на основе алюминия с добавками меди, магния и марганца. Основной конструкционный материал в авиа- и ракетостроении.
Константан – сплав на основе меди, никеля и марганца, используется для изготовления электроизмерительных приборов.
Латунь – сплав меди и цинка, с небольшими добавками никеля, олова, свинца, марганца. Используется для изготовления деталей машин и запорной аппаратуры.
Легированная сталь – сталь, в состав которой включены легирующие добавки, повышающие прочность, коррозионную устойчивость, жаропрочность и другие свойства сплава.
Легирующие добавки – вещества, вводимые в сплав в определённых количествах, для придания сплаву необходимых свойств.
Мельхиор – медно-никелевый сплав с добавлением железа, используется для изготовления монет, инструментов, столовых приборов.
Нейзильбер – трёхкомпонентный сплав на основе меди, цинка и никеля.
Силумин – сплав алюминия с кремнием. Применяется для литья деталей в авто- моторостроении.
Сплав — материал с металлическими свойствами, состоящий из двух или более компонентов, один из которых обязательно металл.
Сплав Вуда – легкоплавкий сплав на основе висмута, свинца, олова и кадмия. Используется для изготовления металлических моделей, заливки образцов, пайки некоторых сплавов.
Сталь – сплав железа с углеродом, причем доля углерода не превышает 2,14%.
Цветные металлы – алюминий, медь, никель, цинк, олово, свинец и другие металлы, не относящиеся к чёрным.
Цементит – карбид железа Fe3C, образуется в виде отдельной фазы в чугуне с высоким содержанием углерода.
Чёрные металлы – железо, марганец, иногда к чёрным металлам относят хром.
Чугун – сплав железа с углеродом, содержание углерода в пределах от 2,14 до 4,3%.
Электрон – сплав на основе магния и алюминия с добавлением цинка, и марганца. Используется в авиа- и ракетостроении.
Основная литература: Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
Дополнительная литература:
1. Рябов, М.А. Сборник задач, упражнений и тестов по химии. К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
2. Рудзитис, Г.Е. Химия. 10 класс: учебное пособие для общеобразовательных организаций. Углублённый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М.: Просвещение. – 2018. – 352 с.
Открытые электронные ресурсы:
- Единое окно доступа к информационным ресурсам [Электронный ресурс]. М. 2005 – 2018. URL: http://window.edu.ru/ (дата обращения: 01.06.2018).
ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ДЛЯ САМОСТОЯТЕЛЬНОГО ИЗУЧЕНИЯ
Сплавы металлов и их классификация
Одним из первых металлов, который человек стал применять для своих нужд, была медь. Но ещё в III тысячелетии люди обнаружили, что медь, сплавленная с оловом, позволяет делать более прочное оружие, долговечную посуду. Материал, полученный при сплавлении меди с оловом, получил название «бронза». Это был первый сплав, изготовленный человеком.
Сплавом называют искусственный материал с металлическими свойствами, состоящий из двух или более компонентов, из которых, по крайней мере, один является металлом.
В зависимости от количества компонентов различают двойные (бинарные), тройные и многокомпонентные сплавы. Сплавы могут иметь однородную структуру (гомогенные сплавы), а также состоять из нескольких фаз (гетерогенные сплавы). В зависимости от своих свойств сплавы подразделяются на легкоплавкие, тугоплавкие, жаропрочные, высокопрочные, твердые, коррозионно-устойчивые. По предполагаемой технологии обработки различают литейные (изделия производят путём литья) и деформируемые (обрабатывают путём ковки, проката, штамповки, прессования) сплавы.
Чёрные металлы и сплавы на их основе
В зависимости от природы металла, составляющего основу сплава, различают чёрные и цветные сплавы. В чёрных сплавах основным металлом является железо. Самыми распространенными из чёрных сплавов являются сталь и чугун. К чёрным металлам относятся железо, а также марганец и хром, которые входят в состав чёрных сплавов.
Чугун
Чугун – сплав на основе железа, содержание углерода в котором превышает точку предельной растворимости углерода в расплаве железа (2,14%). При остывании сплава, углерод кристаллизуется в виде отдельных включений цементита и графита. Углерод придает чугуну твердость, но снижает пластичность сплава, поэтому чугун хрупкий. Чугун применяют для изготовления литых деталей (коленчатых валов, колёс, труб, радиаторов отопления, ванн, решеток ограждения), кухонной посуды (сковородок, чугунков, казанов).
Сталь
В стали содержание углерода значительно меньше. В низкоуглеродистых сталях количество углерода не превышает 0,25%, в высокоуглеродистой стали содержание углерода может достигать 2%. Самые первые стальные изделия появились 4000 лет назад. В настоящее время выплавляют стальные сплавы с различными свойствами. Это конструкционные, нержавеющие, инструментальные, жаропрочные стали.
Легирующие добавки
Для придания стали особых свойств в процессе её изготовления, вводят легирующие добавки. Легирующими добавками называют вещества, которые добавляют в сплав в определенном количестве для изменения механических и физических свойств материала.
Легированные стали
В зависимости от количества легирующих добавок различают низколегированную, среднелегированную и высоколегированную сталь. Марка стали обозначается с помощью букв и цифр. Буква указывает на химическую природу легирующей добавки, а цифра, стоящая после буквы – на примерное содержание этой добавки в сплаве. Если содержание добавки меньше 1%, то цифру не ставят. Цифры впереди букв показывают содержание углерода в сотых долях процента. Например, в стали марки 18ХГТ содержится 0,18 % С, 1 % Сr, 1 % Мn, около 0,1 % Тi.
Стали применяют для изготовления армирующих железнодорожных рельсов, дробильных установок, конструкций, турбин электростанций и двигателей самолётов, инструментов (пилы, сверла, резцы, зубила, фрезы), химической аппаратуры, деталей автомобилей, тракторов, дорожных машин, труб и много другого.
Цветные металлы и сплавы на их основе
К цветным металлам относят алюминий, цинк, медь, никель, олово, свинец и др. Сплавы на основе цветных металлов называют цветными. Это бронза, латунь, силумин, дюралюминий, баббиты и многие другие. В авиации широкое применение нашли легкие и прочные сплавы на основе алюминия и титана. Изделия из медных сплавов: бронзы и латуни, применяются в химической промышленности, для изготовления запорной аппаратуры: кранов, вентилей. Сплавы на основе олова и свинца используют для изготовления подшипников. Из мельхиора и нейзильбера – сплавов меди и никеля, изготовляют столовые наборы, монеты.
ПРИМЕРЫ И РАЗБОР РЕШЕНИЙ ЗАДАЧ ТРЕНИРОВОЧНОГО МОДУЛЯ
1. Расчет массовой доли металла в сплаве
Условие задачи: Кусочек нейзильбера массой 2,00 г поместили в раствор гидроксида натрия. В ходе реакции выделилось 0,14 л водорода (н.у.). Вычислите массовую долю цинка в сплаве. Ответ запишите в процентах с точностью до десятых долей.
Шаг первый: запишем уравнение реакции цинка с раствором гидроксида натрия:
Zn + 2NaOH → Na2ZnO2 + H2↑.
Один моль цинка вытесняет из щёлочи один моль водорода.
Шаг второй: найдём количество цинка, которое вытеснило 0,14 л водорода.
Для этого найдём в периодической таблице элементов Д.И. Менделеева молярную массу цинка: М(Zn) = 65 г/моль. При нормальных условиях 1 моль любого газа занимает объём, равный 22,4 л. Составим пропорцию:
65 г цинка вытесняет 22,4 л водорода;
х г цинка вытесняет 0,14 л водорода.
65 : х = 22,4 : 0,14, откуда х = (65·0,14) : 22,4 = 0,41 (г) – масса цинка в сплаве.
Шаг третий: найдём массовую долю цинка в сплаве:
ω = (0,41 : 2,00)*100 = 20,5 (%).
Ответ: 20,5
2. Расчёт массы легирующей добавки
Условие задачи: Для придания стали противокоррозионных свойств в сплав добавляют хром. Сталь марки С1 должна содержать 12% хрома, 1% кремния, 1,5% марганца и 0,2% углерода. Сколько хрома необходимо добавить к железному лому (посторонними примесями пренебрегаем) массой 500 кг, чтобы получить нержавеющую сталь требуемой марки? Ответ записать в килограммах с точностью до десятых долей.
Шаг первый: найдём массовую долю железа в стали марки С1:
Для этого от 100% отнимем массовые доли остальных элементов:
100 – 12 – 1 – 1,5 – 0,2 = 85,3 (%).
Шаг второй: найдём массу одного процента сплава.
Для этого массу железного лома разделим на массовую долю железа:
500 : 85,3 = 5,9 (кг).
Шаг третий: найдём необходимую массу хрома. Для этого массу одного процента сплава умножим на массовую долю хрома в сплаве:
5,9*12 = 70,8 (кг).
Ответ: 70,8
Тугоплавкие металлы: вольфрам, молибден, ниобий, тантал
Свойства тугоплавких металлов
За счёт того, что они расположены в соседних группах периодической таблицы, физические свойства у тугоплавких металлов достаточно близкие:
- Плотность металла колеблется в интервале от 6100 до 10000 кг/м3. По этому показателю выделяется только вольфрам. У него он равен 19000 кг/м3.
- Температура плавления. Она превышает температуру плавления железа и колеблется от 1950 °С у ванадия до 3395 °С у вольфрама.
- Удельная теплоёмкость у них незначительно отличается друг от друга и находится в пределах от 200 до 400 Дж/(кг-град).
- Коэффициент теплопроводности сильно меняется от элемента к элементу. Если у ванадия он равен 31 Вт/(м-град), то у вольфрама он достигает величины в 188 Вт/(м-град).
Физические свойства тугоплавких металлов
Химические свойства также достаточно схожие:
- Очень похожее строение атома.
- Обладают высокой химической активностью. Это свойство определяет основные трудности при сохранении стабильности их соединений.
- Прочность межатомных связей определяет высокую температуру плавления. Это обстоятельство объясняет высокую механическую прочность, твёрдость и электрические характеристики (в частности сопротивление).
- Проявляют хорошую устойчивость при воздействии различных кислот.
К основным недостаткам тугоплавких металлов относятся:
- Низкая коррозийная стойкость. Процесс окисления происходит достаточно быстро. Его разделяют на две последовательные стадии. Непосредственное взаимодействие металла с кислородом окружающего воздуха, что приводит к образованию оксидной плёнки. На второй стадии происходит процесс диффузии (проникновения) атомов кислорода через образовавшуюся оксидную плёнку.
- Трудности со свариваемостью тугоплавких металлов. Это вызвано высокой химической активностью к окружающему воздуху при высоких температурах, хрупкостью при насыщении различными примесями. Кроме того, трудно определить точку перегрева и практически невозможно контролировать повышение предела текучести.
- Трудности их получения использования в чистом виде без примесей.
- Необходимость применения специальных покрытий от быстрого окисления. Для сплавов, основу которых составляет вольфрам и молибден, разработаны силицидные покрытия.
- Трудности, связанные с механической обработкой. Для качественной обработки их сначала необходимо нагреть.
Таблица характеристик
Металлы и сплавы — непременная основа для ковки, литейного производства, ювелирной продукции и многих других сфер производства. Чтобы не делал мастер (ювелирные украшения из золота, ограды из чугуна, ножи из стали или браслеты из меди), для правильной работы ему необходимо знать температуры, при которых плавится тот или иной элемент.
Чтобы узнать этот параметр, нужно обратиться к таблице. В таблице также можно найти и градус кипения.
Среди наиболее часто применяемых в быту элементов показатели температуры плавления такие:
- алюминий — 660 °C;
- температура плавления меди — 1083 °C;
- температура плавления золота — 1063 °C;
- серебро — 960 °C;
- олово — 232 °C. Олово часто используют при пайке, так как температура работающего паяльника составляет как раз 250–400 градусов;
- свинец — 327 °C;
- температура плавления железо — 1539 °C;
- температура плавления стали (сплав железа и углерода) — от 1300 °C до 1500 °C. Она колеблется в зависимости от насыщенности стали компонентами;
- температура плавления чугуна (также сплав железа и углерода) — от 1100 °C до 1300 °C;
- ртуть — -38,9 °C.
Как понятно из этой части таблицы, самый легкоплавкий металл — ртуть, которая при плюсовых температурах уже находится в жидком состоянии.
Градус кипения всех этих элементов почти вдвое, а иногда и ещё выше градуса плавления. Например, у золота он 2660 °C, у алюминия — 2519 °C, у железа — 2900 °C, у меди — 2580 °C, у ртути — 356,73 °C.
У сплавов типа стали, чугуна и прочих металлов расчёт примерно такой же и зависит от соотношения компонентов в сплаве.
Читать также: Ремонт цепей для бензопил своими руками
Максимальная температура кипения у металлов — у рения — 5596 °C. Наибольшая температура кипения — у наиболее тугоплавящихся материалов.
Бывают таблицы, в которых также указана плотность металлов. Самым лёгким металлом является литий, самым тяжёлым — осмий. У осмия плотность выше, чем у урана и плутония, если рассматривать её при комнатной температуре. К лёгким металлам относятся: магний, алюминий, титан. К тяжёлым относится большинство распространённых металлов: железо, медь, цинк, олово и многие другие. Последняя группа — очень тяжёлые металлы, к ним относятся: вольфрам, золото, свинец и другие.
Ещё один показатель, встречающийся в таблицах — это теплопроводность металлов. Хуже всего тепло проводит нептуний, а лучший по теплопроводности металл — серебро. Золото, сталь, железо, чугун и прочие элементы находится посередине между этими двумя крайностями. Чёткие характеристики для каждого можно найти в нужной таблице.
Каждый металл или сплав обладает уникальными свойствами, в число которых входит температура плавления. При этом объект переходит из одного состояния в другое, в конкретном случае становится из твёрдого жидким. Чтобы его расплавить, необходимо подвести к нему тепло и нагревать до достижения нужной температуры. В момент, когда достигается нужная точка температуры данного сплава, он ещё может остаться в твёрдом состоянии. При продолжении воздействия начинает плавиться.
Наиболее низкая температура плавления у ртути – она плавится даже при -39 °C, самая высокая у вольфрама – 3422 °C. Для сплавов (стали и других) определить точную цифру крайне сложно. Все зависит от соотношения компонентов в них. У сплавов она записывается как числовой промежуток.
Производство тугоплавких металлов
Все способы производства тугоплавких металлов основаны на методиках так называемой порошковой металлургии. Сам процесс происходит в несколько этапов:
- На начальном этапе получают порошок металла.
- Затем методами химического восстановления (обычно аммонийных солей или оксидов) выделяют требуемый металл. Такое выделение получается в результате воздействия на порошок водорода.
- На завершающем этапе получают химическое соединение, называемое гексафторидом соответствующего металла, и уже из него сам металл.
Технологии производства
Высокие температуры плавления предопределяют порошковую металлургию основным способом получения конечной продукции.
Обычно вопрос о том, какие металлы – тугоплавкие, решается тем, к какой из трёх категорий они относятся:
- Твёрдые сплавы;
- Оксидные или карбидные дисперсно-упрочненные материалы;
- Материалы с легированными свойствами.
Так, все продукты на основе вольфрама и большая часть молибденовых продуктов перерабатываются с помощью порошковой металлургии, поскольку из-за высокой температуры плавления, они не могут быть произведены методом распыления. Таким образом, процессы химического восстановления и электролиз — единственные практические методы.
Порошки, полученные электролитическим способом из водных электролитов или в расплавленном состоянии, имеют высокую чистоту и активны во время спекания. Однако у них есть следующие недостатки:
- Для удаления из электролита остаточных примесей необходима очистка;
- Процесс часто является дорогостоящим, потребляя много электроэнергии из-за низкого КПД по току;
- Процесс ограничен производством чистых металлических порошков, так как этим методом невозможно производить порошки сплавов.
Восстановителями, используемыми в большинстве процессов, являются углерод и водород — в их элементарной форме, либо в виде газообразных соединений или смесей (углеводородов, крекинг-аммиака или монооксида углерода).
Ещё недавно для производства молибдена и его сплавы применялось вакуумное литьё, однако в современных производствах и здесь используется порошковая металлургия. Эффективность восстановления металлического порошка зависит от:
- Требуемой энергии активации;
- Химического состава и степени дисперсности металлопорошка;
- Скорости потока восстанавливающего газа – водорода.
Порошковая металлургия — единственный путь производства сплавов, компонентами которых являются тугоплавкие металлы, в том числе, и на уровне нанопорошков. Среди различных методов, исследуемых для производства тугоплавких наносплавов — традиционный путь реакции газ-твердое тело, реализация которого позволяет производить наноструктурированные порошки в значительных количествах и с широкими возможностями обеспечения качества.
Важно подчеркнуть, что высокотемпературные технологии порошковой металлургии позволяют изготавливать материалы по индивидуальному заказу. Правильно подобрав исходный материал, можно соответствующим образом контролировать состав конечного продукта.
Третий способ – использование 3D-печати. Это активно развивающаяся технология, которая идеально подходит для производства легких, высокостабильных компонентов из вольфрама, молибдена, ниобия, тантала и их сплавов со сложной геометрической структурой.
Нанопорошки тугоплавких металлов получают следующими способами:
- Селективным лазерным спеканием.
- Селективным лазерным плавлением.
- Электронно-лучевым плавлением.
- Прямым осаждением.
- Быстрым прототипированием.
Ключевыми преимуществами металлических порошков, распыленных газом, являются идеально сферическая форма, отличная воспроизводимость, низкое содержание оксидов.
Применение тугоплавких металлов
Начиная со второй половины двадцатого века тугоплавкие металлы стали применяться во многих отраслях промышленного производства. Порошки тугоплавких металлов используются для производства первичной продукции. Тугоплавкие металлы вырабатывают в виде проволоки, слитков, арматуры, прокатного металла и фольги.
Отдельное место такие металлы занимают в технологии выращивания лейкосапфиров. Они относятся к классу монокристаллов и называются искусственными рубинами.
Изделия из тугоплавких металлов входят в состав бытовых и промышленных электрических приборов, огнеупорных конструкций, деталей для двигателей авиационной и космической техники. Особое место занимают тугоплавкие металлы при производстве деталей сложной конфигурации.
Вольфрам
Этот металл открыли в далёком 1781 г. Его температура плавления равна 3380 °С. Поэтому он на сегодняшний день является самым тугоплавким металлом. Получают вольфрам из специального порошка, подвергая его химической обработке. Этот процесс основан на прессовании с последующим спеканием при высоких температурах. Далее его подвергают ковке и волочению на станках. Это связано с его наибольшей тугоплавкостью. Так получают волокнистую структуру (проволоку). Она достаточно прочная и практически не ломается. На конечном этапе его раскатывают в виде тонких нитей или гибкой ленты. Для проведения механической обработки необходимо создать защитную среду из инертного газа. В этой среде температура должна превышать 400 °С. При температуре окружающей среды он приобретает свойства парамагнетика. Ему присущи следующие недостатки:
- сложность в создании условий для механической обработки;
- быстрое образование на поверхности оксидных плёнок. Если в контакте имеются серосодержащие вещества, образуются сульфидные плёнки;
- создание хорошего электрического контакта между несколькими деталями возможно только при создании большого давление.
Вольфрам
Для улучшения свойств вольфрама (тугоплавкости, устойчивости к коррозии, износостойкости) в него добавляют легирующие металлы. Например, рений и торий.
Металл используется для производства нитей накаливания для осветительных и сушильных ламп. Его добавляют в сварочные электроды, элементы электронных ламп и рентгеновских трубок. Также применяется при производстве элементов ракет, в реактивных двигателях, артиллерийских снарядах.
Как происходит
Плавление всех металлов происходит примерно одинаково — при помощи внешнего или внутреннего нагревания. Первый осуществляется в термической печи, для второго используют резистивный нагрев при пропускании электрического тока или индукционный нагрев в высокочастотном электромагнитном поле. Оба варианта воздействуют на металл примерно одинаково.
При увеличении температуры увеличивается и амплитуда тепловых колебаний молекул, возникают структурные дефекты решетки, выражающиеся в росте дислокаций, перескоке атомов и других нарушениях. Это сопровождается разрывом межатомных связей и требует определенного количества энергии. В это же время происходит образование квази-жидкого слоя на поверхности тела. Период разрушения решетки и накопления дефектов называется плавлением.
Ниобий
Температура плавления ниобия составляет 2741 °С. По своим химическим, физическим и механическим свойствам очень напоминает тантал. Он достаточно пластичен. Обладает хорошей свариваемостью и высокой теплопроводностью даже без дополнительного нагрева. Как и все остальные металлы его получают из порошка. Конечные заготовки из ниобия – проволока, лента, труба.
Ниобий
Сам металл и его сплавы демонстрируют эффект сверхпроводимости. Его широко применяют для изготовления анодов, экранных и антидинатронных сеток в электровакуумных приборах. Благодаря хорошей пористости, его успешно применяют в качестве газопоглотителей. В микроэлектронике он идёт на изготовление резисторов в микросхемах.
Ниобий хорошо себя проявил в качестве легирующей добавки. Используется при создании различных жаростойких конструкций, агрегатов работающих в агрессивных и радиоактивных средах. Из сплава стали и ниобия изготавливают некоторые элементы реактивных двигателей. Благодаря его свойству не взаимодействовать с радиоактивными веществами при высоких температурах, например, с ураном, применяется при изготовлении оболочек для урановых элементов, отводящих тепло в реакторах.
Сплавы металлов
Чтобы проектировать изделия из сплавов, сначала изучают их свойства. Для изучения в небольших емкостях расплавляют изучаемые металлы в разном соотношении между собой. По итогам строят графики.
Нижняя ось представляет концентрацию компонента А с компонентом В. По вертикали рассматривают температуру. Здесь отмечают значения максимальной температуры, когда весь металл находится в расплавленном состоянии.
При охлаждении один из компонентов начинает образовывать кристаллы. В жидком состоянии находится эвтектика – идеальное соединение металлов в сплаве.
Металловеды выделяют особое соотношение компонентов, при котором температура плавления минимальная. Когда составляют сплавы, то стараются подбирать количество используемых веществ, чтобы получать именно эвтектоидный сплав. Его механические свойства наилучшие из возможных. Кристаллические решетки образуют идеальные гранецентрированные положения атомов.
Изучают процесс кристаллизации путем исследования твердения образцов при охлаждении. Строят специальные графики, где наблюдают, как изменяется скорость охлаждения. Для разных сплавов имеются готовые диаграммы. Отмечая точки начала и конца кристаллизации, определяют состав сплава.
Тантал
Внешне имеет светло-серый цвет с небольшим голубоватым оттенком. Температура плавления близка к 3000 °С. Хорошо поддается основным видам обработки. Его можно ковать, прокатывать, производить волочение для изготовления проволоки. Эти операции не требуют значительного нагрева. Для удобства дальнейшего использования тантал изготавливают в форме фольги и тонких листов. Повышение температуры вызывает активное взаимодействие со всеми газами, кроме инертных – с ними никаких реакций не наблюдается.
Тантал
Из тантала производят внутренние элементы генераторных ламп (магнетронов и клистронов). Он активно используется при производстве пластин в электролитических конденсаторах. Очень удобен для изготовления пленочных резисторов. Активно применяется для изготовления так называемых лодочек в испарителях, в которых осуществляется термическое напыление различных материалов на тонкие пленки.
Ввиду ряда своих уникальных качеств, считается незаменимым в ядерной, аэрокосмической и радиоэлектронной промышленности.
Классификация
В зависимости от температуры плавления тугоплавкие металлы причисляются к основной либо дополнительной группе.
Основная группа
Данный сегмент включает пять позиций: вольфрам, ниобий, тантал, молибден, рений. Плавятся при 2200°С+.
Свойства четвёртой группы элементов
| Название | Ниобий | Молибден | Тантал | Вольфрам | Рений |
| Температура плавления | 2750 K (2477 °C) | 2896 K (2623 °C) | 3290 K (3017 °C) | 3695 K (3422 °C) | 3459 K (3186 °C) |
| Температура кипения | 5017 K (4744 °C) | 4912 K (4639 °C) | 5731 K (5458 °C) | 5828 K (5555 °C) | 5869 K (5596 °C) |
| Плотность | 8,57 г·см³ | 10,28 г·см³ | 16,69 г·см³ | 19,25 г·см³ | 21,02 г·см³ |
| Модуль Юнга | 105 ГПа | 329 ГПа | 186 ГПа | 411 ГПа | 463 ГПа |
| Твёрдость по Виккерсу | 1320 МПа | 1530 МПа | 873 МПа | 3430 МПа | 2450 МПа |
Молибден
Самый востребованный из тугоплавких элементов.
Сфера использования номер один – металлургия:
- Молибденом «усиливают» сталь, чтобы получить твердый сплав.
- На пару с нержавеющей сталью применяют как материал инфраструктуры трубопроводов, деталей автомобилей, другой продукции машиностроения.
- Благодаря температуре плавления, износостойкости, малой истираемости используется как легирующая присадка.
Молибдену требуется пара процентов лигатур в составе, чтобы свойства сплава изменились.
Например, полпроцента титана плюс 0,08% циркония создают молибденовый сплав, не снижающий прочность до 1060°C.
Неординарные параметры по трению обусловили использование молибдена как долговечной смазки с высоким КПД.
Материал незаменим для ртутных реле, поскольку амальгама с данным металлом ртутью не формируется.
Вольфрам
Открыт в конце 18 века. Самый твердый и самый тугоплавкий (3422°C) металл.
Тугоплавкий прочный металл, светло-серого цвета – вольфрам
Вместе с медью и железом используется как основа (до 80%) сплавов с рением, торием, никелем. Такие добавки повышают плотность, порог стойкости к ржавлению, надежность.
Востребован как материал систем электроснабжения, приборов, боеприпасов, ядерных боеголовок ракет. Никелевые сплавы как материал клюшек ценят поклонники гольфа.
Вольфрам в слитках
Вольфрам, его сплавы востребованы там, где нужна повышенная плотность в условиях запредельных температур.
Тантал
Самый стойкий к кислотам, коррозии из сегмента тугоплавких металлов.
Тяжёлый твёрдый металл серого цвета – тантал
Поэтому используется в конденсаторах смартфонов, планшетов, других гаджетов.
Совместим с биологическими организмами (не меняется под воздействием природных кислот). Благодаря этому применяется медициной.
В природе ниобий и тантал соседи. Не случайно названы по именам отца и дочери – Тантала и Ниобы, персонажей древнегреческих мифов.
Ниобий
Металл с небанальными характеристиками:
- Самый легкий (малой плотности) в сегменте.
- Уникален благодаря свойству менять коэффициент твердости и упругости в зависимости от степени отжига.
- Самый частый в сплавах-суперпроводниках.
Применяется как материал конденсаторов, газовых турбин ракет, самолетов. А также элемент ядерных реакторов и ламп электронных приборов.
Вместе с гафнием и титаном – материал двигателей космических аппаратов (например, американского Аполлона).
Рений
Был открыт позже всех из перечисленных ранее металлов. Он полностью оправдывает свое название «редкоземельный металл», потому что находится в небольших количествах в составе руды других металлов, таких как платина или медь. В основном его используют как легирующую добавку. Полученные сплавы приобретают хорошие характеристики прочности и ковкости. Это один из самых дорогих металлов, поэтому его применение приводит к резкому увеличению цены всего оборудования. Те не менее, его применяют в качестве катализатора.
Виды и области применения
Благодаря своим уникальным качествам тугоплавкие металлы очень полезны для различных областей применения и отраслей. Их основные преимущества:
- Сверхвысокая точка плавления. В частности, к тугоплавким металлам относятся вольфрам, молибден и тантал, которые применяются при производстве стекла;
- Прочность при сверхвысоких температурах. Например, конусы ракет, сделанные из вольфрама, имеют вдвое большую прочность на разрыв, чем железо при нормальных температурах;
- Превосходная стойкость к истиранию и износу, что позволяет продлить срок службы седел клапанов, уплотнений, форсунок и других участков, подверженных сильному износу;
- Отличная коррозионная стойкость, поэтому особо ответственные трубопроводы на химических предприятиях обычно изготавливаются из тугоплавких металлов;
- Устойчивость к тепловому удару. В частности, вольфрамовые изделия могут противостоять нагрузкам, вызванным быстрым расширением из-за резких перепадов температуры;
- Тепловая и электрическая проводимость, вследствие чего из вольфрама и молибдена изготавливают детали радиаторов;
- Чрезвычайная твердость, поэтому высокостойкий режущий штамповый и бурильный инструмент производят из карбида вольфрама;
- Высокая плотность тугоплавких металлов – причина их применения при изготовлении головок клюшек для гольфа и авиационных гироскопов.
Кроме того, эти материалы используются в качестве катализаторов химических реакций, при процессах ядерного синтеза и т.д.
К тугоплавким металлам относятся получившие особое распространение вольфрам, молибден, ниобий, тантал, рений и хром. Об особенностях их применения – далее.
Вольфрам
Вольфрам — самый распространенный среди тугоплавких металлов. Он имеет самую высокую температуру плавления и одну из самых высоких плотностей. Обладает также высокой устойчивостью к коррозии. Широко используется в проволочных волокнах, например, в большинстве ламп накаливания, используемых в домах, а также в промышленных дуговых лампах и прочей технике для освещения.
Молибден
Молибден — наиболее используемый тугоплавкий металл из всех, потому что он дешевле, чем большинство других, и, когда он превращен в сплав, может быть очень устойчивым к ползучести и высоким температурам. Он также не образует амальгам, что делает его устойчивым к коррозии.
Молибден используется для упрочнения стальных сплавов, особенно в конструкционных трубопроводах и насосно-компрессорных трубах. Этот металл также обладает отличными антифрикционными качествами, что делает его идеальным компонентом масел и смазок, используемых в автомобилях.
Ниобий
Обладает оптимальным сочетанием пластичности и прочности. Его можно использовать при изготовлении электролитических конденсаторов, сверхпроводников, ядерных реакторов и электронных ламп.
Тантал
Более других устойчив к коррозии, поэтому находит применение в медицине (особенно – хирургии), а также в средах с повышенной кислотностью. Тантал также является основным компонентом компьютерных, телефонных и конденсаторных цепей.
Рений
Известен своей высокой прочностью на разрыв и пластичностью. Он широко используется в ядерных реакторах, гироскопах и других электрических компонентах. Из-за своей редкости рений очень дорог. Понятие коррозионной стойкости особенно актуально именно для рения, потому что он очень летуч. Может терять устойчивость к воздействию кислорода при высоких температурах, поскольку оксидный слой активно испаряется.
Какой металл является самым тугоплавким
Тугоплавкие металлы — описание, изделия из тугоплавких Ме
Определение «тугоплавкие металлы» не требует дополнительных пояснений в силу исчерпывающей информативности самого термина. Единственным нюансом остается пороговая температура плавления, после которой вещество можно считать тугоплавким.
Разногласия в критическом параметре
Одни источники устанавливают пороговую величину как 4000 F. В переводе на привычную шкалу это дает 2204 0С. Согласно этому критерию, к жаропрочным относятся только пять элементов: вольфрам, ниобий, рений, тантал и молибден. Например, температура плавления вольфрама составляет 3422 0С.
плавка вольфрама водородной горелкой
Другое утверждение позволяет расширить класс температуростойких материалов, поскольку принимает за точку отсчета температуру плавления железа – 1539 0С. Это позволяет увеличить список еще на девять элементов, включив в него титан, ванадий, хром, иридий, цирконий, гафний, родий, рутений и осмий.
Существует еще несколько пороговых величин температуры, однако они не получили широкого распространения.
Сравнительная таблица степени тугоплавкости чистых металловСледует отметить, что тугоплавкие материалы не ограничиваются исключительно металлами. К этой категории относится ряд соединений – сплавы и легированные металлы, разработанных, чтобы улучшить определенные характеристики исходного материала.
Относительно чистых элементов, можно привести наглядную таблицу степени их температурной устойчивости. Возглавляет ее самый тугоплавкий металл, известный на сегодня, – вольфрам с температурой плавления 3422 0С. Такая осторожная формулировка связана с попытками выделить металлы, обладающие порогом расплава, превосходящим вольфрам.
Поэтому вопрос, какой металл самый тугоплавкий, может в будущем получить совсем иное определение.
Пороговые величины остальных соединений приведены ниже:
- рений 3186;
- осмий 3027;
- тантал 3014;
- молибден 2623;
- ниобий 2477;
- иридий 2446;
- рутений 2334;
- гафний 2233;
- родий 1964;
- ванадий 1910;
- хром 1907;
- цирконий 1855;
- титан 1668.
Остается добавить еще один интересный факт, касающийся физических свойств жапропрочных элементов. Температура плавления некоторых из них чувствительная к чистоте материала. Ярким примером этому выступает хром, температура плавления которого может варьироваться от 1513 до 1920 0С, в зависимости от химического состава примесей. Поэтому, данные интернет пространства часто разнятся точными цифрами, однако качественная составляющая от этого не страдает.
Хром в чистом виде
Общие свойства жаропрочных материалов
Относительная схожесть физико-химических характеристик данных элементов, обусловлена общностью атомного строения и тем, что они оказываются переходными металлами. Напротив, различия в свойствах, связаны с их принадлежностью к широкому спектру групп Периодической таблицы: IV – VII.
Базовая общая характеристика тугоплавких материалов – прочные межатомные связи. Для их разрыва требуется высокая энергия, которая и обуславливает температуру плавления в тысячи градусов по Цельсию. Дополнительно, данное свойство сказывается на высоких значениях таких параметров тугоплавких металлов, как: твердость, механическая прочность, электрическое сопротивление.
Следующая характеристика, объединяющая данные элементы, – высокая химическая активность. Она связана с общей тенденцией тугоплавких металлов образовывать химические связи посредством свободной p- и частично заполненной d-орбитали, отдавая электроны с наружных уровней s и d. Это свойство затрудняет получение чистых тугоплавких металлов, разбивая технологическое производство на несколько этапов.
Строение жаропрочных элементов также идентично, все они характеризуются объемно-центрированной кубической кристаллической решеткой. Для этой структуры характерно «охрупчивание». Исключение составляет рений, обладающий гексагональной ячейкой. Переход в хрупкое состояние для каждого металла происходит при определенной температуре, регулирование которой достигается при помощи легирования.
Каждый тугоплавкий металл, по определению жаропрочный, однако не любой из них жаростойкий. Большинство тугоплавких металлов устойчивы к окислению и действию агрессивных сред: кислоты, щелочи; в обычных условиях.
Однако, с повышением температуры до 400 0С их активность аномально возрастает. Это требует создания определенных условий эксплуатации.
Поэтому, изделия из тугоплавких металлов, при повышенных температурах использования, часто помещают в атмосферу инертных газов или добиваются степени разреженности воздуха до условий вакуума.
Получение тугоплавких материалов
Как отмечалось ранее, основной препятствующий фактор производству жаропрочных металлов их высокая химическая активность, препятствующая выделению элементов в чистом виде.
Основной технологией получения остается порошковая металлургия. Данная методика позволяет получать порошки тугоплавких металлов различными способами:
- Восстановление триоксидом водорода. Процесс производится в несколько этапов, внутри многотрубных печей при 750 – 950 °С. Технология применима под порошки тугоплавких металлов: вольфрам и молибден.
- Восстановлением водородом перрената. Схема реализуется в производстве металлического рения. Рабочие температуры составляют около 500 °С. Заключительная стадия предусматривает отмывание порошка от щелочи. Для этого последовательно используется горячая вода и раствор соляной кислоты.
- Использование солей металлов. Технология развита для выделения молибдена. Основным сырьем выступает аммонийная соль металла и его металлический порошок, вводимый в смесь на уровне 5 — 15% от массы. Состав проходит термическую обработку 500 – 850 °С в проточном инертном газе. Восстановление металла проходит в атмосфере водорода при температурах 800 – 1000 °С.
Производство тугоплавких металлов — порошковая металлургия
Экскурсия на производство
Способы получения жаропрочных металлов продолжают совершенствоваться, как и химическая технология тугоплавких неметаллических и силикатных материалов, что связано с развитием ядерной энергетики, авиастроения, появлением новых моделей ракетных двигателей.
Одно из крупнейших предприятий по производству вольфрама на территории РФ – унечский завод тугоплавких металлов. Этот предприятие относительно молодое, строительство его началось в 2007 году на территории населенного пункта Унеча. Производственный акцент завода направлен на порошки тугоплавких металлов, точнее вольфрама и его карбидов.
В дальнейшем, для получения слитков рассыпчатую массу спекают или сдавливают прессом. Подобным образом порошки тугоплавких металлов обрабатываются для производства жаропрочных изделий.
Применение тугоплавких материалов
Применение чистых жаропрочных металлов имеет приоритеты по ряду направлений:
- производство космических кораблей;
- изготовление управляемых снарядов, ракет;
- электронная и вакуумная техника.
Космическая промышленность
Последний пункт затрагивает электроды электровакуумных радиоламп. Например, высокочистый ниобий используется для производства сеток, трубок электронных деталей. Также из него изготавливаются электроды – аноды электровакуумных приборов.
Электровакуумные радиолампы
Аналогичное применение свойственно молибдену, вольфраму. Эти металлы в чистом виде используются не только как нити накаливания, но и под электроды радиоламп, крючки, подвески электровакуумного оборудования. Монокристаллы вольфрама, напротив, эксплуатируются как подогреватели электродов, в частности катодов, а также при изготовлении электрических контактов, предохранителей.
Чистые ванадий и ниобий используются в ядерной энергетике, где их них изготовлены трубы атомных реакторов, оболочки тепловыделяющих элементов. Область применения высокочистого тантала – химия (посуда и аппаратура), поскольку металл обладает высокой стойкостью к коррозии.
Отдельно следует рассматривать тугоплавкий припой, поскольку он не включает металлов, имеющих высокие температуры плавления. Например, тугоплавкое олово не содержит порошки тугоплавких металлов. В качестве добавок тут используются медь, серебро, никель или магний.
Тугоплавкие металлы и сплавы востребованы как прокат, так и в других сферах. В частности, применение сплавов обусловлено способностью, модифицировать определенные свойства металла: понизить температуру охрупчивания, улучшить жаропорочные характеристики.
Прокат из тугоплавких металлов достаточно широк по ассортименту и включает:
- полосы обычные и для глубокой вытяжки;
Термоэлектродная проволока вольфрам-рениевая
Наиболее крупным отечественным производителем данного типа продукции выступает опытный завод тугоплавких металлов и твердых сплавов.
тугоплавкие металлы
Источник: http://xlom.ru/spravochnik/tugoplavkie-metally-opisanie-izdeliya-iz-tugoplavkix-me/
Самый тугоплавкий металл в мире — Справочник металлиста
С древних времен человек научился обрабатывать и использовать в своей жизни металлы.
Какие-то из них подходят для изготовления посуды и других товаров народного потребления, из других, например нержавеющая сталь, делают оружие и медицинские инструменты.
А некоторые металлы и сплавы используются для строительства сложных технических механизмов, например космический корабль или самолет. Одной из характеристик, на которую обращают внимание при выборе того или иного материала, является его тугоплавкость.
Самый тугоплавкий металл вольфрам
Тугоплавкость металлов
Внимание этой характеристике уделяют все инженеры и конструкторы, работающие в машиностроении. В зависимости от величины этой характеристики, человек может рассчитать и определить в какую конструкцию можно применить те или иные тугоплавкие материалы.
Материалы, температура плавления который выше температуры плавления железа, равной 1539 °С, называются тугоплавкими. Самые тугоплавкие материалы:
- тантал;
- ниобий;
- молибден;
- рений;
- вольфрам.
ТанталМолибден
Полный список содержит больше химических элементов, но не все из них получили распространенное применение в производстве и некоторые обладают меньшими температурами плавления или радиоактивны.
Вольфрам – самый тугоплавкий металл. На вид он светло-серого цвета, твердость и вес достаточно велики. Однако, он становится хрупким при низких температурах и его легко сломать (хладноломкость). Если нагреть вольфрам больше 400 °С, он станет пластичным. С другими веществами вольфрам плохо соединяется. Добывают его из сложных и редких минералов руд, таких как:
- шеелит;
- ферберит;
- вольфрамит;
- гюбнерит.
Переработка руды очень сложный и дорогостоящий процесс. Извлеченный материал формируют в бруски или готовые детали.
Гюбнерит
Вольфрам был открыт в XVIII веке, но долгое время не существовало печей, способных нагреваться до температуры плавления этого тугоплавкого металла. Ученые провели множество исследований и подтвердили, что вольфрам самый тугоплавкий металл. Стоит отметить, что по одной из теорий, сиборгий имеет большую температуру плавления, но не удается провести достаточное количество исследований, т.к. он радиоактивен и нестабилен.
Добавление вольфрама в сталь увеличивает ее твердость, поэтому его стали применять в изготовлении режущего инструмента, что увеличило скорость резания и тем самым привело к росту производства.
Высокая стоимость и трудность обработки этого тугоплавкого металла сказываются на сферах его применения. Он используется в тех случаях, когда нет возможности применить другой. Его достоинства:
- устойчив к высоким температурам;
- повышенная твердость;
- прочный или упругий при определенных температурах;
Переработка металлической руды
Все эти характеристики помогают вольфраму найти широкое применение в различных сферах, таких как:
- металлургия, для легированных сталей;
- электротехника, для нитей накаливания, электродов и др.;
- машиностроение, в изготовлении узлов зубчатых передач и валов, редукторов и многом другом;
- авиационное производство, в изготовлении двигателей;
- космическая отрасль, применяется в соплах ракет и реактивных двигателях;
- военно-промышленный комплекс, для бронебойных снарядов и патронов, брони военной техники, в устройстве торпед и гранат;
- химическая промышленность, вольфрам обладает хорошей коррозийной стойкостью к действию кислот, поэтому из него делают сетки для фильтров. Кроме того соединения с вольфрамом используют в качестве красителей тканей, в производстве одежды для пожарных и многом другом.
Такой перечень отраслей, где используется этот тугоплавкий металл говорит о том, что его значение для человечества очень велико. Ежегодно по всему миру изготавливают десятки тысяч тон чистого вольфрама и с каждым годом потребность в нем растет.
Тугоплавкие металлы
Тугоплавкие металлы были выделены в отдельный класс благодаря объединяющему их свойству — высокой температуре плавления. Она выше, чем у железа, которая равна 1539 °C. Поэтому металлы данной группы и получили такое название. Они принадлежат к числу так называемых редкоземельных элементов. Так, например, по распространённости в земной коре ниобий и тантал составляют 3%, а цирконий только 2%.
Тугоплавкие металлы
По температурному показателю плавления кроме перечисленных, к ним относятся металлы, так называемой платиновой группы. Ещё их называют благородными или драгоценными.
Определённая схожесть строения атома обусловила схожесть их свойств. На основании этого можно обобщить некоторые черты проявления таких металлов в земной коре и определиться с технологией их добычи, производства и переработки.
Свойства тугоплавких металлов
За счёт того, что они расположены в соседних группах периодической таблицы, физические свойства у тугоплавких металлов достаточно близкие:
- Плотность металла колеблется в интервале от 6100 до 10000 кг/м3. По этому показателю выделяется только вольфрам. У него он равен 19000 кг/м3.
- Температура плавления. Она превышает температуру плавления железа и колеблется от 1950 °С у ванадия до 3395 °С у вольфрама.
- Удельная теплоёмкость у них незначительно отличается друг от друга и находится в пределах от 200 до 400 Дж/(кг-град).
- Коэффициент теплопроводности сильно меняется от элемента к элементу. Если у ванадия он равен 31 Вт/(м-град), то у вольфрама он достигает величины в 188 Вт/(м-град).
Физические свойства тугоплавких металлов
Химические свойства также достаточно схожие:
- Очень похожее строение атома.
- Обладают высокой химической активностью. Это свойство определяет основные трудности при сохранении стабильности их соединений.
- Прочность межатомных связей определяет высокую температуру плавления. Это обстоятельство объясняет высокую механическую прочность, твёрдость и электрические характеристики (в частности сопротивление).
- Проявляют хорошую устойчивость при воздействии различных кислот.
К основным недостаткам тугоплавких металлов относятся:
- Низкая коррозийная стойкость. Процесс окисления происходит достаточно быстро. Его разделяют на две последовательные стадии. Непосредственное взаимодействие металла с кислородом окружающего воздуха, что приводит к образованию оксидной плёнки. На второй стадии происходит процесс диффузии (проникновения) атомов кислорода через образовавшуюся оксидную плёнку.
- Трудности со свариваемостью тугоплавких металлов. Это вызвано высокой химической активностью к окружающему воздуху при высоких температурах, хрупкостью при насыщении различными примесями. Кроме того, трудно определить точку перегрева и практически невозможно контролировать повышение предела текучести.
- Трудности их получения использования в чистом виде без примесей.
- Необходимость применения специальных покрытий от быстрого окисления. Для сплавов, основу которых составляет вольфрам и молибден, разработаны силицидные покрытия.
- Трудности, связанные с механической обработкой. Для качественной обработки их сначала необходимо нагреть.
Производство тугоплавких металлов
Все способы производства тугоплавких металлов основаны на методиках так называемой порошковой металлургии. Сам процесс происходит в несколько этапов:
- На начальном этапе получают порошок металла.
- Затем методами химического восстановления (обычно аммонийных солей или оксидов) выделяют требуемый металл. Такое выделение получается в результате воздействия на порошок водорода.
- На завершающем этапе получают химическое соединение, называемое гексафторидом соответствующего металла, и уже из него сам металл.
Применение тугоплавких металлов
Начиная со второй половины двадцатого века тугоплавкие металлы стали применяться во многих отраслях промышленного производства. Порошки тугоплавких металлов используются для производства первичной продукции. Тугоплавкие металлы вырабатывают в виде проволоки, слитков, арматуры, прокатного металла и фольги.
Отдельное место такие металлы занимают в технологии выращивания лейкосапфиров. Они относятся к классу монокристаллов и называются искусственными рубинами.
Изделия из тугоплавких металлов входят в состав бытовых и промышленных электрических приборов, огнеупорных конструкций, деталей для двигателей авиационной и космической техники. Особое место занимают тугоплавкие металлы при производстве деталей сложной конфигурации.
Этот металл открыли в далёком 1781 г. Его температура плавления равна 3380 °С. Поэтому он на сегодняшний день является самым тугоплавким металлом. Получают вольфрам из специального порошка, подвергая его химической обработке. Этот процесс основан на прессовании с последующим спеканием при высоких температурах. Далее его подвергают ковке и волочению на станках. Это связано с его наибольшей тугоплавкостью.
Так получают волокнистую структуру (проволоку). Она достаточно прочная и практически не ломается. На конечном этапе его раскатывают в виде тонких нитей или гибкой ленты. Для проведения механической обработки необходимо создать защитную среду из инертного газа. В этой среде температура должна превышать 400 °С. При температуре окружающей среды он приобретает свойства парамагнетика.
Ему присущи следующие недостатки:
- сложность в создании условий для механической обработки;
- быстрое образование на поверхности оксидных плёнок. Если в контакте имеются серосодержащие вещества, образуются сульфидные плёнки;
- создание хорошего электрического контакта между несколькими деталями возможно только при создании большого давление.
Вольфрам
Для улучшения свойств вольфрама (тугоплавкости, устойчивости к коррозии, износостойкости) в него добавляют легирующие металлы. Например, рений и торий.
Металл используется для производства нитей накаливания для осветительных и сушильных ламп. Его добавляют в сварочные электроды, элементы электронных ламп и рентгеновских трубок. Также применяется при производстве элементов ракет, в реактивных двигателях, артиллерийских снарядах.
По внешнему виду и характеристикам очень похож на вольфрам. Главным отличием является то, что его удельный вес почти в два раза меньше. Его получают аналогичным образом. Он широко применяется в радиоэлектронной промышленности, для изготовления различных испарителей в вакуумной технике, разрывных электрических контактов. Как и вольфрам, он является парамагнетиком. Для изготовления электродов стекловаренных (стеклоплавильных) печей он просто незаменим.
Ниобий
Температура плавления ниобия составляет 2741 °С. По своим химическим, физическим и механическим свойствам очень напоминает тантал. Он достаточно пластичен. Обладает хорошей свариваемостью и высокой теплопроводностью даже без дополнительного нагрева. Как и все остальные металлы его получают из порошка. Конечные заготовки из ниобия – проволока, лента, труба.
Ниобий
Сам металл и его сплавы демонстрируют эффект сверхпроводимости. Его широко применяют для изготовления анодов, экранных и антидинатронных сеток в электровакуумных приборах. Благодаря хорошей пористости, его успешно применяют в качестве газопоглотителей. В микроэлектронике он идёт на изготовление резисторов в микросхемах.
Ниобий хорошо себя проявил в качестве легирующей добавки. Используется при создании различных жаростойких конструкций, агрегатов работающих в агрессивных и радиоактивных средах. Из сплава стали и ниобия изготавливают некоторые элементы реактивных двигателей. Благодаря его свойству не взаимодействовать с радиоактивными веществами при высоких температурах, например, с ураном, применяется при изготовлении оболочек для урановых элементов, отводящих тепло в реакторах.
Тантал
Внешне имеет светло-серый цвет с небольшим голубоватым оттенком. Температура плавления близка к 3000 °С. Хорошо поддается основным видам обработки. Его можно ковать, прокатывать, производить волочение для изготовления проволоки.
Эти операции не требуют значительного нагрева. Для удобства дальнейшего использования тантал изготавливают в форме фольги и тонких листов.
Повышение температуры вызывает активное взаимодействие со всеми газами, кроме инертных – с ними никаких реакций не наблюдается.
Тантал
Из тантала производят внутренние элементы генераторных ламп (магнетронов и клистронов). Он активно используется при производстве пластин в электролитических конденсаторах. Очень удобен для изготовления пленочных резисторов. Активно применяется для изготовления так называемых лодочек в испарителях, в которых осуществляется термическое напыление различных материалов на тонкие пленки.
Ввиду ряда своих уникальных качеств, считается незаменимым в ядерной, аэрокосмической и радиоэлектронной промышленности.
Рений
Был открыт позже всех из перечисленных ранее металлов. Он полностью оправдывает свое название «редкоземельный металл», потому что находится в небольших количествах в составе руды других металлов, таких как платина или медь.
В основном его используют как легирующую добавку. Полученные сплавы приобретают хорошие характеристики прочности и ковкости. Это один из самых дорогих металлов, поэтому его применение приводит к резкому увеличению цены всего оборудования.
Те не менее, его применяют в качестве катализатора.
Хром
Хром — уникальный металл. Широко применяется в промышленности благодаря своим замечательным свойствам: прочности, устойчивости к внешним воздействиям (нагреву и коррозии), пластичности. Достаточно твердый, но хрупкий металл. Имеет серо-стальной цвет. Весь необходимый хром извлекают из руды двух видов хромита железа или окиси хрома.
Основными его свойствами являются:
- Даже при нормальной температуре обладает почти идеальным антиферромагнитным упорядочением. Это придаёт ему отличные магнитные свойства.
- По-разному реагирует на воздействие водорода и азота. В первом случае сохраняет свою прочность. Во втором, становится хрупким и полностью теряет все свои пластические свойства.
- Обладает высокой устойчивостью против коррозии. Это происходит благодаря тому, что при взаимодействии с кислородом на поверхности образуется тонкая защитная плёнка. Она служит для защиты от дальнейшей коррозии.
Кристаллы хрома
Он используется в металлургической, химической, строительной индустриях. Хром, как легирующая добавка, обязательно используется для производства различных марок нержавеющей стали. Особое место занимает при изготовлении такого материала как нихром.
Этот материал способен выдерживать очень высокие температуры. Поэтому его используют в различных нагревательных элементах. Хромом активно покрывают поверхности различных деталей (металла, дерева, кожи). Это процесс осуществляется с помощью гальваники.
Токсичность некоторых солей хрома используют для сохранения древесины от повреждения, вредного воздействия грибков и плесени. Они также хорошо отпугивают муравьёв, термитов, насекомых разрушителей деревянных конструкций. Солями хрома обрабатывают кожу. Хром применяется при изготовлении различных красителей.
Благодаря высокой теплостойкости его используют как огнеупорный материал для доменных печей. Каталитические свойства соединений хрома успешно используют при переработке углеводородов. Его добавляют при производстве магнитных лент наивысшего качества. Именно он обеспечивает низкий коэффициент шума и широкую полосу пропускания.
Источник: https://stankiexpert.ru/spravochnik/materialovedenie/tugoplavkie-metally.html
Связанные статьи:
- Редкие металлыРедкие металлы, условное наименование группы металлов (более чем 50), список которых дан в таблице. Это металлы, относительно новые в технике либо ещё
- Раскисление металловРаскисление металлов, процесс удаления из расплавленных металлов (в основном стали и др. сплавов на базе железа) растворённого в них кислорода, что есть
Источник: http://australianembassy.ru/tugoplavkie-metally/
Какой металл считается самым тугоплавким
Металл с давних времён используются человеком в различных сферах деятельности. Чтобы получить качественное металлическое изделие, важно подобрать хороший материал, оценивая при этом его характеристики. Важный параметр — тугоплавкость. Для изготовления некоторых изделий подходят только самые тугоплавкие металлы.
Исторические сведенияПрежде чем изучать характеристики самых тугоплавких металлов в мире следует ознакомиться с их историей открытия. Металлообработка известна человеку несколько тысяч лет. Однако активное получение тугоплавких металлов началось только со второй половины 19 века.
Изначально они использовались только в электротехнике. С появлением новых технологий в строении самолётов, машин, поездов и ракет детали с высоким показателем плавления начали использоваться активнее. Пик популярности заготовок, выдерживающих температуры более 1000 градусов, пришёлся на середину 20 века.
ОпределениеТугоплавкий металл — отдельный класс, к которому относятся металлические заготовки, выдерживающие воздействие критически высоких температур. Обычно у представителей этого класса температура плавления более 1600 градусов, что считается точкой плавления железа. К ним относят благородные сплавы. Их ещё называют представителями платиновой группы.
ВидыВиды металлов и сплавов, обладающие устойчивостью к повышенным температурам:
- Вольфрам. Впервые о нем узнали в 1781 году. Чтобы расплавить, его потребовалось разогреть до 3380 градусов. Вольфрам считается самым тугоплавким. Изготавливается он из порошка, который обрабатывается химическим способом. Сначала смесь разогревается, а затем подвергается давлению. На выходе получаются спрессованные заготовки.
- Ниобий. Плавится при 2500 градусах. Обладает высокой теплопроводностью, обрабатывается не так сложно, как вольфрам. Изготавливается из порошка, который запекают и обрабатывают с помощью высокого давления. Из ниобия делают проволоку, трубы и ленту.
- Молибден. Визуально его можно спутать с вольфрамом. Изготавливается он из порошка при запекании и воздействии давлением. Как и вольфрам обладает парамагнетическими свойствами. Используется в радиоэлектронике, изготовлении промышленного оборудования, печей и электродов.
- Тантал. Плавится при 3000 градусах. Чтобы сделать проволоку из тантала или закалить материал, его не нужно нагревать до критических температур. Используется для изготовления элементов в радиоэлектронике (конденсаторы, пленочные резисторы). Популярен в ядерной промышленности.
- Рений. Материал, который ученые открыли позже остальных. Найти его можно в медной и платиновой руде. Используется на промышленном производстве, как легирующая добавка.
К материалам с высокими температурами плавления относится и хром. Благодаря своим уникальным характеристикам он применяется в различных сферах промышленности. Обладает повышенной устойчивостью к критическим температурам и коррозийным процессам. Однако стоит учитывать его хрупкость.
СвойстваЧтобы понимать, где лучше использовать материал, нужно знать свойства тугоплавких металлов. Из них изготавливаются детали для промышленного оборудования, техники и электроники. Характеристики тяжелых тугоплавких металлов будут описаны ниже.
Физические свойстваХарактеристики:
- Плотность — до 10000 кг/м3. У вольфрама этот показатель достигает 19000 кг/м3.
- Средняя температура плавления — 2500 градусов по Цельсию. Самая высокая температура плавления металла у вольфрама — 3390 градусов.
- Удельная теплоёмкость — 400 Дж.
Тугоплавкие предметы не выдерживают ударов и падений.
Химические свойстваХимические свойства:
- Это твердые вещества, обладающие высокой химической активностью.
- Прочная межатомная структура.
- Сопротивляемость длительному воздействию кислот и щелочей.
- Высокий показатель парамагнитности.
Эти материалы имеют некоторые недостатки. Главным из них является трудный процесс обработки и изготовления продукции из него.
ПрименениеИзначально тугоплавкие металлы использовались при изготовлении конденсаторов и транзисторов для радиоэлектроники. Количество их сфер применения увеличилось только к середине 20 века. Промышленной комплекс расширился до изготовления деталей для станков, автомобилей, самолётов и ракет.
Сплавы, выдерживающие воздействие критических температур, начали использоваться для изготовления посуды. Тугоплавкие металлы применяются в процессе производства строительных и соединительных материалов. Из них делают детали для бытовых приборов и электроники.
Самым тугоплавким считается вольфрам. Его температура плавления в 3390 градусов превышает показатели других материалов. Однако нельзя забывать про то, что при падении вольфрамовой детали с высоты, она треснет или разобьётся на отдельные части.
Вольфрам — Самый ТУГОПЛАВКИЙ Металл На ЗЕМЛЕ!
Остальные материалы с высоким показателем плавления, немногим отличаются от вольфрама. Используются в машиностроении, кораблестроении, ядерной энергетики, изготовлении промышленного оборудования.
Их разработка и исследование продолжается и по сей день.
Какой металл считается самым тугоплавким Ссылка на основную публикацию
Источник: https://metalloy.ru/obrabotka/termo/samyj-tugoplavkij-metall
Тугоплавкие металлы и их сплавы
Если верить википедии, к тугоплавким относятся металлы, которые имеют температуру плавления от 2200 °C. Под это утверждение подпадают ниобий, рений, молибден, тантал и вольфрам.
| Название | Температура плавления |
| Ниобий | 2477°C |
| Молибден | 2623 °C |
| Тантал | 3017 °C |
| Вольфрам | 3422 °C |
| Рений | 3186 °C |
Тугоплавкие металлы широко применяются во многих отраслях промышленности и в повседневной жизни. Их применяют при изготовлении лампочек накаливания, мобильных телефонов, компьютеров или, например, ядерных реакторов.
В более широком понятии и практическом применении к тугоплавким металлам еще относят ванадий, гафний, рутений, хром, цирконий и осмий.
Их также используют в качестве легирующих элементов в сплавах с металлами из первой группы для улучшения комплекса эксплуатационных или технологических свойств.
Сами по себе чистые металлы конечно применяются в производстве, например чистые молибден и вольфрам применяют в радиоэлектронной промышленности, химическом машиностроении или при производстве печей для термообработки. Но большинство из них склонны к хрупкому разрушению при высоких температурах, также они обладают относительно низкой жаропрочностью. Гораздо интереснее, с точки зрения повышения эксплуатационных свойств, представляется использование сплавов этих металлов.
Тугоплавкие сплавы на основе вольфрама
Представителем таких сплавов является сплав вольфрама и ниобия ВВ2 с температурой жаропрочности до 1200°C. Для повышения коррозионной стойкости и тугоплавкости вольфрамовые сплавы легируют рением. А для повышения износостойкости торием.
Сплавы на основе молибдена
Молибден и его сплавы являются наверное самыми частоиспользуемыми из всех тугоплавких. В промышленности часто используются сплавы легированные цирконием, бором, титаном, ниобием: сплавы ЦМ3, ЦМ6, ЦМ2А, ВМ3
Тугоплавкие сплавы на основе ниобия
Ниобий и его сплавы, благодаря высокой коррозионной стойкости, высокой жаропрочности (до 1300°C) и хорошей работе при нейтронном облучении, нашли широкое применение при изготовлении изделий атомной промышленности. В качестве примера сплавов на основе ниобия стоит назвать сплавы ВН2, ВН2А, ВН3.
Способы повышения жаропрочности и жаростойкости сплавов
Жаропрочность тугоплавких сплавов, как уже было сказано выше, повышают легированием элементами с более высокой температурой плавления, образующими в сплаве твердые растворы замещения. Большей эффективности повышения жаропрочности и в некоторых случаях износостойкости, удается добиться при дисперсионном твердении сплава с образованием карбидов (ZrC, NiC), нитридов (TiN) и оксидов (ZrO2).
Все тугоплавкие металлы обладают низкой жаростойкостью, поэтому для их защиты при температурах выше 400°C используют интерметаллидные и керамические покрытия. Для молибдена и вольфрама используют покрытия на основе кремния (MoSi2, WSi2). [1]
Литература:
- Ю.М. Лахтин, В.П. Леонтьева., Материаловедение, 1990
Источник: https://HeatTreatment.ru/tugoplavkie-metally-i-ih-splavy.html
Самый тугоплавкий металл в мире: свойства, получение, применение — Сайт о
Металлы относятся к самым распространенным материалам наравне со стеклом и пластмассами. Они используются людьми с давних времен.
На практике люди познавали свойства металлов и с выгодой использовали их для изготовления посуды, бытовых предметов, различных сооружений и произведений искусства.
Основной характеристикой этих материалов является их тугоплавкость и твердость. Собственно, от этих качеств зависит их применение в той или иной области.
Физические свойства металлов
Все металлы обладают следующими общими свойствами:
- Цвет – серебристо-серый с характерным блеском. Исключение составляют: медь и золото. Они соответственно выделяются красноватым и желтым оттенком.
- Агрегатное состояние – твердое тело, кроме ртути, которая является жидкостью.
- Тепло- и электропроводность – для каждого вида металлов выражается по-разному.
- Пластичность и ковкость – изменяющийся параметр в зависимости от конкретного металла.
- Температура плавления и кипения – устанавливает тугоплавкость и легкоплавкость, обладает разными значениями для всех материалов.
Все физические свойства металлов зависят от строения кристаллической решетки, ее формы, прочности и пространственного расположения.
Тугоплавкие и легкоплавкие металлы
- Тугоплавкие – их температура плавления превышает точку плавления железа (1539 °C). К ним можно отнести платину, цирконий, вольфрам, тантал. Таких металлов всего несколько видов. На практике их применяется еще меньше.
Некоторые не используются, так как они имеют высокую радиоактивность, другие – слишком хрупкие и не обладают нужной мягкостью, третьи – подвержены коррозии, а есть такие, что экономически невыгодные.
Какой металл самый тугоплавкий? Как раз об этом пойдет речь в данной статье.
- Легкоплавкие – это металлы, которые при температуре меньше или равной температуре плавления олова 231,9 °C могут изменить свое агрегатное состояние. Например, натрий, марганец, олово, свинец. Металлы применяются в радио- и электротехнике.
Их часто используют для антикоррозийных покрытий и в качестве проводников.
Вольфрам – самый тугоплавкий металл
Это твердый и тяжелый материал с металлическим блеском, светло-серого цвета, обладающий высокой тугоплавкостью. Механической обработке поддается трудно. При комнатной температуре он является хрупким металлом и легко ломается.
Вызвано это загрязнением его примесями кислорода и углерода. Технически чистый вольфрам при температуре более 400 градусов Цельсия становится пластичным. Проявляет химическую инертность, плохо вступает в реакции с другими элементами.
В природе вольфрам встречается в виде сложных минералов, таких как:
- шеелит;
- вольфрамит;
- ферберит;
- гюбнерит.
Вольфрам получают из руды, применяя сложные химические переработки, в виде порошка. Используя методы прессования и спекания, изготовляют детали простой формы и бруски. Вольфрам — очень стойкий элемент к температурным воздействиям. Поэтому размягчить металл не могли в течение ста лет.
Не имелось таких печей, которые могли бы разогреваться до нескольких тысяч градусов. Ученые доказали, что самым тугоплавким металлом является вольфрам.
Хотя существует мнение, что сиборгий, по теоретическим данным, обладает большей тугоплавкостью, но утверждать твердо этого нельзя, так как он радиоактивный элемент и имеет маленький срок существования.
Исторические сведения
Знаменитый шведский химик Карл Шееле, имеющий профессию аптекаря, в небольшой лаборатории, проводя многочисленные опыты, открыл марганец, барий, хлор и кислород.
А незадолго до смерти в 1781 году выявил, что минерал тунгстен является солью неизвестной тогда кислоты. После двух лет работы его ученики, два брата д’Элуяр (испанские химики), выделили из минерала новый химический элемент и назвали его вольфрамом.
Только через столетие вольфрам – самый тугоплавкий металл — произвел настоящий переворот в промышленности.
Режущие свойства вольфрама
В 1864 году английский ученый Роберт Мюшет использовал вольфрам как легирующую добавку к стали, которая выдерживала красное каление и еще больше увеличивала твердость. Резцы, которые изготовляли из полученной стали, увеличили скорость резания металла в 1,5 раза, и она стала составлять 7,5 метра в минуту.
Работая в этом направлении, ученые получали все новые технологии, увеличивая скорость обработки металла с использованием вольфрама.
В 1907 году появилось новое соединение вольфрама с кобальтом и хромом, которое стало основоположником твердых сплавов, способных увеличивать скорость резания.
В настоящее время она возросла до 2000 метров в минуту, и все это благодаря вольфраму – самому тугоплавкому металлу.
Применение вольфрама
Этот металл обладает сравнительно высокой ценой и тяжело обрабатывается механическим способом, поэтому применяют его там, где невозможно заменить другими, сходными по свойствам материалами.
Вольфрам прекрасно выдерживает высокие температуры, имеет значительную прочность, наделен твердостью, упругостью и тугоплавкостью, поэтому находит широкое использование во многих областях промышленности:
- Металлургической. Она является основным потребителем вольфрама, который идет на производство высокого качества легированных сталей.
- Электротехнической. Температура плавления самого тугоплавкого металла составляет почти 3400 °C. Тугоплавкость металла позволяет применять его для производства нитей накаливания, крючков в осветительных и электронных лампах, электродов, рентгеновских трубок, электрических контактов.
- Машиностроительной. Благодаря повышенной прочности сталей, содержащих вольфрам, изготавливают цельнокованые роторы, зубчатые колеса, коленчатые валы, шатуны.
- Авиационной. Какой самый тугоплавкий металл используют для получения твердых и жаропрочных сплавов, из которых делают детали авиационных двигателей, электровакуумных приборов, нити накаливания? Ответ прост – это вольфрам.
- Космической. Из стали, содержащей вольфрам, производят реактивные сопла, отдельные элементы для реактивных двигателей.
- Военной. Высокая плотность металла позволяет изготавливать бронебойные снаряды, пули, броневую защиту торпед, снарядов и танков, гранаты.
- Химической. Стойкая вольфрамовая проволока против кислот и щелочей используется для сеток к фильтрам. С помощью вольфрама меняют скорость химических реакций.
- Текстильной. Вольфрамовая кислота используется как краситель для тканей, а вольфрамит натрия применяют для производства кожи, шелка, водоустойчивых и огнестойких тканей.
Приведенный перечень использования вольфрама в разных областях индустрии указывает на высокую ценность этого металла.
Получение сплавов с вольфрамом
Вольфрам, самый тугоплавкий металл в мире, часто используют для получения сплавов с другими элементами для улучшения свойств материалов. Сплавы, которые содержат вольфрам, как правило, получают по технологии порошковой металлургии, так как при общепринятом способе все металлы превращаются в летучие жидкости или газы при его температуре плавления.
Процесс сплавления проходит в вакууме или в атмосфере аргона, чтобы избежать окисления. Смесь, состоящую из металлических порошков, прессуют, спекают и подвергают плавке. В некоторых случаях только вольфрамовый порошок подвергают прессовке и спеканию, а затем пористую заготовку насыщают расплавом другого металла.
Сплавы вольфрама с серебром и медью получают именно таким способом. Даже небольшие добавки самого тугоплавкого металла увеличивают жаростойкость, твердость и стойкость к окислению в сплавах с молибденом, танталом, хромом и ниобием. Пропорции в этом случае могут быть совершенно любыми в зависимости от потребностей промышленности.
Более сложные сплавы, зависящие от соотношения компонентов с железом, кобальтом и никелем, имеют следующие свойства:
- не тускнеют на воздухе;
- обладают хорошей химической стойкостью;
- имеют отличные механические свойства: твердость и износоустойчивость.
Довольно сложные соединения образует вольфрам с бериллием, титаном и алюминием. Они выделяются устойчивостью при высокой температуре к окислению, а также жаропрочностью.
Свойства сплавов
В практической деятельности вольфрам часто соединяют с группой иных металлов.
Соединения вольфрама с хромом, кобальтом и никелем, обладающие повышенной стойкостью к кислотам, используют для изготовления хирургических инструментов.
А особые жаропрочные сплавы, кроме вольфрама – самого тугоплавкого металла, содержат в своем составе хром, никель, алюминий, никель. Вольфрам, кобальт и железо входит в состав лучших марок магнитной стали.
Вольфрамсодержащие стали устойчивы к истиранию, не трескаются, неизменно сохраняют твердость. Режущие инструменты не только увеличивают скорость обработки металла, но и имеют длительный срок службы.
Самые легкоплавкие и тугоплавкие металлы
К легкоплавким относятся все металлы, температура плавления которых меньше, чем у олова (231,9 °C). Элементы этой группы находят применение в качестве антикоррозийных покрытий, в электро- и радиотехнике, входят в состав антифрикционных сплавов.
Ртуть, точка плавления которой -38,89 °C, при комнатной температуре является жидкостью и находит широкое применение в научных приборах, ртутных лампах, выпрямителях, переключателях, в хлорном производстве. У ртути самая низкая температура плавления по сравнению с другими металлами, входящими в группу легкоплавких.
К тугоплавким металлам принадлежат все, температура плавления которых больше, чем у железа (1539 °C). Чаще всего их используют в качестве добавок при изготовлении легированных сталей, а также они могут служить и основой для некоторых специальных сплавов.
Вольфрам, имеющий максимальную температуру плавления 3420 °C, в чистом виде используют в основном для нитей накала в электролампах.
Довольно часто в кроссвордах задают вопросы, какой из металлов самый легкоплавкий или самый тугоплавкий? Теперь, не задумываясь, можно ответить: самый легкоплавкий – ртуть, а самый тугоплавкий – вольфрам.
Коротко о железе
Этот металл называют основным конструкционным материалом. Детали из железа встречаются как на космическом корабле или подводной лодке, так и дома на кухне в виде столовых приборов и различных украшений.
Этот металл имеет серебристо-серый цвет, обладает мягкостью, пластичностью и магнитными свойствами. Железо является очень активным элементом, на воздухе образуется оксидная пленка, которая препятствует продолжению реакции.
Во влажной среде появляется ржавчина.
Температура плавления железа
Железо обладает пластичностью, хорошо поддается ковке и плохо обрабатывается литьем. Этот прочный металл легко обрабатывается механическим способом, используется для изготовления магнитоприводов.
Хорошая ковкость позволяет его применять для декоративных украшений. Является ли железо самым тугоплавким металлом? Следует отметить, что его температура плавления равна 1539 °C.
А по определению, к тугоплавким относятся металлы, температура плавления которых больше, чем у железа.
Однозначно можно сказать, что железо — не самый тугоплавкий металл, и даже не принадлежит к этой группе элементов. Он относится к среднеплавким материалам. Назовите самый тугоплавкий металл? Такой вопрос не застанет теперь вас врасплох. Можно смело отвечать – это вольфрам.
Вместо заключения
Примерно тридцать тысяч тонн в год вольфрама производится во всем мире. Этот металл непременно входит в состав наилучших сортов сталей для изготовления инструментов. На нужды металлургии расходуется до 95% всего вырабатываемого вольфрама.
Для удешевления процесса в основном используют более дешевый сплав, состоящий из 80% процентов вольфрама и 20% железа. Используя свойства вольфрама, его сплав с медью и никелем применяют для производства контейнеров, используемых под хранение радиоактивных веществ.
В радиотерапии этот же сплав служит для изготовления экранов, обеспечивая надежную защиту.
Источник: https://nzmetallspb.ru/benzoinstrument/samyj-tugoplavkij-metall-v-mire-svojstva-poluchenie-primenenie.html
Тугоплавкие металлы — характеристики, свойства и применение
Еще с конца 19 века были известны тугоплавкие металлы. Тогда им не нашлось применения. Единственная отрасль, где их использовали, была электротехника и то в очень ограниченных количествах. Но все резко поменялось с развитием сверхзвуковой авиации и ракетной техники в 50-е года прошлого столетия. Производству потребовались новые материалы, способные выдерживать значительные нагрузки в условиях температур свыше 1000 ºC.
Список и характеристики тугоплавких металлов
Тугоплавкость характеризуется повышенным значением температуры перехода из твердого состояния в жидкую фазу. Металлы, плавление которых осуществляется при 1875 ºC и выше, относят к группе тугоплавких металлов. По порядку возрастания температуры плавки сюда входят следующие их виды:
- Ванадий
- Хром
- Родий
- Гафний
- Рутений
- Вольфрам
- Иридий
- Тантал
- Молибден
- Осмий
- Рений
- Ниобий.
Современное производство по количеству месторождений и уровню добычи удовлетворяют только вольфрам, молибден, ванадий и хром. Рутений, иридий, родий и осмий встречаются в естественных условиях довольно редко. Их годовое производство не превышает 1,6 тонны.
Жаропрочные металлы обладают следующими основными недостатками:
- Повышенная хладноломкость. Особенно она выражена у вольфрама, молибдена и хрома. Температура перехода у металла от вязкого состояния к хрупкому чуть выше 100 ºC, что создает неудобства при их обработке давлением.
- Неустойчивость к окислению. Из-за этого при температуре свыше 1000 ºC тугоплавкие металлы применяются только с предварительным нанесением на их поверхность гальванических покрытий. Хром наиболее устойчив к процессам окисления, но как тугоплавкий металл он имеет самую низкую температуру плавления.
К наиболее перспективным тугоплавким металлам относят ниобий и молибден. Это связано с их распространённостью в природе, а, следовательно, и низкой стоимостью в сравнении с другими элементами данной группы.
Помимо этого, ниобий зарекомендовал себя как металл с относительно низкой плотностью, повышенной технологичностью и довольно высокой тугоплавкостью. Молибден ценен, в первую очередь, своей удельной прочностью и жаростойкостью.
Самый тугоплавкий металл встречаемый в природе — вольфрам. Его механические характеристики не падают при температуре окружающей среды свыше 1800 ºC. Но перечисленные выше недостатки плюс повышенная плотность ограничивают его область использования в производстве. Как чистый металл он применяется все реже и реже. Зато увеличивается ценность вольфрама как легирующего компонента.
Физико-механические свойства
Металлы с высокой температурой плавления (тугоплавкие) являются переходными элементами. Согласно таблице Менделеева выделяют 2 их разновидности:
- Подгруппа 5A – тантал, ванадий и ниобий.
- Подгруппа 6A – вольфрам, хром и молибден.
Наименьшей плотностью обладает ванадий – 6100 кг\м3, наибольшей вольфрам – 19300 кг\м3. Удельный вес остальных металлов находится в рамках этих значений. Эти металлы отличаются малым коэффициентом линейного расширения, пониженной упругостью и теплопроводностью.
Данные металлы плохо проводят электрический ток, но обладает таким качеством как сверхпроводимость. Температура сверхпроводящего режима составляет 0,05-9 К исходя из вида металла.
Абсолютно все тугоплавкие металлы отличаются повышенной пластичностью в комнатных условиях. Вольфрам и молибден помимо этого выделяются на фоне остальных металлов более высокой жаропрочностью.
Коррозионная стойкость
Жаропрочным металлам свойственна высокая стойкость к большинству видов агрессивных сред. Сопротивление коррозии элементов 5A подгрупп увеличивается от ванадия к танталу. Как пример, при 25 ºC ванадий растворяется в царской водке, между тем как ниобий полностью инертен по отношению к данной кислоте.
Тантал, ванадий и ниобий отличаются устойчивостью к воздействию расплавленных щелочных металлов. При условии отсутствия в их составе кислорода, которые значительно усиливает интенсивность протекания химической реакции.
Молибден, хром и вольфрам имеют большую сопротивляемость к коррозии. Так азотная кислота, которая активно растворяет ванадий, значительно менее воздействует на молибден. При температуре 20 ºC данная реакция вообще полностью останавливается.
Все тугоплавкие металлы охотно вступают в химическую связь с газами. Поглощение водорода из окружающей среды ниобием осуществляется при 250 ºC. Тантал при 500 ºC. Единственный способ остановить эти процессы – проведение вакуумного отжига при 1000 ºC. Стоит заметить, что вольфрам, хром и молибден куда менее склонны к взаимодействию с газами.
Как уже было сказано ранее, лишь хром отличается сопротивляемостью к окислению. Данное свойство обусловлено его способностью образовывать твердую пленку оксида хрома на своей поверхности. Растворение кислорода хромом происходит только при 700 С. У остальных тугоплавких металлов процессы окисления начинаются ориентировочно при 550 ºC.
Хладноломкость
Распространению использования жаропрочных металлов в производстве мешает обладание ими повышенной склонности к хладноломкости. Это означает, что при падении температуры ниже определенного уровня происходит резкое возрастание хрупкости металла. Для ванадия такой температурой служит отметка в -195 ºC, для ниобия -120 ºC, а вольфрама +330 ºC.
Наличие хладноломкости жаропрочными металлами обусловлено содержанием примесями в их составе. Молибден особой чистоты (99,995%) сохраняет повышенные пластические свойства вплоть до температуры жидкого азота. Но внедрение всего 0,1% кислорода сдвигает точку хладноломкости к -20 С.
Области применения
До середины 40-х годов тугоплавкие металлы использовались только как легирующие элементы для улучшения механических характеристик стальных цветных сплавов на основе меди и никеля в электропромышленности. Соединения молибдена и вольфрама применялись также в производстве твердых сплавов.
Техническая революция, связанная с активным развитием авиации, ядерной промышленности и ракетостроения, нашла новые способы использования тугоплавких металлов. Вот неполный перечень новых сфер применения:
- Производство тепловых экранов головного узла и каркасов ракет.
- Конструкционный материал для сверхзвуковых самолётов.
- Ниобий служит материалом сотовой панели космических кораблей. А в ракетостроении его используют в качестве теплообменников.
- Узлы термореактивного и ракетного двигателя: сопла, хвостовые юбки, лопатки турбин, заслонки форсунок.
- Ванадий является основой для изготовления тонкостенных трубок тепловыделяющих элементов термоядерного реактора в ядерной промышленности.
- Вольфрам применяется как нить накаливания электроламп.
- Молибден все шире и шире используется в производстве электродов, применяемых для плавки стекла. Помимо этого, молибден — металл, используемый для производства форм литья под давлением.
- Производство инструмента для горячей обработки деталей.
Источник: https://prompriem.ru/metally/tugoplavkie-metally.html
Самый тугоплавкий металл на земле
Любознательных людей наверняка интересует вопрос, какой металл самый тугоплавкий? Прежде чем дать на него ответ, стоит разобраться с сами понятием тугоплавкости. Все известные науки металлы имеют разную температуру плавления в связи с различной степенью устойчивости связей между атомами в кристаллической решетке. Чем слабее эта связь, тем меньшая температура требуется, чтобы ее разорвать.
Самые тугоплавкие металлы в мире используются в чистом виде или в составе сплавов для производства деталей, которые работают в экстремальных термических условиях. Они позволяют эффективно противостоять высоким температурам и значительно продляют эксплуатационный период агрегатов. Но стойкость металлов данной группы к термическому воздействию заставляет металлургов прибегать к нестандартным методам их производства.
Какой металл самый тугоплавкий?
Самый тугоплавкий металл на Земле был открыт в 1781 году шведским ученым Карлом Вильгельмом Шееле. Новый материал получил название вольфрам. Шееле удалось синтезировать триокись вольфрама путем растворения руды в азотной кислоте.
Чистый металл был выделен двумя годами позже испанскими химиками Фаусто Фермином и Хуаном Хосе де Элюар. Новый элемент не сразу получил признание и был взят на вооружение промышленниками.
Дело в том, что технологии того времени не позволяли обрабатывать столь тугоплавкое вещество, поэтому большинство современников не придали особого значения научному открытию.
Вольфрам был оценен гораздо позже. На сегодняшний день его сплавы используются при производстве термостойких деталей для различных отраслей промышленности. Нить накаливания в газоразрядных бытовых лампах также изготавливается из вольфрама.
Также он применяется в аэрокосмической промышленности для производства ракетных сопел, используется в качестве многоразовых электродов в газодуговой сварке.
Кроме тугоплавкости вольфрам также обладает высокой плотностью, что позволяет использовать его для изготовления высококачественных клюшек для гольфа.
Соединения вольфрама с неметаллами также широко применяется в промышленности. Так сульфид используется в качестве термостойкой смазки, способной переносить температуры до 500 градусов по Цельсию, карбид служит для изготовления резцов, абразивных дисков и сверл, способных обрабатывать самые твердые вещества и переносить высокие температуры нагрева. Рассмотрим, наконец, промышленное получение вольфрама. Самый тугоплавкий металл имеет температуру плавления 3422 градуса по Цельсию.
Как получают вольфрам?
В природе чистый вольфрам не встречается. Он входит в состав горных пород в виде триоксида, а также вольфрамитов железа, марганца и кальция, реже меди или свинца. По оценкам ученых содержание вольфрама в земной коре в среднем составляет 1,3 грамма на одну тонну.
Это достаточно редкий элемент по сравнению с другими видами металлов. вольфрама в руде после добычи обычно не превышает 2%.
Поэтому добытое сырье отправляется на обогатительные фабрики, где методом магнитной или электростатической сепарации массовая доля металла доводится до отметки 55-60%.
Процесс его получения разделяется на технологические этапы. На первом этапе выделяют чистый триоксид из добытой руды. Для этого используют метод термического разложения. При температурах от 500 до 800 градусов по Цельсию все лишние элементы расплавляются, а тугоплавкий вольфрам в виде оксида легко можно собрать из расплава. На выходе получается сырье с содержанием оксида шестивалентного вольфрама на уровне 99%.
Полученное соединение тщательно измельчают и проводят восстановительную реакцию в присутствии водорода при температуре 700 градусов по Цельсию. Это позволяет выделить чистый металл в виде порошка.
Далее его спрессовывают под высоким давлением и спекают в водородной среде при температурах 1200-1300 градусов по Цельсию.
После этого полученная масса отправляется в электрическую плавильную печь, где под воздействием тока нагревается до температуры свыше 3000 градусов. Так вольфрам переходит в расплавленное состояние.
Для окончательной очистки от примесей и получения монокристаллической структурной решетки используется метод зонной плавки. Он подразумевает, что в определенный момент времени расплавленной находится только некоторая зона из общей площади металла. Постепенно двигаясь, эта зона перераспределяет примеси, в результате чего в конечном итоге они скапливаются в одном месте и их легко можно удалить из структуры сплава.
Готовый вольфрам поступает на склад в виде штабиков или слитков, предназначенных для последующего производства нужной продукции. Для получения сплавов вольфрама все составные элементы измельчают и смешивают в виде порошка в необходимых пропорциях. Далее производится спекание и плавка в электрической печи.
Источник: https://promplace.ru/vidy-metallov-i-klassifikaciya-staty/samyi-tugoplavkii-metall-1551.htm
Наиболее тугоплавкий металл. Характеристика металлов
Металлы — это самый распространенный материал (наряду с пластмассами и стеклом), который применяется людьми с древних времен. Уже тогда человеку была известна характеристика металлов, он с выгодой использовал все их свойства для создания прекрасных произведений искусства, посуды, предметов быта, сооружений.
Одной из главных черт при рассмотрении этих веществ является их твердость и тугоплавкость. Именно эти качества позволяют определять область использования того или иного металла. Поэтому рассмотрим все физические свойства и особое внимание уделим вопросам плавкости.
Легкоплавкие и тугоплавкие металлы
Данный параметр является очень важным, когда речь заходит об областях применения рассматриваемых веществ. Тугоплавкие металлы и сплавы — это основа машино- и кораблестроения, выплавки и литья многих важный изделий, получения качественного рабочего инструмента. Поэтому знание температур плавления и кипения играет основополагающую роль.
Характеризуя металлы по прочности, можно разделить их на твердые и хрупкие. Если же говорить о тугоплавкости, то здесь выделяют две основные группы:
- Легкоплавкие — это такие, которые способны менять агрегатное состояние при температурах ниже 1000 оС. Примерами могут служить: олово, свинец, ртуть, натрий, цезий, марганец, цинк, алюминий и другие.
- Тугоплавкими считаются те, чья температура плавления выше обозначенной величины. Их не так много, а на практике применяется еще меньше.
Таблица металлов, имеющих температуру плавления свыше 1000 оС, представлена ниже. Именно в ней и располагаются самые тугоплавкие представители.
| Название металла | Температура плавления, оС | Температура кипения, оС |
| Золото, Au | 1064.18 | 2856 |
| Бериллий, Ве | 1287 | 2471 |
| Кобальт, Со |
Источник: https://FB.ru/article/182368/naibolee-tugoplavkiy-metall-harakteristika-metallov
Металлы с высокой температурой плавления
Точка плавления вещества — это температура, при которой оно переходит из твердого состояния в жидкое. Металлы обладают высокой температурой плавления, поскольку они существуют в твердой кристаллической форме. Металлы с высокой температурой плавления имеют сильные межмолекулярные силы между атомами. Силы электростатического притяжения между ионами металлов и свободными электронами создают прочные металлические связи с более прочными связями, что приводит к более высоким температурам плавления.
Огнеупорные металлы
Есть два принятых определения тугоплавких металлов.Один утверждает, что металл должен иметь температуру плавления выше 2200 ° C, в то время как другой утверждает, что все металлы с температурой плавления выше 1850 ° C считаются тугоплавкими металлами. В более широком смысле следующие 14 металлов классифицируются как тугоплавкие.
Металл | Точка плавления | Приложения |
Вольфрам (Вт) | 3420 ° С | Лампы накаливания, электроды сварочные, нагревательные элементы для печей |
Рений (Re) | 3180 ° С | Детали реактивных двигателей, легирование, нити для печей, рентгеновские аппараты |
Тантал (Ta) | 2966 ° С | Лопатки турбин двигателей, медицинские приборы, военные, полупроводники |
Молибден (Мо) | 2620 ° С | Покрытия, солнечные элементы, инструментальная и быстрорежущая сталь |
Ниобий (Nb) | 2468 ° С | Сверхпроводники, легирование стали, инструментальные стали, натриевые лампы |
Хром (Cr) | 1907 ° С | Легирование, покрытие, катализатор |
Гафний (Hf) | 2227 ° С | Управляющие стержни ядерных реакторов, легирование, микропроцессоры |
Иридий (Ir) | 2454 ° С | Отвердитель, легирование (особенно осмием), наконечники ручки, подшипники компаса |
Осмий (Os) | 3050 ° С | Легирование, иглы, наконечники ручек |
Родий (Rh) | 1960 ° С | Легирование, катализатор, украшения |
Рутений (Ру) | 2310 ° С | Солнечные элементы, легированные (особенно платиной и палладием), ювелирные изделия |
Титан (Ti) | 1668 ° С | Легирование, самолеты, корабли, гребные валы, теплообменники |
Ванадий (В) | 1910 ° С | Легирование (особенно сталью и титаном) |
Цирконий (Zr) | 1855 ° С | Реакторы ядерные, магниты (легированные ниобием), химическая промышленность |
Тугоплавкие металлы имеют узкоспециализированное применение, например, в осветительных приборах, инструментах, смазочных материалах и стержнях ядерной реакции.Их нельзя формовать, их можно обрабатывать только методом порошковой металлургии.
Лютеций, Лоуренсий и Протактиний также имеют высокие температуры плавления. Но они очень радиоактивны или имеют очень ограниченное применение и обычно не используются.
Для сравнения: температура плавления стали обычно находится в диапазоне 1370-1510 ° C (в зависимости от конкретного сплава). Сталь, конечно, не тугоплавкий металл, а сплав на основе железа, который иногда легируют тугоплавкими металлами, указанными выше.
Другие распространенные металлы с высокой температурой плавления
Следующие четыре металла являются наиболее часто используемыми металлами с высокими температурами плавления, но ниже 1850 ° C, и как таковые не считаются тугоплавкими металлами:
Палладий (Pd)
Палладий — блестящий серебристо-белый металл, плавящийся при 1555 ° C и имеющий плотность 12,02 г / см. 3 . Металл очень устойчив к коррозии на воздухе, но может потускнеть на влажном воздухе, содержащем серу. Он не имеет биологической роли и не токсичен.
Металл образуется как побочный продукт при переработке медных и никелевых руд. Он чрезвычайно пластичен и легко превращается в тонкий лист, используемый в декоративных целях или в качестве украшений.
Чаще всего используется при производстве автомобильных каталитических нейтрализаторов. Он также широко используется для обесцвечивания золота при изготовлении украшений из белого золота. Другие популярные применения включают стоматологию, керамические конденсаторы, изготовление электрических контактов и хирургических инструментов.
Скандий (Sc)
Скандий — серебристо-белый металл, плавящийся при 1541 ° C и имеющий плотность 3,0 г / см 3 . Это мягкий металл, который медленно меняет цвет на желтоватый или розоватый при контакте с воздухом из-за образования оксида скандия (Sc 2 O 3 ) на поверхности. Его биологическая роль неизвестна, но предполагается, что он является канцерогеном.
Скандий — главный элемент торвейтита, очень собираемого минерала, обнаруженного в Скандинавии. Скандий считается редкоземельным элементом, поскольку он имеет аналогичные химические свойства с другими редкоземельными элементами и содержится в тех же рудах.
Скандий увеличивает температуру рекристаллизации алюминия до более чем 600 ° C. Это намного выше температурного диапазона термообрабатываемых алюминиевых сплавов. Это мощный легирующий элемент, который значительно улучшает механические и физические характеристики алюминиевого сплава. Эти сплавы набирают популярность в авиационной и транспортной отраслях.
Железо (Fe)
Железо — серебристо-серый металл, плавящийся при 1535 ° C и имеющий плотность 7,87 г / см. 3 .Это пластичный мягкий металл, который относительно хорошо проводит тепло и электричество. В чистом виде он обладает высокой реакционной способностью и легко окисляется на воздухе с образованием красно-коричневых оксидов железа или ржавчины. Он известен своей биологической ролью и жизненно важен для функционирования живых организмов. Считается нетоксичным.
Железо получают путем плавки / восстановления железной руды (гематита и магнетита) в чушковый чугун, содержащий большое количество углерода и других примесей, в доменных печах при температуре около 2000 ° C с последующим удалением этих примесей.
Железо (вместе с его сплавами) — самый распространенный промышленный металл в мире. Большая часть производимого чугуна используется для производства различных марок стали. Добавление никеля, хрома, ванадия и вольфрама улучшает коррозионную стойкость, а добавление 3-5 мас.% Углерода создает недорогой сплав для труб и других неструктурных применений.
Иттрий (Y)
Иттрий — серебристо-белый металл, плавящийся при 1525 ° C и имеющий плотность 4,47 г / см 3 . Он в меру мягкий и пластичный.Он не имеет известной биологической роли, но может быть очень токсичным для людей и животных.
Металл получают восстановлением фторида иттрия кальциево-магниевым сплавом в дуговой печи при 1600 ° C, достаточном для плавления иттрия.
Иттрий часто используется в качестве легирующего элемента для повышения прочности алюминиевых и магниевых сплавов. Его оксид используется в качестве добавки к стеклу объектива камеры, чтобы сделать его термостойким и ударопрочным.
Какие элементы имеют самую высокую точку плавления в мире?
Какие элементы имеют самую высокую точку плавления?
Просмотры сообщений: 3155
Как мы все знаем, температура плавления — это температура, при которой вещество переходит из твердого состояния в жидкое.Некоторые из металлов имеют очень высокую температуру плавления, по крайней мере, 2000 градусов по Цельсию, а также обладают очень высокой физической прочностью. Эти металлы имеют обозначение тугоплавкие металлы . Ниобий, молибден , тантал , вольфрам и рений являются тугоплавкими металлами.
Какие элементы имеют самую высокую точку плавления?
Многие металлы обладают некоторыми важными характеристиками, включая твердость, пластичность, пластичность, предел прочности, плотность и температуру плавления, их свойства не могут быть продемонстрированы неметаллами.
Высокая температура плавления элементов обусловлена сильными межмолекулярными взаимодействиями между атомами. Металлы в основном участвуют в металлических связях, которые представляют собой электростатическую силу притяжения между ионами металлов и свободными электронами в их кристаллической решетке.
Вольфрам и молибден — самые распространенные жаропрочные металлы. Из-за их устойчивости к высоким температурам они используются в разнообразном оборудовании, например, в лампах.
Тантал, иридий, платина, золото, вольфрам, гафний и серебро — тяжелые металлы.Плотно упакованные металлические конструкции обладают высокой температурой плавления. Например, вольфрам — это металл класса с самой высокой температурой плавления . Итак, нить лампы накаливания сделана из вольфрама. Вольфрам плавится при чрезвычайно высоких температурах, составляющих 3380 градусов Цельсия, тогда как цезий имеет очень низкую температуру плавления 28,5 ° C.
Список элементов с высокой температурой плавления выглядит следующим образом:
| Элементы | Точки плавления |
| Cu | 1083 |
| Мн | 1245 |
| Be | 1278 |
| Ni | 1453 |
| Co | 1495 |
| Er | 1522 |
| Y | 1523 |
| Fe | 1535 |
| SC | 1539 |
| Pd | 1552 |
| Па | 1568 |
| Lr | 1627 |
| Лю | 1656 |
| Ti | 1660 |
| Чт | 1750 |
| Pt | 1772 |
| Zr | 1852 |
| Cr | 1857 |
| 1890 |
Спасибо, что прочитали нашу статью, и надеемся, что она будет вам полезна.Если вы хотите узнать больше об элементах, имеющих самую высокую температуру плавления, вы можете посетить Advanced Refractory Metals ( ARM ) для получения дополнительной информации.
со штаб-квартирой в Лейк-Форест, Калифорния, США, ARM является ведущим производителем и поставщиком тугоплавких металлов по всему миру, обеспечивая клиентов высококачественными тугоплавкими металлами, такими как вольфрам , молибден, тантал, рений, титан, и цирконий по очень конкурентоспособной цене.
17 металлов с наивысшими температурами плавления (и почему) — Материаловедение и инженерия
Знаете ли вы, что вольфрам плавится более чем на 3400 ° C (6200 ° F) выше, чем ртуть? Вольфрам — это металл с наивысшей температурой плавления, но почему для превращения вольфрама из твердого в жидкое требуется столько энергии?
Температура плавления материала в первую очередь связана с прочностью сцепления. Материалы с прочными связями между атомами будут иметь высокую температуру плавления.Однако другие факторы, такие как кристаллическая структура, атомный вес и электронная структура, также могут влиять на температуру плавления.
Но прежде чем мы погрузимся в статью, посвященную металлам, я хочу быстро отметить, что металлы не обязательно имеют самую высокую температуру плавления по сравнению с другими материалами.
Металлическое соединение определенно прочнее, чем соединение Ван-дер-Ваальса, но керамика (имеющая ионную или ковалентную связь) имеет еще более высокие температуры плавления! Графит, карбид гафния, карбид тантала и другие керамические материалы имеют даже более высокие температуры плавления, чем вольфрам!
Список металлов с высокой температурой плавления
Прежде чем я перейду к научному объяснению, вот список тех 17 элементарных металлов с наивысшими температурами плавления.(Я также перечислил кристаллическую структуру, которая появится позже). Как видите, вольфрам занимает первое место с удивительной температурой плавления 3380 ° C.
- Вольфрам (Вт)
3380 ° C, BCC - Рений (Re)
3180 ° C, HCP - Осмий (Os)
3027 ° C, HCP - Тантал (Ta)
3014 ° C, BCC - Молибден (Mo)
2617 ° C, BCC - Ниобий (Nb)
2468 ° C, BCC - Иридий (Ir)
2447 ° C, FCC Рутений (Ru) - Гафний (Hf)
2227 ° C, HCP - Технеций (Tc)
2200 ° C, HCP, Радиоактивный - Родий (Rh)
1963 ° C, FCC - Ванадий (V)
1902 ° C, BCC - Хром (Cr)
1857 ° C, BCC - Цирконий (Zr)
1852 ° C, HCP - Платина (Pt)
1769 ° C, FCC - Торий (Th)
1755 ° C, FCC, радиоактивный - Титан (Ti)
1670 ° C, HCP
2250 ° C, HCP
Сплавы с высокой температурой плавления
Сплавы с высокой температурой плавления на самом деле не относятся к категории материалов.Каждый раз, когда вы объединяете металлы в твердый раствор (т.е. делаете сплав), температура плавления будет снижаться.
Если вам нужен металл с высокой температурой плавления, вам, вероятно, придется выбирать чистый металл. Во многих случаях вам, вероятно, удастся избежать легкого легирования одним из чистых элементов, перечисленных выше, но на самом деле невозможно разработать сплавы с повышенной температурой плавления.
«Жаропрочные» сплавы — это настоящая категория в материаловедении. В большинстве случаев материалы выходят из строя при высоких температурах еще до того, как они расплавятся.Высокие температуры делают металлы более мягкими и более подверженными окислению или коррозии.
Эта статья посвящена исключительно явлению металлов с высокими температурами плавления, но суперсплавы (на основе Ni, Co или Fe, 1300-1500 ° C в верхнем диапазоне), титановые сплавы и вольфрамовые сплавы могут считаться жаропрочными сплавами. благодаря сочетанию высокой температуры плавления, хорошей прочности при высоких температурах и стойкости к окислению / коррозии
В чем причина высоких точек плавления?
Простой ответ: энергия связи.
Твердое тело можно представить как группу связанных вместе атомов, которые колеблются взад и вперед, но обычно остаются в одном и том же положении.
Колебание атомов — их кинетическая энергия — это то, что мы обычно называем температурой. Более высокая температура означает, что атомы вибрируют быстрее. В какой-то момент они так быстро вибрируют, что могут порвать свои узы и проскользнуть мимо друг друга.
У каждого атома своя вибрация, поэтому даже в твердом состоянии есть некоторые атомы, которые могут временно разрывать свои связи и перемещаться через материал.Это явление называется «диффузией».
«Таяние» — это когда большая часть облигаций разрывается. В кристаллических твердых телах, таких как металлы, все связи имеют одинаковую длину и силу, поэтому есть точная точка, в которой почти все атомы получают достаточно тепловой энергии, чтобы разорвать свои связи. Чем больше энергии требуется для достижения этой точки, тем выше температура плавления.
Так когда же атомы достигают этой точки?
Наиболее очевидный фактор — это прочность прямого соединения. Прочность связи немного сложно определить количественно, но двумя показателями прочности связи являются энтальпия образования , которая представляет собой изменение энтальпии для образования моля материала, и энергия диссоциации связи , которая представляет собой энергию, высвобождаемую при разрыве связь между двумя атомами.
В таблице энергий связей Каллистера учебник фактически представляет таблицу энтальпии образования. Вот график прочности связи (представленной энтальпией образования И энергией диссоциации связи) по сравнению с температурой плавления.
Есть еще несколько свойств, которые влияют на точку плавления, но не учитываются в энтальпии образования или энергии диссоциации связи. Например: сколько связей окружает атом?
В целом, мы считаем, что большинство эффектов от связей являются результатом ближайших соседей атома или тех, которые непосредственно «касаются» его.(Хотя есть эффект и от соседних атомов — например, если вы делаете наночастицы всего с несколькими атомами вместе, связи меньше, чем обычно, и наночастица будет иметь более низкую температуру плавления, чем объемный материал).
Кристаллическая структура элемента определяет длину связи и количество ближайших соседей (также называемое «координационным числом»). Это влияет на прочность связи таким образом, что она не улавливается энергией диссоциации связи, но отражается на температуре плавления.
Вот почему элементы с высокими температурами плавления обычно имеют кристаллическую структуру с высокой степенью упаковки: FCC, HCP или BCC. Фактически, элементы с самой высокой температурой плавления обычно имеют структуру ОЦК. BCC почти плотно упакован, поэтому он довольно стабилен, но я полагаю, что немного более низкая плотность позволяет атомам больше шевелиться, не разжижаясь. Чтобы получить (очень сложное) математическое доказательство того, почему ОЦК имеет тенденцию быть наиболее стабильной высокотемпературной фазой, ознакомьтесь с этой статьей Александра и МакТага.
Поскольку металлическая связь означает, что атомы окружены морем электронов, существует также несколько характеристик электронной структуры атома, которые также могут влиять на прочность связи, измеренную путем плавления.
Например, вы заметите, что многие металлы с высокими температурами плавления имеют частично полные d-суборбитали.
Это означает, что у этих атомов есть много электронов, которые вносят вклад в море электронов, обычно увеличивая силы взаимодействия в металле.
Более крупные атомы также имеют тенденцию быть более плотно упакованными и весят больше. Поскольку кинетическая энергия равна, более тяжелые атомы будут колебаться медленнее при той же температуре, что и более легкий атом. Более медленные колебания означают, что у атомов будет больше времени для взаимодействия друг с другом, что также может способствовать повышению температуры плавления.
Каковы общие свойства металлов с высокой температурой плавления?
Поскольку я выбрал 17 элементов с наивысшей температурой плавления, эти элементы весьма разнообразны.Их температуры плавления колеблются от 1670 ° C до 3380 ° C, поэтому у них нет ничего общего.
Однако все они имеют кристаллические структуры BCC, HCP или FCC, которые являются наиболее плотно упакованными и наиболее стабильными кристаллическими структурами.
Металлы из моего списка с наивысшей температурой плавления также тугоплавкие металлы . Это особый вид металла с определенным набором свойств. Вы можете прочитать все о тугоплавких металлах в этой статье, но вкратце их:
- Плотный
- Твердый (особенно вольфрам и рений)
- Химически инертный
- Легко окисляемый
- Устойчивый к ползучести
Тугоплавкие металлы также имеют кристаллическую структуру BCC (за исключением рения, который является HCP).
Применение металлов с высокой температурой плавления
Для многих областей применения требуются металлы с высокой температурой плавления. Для таких применений, как нити накаливания ламп накаливания, где требуется только металл с высокой температурой плавления и ничего больше, обычно выбирают вольфрам.
Вольфрам — металл с самой высокой температурой плавления. Кроме того, он относительно дешев, поэтому нет никаких аргументов в пользу использования «более дешевого» металла с немного более низкой температурой плавления.Такие элементы, как рений, тантал и молибден, обычно используются, потому что они обладают некоторыми другими свойствами в дополнение к высокой температуре плавления (например, более низкой плотностью).
Вольфрам (Вт)Металл, который может выдерживать самые высокие температуры, также не особенно дорогой, поэтому вольфрам — лучший металл для высокотемпературных применений, таких как накаливания ламп , сварочные электроды , и нагревательные элементы печи .
Рений (Re)Используется в суперсплавах для реактивных двигателей для замедления диффузии (в основном для этой цели используется 70% извлеченного рения ). Это редкий / дорогой элемент, поэтому он редко используется в качестве основного основного металла в сплаве.
Осмий (Os)На самом деле, его применение почти не имеет ничего общего с его высокой температурой плавления, потому что оксид осмия очень токсичен. Однако он может быть чрезвычайно твердым / износостойким при обычных температурах — например, вы могли использовать сплав осмия и иридия для наконечников перьевых ручек.
Тантал (Ta)Тантал используется для изготовления жаропрочных, устойчивых к коррозии сплавов, таких как те, которые используются в деталях вакуумных печей .
Молибден (Mo)Как и многие другие материалы в его списке, молибден в основном используется для сплава с другими металлами. Он находит широкое применение в суперсплавах для реактивных двигателей. Это полезный легирующий элемент, поскольку он относительно легкий. Mo и Nb имеют наилучшее сочетание низкой плотности и высокой температуры плавления.
Ниобий (Nb)Ниобий — элемент, используемый в суперсплавах. Сплавы на основе ниобия также используются в аэрокосмической технике в качестве материалов для сопел двигателей жидких ракет.
Иридий (Ir)Свечи зажигания на основе иридия используются в авиации. Он в основном используется в приложениях, связанных с электроникой.
Рутений (Ru)Когда дело доходит до высокотемпературных применений, рутений используется в качестве легирующей добавки к суперсплавам.Рутений также может быть сплавлен с платиной для повышения износостойкости платины без потери других свойств платины.
Гафний (Hf)Как и многие другие материалы в этом списке, гафний в основном используется для сплава с другими металлами, такими как Fe, Ti, Nb, Ta и другими. Сплав C103, состоящий из Nb (89%), Hf (10%) и Ti (1%), использовался в соплах жидкостных ракетных двигателей маршевого двигателя Apollo Lunar Modules. Иногда его добавляют в суперсплавы на основе никеля для улучшения адгезии защитных оксидных слоев.
Технеций (Tc)Технеций радиоактивен, что как бы ограничивает его применение. Однако его можно использовать для получения медицинских радиоактивных изображений, а также его можно легировать сталью для повышения коррозионной стойкости. Вам просто нужно убедиться, что эта сталь находится в месте, недоступном для людей!
Родий (Rh)Родий — благородный металл, который редко вступает в реакцию с другими химическими веществами, что может сделать его хорошим катализатором. Как и Pt, Rh используется для проводов, которые могут подвергаться воздействию горячей / коррозионной среды.Pt может выдерживать высокие температуры и коррозию без легирования , что позволяет ей сохранять свою электропроводность. Родий даже реже платины.
Ванадий (V)Ванадий используется в реактивных двигателях в качестве легирующей добавки к техническому титановому сплаву (Ti-6Al-4V). Один сплав на основе ванадия (V-4Cr-4Ti) является многообещающим кандидатом для использования в будущих термоядерных реакторах
. Хром (Cr)Хотя хром имеет высокую температуру плавления, он более известен своей низкой плотностью и стойкостью к окислению.Cr является основным легирующим элементом (помимо железа) в нержавеющей стали, и он легируется в турбинах из суперсплавов. Даже если жаропрочные сплавы не содержат непосредственно Cr, они могут иметь тонкое покрытие из сплава Cr для стойкости к окислению.
Цирконий (Zr)Когда дело доходит до высокотемпературных применений, цирконий широко используется в форме оксида циркония. YSZ — ZrO 2 -8 мас.% Y 2 O 3 (так называемый оксид циркония, стабилизированный иттрием) — широко используемое защитное покрытие, целью которого является повышение максимальной рабочей температуры суперсплавов, используемых в реактивных двигателях.
Платина (Pt)Платина — благородный металл, который редко вступает в реакцию с другими химическими веществами, что может сделать его хорошим катализатором. Среди высокотемпературных применений Pt используется для проводов, которые могут подвергаться воздействию горячей / коррозионной среды. Pt может выдерживать высокие температуры и коррозию без легирования , что позволяет ей сохранять свою электропроводность.
Торий (Th)Торий радиоактивен. Тем не менее, торий (диоксид тория) имеет самую высокую температуру плавления из всех известных оксидов — 3300 ° C.Таким образом, он может оставаться твердым в пламени и использоваться в газовых оболочках.
Титан (Ti)Титан применяется в компрессорах реактивных двигателей (Ti-6Al-4V).
Последние мысли
Вот и все! 17 металлов с самой высокой температурой плавления — вообще говоря, потому что у них самые прочные связи.
Определенная подгруппа этой группы с наивысшими температурами плавления, такая как вольфрам, рений и тантал, называется тугоплавкими металлами .Вы можете прочитать все о тугоплавких металлах, щелкнув эту статью!
Ссылки и дополнительная литература
Для (очень сложного) математического доказательства того, почему BCC является наиболее стабильной высокотемпературной фазой, ознакомьтесь с этой статьей Александра и МакТага.
В этой статье мы нашли информацию о корреляции между энергией связи и температурой плавления для разных элементов.
Энергии диссоциации связи для различных элементов были взяты из этой статьи.
Узнайте о тугоплавких металлах
Термин «тугоплавкий металл» используется для описания группы металлических элементов, которые имеют исключительно высокие температуры плавления и устойчивы к износу, коррозии и деформации.
В промышленности термин тугоплавкий металл чаще всего относится к пяти наиболее часто используемым элементам:
Однако более широкие определения также включали менее часто используемые металлы:
Характеристики
Отличительной чертой тугоплавких металлов является их термостойкость.Все пять промышленных тугоплавких металлов имеют температуру плавления выше 3632 ° F (2000 ° C).
Прочность тугоплавких металлов при высоких температурах в сочетании с их твердостью делает их идеальными для режущих и сверлильных инструментов.
Тугоплавкие металлы также очень устойчивы к тепловому удару, а это означает, что повторное нагревание и охлаждение нелегко вызвать расширение, напряжение и растрескивание.
Все металлы имеют высокую плотность (они тяжелые), а также хорошие электрические и теплопроводные свойства.
Еще одним важным свойством является их сопротивление ползучести, склонность металлов к медленной деформации под действием напряжения.
Благодаря своей способности образовывать защитный слой тугоплавкие металлы также устойчивы к коррозии, хотя они легко окисляются при высоких температурах.
Огнеупорные металлы и порошковая металлургия
Из-за их высоких температур плавления и твердости тугоплавкие металлы чаще всего обрабатываются в виде порошка и никогда не производятся путем литья.
Металлические порошки изготавливаются определенного размера и формы, затем смешиваются для создания правильного сочетания свойств перед уплотнением и спеканием.
Спекание включает нагрев металлического порошка (в форме) в течение длительного периода времени. Под действием тепла частицы порошка начинают связываться, образуя твердую деталь.
Спекание может связывать металлы при температурах ниже их точки плавления, что является значительным преимуществом при работе с тугоплавкими металлами.
Карбидные порошки
Одно из первых применений многих тугоплавких металлов возникло в начале 20 века с разработкой цементированных карбидов.
Widia , первый коммерчески доступный карбид вольфрама, был разработан Osram Company (Германия) и поступил на рынок в 1926 году. Это привело к дальнейшим испытаниям с такими же твердыми и износостойкими металлами, что в конечном итоге привело к разработке современных спеченных карбидов.
Для изделий из карбидных материалов часто используются смеси различных порошков.Этот процесс смешивания позволяет вводить полезные свойства различных металлов, тем самым создавая материалы, превосходящие то, что можно было бы создать из отдельного металла. Например, исходный порошок Widia состоял на 5-15% из кобальта.
Примечание. Подробнее о свойствах тугоплавких металлов см. В таблице внизу страницы.
Приложения
Сплавы и карбиды на основе тугоплавких металлов используются практически во всех основных отраслях промышленности, включая электронику, аэрокосмическую, автомобильную, химическую, горнодобывающую промышленность, ядерные технологии, обработку металлов и протезирование.
Следующий список конечного использования тугоплавких металлов был составлен Ассоциацией тугоплавких металлов:
Металлический вольфрам
- Нити накаливания для ламп накаливания, люминесцентных и автомобильных ламп
- Аноды и мишени для рентгеновских трубок
- Semiconductor поддерживает
- Электроды для дуговой сварки в инертном газе
- Катоды большой емкости
- Электроды для ксенона ламповые
- Автомобильные системы зажигания
- Сопла реактивные
- Излучатели электронные ламповые
- Тигли для переработки урана
- Нагревательные элементы и радиационные экраны
- Легирующие элементы в сталях и суперсплавах
- Армирование металломатричных композитов
- Катализаторы химических и нефтехимических процессов
- Смазочные материалы
молибден
- Легирующие добавки в чугуны, стали, нержавеющие стали, инструментальные стали и суперсплавы на основе никеля
- Шлифовальные шпиндели высокоточные
- Распылительная металлизация
- Плашки для литья под давлением
- Детали ракет и ракетных двигателей
- Электроды и стержни для перемешивания в производстве стекла
- Нагревательные элементы электропечи, лодки, тепловые экраны и футеровка глушителя
- Насосы, желоба, клапаны, мешалки и термопары для рафинирования цинка
- Производство стержней управления ядерными реакторами
- Электроды переключатели
- Опоры и подложки для транзисторов и выпрямителей
- Нити накаливания и опорные тросы для автомобильных фар
- Геттеры для вакуумных трубок
- Юбки, конусы и тепловые экраны ракет
- Компоненты ракет
- Сверхпроводники
- Химико-технологическое оборудование
- Теплозащитные экраны в высокотемпературных вакуумных печах
- Легирующие добавки в ферросплавы и сверхпроводники
Карбид вольфрама цементированный
- Карбид вольфрама цементированный
- Инструмент режущий для обработки металлов
- Оборудование для атомной энергетики
- Инструмент для горного и нефтяного бурения
- Плашки формовочные
- Валки для формовки металла
- Нитенаправители
Вольфрамовый тяжелый металл
- Втулки
- Седла клапана
- Лезвия для резки твердых и абразивных материалов
- Наконечники для шариковой ручки
- Пилы и сверла по камню
- Хэви-метал
- Щиты радиационные
- Противовесы самолетов
- Противовес для часов с автоподзаводом
- Механизмы балансировки аэрофотоаппарата
- Противовесы лопастей несущего винта вертолета
- Золотые вставки для булав
- Корпуса дротиков
- Взрыватели вооружения
- Гашение колебаний
- Военная артиллерия
- Пулизы для дробовика
Тантал
- Конденсаторы электролитические
- Теплообменники
- Нагреватели байонетные
- Колодцы для термометров
- Нити для вакуумных трубок
- Химико-технологическое оборудование
- Комплектующие для высокотемпературных печей
- Тигли для работы с жидким металлом и сплавами
- Режущие инструменты
- Компоненты аэрокосмических двигателей
- Имплантаты хирургические
- Добавка в суперсплавы
Физические свойства тугоплавких металлов
| Тип | Установка | Пн | Ta | Nb | Вт | правый | Zr |
| Типичная коммерческая чистота | 99.95% | 99,9% | 99,9% | 99,95% | 99,0% | 99,0% | |
| Плотность | см / куб.см | 10,22 | 16,6 | 8,57 | 19,3 | 21,03 | 6,53 |
| фунтов / дюйм 2 | 0,369 | 0.60 | 0,310 | 0,697 | 0,760 | 0,236 | |
| Точка плавления | Цельсия | 2623 | 3017 | 2477 | 3422 | 3180 | 1852 |
| ° F | 4753.4 | 5463 | 5463 | 6191,6 | 5756 | 3370 | |
| Температура кипения | Цельсия | 4612 | 5425 | 4744 | 5644 | 5627 | 4377 |
| ° F | 8355 | 9797 | 8571 | 10 211 | 10 160,6 | 7911 | |
| Типичная твердость | DPH (Виккерс) | 230 | 200 | 130 | 310 | – | 150 |
| Теплопроводность (при 20 ° C) | кал / см 2 / см ° C / сек | – | 0.13 | 0,126 | 0,397 | 0,17 | – |
| Коэффициент теплового расширения | ° C x 10 -6 | 4,9 | 6,5 | 7,1 | 4,3 | 6,6 | – |
| Удельное электрическое сопротивление | Микроом-см | 5,7 | 13,5 | 14,1 | 5,5 | 19,1 | 40 |
| Электропроводность | % МАКО | 34 | 13.9 | 13,2 | 31 | 9,3 | – |
| Предел прочности (KSI) | Окружающий | 120-200 | 35-70 | 30-50 | 100-500 | 200 | – |
| 500 ° С | 35-85 | 25-45 | 20-40 | 100-300 | 134 | – | |
| 1000 ° С | 20-30 | 13-17 | 5-15 | 50-75 | 68 | – | |
| Минимальное удлинение (калибр 1 дюйм) | Окружающий | 45 | 27 | 15 | 59 | 67 | – |
| Модуль упругости | 500 ° С | 41 | 25 | 13 | 55 | 55 | |
| 1000 ° С | 39 | 22 | 11.5 | 50 | – | – |
Источник: http://www.edfagan.com
вольфрам | Использование, свойства и факты
Возникновение, свойства и использование
Количество вольфрама в земной коре оценивается в 1,5 частей на миллион, или примерно 1,5 грамма на тонну породы. Китай — доминирующий производитель вольфрама; в 2016 году он произвел более 80 процентов всего добытого вольфрама и содержал почти две трети мировых запасов.Вьетнам, Россия, Канада и Боливия производят большую часть остатка. Вольфрам не встречается в виде свободного металла. Он примерно так же богат, как олово или молибден, на которые он похож, и вдвое меньше, чем уран. Хотя вольфрам встречается в виде вольфрама-дисульфида вольфрама, WS 2 , наиболее важными рудами в данном случае являются вольфраматы, такие как шеелит (вольфрамат кальция, CaWO 4 ), столзит (вольфрамат свинца, PbWO 4 ) и вольфрамит. — твердый раствор или смесь или оба изоморфных веществ вольфрамат двухвалентного железа (FeWO 4 ) и марганцевый вольфрамат (MnWO 4 ).
Для вольфрама руды концентрируются с помощью магнитных и механических процессов, а затем концентрат плавится с щелочью. Неочищенные расплавы выщелачивают водой с получением растворов вольфрамата натрия, из которых при подкислении осаждается водный триоксид вольфрама, а затем оксид сушат и восстанавливают до металла водородом.
Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишитесь сейчасВольфрам довольно устойчив к воздействию кислот, за исключением смесей концентрированной азотной и плавиковой кислот, и он может быстро подвергаться воздействию щелочных окисляющих расплавов, таких как плавленые смеси нитрата калия и гидроксида натрия или пероксида натрия; водные щелочи, однако, не действуют.Он инертен по отношению к кислороду при нормальной температуре, но легко соединяется с ним при нагревании красного цвета с образованием триоксидов и подвергается действию фтора при комнатной температуре с образованием гексафторидов.
Металлический вольфрам имеет блеск от никелево-белого до сероватого цвета. Среди металлов он имеет самую высокую температуру плавления при 3410 ° C (6170 ° F), самую высокую прочность на разрыв при температурах более 1650 ° C (3002 ° F) и самый низкий коэффициент линейного теплового расширения (4,43 × 10 ). −6 на 1 ° C при 20 ° C [68 ° F]).Вольфрам обычно хрупкий при комнатной температуре. Однако чистый вольфрам можно сделать пластичным путем механической обработки при высоких температурах, а затем из него можно получить очень тонкую проволоку. Вольфрам сначала был коммерчески использован в качестве материала нити накала лампы, а затем использовался во многих электрических и электронных устройствах. Он используется в форме карбида вольфрама для изготовления очень твердых и вязких штампов, инструментов, калибров и бит. Много вольфрама идет на производство вольфрамовых сталей, а некоторые из них использовались в аэрокосмической промышленности для изготовления горловин сопел ракетных двигателей и поверхностей входа на переднюю кромку.(Для получения информации о добыче, извлечении и применении вольфрама, см. обработка вольфрама.)
Природный вольфрам представляет собой смесь пяти стабильных изотопов: вольфрама-180 (0,12 процента), вольфрама-182 (26,50 процента), вольфрама-183 (14,31 процента), вольфрама-184 (30,64 процента) и вольфрама-186 (28,43 процента). ). Кристаллы вольфрама изометричны и, как показывает рентгеноструктурный анализ, имеют объемно-центрированную кубическую форму.
Соединения
Вольфрам относительно инертен с химической точки зрения.Однако были получены соединения, в которых элемент имеет степень окисления от 0 до +6. Состояния выше +2, особенно +6, являются наиболее распространенными. В состояниях +4, +5 и +6 вольфрам образует множество комплексов.
Наиболее важным соединением вольфрама является карбид вольфрама (WC), который отличается своей твердостью (9,5 по шкале Мооса, где максимум, алмаз, равен 10). Он используется отдельно или в сочетании с другими металлами для придания износостойкости чугуну и режущим кромкам пил и сверл.Вольфрам также образует твердые, тугоплавкие и химически инертные межузельные соединения с бором, азотом и кремнием при прямой реакции с этими элементами при высоких температурах.
Производство и анализ высокопроизводительных тугоплавких высокоэнтропийных сплавов с помощью селективной лазерной плавки (SLM)
Материалы (Базель). 2019 Март; 12 (5): 720.
Поступила 24.01.2019; Принято 22 февраля 2019 г.
Лицензиат MDPI, Базель, Швейцария. Эта статья представляет собой статью в открытом доступе, распространяемую в соответствии с условиями лицензии Creative Commons Attribution (CC BY) (http: // creativecommons.org / licenses / by / 4.0 /). Эту статью цитировали в других статьях в PMC.Реферат
Тугоплавкие высокоэнтропийные сплавы (ВЭА) обладают превосходными механическими свойствами, которые могут сделать их заменителями некоторых суперсплавов. Однако высокая температура плавления огнеупорных HEA приводит к проблемам обработки при использовании традиционных методов обработки. В данной работе единый твердый раствор ОЦК сплава NbMoTaW был сформирован методом селективного лазерного плавления (SLM) с линейной плотностью энергии до 2.83 Дж / мм. Распределение состава было проанализировано, и элемент с более низкой температурой плавления и меньшей плотностью показал отрицательное отклонение (не более 5%) мольного соотношения в сформированном сплаве. HEA показывает превосходную микроструктуру, микротвердость и коррозионную стойкость по сравнению с традиционными суперсплавами, что делает его новым металлом-заменителем с большими перспективами применения в аэрокосмической и энергетической областях.
Ключевые слова: аддитивное производство, высокоэнтропийный сплав (ВЭА), селективное лазерное плавление (SLM), микроструктура, суперсплавы
1.Введение
«Суперсплав» — это общее название сплавов на основе железа, никеля и кобальта, учитывая их высокую износостойкость, ползучесть и усталостную прочность при высоких температурах. Они широко используются в авиационной, аэрокосмической, автомобильной и химической промышленности, работая в условиях высоких температур (≤ 1100 ° C). Однако в условиях сверхвысоких температур до 1500 ° C и 3000 ° C традиционные сверхсплавы бессильны. Вместо этого новый тип тугоплавких высокоэнтропийных сплавов (ВЭА) показал свои преимущества.Сплавы с высокой энтропией или многоэлементные сплавы в общих чертах определяются как сплавы твердых растворов, которые содержат более пяти основных элементов в равных или почти равных атомных процентах (ат.%) [1,2,3]. HEA обычно обладают неожиданными свойствами, такими как высокая прочность, высокая твердость, отличное сопротивление размягчению, а также износостойкость и коррозионная стойкость [4,5,6,7,8,9]. В соответствии с эффектами коктейля HEA, свойства сплава можно регулировать путем изменения состава и легирования [4,5,10]. В сочетании с высокотемпературными элементами, HEA будут обладать превосходными свойствами, такими как высокая температура плавления, что соответствует требованиям, предъявляемым к высокотемпературным несущим конструкциям и системам тепловой защиты для аэрокосмической техники.Следовательно, HEA можно рассматривать как потенциальные заменители сверхсплавов. Соответственно, Сеньков и другие [11,12] приготовили тугоплавкий HEA с объемноцентрированной кубической (ОЦК) структурой с почти эквиатомными концентрациями, используя NbMoTaW, который был получен вакуумной дуговой плавкой. Предел текучести этого тугоплавкого HEA составлял 1058 МПа при комнатной температуре и 405 МПа при 1600 ° C, что выше, чем температура плавления большинства существующих суперсплавов на основе никеля. Этот огнеупорный HEA может иметь многообещающие применения во многих областях, таких как аэрокосмическая, морская и энергетическая.
Однако пластичность HEA NbMoTaW при комнатной температуре низкая. Более того, полное смешение элементов в огнеупорных HEA все еще остается проблемой. Чтобы добиться равномерного распределения элементов в сплаве, кнопки обычно переплавляют четыре раза и переворачивают для каждой плавки вакуумно-дуговой плавкой [11,12]. Низкая пластичность при комнатной температуре и высокая прочность огнеупорных HEA делают их очень трудными для обработки [13]. Между тем, температура плавления также слишком высока для производства традиционной термической формовкой, такой как литье по выплавляемым моделям.Для процесса литья самая высокая температура плавления составляет всего 1800 ° C, что далеко не достаточно для сплава NbMoTaW в этом исследовании. Кроме того, хотя дуговое плавление может доходить до точки плавления, этот метод не может формировать произвольную форму.
Селективное лазерное плавление (SLM) — это технология изготовления слоев на основе порошкового слоя, с помощью которой можно напрямую изготавливать металлические детали в соответствии с трехмерными (3D) данными компьютерного проектирования (CAD) путем выборочного плавления последовательных слоев металлических порошков [ 9,13].SLM — это сложный процесс, при котором в каждом цикле лазерного импульса выделяется высокая плотность энергии, а тепло постоянно рассеивается по-разному. Передача тепла происходит не только между твердым телом, жидкостью и газом, но также включает взаимодействия между плазмой, электронами и фотонами. показывает простую сводку температурных режимов во время процесса SLM-сканирования. Фактически, существует несколько методов отвода тепла, в том числе отвод тепла за счет излучения плазмы, отраженного света, излучения, фазового перехода, тепловой конвекции и теплопроводности.Иногда брызги частиц также отводят тепло непосредственно из системы.
Процесс рассеивания тепла при селективном лазерном плавлении (SLM).
По сравнению с традиционным производством, SLM позволяет изготавливать трехмерные детали сложной формы без инструментов и пресс-форм. Таким образом, SLM имеет много преимуществ, особенно при обработке тугоплавких металлических материалов. Во время процесса только очень небольшой объем материала нагревается лазером за короткое время взаимодействия; поэтому температура ванны расплава может мгновенно достигать нескольких тысяч градусов, а процесс SLM имеет очень высокие скорости охлаждения, что способствует образованию твердых растворов в HEA и по-прежнему формирует зерна на заключительной стадии.Фактически, были проведены некоторые исследования [14,15,16,17,18,19] для получения HEA непосредственно с помощью лазера. Zhang et al. [14] синтезировали огнеупорное ВЭА покрытие с составом, близким к TiZrNbWMo, на стали C45 методом лазерной наплавки. Al 0,3 CoCrFeNi HEA был изготовлен методом прямого лазерного изготовления Джозефом и др. [15], которые показали, что материалы демонстрируют значительную асимметрию растяжения / сжатия в скорости деформационного упрочнения и пластичности сплава. Кунсе и другие [16,17] синтезировали два HEA, ZrTiVCrFeNi и TiZrNbMoV, из смеси элементных порошков, близких к эквимолярному соотношению, с использованием лазерной технологии формирования сетки (LENS), и оба сплава показали двухфазную структуру, а также водородную структуру. емкость накопителя.
Однако производство NbMoTaW HEA по-прежнему является серьезной проблемой для традиционной горячей обработки. Примечательно, что исследований по приготовлению огнеупорного HEA с помощью SLM проводилось очень мало. Поэтому в данной работе мы исследовали смешиваемость и затвердевание огнеупорного ВЭА NbMoTaW, синтезированного методом SLM, а также провели анализ образцов на элементный анализ, микротвердость и коррозионную стойкость.
2. Материалы и методы
NbMoTaW HEA был изготовлен из смешанных многоэлементных порошков.Порошки Nb (99,9%), Mo (99,9%), Ta (99,9%) и W (99,9%) были взвешены с номинальным составом в равных атомных процентах соответственно. Форма зерен порошка была сферической или почти сферической. Частицы смешивали с массовым соотношением м w : м Ta : м Mo : м Nb 184: 181: 96: 93, а затем порошки механически измельчали в планетарной шаровой мельнице KQM-X / B в течение 2 часов и сушили при 45 ° C в течение 8 часов.
В эксперименте процесс SLM проводился с использованием оборудования FORWEDO LM120 с волоконным лазером P L (максимальная мощность лазера) 500 Вт в защитной атмосфере аргона с количеством кислорода менее 20 ppm. Подложка представляла собой пластину из стали С45 размером 50 мм × 50 мм × 20 мм. Изготовленная модель образца представляла собой кубоид размером около 10 мм × 10 мм × 0,5 мм.
Основными параметрами процесса SLM являются скорость лазерного сканирования ( v ), расстояние штриховки ( ds ), толщина слоя ( dz ), коэффициент мощности лазера ( f p ) и лазерное пятно. диаметр ( d L ).Температура плавления NbMoTaW выше, чем у большинства обычных металлических сплавов. Следовательно, для полного расплавления смешанного порошка и формирования HEA в достаточной степени важна надлежащая более высокая подводимая энергия с комбинацией мощности лазера и скорости сканирования. Исходные параметры были выбраны следующим образом: ds был 0,1 мм, dz 0,1 мм, f p 0,8 и v 250 мм / с, с S-образным поперечным сканированием в x и y. направления.Для изготовления деталей NbMoTaW HEA требуется более высокая плотность энергии, поэтому был дополнительный процесс переплава, который имел те же параметры, что и исходный процесс, но подвергался двойному переплавлению для каждого слоя, что означает, что было в 3 раза больше энергии лазера. Таким образом, исходный процесс с линейной плотностью энергии 0,943 Дж / мм в соответствии с уравнением (1) и стратегия сканирования проиллюстрированы на.
где ρQ — линейная плотность энергии, n — количество циклов переплавки, а A mix — скорость лазерного поглощения смешанного порошка.
Образцы для испытаний состава, обозначенные как S1, S2 и S3, были изготовлены методом переплавки. Впоследствии образцы были вырезаны, и их поверхность подверглась дальнейшему анализу. Морфологию микроструктур на поверхности образцов наблюдали в сканирующем электронном микроскопе (SEM) HITACHI SU-8010 (Hitachi, Япония, Токио), а эксперименты по элементному анализу проводили с помощью энергодисперсионного спектрометра (EDS). Кристаллическую структуру идентифицировали с помощью рентгеновского дифрактометра D8 (XRD,) с мишенью из Cu (λ = 1.54 Å). Размер частиц анализировали с помощью лазерного дифракционного анализатора размера частиц Mastersizer 2000 (Малверн, Великобритания) и исследовали средний размер частиц.
Скорость абсорбции ( A ) порошка была измерена косвенно. Впоследствии A порошка для волоконного лазера исследовали путем тестирования отражательной способности ( R ) элементов. Можно предположить, что пропускание лазера не происходит в металлических порошках, и соотношение между поглощением и отражением металла составляет A = 1– R [20].Коэффициент отражения порошка измеряли в системе Avantes Co., Нидерланды. Размер зерен и дендритов рассчитывали по стандартной справке [21].
Кроме того, предполагается, что этот материал будет в основном использоваться в области морской техники; таким образом, он должен противостоять коррозии морской водой, что было проверено в этом исследовании. Поэтому для получения потенциодинамических поляризационных кривых для изучения коррозионной стойкости NbMoTaW HEA были проведены трехэлектродные электрохимические испытания на коррозию для HEA и нержавеющей стали 316 L с массовой долей 3.5% -ный раствор NaCl. Образцы из HEA и стали 316 L в качестве рабочего электрода вырезали на квадрат 6 мм × 6 мм. Затем поверхности рисунков были покрыты непроводящей смолой, и осталась только одна поверхность. Кроме того, в качестве электрода сравнения использовался каломельный электрод, а в качестве вспомогательного электрода — платиновая пластина. Диапазон напряжения сканирования был установлен от -0,2 В до +0,2 В.
3. Результаты и обсуждение
3.1. Экспериментальные порошки
Основные физические свойства порошков, такие как форма и лазерное поглощение, показаны на рис.Порошки W, Ta и Nb имели гранулированную форму, а порошок Мо имел сферическую форму. Порядок скорости поглощения лазера в порошковых элементах для лазера: A Mo > A W > A Nb > A Ta , как показано на, и чем выше поглощение, тем больше энергии будет получать порошок одновременно. Таким образом, средний размер порошка рассчитан в том же соответствующем порядке: D Mo (94.9 мкм)> D W (45,0 мкм)> D Nb (21,5 мкм)> D Ta (13,7 мкм). Примечательно, что абсорбция смешанного порошка выше, чем абсорбция большинства порошков, за исключением порошка Мо, что позволяет предположить, что процесс смешивания помогает улучшить абсорбцию. Поглощение порошка Мо выше, чем у смешанного порошка, поскольку порошок Мо может легко улавливать лазерное излучение в полой структуре с зазорами.
Основные физические свойства порошков (слева: формы порошков; в центре: лазерное поглощение порошков; справа: энергетические спектры).Смешанные порошки ( a ) Nb, ( b ) Mo, ( c ) Ta, ( d ) W и ( e ).
3.2. Фаза и состав
Картины дифракции рентгеновских лучей на порошке (XRD) деталей NbMoTaW HEA, изготовленных с помощью SLM, показаны на a. Поверхность образца гладкая и имеет характерный металлический блеск, что свидетельствует об относительно высокой плотности. Результаты XRD, показанные на b, по сравнению с c, показывают, что существует только один твердый раствор со структурой BCC без другой металлической фазы в сплаве.Между тем, экспериментальный параметр решетки составляет 3,2034 Å по сравнению с «теоретическим» параметром кристаллической решетки, a mix = 3,2230 Å [12], который можно рассчитать с помощью следующего уравнения:
где c i и a i — атомная доля и параметр решетки элемента i, соответственно. Кроме того, дифракционные пики (100), (200) и (211) относительно концентрированы, что означает, что состав однороден.Экспериментальные результаты хорошо согласуются с результатами для литого HEA NbMoTaW, приведенными в ссылках [11,12]. Таким образом, очевидно, что процесс SLM является эффективным методом формирования NbMoTaW HEA.
Картины порошковой рентгеновской дифракции (XRD) деталей и результатов NbMoTaW HEA. ( a ) Образцы деталей из высокоэнтропийного сплава NbMoTaW, изготовленных методом SLM. ( b ) Результат XRD для одной структуры сплава, ( c ) Результат XRD для сплава и небольшого количества другой фазы вольфрама.
После фазового подтверждения деталей был исследован элементный состав, как показано в а. Макроскопический состав относительно однороден. Анализ EDS четвертичного сплава показывает, что четыре элемента равномерно распределены в макромасштабе, как показано на b. Кроме того, распределение состава между микрозернами измеряется в c. Амплитуды колебаний состава Nb и Mo в микромасштабе больше, чем у Ta и W. Очевидно, что температуры плавления Nb и Mo ниже, чем у Ta и W.Во время процесса охлаждения Ta и W сначала осаждаются и равномерно распределяются в основной части, а Nb и Mo показывают сегрегацию между внутренними зернами и границами.
Результаты анализа состава. ( a ) Распределение состава, ( b ) EDS-анализ, ( c ) Распределение состава между микрозернами.
Видно, что элементы в выборках в целом распределены равномерно, но по-прежнему наблюдается разделение компонентов. Таким образом, были выполнены три группы экспериментов по воспроизводимости спекания для проверки отклонения состава образцов.Результаты распределения состава и дисперсия NbMoTaW показаны в. Из таблицы, хотя W и Mo приблизились к теоретическому ат.% (Ат.%) В 25% во всех трех образцах, у Ta было наибольшее среднее молярное отношение (ат.%) С 28,21%, у Nb было самое низкое среднее отношение (21,50%). , и их экспериментальные флуктуации (0,99 и 0,16 соответственно) в трех экспериментах невелики. Таким образом, очевидно, что в узорах присутствует определенная степень композиционного отклонения.
Таблица 1
| Элемент | S1 (ат.%) | S2 (ат.%) | S3 (ат.%) | Ср.(ат.%) | Разница |
|---|---|---|---|---|---|
| Вт | 27,26 | 24,76 | 24,35 | 25,46 | 1,65 |
| Ta | 28,09 | 29,49 | 27,06 | 28,21 | 0,99 |
| Nb | 21,61 | 20,97 | 21,93 | 21,50 | 0,16 |
| Пн | 23.05 | 24,79 | 26,67 | 24,84 | 2,19 |
Существует несколько факторов, приводящих к отклонению состава, таких как температура плавления, плотность жидкости, стороны порошка и поглощение энергии порошками. Согласно a – c, поскольку точки плавления порошка, плотности жидкости и ат.% Имеют одинаковые тенденции распределения, Mo и Nb с более низкими температурами плавления и плотностями показали отрицательные отклонения -0,16 ат.% И -3,5 ат.%, Соответственно. , по сравнению с номинальным составом 25%.Поэтому, как правило, когда смешанный порошок мгновенно нагревается лазером, сначала плавятся порошки с более низкой температурой плавления, а жидкость распространяется по большей площади поверхности и поглощает больше энергии, чем твердые порошки. Между тем, поскольку энергия с высокой плотностью непрерывно вводится, порошки с высокой температурой плавления также плавятся, и происходит процесс смешения различных металлических жидкостей. Жидкость с более низкой плотностью имеет тенденцию всплывать на поверхность, а жидкость с высокой плотностью имеет тенденцию падать, что означает, что жидкость с более низкой плотностью на поверхности подвергается воздействию лазера и получает больше энергии.В конце концов, эти элементы с более низкими температурами плавления раньше достигают точки кипения и больше испаряются в процессе SLM, что приводит к отрицательному отклонению состава.
( a ) Результаты распределения состава (среднее значение). ( b ) Температура плавления Nb, Mo, Ta, W. ( c ) Плотность жидкости Nb, Mo, Ta, W. ( d ) Средний размер частиц четырех порошков и лазерная поглощающая способность.
Однако окончательные результаты отклонения фактически объединены с такими факторами, как температура плавления, размер частиц, лазерное поглощение и т. Д.d показывает средний размер частиц четырех порошков (черный) и коэффициент поглощения лазерного излучения (синий). Очевидно, что средний размер частиц и коэффициент поглощения лазерного излучения имеют одинаковую тенденцию к изменению и определенную степень причинно-следственной связи. Между тем, вместе взятые a, b, стоит отметить, что, хотя Mo и Nb имеют очень похожие точки плавления, разница в составе между ними относительно велика, что вызвано размером частиц и лазерным поглощением. В частности, для порошка Мо, хотя он имеет более высокую скорость поглощения лазерного излучения, больший размер порошка замедляет скорость плавления, что вызывает меньшую потерю массы и отклонение по сравнению с ниобием.
Таким образом, можно увидеть, что NbMoTaW HEA, созданный с помощью процесса SLM, показывает приблизительное эквимолярное распределение соотношения. Несмотря на то, что максимальное отклонение состава составляет 3,5%, для HEA приемлемый диапазон составляющих от 5 до 35%, и отклонение состава не влияет на фазу и микроструктуру. Фактически, NbMoTaW HEA, сформированный SLM, может продемонстрировать три преимущества в производительности.
3.3. Микроструктура
На основании наблюдений SEM в плоскости XY границы зерен NbMoTaW HEA, образованные с помощью SLM, видны на a.Средний размер зерна составляет 13,4 мкм, что намного меньше по сравнению с размером зерна 200 мкм HEA NbMoTaW в литом состоянии [12], как показано на b. Кроме того, с дальнейшим усилением, в c, многие дендриты с пластинчатой мартенситной структурой появляются на вершине ванн расплава. Преимущественная ориентация зерен — во всех направлениях, а вторые ветви переплетены друг с другом. Расстояние между первичными и вторичными ветвями дендритов составляет в среднем 6,59 мкм и 1,68 мкм, соответственно, по сравнению с расстоянием между ветвями дендритов в литом состоянии примерно от 20 до 30 мкм по диаметру [12].
Различные значения увеличения зернистости структуры HEA, полученные с помощью сканирующего электронного микроскопа (SEM) в плоскости XY. ( a ) Рисунок зернистости в этом исследовании. ( b ) Рисунок зерна HEA из литого NbMoTaW [12]. ( c ) Рисунок зерна рисунка с дальнейшим усилением в этом исследовании. ( d ) Зернистость HEA из литого NbMoTaW с дальнейшим усилением [12].
Фактически, в условиях быстрого затвердевания при лазерной обработке зерна и дендриты как субструктура росли и развивались с чрезвычайно высоким градиентом температуры и скоростью охлаждения.Зерна были очень мелкими, а расстояние между первичными ветвями дендритов составляло примерно половину размера зерна. Это означает, что при формировании зародышей зерна их движущая сила роста была большой, но время роста было ограниченным. Таким образом, дендритные ветви имели тонкую форму, а расстояние между ветвями дендритов было намного меньше, чем в других процессах затвердевания, таких как литье.
Считается, что тонкая структура улучшает механические свойства готовой детали. Сообщалось, что HEA NbMoTaW в литом состоянии является хрупким с пластической деформацией p = 0.2% [11], что серьезно ограничивает возможности его применения. Хорошо известный закон Холла – Петча (HP) [22,23] иллюстрирует зависимость размера зерна от макроскопической пластичности и взаимосвязь между напряжениями хрупкого разрушения и поликристаллической структурой. Следовательно, пластичность, усталостная прочность и скорость ползучести поликристаллического ОЦК-металла улучшаются при уменьшении размера зерна [24]. Таким образом, сплав NbMoTaW, изготовленный методом SLM, является многообещающим методом для производства тугоплавких деталей из ВЭА, хотя дальнейшее изучение механических свойств все еще необходимо.
3.4. Микротвердость
В этом исследовании микротвердость ( H v ) изготовленных образцов была измерена в плоскости XY по сравнению с данными микротвердости чистого Nb, Mo, Ta, W и четырех видов сверхсплавов [25, 26]. Результаты показаны на рисунке, и на нем стоит отметить два момента.
Сравнение микротвердости (в плоскости XY) для различных чистых металлов и сплавов [12,25,26].
Во-первых, среднее значение микротвердости образца NbMoTaW HEA s (спекание SLM) составляет 826 Hv.Однако самая высокая микротвердость Nb, Mo, Ta и W составляет 410Hv, а микротвердость сверхсплавов находится только в диапазоне 310–437 Hv. Таким образом, очевидно, что HEA NbMoTaW намного тверже суперсплавов и содержащихся в нем чистых элементов. Кроме того, согласно исследованиям Сенкова и соавт. [11], NbMoTaW HEA не вызывает резких изменений твердости при высоких температурах, а это означает, что NbMoTaW HEA также имеет лучшие свойства твердости при высоких температурах, чем суперсплавы.
Во-вторых, по сравнению с образцом HEA a (спекание дуговой плавкой) (446 Hv) [12], образец HEA s также демонстрирует лучшие характеристики твердости, что показывает преимущество измельчения зерна за счет быстрого охлаждения. в процессе УУЗР.Также видно, что измельчение зерна может значительно улучшить твердость высокоэнтропийных сплавов. Следовательно, SLM может быть эффективным средством повышения твердости высокоэнтропийных сплавов.
3.5. Коррозионная стойкость
Согласно электрохимической теории, есть два параметра, характеризующие коррозионную активность, потенциал самокоррозии ( E corr ) и ток самокоррозии ( I corr ), среди которых самокоррозионный потенциал это всего лишь ссылка.Ключевым параметром для оценки коррозионной активности металлов является ток свободной коррозии. Более низкая плотность ( I corr ) означает более высокую коррозионную стойкость. В этом исследовании площади поверхности двух типов рисунков одинаковы, поэтому плотность тока свободной коррозии можно заменить на ток свободной коррозии. В I corr из NbMoTaW HEA и стали 316L можно получить линейную подгонку: потенциал самокоррозии HEA E corrH = -91.57 мВ, ток свободной коррозии I corrH = 8,716 × 10 −11 A; для стали 316 L, E corrS = −242,45 мВ, I corrS = 8,815 × 10 — 9 A. Как видно, потенциал самокоррозии HEA более отрицательный, чем у HEA. Сталь 316L, что означает, что HEA имеет более сильную склонность к коррозии. Это связано с наличием небольшого количества сегрегации состава в сплаве, как упоминалось ранее, которое легко формирует коррозионные пары и делает сплав более «активным».Однако ток свободной коррозии HEA снижен на два порядка по сравнению со сталью 316 L. Следовательно, в целом высокоэнтропийный сплав NbMoTaW имеет лучшую коррозионную стойкость. Фактически, хотя в HEA существует небольшая сегрегация элементов, все элементы Nb, Mo и Ta, содержащиеся в сплаве, являются легко пассивируемыми металлами, что способствует превосходной коррозионной стойкости в растворе NaCl с концентрацией 3,5 мас.%.
Картины поляризационных кривых WMoNbTa HEA и 316 L.
Кроме того, чтобы более наглядно показать разницу в коррозионной стойкости между двумя материалами, образцы стали NbMoTaW и 316 L также были сканированы при высоком напряжении в диапазоне от -1,5 до +2 В в 3,5% -ном растворе NaCl. окружающая обстановка. В этом растворе корродировались два вида рисунков, но степень коррозии была совершенно разной, как показано на рис.
Коррозия поверхности образца в диапазоне высоких напряжений. ( a ) Образец нержавеющей стали 316 L. ( b ) Образец NbMoTaW HEA.
Из a очевидно, что в стали 316 L происходит сильная коррозия с глубиной коррозии даже до 1 мм. Однако в случае b для сплава NbMoTaW из-за эффекта коррозии только трещина образца имеет определенную степень расширения. При этом точечная коррозия возникает и на гладкой поверхности рисунка. Таким образом, из-за снижения веса NbMoTaW HEA также демонстрирует более высокую коррозионную стойкость, чем сталь 316 L.
4. Выводы
В этой статье в качестве материала-заменителя суперсплавов высокоэнтропийный суперсплав NbMoTaW может быть получен с помощью SLM.Кроме того, из-за температуры плавления, плотности жидкости, размера частиц и поглощения энергии порошков элемент с самой низкой точкой плавления и плотностью показал отрицательное отклонение (не более 5%) мольного соотношения в изготовленном сплаве. К счастью, для HEA допустимый диапазон составляющих 5–35%, и отклонение состава не влияет на фазу и микроструктуру. Фактически, NbMoTaW HEA, сформированный SLM, может продемонстрировать три преимущества в производительности.
Первый — это микроструктура, поскольку анализ микроструктуры образца показал, что очень мелкие зерна и дендриты, полученные в образце HEA с помощью SLM, имели размер 13.4 мкм и 6,59 мкм соответственно, что намного меньше, чем наблюдаемые в отлитых образцах. Во-вторых, микротвердость NbMoTaW HEA s может достигать 826 HV, что намного выше данных микротвердости HEA a , чистого Nb, Mo, Ta, W и четырех видов сверхсплавов. Это вызвано эффектом измельчения зерна в процессе SLM. Наконец, что касается коррозионной стойкости, ток свободной коррозии для NbMoTaW составляет I corrH = 8,716 × 10 −11 A, а для стали 316 L I corrS = 8.815 × 10 −9 А; ток свободной коррозии HEA снижен на два порядка по сравнению со сталью 316 L. Следовательно, в целом высокоэнтропийный сплав NbMoTaW имеет лучшую коррозионную стойкость.
Выражение признательности
Это исследование финансировалось Национальным фондом естественных наук Китая, грант номер 51505366, Китайским фондом постдокторантуры, грант номер 2015M570827, План фундаментальных исследований естествознания в провинции Шэньси, Китай, номер гранта 2017JM5046, и Национальная наука и Крупный технологический проект, номер гранта 2017ZX04014001-005.APC финансировался Национальным фондом естественных наук Китая, номер гранта 51505366.
Вклад авторов
Написание — рецензирование и редактирование, H.Z .; Письмо — обзор и редактирование, Ю.З .; Письмо — подготовка оригинального проекта, S.H .; курирование данных, С.З .; Письмо — обзор и редактирование, F.W .; администрация проекта, D.L.
Конфликт интересов
Авторы заявили, что у них нет конфликта интересов в отношении данной работы. Мы заявляем, что у нас нет никаких коммерческих или ассоциативных интересов, представляющих конфликт интересов в связи с представленной работой.
Ссылки
1. Yeh J.W., Chen S.K., Lin S.J., Gan J.Y., Chin T.S., Shun T.T., Tsau C.-H., Chang S.-Y. Наноструктурированные высокоэнтропийные сплавы с множеством основных элементов: новые концепции и результаты проектирования сплавов. Adv. Англ. Матер. 2004. 6: 299–303. DOI: 10.1002 / adem.200300567. [CrossRef] [Google Scholar] 2. Цзян-Вэй Ю. Последние достижения в высокоэнтропийных сплавах. Аня. Чим. Sci. Матер. 2006; 31: 633–648. [Google Scholar] 3. Кантор Б., Чанг И., Найт П., Винсент А. Развитие микроструктуры в эквиатомных многокомпонентных сплавах.Матер. Sci. Англ. А. 2004; 375: 213–218. DOI: 10.1016 / j.msea.2003.10.257. [CrossRef] [Google Scholar] 4. Чжан Ю., Ян Х., Ляу П.К. Оптимизация конструкции и свойств высокоэнтропийных сплавов. JOM. 2012; 64: 830–838. DOI: 10.1007 / s11837-012-0366-5. [CrossRef] [Google Scholar] 5. Йе Дж. Стратегии проектирования сплавов и будущие тенденции в высокоэнтропийных сплавах. JOM. 2013; 65: 1759–1771. DOI: 10.1007 / s11837-013-0761-6. [CrossRef] [Google Scholar] 6. Zhang Y., Zuo T.T., Tang Z., Gao M.C., Dahmen K.A., Liaw P.K., Lu Z.П. Микроструктуры и свойства высокоэнтропийных сплавов. Прог. Матер. Sci. 2014; 61: 1–93. DOI: 10.1016 / j.pmatsci.2013.10.001. [CrossRef] [Google Scholar] 7. Гао Дж., Ли Р. Микроструктура и жаропрочность высокоэнтропийного сплава AlZnMnSnSbPbMg. J. Funct. Матер. 2009; 4:21. [Google Scholar] 8. Чжан Ю., Цзо Т., Ченг Ю., Ляу П.К. Высокоэнтропийные сплавы с высокой намагниченностью насыщения, удельным электрическим сопротивлением и ковкостью. Sci. Отчет 2013; 3: 1455. DOI: 10,1038 / srep01455. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 9.Глудовац Б., Хоэнвартер А., Катур Д., Чанг Э. Х., Джордж Э. П., Ричи Р. О. Устойчивый к разрушению высокоэнтропийный сплав для криогенных применений. Наука. 2014; 345: 1153–1158. DOI: 10.1126 / science.1254581. [PubMed] [CrossRef] [Google Scholar] 10. Гао М.К., Алман Д.Э. Поиск следующих однофазных высокоэнтропийных составов сплавов. Энтропия. 2013; 15: 4504–4519. DOI: 10.3390 / e15104504. [CrossRef] [Google Scholar] 11. Сеньков О.Н., Уилкс Г.Б., Скотт Дж. М., Чудо Д. Б. Механические свойства тугоплавких высокоэнтропийных сплавов Nb25Mo25Ta25W25 и V20Nb20Mo20Ta20W20.Интерметаллиды. 2011; 19: 698–706. DOI: 10.1016 / j.intermet.2011.01.004. [CrossRef] [Google Scholar] 12. Сеньков О.Н., Вилкс Г.Б., Миракл Д.Б., Чуанг К.П., Ляу П.К. Тугоплавкие высокоэнтропийные сплавы. Интерметаллиды. 2010; 18: 1758–1765. DOI: 10.1016 / j.intermet.2010.05.014. [CrossRef] [Google Scholar] 14. Чжан М., Чжоу X., Ю X., Ли Дж. Синтез и характеристика покрытия из тугоплавкого высокоэнтропийного сплава TiZrNbWMo методом лазерной наплавки. Серфинг. Пальто. Technol. 2017; 311: 321–329. DOI: 10.1016 / j.surfcoat.2017.01.012. [CrossRef] [Google Scholar] 15. Джозеф Дж., Стэнфорд Н., Ходжсон П., Фабиянич Д.М. Асимметрия растяжения / сжатия в гранецентрированном кубическом высокоэнтропийном сплаве аддитивного производства. Scr. Матер. 2017; 129: 30–34. DOI: 10.1016 / j.scriptamat.2016.10.023. [CrossRef] [Google Scholar] 16. Kunce I., Polanski M., Bystrzycki J. Структура и водородные свойства высокоэнтропийного сплава ZrTiVCrFeNi, синтезированного с использованием Laser Engineered Net Shaping (LENS) Int. J. Hydrogen. Энергия. 2013; 38: 12180–12189. DOI: 10.1016 / j.ijhydene.2013.05.071. [CrossRef] [Google Scholar] 17. Kunce I., Polanski M., Bystrzycki J. Микроструктура и свойства хранения водорода высокоэнтропийного сплава TiZrNbMoV, синтезированного с использованием Laser Engineered Net Shaping (LENS) Int. J. Hydrogen. Энергия. 2014; 39: 9904–9910. DOI: 10.1016 / j.ijhydene.2014.02.067. [CrossRef] [Google Scholar] 18. Доббельштейн Х., Тиле М., Гуревич Е.Л., Джордж Е.П., Остендорф А. Прямое осаждение металла тугоплавкого высокоэнтропийного сплава MoNbTaW. Phys. Процедуры. 2016; 83: 624–633.DOI: 10.1016 / j.phpro.2016.08.065. [CrossRef] [Google Scholar] 19. Ван Р., Чжан К., Дэвис К., Ву X. Эволюция микроструктуры, механических и коррозионных свойств высокоэнтропийного сплава AlCoCrFeNi, полученного прямым лазерным изготовлением. J. Alloys Compd. 2017; 694: 971–981. DOI: 10.1016 / j.jallcom.2016.10.138. [CrossRef] [Google Scholar] 20. Толочко Н.К., Хлопков Ю.В., Можжаров С.Е., Игнатьев М.Б., Лауи Т., Титов В.И. Поглощение порошковых материалов, пригодных для лазерного спекания. Быстрый прототип. Дж.2000. 6: 155–161. DOI: 10.1108 / 13552540010337029. [CrossRef] [Google Scholar] 21. GB / T 6394-2002, Метод измерения среднего размера зерна металлов. Стандартизация и качество машиностроения; Beijin, China: 2004. [Google Scholar] 22. Холл Э. Деформация и старение мягкой стали: III обсуждение результатов. Proc. Phys. Soc. Б. 1951; 64: 747. DOI: 10.1088 / 0370-1301 / 64/9/303. [CrossRef] [Google Scholar] 23. Петч Н.Дж. Прочность поликристаллов на скол. J. Iron Steel Inst. 1953; 174: 25–28.[Google Scholar] 24. Армстронг Р.В. Влияние размера зерна поликристалла на некоторые механические свойства материалов. Металл. Матер. Пер. 1970; 1: 1169–1176. DOI: 10.1007 / BF027. [CrossRef] [Google Scholar] 25. Шабалин И.Л. Сверхвысокотемпературные материалы. 1-е изд. Springer; Нью-Йорк, Нью-Йорк, США: 2014. С. 237–531. [Google Scholar] 26. Анонимный. Практическое руководство по инженерным материалам. 2. Практическое руководство по деформированному суперсплаву и литому суперсплаву. 2-е изд. Стандарты прессы Китая; Пекин, Китай: 2002.С. 9–829. [Google Scholar]тугоплавких металлов в аэрокосмической и оборонной промышленности
Рынки аэрокосмической и оборонной промышленности (A&D), основанные в беспрецедентный период инноваций, сегодня являются одними из крупнейших и наиболее прибыльных отраслей в мире. Трудно оценить чистую стоимость мирового рынка с какой-либо точностью, но аэрокосмический и оборонный секторы США недавно зарегистрировали рекордный годовой доход в 760 миллиардов долларов США. Это во многом объясняется продолжающейся цифровой трансформацией и инновациями, несмотря на растущую геополитическую неопределенность и напряженность.Тугоплавкие металлы играют центральную роль в этих ключевых факторах роста, обеспечивая решения для инноваций с низким уровнем риска в системах управления полетом и баллистике.
В этом сообщении в блоге H.C. Starck Solutions исследует использование тугоплавких металлов в аэрокосмической и оборонной промышленности.
Аэрокосмическая промышленность и оборона: дополнительные преимущества за счет тугоплавких металлов
Огнеупорные металлы представляют собой критически важный класс материалов в высокопроизводительных промышленных и производственных помещениях. Они включают основную группу из пяти элементов: ниобий (Nb), молибден (Mo), рений (Re), тантал (Ta) и вольфрам (W).Хотя определение того, что считается тугоплавким металлом, варьируется — в некоторых областях материаловедения и металлургии рассматриваются более широкие спецификации, чем в других, — эти пять элементов являются окончательными огнеупорами.
Эти материалы объединяет исключительная устойчивость к экстремальным температурам и уникальные физические и химические свойства. Из пяти тугоплавких металлов ниобий имеет самую низкую температуру плавления (2750 ° C), а тантал имеет самую низкую твердость по Виккерсу (873 МПа).Это уже выдающиеся свойства, которые только улучшаются во всем семействе тугоплавких металлов, охватывая температуру плавления до 3422 ° C и максимальную твердость по Виккерсу 4000 МПа.
Вольфрам — это тугоплавкий металл, который используется в аэрокосмической и оборонной промышленности. Он имеет самую высокую температуру плавления среди всех металлов, известных человеку: 3422 ° C (6192 ° F). В сочетании с его высокой плотностью (19,3 г / см 3 ) и чрезвычайной твердостью, он обычно используется для изготовления критически важных продуктов, которые способствуют стабильности в полете или обеспечивают мощную проникающую способность для сложных боеприпасов.Молибден и тантал также используются в столь же требовательных приложениях военной и гражданской авиации.
Для получения дополнительной информации о материалах, используемых в аэрокосмической и оборонной промышленности, просмотрите наши Продукция по отраслям.
Тантал необходим для создания пенетраторов взрывной формы (EFP), в то время как молибденовые нагревательные элементы и зоны нагрева используются в ряде процессов термообработки, предназначенных для улучшения физических свойств компонентов, предназначенных для использования в аэрокосмической и оборонной промышленности.Ниобий — еще один критически важный огнеупор, который выводит аэрокосмическую промышленность на новый уровень, обеспечивая новое решение в области материалов для ракетных сопел и устройств защиты от огня.
Многие финансовые аналитики утверждают, что расходы на оборону и рост коммерческой авиации антицикличны, что означает, что сектор часто процветает, несмотря на экономические спады или спады. Другие считают, что в рыночной стоимости сектора не бывает заметной периодичности. Однако неизменным фактом является то, что инновации в аэрокосмической и оборонной сферах часто подкрепляются новыми материальными решениями.Композиты сыграли важную роль в первых успехах авиационной промышленности; Теперь тугоплавкие металлы предлагают аналогичные инновации для удовлетворения растущего мирового спроса.
Среди многих инноваций в аэрокосмической отрасли было начало аддитивного производства (AM) для производства высокопроизводительных компонентов. Если вы хотите узнать больше о том, как AM все чаще используется в аэрокосмической отрасли, прочтите статью «Аддитивное производство для космических приложений».
тугоплавкие металлы марки H.C. Starck Solutions
H.C. Starck Solutions специализируется на производстве огнеупоров и сплавов высокой чистоты для сложных областей применения. Мы предлагаем широкий спектр проверенных продуктов для аэрокосмической и оборонной промышленности, помогая производителям удовлетворить постоянный спрос на высокопроизводительные решения. Наша продуктовая линейка включает:
- Балансировочные грузы WHA для самолетов и вертолетов
- Nb C-103 Лист и сопла для силовых установок
- Поковки TZM для производства лопастей двигателей
- Защитные компоненты WHA для космических кораблей
- Mo, Ta и ракеты WHA компоненты
Если вам нужна дополнительная информация об использовании тугоплавких металлов в аэрокосмической и оборонной сферах, просто свяжитесь с членом H.Команда К. Старка сегодня.
Ссылки:
https://www.wearefinn.com/topics/posts/five-trends-that-will-shape-the-aerospace-and-defence-industry-in-2019/
https: // www.
