Металлы IIA группы — Умскул Учебник
На этой странице вы узнаете- Какие из щелочноземельных металлов самые распространенные и самые редкие?
- Как появляется накипь на чайнике?
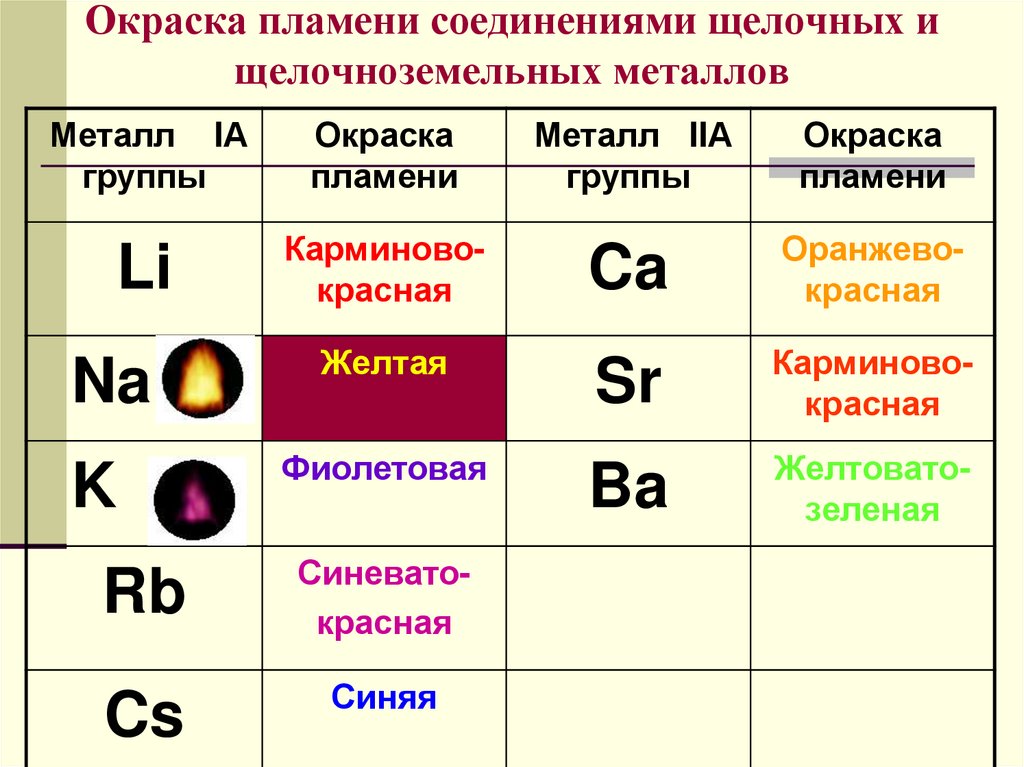
- Как распознать катионы щелочноземельных металлов?
Металлы IIA группы — очень активные! Если кинуть их в воду, то происходят мощные взрывы. Давайте познакомимся с этими металлами поближе.
Что особенного в элементах IIА группыIIA группа называется главной подгруппой второй группы, в которую входят щелочноземельные металлы. К ним относятся всего 4 химических элемента: кальций Ca, стронций Sr, барий Ba и радий Ra. В отличие от щелочных металлов, они существенно более твердые, но всё также имеют серебристо-белый цвет.
Электронная конфигурация металлов IIA группы достаточно простая: эти элементы содержат два электрона на внешнем энергетическом уровне, и в основном состоянии имеют конфигурацию ns2.
Но так как для образования связей с другими элементами необходимо наличие валентных электронов, то металлам IIA группы необходимо распарить электроны. Таким образом они помещают каждый в свою «комнату» – в квантовую ячейку.
К чему же это все приводит? Атомы этих металлов переходят в возбужденное состояние и в составе сложных веществ приобретают электронную конфигурацию ns1np1.
В результате, появляются два неспаренных электрона, поэтому у металлов IIA группы постоянная валентность II и постоянная степень окисления +2.
| Какие из щелочноземельных металлов самые распространенные и самые редкие? В природе самым распространенным щелочноземельным металлом является кальций, содержание которого относительно массы земной коры оценивается до 13,3 %. Радиоактивный радий — самый редкий из всех щелочноземельных металлов, его содержание около 1⋅10−10 %. 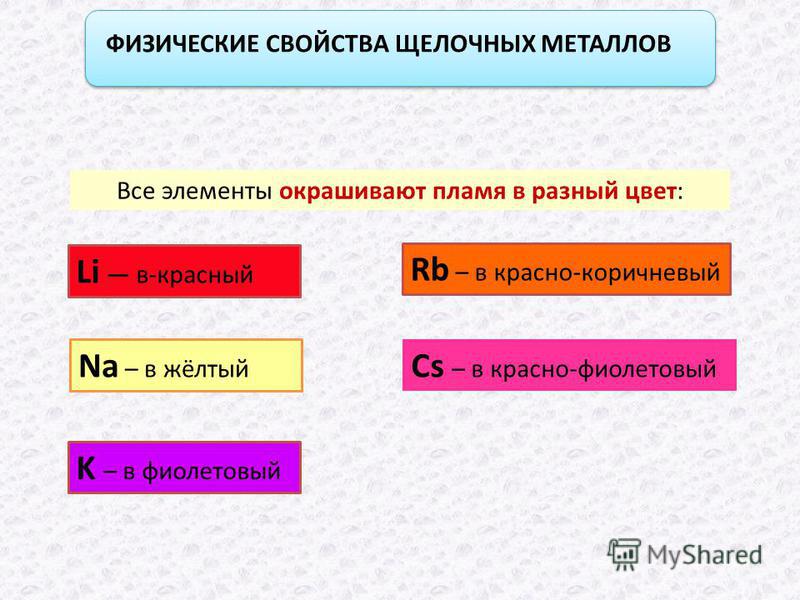 |
Как и при получении щелочных металлов, основным способом получения щелочноземельных металлов, а также магния и бериллия является электролиз расплавов солей и гидроксидов:
Подробнее об электролизе можно почитать в статье «Электролиз расплавов и растворов».
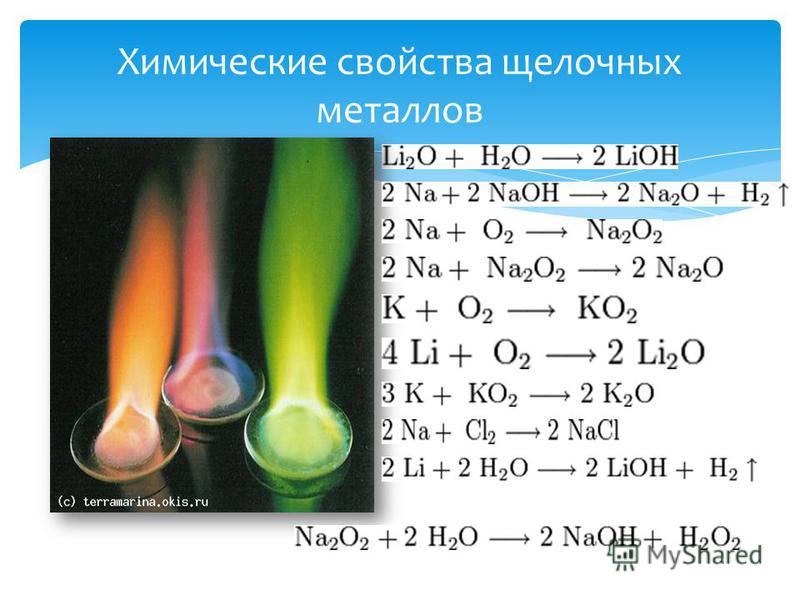
Химические свойства- Как и для щелочных металлов, металлы IIA группы реагируют с простыми веществами.
- Все щелочноземельные металлы взаимодействуют с холодной водой с образованием соответствующих гидроксидов. Магний же реагирует только с горячей водой:
- Щелочноземельные металлы в расплаве способны вытеснять менее активные металлы из их оксидов.
- Металлы IIA группы являются чуть менее активными, чем щелочные металлы, поэтому они могут реагировать с растворами кислот, при этом образуя соответствующие соли:
- Магний способен вытеснять металлы из растворов солей:
- Как и щелочные металлы, металлы IIA группы образуют ацетилениды (то есть карбиды, которые при гидролизе образуют ацетилен).
 Но магний, помимо ацетиленида, образует карбид особого строения:
Но магний, помимо ацетиленида, образует карбид особого строения:
- Взаимодействие с кислородом:
| Как появляется накипь на чайнике? Думаю, ты не раз обнаруживал на дне чайника непонятные белые образования после кипячения воды. Это называется накипью. В чем же причина её образования? Все дело в растворенных в воде солях кальция и магния. Обычно с ней борются при помощи кипячения с лимонной кислотой, которая разрушает накипь. |
Под жесткостью воды подразумевают совокупность свойств, зависящих от присутствия в ней преимущественно солей кальция и магния: гидрокарбонатов, сульфатов и хлоридов. При этом различают:
- постоянную жесткость, или некарбонатную, которая обусловлена присутствием сульфатов и хлоридов кальция и магния;
- временную жесткость, или карбонатную, которая обусловлена присутствием гидрокарбонатов кальция и магния.

- Кипячение воды. При этом гидрокарбонаты будут разлагаться на соответствующие карбонаты, которые оседают на стенках чайника, например:
- Добавление карбоната натрия. Этим способом можно устранить и постоянную, и временную жесткость:
- Во IIA группу входят щелочноземельные металлы, а также бериллий и магний.
- У этих элементов постоянная валентность II, степень окисления +2.
- Для них характерны реакции с простыми веществами, водой, кислотами.
- Некоторые соли кальция и магния определяют жесткость воды.
Задание 1.
Характерная степень окисления металлов IIA группы равна:
- +1;
- +2;
- +3;
- +4.
Задание 2.
Какой из металлов IIA группы реагирует с водой только при нагревании?
- Бериллий;
- Кальций;
- Магний;
- Барий.
Задание 3.
Что образует кальций при взаимодействии его с кислородом?
- Оксид кальция;
- Пероксид кальция;
- Надпероксид кальция;
- Озонид кальция.
Задание 4.
Чем обусловлена временная жесткость воды?
- Присутствием хлоридов кальция и магния;
- Присутствием гидрокарбонатов кальция и магния;
- Присутствием сульфатов кальция и магния;
- Присутствием карбонатов кальция и магния.
ОТВЕТЫ: 1. — 2; 2. — 3; 3. — 1; 4. — 2.
Щелочноземельные металлы: получение, применение, свойства, характеристики
Главная » Металлы » Особенности и свойства щелочноземельных металлов
На чтение 4 мин
Содержание
- Общая характеристика
- Элементы и их нахождение в таблице Менделеева
- Бериллий
- Магний
- Кальций
- Стронций
- Барий
- Радий
- Присутствие в природе
- Свойства
- Физические
- Химические
- Способы получения
- Сферы применения
Щелочноземельные металлы — химически активные элементы, которые занимают вторую группу периодической таблицы Менделеева. Найти их в чистом виде не возможно, поскольку они имеют высокую химическую активность. Обладают похожими и уникальными свойствами.
Найти их в чистом виде не возможно, поскольку они имеют высокую химическую активность. Обладают похожими и уникальными свойствами.
Общая характеристика
Щелочноземельные металлы — совокупность химических элементов с похожими характеристиками. При взаимодействии оксидов этих металлов с водой создается щелочная среда.
При нормальных условиях сохраняют твердую структуру, металлический блеск, высокую температура плавления.
Щелочноземельные металлы имеют несколько похожих особенностей. Плотность химического элемента возрастает зависимо от порядкового номера. Эти материалы невозможно разрезать ножом (исключением является стронций).
Элементы и их нахождение в таблице Менделеева
Каждый элемент имеет определенные особенности. Чтобы понять, как работать с подобными металлами, необходимо изучить их характеристики.
Бериллий
Характеристики:
- номер — 4;
- простое вещество — твердый материал;
- цвет — светло-серый.

Особенности — металлический блеск, высокая токсичность.
Бериллий (Фото: Instagram / chemistry_easy)Магний
Характеристики:
- номер — 12;
- простое вещество — легкий, ковкий материал;
- цвет — белый с серебристыми отливами.
Особенности — металлический блеск, малый удельный вес.
Кальций
Характеристики:
- номер – 20;
- простое вещество – мягкий материал;
- цвет — белый с серебристыми отливами.
Стронций
Характеристики:
- номер — 38;
- простое вещество — мягкий, ковкий, пластичный материал;
- цвет — белый с серебристыми отливами.
Стронций в ампуле с аргоном (Фото: Instagram / chemical_elements)Имеет радиоактивные изотопы.
Барий
Характеристики:
- номер — 58;
- простое вещество — ковкий, мягкий материал;
- цвет — белый с серебристыми отливами.
Радий
Характеристики:
- номер – 88;
- простое вещество — твердый материал;
- цвет — белый с серебристыми отливами.
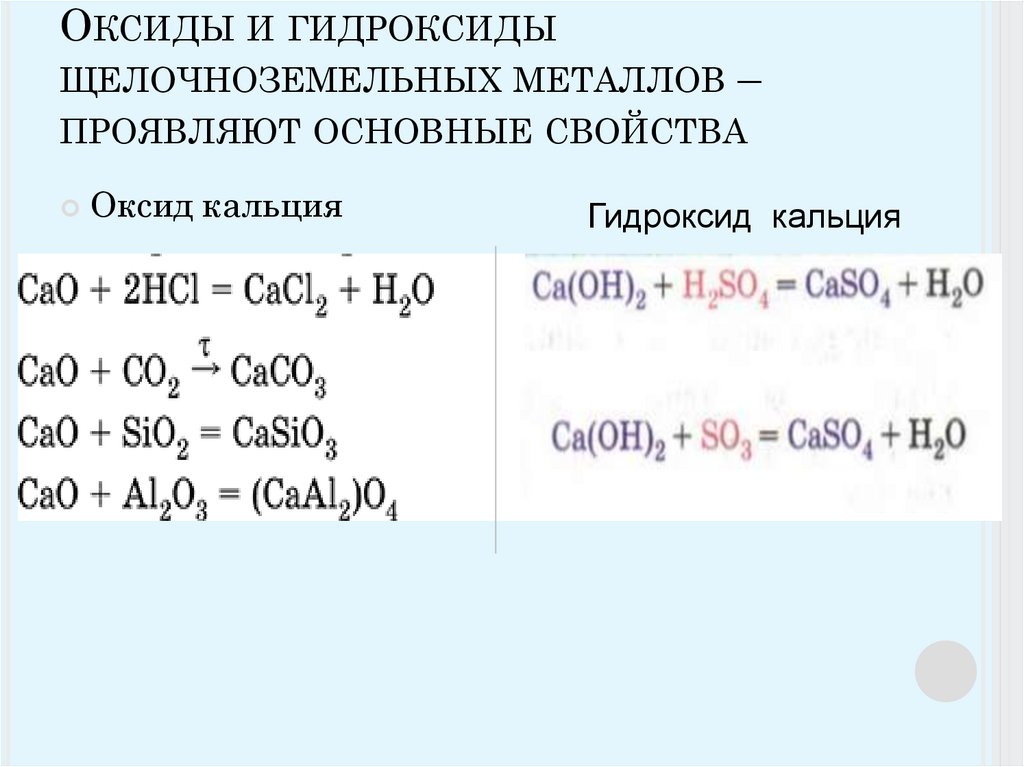
Особенности — радиоактивен, поверхности радия быстро тускнеют на воздухе.
Присутствие в природе
Элементы можно найти в природе, но только в виде сплавов, поскольку они имеют высокую химическую активность. Чаще всех встречается кальций. Ему немного уступает магний. Стронций с барием также достаточно распространены. Бериллий с радием считаются самыми редкими из этой группы.
Интересный факт про радий (Фото: Instagram / fakt_zhizni)Свойства
Свойства щелочных и щелочноземельных металлов позволяют определить в каких сферах деятельности их можно применять.
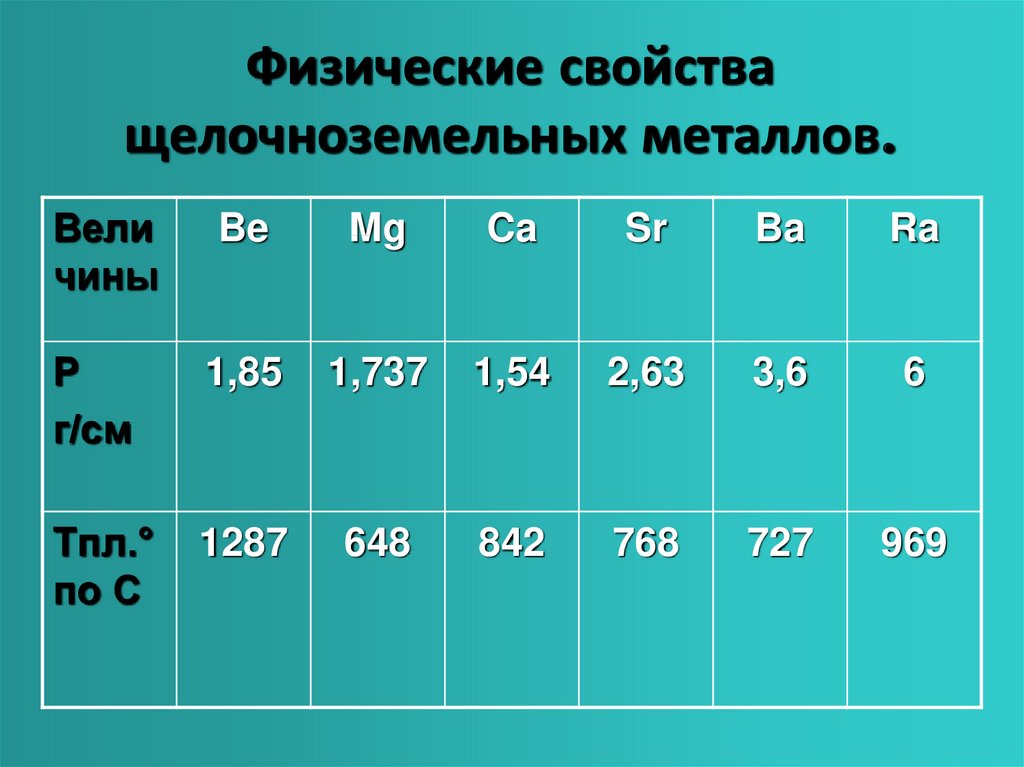
Физические
Свойства:
| Атомный номер | Валентность | Температура плавления | Плотность | Температура кипения | |
| Магний | 12 | 2 | 650 | 1.737 | 1105 |
| Стронций | 38 | 2 | 769 | 2.54 | 1384 |
| Бериллий | 4 | 2 | 1279 | 1. 848 848 | 2970 |
| Кальций | 20 | 2 | 839 | 1.55 | 1484 |
| Радий | 88 | 2 | 700 | 5.5 | 1737 |
| Барий | 56 | 2 | 729 | 3.5 | 1637 |
Химические
Чем выше порядковый номер элемента, тем сильнее его химическая активность. Надпероксиды, озониды этих элементов ученые еще не изучили до конца. Они нестабильны.
У гидроксидов, оксидов этих химических элементов при возрастании порядкового номера усиливаются свойства. Применяются в разных сферах промышленности.
При взаимодействии с открытым воздухом щелочноземельные металлы покрываются оксидной пленкой. В реакцию с посторонними элементами вступают только при сильном нагревании.
Радий, стронций, барий активно взаимодействуют с азотом, кислородом. Для их хранения нужны герметичные емкости, которые будут заполнены керосином.
Способы получения
Для получения гидроксидов на чистые химические элементы воздействуют водой без примесей. Реакция должна протекать при комнатной температуре. При этом выделяется водород.
Реакция должна протекать при комнатной температуре. При этом выделяется водород.
Для получения чистых щелочноземельных металлов проводится разложение сложных веществ на более простые. После этого осуществляться восстановление. Для получения стронция, кальция, магния применяется технология электролиза. Барий, бериллий получают с помощью восстановления. Сложнее всего добывать чистый радий. Для его получения нужно перерабатывать урановую руду.
Банки с жидкостью для электролиза (Фото: Instagram / take_n_make)Сферы применения
Сферы применения:
- Кальций. Компонент многих строительных материалов. Он применяется при изготовлении топлива, огнеупорных материалов, лекарственных средств.
- Бериллий. Применяется для изготовления олова, содержится в составе различных минералов. Используется при производстве ракетного топлива.
- Соли стронция содержатся в разных минералах. Применяется в металлургии, радиоэлектронике, ядерной энергетике, производстве чистого урана, магнитных материалов, источников электричества.
 Изотопы применяются для лечения злокачественных образований в организме человека.
Изотопы применяются для лечения злокачественных образований в организме человека. - Магний. Востребован в металлургии, поскольку легко поддается обработке. Используется при изготовлении ноутбуков, электронных книг, телефонов, часов, измерительных приборов. Применяется в военной, космической отрасли.
- Радий. Востребован в медицине, ядерной промышленности. Раньше применялся в качестве красителя для циферблатов, стрелок. Сейчас его для этого не используют из-за высокой токсичности.
- Барий. Применяется при производстве вакуумных приборов, оптических линз, источников тока, жидких теплоносителей. Часто используется в атомной энергетике.
Основные представители щелочноземельных металлов химически активны, обладают уникальными свойствами. На открытом воздухе быстро покрываются оксидной пленкой. Применяются в разных сферах деятельности.
( 3 оценки, среднее 5 из 5 )
Поделиться
Щелочно-земельный металл Определение и значение
- Основные определения
- Викторина
- Примеры
- Научная
Показывает уровень сложности слова.
[ al-kuh-lahyn-urth, -lin- ]
/ ˈæl kəˌlaɪnˈɜrθ, -lɪn- /
Сохранить это слово!
Показывает уровень сложности слова.
сущ. Химия.
любой из группы двухвалентных металлов, включая барий, радий, стронций, кальций и, как правило, магний, гидроксиды которых являются щелочами, но менее растворимы, чем гидроксиды щелочных металлов.
ВИКТОРИНА
ВЫ ПРОЙДЕТЕ ЭТИ ГРАММАТИЧЕСКИЕ ВОПРОСЫ ИЛИ НАТЯНУТСЯ?
Плавно переходите к этим распространенным грамматическим ошибкам, которые ставят многих людей в тупик. Удачи!
Вопрос 1 из 7
Заполните пропуск: Я не могу понять, что _____ подарил мне этот подарок.
Происхождение щелочноземельного металла
Впервые записано в 1900–05 гг. , щелочная порода, щелочная почва
Dictionary.com Полный текст На основе Random House Unabridged Dictionary, © Random House, Inc. 2022
Как использовать щелочноземельный металл в предложении
У меня в голове возникают следующие вопросы: сердце Парижа?
Аяан Хирси Али: Наш долг — сохранить существование Charlie Hebdo|Аяан Хирси Али|8 января 2015 г.
 |DAILY BEAST
|DAILY BEASTНевольно возникает вопрос, что, черт возьми, Эндрю делал, болтаясь с полураздетыми подростками?
Букингемский дворец оспаривает сексуальные обвинения против принца «Рэнди Энди»|Том Сайкс|4 января 2015 г.|DAILY BEAST на земле.
Марио Куомо, всегда двигая нас к свету|Майк Барникл|4 января 2015 г.|DAILY BEAST
Вкус металлических столовых приборов после многих лет использования пластика тоже может быть забавным.
Его первый день на свободе после 40 лет: приспособление к жизни на улице|Джастин Рорлих|3 января 2015 г.|DAILY BEAST
В предыдущие десятилетия хип-хоп был чем-то, что обычно проповедовали против, так же как рок-н-ролл и хэви-метал до этого.
Долой короля: христианство не прячется в шкафу Рэпа|Stereo Williams|28 декабря 2014|DAILY BEAST
Всевышний сотворил лекарства из земли, и мудрый человек не возненавидит их.
Библия, Версия Дуэ-Реймса|Разное
У Величия на небесах есть колония и народ на земле, которая в противном случае находится под властью лукавого.
Solomon and Solomonic Literature|Moncure Daniel Conway
Отдельные образцы могут быть слегка щелочными, особенно после полноценного приема пищи.
Руководство по клинической диагностике|Джеймс Кэмпбелл Тодд
Все, что есть на земле, снова вернется в землю, и все воды вернутся в море.
Библия, версия Дуэ-Реймса|Разные
С помощью жалких приспособлений того времени было трудно выжать пропитание из сопротивляющейся земли.
Неразгаданная загадка социальной справедливости | Стивен Ликок
Научные определения щелочноземельного металла и радий. Поскольку щелочноземельные металлы имеют два электрона на внешней оболочке, они легко реагируют с другими элементами и встречаются в природе только в соединениях. См. периодическую таблицу.
Научный словарь American Heritage®
Авторские права © 2011. Опубликовано издательством Houghton Mifflin Harcourt Publishing Company. Все права защищены.
Структурная химия щелочных и щелочноземельных металлов | Усовершенствованная структурная неорганическая химия
Фильтр поиска панели навигации Oxford AcademicAdvanced Структурная неорганическая химияАтомная, молекулярная и оптическая физикаФизика конденсированного состоянияКристаллографияКнигиЖурналы Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Oxford AcademicAdvanced Структурная неорганическая химияАтомная, молекулярная и оптическая физикаФизика конденсированного состоянияКристаллографияКнигиЖурналы Термин поиска на микросайте
Расширенный поиск
Иконка Цитировать Цитировать
Разрешения
- Делиться
- Твиттер
- Подробнее
Cite
Li, Wai-Kee, Gong-Du Zhou, and Thomas Chung Wai Mak,
«Структурная химия щелочных и щелочноземельных металлов»
,
Advanced Structural Inorganic Union
0 90 Crystallography Texts on Crystallography(
Oxford,
2008;
онлайн-издание,
Oxford Academic
, 1 мая 2008 г.
), https://doi.org/10.1093/acprof:oso/9780199216949.003.0012,
, по состоянию на 4 ноября 2022 г.
3
3
Выберите формат Выберите format.ris (Mendeley, Papers, Zotero).enw (EndNote).bibtex (BibTex).txt (Medlars, RefWorks)
Закрыть
Фильтр поиска панели навигации Oxford AcademicAdvanced Структурная неорганическая химияАтомная, молекулярная и оптическая физикаФизика конденсированного состоянияКристаллографияКнигиЖурналы Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Oxford AcademicAdvanced Структурная неорганическая химияАтомная, молекулярная и оптическая физикаФизика конденсированного состоянияКристаллографияКнигиЖурналы Термин поиска на микросайте
Advanced Search
Abstract
В этой главе рассматривается структурная химия элементов групп 1 и 2, кроме водорода. Для металлов 1-й группы особое внимание уделяется оксидам, нитриду лития, неорганическим комплексам щелочных металлов, соединениям метиллития, π-комплексам лития, натрия и калия, алкалидам и электрридам и др. Для металлов 2-й группы охват включает их комплексы, нитриды, низковалентные оксиды и нитриды, полимерные цепи, реактивы Гриньяра, металлоцены и др. Глава завершается разделом, посвященным комплексам щелочных и щелочноземельных металлов с обращенной краун-структурой.
Для металлов 1-й группы особое внимание уделяется оксидам, нитриду лития, неорганическим комплексам щелочных металлов, соединениям метиллития, π-комплексам лития, натрия и калия, алкалидам и электрридам и др. Для металлов 2-й группы охват включает их комплексы, нитриды, низковалентные оксиды и нитриды, полимерные цепи, реактивы Гриньяра, металлоцены и др. Глава завершается разделом, посвященным комплексам щелочных и щелочноземельных металлов с обращенной краун-структурой.
Предмет
Физика конденсированных средАтомная, молекулярная и оптическая физика Кристаллография
В настоящее время у вас нет доступа к этой главе.
Войти
Получить помощь с доступом
Получить помощь с доступом
Доступ для учреждений
Доступ к контенту в Oxford Academic часто предоставляется посредством институциональных подписок и покупок.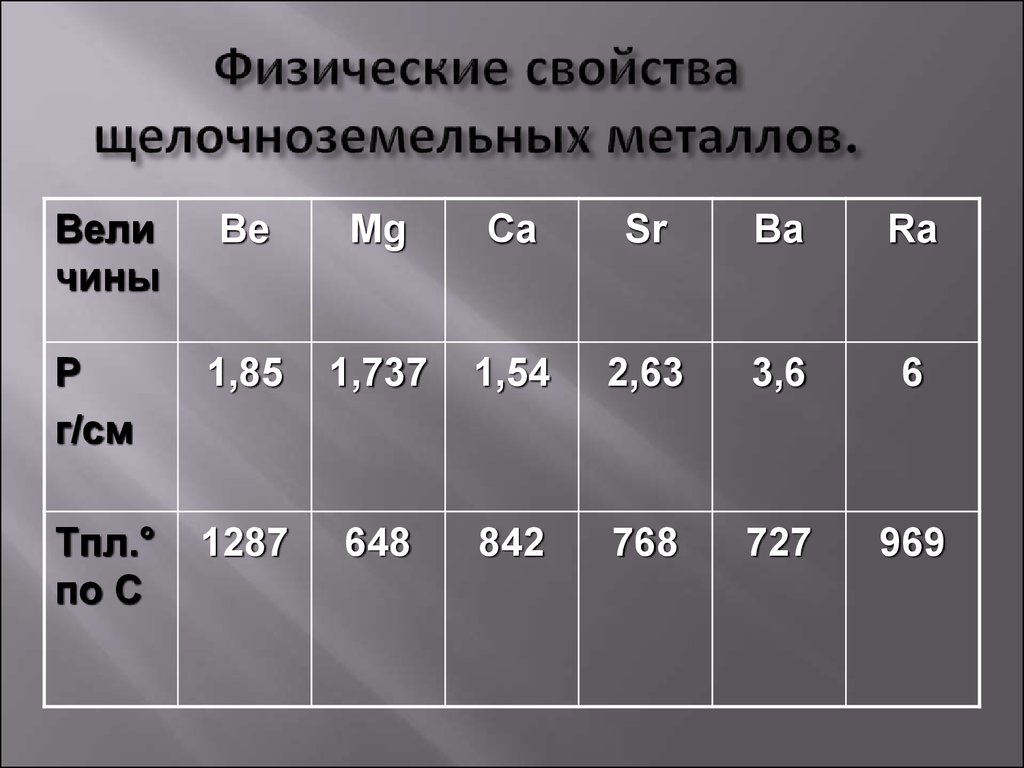 Если вы являетесь членом учреждения с активной учетной записью, вы можете получить доступ к контенту одним из следующих способов:
Если вы являетесь членом учреждения с активной учетной записью, вы можете получить доступ к контенту одним из следующих способов:
Доступ на основе IP
Как правило, доступ предоставляется через институциональную сеть к диапазону IP-адресов. Эта аутентификация происходит автоматически, и невозможно выйти из учетной записи с IP-аутентификацией.
Войдите через свое учреждение
Выберите этот вариант, чтобы получить удаленный доступ за пределами вашего учреждения. Технология Shibboleth/Open Athens используется для обеспечения единого входа между веб-сайтом вашего учебного заведения и Oxford Academic.
- Нажмите Войти через свое учреждение.
- Выберите свое учреждение из предоставленного списка, после чего вы перейдете на веб-сайт вашего учреждения для входа.
- Находясь на сайте учреждения, используйте учетные данные, предоставленные вашим учреждением.
 Не используйте личную учетную запись Oxford Academic.
Не используйте личную учетную запись Oxford Academic. - После успешного входа вы вернетесь в Oxford Academic.
Если вашего учреждения нет в списке или вы не можете войти на веб-сайт своего учреждения, обратитесь к своему библиотекарю или администратору.
Войти с помощью читательского билета
Введите номер своего читательского билета, чтобы войти в систему. Если вы не можете войти в систему, обратитесь к своему библиотекарю.
Члены общества
Доступ члена общества к журналу достигается одним из следующих способов:
Войти через сайт сообщества
Многие общества предлагают единый вход между веб-сайтом общества и Oxford Academic. Если вы видите «Войти через сайт сообщества» на панели входа в журнале:
- Нажмите Войти через сайт сообщества.
- При посещении сайта общества используйте учетные данные, предоставленные этим обществом.
- После успешного входа вы вернетесь в Oxford Academic.
Если у вас нет учетной записи сообщества или вы забыли свое имя пользователя или пароль, обратитесь в свое общество.
Вход через личный кабинет
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам. Смотри ниже.
Личный кабинет
Личную учетную запись можно использовать для получения оповещений по электронной почте, сохранения результатов поиска, покупки контента и активации подписок.
Некоторые общества используют личные аккаунты Oxford Academic для предоставления доступа своим членам.
Просмотр ваших зарегистрированных учетных записей
Щелкните значок учетной записи в правом верхнем углу, чтобы:
- Просмотр вашей личной учетной записи и доступ к функциям управления учетной записью.

