Изопропиловый спирт (пропанол-2, изопропанол, i-propanol, isopropyl alcohol) – химическое соединение, получившее широкое распространение благодаря растворяющей способности, дезинфицирующим и консервирующим свойствам. Этот спирт используют во многих видах промышленности, а также автомобилисты и медики.
Изопропиловый спирт – что это такое?
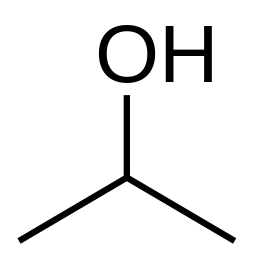
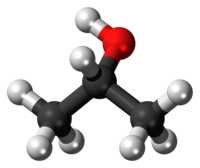
Изопропиловый спирт – вторичный одноатомный спирт. Химическая формула изопропанола СН3 – СН (ОН) – СН3. Изопропанол можно рассматривать как производное насыщенного углеводорода пропана СН3 – СН2 – СН3, в молекуле которого один атом водорода замещен на спиртовую — гидроксильную группу (-ОН). Поскольку гидроксильная группа в молекуле одна, то спирт называют одноатомным. Как видно из химической формулы изопропилового спирта, углерод, связанный с гидроксильной группой, соединен с двумя группами СН3. Поэтому спирт называют вторичным.
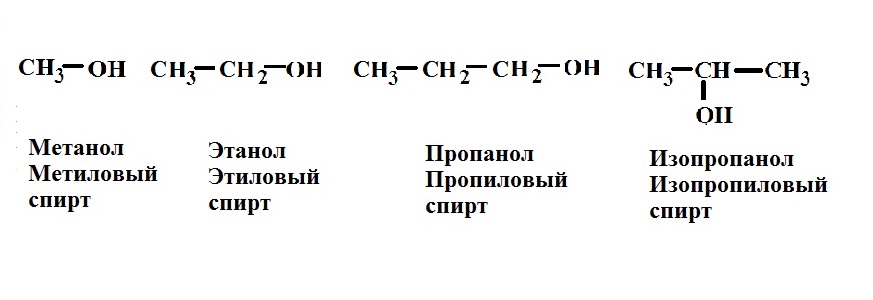
Структурная формула изопропилового спирта, а также формулы некоторых других одноатомных спиртов приведены на рисунке.
Физические свойства
Многие свойства изопропанола, температура кипения например, обусловлены наличием спиртовой группы (-ОН). Эта группа обладает высокой полярностью. В результате чего группа –ОН одной молекулы изопропанола образует связь с группой –ОН другой молекулы изопропанола. Таким образом, молекулы ассоциируются, то есть соединяются между собой. Такую связь называют водородной. Она слабая, но имеет большое значение в природе.
Благодаря водородным связям вода H2O при обычных условиях — жидкость, а не газ, как, например, похожее по строению вещество H2S сероводород. Именно наличие водородных связей приводит к тому, что твердая фаза воды – лед — имеет меньшую плотность в природе, чем жидкая фаза, в результате чего лед не тонет.
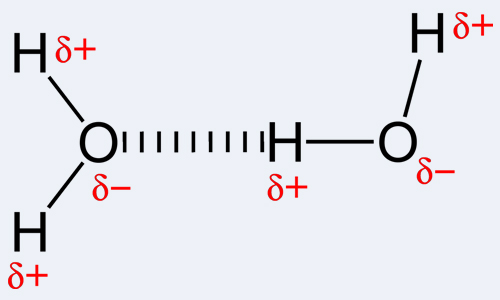
Образование водородных связей объясняет высокую температуру кипения изопропилового спирта и других низкомолекулярных спиртов в сравнении с соединениями схожего строения. Например, температура кипения пропана -42 °С, то есть пропан при любых температурах выше -42°С находится в газообразном состоянии. Температура кипения изопропилового спирта намного выше и составляет 82,4 °С. Это означает, что изопропанол при обычной температуре находится в жидком состоянии.
Если сравнить температуру кипения изопропилового спирта и метилового, то у первого она несколько выше: 82 градуса против 65. Это означает, что при обычных условиях изопропиловый спирт меньше испаряется, чем метиловый.
Температура плавления и температура кипения изопропилового спирта и некоторых других соединений представлены в таблице.
| Вещество | Температура кипения, оС | Температура плавления, оС |
| Метанол | 65 | -98 |
| Этанол | 78 | -117 |
| Пропанол | 97 | -127 |
| Изопропанол | 82 | -88 |
| Пропан | -42 | -190 |
Образование водородных связей между спиртовыми группами изопропанола и молекулами воды обуславливает растворимость этого спирта в воде. Растворимость зависит от количества углеродных атомов в цепи, чем их меньше, тем лучше растворяется спирт. Поэтому среди спиртов наибольшей растворимостью в воде обладает метанол, который можно смешать с водой в любом соотношении. Этанол растворяется в воде чуть хуже метанола, а изопропанол — хуже этанола.
Основные характеристики изопропилового спирта
Растворяется в ацетоне, в бензоле хорошо растворяется, смешивается с водой, эфиром, этанолом.
Плотность 0,7851 г/см3 (20 °С).
Нижний предел взрываемости — 2,5% (по объему).
Температура плавления -89,5 °С.
Температура кипения +82,4°С.
Зависимость температуры кипения изопропилового спирта от давления представлена в таблице.
| Давление паров, мм рт.ст. | Температура кипения, оС |
| 1 | -26,1 |
| 10 | 2,4 |
| 40 | 23,8 |
| 100 | 39,5 |
| 400 | 67,8 |
| 1020,7 | 90 |
Химические свойства
Изопропиловый спирт представляет собой бесцветную жидкость. Обладает характерным запахом, не похожим на запах этилового спирта. Не проводит электрический ток.
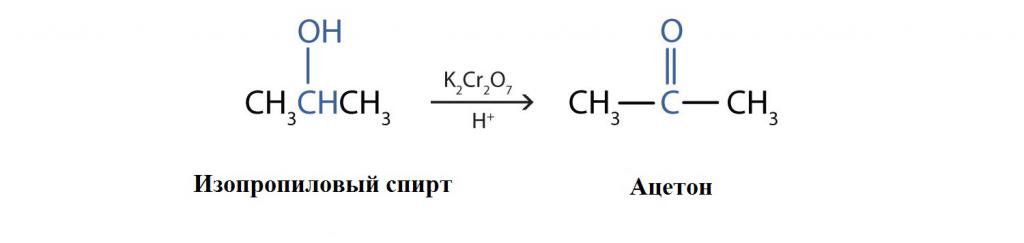
Вступает в многочисленные химические реакции, что используется для промышленных синтезов. Большая часть произведенного изопропилового спирта идет на производство ацетона. Для получения ацетона изопропанол необходимо окислить сильным окислителем – смесью K2Cr2O7 + H2SO4 или KMnO4 + H2SO4.
Получение
В России в 2017 году произведено около 40 тыс. тонн изопропилового спирта, почти на 20% меньше, чем в 2016 году. Объем производства достаточно мал — за этот же период метанола произведено почти 4 млн тонн.
Производят изопропиловый спирт в России два предприятия: ЗАО «Завод синтетического спирта» в городе Орске Оренбургской области и ООО «Синтез Ацетон» в городе Дзержинске Нижегородской области.

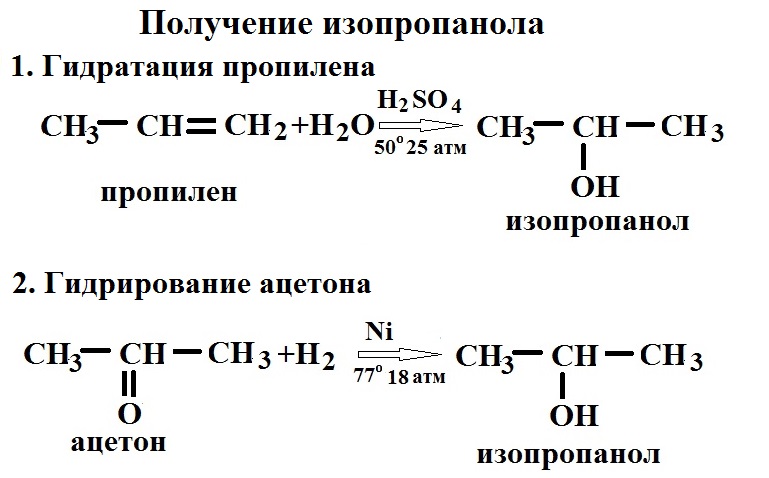
В Орске производят изопропанол методом сернокислотной гидратации пропилена или пропан-пропиленовой фракции, полученной из газов термического или каталитического крекинга. Получают два вида изопропанола, отличающихся степенью очистки: технический (87%) и абсолютизированный (99,95%). В Дзержинске изопропанол получают гидрированием ацетона.
Побочным продуктом при получении изопропилового спирта гидратацией пропилена является диизопропиловый спирт, который представляет особую ценность как вещество, имеющее высокое октановое число, равное 98.
Применение
Изопропиловый спирт – отличный растворитель, поэтому имеет широкую сферу применения. Его используют в основном в химической промышленности, а также в нефтеперерабатывающей, лесохимической, мебельной, медицинской, пищевой, парфюмерной отраслях промышленности, в полиграфии, домашнем хозяйстве. Направления применения:
- растворитель,
- консервант,
- обезвоживающее средство,
- экстрагент примесей,
- стабилизатор,
- антиобледенитель.
Применение изопропанола в химической и автомобильной промышленности
Применение в химической промышленности следующее:
- сырье для производства ацетона,
- производство пластмасс – полиэтилена низкого давления и полипропилена,
- синтез изопропилацетата,
- производство инсектицидов,
- растворитель при производстве этилцеллюлозы, ацетилцеллюлозы, нитроцеллюлозы в лакокрасочной промышленности,
- безопасная транспортировка нитроцеллюлозы (в нее добавляют 30% изопропанола),
- экстрагент в тонкой химической технологии.
- применение в нефтеперерабатывающей промышленности:
- растворитель карбамида, применяемого для депарафинизации дизельного топлива,
- добавка к маслам, усиливающая их антикоррозионные свойства и понижающая температуру застывания,
- «удаление» воды из бензиновых баков.
Вода попадает в топливные магистрали и баки нефтебаз путем конденсации из влажного воздуха. При низких температурах она замерзает и может образовать ледяную пробку. При добавлении абсолютированного изопропанола вода в нем растворяется и не замерзает.
В автомобильной промышленности:
- «удаление» воды из бензобаков путем ее растворения,
- как компонент топлива для повышения октанового числа и уменьшения токсичных выбросов,
- антиобледенитель ветрового стекла,
- антифриз для радиаторов,
- удаление тормозной жидкости с гидравлических тормозных систем.

Применение изопропанола в других видах хозяйственной деятельности
Применение в мебельной и лесохимической промышленности:
- экстракция смол из древесины в смеси с другими растворителями,
- снятие старого лакового покрытия, растворитель французской полировки, клеев, масел,
- связующее вещество в полиролях и очистителях.
В полиграфии изопропанол применяют для увлажнения в печатных процессах. В электронике — в качестве растворителя для очистки контактных разъемов, магнитных лент, головок дисков, лазерных линз, для удаления термопасты, очистки клавиатуры, ЖК-мониторов, стеклянных экранов. Нельзя применять его только для очистки винила, так как изопропанол вступает с ним в реакцию.
Применение в медицинской промышленности и медицине:
- входит в состав антисептических растворов, пропитывающих жидкостей для салфеток,
- обеззараживающее средство для протирания места инъекции,
- 75% водный раствор используют как дезинфицирующее средство для рук,
- дезинфицирующие тампоны,
- осушитель для профилактики отита,
- консервирующее средство для сохранения генетического материала и анализов (менее токсичен, чем формальдегид).
Изопропанол имеет преимущества перед этанолом: более выраженное антисептическое действие и низкую цену. Поэтому в тех случаях, когда раньше применяли этанол, сейчас используют изопропанол.
В косметической и парфюмерной промышленностях изопропанол применяют в производстве:
- косметических средств,
- средств личной гигиены,
- духов, одеколонов, лаков.
В пищевой промышленности изопропанол используют при производстве замороженных продуктов в качестве хладоносителя.
В домашнем хозяйстве:
- для очищения различных поверхностей, кроме резиновых и виниловых,
- для удаления пятен с тканей, древесины,
- для удаления клея от наклеек (на бумажные изопропанол не действует).
Токсичность
Изопропанол применяется в медицине в качестве местного антисептика. При местном использовании быстро испаряется и не оказывает негативного влияния.
При вдыхании паров раздражает дыхательные пути, может вызвать головную боль. Высокая концентрация изопропанола в воздухе тормозит работу ЦНС, приводит к потере сознания. Поэтому работать с изопропанолом можно только в хорошо проветриваемом помещении.
Внутрь изопропанол не применяется, поскольку он токсичен. Попадая в печень, превращается в ядовитое вещество — ацетон, поражающий печень, почки и головной мозг. 200 мл изопропанола являются смертельной дозой.
Изопропиловый спирт — Википедия
| Изопропанол | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Пропан-2-ол |
| Традиционные названия | Изопропиловый спирт |
| Хим. формула | C3H8O |
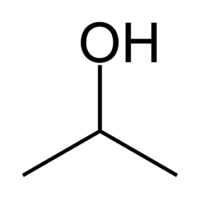
| Рац. формула | CH3CH(OH)CH3 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 60,09 г/моль |
| Плотность | 0,7851 г/см³ |
| Динамическая вязкость | 0,00243 Па·с |
| Энергия ионизации | 10,1 ± 0,1 эВ[1] |
| Термические свойства | |
| Т. плав. | -89,5 °C |
| Т. кип. | 82,4 °C |
| Т. всп. | 11,7 °C |
| Т. свспл. | 400 °C |
| Пр. взрв. | 2 ± 1 об.%[1] |
| Мол. теплоёмк. | 155,2 Дж/(моль·К) |
| Давление пара | 4,4 кПа при 20 °C |
| Химические свойства | |
| pK a | 16,5 |
| Растворимость в бензоле | хорошо растворим |
| Растворимость в ацетоне | растворим |
| Оптические свойства | |
| Показатель преломления | 1,3776 (nD, 20°C) |
| Структура | |
| Дипольный момент | 1,66 Д |
| Классификация | |
| Рег. номер CAS | 67-63-0 |
| PubChem | 3776 |
| Рег. номер EINECS | 200-661-7 |
| SMILES | |
| InChI | |
| RTECS | NT8050000 |
| ChEBI | 17824 и 43588 |
| Номер ООН | 1219 |
| ChemSpider | 3644 |
| Безопасность | |
| ЛД50 | 12800 мг/кг (кролик) |
| Токсичность | Класс опасности 3 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Изопропи́ловый спирт (пропано́л-2, втор-пропанол, изопропано́л, диметилкарбино́л, ИПС) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует изомер изопропанола — пропанол-1.
При нормальных условиях прозрачная, бесцветная жидкость с резким запахом и мягким горьким вкусом[2].
Изопропиловый спирт используется в качестве заменителя этилового спирта в косметике, парфюмерии, бытовой химии, жидкостей для автомобилей, медицинских целях, в средствах для очистки стёкол, оргтехники и как растворитель органических веществ промышленности.
В развитых странах изопропанол широко используется в товарах личной гигиены и в медицине, благодаря своей относительно низкой токсичности[3].
75 % водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь клеточные мембраны бактерий, таким образом обеспечивает более высокую эффективность и лучшее обеззараживание [4].
Изопропиловый спирт также используется в медицине в качестве вспомогательного компонента профилактического средства от наружного отита[5].
Эффективен при лечении дерматита протиранием пораженных участков кожи, с малым вредным влиянием на кожу.
Как и все летучие спирты, огнеопасен. Умеренно токсичен, требует осторожного обращения.
Свойства
Химические свойства
Рациональная химическая формула изопропилового спирта CH 3 CH ( OH ) CH 3 {\displaystyle {\ce {Ch4CH(OH)Ch4}}} .
Изопропанол обладает всеми свойствами вторичных спиртов жирного ряда, образует простые и сложные эфиры.
Гидроксильная группа может быть вытеснена галогенами.
С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол.
При дегидрировании превращается в ацетон[6].
Реагирует с сильными окислителями.
В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения.
Растворяет некоторые виды пластмасс и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резким, чем у этанола, по запаху их можно в некоторых случаях отличить.
Коэффициент преломления nD = 1,3776 при 20 °C. Динамическая вязкость при стандартных условиях 2,43 мПа·с — немного более вязкий, чем вода . Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К). Удельная теплота сгорания 34,1 МДж/кг.
Пар хорошо смешивается с воздухом, в диапазоне взрывоопасных концентраций образует взрывчатые смеси. Давление насыщенного пара при 20 °C — 4,4 кПа. Относительная плотность пара по воздуху — 2,1, относительная плотность смеси насыщенный пар/воздух — 1,05 при 20 °C.
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях.
С водой образует азеотропную смесь 87,9 % изопропилового спирта с температурой кипения 80,2 °C.
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице, при замерзании концентрированных растворов наблюдается переохлаждение[7]:
| Концентрация спирта, об % | Концентрация спирта, вес. % | Температура замерзания, °C |
|---|---|---|
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Получение
Применяются два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена[8][9].
Основным способом получения изопропанола в российской промышленности является сернокислотная гидратация пропилена
- CH 3 CH = CH 2 + H 2 SO 4 ⟶ ( CH 3 ) 2 CHOSO 2 OH + H 2 O ⟶ ( CH 3 ) 2 CHOH {\displaystyle {\ce {Ch4CH=Ch3 + h3SO4 ->(Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH}}} .
Сырьем может служить, в том числе кроме пропилена, пропан-пропиленовая фракция с содержанием пропилена 30—90 % (фракция получаемая при пиролизе и крекинге нефти). Сейчас начинают чаще использовать чистый пропилен, так как в этом случае процесс можно вести при невысоких давлениях, при этом существенно снижается образование побочных продуктов реакции — полимеров и ацетона.
На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата ( CH 3 ) 2 CHOSO 2 OH {\displaystyle {\ce {(Ch4)2CHOSO2OH}}} , серной кислоты H 2 SO 4 {\displaystyle {\ce {h3SO4}}} и воды H 2 O {\displaystyle {\ce {h3O}}} . На второй стадии процесса — сернокислотный экстракт нагревается с водой и отгоняется образующийся изопропиловый спирт.
Прямую гидратацию пропилена осуществляют в основном в присутствии катализатора — (в скобках указаны условия процессов): ортофосфорной кислоты H 3 PO 4 {\displaystyle {{\ce {h4PO4}}}} на твёрдом неорганическом носителе при 240—260°С и 2,5—6,5 МПа) или на носителе из катионообменной смолы при 130—160°С и 8,0—10,0 МПа.
Изопропиловый спирт получают также окислением алканов воздухом, а также и другими способами[6].
Современный способ гидрирования ацетона водородом:
- C H 3 C O C H 3 + H 2 → k a t C H 3 C H ( O H ) C H 3 {\displaystyle \mathrm {CH_{3}COCH_{3}+H_{2}{\xrightarrow {kat}}CH_{3}CH(OH)CH_{3}} }
Гидрирование ацетона впаровой фазе в присутствии твёрдого медно-никельхромитного катализатора[10][11].
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск)[12] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)[11][13].
Применение
Изопропиловый спирт используют для получения:
По причине особого государственного регулирования этанола, изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием.
Медицина
70 % изопропиловый спирт применяется вместо этилового спирта в качестве антисептика для пропитки медицинских салфеток.
Влияние на человека
- Ингаляционное
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест 0,6 мг/м³ (ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает[14].
Изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству изопропиловый спирт заменяет этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пламя, полностью разлагается на простые составляющие — воду и углекислый газ, которые не вызывают раздражений и иных побочных эффектов. При горении с достаточным избытком воздуха изопропанол не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости с площадью менее 20 см² в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций у людей[15].
- Пероральное
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко[2].
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола, если только не выпил единовременно от 500 мл.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов[2].
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием[14], наркотический эффект от приёма изопропанола почти в 2 раза превышает аналогичный эффект этанола[16]. Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов вызывает состояние глубокого наркоза и смерть[15].
При длительном воздействии больших концентраций паров в воздухе вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта человеку потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Длительное вдыхание воздуха с концентрацией, значительно превышающем ПДК, может вызвать потерю сознания. Тяжёлое отравление изопропиловым спиртом происходит редко.
Примечания
- ↑ 1 2 http://www.cdc.gov/niosh/npg/npgd0359.html
- ↑ 1 2 3 R. J. Slaughter, R. W. Mason, D. M. G. Beasley, J. A. Vale, L. J. Schep. Isopropanol poisoning // Clinical Toxicology (Philadelphia, Pa.). — 2014-06-01. — Т. 52, вып. 5. — С. 470–478. — ISSN 1556-9519. — DOI:10.3109/15563650.2014.914527.
- ↑ Papa, A. J. «Propanols» // Ullmann’s Encyclopedia of Industrial Chemistry : Weinheim: Wiley-VCH. — 2005.
- ↑ «Guide to Local Production: WHO-recommended Handrub Formulations» (англ.) // World Health Organization. — 2009. — Август.
- ↑ Otitis Externa (Swimmer’s Ear) (26 февраля 2010). Проверено 21 февраля 2016. Архивировано 26 февраля 2010 года.
- ↑ 1 2 ХиМиК.Ру — Изопропиловый спирт
- ↑ Ссылка один (англ.),Ссылка два
- ↑ «Isopropyl Alcohol, by John E. Logsdon and Richard A. Loke», Kirk‑Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc, Article Online Posting Date: December 4, 2000
- ↑ A. J. Papa (2005), «Propanols», Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_173
- ↑ СПОСОБ ПОЛУЧЕНИЯ ПРОПАНОЛА-2 — Патент РФ 2047590
- ↑ 1 2 ООО Синтез Ацетон (недоступная ссылка — история). Проверено 26 ноября 2011. Архивировано 21 марта 2012 года.
- ↑ О заводе | Завод синтетического спирта
- ↑ ПРОИЗВОДСТВО ИЗОПРОПИЛОВОГО СПИРТА В РОССИИ
- ↑ 1 2 ГОСТ 9805-84. Спирт изопропиловый. Технические условия[1]
- ↑ 1 2 Review of Inhalants: Euphoria to Dysfunction Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.,National Institute on Drug Abuse (недоступная ссылка — история). Проверено 10 августа 2011. Архивировано 15 октября 2011 года.
- ↑ «Достоинства и недостатки современных кожных антисептиков» С. В. Волкова, Е. В. Клементенок
Изопропиловый спирт температура кипения
Изопропиловый спирт (пропанол-2, изопропанол, i-propanol, isopropyl alcohol) – химическое соединение, получившее широкое распространение благодаря растворяющей способности, дезинфицирующим и консервирующим свойствам. Этот спирт используют во многих видах промышленности, а также автомобилисты и медики.
Изопропиловый спирт – что это такое?
Изопропиловый спирт – вторичный одноатомный спирт. Химическая формула изопропанола СН3 – СН (ОН) – СН3. Изопропанол можно рассматривать как производное насыщенного углеводорода пропана СН3 – СН2 – СН3, в молекуле которого один атом водорода замещен на спиртовую — гидроксильную группу (-ОН). Поскольку гидроксильная группа в молекуле одна, то спирт называют одноатомным. Как видно из химической формулы изопропилового спирта, углерод, связанный с гидроксильной группой, соединен с двумя группами СН3. Поэтому спирт называют вторичным.

Структурная формула изопропилового спирта, а также формулы некоторых других одноатомных спиртов приведены на рисунке.

Физические свойства
Многие свойства изопропанола, температура кипения например, обусловлены наличием спиртовой группы (-ОН). Эта группа обладает высокой полярностью. В результате чего группа –ОН одной молекулы изопропанола образует связь с группой –ОН другой молекулы изопропанола. Таким образом, молекулы ассоциируются, то есть соединяются между собой. Такую связь называют водородной. Она слабая, но имеет большое значение в природе.
Благодаря водородным связям вода H2O при обычных условиях — жидкость, а не газ, как, например, похожее по строению вещество H2S сероводород. Именно наличие водородных связей приводит к тому, что твердая фаза воды – лед — имеет меньшую плотность в природе, чем жидкая фаза, в результате чего лед не тонет.

Образование водородных связей объясняет высокую температуру кипения изопропилового спирта и других низкомолекулярных спиртов в сравнении с соединениями схожего строения. Например, температура кипения пропана -42 °С, то есть пропан при любых температурах выше -42°С находится в газообразном состоянии. Температура кипения изопропилового спирта намного выше и составляет 82,4 °С. Это означает, что изопропанол при обычной температуре находится в жидком состоянии.
Если сравнить температуру кипения изопропилового спирта и метилового, то у первого она несколько выше: 82 градуса против 65. Это означает, что при обычных условиях изопропиловый спирт меньше испаряется, чем метиловый.
Температура плавления и температура кипения изопропилового спирта и некоторых других соединений представлены в таблице.
| Вещество | Температура кипения, о С | Температура плавления, о С |
| Метанол | 65 | -98 |
| Этанол | 78 | -117 |
| Пропанол | 97 | -127 |
| Изопропанол | 82 | -88 |
| Пропан | -42 | -190 |
Образование водородных связей между спиртовыми группами изопропанола и молекулами воды обуславливает растворимость этого спирта в воде. Растворимость зависит от количества углеродных атомов в цепи, чем их меньше, тем лучше растворяется спирт. Поэтому среди спиртов наибольшей растворимостью в воде обладает метанол, который можно смешать с водой в любом соотношении. Этанол растворяется в воде чуть хуже метанола, а изопропанол — хуже этанола.
Основные характеристики изопропилового спирта
Растворяется в ацетоне, в бензоле хорошо растворяется, смешивается с водой, эфиром, этанолом.
Плотность 0,7851 г/см 3 (20 °С).
Нижний предел взрываемости — 2,5% (по объему).
Температура плавления -89,5 °С.
Температура кипения +82,4°С.
Зависимость температуры кипения изопропилового спирта от давления представлена в таблице.
| Давление паров, мм рт.ст. | Температура кипения, о С |
| 1 | -26,1 |
| 10 | 2,4 |
| 40 | 23,8 |
| 100 | 39,5 |
| 400 | 67,8 |
| 1020,7 | 90 |
Химические свойства
Изопропиловый спирт представляет собой бесцветную жидкость. Обладает характерным запахом, не похожим на запах этилового спирта. Не проводит электрический ток.
Вступает в многочисленные химические реакции, что используется для промышленных синтезов. Большая часть произведенного изопропилового спирта идет на производство ацетона. Для получения ацетона изопропанол необходимо окислить сильным окислителем – смесью K2Cr2O7 + H2SO4 или KMnO4 + H2SO4.

Получение
В России в 2017 году произведено около 40 тыс. тонн изопропилового спирта, почти на 20% меньше, чем в 2016 году. Объем производства достаточно мал — за этот же период метанола произведено почти 4 млн тонн.
Производят изопропиловый спирт в России два предприятия: ЗАО «Завод синтетического спирта» в городе Орске Оренбургской области и ООО «Синтез Ацетон» в городе Дзержинске Нижегородской области.

В Орске производят изопропанол методом сернокислотной гидратации пропилена или пропан-пропиленовой фракции, полученной из газов термического или каталитического крекинга. Получают два вида изопропанола, отличающихся степенью очистки: технический (87%) и абсолютизированный (99,95%). В Дзержинске изопропанол получают гидрированием ацетона.
Побочным продуктом при получении изопропилового спирта гидратацией пропилена является диизопропиловый спирт, который представляет особую ценность как вещество, имеющее высокое октановое число, равное 98.

Применение
Изопропиловый спирт – отличный растворитель, поэтому имеет широкую сферу применения. Его используют в основном в химической промышленности, а также в нефтеперерабатывающей, лесохимической, мебельной, медицинской, пищевой, парфюмерной отраслях промышленности, в полиграфии, домашнем хозяйстве. Направления применения:
- растворитель,
- консервант,
- обезвоживающее средство,
- экстрагент примесей,
- стабилизатор,
- антиобледенитель.
Применение изопропанола в химической и автомобильной промышленности
Применение в химической промышленности следующее:
- сырье для производства ацетона,
- производство пластмасс – полиэтилена низкого давления и полипропилена,
- синтез изопропилацетата,
- производство инсектицидов,
- растворитель при производстве этилцеллюлозы, ацетилцеллюлозы, нитроцеллюлозы в лакокрасочной промышленности,
- безопасная транспортировка нитроцеллюлозы (в нее добавляют 30% изопропанола),
- экстрагент в тонкой химической технологии.
- применение в нефтеперерабатывающей промышленности:
- растворитель карбамида, применяемого для депарафинизации дизельного топлива,
- добавка к маслам, усиливающая их антикоррозионные свойства и понижающая температуру застывания,
- «удаление» воды из бензиновых баков.
Вода попадает в топливные магистрали и баки нефтебаз путем конденсации из влажного воздуха. При низких температурах она замерзает и может образовать ледяную пробку. При добавлении абсолютированного изопропанола вода в нем растворяется и не замерзает.
В автомобильной промышленности:
- «удаление» воды из бензобаков путем ее растворения,
- как компонент топлива для повышения октанового числа и уменьшения токсичных выбросов,
- антиобледенитель ветрового стекла,
- антифриз для радиаторов,
- удаление тормозной жидкости с гидравлических тормозных систем.

Применение изопропанола в других видах хозяйственной деятельности
Применение в мебельной и лесохимической промышленности:
- экстракция смол из древесины в смеси с другими растворителями,
- снятие старого лакового покрытия, растворитель французской полировки, клеев, масел,
- связующее вещество в полиролях и очистителях.
В полиграфии изопропанол применяют для увлажнения в печатных процессах. В электронике — в качестве растворителя для очистки контактных разъемов, магнитных лент, головок дисков, лазерных линз, для удаления термопасты, очистки клавиатуры, ЖК-мониторов, стеклянных экранов. Нельзя применять его только для очистки винила, так как изопропанол вступает с ним в реакцию.
Применение в медицинской промышленности и медицине:
- входит в состав антисептических растворов, пропитывающих жидкостей для салфеток,
- обеззараживающее средство для протирания места инъекции,
- 75% водный раствор используют как дезинфицирующее средство для рук,
- дезинфицирующие тампоны,
- осушитель для профилактики отита,
- консервирующее средство для сохранения генетического материала и анализов (менее токсичен, чем формальдегид).
Изопропанол имеет преимущества перед этанолом: более выраженное антисептическое действие и низкую цену. Поэтому в тех случаях, когда раньше применяли этанол, сейчас используют изопропанол.
В косметической и парфюмерной промышленностях изопропанол применяют в производстве:
- косметических средств,
- средств личной гигиены,
- духов, одеколонов, лаков.
В пищевой промышленности изопропанол используют при производстве замороженных продуктов в качестве хладоносителя.
В домашнем хозяйстве:
- для очищения различных поверхностей, кроме резиновых и виниловых,
- для удаления пятен с тканей, древесины,
- для удаления клея от наклеек (на бумажные изопропанол не действует).
Токсичность
Изопропанол применяется в медицине в качестве местного антисептика. При местном использовании быстро испаряется и не оказывает негативного влияния.
При вдыхании паров раздражает дыхательные пути, может вызвать головную боль. Высокая концентрация изопропанола в воздухе тормозит работу ЦНС, приводит к потере сознания. Поэтому работать с изопропанолом можно только в хорошо проветриваемом помещении.
Внутрь изопропанол не применяется, поскольку он токсичен. Попадая в печень, превращается в ядовитое вещество — ацетон, поражающий печень, почки и головной мозг. 200 мл изопропанола являются смертельной дозой.
| Изопропанол | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование | Пропан-2-ол |
| Традиционные названия | Изопропиловый спирт |
| Хим. формула | C3H8O |
| Рац. формула | CH3CH(OH)CH3 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 60,09 г/моль |
| Плотность | 0,7851 г/см³ |
| Динамическая вязкость | 0,00243 Па·с |
| Энергия ионизации | 10,1 ± 0,1 эВ [1] |
| Термические свойства | |
| Т. плав. | -89,5 °C |
| Т. кип. | 82,4 °C |
| Т. всп. | 11,7 °C |
| Т. свспл. | 400 °C |
| Пр. взрв. | 2 ± 1 об.% [1] |
| Мол. теплоёмк. | 155,2 Дж/(моль·К) |
| Давление пара | 4,4 кПа при 20 °C |
| Химические свойства | |
| pKa | 16,5 |
| Растворимость в бензоле | хорошо растворим |
| Растворимость в ацетоне | растворим |
| Оптические свойства | |
| Показатель преломления | 1,3776 ( nD , 20°C) |
| Структура | |
| Дипольный момент | 1,66 Д |
| Классификация | |
| Рег. номер CAS | 67-63-0 |
| PubChem | 3776 |
| Рег. номер EINECS | 200-661-7 |
| SMILES | |
| RTECS | NT8050000 |
| ChEBI | 17824 и 43588 |
| Номер ООН | 1219 |
| ChemSpider | 3644 |
| Безопасность | |
| ЛД50 | 12800 мг/кг (кролик) |
| Токсичность | Класс опасности 3 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Изопропи́ловый спирт (пропано́л-2, втор-пропанол, изопропано́л, диметилкарбино́л, сокр. ИПС — широко используемое сокращение) — органическое соединение, простейший вторичный одноатомный спирт алифатического ряда. Существует 1 изомер изопропанола — пропанол-1, обладающий прямой цепью.
При нормальных условиях прозрачная, бесцветная жидкость с резким характерным запахом и мягким горьким вкусом, типичным для спиртов с короткой углеводородной цепью [2] .
Как и все летучие спирты, огнеопасен. Токсичен (считается, что в 6 раз более этанола), требует осторожного обращения.
Содержание
Свойства [ править | править код ]
Химические свойства [ править | править код ]
Рациональная химическая формула изопропилового спирта CH 3 CH ( OH ) CH 3 <displaystyle <ce >> и является похожей на ацетон и подобные ему соединения, представляет собой разветвленную цепь с графической формулой .
Изопропанол обладает всеми свойствами вторичных спиртов жирного ряда, образует простые и сложные эфиры.
С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол.
При дегидрировании, например ферментом алкогольдегидрогеназой в организме млекопитающего, превращается в ацетон [3] .
Реагирует с сильными окислителями.
В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения.
Растворяет некоторые виды пластмасс и резины.
Физические свойства [ править | править код ]
Бесцветная жидкость с характерным спиртовым запахом, более резким и неприятным, чем у этанола, их можно отличить по запаху.
Коэффициент преломления nD = 1,3776 при 20 °C. Динамическая вязкость при стандартных условиях 2,43 мПа·с — немного более вязкий, чем вода . Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К) . Удельная теплота сгорания 34,1 МДж/кг .
Пар хорошо смешивается с воздухом, в диапазоне взрывоопасных концентраций образует взрывчатые смеси. Давление насыщенного пара при 20 °C — 4,4 кПа. Относительная плотность пара по воздуху — 2,1, относительная плотность смеси насыщенный пар/воздух — 1,05 при 20 °C.
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях.
С водой образует азеотропную смесь 87,9%-го изопропилового спирта с температурой кипения 80,2 °C.
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице, при замерзании концентрированных растворов наблюдается переохлаждение [4] :
| Концентрация спирта, об % | Концентрация спирта, вес. % | Температура замерзания, °C |
|---|---|---|
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
Получение [ править | править код ]
Применяются два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена [5] [6] .
Основным способом получения изопропанола в российской промышленности является сернокислотная гидратация пропилена
(Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH>>>»> CH 3 CH = CH 2 + H 2 SO 4 ⟶ ( CH 3 ) 2 CHOSO 2 OH + H 2 O ⟶ ( CH 3 ) 2 CHOH <displaystyle <ce (Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH>>> (Ch4)2CHOSO2OH + h3O -> (Ch4)2CHOH>>>»/> .
Сырьем может служить, в том числе кроме пропилена, пропан-пропиленовая фракция с содержанием пропилена 30—90 % (фракция получаемая при пиролизе и крекинге нефти). Сейчас начинают чаще использовать чистый пропилен, так как в этом случае процесс можно вести при невысоких давлениях, при этом существенно снижается образование побочных продуктов реакции — полимеров и ацетона.
На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата ( CH 3 ) 2 CHOSO 2 OH <displaystyle <ce <(Ch4)2CHOSO2OH>>> , серной кислоты H 2 SO 4 <displaystyle <ce >> и воды H 2 O <displaystyle <ce >> . На второй стадии процесса — сернокислотный экстракт нагревается с водой и отгоняется образующийся изопропиловый спирт.
Прямую гидратацию пропилена осуществляют в основном в присутствии катализатора — (в скобках указаны условия процессов): ортофосфорной кислоты H 3 PO 4 <displaystyle <<ce >>> на твёрдом неорганическом носителе при 240—260°С и 2,5—6,5 МПа) или на носителе из катионообменной смолы при 130—160°С и 8,0—10,0 МПа.
Изопропиловый спирт получают также окислением алканов воздухом, а также и другими способами [3] .
Современный способ гидрирования ацетона водородом:
C H 3 C O C H 3 + H 2 → k a t C H 3 C H ( O H ) C H 3 <displaystyle mathrm COCH_<3>+H_<2><xrightarrow >CH_<3>CH(OH)CH_<3>> > 3>
Гидрирование ацетона в паровой фазе в присутствии твёрдого медно-никельхромитного катализатора [7] [8] .
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск) [9] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск) [8] [10] .
Применение [ править | править код ]
Изопропиловый спирт используется в качестве заменителя этилового спирта в медицине (в последнее время очень активно, так как не уступает по антисептической активности этанолу), в косметике, парфюмерии, бытовой химии, жидкостей для автомобилей (стеклоомывающих в основном, а также антифризов), медицинских целях, в средствах для очистки стёкол, оргтехники и как растворитель органических веществ промышленности.
В развитых странах изопропанол широко используется в товарах личной гигиены и в медицине благодаря своей относительно низкой токсичности [11] .
75%-й водный раствор диметилкарбинола используется как дезинфицирующее средство для рук. Вода способствует проникновению сквозь клеточные мембраны бактерий, таким образом обеспечивая более высокую эффективность и лучшее обеззараживание [12] .
Изопропиловый спирт также используется в медицине в качестве вспомогательного компонента профилактического средства от наружного отита [13] .
Эффективен при лечении дерматита протиранием пораженных участков кожи, с малым вредным влиянием на кожу.
Изопропиловый спирт также используют как исходное сырье для синтеза:
По причине особого государственного регулирования этанола изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители). Часто используется при сварке оптических волокон для очистки волокна перед скалыванием.
Медицина [ править | править код ]
70%-й изопропиловый спирт применяется вместо этилового спирта в качестве антисептика для пропитки медицинских салфеток.
Влияние на человека [ править | править код ]
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест — 0,6 мг/м³ (ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает [14] .
Изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству изопропиловый спирт заменяет этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пламя, полностью разлагается на простые составляющие — воду и углекислый газ. При горении с достаточным избытком воздуха изопропанол не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций у людей [15] .
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко [2] .
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола, если только не выпил единовременно от 500 мл.
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов [2] .
Наркотические свойства [ править | править код ]
Изопропиловый спирт обладает наркотическим действием [14] , наркотический эффект от приёма изопропанола почти в 2 раза превышает аналогичный эффект этанола [16] . Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов, вызывает состояние глубокого наркоза и смерть [15] .
При длительном воздействии больших концентраций паров в воздухе вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта человеку потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Длительное вдыхание воздуха с концентрацией, значительно превышающем ПДК, может вызвать потерю сознания. Тяжёлое отравление изопропиловым спиртом происходит редко.
Химическая формула (рациональная) изопропилового спирта: CH3CH(OH)CH3.
Изопропанол обладает свойствами вторичных спиртов жирного ряда, в том числе образует простые и сложные эфиры. Гидроксильная группа может быть вытеснена представителями ряда галогенов. С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол. В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения. При дегидрировании превращается в ацетон. [2]
Реагирует с сильными окислителями. Агрессивен в отношении некоторых видов пластика и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резковатым по сравнению с этанолом (по чему их можно в некоторых случаях отличить), tплавления −89,5 °C, tкипения 82,4 °C, плотность 0,7851 г/см³ (при 20 °C), tвспышки 11,7 °C. Нижний предел взрываемости в воздухе 2,5 % по объёму (при 25 °C). Температура самовоспламенения 456 °C. Коэффициент преломления 1,3776 (в жидком состоянии, при 20 °C). Динамическая вязкость при стандартных условиях 2,43 мПа·с. Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К).
Пар хорошо смешивается с воздухом, легко образует взрывчатые смеси. Давление паров — 4,4 кПа (при 20 °C). Относительная плотность пара — 2,1, относительная плотность смеси пар/воздух — 1,05 (при 20 °C).
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях. С водой образует азеотропную смесь (87,9 % изопропилового спирта, tкипения 83,38 °C).
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице [3] :
| Концентрация спирта об % | Концентрация спирта вес % | Температура замерзания °C |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
Получение
Существует два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена. [4] [5]
Основным способом получения изопропанола в Российской промышленности является сернокислотная гидратация пропилена
Сырьем может служить пропан-пропиленовая фракция с содержанием пропилена 30-90 % (фракция пиролиза и крекинга нефти). Однако наблюдается тенденция к использованию чистого пропилена, так как в этом случае процесс можно вести при невысоких давлениях, резко снижается образование побочных продуктов реакции — полимеров и ацетона. На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (Ch4)2CHOSO2OH, H2SO4 и Н2О, на второй — сернокислотный экстракт нагревается с водой и удаляется образующийся изопропиловый спирт. Прямую гидратацию пропилена осуществляют в основном в присутствии твердого катализатора (в скобках указаны условия процессов): Н3РО4 на носителе (240—260°С; 2,5-6,5 МПа) или катионообменной смолы (130—160°С; 8,0-10,0 МПа). Изопропиловый спирт получают также окислением парафинов воздухом и другими способами. [2]
Гидрирование ацетона водородом (в фазе пара) в присутствии стационарного медно-никельхромитного катализатора. [6] [7]
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск) [8] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск) [9] [7]
Применение
Изопропиловый спирт используют для получения:
- ацетона (дегидрированием или неполным окислением)
- пероксида водорода
- метилизобутилкетона
- изопропилацетата
- изопропиламина.
По причине особого государственного регулирования этанола, изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
- косметики
- парфюмерии
- бытовой химии
- дезинфицирующих средств
- средства для автомобилей (антифриз, растворитель в зимних стеклоомывателях)
- репеллентов
- промывок печатных плат после пайки с флюсом, продается под названием «Очиститель универсальный».
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители).
Медицина
70 % изопропиловый спирт применяется вместо этилового спирта как антисептик для пропитки медицинских салфеток.
Влияние на человека
Оказывает раздражающее воздействие на глаза и дыхательные пути, при кратком воздействии больших концентраций паров вызывает головную боль. Может оказывать угнетающее действие на центральную нервную систему. Воздействие на уровне, значительно превышающем ПДК, может вызвать потерю сознания. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обуславливает его токсическое действие. Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто уже при дозах порядка 50 мл и более.
Предельно допустимая концентрация изопропанола в воздухе равна 10 миллиграммов на кубический метр.
Изопропанол органолептически заметно отличается от этанола и не может быть ошибочно принят за этанол. Имеет отличный от этанола запах, более «грубый». При приеме внутрь вызывает опьянение, сходное с алкогольным. Изопропанол окисляется в организме при участии альдегиддегидрогеназы до ацетона. Скорость окисления в среднем в 2 — 2,5 раза ниже, чем у этанола, поэтому опьянение изопропанолом очень стойкое. При частом употреблении к изопропанолу быстро развивается непереносимость, а в отдельных случаях — гиперчувствительность и аллергия. Хотя токсичность изопропанола примерно в 3,5 раза больше, чем у этанола, но при этом опьяняющее действие его также выше в 10 раз [источник не указан 546 дней] . По этой причине смертельных отравлений изопропанолом не зафиксировано, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола.
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием. [1] Наркотический эффект изопропанола почти в 2 раза превышает аналогичный эффект этанола. [10] Концентрация 1,2 %, воздействующая в течение 4 часов оказывает наркотический эффект. При аналогичном воздействии в течение 8 часов — в половине случаев наблюдается смертельный исход. [11]
Изопропиловый спирт — Isopropyl alcohol
| |||
| имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC | |||
| Другие имена
2-пропанол Изопропилового спирт затирание сек -пропил , спирт сек Пропанола изопропилового спирт я -PrOH Диметил карбинол IPA | |||
| Идентификаторы | |||
| 3D модель ( JSmol ) | |||
| 635639 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ИКГВ InfoCard | 100.000.601 | ||
| 1464 | |||
| KEGG | |||
| номер RTECS | NT8050000 | ||
| UNII | |||
| номер ООН | 1219 | ||
| |||
| свойства | |||
| С 3 Н 8 О | |||
| Молярная масса | 7001600960000000000 ♠60,096 г · моль -1 | ||
| Внешность | Бесцветная жидкость | ||
| плотность | 0,786 г / см 3 (20 ° С) | ||
| Температура плавления | -89 ° С (-128 ° F, 184 К) | ||
| Точка кипения | 82,6 ° С (180,7 ° F, 355,8 К) | ||
| Смешивается с водой | |||
| Растворимость | Смешивается с бензолом , хлороформом , этанолом , эфиром , глицерин ; растворим в ацетоне | ||
| войти P | 0,16 | ||
| Кислотность (р К ) | 16,5 | ||
| -45,794 · 10 -6 см 3 / моль | |||
| 1,3776 | |||
| вязкость | 2.86 с Р при 15 ° С 1,96 гр Р при 25 ° С 1,77 гр Р при 30 ° C | ||
| 1,66 D (газ) | |||
| Фармакология | |||
| D08AX05 ( ВОЗ ) | |||
| опасности | |||
| Основные опасности | легковоспламеняющийся | ||
| Паспорт безопасности | См: Страница данных Внешний MSDS | ||
| СГС пиктограммы |   | ||
| сигнальное слово СГС | Опасность | ||
| h325 , h419 , h436 | |||
| P210 , P261 , P305 + 351 + 338 | |||
| NFPA 704 |  | ||
| точка возгорания | Открытые чашки: 11,7 ° C (53,1 ° F, 284,8 К) закрытый тигль: 13 ° C (55 ° F) | ||
| 399 ° С (750 ° F, 672 К) | |||
| пределы взрываемости | 2-12.7% | ||
| 980 мг / м 3 (ДАС), 1225 мг / м 3 (СТЭЛ) | |||
| Смертельная доза или концентрация ( LD , LC ): | |||
| 12800 мг / кг (дермальный, кролик) 3600 мг / кг (перорально, мышь) 5045 мг / кг (перорально, крыса) 6410 мг / кг (перорально, кролик) | |||
| 53000 мг / м 3 (ингаляции, мышь) 12000 частей на миллион (крыса, 8 ч) | |||
| 16 000 частей на миллион (крыса, 4 ч) 12800 частей на миллион (мышь, 3 ч) | |||
| Пределы воздействия здоровья США ( NIOSH ): | |||
| PEL (допустимый) | С 400 частей на миллион (980 мг / м 3 ) | ||
| REL (рекомендуется) | СПВ 400 частей на миллион (980 мг / м 3 ) СТ 500 частей на миллион (1225 мг / м 3 ) | ||
| IDLH (Непосредственная опасность) | 2000 частей на миллион | ||
| Родственные соединения | |||
| 1-пропанол , этанол , 2-бутанол | |||
| Дополнительная страница данных | |||
| Показатель преломления ( п ), Диэлектрическая постоянная (ε г ) и т.д. | |||
Термодинамические | Фазовое поведение твердое тело-жидкость-газ | ||
| УФ , ИК , ЯМР , МС | |||
| За исключением случаев, когда указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
 Y проверить ( что ?) Y проверить ( что ?)  Y Y N N | |||
| ссылки Infobox | |||
Изопропиловый спирт ( ИЮПАК название пропан-2-ол ; обычно называют изопропанол или 2-пропанол) представляет собой соединение с химической формулой CH 3 CHOHCH 3 . Это бесцветное , воспламеняется химическое соединение с сильным запахом . В качестве изопропиловых групп , связанных с гидроксильной группой, это самый простым пример вторичного спирта , где спирт атом углерода присоединен к двум другим атомам углерода. Это структурный изомер из 1-пропанола и этилового эфира .
Он используется при изготовлении самых разнообразных промышленных и бытовых химических веществ, а также является общим компонентом химических веществ , таких как антисептики , дезинфицирующие и моющие средства.
имена
Изопропиловый спирт также известен как 2-пропанол, Sec -пропила спирта, IPA, или изопропанол. ИЮПАК считает изопропанол неверное имя в качестве углеводородного изопропан не существует.
свойства
Изопропиловый спирт смешивается в воде, этаноле , эфире и хлороформе . Оно растворяет этилцеллюлозу , поливинилбутираль , многие масла, алкалоиды, камедь и природные смолы. В отличие от этанола или метанола , изопропилового спирта не смешивается с растворами солей и могут быть отделены от водных растворов путем добавления соли , такие как хлорид натрия . Процесс просторечия называется высаливанием , и причины концентрируют изопропиловый спирт , чтобы отделить в отдельный слой.
Изопропиловый спирт образует азеотропную смесь с водой, которая дает температуру кипения 80,37 ° C (176,67 ° F) и композицией 87,7 мас% (91% по объему) изопропилового спирта. Водно-изопропил смеси спиртов привели к снижению точки плавления. Она имеет слегка горьковатый вкус, и это не безопасно пить.
Изопропиловый спирт становится все более вязким при понижении температуры и замерзает при -89 ° С (-128 ° F).
Изопропиловый спирт имеет максимальную оптическую плотность при 205 нм в качестве ультрафиолетовой и видимой области спектра.
Реакции
Изопропиловый спирт может быть окислен до ацетона , который является соответствующим кетоном . Это может быть достигнуто с помощью окислительных агентов , таких как хромовая кислота , или путем дегидрирования изопропилового спирта над медным нагретым катализатором :
- (СН 3 ) 2 СНОН → (СН 3 ) 2 СО + Н 2
Изопропиловый спирт часто используется в качестве как растворитель и гидрид источника в сокращении Меервейно-Ponndorf-Верлея и другие передачи гидрогенизации реакций. Изопропиловый спирт может быть превращен в 2-бромпропан с помощью трибромида фосфора , или дегидратирует до пропена при нагревании с серной кислотой .
Как и большинство спиртов, изопропиловый спирт реагирует с активными металлами , такими как калий с образованием алкоголятов , которые можно назвать isopropoxides . Реакция с алюминием (инициирована следом ртути ) используется для приготовления катализатора изопропоксида алюминия .
история
В 1920 году Standard Oil сначала получают изопропиловый спирт гидратацией пропена . Его используют главным образом в то время не было тереть спирт , а для окисления в ацетон , чей первой главной польза была в первой мировой войне для подготовки кордита , бездымного, низкий взрывной пропеллент.
производство
В 1994 году 1,5 миллиона тонн изопропилового спирта были произведены в Соединенных Штатах, Европе и Японии. Это в первую очередь получают путем объединения воды и пропена в реакции гидратации или путем гидрирования ацетона . Есть два маршрута для процесса гидратации и оба процесса требуют, чтобы изопропиловый спирт быть отделен от воды и других побочных продуктов путем перегонки . Изопропиловый спирт и вода образуют азеотроп и простая перегонка дает материал , который является 87,9% по массе изопропилового спирта и 12,1% по весу воды. Чистый ( безводный ) изопропиловый спирт производится путем азеотропной перегонки влажного изопропилового спирта с использованием либо диизопропиловый эфира или циклогексана в качестве азеотропных агентов.
Косвенная гидратация
Косвенная гидратация пропена реагирует с серной кислотой с образованием смеси сульфатов эфиров. Этот процесс может использовать низкокачественный пропен, и преобладает в США. Эти процессы дают прежде всего изопропиловый спирт , а не 1-пропанола, так как добавление воды или серной кислоты к пропена следует правилу Марковникова . После гидролиза этих сложных эфиров пара производит изопропиловый спирт, путем перегонки. Диизопропиловый эфир является значительным побочным продуктом этого процесса; он возвращается обратно в процесс и гидролизуют с получением желаемого продукта.
Прямая гидратация
Прямая гидратация реагирует пропна и воду, либо в газовой фазе или в жидкой фазе, при высоких давлениях в присутствии твердых или поддерживаемых кислотных катализаторов . Этот тип процесса обычно требует пропилена более высокой чистоты (> 90%). Прямая гидратация чаще используется в Европе.
Гидрирование ацетона
Сырой ацетон гидрирует в жидкой фазе над никелем Ренея или смесь из меди и оксида хрома с получением изопропилового спирта. Этот процесс полезен, когда она соединена с избытком производства ацетона, таких как процесс кумола .
Пользы

В 1990 г. были использованы 45000 метрических тонны изопропилового спирта в Соединенных Штатах, в основном , в качестве растворителя для покрытий или для промышленных процессов. В этом году было использовано 5400 тонн для бытовых целей и в продуктах личной гигиены. Изопропиловый спирт является популярным , в частности , для фармацевтического применения, из — за его низкую токсичность. Некоторые изопропиловый спирт используют в качестве промежуточного химического вещества. Изопропиловый спирт может быть превращен в ацетон, но процесс кумола является более значительным. Он также используется в качестве добавки к бензину .
растворитель
Изопропиловый спирт растворяет широкий спектр неполярных соединений. Кроме того , быстро испаряется, уходит почти нулевой следы масла, по сравнению с этанолом, и является относительно нетоксичным, по сравнению с альтернативными растворителями. Таким образом, он широко используется в качестве растворителя и в качестве моющей жидкости, особенно для растворения масла. Вместе с этанол, н-бутанол, и метанол, он принадлежит к группе растворителей, спиртов около 6,4 млн т из которых были использованы во всем мире в 2011 году.
Примеры такого применения включают в себя чистящие очки , электронные устройства , такие как контактные штифты (например , те , на ROM картриджей ), магнитной ленте и дисковых головок (таких , как те , в аудио- и видеомагнитофонов и гибких дисков дисков), Линзы лазеров в оптическом диске диски (например, компакт — диск , DVD ) и удаление термопасты с радиаторов и IC пакетов (например, ЦП ).
промежуточный
Изопропиловый спирт этерифицируют с получением изопропилацетата , другой растворитель. Он вступает в реакцию с сероуглеродом и гидроксидом натрия , чтобы дать isopropylxanthate натрия , в гербицид и флотации руды реагент. Изопропиловый спирт реагирует с тетрахлоридом титана и алюминия металла с получением титана и алюминия isopropoxides , соответственно, бывший катализатор, и последний химический реагент. Это соединение может служить в качестве химического реагента в себе, действуя в качестве донора в дигидрофосфате гидрирования с переносом .
медицинская
Спирт затирания , дезинфицирующее средство для рук , и дезинфицирующие колодки обычно содержат 60-70% раствор изопропилового спирта в воде . Вода требуется , чтобы открыть поры мембраны бактерий, который действует в качестве шлюза для изопропилового спирта. 75% об / об растворе в воде может быть использован в качестве дезинфицирующего средства для рук. Изопропиловый спирт используется в качестве вспомогательного средства в воде сушки для профилактики наружного отита , более известной как ухо пловца.
Раннее использует в качестве анестетика
Несмотря на то, изопропиловый спирт может быть использован для анестезии, многие его негативные атрибуты или недостатки запретить это использование. Изопропиловый спирт также может быть использован так же, как эфир в качестве растворителя или в качестве анестезирующего средства путем вдыхания паров или перорально. Ранние применения включали использование в качестве растворителя для общей анестезии мелких млекопитающих и грызунов ученых и некоторых ветеринары. Тем не менее, это было вскоре прекращено, так как возникло много осложнений, в том числе раздражение дыхательных путей, внутреннего кровотечения, а также зрительные и слуховые проблемы. В редких случаях наблюдается дыхательная недостаточность приводит к смерти животных.
автомобильный
Изопропиловый спирт является основным ингредиентом в «газовой сушилки» топливных присадок . В значительных количествах воды является проблемой в топливных баках, так как она отделяется от бензина и может замерзнуть в линиях питания при низких температурах. Алкоголь не удаляет воду из бензина, но Спирт , растворяет воду в бензине. После того, как растворимая , вода не создает такой же риск , как нерастворимую воду, так как он больше не накапливается в линиях подачи и замерзает, но потребляется с самим топливом. Изопропиловый спирт часто продается в аэрозольных баллончиках в качестве ветрового стекла или дверного замок обледенения. Изопропиловый спирт также используется для удаления тормозной жидкости следы от гидравлических тормозных систем, так что тормозная жидкость (обычно DOT 3 , DOT 4 , или минеральное масло ) не загрязнять тормозные колодки и привести к ухудшению торможения.
лаборатория
В качестве биологического образца консерванта, изопропиловый спирт обеспечивает сравнительно нетоксичной альтернативу формальдегид и другие синтетические консерванты. Изопропиловый спирт растворы 70-99% используются для сохранения образцов.
Изопропиловый спирт часто используется в экстракции ДНК . Лабораторный работник добавляет его в раствор ДНК для осаждения ДНК, который затем образует осадок после центрифугирования. Это возможно потому , что ДНК является нерастворимым в изопропиловом спирте.
безопасности
Изопропиловый спирт пара является более плотной , чем воздух и воспламеняется , с диапазоном воспламеняемости от 2 до 12,7% в воздухе. Это следует держать вдали от источников тепла и открытого пламени. Перегонка изопропилового спирта в течение магния сообщалось, образуя пероксиды , которые могут взорваться от концентрации. Изопропиловый спирт является раздражителем кожи. Носить защитные перчатки рекомендуется.
токсикология
Изопропиловый спирт и его метаболита , ацетон , действуют в качестве центральной нервной системы (ЦНС) депрессантов . Отравление может произойти от приема пищи, ингаляции, или поглощения кожи. Симптомы изопропилового спирта включают отравление гиперемию , головную боль , головокружение , депрессия ЦНС , тошнота , рвота , анестезии , переохлаждение , низкое кровяное давление , шок , угнетение дыхания и кома . Передозировка может вызвать фруктовый запах на дыхании в результате его метаболизма в ацетон . Изопропиловый спирт не вызывает анион разрыв ацидоза , но он производит osmolal зазора между вычисленным и измеренным osmolalities сыворотки, как и другие спирты.
Изопропиловый спирт окисляется с образованием ацетона алкогольдегидрогеназы в печени, и имеет биологическую полураспада в организме человека от 2,5 до 8,0 часов. В отличие от метанола или этиленгликоля отравления, метаболиты изопропилового спирта являются менее токсичными, и лечение в основном поддерживает. Кроме того, нет никаких указаний на использование Fomepizole , ингибитор дегидрогеназы спирта, если совместно проглатывание смесью метанол или этиленгликоль не подозревается.
Рекомендации
внешняя ссылка
| Изопропанол | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Пропан-2-ол |
| Сокращения | Изопропанол, 2-пропанол |
| Традиционные названия | Изопропиловый спирт |
| Химическая формула | CH3CH(OH)CH3 |
| Эмпирическая формула | C3H8O |
| Физические свойства | |
| Состояние (ст. усл.) | жидкость |
| Отн. молек. масса | 60,09 а. е. м. |
| Молярная масса | 60,09 г/моль |
| Плотность | 0,7851 г/см³ |
| Динамическая вязкость (ст. усл.) | 0,00243 Па·с (при 20 °C) |
| Термические свойства | |
| Температура плавления | -89,5 °C |
| Температура кипения | 82,4 °C |
| Температура вспышки | 11,7 °C |
| Температура самовоспламенения | 400 °C |
| Молярная теплоёмкость (ст. усл.) | 155,2 Дж/(моль·К) |
| Давление пара | 4,4 кПа при 20 °C |
| Химические свойства | |
| pKa | 16,5 |
| Растворимость в бензоле | хорошо растворим |
| Растворимость в ацетоне | растворим |
| Оптические свойства | |
| Показатель преломления | 1,3776 |
| Структура | |
| Дипольный момент | 1,66 Д |
| Классификация | |
| Рег. номер CAS | 67-63-0 |
| SMILES | CC(O)C |
| Безопасность | |
| Токсичность | довольно высокая |
Изопропиловый спирт, пропанол-2 (2-пропанол), изопропанол, диметилкарбинол, ИПС — простейший вторичный одноатомный спирт алифатического ряда. Существует изомер изопропанола — 1-пропанол. Принадлежит к веществам 3-го класса опасности (умеренно опасные вещества) по степени воздействия на организм, обладает наркотическим действием. Граница ПДК для паров изопропанола в воздухе составляет 10 мг/м3. Отравление изопропиловым спиртом возникает в результате вдыхания паров, содержащих концентрацию, превышающую ПДК, кумулятивными свойствами не обладает[1]. Потребление внутрь уже в небольших дозах вызывает отравление. Широко используется как технический спирт в средствах для чистки стёкол, оргтехники и т. п. и как растворитель в промышленности (где растворители необходимы).
Свойства
Химические свойства
Химическая формула (рациональная) изопропилового спирта: CH3CH(OH)CH3.
Изопропанол обладает свойствами вторичных спиртов жирного ряда, в том числе образует простые и сложные эфиры. Гидроксильная группа может быть вытеснена представителями ряда галогенов. С ароматическими соединениями изопропиловый спирт конденсируется с образованием производных, таких как изопропилбензол и изопропилтолуол. В изопропаноле хорошо растворяются многие эфирные масла, алкалоиды, некоторые синтетические смолы и другие химические соединения. При дегидрировании превращается в ацетон.[2]
Реагирует с сильными окислителями. Агрессивен в отношении некоторых видов пластика и резины.
Физические свойства
Бесцветная жидкость с характерным спиртовым запахом, более резковатым по сравнению с этанолом (по чему их можно в некоторых случаях отличить), tплавления −89,5 °C, tкипения 82,4 °C, плотность 0,7851 г/см³ (при 20 °C), tвспышки 11,7 °C. Нижний предел взрываемости в воздухе 2,5 % по объёму (при 25 °C). Температура самовоспламенения 456 °C. Коэффициент преломления 1,3776 (в жидком состоянии, при 20 °C). Динамическая вязкость при стандартных условиях 2,43 мПа·с. Молярная теплоёмкость (ст. усл.) — 155,2 Дж/(моль·К).
Пар хорошо смешивается с воздухом, легко образует взрывчатые смеси. Давление паров — 4,4 кПа (при 20 °C). Относительная плотность пара — 2,1, относительная плотность смеси пар/воздух — 1,05 (при 20 °C).
Растворим в ацетоне, хорошо растворим в бензоле, с остальными растворителями (вода, органические) смешивается в любых соотношениях. С водой образует азеотропную смесь (87,9 % изопропилового спирта, tкипения 83,38 °C).
Зависимость температуры замерзания смеси изопропилового спирта с водой от концентрации изопропилового спирта в смеси представлена в таблице[3]:
| Концентрация спирта об % | Концентрация спирта вес % | Температура замерзания °C |
| 0 | 0 | 0 |
| 10 | 8 | −4 |
| 20 | 17 | −7 |
| 30 | 26 | −15 |
| 40 | 34 | −18 |
| 50 | 44 | −21 |
| 60 | 54 | −23 |
| 70 | 65 | −29 |
| 80 | 76 | −37* |
| 90 | 88 | −57* |
| 100 | 100 | −90* |
(*Наблюдается переохлаждение)
Получение
Существует два метода промышленного производства изопропанола — гидрирование ацетона и гидратация пропилена.[4][5]
Основным способом получения изопропанола в Российской промышленности является сернокислотная гидратация пропилена
- CH3CH=CH2 + H2SO4 → (CH3)2CHOSO3H + H2O → (CH3)2CHOH.
Сырьем может служить пропан-пропиленовая фракция с содержанием пропилена 30-90 % (фракция пиролиза и крекинга нефти). Однако наблюдается тенденция к использованию чистого пропилена, так как в этом случае процесс можно вести при невысоких давлениях, резко снижается образование побочных продуктов реакции — полимеров и ацетона. На первой стадии процесса образуется сернокислотный экстракт, содержащий равновесную смесь изопропилового спирта, изопропилсульфата (Ch4)2CHOSO2OH, H2SO4 и Н2О, на второй — сернокислотный экстракт нагревается с водой и удаляется образующийся изопропиловый спирт. Прямую гидратацию пропилена осуществляют в основном в присутствии твердого катализатора (в скобках указаны условия процессов): Н3РО4 на носителе (240—260°С; 2,5-6,5 МПа) или катионообменной смолы (130—160°С; 8,0-10,0 МПа). Изопропиловый спирт получают также окислением парафинов воздухом и другими способами.[2]
Современный способ:
Гидрирование ацетона водородом (в фазе пара) в присутствии стационарного медно-никельхромитного катализатора.[6][7]
В России изопропанол производят из пропилена на ЗАО «Завод синтетического спирта» (г. Орск)[8] и методом гидрирования ацетона водородом — ООО «Синтез Ацетон», (г. Дзержинск)[9][7]
Применение
Изопропиловый спирт используют для получения:
По причине особого государственного регулирования этанола, изопропиловый спирт часто является его заменителем во многих областях его применения. Так, изопропанол входит в состав:
Изопропиловый спирт применяется в промышленности, при резании алюминия, токарных, фрезерных и прочих работах. В смеси с маслом позволяет значительно повысить производительность работы. Изопропиловый спирт применяется как референс-стандарт в газовой хроматографии (например, при испытании лекарственных средств на остаточные органические растворители).
Медицина
70 % изопропиловый спирт применяется вместо этилового спирта как антисептик для пропитки медицинских салфеток.
Влияние на человека
Оказывает раздражающее воздействие на глаза и дыхательные пути, при кратком воздействии больших концентраций паров вызывает головную боль. Может оказывать угнетающее действие на центральную нервную систему. Воздействие на уровне, значительно превышающем ПДК, может вызвать потерю сознания. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обуславливает его токсическое действие. Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто уже при дозах порядка 50 мл и более.
Предельно допустимая концентрация изопропанола в воздухе равна 10 миллиграммов на кубический метр.
Изопропанол органолептически заметно отличается от этанола и не может быть ошибочно принят за этанол. Имеет отличный от этанола запах, более «грубый». При приеме внутрь вызывает опьянение, сходное с алкогольным. Изопропанол окисляется в организме при участии альдегиддегидрогеназы до ацетона. Скорость окисления в среднем в 2 — 2,5 раза ниже, чем у этанола, поэтому опьянение изопропанолом очень стойкое. При частом употреблении к изопропанолу быстро развивается непереносимость, а в отдельных случаях — гиперчувствительность и аллергия. Хотя токсичность изопропанола примерно в 3,5 раза больше, чем у этанола, но при этом опьяняющее действие его также выше в 10 раз[источник не указан 546 дней]. По этой причине смертельных отравлений изопропанолом не зафиксировано, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола.
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием.[1] Наркотический эффект изопропанола почти в 2 раза превышает аналогичный эффект этанола.[10] Концентрация 1,2 %, воздействующая в течение 4 часов оказывает наркотический эффект. При аналогичном воздействии в течение 8 часов — в половине случаев наблюдается смертельный исход.[11]
Примечания
- ↑ 1 2 ГОСТ 9805-84. Спирт изопропиловый. Технические условия[1]
- ↑ 1 2 ХиМиК.Ру — Изопропиловый спирт
- ↑ Ссылка один (англ.),Ссылка два
- ↑ «Isopropyl Alcohol, by John E. Logsdon and Richard A. Loke», Kirk‑Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc, Article Online Posting Date: December 4, 2000
- ↑ A. J. Papa (2005), «Propanols», Ullmann’s Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_173
- ↑ СПОСОБ ПОЛУЧЕНИЯ ПРОПАНОЛА-2 — Патент РФ 2047590
- ↑ 1 2 ООО Синтез Ацетон
- ↑ О заводе | Завод синтетического спирта
- ↑ ПРОИЗВОДСТВО ИЗОПРОПИЛОВОГО СПИРТА В РОССИИ
- ↑ «Достоинства и недостатки современных кожных антисептиков» С. В. Волкова, Е. В. Клементенок
- ↑ Review of Inhalants: Euphoria to Dysfunction Charles Wm. Sharp, Ph.D., Mary Lee Brehm, Ph.D.,National Institute on Drug Abuse
Изопропиловый спирт
Изопропиловый спирт
Рейтинг: / 7- Подробности
- Просмотров: 11883
Изопропиловый спирт.
Химическая формула продукта: C3H8O
Торговые обозначения:
• Isopropyl Alcohol
• Dimethylcarbinol;
• sec-Propyl alcohol
• Rubbing alcohol
• Petrohol
• 1-Methylethanol
• 1-Methylethyl alcohol
• 2-Hydroxypropane
• 2-Propyl alcohol
• Изопропанол
• Изопропиловый спирт
Описание продукта:
Изопропиловый спирт является прозрачной и легковоспламеняющейся жидкостью при комнатной температуре с запахом, напоминающим смесь этанола и ацетона; Полностью смешивается с водой, этанолом, ацетоном, хлороформом и бензолом; Плавящегося при -89 °C и кипящего при 82 °C. Изопропанол подвергается всем химическим реакциям, типичным для вторичных спиртов. Изопропанол бурно реагирует с сильными окислителями. При пожаре он может разлагаться с образованием токсичных газов, таких как окись углерода. Производится из пропена путем косвенной гидратации (сильнокислотный процесс) или прямого каталитического восстановления ацетона. Это недорогой растворитель во многих областях применения. Изопропиловый спирт аналогичен этиловому спирту в свойствах растворителя и скорости испарения. Его высокая скрытая растворительная способность для нитрата целлюлозы, ацетата бутирата целлюлозы и ацетата пропионата целлюлозы, а также его умеренная скорость испарения и полная смешиваемость с большинством растворителей делают ее полезной для лаков, чернил и разбавителей. Изопропанол — это зрелый товар, который, согласно прогнозам, будет расти в среднем на 1-3 процента в год. Ожидается, что потребление Изопропанол для производства моноизопропиламина для гербицидов (главным образом глифосата) будет самым быстрорастущим сегментом, в то время как производные кетона, используемые в качестве растворителей в покрытиях и чернилах, останутся плоскими или незначительно увеличатся. Правительственные постановления, касающиеся летучих органических соединений, были и будут и впредь являться одним из основных соображений в будущем планировании производителей ПНД. Изопропанол используется также для производства ацетона (окисление изопропанола является в настоящее время основным источником ацетона) и его производных и других химических веществ (таких как изопропилацетат, изопропиламин, диизопропиловый эфир, изопропил ксантогенат, сложные эфиры жирных кислот, гербицидные эфиры и алюминий Изопропоксид). Другие применения включают применение в качестве хладагента в производстве пива, связующий агент, дегидратирующий агент, модификатор полимеризации при производстве поливинилфторида, ингибитор пенообразования, антиобледенитель, консервант, теплообменную среду и В стеклоочистителях. Он также используется в качестве ароматизатора, а также в продуктах домашнего и личного ухода, фармацевтических препаратах.
Растворитель — это вещество, обычно жидкое, которое действует как растворитель или способно растворять другое вещество. В растворах твердых веществ или газов в жидкости жидкость является растворителем. Во всех других гомогенных смесях (то есть жидкостях, твердых веществах или газах, растворенных в жидкостях, твердых веществах в твердых веществах и газах в газах) растворитель является компонентом наибольшего количества. Вещества меньшей доли называются растворенными веществами. Растворитель предлагает несколько функций во время химической реакции. Он решает вещество, которое реагирует с другим, для получения нового набора веществ (реагента) и соединения, которое поставляет молекулу, ион или свободный радикал, который рассматривается как атакующий вид в химической реакции (реагент). Растворитель является проводящим к столкновениям между реагентами и реагентами для превращения реагентов в новые продукты. Растворитель также принимает рулон регулирования температуры, либо для обеспечения энергии сталкивающихся частиц для быстрой реакции, и для поглощения тепла в экзотермической реакции. Соответствующий растворитель следует выбирать на основании неактивности в реакционных условиях, растворения реагентов, а также реагентов, соответствующей температуры кипения и легкого удаления в конце реакции. Наиболее распространенным растворителем является вода. Другими распространенными растворителями, которые растворяют в воде нерастворимые (или почти нерастворимые) вещества, являются ацетон, спирт, муравьиная кислота, уксусная кислота, формамид. BTX, дисульфид углерода, диметилсульфоксид, четыреххлористый углерод, хлороформ, простой эфир, тетрагидрофуран, фурфурол, гексан и скипидар. Они могут быть классифицированы как полярные и неполярные типы. Они могут быть классифицированы как полярные и неполярные типы. Полярные растворители, подобно воде, имеют молекулы, электрические заряды которых неравномерно распределены, оставляя один конец каждой молекулы более положительным, чем другой. Обычно полярный растворитель имеет связь O-H, примерами которой являются вода (HOH), метанол (CH3OH) и уксусная кислота (CH3COOH). Пропанол, бутанол, муравьиная кислота, формамид являются полярными растворителями. Диполярные растворители, содержащие твердую связь C-O без связи O-H, представляют собой ацетон [(CH3) 2C = O], этилацетат (CH3COOCH2CH3), метилэтилкетон, ацетонитрил, N, N-диметилформамид и диметилсульфоксид. Неполярные растворители, такие как четыреххлористый углерод (CCl4), бензол (C6H6) и диэтиловый эфир (CH3CH2OCH2CH3), имеют молекулы, электрические заряды которых равномерно распределены и не смешиваются с водой. Гексан, тетрагидрофуран и метиленхлорид являются неполярными растворителями.
Одним из распространенных видов домашнего использования спиртов является чистящее средство. Многие унитазы и очистители окон, например, содержат изопропиловый спирт. В отличие от воды, спиртовой раствор может растворять липкие, смолистые остатки, что делает его идеальным для удаления сока или жевательной резинки с рук и поверхностей. Говорят, что изопропиловый спирт удаляет остатки лака для волос из зеркал и окон. DVD-диски и компакт-диски, которые приобрели отпечатки пальцев, выигрывают от того, что на мягкую ткань натирают их изопропиловым спиртом — спирт удаляет отпечатки пальцев, не повреждая деликатный пластик диска. Привычные пловцы знают, что одним из наиболее раздражающих и потенциально болезненных побочных эффектов любви к воде является ее тенденция застревать глубоко в ушном канале. В лучшем случае это приводит к раздражающим нескольким часам попытки удалить остаточную воду, в течение которой это может быть трудно услышать. В худшем случае, влажность глубоко в ухе создает идеальную среду для инфекционных патогенов, что приводит к уху пловцов, что может быть довольно болезненным. Растительный спирт может фактически помочь пловцам предотвратить инфекцию. Согласно паспортам безопасности материалов для изопропилового спирта, химическое вещество имеет давление пара 44 мм рт.ст. при комнатной температуре по сравнению с давлением паров воды 23,8 мм рт.ст. Это означает, что испариться изопропиловому спирту гораздо легче, чем воде. В результате, в то время как лужа воды — будь то на прилавке или в ухе — прилипает на какое-то время, лужа растирающего спирта быстро испаряется. Когда спиртовая смесь смешивается с водой, полученная смесь имеет давление пара между таковыми исходных соединений. Это означает, что наливание немного растирающего спирта в ухо, чтобы смешать с водой, оставленной после купания, дает смесь, которая испаряется намного быстрее, чем сама вода, высушивая ухо и предотвращая инфекцию. Изопропиловый спирт является очень часто используемым веществом — мы используем его чаще, чем мы знаем каждый день. Изопропиловый спирт используется для различных целей в домашних условиях, а также для различных промышленных процессов и фармацевтических применений. Микробы и вредные бактерии, которые могут привести к болезни и инфекции, определенно являются проблемой. Хорошо, что изопропиловый спирт является дезинфицирующим средством, поэтому он убивает эти надоедливые микробы и вредные бактерии. В больницах и в наших домах используются различные продукты, которые используют изопропиловый спирт. Кроме того, при спиртовом спирте изопропиловый спирт присутствует в спиртовых тампонах, спиртовых тампонах и дезинфицирующем средстве для рук, которое может дезинфицировать мелкие порезы и раны, чтобы мы могли избежать заражения. Иногда вода просто не делает этого. Хотя вода является универсальным растворителем, есть некоторые вещи, которые вода просто не может растворить. Изопропиловый спирт, в отличие от воды, может растворять многие неполярные соединения, такие как хлороформ и некоторые масла. Вот пример того, когда изопропиловый спирт является лучшим растворителем, чем вода: Вам приходилось чистить сухую доску для стирания? Вы сделали ошибку, используя воду? Если у вас есть, вы, возможно, заметили, что использование воды обычно оставляет полосы. Как насчет очистки экрана компьютера только водой? Вода не настолько эффективна, чтобы убрать накопленную грязь с экрана. Изопропиловый спирт действует как шарм как для сухих досок для стирания, так и для компьютерных экранов. На самом деле существует альтернатива использованию формальдегида, и это изопропиловый спирт, который иногда используется, потому что он не токсичен, как формальдегид. Другое использование изопропилового спирта в лаборатории — это извлечение ДНК: изопропиловый спирт не может растворить ДНК, поэтому его можно использовать для его экстракции. Здесь к раствору ДНК добавляют изопропиловый спирт для выделения или отделения ДНК от остальной части раствора. Кроме того, в лабораториях биологии изопропиловый спирт широко используется в химических лабораториях. Изопропиловый спирт используется для взаимодействия с различными веществами, для образования различных химических продуктов.
Физико-химические свойства.
|
№ |
Показатель |
Значение |
|
1 |
Физическое состояние и внешний вид изопропиловый спирт |
Жидкость |
|
2 |
Запах изопропиловый спирт |
напоминает смесь этанола и ацетона. |
|
3 |
Вкус изопропиловый спирт |
Горький. (Немного). |
|
4 |
Молекулярный вес изопропиловый спирт |
60,1 г / моль |
|
5 |
Цвет изопропиловый спирт |
Бесцветный. |
|
6 |
Точка кипения изопропиловый спирт |
82,5 ° C (180,5 ° F) |
|
7 |
Температура плавления изопропиловый спирт |
-88,5 ° C (-127,3 ° F) |
|
8 |
Критическая температура изопропиловый спирт |
235 ° C (455 ° F) |
|
9 |
Удельный вес изопропиловый спирт |
0,78505 (вода = 1) |
|
10 |
Давление пара изопропиловый спирт |
4,4 кПа (при 20 ° C) |
|
11 |
Плотность паров изопропиловый спирт |
2,07 (Воздух = 1) |
|
12 |
Порог восприятия запаха изопропиловый спирт |
22 ppm |
|
13 |
Растворимость изопропиловый спирт |
Легко растворим в холодной воде, горячей воде, метаноле, диэтиловом эфире, н-октаноле, ацетоне. Нерастворим в солевом растворе. Растворим в бензоле. Смешивается с большинством органических растворителей, включая спирт, этиловый спирт, хлороформ. |
Транспортировка и хранение изопропиловый спирт.
Меры предосторожности: Беречь от тепла. Хранить вдали от источников возгорания. Заземлите все оборудование, содержащее материал. Не глотать. Не вдыхать газы / пары / пары / аэрозоль. Избегать попадания в глаза. Носить соответствующую защитную одежду. В случае недостаточной вентиляции, наденьте подходящее респираторное оборудование. При проглатывании немедленно обратитесь к врачу и покажите контейнер или этикетку. Беречь от несовместимых веществ, таких как окисляющие вещества, кислоты.
Хранение: Изопропиловый спирт купить и хранить в отдельной и утвержденной зоне. Хранить контейнер в прохладном, хорошо проветриваемом помещении. Держите контейнер плотно закрытым и запечатанным до готовности. Избегайте всех возможных источников воспламенения (искры или пламя).
Перед началом работы с изопропиловым спиртом необходимо обучить людей правильному обращению с ними и их хранению, а также знать, как использовать надлежащие средства индивидуальной защиты. Хранить состав в плотно закрытом контейнере в прохладном, сухом, хорошо проветриваемом месте вдали от несовместимых веществ. Хранить вдали от источников тепла, искр, пламени и других источников воспламенения, а также сильных окислителей, ацетальдегида, хлора, окиси этилена, кислот и изоцианатов. Огнеопасный шкаф безопасности — лучший вариант хранения. Изопропиловый спирт легко воспламеняется и легко воспламеняется. Пары могут образовывать взрывоопасные смеси с воздухом, двигаясь к источнику воспламенения и обратно. Использование водяного аэрозоля для тушения пожаров может быть неэффективным.
Области применения.
• Изопропиловый спирт купить и применить в качестве технологического растворителя. Экстракция и очистка натуральных продуктов, таких как растительные и животные масла и жиры, смолы смолы, воски, красители, ароматизаторы, алкалоиды, витамины, ламинария и альгинаты. Перевозчик в производстве пищевых продуктов. Очистка, кристаллизация и осаждение органических химических веществ.
• Изопропиловый спирт купить в качестве агента покрытия и растворителя красителей. Синтетические полимеры, такие как фенольные лаки и нитроцеллюлозные лаки. Цементы, грунтовки, краски и чернила.
• Изопропиловый спирт выступает в качестве средства для чистки и сушки. Производство электронных деталей для металлов и фотопленок и бумаги, в чистящих средствах для стекла, жидких мылах и моющих средствах, а также в аэрозолях.
• Изопропиловый спирт является растворителем в препаратах местного применения. Фармацевтическая продукция: втирания, массажные растворы, такие актуальные как спирт для растирания (70% 2-пропанольные аэрозоли. Косметика: тоники для волос, парфюмерия, лосьоны для кожи, ополаскиватели для волос и лосьоны с постоянной волной, очистители кожи и дезодоранты, лаки для ногтей, шампуни.
• Изопропиловый спирт является аэрозольным растворителем. Изопропиловый спирт купить и применить в чистящих средствах, воски, полироли, краски, антиобледенители, спреи для обуви и носков, репелленты для насекомых, спреи для волос, дезодоранты, освежители воздуха. Медицинские и ветеринарные продукты: антисептики, фунгициды для ног, первая помощь и медицинские спреи для пара, соски для кожи, ветеринарные розовые глаза, раны и отбеливающие спреи, инсектициды для дома и сада.
• Изопропиловый спирт купить и использовать в качестве дезинфицирующего средства для успокоения кожи и очистки бактерий и других загрязняющих веществ. Изопропиловый спирт также считается полезным при лечении акне в силу его очищающих свойств, хотя это не было доказано ни в каких медицинских исследованиях. Большинство людей используют Изопропиловый спирт для втирания как альтернативу дорогостоящим вяжущим средствам или тонизирующим средствам против угрей, где спиртовое растирание является основным средством в сочетании с другими целебными ингредиентами для лечения акне, такими как гвоздика или масло чайного дерева.
• Изопропиловый спирт является агентом для создания линиментных жидкостей. Линимент — это жидкость, которую можно протирать по поверхности болей в мышцах или болезненных суставах, чтобы уменьшить боль и припухлость. Согласно ученым, алкоголь является эффективным линиментом, потому что он действует как незначительный раздражитель для кожи, увеличивая кровообращение и кровоток в область. Это увеличение кровообращения помогает облегчить боль и воспаление.
• Изопропиловый спирт цена не дорогая для использования при производстве вяжущих жидкостей. Вяжущие вещества — это вещества, которые могут сжимать или затягивать ткани вашего тела, например, поры в коже, когда они применяются местно. Изопропиловый спирт действует как вяжущее вещество и часто используется в тонизирующих средствах для кожи и сжимая формулы наряду с другими вяжущими средствами, такими как гамамелис. Это помогает придать вашей коже более гладкий вид и сделать поры менее заметными. Вяжущие средства также помогают остановить кровотечение при незначительных порезах и царапаниях, затягивая капилляры, которые теряют кровь
Изопропиловый спирт цена одна из самых низких на рынке
Изопропиловый спирт купить вы сможете, позвонив 8 (495) 518-517-6 или написав нашим менеджерам на общую почту Этот адрес электронной почты защищен от спам-ботов. У вас должен быть включен JavaScript для просмотра.
Изопропиловый спирт купить по низким оптовым ценам
Изопропиловый спирт купить со склада в Москве
Изопропиловый спирт купить со склада в Нижнем Новгороде
Изопропиловый спирт купить со склада в Санкт Петербурге
Изопропиловый спирт купить со склада в Казани
- < Назад
- Вперёд >
 |
 |
Алф. указатель: 1-9 A-Z А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Щ Э Я
Синонимы:
2-пропанол |

|