Гипохлорит кальция / общая информация
Гипохлорит кальция / общая информация
Соль кальция и хлорноватистой кислоты с формулой Сa(ClO)2, образует кристаллогидраты. Устойчив в сухой атмосфере без CO2.
Формула: Ca(ClO)2
Название ИЮПАК: Calcium hypochlorite
Молярная масса: 142,98 г/моль
Насыпная плотность: 0,9 г/см3
Температура плавления: 100°C
Растворимость: Вода
ТУ Гипохлорит кальция в каталоге продукции
Область применения
Гипохлорит кальция — широко распространенный реагент для нейтрализации стоков золотодобычи, обеззараживания и очистки воды и водопроводных сооружений, дезинфекции различных поверхностей, содержащий 65-70% активного хлора.
Нейтрализация цианидов в золотодобыче
Эффективное обеззараживание воды
Дезинфекция общественных зон
Отбеливание ткани и бумаги
Приоритеты
Проект соответствует приоритетам, обозначенным в ежегодном Послании Президента РФ Федеральному собранию от 4 декабря 2014 года.
- Улучшение инвестиционного климата;
- Поддержка высокотехнологичных секторов экономики;
- Сбалансированное региональное развитие.
Проект отвечает основным приоритетам, отраженным в Стратегии социально-экономического развития Чувашской Республики до 2020 года.
Импортозамещение
Проект включен в отраслевой план мероприятий по импортозамещению в отрасли химической промышленности Российской Федерации, утвержденный приказом № 646 Минпромторга России от 31 марта 2015 года.
Инвестиции
Проект включен в Перечень комплексных инвестиционных проектов по приоритетным направлениям гражданской промышленности в соответствии с постановлением Правительства РФ.
Экология
Цех по производству гранулированного гипохлорита кальция спроектирован как современное высокотехнологичное предприятие. В проекте заложен ряд технологических и технических решений, способствующих минимизации негативного воздействия на окружающую среду в рамках требований Российского экологического законодательства и международных стандартов.
При производстве гипохлорита кальция выбросы в атмосферу будут практически исключены за счет использования систем улавливания промышленных выбросов со всех технологических схем производства. Все побочные продукты предполагается перерабатывать для дальнейшего использования в производственном цикле цехов ПАО «Химпром» или для получения других товарных продуктов.
Производственный цикл
В производстве гипохлорита кальция используются не только основные сырьевые ресурсы, но и попутно получаемые полупродукты, которые снижают расход сырья и сводят к минимуму загрязнение окружающей среды.
Контакты управления реализации
Для получения дополнительной информации, а так же по вопросам приобретения и поставки
Единый номер: +7(8352)73-55-55
Телефон бюро сбыта: (8352)73-52-86
Электронная почта: [email protected]
Сделать запрос
- Общая информация
- Область применения
- Приоритеты
- Импортозамещение
- Инвестиции
- Экология
- Производственный цикл
Кальция гипохлорит технический– поставщик хлорноватистокислого кальция «ХИМПЭК»
Дезинфицирующие средства
Гипохлорит кальция – соль кальция и хлорноватистой кислоты. Гипохлорит кальция – дезинфицирующее средство для промышленного применения. Свидетельство о регистрации RU.77.99.23.002.E.015572.11.12. от 06.11.12 Цена: уточняйте у менеджера Узнать цену |
Физико-химические показатели
Общее описание
Внешний вид
Условия транспортировки и хранения
Области применения
| Наименование показателя | Спецификация импортного продукта |
| Внешний вид | Порошкообразный продукт белого или светло-серого цвета |
| Массовая доля активного хлора (Cl+1), %, | не менее 45,0 |
| Уменьшение м.д.активного хлора после года хранения, % | 7,7 |
| Коэффициент термостабильности, %, | не менее 0,8 |
| Массовая доля хлорида кальция, (CaCl2), %, не более | 10,0 |
| Массовая доля воды (H 2O), %, не более | 4,0 |
| Массовая доля нерастворимого остатка, %, не более | 15,0 |
Примечание: допускается снижение массовой доли активного хлора в пределах гарантийного срока хранения до 35%.
| Класс опасности по степени воздействия на организм человека | 3 |
| Виды опасности | |
| Взрыво- и пожароопасность | Не горюч, взрывобезопасен. Однако при контакте с жидкими маслообразными органическими веществами и пылевидными органическими продуктами может вызвать их загорание. Емкости могут взрываться при нагревании. |
| Опасность для человека | Обладает местно-раздражающим действием на кожу и выраженным на слизистые оболочки глаз, не оказывает сенсибилизирующего действия. В тяжелых случаях наблюдается одышка, кашель, учащение пульса, тошнота. В тяжелых случаях наблюдается одышка, кашель, учащение пульса, тошнота. |
| Средства индивидуальной защиты | Все работающие с ГК должны быть обеспечены специальной одеждой по отраслевым нормам и иметь средства защиты: фильтрующий противогаз марки ФГ-13-В или универсальные респираторы «РУ-60М», «РПГ-67» с патроном марки «В», резиновые сапоги, резиновые перчатки, фартук из прорезиненной ткани и защитные очки «ОП-2», «ОП-3» или моноблок. Во всех случаях газовыделений работу следует вести в противогазе. Следует избегать попадания средства в глаза и на кожу. |
Гарантийный срок хранения продукта — 2 года со дня изготовления. Срок годности 3 года.
Вещество обладает сильными окислительными свойствами, смешивается с водой, при выделении из растворов образует кристаллогидраты. При контакте с воздухом медленно разлагается, что провоцирует снижение активного хлора в составе. Более устойчиво в сухой среде без углекислого газа.
Хлорноватистокислый натрий реагирует с соляной кислотой, выделяя хлор, а также разлагается при нагревании. В щелочных средах в присутствии катализатора способен выделять кислород. Активен в отношении многих других веществ.
Сырье является умеренно токсичным. Опасно при вдыхании в виде концентрированного пара, а также при попадании в организм в виде порошка.
Технический гипохлорит натрия поставляется в виде мелкого порошка белого цвета с характерным хлорным запахом.
Технический гипохлорит кальция упаковывают в бочки с герметичными полимерными вкладышами во избежание разрушения металла. Тару транспортируют железнодорожными вагонами и автомобильными фургонами. Хранят хлорноватистокислый кальций в закрытых складах, избегая разгерметизации заводской упаковки и контакта с воздухом или водой.
Технический гипохлорит кальция широко используется в качестве дезинфектанта за счет невысокой цены, относительной безопасности для человека и окружающей среды. Его применяют для обработки сточных и питьевых вод, физических отходов, оборудования, а также в других сферах:
- в качестве отбеливателя для различных видов сырья;
- для дегазации;
- в качестве окислителя, коррозионно-активного компонента в различных отраслях промышленности.

Склад
В Московской области
Адрес: Истринский район, сельское поселение Ивановское, поселок станция Манихино, 50 км
Посмотреть на карте
Скачать схему проезда
Здесь возможно:
оплатить наличными;
купить от 1 мешка (канистры/мкр/куба/барабана) продукции.
С этим продуктом часто покупают:
| Продукция | Синонимы | CAS № | ГОСТ | Марка/сорт | Упаковка/вес |
| Айсмелт mix (ICEMELT mix), эффективен до -20° Противогололедный реагент | кальция хлорид, натрий хлористый модифицированный, ХКНМ | натрий хлорид 7647-14-5, кальций хлорид 10043-52-4 | 39297743-01-2008 | Мешок 25 кг | |
| Айсмелт power (ICEMELT power), эффективен до -31° Противогололедный реагент | кальция хлорид, натрий хлористый модифицированный, ХКНМ | 10043-52-4 | 39297743-02-2007 | Мешок 25 кг | |
| Кальция карбид | углеродистый кальций, ацетиленид кальция | 75-20-7 | 1460-81 | второй | Металлический барабан 120 кг |
| Кальция формиат технический | муравьинокислый кальций, кальциевая соль муравьиной кислоты | 544-17-2 | импорт | Мешок 25 кг | |
| Натрия гидросульфид | сульфогидрат натрия, натрий сернистый кислый, натрия бисульфид | 16721-80-5 | импорт | Мешок 25 кг | |
| Натрия сульфид | натрий сернистый | 1313-82-2 | импорт | Мешок 25 кг, 40 кг | |
| Калий хлористый | хлорид калия, калийная соль, калий хлорид | 7778-54-3 | 4568-95, РБ 600122610.  010-2002 010-2002 | первый | МКР 850 кг, Мешок 50 кг |
| Аммония хлорид технический (аммоний хлористый) | хлорид аммония, нашатырь | 12125-02-9 | 2210-73, импорт | Мешок 25 кг, 35 кг | |
| Барий хлористый технический (хлорид бария) | хлорид бария, барий хлористый 2-водный, барий хлористый дигидрат | 10326-27-9 | импорт | Мешок 25 кг | |
| Галит (соль техническая) | соль техническая, натрий хлористый, хлорид натрия, соль каменная, концентрат минеральный «Галит» | 7647-14-5 | 2111-006-00352816-08 | первый, второй | МКР 1000 кг, Мешок 50 кг |
| Известь хлорная | кальция гипохлорита смесь сухая, хлорная известь, хлорка, известь белильная | 22464-76-2 | 1692-85 | марка А, 3 сорт | Мешок 19-23 кг |
| Кальций хлористый 2-водный (E509) | хлорид кальция | 10043-52-4 | 9199-087-00206457-2010 | Мешок 30 кг | |
| Кальций хлористый пищевой «Fudix» (E509) | регулятор кислотности Е-509, хлорид кальция | 10043-52-4 | 39297743-05-2009 | Мешок 25 кг | |
| Хлорамин Б | монохлорамин б | 127-52-6 | импорт | Мешок 15 кг, Барабан 15 кг, п/э пакет 300 г. 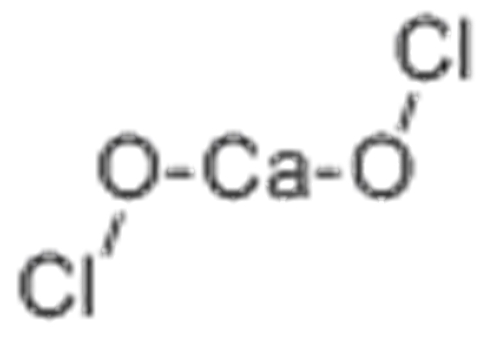 , уложенные в мешок или барабан , уложенные в мешок или барабан |
Гипохлорит кальция: структура, свойства и применение
Вы должны знать химический «хлорный порошок» и его основные области применения. Отбеливающий порошок — это общее название, и точное содержание любого отбеливающего порошка зависит от промышленных процессов, используемых для его производства.
Но знаете ли вы, из каких химических компонентов состоит хлорная известь? Что такое гипохлорит кальция? Какова структура гипохлорита кальция? Каковы его плюсы и минусы?
Чтобы получить ответ на все эти вопросы, следуйте этой статье.
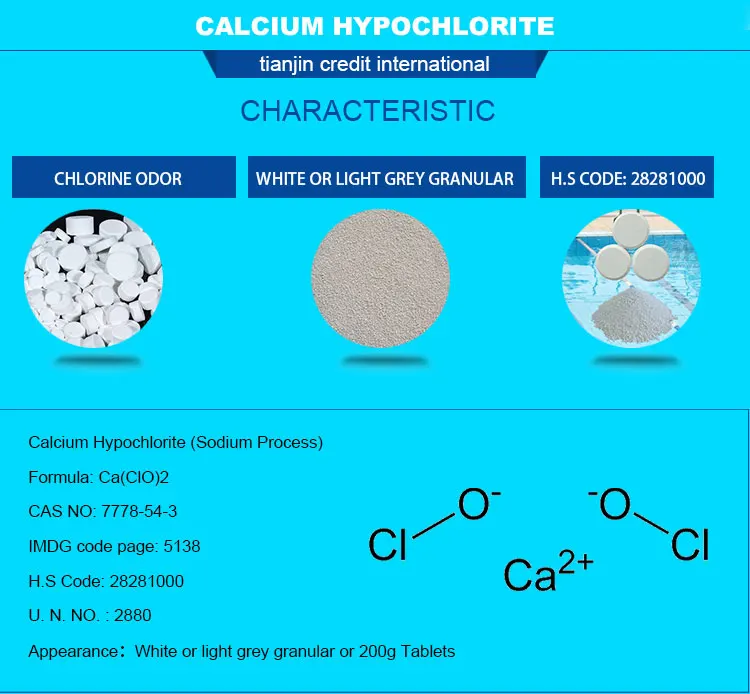
Что такое гипохлорит кальция?Химическое соединение, гипохлорит кальция, имеет химическую формулу Ca(ClO)₂. Он широко известен как отбеливающий порошок, кальциевая соль хлорноватистой кислоты, хлорид извести и хлорированная известь. Это электростатическое или ионное соединение, содержащее Ca²⁺ (ион кальция) и два ClO⁻ (ион гипохлорита).
Ответить, что такое гипохлорит кальция? Это белое концентрированное химическое вещество, доступное на рынке в виде порошка, кристаллов или таблеток. Основным применением гипохлорита кальция является дезинфекция и санитарная обработка воды в плавательных бассейнах и питьевой воды. По сравнению с другими источниками хлора для очистки воды он проще и безопаснее в использовании.
Основным применением гипохлорита кальция является дезинфекция и санитарная обработка воды в плавательных бассейнах и питьевой воды. По сравнению с другими источниками хлора для очистки воды он проще и безопаснее в использовании.
Хотя он стабилен при комнатной температуре, он медленно разлагается во влажных условиях, придавая ему характерный запах хлора. Он является активным ингредиентом отбеливающих порошков, хлорированной извести и т. д.
История гипохлорита кальцияВ конце 18 века Чарльз Теннант и Чарльз Макинтош разработали промышленный процесс производства хлорида извести, т. е. гипохлорита кальция. В 1799 году он был запатентован. Во время Первой мировой войны врачи активно использовали его для дезинфекции ран и окопов.
Структура гипохлорита кальцияЭто неорганический комплекс, имеющий химическую формулу Ca(ClO)₂. Это белое малорастворимое твердое вещество. Это одно из основных соединений гипохлоритов.
Структура гипохлорита кальция состоит из аниона гипохлорита и катиона кальция. Катион кальция (Ca²⁺) координируется с шестью атомами O в искаженной октаэдрической геометрии. Анион гипохлорита (ClO⁻) имеет прямую или линейную структуру и связан с катионом кальция через атомы кислорода.
Катион кальция (Ca²⁺) координируется с шестью атомами O в искаженной октаэдрической геометрии. Анион гипохлорита (ClO⁻) имеет прямую или линейную структуру и связан с катионом кальция через атомы кислорода.
Структура гипохлорита кальция представлена ниже:
Получение гипохлорита кальцияСуществует два способа получения гипохлорита кальция. Это
1. Процесс с кальцием:В промышленности гипохлорит кальция получают путем обработки известковой воды газообразным хлором. Поскольку известковая вода содержит кальций, этот процесс обычно называют кальциевым. Химическая реакция протекает следующим образом
2Ca(OH)₂ + 2Cl₂ → Ca(OCl)₂ + CaCl₂ + 2H₂O
Реакцию проводят поэтапно, чтобы получить различные составы, каждый из которых содержит различные концентрации хлорида кальция, гипохлорита и непрореагировавшей извести.
2. Натриевый процесс: В этом процессе гашеную известь обрабатывают газообразным хлором и гидроксидом натрия с получением смеси гипохлорита кальция Ca(ClO)₂, хлорида кальция CaCl₂, воды и хлорида натрия NaCl. Реакция протекает следующим образом
Реакция протекает следующим образом
2Ca(OH)₂ + 3Cl₂ + 2NaOH → Ca(OCl)₂ + CaCl₂ + 2H₂O + 2NaCl
Свойства гипохлорита кальцияСвойства гипохлорита кальция подразделяются на два класса. Они приведены ниже:
1. Физические свойства:Среди свойств гипохлорита кальция физические свойства определяют его внешний вид, химическую формулу, природу, массу и другие характеристики. Некоторые из них приведены ниже:
- Молекулярная формула гипохлорита кальция Ca(OCl)₂.
- Существует в виде бело-серых гранул.
- Молекулярная масса гипохлорита кальция составляет 142,98 г/моль.
- При 20°C его плотность составляет 2,35 г/см³.
- Температура плавления гипохлорита кальция 100°С, температура кипения 175°С.
- Хорошо растворяется в спирте.
- При комнатной температуре растворимость гипохлорита кальция в воде составляет 21 г/100 мл.

- Это негорючее вещество, но оно ускоряет горение горючих материалов.
- Имеет запах хлора.
- Гипохлорит кальция обычно доступен в виде гранул, белого порошка или плоских пластин.
- Удельный вес гипохлорита кальция в воде составляет 1,21 г/см³.
Среди свойств гипохлорита кальция химические свойства определяют характер соединения по отношению к различным реагентам. Некоторые из них приведены ниже:
- Легко разлагается в воде.
- При нагревании гипохлорит кальция выделяет хлор и кислород.
- Гипохлорит кальция не горюч, но действует как окислитель с легковоспламеняющимся материалом.
- Может вступать во взрывоопасную реакцию с аминами, аммиаком или органическими сульфидами.
- Поскольку гипохлорит кальция легко принимает ионы H⁺, он является сильным основанием.

- При растворении гипохлорита кальция в воде он разлагается на ионы гипохлорита и ионы кальция. Кроме того, ионы гипохлорита принимают ионы H⁺ от молекул воды и высвобождают ионы OH⁻.
ClO⁻ + H₂O → HClO + OH⁻
- Легко принимает электроны. Следовательно, он действует как мощный окислитель.
- Реагирует с соляной кислотой с образованием хлорида кальция, хлора и воды. Реакция протекает как
4HCl + Ca(ClO)₂ → CaCl₂ + Cl₂ + H₂O
- Реагирует с диоксидом углерода (CO₂) с образованием карбоната кальция (CaCO₃) и выделением хлора.
2Ca(ClO)₂ + 2CO₂ → 2CaCO3 + 2Cl₂ + O₂
Использование гипохлорита кальцияГипохлорит кальция используется для обеспечения безопасности питьевой воды и дезинфекции больших объемов воды. В плавательных бассейнах он помогает в дезинфекции водоемов и убивает микробы. Некоторые другие применения гипохлорита кальция:
- В органической химии он очень полезен из-за его поведения окислителя.

- Гипохлорит кальция используется для отбеливания конопли, хлопка, волокна, дезинфекции поверхностей, целлюлозы и крахмала, а также в качестве дезинфицирующего средства для очистки воды.
- Также используется в некоторых отбеливающих растворах.
- Также используется в качестве твердого огнетушителя.
- Из-за присутствия реактивного хлора гипохлорит кальция используется для очистки сточных вод и питьевой воды.
- Расщепляет кетокислотные и гликолевые связи с образованием дезинтегрированных карбоновых кислот или альдегидов.
- Используется для получения хлороформа в ходе галоформных реакций.
- Гипохлорит кальция также используется в жесткой воде для предотвращения засорения фильтров или труб.
- Используется для дезинфекции и дезодорации в производстве напитков, пищевой и сахарной промышленности.
- Помогает при отделке и придании дополнительного блеска в ковровой промышленности.

- Гипохлорит кальция (известный как отбеливающий порошок) также используется для отбеливания льна и хлопка.
- Он действует как средство от комаров, уничтожая личинки комаров в стоках, желобах, прудах и т. д.
Несмотря на множество применений гипохлорита кальция, все же может возникнуть вопрос: опасен ли гипохлорит кальция? Если вы используете его с осторожностью и осторожностью, это не так опасно. Но использование его без мер предосторожности может привести к сильным последствиям. Некоторые из побочных эффектов использования гипохлорита кальция:
- При контакте с водой или влагой выделяет газообразный хлор. Это может привести к некоторым проблемам со здоровьем.
- В присутствии кислоты выделяет высокотоксичные пары газообразного хлора.
- Умеренное использование раствора гипохлорита кальция может вызвать раздражение кожи.
 Иногда это может вызвать серьезные ожоги кожи.
Иногда это может вызвать серьезные ожоги кожи. - Оказывает разъедающее воздействие на влажные ткани, такие как глаза, верхние дыхательные пути и т. д.
- Вдыхание гипохлорита кальция может вызвать кашель, проблемы с дыханием и одышку.
- Более концентрированные растворы гипохлорита кальция могут вызывать значительные ожоги пищевода и желудка.
Подводя итог, можно сказать, что гипохлорит кальция является важной солью хлорноватистой кислоты и получается путем обработки известкового шлама Ca(OH)₂ с помощью Cl₂. Это стабильное соединение, имеющее коммерческое название «перхлорон». Иногда его используют вместо хлорной извести.
Благодаря своим негигроскопическим свойствам он превосходит хлорную известь. Гипохлорит кальция доступен в продаже, но чаще всего образуется на месте на месте использования. Это широко используемое неорганическое соединение.
Гипохлорит кальция разлагается при контакте с водой с выделением хлора. Он остается стабильным, потому что гипохлорит кальция разлагается только при контакте с водой. Как правило, отбеливающий порошок представляет собой смесь многих соединений хлора, которые выделяют образующийся кислород.
Он остается стабильным, потому что гипохлорит кальция разлагается только при контакте с водой. Как правило, отбеливающий порошок представляет собой смесь многих соединений хлора, которые выделяют образующийся кислород.
A) Ключевые преимущества и недостатки использования гипохлорита кальция:
Преимущества:
- Удобен при транспортировке и хранении.
- Можно долго хранить.
- Простое и эффективное использование делает его предпочтительным по сравнению с другими хлорсодержащими составами для обработки воды.
- Это экономичный и легкодоступный химикат.
Недостатки:
- Может вызвать засорение.
- Требуется надлежащее хранение. Утечка даже небольшого количества может привести к серьезным последствиям.

- Обладает низкой растворимостью.
- Воздействие огня может привести к резкому увеличению интенсивности пожара.
- Конечная концентрация хлора в воде зависит от достигнутой степени растворения.
A) Гипохлорит кальция должен храниться в сухом, хорошо проветриваемом помещении при температуре ниже 50ºC, изолированном от кислот, аминов, аммиака и других хлорирующих или окисляющих агентов. Поскольку эти соединения легко воспламеняются при воздействии на них, а гипохлорит кальция действует как окислитель, его хранят в сухом месте.
3) Какова функция гипохлорита кальция? A) Гипохлорит кальция является отбеливающим средством. Он может производить хлор, который действует как окислитель. Вот почему гипохлорит кальция или хлорная известь используется в качестве очищающего и дезинфицирующего средства.
A) Гипохлорит кальция представляет собой неорганическое соединение с формулой Ca(OCl)₂. Это соединение относительно стабильно и содержит больше доступного хлора, чем отбеливающий раствор. Он плохо растворяется в воде и предпочтительно используется в воде от мягкой до средней жесткости.
Отбеливающий порошок сочетает в себе хлорид кальция, гипохлорит кальция и гидроксид кальция. Это смесь, состоящая в основном из двухосновного гипохлорита кальция Ca₃(OCl)₂(OH)₄, гипохлорита кальция Ca(OCl)₂ и двухосновного хлорида кальция Ca3Cl₂(OH)₄. Его формируют из слегка влажной гашеной извести.
Гипохлорит кальция – химическое уравнение, структура, свойства и производство
Гипохлорит кальция можно определить как химическое соединение, имеющее формулу Ca(ClO)2.
Обычно его называют либо оксихлоридом кальция, либо отбеливающим порошком. Его можно назвать ионным соединением, состоящим из двух анионов гипохлорита (ClO–) и катиона кальция (Ca2+). Несмотря на стабильность при комнатной температуре, гипохлорит кальция медленно разлагается во влажной среде, придавая ему характерный запах хлора. Общее название гипохлорита кальция можно дать как хлорная известь.
Несмотря на стабильность при комнатной температуре, гипохлорит кальция медленно разлагается во влажной среде, придавая ему характерный запах хлора. Общее название гипохлорита кальция можно дать как хлорная известь.
Гипохлорит кальция представляет собой соединение, которое, как известно, является активным ингредиентом большинства коммерческих отбеливающих средств, таких как хлорная известь и отбеливающие порошки хлора.
Гипохлорит кальция Химическое уравнение
(изображение будет загружено в ближайшее время)
Коммерчески гипохлорит кальция доступен в гидратированной и безводной формах и является одним из основных ингредиентов как отбеливающего порошка, так и хлорного порошка. Соединение Ca(ClO)2 производится в промышленных масштабах путем реакции газообразного хлора с гидроксидом кальция.
Представление химического уравнения для этой реакции может быть дано следующим образом.
2Ca(OH)2 + 2Cl2 → Ca(ClO)2 + h3O + CaCl2
Обычно отбеливающий порошок представляет собой смесь гипохлорита кальция, и его двухосновная форма может быть представлена как (Ca(ClO2). 2Ca(OH)2). Напротив, двухосновная форма хлорида кальция может быть представлена как (CaCl2.2Ca(OH)2). Поскольку оно содержит два иона ClO–, это соединение имеет более высокую доступность хлора, чем гипохлорит натрия (NaOCl).
2Ca(OH)2). Напротив, двухосновная форма хлорида кальция может быть представлена как (CaCl2.2Ca(OH)2). Поскольку оно содержит два иона ClO–, это соединение имеет более высокую доступность хлора, чем гипохлорит натрия (NaOCl).
Структура гипохлорита кальция
Структура молекулы Ca(ClO)2 состоит из одного иона Ca+ и двух ионов ClO–. Представление можно дать следующим образом.
(изображение будет загружено в ближайшее время)
Каждый ион хлорита имеет заряд -1, тогда как ион кальция содержит заряд +2. Так, один катион кальция может образовывать ионные связи с помощью двух ионов гипохлорита.
Properties of Calcium Hypochlorite
Chemical Data
IUPAC Name | Calcium Hypochlorite |
Calcium Hypochlorite Chemical Formula or calcium hypochlorite formula | Ca(ClO)2 |
Molar Mass or Molecular Weight | 142. |
Density at 20℃ | 2.35 gms per cubic centimetre |
Melting Point | 373K (100℃) |
Boiling Point | Decomposes at 448K (175℃) |
Физические свойства
При комнатной температуре соединение гипохлорита кальция представляет собой белое или серое твердое вещество.
Растворимость в воде 21 г/100 мл, при растворении вступает в реакцию с водой.
Растворимость в жесткой воде относительно низкая по сравнению с его растворимостью в мягкой или средней жесткости воде.
Соединение Ca(ClO)2 имеет сильный запах хлора (из-за его реакции с молекулами воды, присутствующими в воздухе).

Химические свойства
Соединение гипохлорита кальция действует как сильное основание, потому что оно легко принимает H+. Также при растворении в воде анион гипохлорита принимает протон от h3O, высвобождая ион ОН–.
Химическое уравнение для этой реакции может быть представлено как ClO- + h3O → HClO + OH-
Это также соединение, которое является сильным окислителем, потому что оно может легко принять электрон.
Гипохлорит кальция представляет собой соединение, которое реагирует с соляной кислотой с образованием воды, хлорида кальция (CaCl2), а также газообразного хлора (Cl2).
Химическое уравнение этой реакции можно представить в виде 4HCl + Ca(ClO)2 → CaCl2 + Cl2 + h3O.

Производство гипохлорита кальция
Гипохлорит кальция представляет собой соединение, получаемое в промышленных масштабах путем обработки извести (Ca(OH)2) газообразным хлором. Эта реакция проводится поэтапно для получения различных композиций, каждая из которых имеет разную концентрацию гипохлорита кальция, вместе с непрореагировавшим хлоридом кальция и известью. Химическое представление может быть показано как,
2 Cl2 + 2 Ca(OH)2 → Ca(CIO)2 + CaCl2 + 2 h3O
Хлорную известь готовят на слегка влажной гашеной извести. Это также не простая смесь хлорида кальция, гидроксида кальция и гипохлорита кальция. Однако вместо этого это смесь, которая в основном содержит двухосновный гипохлорит кальция, гипохлорит кальция Ca(ClO)2, Ca3(ClO)2(OH)4 (может также записываться как Ca(ClO)2 · 2 Ca(OH) 2) и двухосновный хлорид кальция Ca3Cl2(OH)4 (гидроксихлорид кальция, который также записывается как CaCl2 · 2 Ca(OH)2).

 Представляет собой порошок белого цвета или слабоокрашенный с запахом хлора.
Представляет собой порошок белого цвета или слабоокрашенный с запахом хлора.




 Иногда это может вызвать серьезные ожоги кожи.
Иногда это может вызвать серьезные ожоги кожи.
 98 gms per mole
98 gms per mole
